推荐厂家
暂无
暂无
 留言咨询
留言咨询
 留言咨询
留言咨询
 金牌3年
金牌3年
 400-860-5168转4865
400-860-5168转4865
 留言咨询
留言咨询
 400-807-5250
400-807-5250
 留言咨询
留言咨询

 400-831-3689
400-831-3689
 留言咨询
留言咨询
 400-860-5168转1674
400-860-5168转1674
 留言咨询
留言咨询




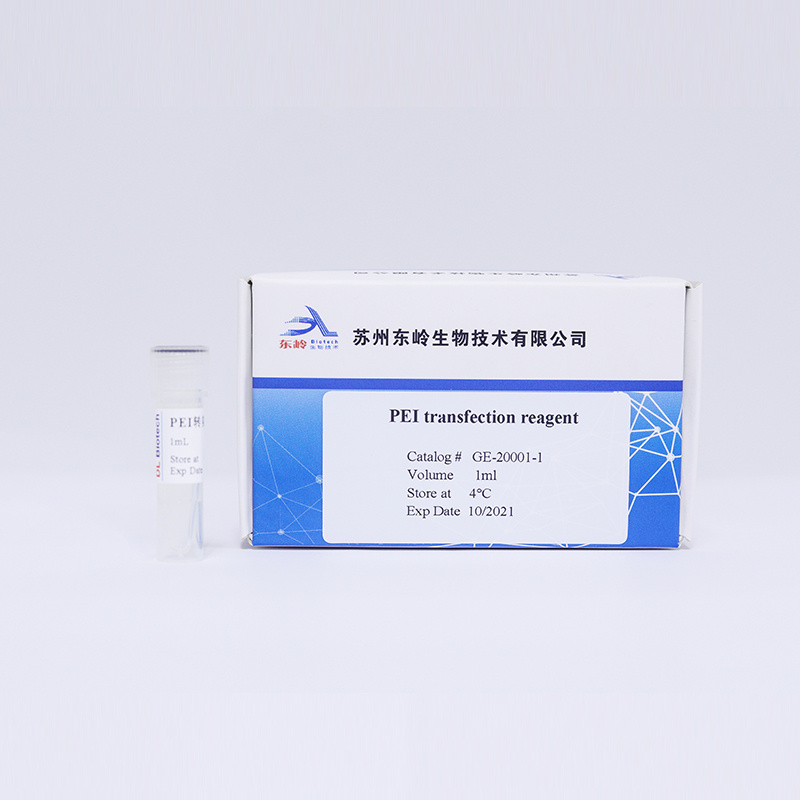
[font=宋体]哺乳动物细胞表达系统具有促使蛋白正确折叠和实现复杂修饰的功能,表达的蛋白更近天然状态,能够运用于制药等活性要求高的领域。利用哺乳动物细胞表达系统生产蛋白通常有两种方式:瞬时转染与稳定转染(构建稳定细胞系),这两种方式在原理、操作流程、应用场景上均有所区别,本文主要就瞬时转染与稳定转染之间的区别做一介绍。[/font][font=宋体] [/font][font=宋体][b]瞬时转染与稳定转染实验原理的异同:[/b][/font][font=宋体] [/font][font=宋体]瞬时转染与稳定转染都是将目的基因转染至特定哺乳动物细胞内,进而表达得到目的蛋白。不同的是瞬时转染的方式外源基因并没有转染到细胞的染色体上而是存在于游离的载体上,这样可以在短时间内获得基因的表达产物,但是随着细胞的不断分裂增殖外源基因最终会丢失,无法继续进行重组蛋白的生产;而利用细胞稳定转染则会将外源基因转染至细胞染色体上,目的基因不会随着细胞传代而消失,稳定转染的细胞株能够长期稳定的生产目的蛋白。[/font][font=宋体] [/font][font=宋体][b]实验操作的差别:[/b][/font][font=宋体][font=Calibri]1. [/font][font=宋体]瞬时转染与稳定转染所用的质粒是不同的,瞬转的质粒不需要带有抗性,而用于稳定转染的质粒一定要带有特定的抗性以便于后续的克隆株筛选。另外,两者所用的培养基及实验试剂也有所区别。[/font][/font][font=宋体][font=Calibri]2. [/font][font=宋体]瞬时转染的操作比构建稳定细胞系的操作简单,构建好质粒后,经过细胞复苏、转染、细胞培养、蛋白纯化等步骤即可得到目的蛋白;而构建稳定细胞系需要先将构建好的质粒线性化,再导入培养好的哺乳动物细胞内,通过一定的转染方式实现质粒与细胞的融合,接着经过细胞池筛选、单克隆筛选、细胞传代培养等步骤才能得到稳定转染的细胞系。对稳定细胞系进行培养能够长期稳定的生产目的蛋白。[/font][/font][font=宋体] [/font][font=宋体][b]瞬时转染与稳定转染优缺点对比[/b][/font][font=宋体] [/font][font=宋体]瞬时转染:[/font][font=宋体]优点:[/font][font=宋体]①能够快速生产得到微量至中量的重组蛋白[/font][font=宋体]②实验成本低[/font][font=宋体]③一个宿主可以带有多个拷贝,表达效率高[/font][font=宋体]缺点:无法长期生产得到重组蛋白[/font][font=宋体] [/font][font=宋体]稳定细胞系构建:[/font][font=宋体]优点:能够长期稳定生产目的蛋白[/font][font=宋体]得到稳转株之后后续生产蛋白的成本大大降低[/font][font=宋体]能够对基因进行基因插入、基因敲除等编辑操作[/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供[url=https://cn.sinobiological.com/services/stable-cell-line-development-service][b]稳定细胞系构建服务[/b][/url],包含过表达细胞系构建服务和[/font][font=Calibri]CHO[/font][font=宋体]稳定细胞株开发服务,详情可以参看[/font][font=Calibri]https://cn.sinobiological.com/services/stable-cell-line-development-service[/font][/font]
常用的基因转染技术是将外源基因导入靶细胞需要一定的载体和导入方法,基因转技术则是将纯化的含有靶基因的质粒DNA送入细胞内,并在细胞内表达。转染方法有多种,根据不同的细胞,贴壁或悬浮细所可选用不同的方法,其目的是要达到设置转染效率,影响转染产率的因素有多种,包括转染方法、操作技术、质粒DNA的纯度、靶细胞的生长状态等,下面重点介绍向几种常用的转染技术:被用于作靶基因转染的细胞,其生长状态如何,将直接决定了基因转染效率。如为贴壁生长的细胞,一般要求在转染前一日,必需应用胰酶处理成单细胞悬液,重新接种于培养皿或瓶,细胞密度以铺满培养器皿的60%为宜,转染当日,在转染前4小时换一将近新鲜培养液。对于悬浮细胞,也需在转染前4小时换一次新鲜培养液。用于转染的质粒DNA必须无蛋白质,无RNA和其了化学物质的污染,OD260/280比值应在1.8以上。应用酚-氯仿抽提法制备的质粒DNA一般难以达到此标准,目前大多采用进口的术提取纯化试剂盒。具体的基因转染技术有鳞酸钙介导的转染法、DEAE葡聚糖介导转染法、脂质体介导转染法及电击基因转导尘等。靶基因被导入细胞后,一般在转染后48小时,靶基因即在细胞内表达。根据不同的实验目的,48小时后即可进行靶基因表达的检测等实验。如若建立稳定的细胞系,则可对靶细胞进行筛选,根据不同基因载体中所含有的抗性标志选用相应的药物,最常用的直核表达基因载体的标志物有潮霉素(hygromycin)和新霉素(neomycin)。
4、 质粒因素从质粒浓度看,细胞密度为1*106/ml,DNA用量在2-5ug/ml转染效率最高。转染率在一定一定范围内随质粒浓度的上升呈线性增高,但是到达一个峰值后,随DNA用量增加而转染率逐渐下降,其原因可能为细胞吸纳DNA有一个饱和度,过量便会产生毒性,使存活率降低,不利于转染率提高。进行小分子量的分子转染时(siRNA/miRNA),应使用高电压、短脉冲时间。大分子量分子转染时(DNA),应使用低电压,长脉冲时间。从质粒的纯度看,用高纯度的DNA才 能提高电转的效率,且应注意以下几点:首先DNA/RNA应该超纯(A260/A2801.8),其次应不含内毒 素,同时质粒应溶于双蒸水而不是TE缓冲溶液。