推荐厂家
暂无
暂无



 400-628-5299
400-628-5299
 留言咨询
留言咨询

 400-628-5299
400-628-5299
 留言咨询
留言咨询

 留言咨询
留言咨询
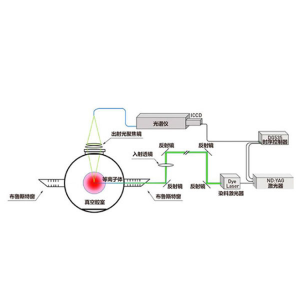
[b]摘要[/b]从首次感染部位向邻近基质的转移入侵是肿瘤发展过程中的关键步骤,研究成果较少。肿瘤入侵的原理以各种体外模型给出了实验性的表述;但是,体内的关键性步骤和机制仍然不清楚。这里,我们通过落射荧光成像和多光子显微镜建立了一个修正的皮肤折叠室模型来阐述关于HT-1080纤维肉瘤细胞的原位移植,生长和入侵。这种策略允许对作为独立细胞或者集体粘丝或者细胞团沿着富含胶原的细胞外基质和增补宿主组织包括纹状肌肉丝和淋巴管的肿瘤生长、肿瘤诱导血管形成和入侵进行重复成像。这个修正的窗口模型将适用于阐述肿瘤转移和入侵的机制,以及相关的实验性治疗。[b]材料与方法[/b]HT-1080双色纤维肉瘤细胞表达细胞质DsRed2和核组蛋白2B(H2B)-EGFP -EGFP (Yamamoto et al. 2004)培养在改良的鹰培养基(PAN Biotech GmbH, Aidenbach, Germany)中,补充10%的胎牛血清(Aurion, Wageningen, The Netherlands),盘尼西林和链霉素(都100ug/ml PAN)和潮霉素B(0.2mg/ml;Invitrogen, Carlsbad, CA, USA)在37%湿润的5%CO2的培养环境中。小鼠被用异氟烷麻醉并被稳定固定在37℃的温控平台上。使用一个落射多光子显微镜[color=red]([/color][color=red]TriM Scope, LaVision BioTec[/color][color=red])[/color],并配备了OPO装置(OPO APE, Berlin, Germany)用于1100nm波段的双光子激发,以及红外修正的20X/0.95N.A(Olympus)物镜。如果没有特定声明,EGFP,DsRed2和SHG的获取都是使用的832nm的激发光。由带通滤波器确定的检测光波段为400/40(蓝),535/50(绿),605/70(红),和710/75(红外)。以5um的步长对深达250um的成像深度进行顺序3D堆栈。通过向尾静脉注射4mg荧光葡聚糖对血管显影。在注射了淋巴归巢环肽LyP-1(100ug)之后活化的淋巴管被检测到。(Laakkonen et al. 2002)图像被使用ImageJ 1.40 g (W. Rasband, NIH), ImSpector 3.4 (LaVision Bio- Tec GmbH), and Photoshop CS 8.0.1 (Adobe Systems Inc.)重构和分析。以宽的平方X长Xπ/6计算肿瘤体积。有丝分裂和细胞凋亡的比例通过H2B-EGFP模式从每区域30到100个细胞中确定。[b]主要结果 [/b][img=,593,498]http://qd-china.com/uploads/bio-product/51.jpg[/img]Fig.1 在背侧皮肤褶皱室中HT-1080纤维肉瘤细胞的滴落和注射方法比较.6(c)、7(d)天后通过明场和落射荧光显微镜观察的细胞应用,生长位置(a,b)和宏观肿瘤形态。在建立的模型中,允许细胞悬浮液或者细胞球粘附到外科手术准备好的真皮组织表面上,获得了在真皮层与盖玻片(a.c)间的3D肿瘤生长。使用细针将细胞球注射进真皮中阻止盖玻片和真皮内产量增加间的反应(b,d)。标尺1mm(概图)和250um(细节)。 [img=,604,379]http://qd-china.com/uploads/bio-product/52.jpg[/img]Fig 2. 肿瘤生长阶段。 a 由落射荧光显微镜监测的移植瘤生长和入侵的时间进程。新生血管的插入,不存在(3天)和存在(7天)。标尺1mm。b 通过以day 1的体积进行归一化的肿瘤体积。mean+-SD(n=9)。c HT-1080移植肿瘤在6天的时候的肿瘤形态,血管化,分生和凋亡。使用多光子显微镜以激发波长1100nm(左)和832nm(右)获取的一个中央中流区域的3D重构。核形态包括了有丝分裂(白色箭头)和凋亡图(黑色箭头)。标尺50um。插图显示了前相(P)、中相(M)和后相(LA)以及凋亡图(A)。d 对时间依赖的分生和凋亡定量化。数据显示3个非依赖性肿瘤的10-25个独立区域的Mean±SEM。 [img=,617,642]http://qd-china.com/uploads/bio-product/53.jpg[/img]Fig 3. 近红外多光子显微镜显示环绕HT-1080双色肿瘤的肿瘤诱导产生血管及其结构。Z轴为一个6天大肿瘤的从肿瘤边缘(-50um)到肿瘤内部区域(-80um)(红色细胞质;黄色细胞核)。通过FITC-葡聚糖注射现实的密布血管(绿),先前存在的线形血管(绿色箭头)和不规则形状的新生血管(蓝色箭头)。胶原纤维(黑色箭头)和肌肉丝(白色箭头),通过二次谐波检测(灰度)。标尺50um。 [img=,583,768]http://qd-china.com/uploads/bio-product/54.jpg[/img]Fig 4. HT-1080双色细胞的原位入侵模型。a 注射后6天入侵类型的分类。缺少入侵(上,左)并且散布单个细胞(上,右;白色箭头),散射的或者紧密地丝状整体入侵(下图)。标尺250um。 b 45个连续的非依赖性肿瘤的按中所分入侵模式的频率。11天时,沿着纹状肌肉纤维集体入侵丝的定位。标尺100um。d 单一细胞侵入脂肪组织随后进行分散的,部分整体的入侵。对照-少量圆的脂肪细胞(星号)被HT-1080细胞包围。1100nm的激发光来检测遍布的血管(Alexa Fluor 660-dextran,红色),,肿瘤细胞质(绿色假彩),SHG(灰度);832nm用于肿瘤细胞核(白色)。标尺100um。[img]http://qd-china.com/uploads/bio-product/55.jpg[/img]Fig 5. HT-1080细胞沿淋巴管的入侵。a 由多光子显微镜对边缘而非肿瘤中心的活化淋巴管产生的单幅图片。用FITC连接的LyP-1缩氨酸来检测。深度已标明在图上(um)。b 3D堆栈投影表明淋巴管内(白色箭头)和外淋巴管入侵(黑色箭头)。标尺100um。
[size=14px] [/size] [size=14px]青蒿素(Arteminsinin)是从植物青蒿中分离出来的倍半萜内酯,与它的一些衍生物一起被公认为一种有效的用于治疗疟疾药物,现已逐渐被认为是潜在的抗肿瘤药物,已有一些研究试图确定青蒿素的蛋白质靶点并破译青蒿素杀死癌细胞的分子机制,但迄今为止,青蒿素的确切抗肿瘤相关靶点仍有很大挖掘空间。[/size] [size=14px] [/size] [size=14px]1、细胞毒性筛查将ART1确定为潜在的抗肿瘤药物[/size] [size=14px]作者首先制备了C-10位的不同芳基取代基的青蒿素衍生物(ART1、ART2和ART3),利用肺癌细胞系H1299和A549比较了它们以及青蒿素(QHS)及其衍生物双氢青蒿素(DHA)的抗肿瘤活性。发现ART1,一种含有萘环的青蒿素衍生物,对肺癌细胞表现出最强的细胞毒性。在肿瘤类器官模型和白血病MV4细胞中均证明ART1是最有效化合物。此外,ART1表现出对正常细胞的抗增殖活性非常弱。结果表明ART1是一种有前途的潜在抗癌药物。[/size] [size=14px]图片[/size] [size=14px]图1 ART1抑制肿瘤生长[/size] [size=14px]2、ART1诱导非经典铁死亡[/size] [size=14px]先前的报告表明青蒿素通过多种方式导致癌细胞死亡,包括细胞凋亡、自噬等。作者发现ART1触发的细胞死亡与凋亡、自噬无关。进一步确定ART1诱导癌细胞死亡的机制,发现ART1诱导的细胞死亡仅被铁死亡抑制剂ferrostatin-1(可防止脂质过氧化物的积累)抑制,而不能被细胞凋亡抑制剂z-VAD-FMK或坏死性凋亡抑制剂necrostatin-1抑制,表明ART1处理触发铁死亡。此外,ART1处理会诱导脂质过氧化,且ART1引起的脂质过氧化是铁依赖性的。深入机制研究发现ART1导致铁死亡已知类别的铁死亡诱导剂不同,它不影响其细胞内GSH水平和GPX4活性。[/size] [size=14px]图片[/size] [size=14px]图2 ART1诱导非经典铁死亡[/size] [size=14px]3、鉴定HSD17B4蛋白作为ART1的直接靶标[/size] [size=14px]为了确定ART1介导诱导铁死亡的蛋白靶点,作者设计了并合成了ART16(生物素标记的ART1)来开展Pulldown。ART16类似于ART1可诱导铁死亡,可用于后续实验。Pulldown+蛋白质组学分析显示HSD17B4蛋白为可能靶点, BLI、Pulldown+WB技术证实了两者的直接结合。[/size] [size=14px]图片[/size] [size=14px]图3 鉴定HSD17B4蛋白作为ART1的直接靶标[/size] [size=14px]4、ART1通过HSD17B4蛋白介导癌细胞死亡[/size] [size=14px]作者采用ART99(含有香豆素荧光团的ART1探针),发现ART99与靶蛋白HSD17B4的共定位。通过敲低HSD17B4来研究ART1诱导的细胞死亡是否由HSD17B4介导,发现HSD17B4敲低可显著减弱ART1的作用。[/size] [size=14px]图片[/size] [size=14px]图4 ART1通过HSD17B4蛋白介导癌细胞死亡[/size] [size=14px]5、ART1靶HSD17B4蛋白直接诱导脂质氧化[/size] [size=14px]HSD17B4蛋白是一种双功能酶,同时具有脱氢酶和水合酶活性,并参与VLCFA(极长链脂肪酸)的过氧化物酶体β氧化。作者发现ART1并未改变细胞中HSD17B4蛋白丰度,也不影响其脱氢酶和水合酶活性。由于ART1中的过氧化物部分对于诱导铁死亡是必不可少的,作者推测ART1可能是一种启动铁死亡的选择性氧化剂,与HSD17B4结合并促进周围脂质的氧化。作者验证发现ART1可以直接氧化铁死亡相关底物。PUFA,易受脂质过氧化的影响,是执行铁死亡所必需的。由于不容易获得超长链多不饱和脂肪酸,AA被用作替代物,作者发现ART1单独可以氧化AA,ART1还可以显著促进由亚铁离子催化的脂质过氧化。此外,活细胞成像探针发现ART1可以氧化细胞中HSD17B4蛋白周围的脂质。这些数据证实ART直接氧化HSD17B4蛋白周边的脂质,积累脂质过氧化物,并最终在癌细胞中促进铁死亡。[/size] [size=14px]图片[/size] [size=14px]图5 ART1靶向HSD17B4蛋白直接诱导脂质氧化[/size] [size=14px]6、ART1优先诱导高间充质状态癌细胞的铁死亡[/size] [size=14px]据报道,高间充质状态的耐药性癌细胞对铁死亡诱导剂敏感。作者检测这些肺癌细胞的上皮间充质状态,发现对ART1敏感细胞系H1299和H1838中的波形蛋白含量较高,表明高间充质状态,而对ART1耐药细胞系HCC366和H1650几乎表现出E-钙粘蛋白的丰度检测不到,这表明ART1的敏感性与癌细胞上皮间充质状态密切相关,ART1可优先诱导间充质癌细胞发生铁死亡。[/size] [size=14px]图片[/size] [size=14px]图6 ART1优先诱导高间充质状态癌细胞的铁死亡[/size] [size=14px]总结[/size] [size=14px]该研究将青蒿素衍生ART1已被确定为铁死亡诱导剂,对癌细胞增殖具有显著的抑制效果。接着使用化学蛋白质组学方法鉴定HSD17B4蛋白,一种在VLCF分解代谢中必不可少的酶,作为ART1的直接靶点。进一步研究发现ART1会导致铁死亡,通过直接氧化HSD17B4蛋白周围的脂肪酸而不干扰蛋白质的正常酶活性,揭示了一种意想不到的机制,其中ART1-HSD17B4用作“特洛伊木马”,潜入过氧化物酶体触发脂质氧化。总之,ART1通过靶向HSD17B4诱导铁死亡提供了一种有希望的癌症治疗方法。[/size]
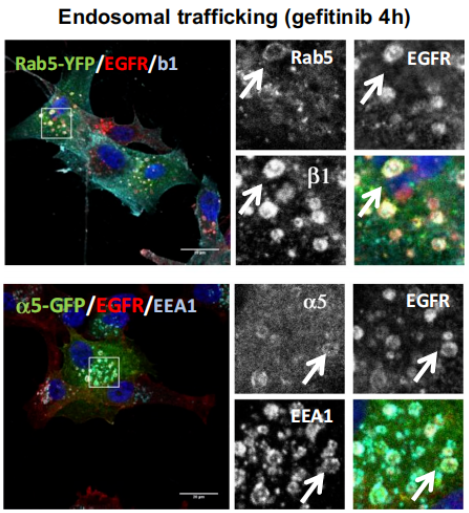
[b][size=15px][color=#595959]2型神经纤维瘤病(NF2)[/color][/size][/b][size=15px][color=#595959]是一种罕见的遗传综合征,易使个体发展为双侧[b]前庭神经鞘瘤(VSs)[/b],可导致高风险的危及生命的神经并发症。NF2相关VS的传统治疗方案通常会导致神经损伤,迄今为止,[/color][/size][b][size=15px][color=#595959]没有[/color][/size][size=15px][color=#595959]FDA[/color][/size][size=15px][color=#595959]批准的NF2药物疗法[/color][/size][/b][size=15px][color=#595959]。该研究的目的是评估中药复方[b]祛毒散结汤(QDSJ)[/b]对NF2相关的VS的[b]抗肿瘤疗效[/b],并研究潜在的[b]作用机制[/b]。[/color][/size] [align=center] [/align] [size=15px][color=#595959]超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url][b]色谱-质谱[/b](UHP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url])分析用于鉴定QDSJ的成分及其靶点。为了确定QDSJ的假定靶点与NF2相关VS的差异基因之间的关系,使用UHPL-MS数据结合前期的基因表达谱数据筛选[b]药物-疾病交叉基因[/b]。将差异表达的基因导入字符串数据库以生成PPI网络。使用GO和KEGG途径富集分析鉴定[b]差异表达的基因靶点和途径[/b]。[/color][/size] [size=15px][color=#595959]分别使用[b]患者来源的神经鞘瘤细胞系和患者来源的异种移植物小鼠模型[/b],检测QDSJ的疗效。H&E染色、[b]免疫[/b]组化和免疫荧光染色用于评估细胞增殖和肿瘤[b]血管[/b]。[/color][/size][font=mp-quote, -apple-system-font, BlinkMacSystemFont, &][size=15px][color=#595959][/color][/size][/font][align=center] [/align] [size=15px][color=#595959]通过UHP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]分析,共鉴定出133个化合物。网络药理学表明,[b]坏死、凋亡、细胞周期、血管生成、粘附连接和神经活性配体受体相互作用[/b]的调节可能与QDSJ治疗NF2相关VS的疗效相关。[/color][/size] [b][size=15px][color=#595959]QDSJ治疗可诱导坏死细胞死亡和神经鞘瘤细胞凋亡[/color][/size][/b][size=15px][color=#595959],并抑制肿瘤生长。组织病理学分析显示QDSJ处理的肿瘤中有细胞坏死区域和肿瘤血管扩大。与对照肿瘤相比,QDSJ治疗的肿瘤中细胞周期蛋白D1和Ki-67阳性的细胞数量显著减少。CD31和αSMA的免疫荧光染色显示QDSJ治疗的肿瘤中肿瘤血管数量和密度减少,血管结构正常化。[/color][/size][font=mp-quote, -apple-system-font, BlinkMacSystemFont, &][size=15px][color=#595959][/color][/size][/font][font=mp-quote, -apple-system-font, BlinkMacSystemFont, &][size=15px][color=#595959][/color][/size][/font][size=15px][color=#595959][/color][/size][color=#3573b9]结论[/color][b][size=15px][color=#595959][/color][/size][/b][font=mp-quote, -apple-system-font, BlinkMacSystemFont, &][size=15px][color=#595959][/color][/size][/font] [b][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size][/b][size=15px][color=#595959]该研究表明,QDSJ对NF2相关神经鞘瘤具有[b]显著的抗肿瘤活性[/b],是未来临床试验的可能[b]候选药物[/b]。[/color][/size][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size][size=15px][color=#595959][/color][/size]