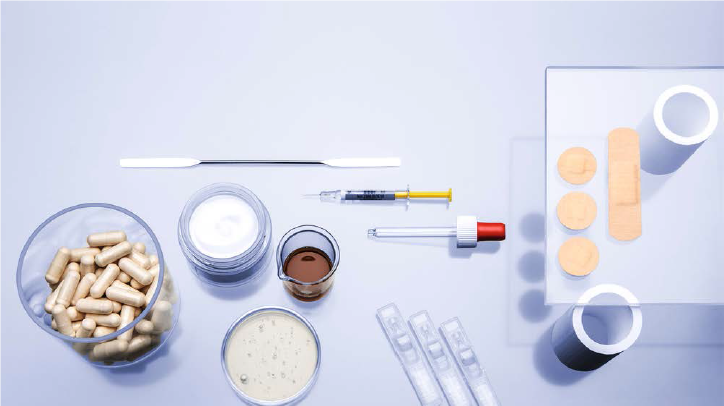
推荐厂家
暂无
暂无


 留言咨询
留言咨询

 400-860-5168转3452
400-860-5168转3452
 留言咨询
留言咨询

 400-860-5168转2232
400-860-5168转2232
 留言咨询
留言咨询


保健品和药品的胶囊壳一样吗?这些胶囊壳的主要成分是什么?重金属含量有没有要求?
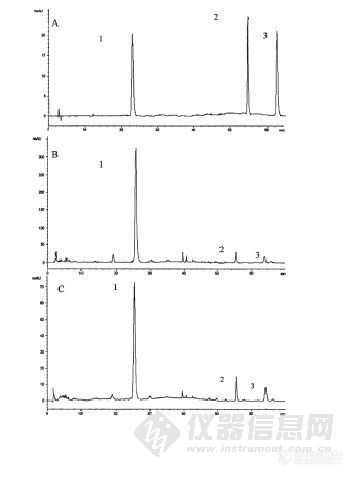
作者:王洋(南京中医药大学)摘要:本文对不同采收期、不同贮存时间的广陈皮药材主要成分的含量进行了测定,归纳总结了其主要的变化规律,旨在揭示个青皮与广陈皮药材“同源不同性”的机理以及初步探索贮存时间对广陈皮内在成分的影响,为广陈皮药材的临床应用提供实验依据。 1.本文所需广陈皮药材样品共13份,收集于广东省新会县广陈皮种植基地,样品分别为2004年11月、2005年10月、2005年11月、2005年12月、2006年10月、2006年11月、2006年12月、2007年5/6月、2007年8月、2007年9月、2007年10月、2007年11月和2007年12月。 2.对各广陈皮样品的主要成分进行了含量测定,确定了测定方法。总黄酮、总生物碱和总多糖采用紫外分光光度法,回归方程、相关系数和线性范围分别为:y=3.397x+0.011,r=0.9998,线性范围:0.04mg/m1~0.24mg/ml;y=7.12x+0.018,r=0.9998,线性范围:0~0.18mg/ml;y=0.083x-0.005,r=0.9997。挥发油成分采用GC/MS法测定,气相色谱条件:色谱柱为DB-5(30m×250μm×0.25μm)石英毛细管色谱柱;进样口温度220℃;程序升温60℃(维持5min),以5℃/min升温至200℃;载气为高纯氦气,流量1mL/min,溶剂延迟3min。质谱条件:MSD离子源为El源,离子源温度230℃,电子能量70eV,扫描质量范围50~550质量数。加速电压1000eV。 橙皮苷、川陈皮素和橘皮素的含量测定采用HPLC法,色谱条件为:流动相体系为甲醇(A)-乙腈(B)-4%醋酸水溶液(C),梯度洗脱。0~25min,A: B:C=10:15:75;25~40nun,A升至50%,A:B:C=50:15:35,保持30min。色谱柱为Platisil ODS柱(5μm,250×4.6mm),柱温30℃,流速1ml/min。检测波长:0~50min,283nm;50~70min,332nm。 3.对不同采收期广陈皮药材主要成分的含量变化进行了对比,结果为:个青皮总黄酮和橙皮苷的含量最高,而广陈皮药材挥发油、生物碱以及多糖类成分均高于个青皮,这可能就是个青皮与广陈皮“同源不同性”的内在机理。 对于不同贮存时间的广陈皮药材,黄酮类成分与总生物碱含量随着贮存时间的延长会基本保持不变或者略有上升。 4.用“老化”模拟实验处理广陈皮药材,结果表明在高温条件下,黄酮类成分化学性质较稳定,且随着烘烤时间的延长,含量会略有上升。另外,在高温条件下,药材内部可能发生了化学成分的转化并产生新的极性较大的物质。谱图:http://ng1.17img.cn/bbsfiles/images/2012/08/201208131431_383497_1606903_3.jpg

[align=center][b]基于HPLC的乳痛安口服主要成分含量研究[/b][/align][align=center]邰晓鹏[sup]1[/sup],臧恒昌[sup]*[/sup][/align][b]摘要 目的:[/b]利用HPLC方法建立乳痛安口服液中蒲公英主要的成分咖啡酸、夏枯草的主要成分迷迭香酸、连翘的主要成分连翘苷含量测定方法,意在探究一种稳定可靠的检测方法,以用于医院内部自制制剂乳痛安口服液含量测定。[b]方法:[/b]配置好乳痛安口服液供试液和咖啡酸、迷迭香酸以及连翘苷标准对照品溶液,确定合适的色谱条件后依次进行线性关系考察、精密度试验、稳定性试验、加样回收率试验、样品含量测定以及阴性对照试验的实验操作,对实验结果进行分析处理。[b]结果:[/b]从乳痛安口服液样品的高效液相色谱图中可以看出,在选定HPLC条件下,医院内部自制的乳痛安口服液中的咖啡酸、迷迭香酸与连翘苷与其他成分分离良好,并得出咖啡酸、迷迭香酸及连翘苷的在一定范围内线性关系良好,口服液稳定性良好,仪器精密度良好。[b]结论:[/b]本研究建立乳痛安口服液三种主要成分的HPLC含量测定方法,相对于原有的乳痛安口服液仅做定性鉴别质量标准有较大改善,方法学试验结果满足分析要求,表明所建立的高效液相色谱方法稳定可靠,可用于医院内部自制制剂乳痛安口服液含量测定,为提高医院内部自制制剂乳痛安口服[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]量标准提供参考。关键词:乳痛安口服液;高效液相色谱;含量测定[b] [/b][align=center][b]Study on the Content of Main Components [/b][/align][align=center][b]inRutongan Orally Treated by HPLC[/b][/align][align=center]Xiao-pengtai[sup]1[/sup],Zang-hengchang[sup]1*[/sup][/align][b]Abstract Objective[/b]: The method for the determination of the content of forsythin, the main component of dandelion in Rutongan oral liquid, and the main component of rosmarinic acid in Prunella vulgaris and the forsythia suspensa by HPLC, was established to explore a stable and reliable detection method. It is used for the determination of the content of the oral preparation of homemade milk emulsion in the hospital. [b]Methods:[/b] Prepare a solution of Rutongan oral solution and caffeic acid, rosmarinic acid, and forsythin standard reference solution. In order to determine the appropriate chromatographic conditions and then perform the linear relationship investigation, precision test, stability test, sample recovery test, sample content determination, and negative control experiment , and the results were analyzed and processed. [b]Results: [/b]From the highperformance liquid chromatograms of Rutongan oral liquid sample, it can be seen that caffeic acid, rosmarinic acid, and forsythin in the hospital's own homemade Rutongan oral liquid and other ingredients under selected HPLC conditions The separation was good, and it was found that the caffeic acid, rosmarinic acid, and forsythin had a good linear relationship within a certain range, the oral liquid had good stability, and the instrument precision was good. [b]Conclusion: [/b]This study establishes HPLC method for the determination of the three main components of Ru Tong An Oral Solution. Compared with the original Ru Tong An Oral Solution, it only has a qualitative improvement in the quality standard for qualitative identification. The method test results meet the analysis requirements. It shows that the established HPLC method is stable and reliable, and it can be used for the determination of the homemade preparation of the hospital's selfmade Ru Tong An oral liquid, and provides reference for improving the quality standard of the hospital's homemade self-made Ru Tong An oral liquid.[b]Keywords:[/b]Rutongan oral liquid High performance liquid chromatography Determination of content[b]1 研究简介1.1 乳痛安口服液简介[/b]乳痛安口服液原名乳痛灵口服液,色棕黄,澄清、味微甜,具主要功效为理气、散结等,在临床科室中主要用于治疗乳腺增生、乳腺炎等相关疾病,且疗效确切。李芝[sup][/sup]研究乳痛安口服液用于大鼠乳腺增生的治疗,结果表明乳痛安口服液可影响大鼠体内生殖激素分泌水平,从而使乳腺增生恢复正常。史栋栋[sup][/sup]通过中药尿液药理学筛选发现咖啡酸具有抑制乳腺癌细胞MCF-7的活性。窦景云[sup][/sup]研究发现夏枯草具有较明显的抗肿瘤作用。[b]1.2 HPLC原理[/b]HPLC是色谱法一个重要分支,因其较高的精密度而广泛应用于中药有效成分含量测定,具有高压、高效、快速、灵敏度高、应用范围广等特点。[b]1.3 HPLC用于医院制剂含量测定[/b]黄力[sup][/sup]利用HPLC测定医院自制制剂药物中水杨酸与氯霉素含量,所建方法可同时测定两种成分的含量,操作简便。梁萍等[sup][/sup]为提高制剂质量,对其含量进行HPLC测定,着色剂在医院制剂中应用广泛。杨江丰[sup][/sup]利用高效液相色谱技术同时测定医院自制制剂中柠檬酸、苹果绿等5中食用色素含量。王继森[sup][/sup]对其含量进行HPLC测定,经方法学验证后可作为该制剂质量提升的依据。[b]2 材料2.1 样品[/b]收集3批乳痛安口服液样品(批号分别为20150715, 20150722, 20150729),所有样品均由泰安市中心医院提供。[b]2.2 试剂[/b]连翘苷对照品(中国食品药品检定研究所批号110821-200406),咖啡酸对照品(中国食品药品检定研究所批号110885-2001102)、迷迭香酸对照品(中国食品药品检定研兖所批号111871-201505)、甲醇、乙腈均为色谱纯(赛默飞世尔科技有限公司)、甲酸(天津市永大化学试剂有限公司20140412) 超纯水。[b]2.3 仪器[/b]日本岛津高效液相色谱仪(LC-10A),美国Agilent 1200型高校液相色谱仪,TG3288型分析天平(上海天平仪器厂)。[b]3 方法3.1 咖啡酸和迷迭香酸方法学考察及含量测定3.1.1供试品溶液的制备[/b]精密量取医院内部自制制剂乳痛安口服液5 ml,置25 ml的棕色量瓶之中,加甲醇定容并摇匀,过滤后取续滤液并用0.22 μm微孔滤膜过滤,备用。[b]3.1.2对照品溶液的制备[/b]精密称取咖啡酸对照品与迷迭香酸对照品适量,加甲醇配制成为咖啡酸浓度为5 ugml-1,迷迭香酸浓度为10 μgml-1的混合标准品溶液,用0.22 μm的微孔滤膜过滤,备用。[b]3.1.3色谱条件[/b]色谱柱为 Athena C18 120A(250 mm×4.6 mm,5 μm),以十八烷基硅烷键合硅胶为填充剂,以0.1%甲酸水-甲醇进行梯度洗脱,详见表3-1;进样量10 μl;检测波长为330 nm;柱温40 ℃,流速为1 ml/min。[img=,690,570]http://ng1.17img.cn/bbsfiles/images/2018/08/201808010902238644_5706_1669358_3.jpg!w690x570.jpg[/img][b]3.1.6稳定性试验[/b]收集医院内部自制制剂乳痛安口服液样品(20150715),按照“3.1.1”条件下配置成供试品溶液,放置在暗处、室温下。按照“3.1.3”色谱条件下分别于0 h、3 h、6 h、9 h、24 h、48 h进样10 μl,记录医院内部自制制剂乳痛安口服液中咖啡酸与迷迭香酸面积,并计算48 h内RSD值。[b]3.1.7加样回收率试验[/b]精密吸取同一已知咖啡酸咖啡酸与迷迭香酸含量的医院内部自制制剂乳痛安口服液1 ml,再分别准确加入10 μg/ml咖啡酸对照品与迷迭香酸对照品溶液0.5 ml、1 ml、1.5 ml。按3.1.1项方法制备成供试品溶液后,按3.1.3项下色谱条件进样平行测定,进样量10 μL,测定医院内部自制制剂乳痛安口服液中咖啡酸与迷迭香酸峰面积积分值并计算结果。[b]3.1.8样品的含量测定[/b]吸取供试品溶液10 μL,注入液相色谱仪,按3.1.3项的色谱条件进样并记录峰面积,利用3.1.4项下的线性关系计算相应的咖啡酸与迷迭香酸含量。[b]3.1.9阴性对照试验[/b]依处方称取药材,其中剔除夏枯草、蒲公英,按乳痛安口服液配置规程制作不含咖啡酸、迷迭香酸的阴性对照品,按3.1.3项下色谱条件进样,进样量10 μL,得阴性对照高效液相图。[b]3.2 连翘苷方法学考察及含量测定3.2.1供试品溶液的制备[/b]精密量取医院内部自制制剂乳痛安口服液5ml,置25ml容量瓶中,加甲醇适量,振摇溶解并定容至刻度,摇匀,放置,滤过,弃初滤液,取续滤液作为供试品溶液。[b] 3.2.2对照品溶液的制备[/b]精密称取连翘苷对照品适量,加甲醇溶解得浓度为0.5 mg/ml的对照品溶液,用0.22 um的微孔滤膜过滤,备用。[b] 3.2.3色谱条件[/b]Diamonsil C18(150x4.6mm,5μm) 柱温:25℃ 流动相:乙腈一水(25:75) 流速:1.0m/min 进样量:10μL 检测波长:277nm 数据采集时间:20min.[b]3.2.4 线性关系考察[/b] 精密吸取连翘苷对照品溶液适量,以甲醇溶解并稀释得1mg/ml连翘苷储备液。精密吸取上述1mg/ml连翘苷储备液,以甲醇进行适当稀释得浓度梯度为0.05mg/ml、0.1mg/ml、0.2mg/ml、0.25mg/ml、0.5mg/ml的对照品溶液。按“3.2.3”项下色谱条件分别进样10μL,测定峰面积积分值,进行线性回归分析。[b]3.2.5稳定性试验[/b]收集医院内部自制制剂乳痛安口服液样品(150722),按3.1.1项方法制备成供试品溶液,置于室温下,按3.2.3项下色谱条件分别于0 h、3 h、6 h、12 h、24 h、48 h进行HPLC分析,进样量10 μL,测定乳痛安口服液中连翘苷峰面积并计算RSD值。[b]3.2.6精密度试验[/b]取0.05 mg/ml、0.25 mg/ml、0.5 mg/ml三个浓度的连翘苷对照品溶液,按3.2.3项下色谱条件各重复进样4次,进样量10 μL,测定医院内部自制制剂乳痛安口服液中连翘苷峰面积积分值并计算RSD值。[b]3.2.7加样回收率试验[/b]精密吸取同一已知连翘苷含量的乳痛安口服液1ml,再分别准确加入0.5mg/ml连翘苷对照品溶液0.5ml、1m1、1.5ml。按3.1.1项方法制备成供试品溶液后,按3.2.3项下色谱条件进样平行测定,进样量10μL,测定医院内部自制制剂乳痛安口服液中连翘苷峰面积积分值并计算结果。[b]3.2.8阴性对照试验[/b]依处方称取药材,其中剔除连翘,按乳痛安口服液配置规程制作不含连翘苷的阴性对照品,按3.1.3项下色谱条件进样,进样量10 μL,得阴性对照高效液相图。[b]3.2.9样品的含量测定[/b]精密吸取3个批次(批号150715, 150722, 150729)的医院内部自制制剂乳痛安口服液各5 ml,按3.2.1项方法制备成供试品溶液后,按3.2.3项下色谱条件进样测定,进样量10 μL,测定医院内部自制制剂乳痛安口服液中连翘苷峰面积积分值并按3.2.4所建立标准曲线定量连翘苷含量。[b]4结果与讨论[/b]图4-1与图4-2为选定色谱条件下咖啡酸与迷迭香酸标准品与医院内部自制制剂乳痛安口服液样品高效液相色谱图,从图中可以看出,在选定的HPLC条件下,医院内部自制乳痛安口服液中咖啡酸、迷迭香酸与其他成分分离良好,咖啡酸保留时间约为15min,迷迭香酸保留时间约为38.5min,证明选定的液相色谱方法可靠,可用于医院内部自制制剂乳痛安口服液中咖啡酸与迷迭香酸含量测定。[img=,690,595]http://ng1.17img.cn/bbsfiles/images/2018/08/201808010903300390_4720_1669358_3.jpg!w690x595.jpg[/img][b]4.1 咖啡酸方法学实验结果及含量测定4.1.1咖啡酸线性关系考察结果[/b]以医院内部自制乳痛安口服液中咖啡酸峰面积积分值对标准品浓度进行线性回归,所得回归方程为Y= 8.5726X -0.8(回归系数R2= 1),证明医院内部自制乳痛安口服液中咖啡酸在10~100 μg/ml范围内线性关系良好,咖啡酸对照品不同浓度下的峰面积如表4-1所示,咖啡酸对照品标准曲线如图4-3所示。[img=,690,587]http://ng1.17img.cn/bbsfiles/images/2018/08/201808010904476757_7540_1669358_3.jpg!w690x587.jpg[/img][b]4.1.3精密度试验结果[/b]10 μg/ml、50 μg/ml、100 μg/ml三个浓度的咖啡酸对照品溶液峰面积RSD值分别为1.1%、1.1%、0.98%,表明仪器精密度良好。[b]4.1.4加样回收率试验结果[/b]医院内部自制制剂乳痛安口服液中咖啡酸的平均回收率为100.12%,见表4-3,回收率高。[img=,690,563]http://ng1.17img.cn/bbsfiles/images/2018/08/201808010905395659_1310_1669358_3.jpg!w690x563.jpg[/img][b]4.2 迷迭香酸方法学实验结果及含量测定结果4.2.1 线性关系考察结果[/b]以迷迭香酸峰面积积分制对浓度进行线性回归,不同浓度的迷迭香酸峰面积如表4-5所示,线性关系回归方程为Y= 8.8993X +4.0679(回归系数R2= 0.9999),迷迭香酸浓度范围在10~100 ug/ml时线性关系良好,如图4-4迷迭香酸标准曲线,即此方法可用于医院内部自制乳痛安口服液中迷迭香酸含量测定。[img=,690,563]http://ng1.17img.cn/bbsfiles/images/2018/08/201808010906511971_4264_1669358_3.jpg!w690x563.jpg[/img][b]4.2.3精密度试验结果[/b]10 μg/ml、50 μg/ml、100 μg/ml三个浓度的迷迭香酸对照品溶液峰面积RSD值分别为1.1%、1.2%、0.96%,表明仪器精密度良好。[b]4.2.4 加样回收率试验结果[/b]医院内部自制制剂乳痛安口服液中迷迭香酸的平均回收率为100.16%,见表4-7,加样回收率高。[img=,690,580]http://ng1.17img.cn/bbsfiles/images/2018/08/201808010907489879_7658_1669358_3.jpg!w690x580.jpg[/img][b]4.2.6 阴性对照结果[img=,690,439]http://ng1.17img.cn/bbsfiles/images/2018/08/201808010908530066_2062_1669358_3.jpg!w690x439.jpg[/img][img=,690,448]http://ng1.17img.cn/bbsfiles/images/2018/08/201808010909528743_2907_1669358_3.jpg!w690x448.jpg[/img][img=,690,469]http://ng1.17img.cn/bbsfiles/images/2018/08/201808010910311538_2163_1669358_3.jpg!w690x469.jpg[/img][img=,690,395]http://ng1.17img.cn/bbsfiles/images/2018/08/201808010911225097_5280_1669358_3.jpg!w690x395.jpg[/img][img=,690,388]http://ng1.17img.cn/bbsfiles/images/2018/08/201808010912077942_8280_1669358_3.jpg!w690x388.jpg[/img][b]4.3.5 阴性对照试验结果[/b]如图4-9所示,连翘苷阴性对照高效液相图没有测得连翘苷。[img=,690,569]http://ng1.17img.cn/bbsfiles/images/2018/08/201808010913033496_1251_1669358_3.jpg!w690x569.jpg[/img][b]4 结论与讨论[/b]医院内部自制制剂乳痛安口服液中蒲公英主要成分咖啡酸、夏枯草主要成分迷迭香酸、连翘中主要成分连翘苷是具有代表性的三种成分,本研究建立乳痛安口服液三种主要成分的HPLC含量测定方法,相对于原有的乳痛安口服液仅做定性鉴别质量标准有较大改善。本研究优化色谱条件,建立乳痛安口服液中三种主要成分含量测定方法,并系统地验证所建立的方法的可行性,以期提升原有乳痛安口服[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]量标准,经过试验条件的摸索,医院内部自制乳痛安口服液中咖啡酸与迷迭香酸色谱条件为0.1%甲酸与甲醇梯度洗脱,医院内部自制乳痛安口服液中连翘苷色谱条件为乙腈一水(25:75),所建立的方法能够较好地将咖啡酸、迷迭香酸、连翘苷与其他成分分开,可用于乳痛安口服液三种主要成分含量测定,线性关系分别为咖啡酸Y= 8.5726X -0.8(R2= 1),迷迭香酸Y= 8.8993X +4.0679(R2= 0.9999),连翘苷Y= 1262.3X -0.1622(R2= 0.9999),研究结果满足分析要求,表明所建立的高效液相色谱方法稳定可靠。[b][b]参考文献[/b][/b] 李芝. 乳痛安口服液治疗大鼠乳腺增生病实验研究[J].泰山医学院学报,2010,31(12):937-939. 史栋栋,况媛媛,王贵明,等.细胞代谢组学用于羽扇豆醇干预人乳腺癌细胞MCF-7的机理探究. 色谱,2014,03(02):56-64. 窦景云, 等.夏枯草药理作用及临床应用研究进展. 现代医药卫生,2013,29(7):1039-1041. 黄力,袁涌,单婷婷,等. 高效液相色谱法同时测定医院制剂药物中的水杨酸和氯霉素的含量. 中国药品标准,2006,(03):70-72. 梁萍,彭建彪. HPLC法测定医院制剂气血双补胶囊中阿魏酸的含量. 中国民族民间医药,2016,25(09):9-10. 杨江丰. 高效液相色谱色测定医院制剂中合成色素的含量. 宁波高等专科学校学报,2001,(S1):121-122. 王继森,朱蓉,张亿,张姮婕. 医院制剂苯甲酸水杨酸软膏中主药含量检测方法改进. 中国药事,2014,28(10):1137-1139.作者简介:邰晓鹏,硕士研究生,研究方向中药制剂方向。*通讯作者:臧恒昌,教授,博士生导师,研究方向为过程控制与优化,Email: zanghcw@126.com,Tel: 0531-88380268[/b]