







专栏由中国医学科学院北京协和医学院药物研究所药物分析学科师生与仪器信息网专业团队一起聚焦现代药物分析技术的进展,以问题为导向,分享药物理化特性表征、质量分析、制剂处方解析、生产工艺监控、体内药物分析等


人体组织器官由具有不同细胞类型的异质细胞群组成。传统批量测序(Bulk Sequencing)方法仅能捕获器官与组织群体细胞成分的平均水平,或者只代表其中占优势数量的细胞信息,单个细胞独有的特性常常被忽略。近年来,随着单细胞测序(Single-cell sequencing)技术的发展,实现了单个细胞水平上DNA或RNA的测序,从而能够特异和精准地探索单个细胞的基因变异水平,弥补了传统批量测序的不足[1]。

图1. 单细胞测序与传统批量测序比较[1]
单细胞基因组测序技术,是在单细胞水平对全基因组进行扩增与测序的一项技术,广泛应用于癌症研究、胚胎发育、辅助生殖、细胞分化、免疫机制、微生物等生物医学方向的研究。本期主要对单细胞基因组测序的技术原理、技术流程、技术平台及其在生物医学领域的应用实例做简单介绍。
技术原理
单细胞基因组测序的原理是将分离的单个细胞的微量全基因组DNA进行扩增,获得高覆盖率的完整的基因组后进行高通量测序,揭示细胞间异质性的基因信息。
技术流程
单细胞基因组测序主要包括四个步骤,即单细胞分离→全基因组扩增→高通量测序→数据分析。目前单细胞基因组测序技术的发展依然面临两方面的技术挑战:一是易于分离和操作的单细胞分离工具(即第一步);二是能够稳定复制单个细胞中微小核酸的方法(即第二步)[2]。
2.1 单细胞分离
从组织中将单个细胞分离出来是单细胞基因组测序的第一步。目前常用的单细胞分离方法主要有:有限稀释法、显微操作法、流式细胞分选术、激光捕获显微切割技术(LCM)、微流控芯片技术等,表1总结了上述提到的单细胞分离方法的原理和优缺点,在使用时可根据不同的科研需求及样品情况综合考虑选择适宜的分离方法[3,4]。
表1. 单细胞分离技术
分离方法 |
原理 |
优点 |
缺点 |
有限稀释法 |
对细胞进行一系列的倍比稀释,最终使细胞处于单个状态,理论上每μL约1个细胞,然后用移液器吸取相应容积的细胞悬液进行单细胞分离。 |
操作简便;成本低,一般不需要特殊的设备。 |
分离效率低;需要研究人员排除大量空白孔和多细胞孔,费时费力;细胞分离过程依赖梯度计算,容易出现错误。 |
显微操作法 |
在高倍倒置显微镜下,利用显微镜操作器(手动或自动)实现单细胞分离。 |
能够准确地控制单细胞的吸取与释放;可以从不同的发育阶段或多样化的群体分离单个细胞。 |
通量低,需要大量的起始量;细胞特异性由显微镜决定,并利用微量移液管分离,可能不够准确。 |
流式细胞分选术 |
通过流式细胞仪,根据细胞特异性分子标志物或细胞光散射特性,分选出单个细胞或特殊细胞群,实现单细胞分离。 |
通量高;基于细胞表面标志物的特异标记,能够确保特定细胞的分离;利用荧光标记可分离亚群。 |
无法扩展到大规模项目;且需要流式细胞仪,设备昂贵。 |
激光捕获显微切割技术(LCM) |
在显微镜下,从冰冻/石蜡包埋组织切片(或细胞固定在装配有可以激光脉冲激活的热塑膜的涂片)中分离某一类型细胞群或单个细胞,实现单细胞分离。 |
无需解离组织,制备细胞悬液;能够直观准确、快速地获取单个细胞或单一细胞亚群;能够保留所分离细胞的完整性。 |
需要适当的组织处理(冷冻保存或固定);显微切割可能存在挑战;小的细胞可能难以分离;可能存在污染。 |
微流控芯片技术 |
通过微流控芯片隔离流动通道中的单个细胞从而达到单细胞分离的目的。 |
通量高;上样体积小;周期短;可根据细胞表面标志物分离特定细胞。 |
细胞大小必须均匀;消耗品昂贵。 |
2.2 全基因组扩增(Whole-Genome Amplification , WGA)
全基因组扩增是单细胞基因组测序的第二步。由于单个哺乳动物细胞中DNA的含量一般少于10pg,达不到测序仪的检测要求,因此在测序之前必须进行全基因组扩增(WGA)以获得足够的材料用于后续的文库制备。目前常用的全基因组扩增方法按原理可分为三类(见表2)[5-7]:基于聚合酶链式反应(PCR)的WGA方法{主要是简并寡核苷酸引物PCR(DOP-PCR)}、多重链置换扩增法(Multiple Displacement Amplification , MDA)和多重退火环状循环扩增技术(Multiple Annealing and Looping-Based Amplification Cycles,MALBAC)等。
表2. 全基因组扩增技术
DOP-PCR |
MDA |
MALBAC |
|
原理 |
基于PCR技术,通过加入部分简并的寡核苷酸引物与模板结合来实现扩增整个基因组的目的。 |
基于恒温核酸扩增技术,恒温条件下,使用一条由6个随机碱基构成的随机引物与模板随机退火;紧接着在具有链置换活性的DNA聚合酶作用下发生链置换反应,并最终完成扩增。 |
结合了MDA法和PCR扩增法的特点,即由一组随机引物启动扩增(每个引物具有通用引物序列和随机碱基),随机引物与模板均匀杂交,随后在具有链置换活性的DNA聚合酶作用下发生链置换反应,最终完成扩增 |
示意图 |
|
|
|
特点 |
该方法实现了高度均匀的扩增,产物产量较高,操作较为简单;但仅产生基因组的稀疏覆盖,实验的条件需要较多优化。 |
MDA可以实现更好的基因组覆盖,产物片段长;但对模板质量要求高,可能产生非特异性产物。 |
一种实现基因组广泛覆盖和均匀扩增的技术,灵敏度高,产物产量高。 |
技术平台:
目前,国内外研究机构使用的大规模单细胞测序技术平台主要有五种:Illumina® Bio-Rad® Single-Cell Sequencing Solution、BD Rhapsody™ Single-Cell Analysis System、10x Chromium Single Cell Gene Expression Solution、ICELL8 Single-Cell System和C1™ 单细胞全自动制备系统。国内也有多家企业进军单细胞测序领域,产品包括新格元自动化单细胞处理系统、万乘基因高通量单细胞测序平台、达普生物星海单细胞测序建库系统、墨卓生物高通量单细胞测序平台、德运康瑞痕量单细胞测序平台和原位测序平台等。各个平台各有特点,这里主要简单介绍一下两种应用较多的技术,即10X Genomics 公司的Chromium( 液滴法) 及 BD 公司的Rhapsody( 微孔法)。
10x Genomics单细胞测序技术:
10X Genomics单细胞测序起源自Drop-Seq技术,应用液滴微流体技术分选单细胞,将单个细胞与含有条形码(Barcode)和引物的凝胶珠一起包裹于油滴中;然后每个油滴中的凝胶珠溶解, 细胞裂解释放mRNA,通过反逆转录产生用于测序的带条形码的cDNA,cDNA在液体油层破坏后进行文库构建,使用测序平台对文库进行测序检测,即可一次性获得大量单细胞的基因表达数据。该平台具有“三高(high)两低(low)”的特点:即通量高,细胞捕获效率高,细胞活性要求高(大于90%),分析时长低,成本低。
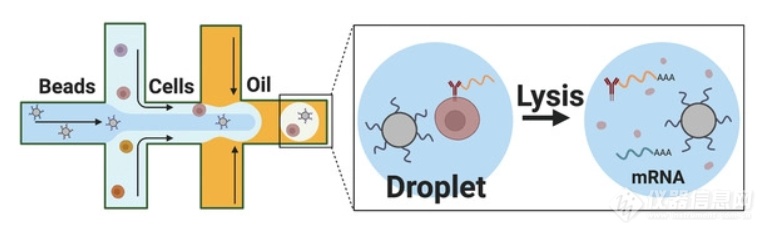

图2. 10X Genomics Chromium Controller技术原理示意图
3.2 BD Rhapsody单细胞测序技术:
BD公司推出的这款Rhapsod™单细胞分析系统采用了Cytoseq分子标签技术,能为单细胞中每个转录本标记特异性分子标签,实现单细胞水平上基因表达谱的绝对定量。同时,将每个细胞标记上特异性细胞标签,实现了高通量平行建库。该技术在基因扩增和后续的测序部分等整体流程与10x Genomics单细胞测序技术相近,主要区别在于起始的单细胞分离和捕获技术。该技术并非基于微流控芯片技术,而是基于蜂巢板技术,基于微孔来保证单细胞的捕获,避免了10x Genomics单细胞测序技术中存在的概率碰撞对捕获效率从影响。细胞悬液经注入孔注入后,自然沉降到反应孔中,随后, 将磁珠同样由注入孔注入,即可在单个反应孔中捕获其中的细胞。微孔和纳米孔方法允许稀释的细胞悬浮液在每孔一个珠子和一个细胞的条件下与寡聚结合珠一起沉降到皮升大小的孔中,从而保证了单孔中是单细胞捕获。
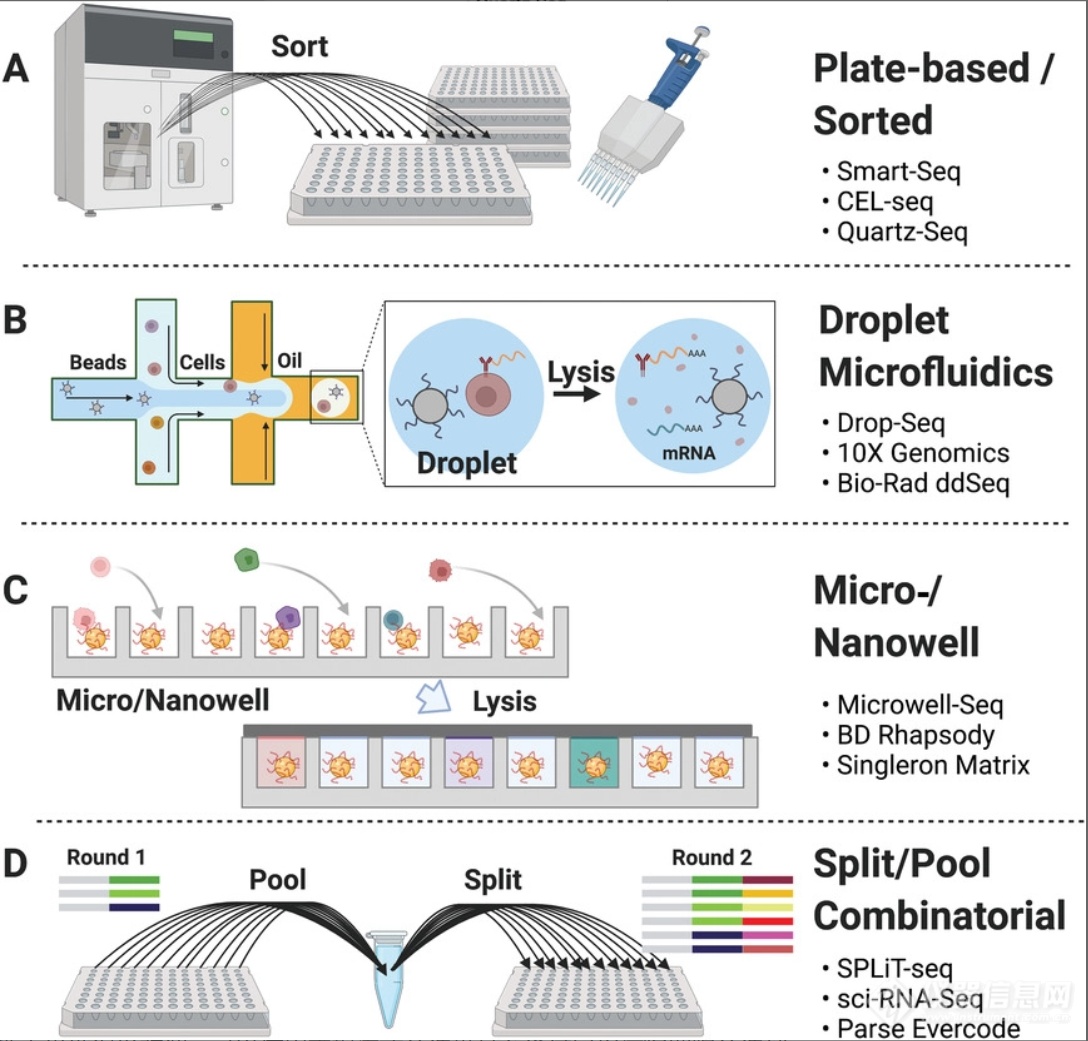

图3. BD Rhapsody技术原理示意图
4、应用实例:
目前,单细胞基因组测序技术的应用可以归纳为两大类,即应用于人类细胞图谱研究和非细胞图谱研究。单细胞基因组学的优势就在于能够揭示单个细胞的基因结构和基因表达状态,反映细胞间的异质性。自2017年“人类细胞图谱计划”提出以来,单细胞测序技术已陆续揭示了多个组织器官的单细胞图谱,如通过对肾脏肿瘤进行单细胞测序,发现肾肿瘤细胞之间的突变频率和位置不尽相同,每个细胞的突变状态和转录情况也均不相同,表明肾肿瘤更加具有异质性,需要开发更加有效的细胞靶向疗法。
2022年发表在Nature杂志上的研究,对人脑血管系统的单细胞图谱进行了分析,描绘出海马和皮质的脑血管细胞组成:内皮细胞、相邻的壁平滑肌细胞 (SMC) 和周细胞、血管周围的免疫细胞和星形胶质细胞等,这些细胞在大脑不同区域存在差异并沿动静脉轴变化,沿动静脉轴的细胞组成异质性产生了大脑健康所必需的功能分段的循环、代谢和渗透特性。揭示了人类大脑血管系统的细胞组成和分子特征,提示了阿尔茨海默病(AD)风险因素在人类中的进化转变,有助于对人类大脑健康基础的了解、疾病机制和治疗靶点的发现[8]。
随着单细胞基因组覆盖范围扩大、通量提升以及多组学技术的不断进步,单细胞基因组学技术将为丰富发育谱系树、生殖细胞突变模式、癌症进化、基因组功能和微生物群落的分辨研究等提供策略[9]。
参考文献:
[1] Xia Y, Gawad C. Bringing precision oncology to cellular resolution with single-cell genomics[J]. Clinical and experimental metastasis, 2022(1):39.
[2] Liang J, Cai W, Sun Z. Single-cell sequencing technologies: current and future. J Genet Genomics. 2014 Oct 20;41(10):513-28. doi: 10.1016/j.jgg.2014.09.005. Epub 2014 Oct 18. PMID: 25438696.
[3] Wang Y, Navin N. Advances and Applications of Single-Cell Sequencing Technologies[J]. Molecular Cell, 2015, 58(4):598-609.
[4] Gross A, Schoendube J, Zimmermann S, Steeb M, Zengerle R, Koltay P. Technologies for Single-Cell Isolation. Int J Mol Sci. 2015 Jul 24;16(8):16897-919.
[5] Gawad C, Koh W , Quake S R. Single-cell genome sequencing: current state of the science[J]. Nature Reviews Genetics, 2016.
[6] Grün D, van Oudenaarden A. Design and Analysis of Single-Cell Sequencing Experiments. Cell. 2015 Nov 5;163(4):799-810.
[7] 徐晓丽 吴凌娟.单细胞全基因组扩增技术与应用.[J]生物化学与生物物理进展 .2019.46(4)
[8] Yang A C , Vest R T , Kern F , et al.A human brain vascular atlas reveals diverse mediators of Alzheimer's risk[J]. Nature, 2022, 603.
[9] Evrony G D, Hinch A G, Luo C. Applications of Single-Cell DNA Sequencing[J]. Annual Review of Genomics and Human Genetics, 2021, 22(1).
相关会议推荐:
第六届基因测序网络会议来袭!六大会场,含单细胞和空间组学会场,点击下图免费报名!
点击链接进入会议官网:https://www.instrument.com.cn/webinar/meetings/geneseq2023/
[来源:仪器信息网] 未经授权不得转载
 中国食品接触材料国家标准进展跟踪
中国食品接触材料国家标准进展跟踪
2023.06.20

欧洲专利局判定Illumina专利无效,华大智造测序仪在多国实现销售
2023.06.21

2023.04.27

2023.06.01

蛋白质-小分子相互作用分析技术进展与应用——限制性蛋白水解-质谱分析技术
2023.06.13
「生命科学、生物技术与诊断展区」一站领略前沿,共绘未来科技蓝图
2024.08.21
版权与免责声明:
① 凡本网注明"来源:仪器信息网"的所有作品,版权均属于仪器信息网,未经本网授权不得转载、摘编或利用其它方式使用。已获本网授权的作品,应在授权范围内使用,并注明"来源:仪器信息网"。违者本网将追究相关法律责任。
② 本网凡注明"来源:xxx(非本网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责,且不承担此类作品侵权行为的直接责任及连带责任。如其他媒体、网站或个人从本网下载使用,必须保留本网注明的"稿件来源",并自负版权等法律责任。
③ 如涉及作品内容、版权等问题,请在作品发表之日起两周内与本网联系,否则视为默认仪器信息网有权转载。
![]() 谢谢您的赞赏,您的鼓励是我前进的动力~
谢谢您的赞赏,您的鼓励是我前进的动力~
打赏失败了~
评论成功+4积分
评论成功,积分获取达到限制
![]() 投票成功~
投票成功~
投票失败了~