







热爱生命科学


5月22日,国家药品监督管理局发布因美纳股份有限公司illumina.Inc.对基因测序仪主动召回的公告,公告显示,召回原因是发现一个网络安全隐患,可能导致仪器分析无法生成正确的结果或对数据安全造成潜在风险。
相关附件:
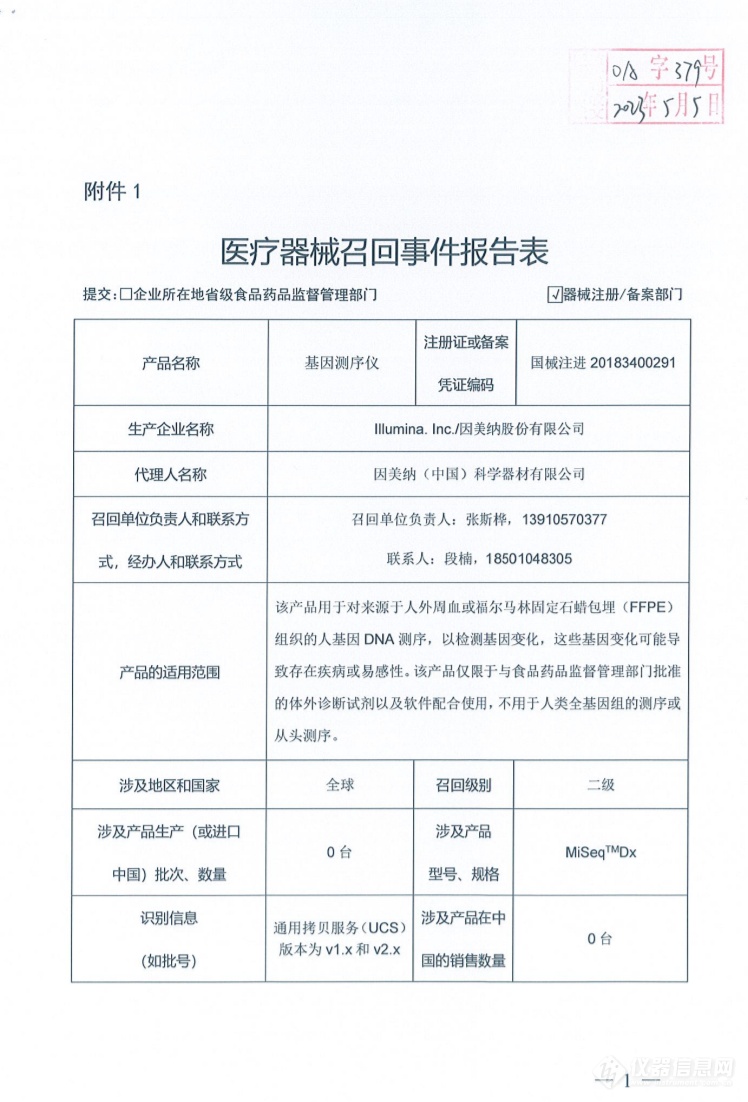

据悉,这已经是今年因美纳在华第二次召回基因测序仪。就在今年的4月6日,上海药品监督管理局官网发布召回公告,称因美纳基因测序仪(型号:NextSeq 550Dx)软件的一个组件UCS存在网络安全隐患,该安全漏洞可导致未经授权的用户远程控制仪器,改变仪器或客户网络上的设置、配置、软件或数据,或影响用于临床诊断的仪器中的患者测试结果,包括导致仪器不提供结果或提供不正确的结果、改变的结果,或数据泄露,此次召回涉及中国277台相关产品。
而在去年6月初,美国食品和药物管理局(FDA)也曾发布信件,警示临床实验室和医疗保健提供商:某些Illumina测序仪存在网络安全漏洞。FDA表示,该漏洞影响NextSeq 550Dx、MiSeq Dx、NextSeq 550、MiSeq、iSeq和MiniSeq等测序仪器上的本地运行管理(LRM)软件。2022年6月13日,FDA发布召回通知,召回illumina旗下NextSeq 550Dx 和MiSeqDx两款基因测序仪,共涉及56个国家2201台设备,其中中国423台。
[来源:仪器信息网] 未经授权不得转载

在超分辨显微镜领域 国产更容易拉近与国际距离——ACCSI2023访世纪桑尼赖博
2023.05.18

国产高端显微镜仍缺乏颠覆性创新产品——ACCSI2023访沃亿生物程柯
2023.05.18

要从市场需求出发进行高端光学显微镜的研究开发——ACCSI2023访力显科技张猛博士
2023.05.18

Illumina Q2财报公布:下调全年预期,中通量市场不佳,GRAIL完成分拆
2024.08.08

2024.06.26

2024.02.26
版权与免责声明:
① 凡本网注明"来源:仪器信息网"的所有作品,版权均属于仪器信息网,未经本网授权不得转载、摘编或利用其它方式使用。已获本网授权的作品,应在授权范围内使用,并注明"来源:仪器信息网"。违者本网将追究相关法律责任。
② 本网凡注明"来源:xxx(非本网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责,且不承担此类作品侵权行为的直接责任及连带责任。如其他媒体、网站或个人从本网下载使用,必须保留本网注明的"稿件来源",并自负版权等法律责任。
③ 如涉及作品内容、版权等问题,请在作品发表之日起两周内与本网联系,否则视为默认仪器信息网有权转载。
![]() 谢谢您的赞赏,您的鼓励是我前进的动力~
谢谢您的赞赏,您的鼓励是我前进的动力~
打赏失败了~
评论成功+4积分
评论成功,积分获取达到限制
![]() 投票成功~
投票成功~
投票失败了~