







快乐就是这么简单。


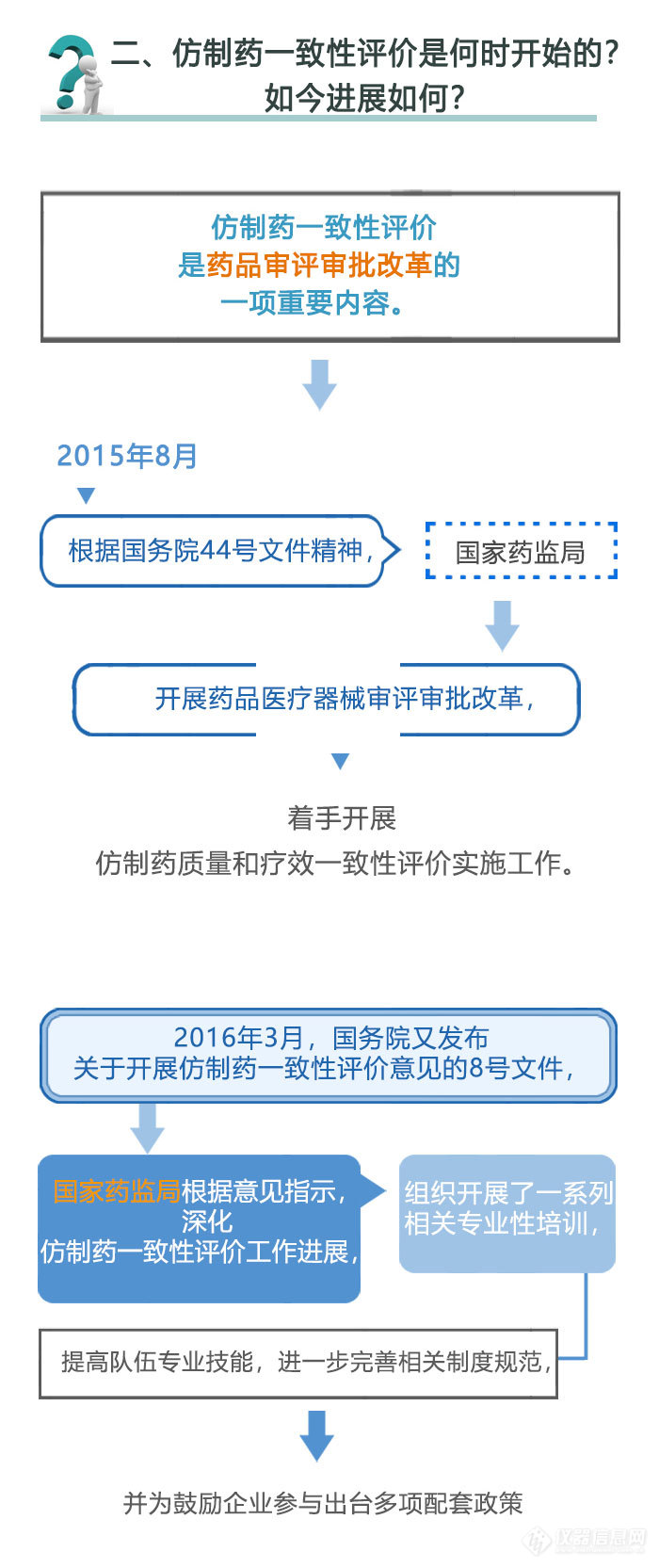
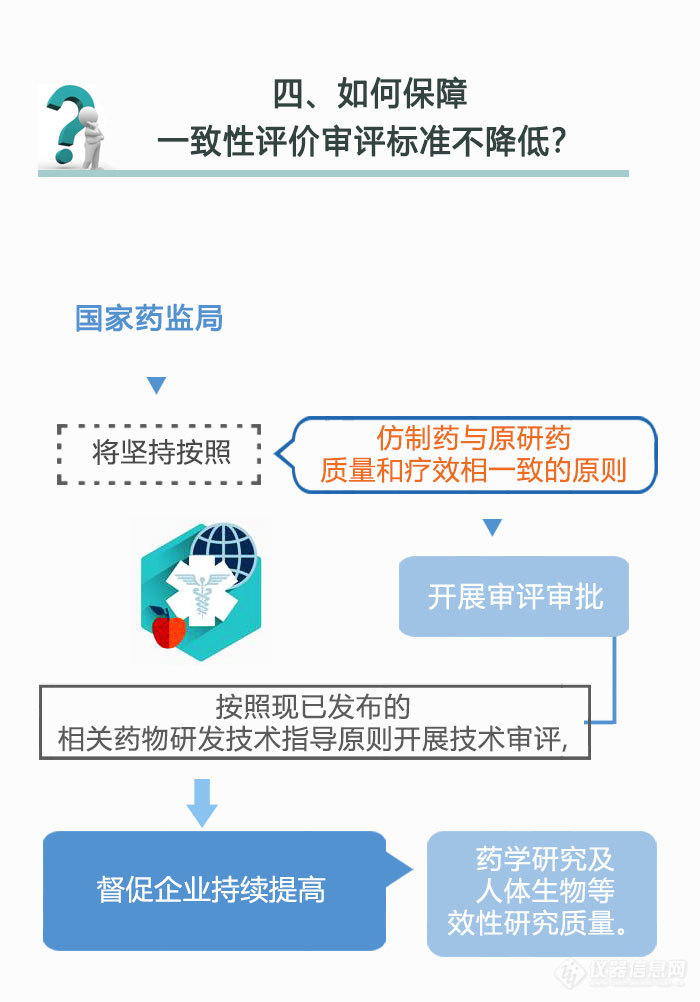
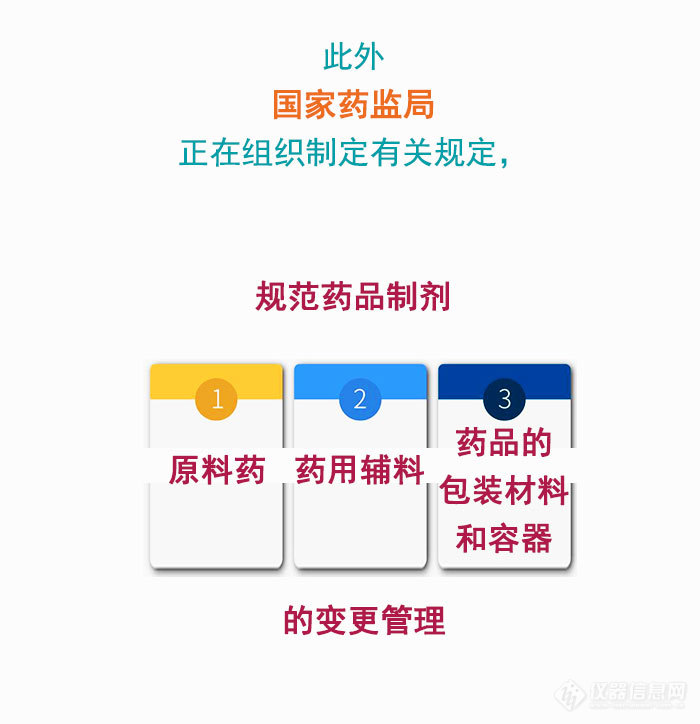
国家药品监督管理局发布图解政策,解答关于仿制药一致性评价的相关问题。据公开资料显示,我国在2012年制定了仿制药质量和疗效一致性评价政策并成立了仿制药质量一致性评价项目办公室,但是我国前期出台的大多是指导原则和文件,并无强制性政策要求。2016年3月5日,国务院办公室印发的《关于开展仿制药质量和疗效一致性评价的意见》(国办发{2016}8号)正式对外公布,标志着悬在我国已上市仿制药头上的“达摩克里斯之剑”利刃出鞘。回顾历史,我们不难发现,各国仿制药一致性评价政策,究其本质都是对历史上法规不完善时审批的品种进行了有效性再评价。一致性评价是我国也是世界各国历史发展中的阶段性政策,甚至可以说是一种必然的阶段。
下面,让我们一起来了解一下仿制药一致性评价。









[来源:仪器信息网] 未经授权不得转载
版权与免责声明:
① 凡本网注明"来源:仪器信息网"的所有作品,版权均属于仪器信息网,未经本网授权不得转载、摘编或利用其它方式使用。已获本网授权的作品,应在授权范围内使用,并注明"来源:仪器信息网"。违者本网将追究相关法律责任。
② 本网凡注明"来源:xxx(非本网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责,且不承担此类作品侵权行为的直接责任及连带责任。如其他媒体、网站或个人从本网下载使用,必须保留本网注明的"稿件来源",并自负版权等法律责任。
③ 如涉及作品内容、版权等问题,请在作品发表之日起两周内与本网联系,否则视为默认仪器信息网有权转载。
![]() 谢谢您的赞赏,您的鼓励是我前进的动力~
谢谢您的赞赏,您的鼓励是我前进的动力~
打赏失败了~
评论成功+4积分
评论成功,积分获取达到限制
![]() 投票成功~
投票成功~
投票失败了~