LAMBDA 465 测量荧光材 料漫反射率
2019/03/03 17:34
阅读:727
分享:方案摘要:
产品配置单:
紫外可见分光光度计 LAMBDA 465 /
型号: LAMBDA 465
产地: 美国
品牌: 珀金埃尔默
面议
参考报价
联系电话
方案详情:
使用光电二极管阵列分光光度计测量荧光样品
光电二极管阵列(PDA)分光光度计让这个问题迎刃而解。样品同时被全波长的光(白光)照射,然后反射方向得到的光被分解成其组分波长,分散到二极管阵列检测器像素上。采用LAMBDA 465 时,将以每1 nm 一个数据点(这款光度计采用1024 像元阵列检测器,覆盖范围达到190~1100 nm)呈现。在这种情况下,光谱真实再现了样品特征,因为记录了荧光波长而不是激发光波长。
带DRA-100 附件的LAMBDA 465 PDA 紫外- 可见分光光度计
LAMBDA 465 紫外- 可见分光光度计能够在不使用附件时达到190~1100 nm 的测量范围。DRA-100 积分球附件是积分球直径为60mm,由球体、连续150 W 氙弧灯(用于高强度照射)和电源组成。它易于安装,不需要与仪器进行电气连接。UV Lab 软件完全支持DRA-100,因此使用这款附件时,它会出现测量对话框。
该附件带标准白板(高性能,可见光区的平均反射率约为99%),搭配一个光阱(用于精确测量暗信号)和包括粉末池的各种用于测量反射率的采样配件,。由于采用氙灯,DRA-100 的工作波长范围为270~1000 nm。

Lambda 465 PDA 紫外- 可见分光光度计的DRA-100 漫反射附件
测量示例
白纸使用荧光增白剂(OBA)使变白。该OBA 基于二苯乙烯(例如4,4' - 二氨基-2,2' 二苯乙烯二磺酸)。这种高荧光化合物在375 nm 附近被激发并在440 nm附近的蓝光区域发射,如下面的荧光光谱所示
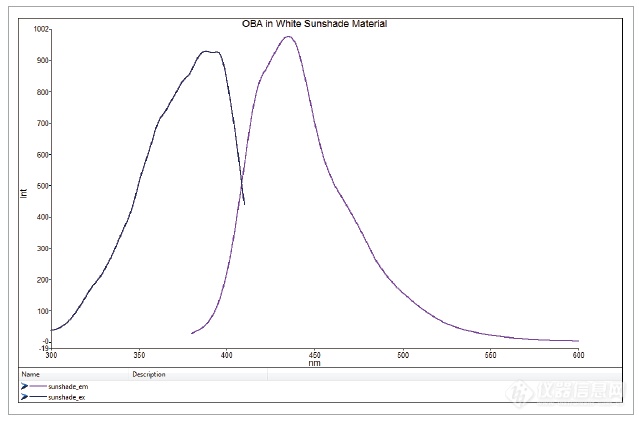
含荧光增白剂的白色遮阳材料的荧光激发和发射光谱
下图 显示了标准白色聚合物与添加有OBA 的相同聚合物之间的色差。从以下光谱可以清楚看出OBA 的额外贡献,色差可以ΔE 值(样品与目标参照物之间的L*a*b*值的差值)表示。
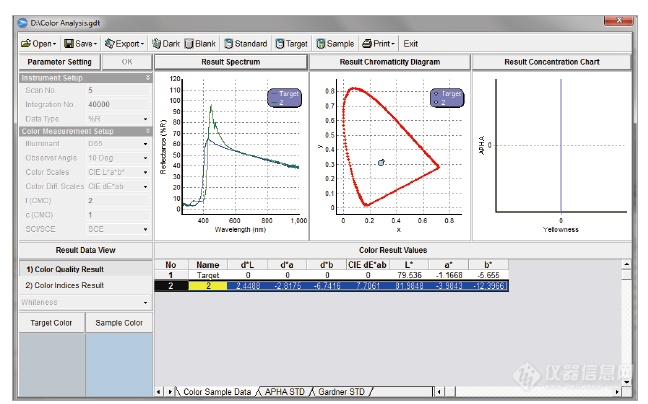
UV Lab Color 可选模块截图,显示标准白色聚合物与光学增白
白色聚合物之间L*a*b* 值的差值。
结论
配备DRA-100 漫反射附件的LAMBDA 465 PDA 紫外-可见分光光度计为快速测量含有荧光剂(如“Day-glo”涂料和颜料及高可见度材料)样品的漫反射率提供了理想的解决方案。
下载本篇解决方案:
更多![]()
HS-GCMS对聚醚多元醇中的氯氟烃和氢氯氟烃的测定分析
本文采用配有 PerkinElmer的TurboMatrix HS-40顶空自动进样器和Clarus 680-SQ8气相色谱-质谱联用仪对聚醚多元醇基体中的三氯氟甲烷(CFC-11)、二氟一氯甲烷(HCFC-22)和二氯一氟乙烷(HCFC-141b)进行了研究。文中给出了研究中所用的仪器方法参数,详细结果证明,该方法具有较好的精密度、线性度、灵敏度和回收率。
环保
2020/07/16
使用NexION 2000 ICP-MS 按照ICH Q3D 和USP <232>/<233>的规定检测和验证药用抗酸剂中的1 级和2A 级元素杂质
美国药典(USP) 宣布药品中元素杂质的新标准将于2018 年1月1日实施。通则<232> 和<2232> 基于给药途径规定了关注元素的列表及其允许的日接触(PDE)限值。此次标准更新使USP在关注元素杂质列表和PDE 方面与人用药品注册技术要求国际协调会(ICH)Q3D 第4 阶段文件相匹配。2016 年6月FDA发布了药品中涵盖ICH Q3D 的元素杂质的指导原则。随着元素杂质评估和监控期限的临近,制药厂商及其服务实验室必须立即开始执行新的法规,否则将承担违规风险。合规性要求分析方法应能准确地检测药品或(如有必要)其成分中较低的元素杂质含量,以确保患者的安全。USP 通则<232>概述了测定制成药品中元素杂质的两种分析方法:电感耦合等离子体质谱法(ICP-MS)或电感耦合等离子体发射光谱法(ICP-OES),以及相关的样品制备步骤。ICP-MS 的高性能最适合在低浓度水平下对1级元素进行常规性测定,尤其是日摄入剂量较大(>10g/ 天)的药品。在此类药品和营养品中,抗酸剂由于具有极高的钙含量,给分析造成了极大的挑战。本文旨在展示如何正确地制备样品、适当地考量各种仪器设计因素,就能轻松地克服这项挑战。在本文中, 我们展示了利用珀金埃尔默公司最新NexION® 2000 ICP-MS,依照USP 通则<233> 的规定,对抗酸剂中1级和2A级元素杂质进行验证的数据
制药/生物制药
2017/06/29
使用NexION 2000 ICP-MS 按照ICH Q3D 和USP <232>/<233>的规定检测和验证药用抗酸剂中的1 级和2A 级元素杂质Co
美国药典(USP) 宣布药品中元素杂质的新标准将于2018 年1月1日实施。通则<232> 和<2232> 基于给药途径规定了关注元素的列表及其允许的日接触(PDE)限值。此次标准更新使USP在关注元素杂质列表和PDE 方面与人用药品注册技术要求国际协调会(ICH)Q3D 第4 阶段文件相匹配。2016 年6月FDA发布了药品中涵盖ICH Q3D 的元素杂质的指导原则。随着元素杂质评估和监控期限的临近,制药厂商及其服务实验室必须立即开始执行新的法规,否则将承担违规风险。合规性要求分析方法应能准确地检测药品或(如有必要)其成分中较低的元素杂质含量,以确保患者的安全。USP 通则<232>概述了测定制成药品中元素杂质的两种分析方法:电感耦合等离子体质谱法(ICP-MS)或电感耦合等离子体发射光谱法(ICP-OES),以及相关的样品制备步骤。ICP-MS 的高性能最适合在低浓度水平下对1级元素进行常规性测定,尤其是日摄入剂量较大(>10g/ 天)的药品。在此类药品和营养品中,抗酸剂由于具有极高的钙含量,给分析造成了极大的挑战。本文旨在展示如何正确地制备样品、适当地考量各种仪器设计因素,就能轻松地克服这项挑战。在本文中, 我们展示了利用珀金埃尔默公司最新NexION® 2000 ICP-MS,依照USP 通则<233> 的规定,对抗酸剂中1级和2A级元素杂质进行验证的数据
制药/生物制药
2017/12/03
使用NexION 2000 ICP-MS 按照ICH Q3D 和USP <232>/<233>的规定检测和验证药用抗酸剂中的1 级和2A 级元素杂质Hg
美国药典(USP) 宣布药品中元素杂质的新标准将于2018 年1月1日实施。通则<232> 和<2232> 基于给药途径规定了关注元素的列表及其允许的日接触(PDE)限值。此次标准更新使USP在关注元素杂质列表和PDE 方面与人用药品注册技术要求国际协调会(ICH)Q3D 第4 阶段文件相匹配。2016 年6月FDA发布了药品中涵盖ICH Q3D 的元素杂质的指导原则。随着元素杂质评估和监控期限的临近,制药厂商及其服务实验室必须立即开始执行新的法规,否则将承担违规风险。合规性要求分析方法应能准确地检测药品或(如有必要)其成分中较低的元素杂质含量,以确保患者的安全。USP 通则<232>概述了测定制成药品中元素杂质的两种分析方法:电感耦合等离子体质谱法(ICP-MS)或电感耦合等离子体发射光谱法(ICP-OES),以及相关的样品制备步骤。ICP-MS 的高性能最适合在低浓度水平下对1级元素进行常规性测定,尤其是日摄入剂量较大(>10g/ 天)的药品。在此类药品和营养品中,抗酸剂由于具有极高的钙含量,给分析造成了极大的挑战。本文旨在展示如何正确地制备样品、适当地考量各种仪器设计因素,就能轻松地克服这项挑战。在本文中, 我们展示了利用珀金埃尔默公司最新NexION® 2000 ICP-MS,依照USP 通则<233> 的规定,对抗酸剂中1级和2A级元素杂质进行验证的数据
制药/生物制药
2017/12/03













