礼遇开学季 | 物美价更美?买一送一?你想要的,Countstar都给!
开学啦,开学啦~一大波福利准备来袭童鞋们准备好了吗?2024/3烂漫樱花月,我们又在此相遇物美价更美重点是还能买一送一拿去,拿去!不用谢!第一弹开学季-经典返场Biolab(IE1000)十多年前买过这款机器的学长学姐看了肯定很熟悉好的东西怎样都要推荐给学弟学妹Countstar Biolab(IE1000)细胞计数仪开学促销价:16,800元不仅如此买机器就送50片计数板!不够?额外加赠2年质保!足足3年质保,让你使用无忧!第二弹新品大促Mira FL-SCountstar Mira FL-S全自动荧光细胞分析仪开学促销价:41,800元再送50片Countstar细胞计数板!可帮助你轻松实现台盼蓝细胞计数、AOPI细胞计数、GFP转染效率分析,消化后的类器官活率分析等第三弹新品大促Mira BF-S使用血球计数板可直接计数神奇?神器!是的,你没有看错Mira BF-S这款机器可兼容多种计数耗材当然也就可以实现多种应用场景台盼蓝细胞分析、血球计数板细胞计数,汇合度分析、类器官计数等Countstar Mira BF-S全自动细胞分析仪开学促销价:31,800元再送50片Countstar细胞计数板!有经典IE1000又有新品Mira FL-S和Mira BF-S还有多重福利什么时候可以享受呢?促销时间:即日起-2024年6月30日宠你,就是要承包你整个春夏学期的快乐!最美的不是樱花季而是和身边的童鞋们一起走过青春岁月当然还有日日陪伴你实验看着你走进校园见证你成长进步的Countstar啦!产品在迭代,初心永不变感谢您一直以来对Countstar的支持与信赖!促销活动的最终解释权归上海睿钰生物科技有限公司所有
新品
2024.03.11
新技术来了 | 新一代细胞灌流系统
新一代细胞灌流系统➡ 理想的灌流系统当前多样化的生产环境中,生物技术公司需要快速调整生产能力以适应波动的市场需求,且越来越倾向于开发自动化程度高的连续性制造工艺,这也受到FDA等监管机构的鼓励。灌流细胞培养方式动物细胞大规模培养操作的生物反应器操作模式在实际生产中主要有3种:Batch(批培养),Fed-Batch(补料分批培养),Perfusion(灌流培养),其中的Perfusion指当接种后,在细胞增长和产物形成过程中,不断地补充新鲜培养基,同时通过细胞截留装置,将细胞截留于反应器内部,而培养基不断地流出,使反应器内的细胞处于一种营养不间断的状态。优点1、细胞所处环境良好,营养充足,代谢废物浓度低;2、提高细胞密度,提高产品产量,规模小型化;3、持续收获,产物质量提高,生产成本降低,这对于性质不稳定的产品尤其必要;4、缩短种子链,缩短生产周期。缺点1、消耗培养基多,利用率低;2、操作周期长,污染概率大;3、需验证长周期下细胞表达产品的稳定性。关注点1、新鲜培养基灌流:灌流速率的大小调节;2、细胞放流:放流速率的大小调节;3、长周期的灌流工艺培养:细胞活率的维持和产量的提高;4、细胞截留装置:细胞的高效截留和产物的高效滤过。细胞截留装置细胞截留装置的宗旨是在对细胞损伤较小的情况下,有效地实现细胞的截留和目的产物的滤过,这也是灌流工艺开发的重点所在。表1 灌流工艺中的细胞截留技术概览(网络来源)几种常见的细胞截留装置特点如表1。这其中,支持连续流生产的切向流过滤系统的应用较为广泛,包括切向流过滤(tangential flow filtration,TFF)和交替切向流过滤(alternating tangential flow filtration,ATF),二者都需要搭配中空纤维柱或平板膜等截留单元。对于TFF,细胞液通过蠕动泵作用形成一个连续的环形流动方向,进入截留单元后,废液会通过膜排出体系之外,细胞会随着环路重新回到培养体系之内。ATF用隔膜泵代替蠕动泵,通过隔膜泵的往复吹吸作用,实现罐内培养基在截留单元中的往复流动,同时代谢废物会随着培养基通过膜排出而细胞截留在反应器内。挑战与机遇灌流培养在工艺开发与操作难度上存在诸多挑战:1、复杂的准备工序,使用门槛较高;2、长周期培养的无菌维持问题;3、验证从收获到纯化得到的各“亚批次”之间的一致性;4、细胞截留装置堵塞风险。基于当前的细胞截留装置在应用过程中暴露出的问题,理想的灌流设备应具有以下特征:低剪切力、设备可选型、支持线性放大、高度自动化、简捷易操作、膜具有长生命周期、低成本、供应链稳定、售后无忧、具有配套灌流工艺解决方案。Biogenstar CTF理想的细胞灌流系统艾力特生物科技自主研发生产的Biogenstar CTF(Cross flow filtration)细胞截留系统由控制系统、创新的脉冲式空气动力循环泵和截留单元组成,配合控制系统搭载的称重系统与补液系统,可与反应器连接。其通过自动化软件为细胞连续流培养提供一站式解决方案。Biogenstar CTF 主要特点该设备可广泛应用于抗体蛋白类药物,细胞及基因治疗药物,疫苗类药物的上游工艺开发、规模放大和商品化生产。帮助生物制品行业的客户轻松实现高密度细胞培养及连续换液,加速生物工艺开发和生产。点击免费样机申请请致电400-680-9622
新品
2023.07.31
好用+大促=?当然是“把TA带回实验室”
@ 所有人HI!Countstar发来一份年中大促通知!炎热的夏天好吃解渴的西瓜才更搭配大汗淋漓的日常尤其是冰镇过的炎热的夏天丝滑好用的细胞分析仪才更搭配繁琐的细胞分析工作尤其是正在促销的是的,集性能和颜值于一身的Countstar Mira系列细胞分析仪终于开始促销了!此次促销不仅有广受欢迎的Countstar Mira系列细胞分析仪,还有热销抢手的Countstar细胞计数板,更有保障产品售后的2年质保,如此诚意满满的促销,跟着小编详细了解下吧。促销时间即日起 — 2023年9月30日终端促销价格历史低价突破想象满足“既要、又要、还要”的一站式All in拨打热线电话 400 820 2912联系Countstar当地销售Countstar Mira系列细胞分析仪自上市以来广受用户好评,该系列细胞分析仪不仅凭借一体机的设计帮您节约实验室空间,更是凭借创新的光学变倍技术帮您完美识别各种不同大小的细胞。无论是通过AO/PI双荧光细胞分析还是经典台盼蓝活率分析,都可以帮您快速精准的实现细胞计数、细胞活率的实验需求。而且,Countstar Mira FL还兼具类器官 AO/PI 计数和死活判定的应用功能,帮您实现对单个细胞、细胞簇的数量、浓度、活率、直径、面积、圆度的实验需求。Countstar Mira BF对血球计数板的兼容,帮您延续使用习惯的同时,提高对细胞分析的效率。四个月的限时优惠,欢迎广大科研工作者们试用选购,让您的细胞分析工作更得心应手。>> 文末小彩蛋 悄悄告诉你,Countstar经典产品:IE1000+50片计数板也在火热促销中,相关促销信息,可以拨打热线电话400 820 2912,也可以咨询Countstar当地销售。
企业动态
2023.06.21
艾力特生物科技2023年度全国经销商大会顺利召开
全国经销商大会 ·顺利召开· 红梅含苞傲冬雪,绿柳吐絮迎新春,在万物竞发的时节,艾力特全国各地的经销商伙伴们齐聚上海,共同举办了以“行者无疆、众行致远“为主题的2023年度经销商大会。 ·共启新章· 大会伊始,艾力特总经理做开幕致辞,他首先与大家分享了艾力特的发展情况和产品布局,并感谢所有经销商伙伴对艾力特的支持与陪伴。展望2023年,我们虽然面临着不确定性的竞争环境,但是机遇与挑战并存,大家一起携手共进,就可以走的更远。 策略是竞争制胜的关键,面对复杂的竞争环境,我们该如何团结一致呢?针对2023年的经销商策略,Countstar全国销售经理与经销商伙伴们进行了全面而细致的分享,多维度的支持体系和科学的评估激励政策都将是新一年的制胜利器,也将是我们走向更紧密合作的基石。 ·共享同营· 产品是赢得市场的永恒利器,在新的市场环境下,Countstar持续发挥细胞分析领域创新者和突破者的优势,将在2023年推出多款细胞分析仪产品,以更好的服务生命科学领域的客户。在新产品讲解和展示环节,艾力特的技术专家与经销商伙伴们全面分享了Castor系列产品和Mira系列产品的特点及应用,并在现场演示了设备的操作和使用,针对新产品可以解决的客户痛点问题进行了热烈的讨论。 站在当下的起点,我们拥有着过去努力的印记,一个个荣誉凸显着我们往日的奋斗历程。站在当下的起点,我们也怀着未来努力的方向,在所有经销商伙伴的见证下,我们一起许下携手同行的愿望,也一同种下并肩共赢的梦想。 新的一年,让我们扬起同心的风帆,荡起共赢的双桨,遨游在无边的疆域,共创出华美的篇章。
企业动态
2023.03.01
Countstar Castor X1高通量智能细胞分析仪全新上市
2022年9月7日,杭州生命科学领域先进实验室仪器与技术的提供者,艾力特生物科技(上海)有限公司(以下简称:艾力特)于近日在“2022 Biocon第九届国际生物药大会”现场举行了“Countstar CastorX1高通量智能细胞分析仪新品发布会”,生物制药领域的代表们与艾力特的专家们共同见证了艾力特全新产品CountstarCastor X1的发布。CastorX1的成功推出为Countstar细胞分析家族再添新成员,该新产品为用户带来更清晰、更智能的成像体验,以及更高效、更精准的分析结果。它集双通道荧光成像和智能数据分析于一体,可以帮助实现基于CHO和HEK293细胞的稳定高效的细胞株开发,加速产业化进程;该全新产品汇聚了细胞成像与定量分析的双重优势,帮助实现对细胞图像的量化分析,为基于HEK293细胞的细胞池筛选、病毒载体工艺开发等提供高效、准确的解决方案!全新一代Castor X1 高通量智能细胞分析仪是Castor高通量智能细胞分析平台的首款产品,“Castor”作为双子座α星,在古希腊语代表“闪亮的一个”,在Countstar产品家族也被赋予了非凡的意义,Castor X1作为该系列产品的先行者,从研发伊始,就聚焦在了高端和新智造。该新产品的上市将实现国产自主研发高通量智能细胞分析仪在该领域“零”的突破,标注着Countstar细胞分析品牌迈上了新的台阶。”CountstarCastor X1 高通量智能细胞分析仪凭借高清成像、精准识别和强大分析的优势,以及对各类 6/12/24/96/384 孔板、细胞培养皿和细胞培养瓶等耗材的兼容性,广泛应用于抗体工艺开发,细胞与基因治疗等行业,帮助实现细胞株开发过程中的单克隆源性验证、克隆生长监测,GFP/RFP细胞转染分析,无标记汇合度分析等多种应用检测,为细胞株开发提供稳定高效的解决方案,加快产业化进程。我们希望用创新和科技为生命科学领域客户带来更高效、更智能的产品体验,为生命科学的产业化发展提供更有价值的产品和技术解决方案,让生命更健康!
新品
2022.09.07
为什么你的生化培养箱,培养皿会干燥?
恒温培养箱简介恒温培养箱是一种能够将箱体内温度维持在一定温度值的实验室设备,并且具有较高的温度性能,如温度精度、波动度和均匀性等。恒温培养箱适用于微生物培养、血清、药物、培养基或标准品等样品保存,已成为现代医药、食品、医学、生化及农业等行业实验室中的不可或缺的实验设备。恒温培养箱常被称为生化培养箱,在用于20~25℃微生物培养时,又被称为低温培养箱(带有制冷功能)。恒温培养箱在制药企业QC微生物实验室,生物安全实验室以及出入境检疫检验等部门具有较大的应用,可用来检测原料、半成品和样品的微生物污染,培养皿是否合格,检测空气、纯化水以及设备表面的污染,生物指示剂的培养以检测湿热灭菌和空间灭菌的效果,培养基无菌模拟灌装试验等。尤其是在生物制药企业的QC微生物实验室中,其使用量可多达十几台甚至几十台。恒温培养箱的分类恒温培养箱可以按如下两种方式进行分类:注:1)低温培养箱也属于强制对流培养箱的范畴2)制冷功能主要分为压缩机和半导体制冷两种;3)下文所介绍的内容均按照以上表格分类进行描述,即恒温恒湿箱为不带有制冷功能的。恒温培养箱的选择在用于30~35℃,35~37℃,42~43℃和56~58℃等温度的微生物培养时,恒温培养箱是更加合适的选择,它不含制冷功能,价格也较低一些。自然对流培养箱和强制对流培养箱相比,价格并没有相差太多,而且升温时间较慢一些,花费的试验时间也更多,温度均匀性也差一些,但是很多培养箱使用部门在选型时反而首选这种型号,这是什么原因呢?在与很多使用人员接触之后,我们发现原因基本都是一样的:他们使用的强制对流培养箱在培养过程中,培养皿会干燥。在微生物培养过程中,为什么自然对流培养箱中的培养皿不会干燥,反而强制对流培养箱(也包含有的低温培养箱)中的会干燥呢?这与恒温培养箱内部气流循环设计有极大的关联。图1 示例:自然对流循环在恒温培养箱内,简单的说,自然对流循环指的是依靠空气重力自身作用进行热交换,这种方式的空气交换速率较慢,所花费的试验时间较长。而强制对流循环指的是依靠内部风机的作用,促进内部气流更快地进行热交换,以缩短试验时间。目前强制对流培养箱(包括低温培养箱)的内部强制对流主要有两种形式: 图2 示例:竖直气流 / 图3 示例:水平气流从图2和图3中可以发现,水平气流更容易将培养基挥发的水分吹走,促进培养基水分挥发,进而导致培养皿干燥。这就是很多使用水平气流强制对流培养箱(包括低温培养箱)培养皿干燥的主要原因。但是使用图2 竖直气流方式的强制对流培养箱(包括低温培养箱)就不会造成培养皿干燥,也无需倒置培养基或使用保鲜膜覆盖。水平气流和竖直气流的不同,除了与恒温培养箱内腔构造设计不同,与风机的位置也有很大关系。水平气流主要采用背部风机的方式,竖直气流主要采用顶部风机的方式,前者恒温培养箱会胖一些(深度方向尺寸大),后者会瘦高一些(深度方向尺寸小)。故选择强制对流培养箱(包括低温培养箱)时,气流方式是必须要考虑的一个重要方面。MMM强制对流培养箱MMM强制对流培养箱包含两种型号:Incucell V和Friocell,前者的温度范围为室温+10℃ ~ 100℃,后者的温度范围为0℃ ~ 100℃。这两种型号均采用竖直气流形式的强制对流循环。图4 MMM强制对流循环德国MMM集团Incucell V强制对流培养箱和Friocell低温培养箱具有其用其独特的顶置风机和暗扣积木夹套设计,在腔体内部形成至下而上的螺旋上升气流,将不规则的气流变得更加规则和均匀。这种气流循环设计,是德国MMM集团与德国慕尼黑工业大学共同研发的成果。图5 Friocell 707 ECO低温培养箱Incucell V强制对流培养箱和Friocell低温培养箱在全球广泛应用于制药工业、食品和饮料加工工业、疾控和出入境系统、化妆品工业、高校科研领域、农业、水资源管理和医院等方面,在中国市场已有千台以上的保有量。德国MMM集团德国MMM集团是世界上最大的实验室箱体制造商之一,其总部位于德国慕尼黑,在全球有多家工厂,生产实验室箱体、脉动真空灭菌柜和清洗机等设备。其实验室箱体主要分为干燥箱、培养箱和稳定性试验箱3个系列,进入中国市场已有20年时间。干燥箱:Ecocell自然对流烘箱、Venticell强制对流烘箱、Vacucell真空干燥箱、Stericell干热灭菌箱、Durocell耐腐蚀干燥箱培养箱:Incucell自然对流培养箱、Incucell V强制对流培养箱、Friocell低温培养箱、CO2cell二氧化碳培养箱稳定性试验箱:Climacell恒温恒湿箱、2~8℃稳定性试验箱、光稳定性试验箱
新品
2020.10.11
汽化过氧化氢灭菌程序及过程介绍
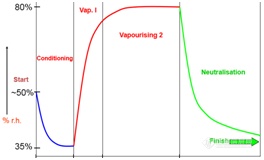
对GMP车间洁净区定期进行灭菌是保证生产产品质量的一个重要环节。目前在我国对空间进行灭菌的常用方法是比较传统的甲醛熏蒸法。甲醛的杀菌能力不容置疑,但是随着科学技术的发展以及人们环保意识的增强,其越来越受到专家的质疑,因为甲醛是一种三致危害物。为了解决甲醛灭菌时间过长以及毒性和残留问题(会产生结晶状残留物),国内有不少企业开始采用汽化过氧化氢灭菌技术。过氧化氢是一种广谱杀菌剂,汽化过氧化氢灭菌技术由于灭菌时间短、无毒、无残留,且灭菌效果容易验证,广泛被欧盟国家认可。我国的GMP认证要与欧盟接轨,洁净区采用过氧化氢灭菌技术必然为大势所趋。目前汽化过氧化氢灭菌已成为各国药典、药品生产质量管理规范(GMP)、消毒灭菌技术规范所推荐的方法,灭菌工艺已经非常成熟,重复性好,有专门的化学指示剂和生物指示剂验证过氧化氢气体分布均匀情况和无菌保证水平。可广泛应用于生物制药、医疗卫生、生物实验室和动物研究实验室等诸多领域。一、试剂与仪器:(1)生物指示剂(BiologicalIndicator,BI):106CFU/片的嗜热脂肪芽孢杆菌,ATCC12980;(2)化学指示剂(ChemicalIndicator,CI);(3)浓度为35%的食品级过氧化氢溶液;(4)胰蛋白胨大豆肉汤培养基(TSB);(5)PEA MLT-17zeta汽化过氧化氢发生器;(6)PEA LiRo气体分布系统;(7)灭菌车间:某疫苗生产单位GMP洁净车间,洁净区层高2.8m、面积100㎡,空间总体积约280m3。图1、某疫苗生产单位GMP洁净车间二、灭菌过程:整个灭菌过程分为以下几个阶段:(1)将PEA MLT-17 zeta发生器和LiRo气体分布系统推入洁净区前,先将设备表面用75%酒精擦拭清除干净,根据灭菌空间体积大小,向储液桶内添加足量的过氧化氢溶液;(2)通过洁净车间的空调系统对洁净区的温度和湿度进行调控,使二者达到设备可以灭菌运行的区间范围;(3)在洁净车间内布置足量的生物指示剂和化学指示剂,并做好标记;(4)在设备端设置灭菌程序,一个完整的灭菌循环主要包含以下4个部分:调试阶段(Waiting,Conditioning,Heating),主要是为人员撤离以及设备预热阶段;快速注入阶段(Vapourizing1),在此阶段过氧化氢气体以一个较快的速率注入待灭菌空间,环境中过氧化氢气体浓度迅速升高;慢速注入阶段(Vapourizing2),在此阶段过氧化氢气体以一个较慢速率注入待灭菌空间,维持过氧化氢气体浓度保持一定的时间;降解阶段(Neutralisation,Afterrun,End),在此阶段过氧化氢气体迅速分解产生水分和氧气,环境中过氧化氢气体浓度迅速下降。图2、灭菌循环主要灭菌程序设置(5)当温、湿度达到指定范围后,关闭空调系统,人员撤出灭菌洁净车间,启动灭菌循环,对车间进行门密封;(6)灭菌循环结束,开启空调通风系统通过洁净空气置换以排除房间内部残留的过氧化氢,从而使房间内空气中过氧化氢气体浓度低于职业允许暴露水平1ppm;(7)收取化学指示剂和生物指示剂,观察统计化学指示剂的变色情况,无菌操作取出生物指示剂将其接种到TSB培养基中,所有培养基均需在培养箱中55℃~60℃的条件下进行培养,观察培养24h后和第7天的结果,同时做好阳性对照和空白对照;(8)经过24 h的培养,若培养液变浑浊,则判定为阳性;若培养液澄清,则为阴性;继续培养至第七天,如果培养液变浑浊,则判定为灭菌不合格;如果培养液澄清,则判定为灭菌合格。三、灭菌结果:汽化过氧化氢灭菌技术,可对空气与物体表面进行生物除染,是一种非常有效的消毒灭菌方法。PEA的汽化过氧化氢灭菌技术整个过程采用全自动化智能控制,可精确控制过氧化氢气体浓度,材料兼容性好,可减少对工作人员与环境的危害,其灭菌过程、工艺具有重现性,绿色、环保、安全可靠。图3、PEA发生器和气体分布系统在车间内的摆放位置及BI和CI的布点位置灭菌循环结束,所有的化学指示剂均变色明显,表明过氧化氢气体在空间内分布均匀;所有的生物指示剂无论是在培养的第24h或者培养结束的第7天,培养基均未变浑浊,表明灭菌合格。汽化过氧化氢灭菌技术是目前用于可密闭空间(如GMP车间、医院病房、实验动物中心、小型仓库等)和各种人造设备(如隔离器、冷冻干燥机、孵化箱、传递窗、生物安全柜、压力蒸汽灭菌器、过滤器和各类风管及管道等)的一种可靠的消毒灭菌方法,具有广阔的发展前景,是取代甲醛和臭氧等传统空间消毒灭菌的理想方法,也是今后空间消毒灭菌的发展趋势。
厂商
2020.04.28
气化过氧化氢空间灭菌的相关法规和验证
一、法规《药品生产质量管理规范(2010年修订)》主要是参照欧盟GMP并结合国内的实际情况进行修订的,共14章,313条,同时还新修订发布了无菌药品、原料药、生物制品、血液制品和中药制剂的附录,各项要求更加细化,明显提升了无菌制剂的洁净度要求。新版药品GMP提出了洁净区A、B、C、D分级以及相应更为严格的环境悬浮粒子与微生物的控制要求,其目的是为了防止生产中污染、混淆、交叉污染和人为差错的产生。新版GMP的发布和实施缩小了中国和国际GMP管理要求的差距,它对于推动中国制药行业的国际化进程,推动制药行业提高质量管理水平,保证人民群众用药安全将起到重要作用。洁净室为了达到相应的室内环境,除了控制洁净室内空气的含尘度外,对细菌和微生物的存在数量也要进行控制。进入洁净室内的空气,虽然经过初效、中效、高效过滤器三级过滤,把大多数尘埃粒子及附着其上的细菌和微生物阻滞在洁净室外,但是它们仍然存在于空调系统的设备、管道、风口及过滤器上,一旦有适宜的环境就会繁衍生殖。还有少量的细菌和微生物穿透各级过滤器进入洁净室内,成为洁净室内微生物。如果不对洁净室进行消毒灭菌,它们将不断繁殖,破坏室内空气环境品质,影响产品质量。因此,应定期对洁净室进行灭菌消毒。新版GMP无菌药品附录1第四十五条认为:必要时,可采用熏蒸的方法降低洁净区内卫生死角的微生物污染,应当验证熏蒸剂的残留水平。这也就对新版GMP下洁净厂房的灭菌设计提出了较高的要求。医药工业的洁净室传统消毒(灭菌)方式主要有:消毒液(甲醛熏蒸)灭菌法、臭氧消毒(灭菌)法。对洁净室气体消毒的传统办法是将消毒液通过蒸发来熏蒸,通常的消毒液有环氧乙烷、过氧乙酸、甲醛溶液等。甲醛杀菌效果的3个重要因素:提升温度、限定相对湿度和改进穿透条件。当相对湿度在65%以上,温度在24~40°C时,消毒效果最好。但甲醛熏蒸存在着一系列不可忽视的缺点:由于每次化学试剂熏蒸消毒灭菌时间最少需24 h,不能天天进行,因此目前各生产厂家大多采用每月1次大消毒,而微生物污染源—— 人、物、料、室外新鲜空气等却天天要进出洁净室,其带入的微生物不能得到及时杀灭,会出现微生物随时间延长而增加的现象。甲醛有强烈的刺激性气味,消毒灭菌后去除残留气味时间长,对生产操作人员身体有害。甲醛作为较高毒性的物质,具有强烈的致癌和促进癌变作用,是公认的变态反应源,也是潜在的强致突变物之一。所以,应用受到限制,欧盟GMP明确规定不能使用甲醛进行洁净厂房灭菌。甲醛熏蒸会出现多聚甲醛聚合物(白色粉末),附着在洁净室内的维护结构和设备管道表面上,在消毒后几天内,其悬浮离子数会增加,甲醛聚合物也逐渐解聚成甲醛,对生产操作人员的危害很大。甲醛气体的穿透性差,一般不能穿透到物品包的中心或导管的内部,不易精确控制操作过程中气体浓度,也不能保证影响甲醛杀菌能力的因素得到有效的控制。臭氧消毒的浓度按臭氧消毒的效率和卫生部颁布的《消毒技术规范(2002年版)》的标准,对空气中的浮游菌,臭氧灭菌的浓度为2~4ppm,只需要将臭氧发生器开启1~1.5h;对物体表面的沉降菌,臭氧灭菌的浓度为10~15ppm,需要将臭氧发生器开启时间调到2~2.5h。环境条件:环境温度16~28℃;相对湿度45%~65%;室内无外界强气流,无强烈阳光照射或其他热辐射。消毒时关闭新风口和回风口排放阀门,使整个被消毒的洁净区空气通过净化系统风管形成循环,臭氧发生器开始工作。臭氧消毒的缺点也非常明显,即高浓度对人体有害,与设备表面和建筑材料的兼容性较差,容易使铜片出现锈斑,橡胶老化,且其灭菌环境要求相对湿度>60%等。汽化过氧化氢(VHP)灭菌技术,是利用过氧化氢在常温下气体状态比液体状态更具杀孢子能力的优点,经生成游离的羟基,用于进攻细胞成分,包括脂类、蛋白质和DNA,达到完全灭菌要求的一种技术。常用于隔离室、隔离器等密闭空间的灭菌。汽化过氧化氢(VHP)灭菌干燥、作用快速、无毒无残留,物质相容性较好,包括很多金属和塑料,适用于房间、生物安全柜、传递窗、动物笼交换站、隔离器和医疗器械等表面的灭菌消毒。生物净化时间短,根据待处理产品的物理特性,生物灭菌时间30~90min,对更广范围的微生物有效,生物灭菌循环中不产生有毒残留物,对于其他物品影响不大(装置、电器、洁净室墙板等)灭菌所需时间短,容易验证。缺点是汽化过氧化氢要做到完全汽化较难,完全做到的汽化过氧化氢造价往往比较昂贵。德国PEA的VHP汽化过氧化氢发生器采用最新的第三代干法闪蒸技术,不仅闪蒸温度控制稳定,汽化完全,产生的过氧化氢气体粒径小,而且在灭菌的不同阶段可以设置不同的注入速率,在保证灭菌效果(可将SAL控制在10-6以下)前提下,提升物料兼容性;相对于国产设备的闭环终端喷放过氧化氢气体,PEA VHP汽化过氧化氢发生器采用开环开放式气体循环方式,气体分布系统的配合使用更使过氧化氢气体分布均匀,有效扩展消毒灭菌体积,降解速度也得到了较大的提升。而移动式脚轮设计,使得灭菌方式更加灵活,可以对不同的区域独立灭菌,相对于固定式空调机组VHP灭菌方式,无疑大大降低了成本和造价。二、验证验证是中外制药企业GMP管理的重要组成内容。验证的定义最早见于美国食品药品监督管理局FDA公布的《药品工艺检查验收标准》(1978年6月):“一个已验证的工艺系指已能证实按预计或所声称的那样运行的工艺。验证的证据是通过尽可能收集和评估工艺开发阶段的数据,以及以后生产阶段的数据获得的。验证必须包括工艺确认(材料、设备、系统、建筑及人员的确认),以及重复性生产的批或运行的整个工艺的控制”。我国新颁布的《药品生产质量管理规范(2010年修订)》在第十四章第三百一十二条将验证定义为“证明任何操作规程(或方法)、生产工艺或系统能够达到预期结果的一系列活动”。GMP中验证概念的引入标志着质量管理从“质量检验”提升至“质量保证”,被称为是GMP发展史的里程碑。无菌药品洁净区域的化学气体熏蒸灭菌,要求其可安全地使用于不锈钢、钢、塑料、玻璃、环氧地面、墙壁等各种表面,并对包括孢子在内的微生物进行快速、有效的灭菌控制,能通过对生物指示剂挑战性试验:经含菌量为105~106和103的菌条灭菌后,应能够降低相应的对数单位。消毒灭菌方法的验证是极其重要的,只有通过验证,才能肯定消毒灭菌方式的有效性和安全性。无菌药品的要求采用了最新的世界卫生组织和欧盟 A、B、C、D 分类,对无菌药品生产的洁净度、级别提出了具体要求,要求达到动态A级的标准,增加了在线监测,特别是对悬浮粒子的静态、动态监测,对浮游菌、沉降菌、生产环境中的微生物和表面微生物的监测都作了详细的规定。目前汽化过氧化氢灭菌法已成为各国药典、药品生产质量管理规范(GMP)、消毒灭菌技术规范所推荐的方法,灭菌工艺已经非常成熟,重复性好,有专门的商业化的非常标准的化学指示剂和生物指示剂用来检测灭菌过程中过氧化氢气体分布的均匀性和最终的灭菌效果。
厂商
2020.04.28
微生物监测在生物安全实验室中的一种应用
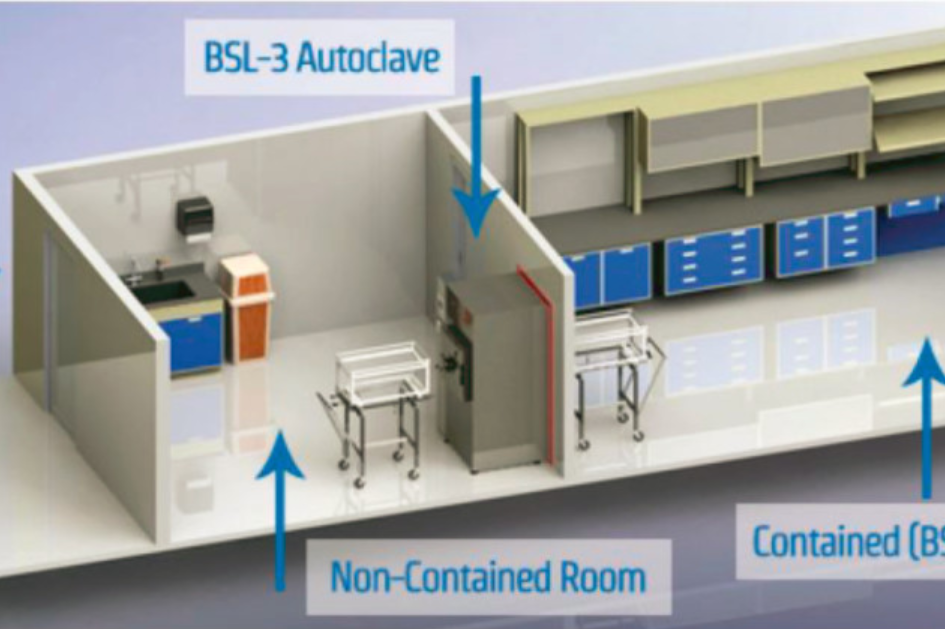
17年前,SARS冠状病毒引起的“非典”事件,回想起来,仍让人心有余悸。17年后,武汉又爆发了轰动全球的新型冠状病毒肺炎感染事件。1月12日,世界卫生组织(WHO)正式将造成武汉肺炎疫情的新型冠状病毒命名为2019-nCov。2月8日下午,国务院应对新型冠状病毒肺炎疫情联防联控机制成员现决定,将新型冠状病毒感染的肺炎暂命名为“新型冠状病毒肺炎”,英文名为“Novel coronavirus pneumonia”,简称“新冠肺炎”,英文简称NCP。2月11日晚,国际病毒分类委员会的冠状病毒研究小组(CSG)在医学类预印本发布平台 medRxiv 发表最新关于新型冠状病毒命名的论文,宣布新型冠病毒“2019-CoV”的正式分类名为严重急性呼吸综合征冠状病毒2(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)。另外,在该篇论文发布前两个小时,世界卫生组织(WHO)也将由新型冠状病毒所致的疾病,正式命名为“COVID-19”。时值春节假期期间,武汉新型冠状病毒肺炎感染事件为中国最重要的节日蒙上了一层阴影;而亿万人东西南北流动的春运,又令肺炎感染事件雪上加霜,也给全国的交通、医院和疾控系统等带来了巨大的挑战。中国疾病预防控制中心表示,本次发现的新型冠状病毒与SARS和MERS冠状病毒虽同属于冠状病毒这一大家族,但基因进化分析显示它们分属于不同的亚群分支,它不是SARS,也不是MERS病毒,它们的病毒基因序列差异比较大。冠状病毒在自然界中非常常见,分为很多类型,所造成的危害差别也很大,引起武汉病毒性肺炎疫情的病原体为一种新的冠状病毒,有别于SARS病毒。中国疾病预防控制中心和各省市疾病预防控制中心(简称疾控中心)承担着全国和各个省市的疾病预防与控制、应急预警与处置、疫情收集与报告、监测检验与评价、健康教育与促进、应用研究与指导、业务培训与保障、技术管理与服务等政府对社会的疾病控制职能。疾控中心的建设要符合我国现行的生物安全实验室各项标准,目前国际上依据实验室所处理对象的生物危险程度,把生物安全实验室分为四级:一级对生物安全隔离的要求最低,四级最高。我国目前有两个四级生物安全实验室:湖北武汉BSL-4病毒实验室(中国科学院武汉国家生物安全实验室 )和国家动物疫病防控高级别生物安全实验室(中国农业科学院哈尔滨兽医研究所)。科研人员在BSL-3实验室工作而三级生物安全实验室,即BSL-3实验室,是国家及几乎所有省和直辖市疾控系统中最高等级的生物安全实验室,在疾病预防与控制、应急预警与处置、监测检验与评价等工作中发挥着巨大的作用。BSL-3实验室相对于BSL-1实验室和BSL-2实验室,主要是进行特殊的诊断和研究,脉动真空灭菌柜和过氧化氢空间灭菌器等都是必不可少的安全设施。德国MMM脉动真空灭菌柜 德国PEA气化过氧化氢空间灭菌器本次新型冠状病毒需要在BSL-3实验室及以上实验室才能进行实验,所以有极高的无菌要求。传递进出的物品都要灭菌,常见待灭菌物质有:固体(如金属器械、实验室设备、实验室玻璃器具等),多孔物质(如衣物、试管等),开口的液体容器(如实验室内装满水溶液的三角瓶等),生物废弃物(如带菌的培养基、动物尸体)等。而如何保证脉动真空灭菌柜灭菌效果是至关重要的,因为BSL-3实验室实验操作过程所产生的固体或少量液体废弃物中含有病毒和细菌等有害物质,若病毒等有害物质未完全灭活被排出实验室,其对周边环境有很大污染风险,甚至会将致命病毒传播出去,因此必须要对BSL-3实验室脉动真空灭菌柜灭菌效果进行验证,把污染风险降到最低程度。BSL-3实验室脉动真空灭菌柜灭菌效果监测方法主要包括以下几类:一、物理参数监测在脉动真空灭菌柜的HMI界面上直接监视腔体和夹套温度、压力、灭菌时间等参数,并使用打印机打印、记录下来。另外,脉动真空灭菌柜在整个工作流程过程中,若有温度或压力未满足参数设定值要求,则系统会发出报警,要求运维人员对相应影响因素进行改进。脉动真空灭菌柜每次运行均须对物理参数进行监测,如灭菌阶段温度、压力和灭菌时间等。若灭菌程序运行过程中有报警发生,必须消除故障后再次运行该程序,直到程序完全运行且无报警发生方可开门取出废弃物。二、化学监测化学监测是利用化学指示剂(CI= Chemical Indicator)在一定温度、作用时间与饱和真空适当结合的条件下受热变色的特点,用于间接指示灭菌效果或灭菌过程的监测方法。化学监测常用的方法有:1)BD测试:用于检查灭菌器腔体经抽真空后残留冷空气的浓度,监测真空水平、是否漏气等,残余冷空气的存在是灭菌器灭菌失败的主要原因。测试时将标准BD测试包放于灭菌器排气口上方,灭菌器内不能放入其它待灭菌物品。循环完成后,取出BD包验证是否满足要求。BSL-3实验室每日开始灭菌运行前进行,合格后方可使用。2)指示胶带:放在灭菌包外,BSL-3实验室每个灭菌包包外均应贴有包外化学指示胶带或包外指示卡,用于指示每一包物品是否经过了灭菌处理。3)指示卡:可以指示灭菌温度和持续作用时间,以间接指示灭菌效果。监测时应放于测试包或待灭菌包内。每次灭菌都要使用,每包必用。灭菌后指示色块达到标准颜色为合格,若发现包内指示卡不合格,应找出原因,重新灭菌处理直到合格为止。三、生物监测:生物监测是一种利用生物指示剂(BI= Biological Indicator)对脉动真空灭菌器灭菌效果进行验证的重要监测方法。将纯棉手术斤折叠成23cm x 23cm x 15cm大小的标准试验包,将两支嗜热脂肪地芽孢杆菌(ATCC7953)放于包中心,将试验包置于灭菌器腔体冷凝水排放口上方,门关闭并密封后从程序列表中选择固体灭菌程序,灭菌周期完成后从包中取出,挤碎指示管内安瓿让培养液浸透管内菌片,放于56℃专用恒温培养箱内培养48h,连同阳性对照管观察结果。所有包内灭菌后指示管内培养液均没有变色,同时阳性对照管内培养液变成黄色,可判定灭菌合格。脉动真空灭菌器每周应进行一次生物监测。BSL-3实验室过氧化氢空间灭菌器灭菌效果监测方法:不同于脉动真空灭菌器是对实验操作过程所产生的固体或液体废弃物进行灭菌,气化过氧化氢空间灭菌系统是对BSL-3实验室物体表面及空间进行消毒或灭菌,能有效降低生物安全实验室的生物负载,也能保证生物安全实验室的无菌操作环境。不同的BSL-3实验室,需要设计不同的过氧化氢空间灭菌方案。过氧化氢空间灭菌器灭菌效果的验证时通过在难以灭菌的位置处放置BI生物指示剂、CI化学指示剂,如天花板、地板等难以到达的角落。CI化学指示剂变色均匀,BI生物指示剂不锈钢片上分布有嗜热脂肪地芽孢杆菌(ATCC12980),灭菌后在55-60℃专用恒温培养箱中进行培养以检测灭菌效果,BI是判断灭菌成功与否的唯一标准。使用生物监测进行灭菌效果的验证时,BI生物指示剂,即嗜热脂肪地芽孢杆菌的培养对恒温培养箱具有较高的要求:1. 其中非常重要的是温度的均一性(TemperatureUniformity/In Space):例如在做56℃嗜热脂肪地芽孢杆菌培养时,要求温度均一性为±1℃,即在任一时刻和搁板上任一位置处,温度均在55~57℃范围之内,超出0.1℃即视为偏差和不合格。2. 升降温时间:微生物实验室恒温培养箱/生化培养箱的使用是非常频繁的,有时候一段时间内开关门的次数会较多,使腔体内温度较快的出现偏差。如何保证恒温培养箱在关门之后进行快速的温度恢复,是衡量其性能的重要因素,故疾控系统、以及出入境检疫检验部门和制药领域的微生物实验室更倾向于采用不锈钢电阻加热管和压缩机制冷的恒温培养箱。3. 培养效果:有些恒温培养箱经过几天运行之后,会出现培养皿中培养液干燥凝固的情况,造成菌体培养失败或失效。恒温培养箱采用顶部回风和侧面送风的循环方式是避免这种情况的一种比较合理的设计。德国MMM恒温培养箱恒温培养箱/生化培养箱不仅可以培养BI生物指示剂,用于脉动真空灭菌器和过氧化氢空间灭菌器灭菌效果的监测,保证生物安全实验室的安全,还可以用于一次性使用卫生用品如手套、口罩和防护服等的微生物检测和卫生保证。如GB19082-2009和GB15979-2002中规定了产品微生物检测方法,其中大肠杆菌检测方法:取样液5mL,接种50mL乳糖胆盐发酵管,置35℃±2℃培养24h,如不产酸也不产气,则报告为大肠杆菌群阴性。如产酸产气,则划线接种伊红美蓝琼脂平板,置35℃±2℃培养18-24h,观察平板上菌落形态。典型的大肠杆菌落为黑紫色或红紫色,圆形,边缘整齐,表面光滑湿润,常具有金属光泽,也有的呈紫黑色,不带或略带金属光泽,或粉红色,中心较深的菌落。取疑似菌落1-2个作革兰氏染色镜检,同时接种乳糖发酵管,置35℃±2℃培养24h,观察产气情况。除了以上生物安全实验室的应用,恒温培养箱/生化培养箱在制药领域无菌控制方面也发挥着必不可少的作用,如《中国药典》2015版四部和2020版四部生物检定通则增修订(公示中)中都明确了其应用和微生物培养的方法。2020版四部生物检定通则增加了灭菌用生物指示剂指导原则,用于脉动真空灭菌器和过氧化氢空间灭菌器灭菌效果的生物监测。2015版四部中如1101无菌检查法,用于检查药典要求无菌的药品、生物制品、医疗器具、辅料、原料及其他品种是否无菌的一种方法,防止微生物污染。恒温培养箱/生化培养箱主要应用包含:培养皿、培养瓶是否合格的检测;空气、纯化水、设备表面等以及原料、样品、半成品的检测,防止微生物污染,保证无菌操作和生产,此时培养的真菌或细菌所需的温度为20~25℃,30~35℃,35~37℃和42~43℃等,要求的温度均一性仍为±1℃。一般疾控系统微生物实验室和出入境检疫检验部门使用几台小的恒温培养箱/生化培养箱(Reach-In)进行BI生物指示剂或细菌、真菌的培养即可满足要求。而对于一些制药企业来说,无论从实验室空间占用方面,还是培养箱内部容积和价格成本方面来说,多台小的恒温培养箱/生化培养箱并不是最优的解决方案,步入式培养箱(Walk-In)反而是更好的选择。Aralab步入式培养箱(通过步入式培养箱门上观察窗进行观察)
厂商
2020.04.28
关于灭菌柜BD测试,您应该知道的!
BD测试是什么?图1:验证中的脉动真空灭菌柜一般脉动蒸汽灭菌柜除了每年的年度工艺参数验证确认外,还要对灭菌过程进行监测从而保证在灭菌确认中所确定的各项灭菌参数能够始终在日常的灭菌工作中保持恒定。针对这一方面ISOl7665也作出了相应的规定。除了要对灭菌基本的工艺参数验证,如灭菌过程的温度、时间和压力运行过程作出记录外,还要使用相应的生物和化学指示物对灭菌过程进行监测,这其中会涉及到相关的国际标准,例如ISO11138(生物指示物),ISO11140(化学指示物),ISO14161(生物指示物的挑选、使用和测试结果解释的评估,通过使用适当的物理、化学和指南),ISO15882(化学指示物的挑选,使用和测试结果解释的指南),EN一285(蒸汽灭菌器≥54L),EN—l3060(小型蒸汽灭菌器我们都知道湿热灭菌原理是利用饱和蒸汽释放潜热使微生物的蛋白质及核酸变性灭活,研究表明如果灭菌蒸汽中含有1%的空气,则灭菌蒸汽的传热系数将降低60%,直接导致灭菌温度达不到设计标准,因此必须将脉动真空灭菌柜内的空气完全排除。所以要求灭菌腔室内最好没有空气残留,让进入腔体的蒸汽是饱和的,最大效力的发挥灭菌效力。通常待灭菌的包裹放置于灭菌舱内,如果要对其进行灭菌的话就必须首先将包裹内部的空气抽出来,然后将蒸汽打入到灭菌包裹的内部,并均匀分布于包裹内的各个部分,然后蒸汽才能在特定的温度和时间下发挥其灭菌功能。所以为了证明灭菌柜空气移除能力而诞生了BD包。(这里做个小小的纠正: BD测试又叫设备排气能力测试和蒸汽穿透测试,很多人把BD测试和真空测试混为一谈。)谈到BD测试包,就不得不说说BD测试的起源:他们设计了一个6.6KG的布包,在这个布包的中心位置放上灭菌指示胶带,然后把它放置于灭菌柜内进行灭菌。如果这个灭菌指示胶带在灭菌后能够均匀地变色,说明这个灭菌器已经具备了将包裹内的空气全部抽出、同时将蒸汽穿透到这个布包内部的能力,这个灭菌器则可以每日进行灭菌工作了。之所以采用这个布包是因为当时医疗卫生领域的大部分灭菌物品为敷料类,或纺织品类和实体的器材,即无腔无孔的器材,因此当时认为这个布包代表了最难排气和蒸汽对灭菌物品的穿透情况,如果能够对它进行灭菌的话,那么医疗领域的大部分物品就都能被灭菌了。最初的BD测试使用的是测试布包,这个测试布包有2个版本,即欧洲版本为7kg,美国的版本为4kg,标准的BD测试布包在实际使用中是非常不方便的,而且其性能的稳定性很差。因为每个人打包的质量并不总是相同的,而且打包使用的布由于多次的洗涤也会影响BD测试的结果。所以目前国际上多使用可反复使用的BD测试装置,它们的形式多种多样,这些装置的内部可放置化学指示条,每次使用完毕后将指示条拿出检查结果并存档,再次使用的时候只需替换其中的指示条即可,既方便又经济。针对这些BD测试装置国际上也都有相应的标准(即ISOll140-4和ISOl1140-5)。BD测试目的成功的B& D测试表明蒸汽可以快速均匀地渗透到测试包中。空气留在包装内可能导致测试失败。由于以下原因,空气可能滞留在包装内:2. 有空气漏入消毒室;综合EN 554及ISO 17665-2两项标准,BD的运行频率得看具体的设备使用情况:2. 当设备连续工作时,每天相同的时刻运行一次,但可以是任意时刻。图2:BD测试因为BD是测试正常工作状态下的机器性能,而“冷锅”状态下运行BD(即每天设备第一次启动运作),不但测试环境不符合正常工作状态下的条件,也不符合BD测试包的设计使用要求,会导致错误的结果指引,因此BD测试并非是每天第一锅做!建议提前运行一遍预热程序,之后再去运行BD测试。BD包放在腔体可用灭菌空间的几何中心轴线上,距离腔体底平面100--200mm的高度,由BD测试支架支撑。BD测试程序中参数要符合BD测试包制造商的要求,特别是作用温度和维持时间。相关的要求参考 ISO 11140-5。常见的BD测试包有115℃121℃、134℃等多种规格的,根据实际情况选择适合的既可,灭菌时间要求参见各BD测试包厂商要求。对121℃而言,灭菌时间为8min,对134℃而言,灭菌时间为3.5min。通常而言测试时间越短,对灭菌器的性能要求越高。因为时间短要求灭菌柜在更短的时间内产生足以令BD测试物变色均匀的热量。BD程序必须要与要运行的灭菌程序具有相同的空气去除阶段,否则就不能检测灭菌状态下的系统性能。正常我们的MMM脉动真空灭菌柜适用于固体多孔程序都会进行四次脉动,与BD测试程序脉动次数一致。BD测试结束后按照BD测试包制造商的使用说明验证测试结果,看颜色变化是否均匀。(图3)我国的BD试验大多采用的是4公斤的包,与美国标准一样。但欧洲标准一般比美国标准更严格,要求使用7公斤测试包。我们MMM Sterivap系列灭菌柜符合欧洲标准。理论上,根据欧洲标准设计出的正常灭菌器可以100%通过4公斤的BD测试,但根据美国标准设计的设备却很大几率不能通过7公斤的BD测试。因此关于BD包的选择,取决于您使用的灭菌器的设计标准,如果是根据美国标准设计,则必须使用4公斤包。如果是欧洲标准设计,最好应使用7公斤的BD包,因为使用4公斤的BD包,理论上会100%通过,但这样的测试结果不足以作为日程设备监测的参考。F&Q&对于BD测试常见的几个问题及解释如下A1:根据美国标准对化学指示剂的定义,b-d测试纸/包是第二类化学指示剂——用于测定测试的化学指示剂。Q2:请问是不是所有的压力蒸汽灭菌器都需要做b-d测试?A3:b-d测试是专用于测试预真空或脉动真空压力蒸汽灭菌器内或物品包内冷空气是否彻底排出,物品包内有否冷空气团存在,作为检测考核预真空压力蒸汽灭菌器是否可以正常工作的重要手段。Q4:请问b-d测试的操作方法,以及b-d测试的结果判定?A5:按照“消毒技术规范”的规定,要求预真空和脉动真空压力蒸汽灭菌器每日进行一次b-d测试,检查他们的空气排除效果。Q6:bd试验不理想(合格),生物监测合格,是否可以继续进行灭菌工作?A7:一般bd测试第一次失败后,可能是由于预真空锅的预热没有达到,或者整个设备管道中的冷空气还没有排尽等因素造成,从而影响了第一次bd测试的结果。第二次bd测试的意义在于完全的排出上述的干扰因素后,评估预真空锅的真空水平。Q8:bd包内的bd纸能否抽出后换成新的继续使用?A8:bd包就是为一次性使用而设计的,重复的使用可能造成包内材料的老化或者性质改变,失去标准包的功能,从而造成实验的不准确。
厂商
2020.03.05
抗击疫情丨逆行而上检修河南省疾控脉动真空灭菌柜
发布时间:2020-02-26浏览次数:2020年2月19日,应河南省疾控预防控制中心BSL-3实验室脉动真空灭菌柜紧急设备检修维护需求,艾力特生命科学第一时间作出响应并派出我司工作人员到达该一线抗疫单位,在做好安全防护工作后对设备进行维护保养,确保该台德国MMM脉动真空灭菌柜能在此后抗疫工作中能继续稳定高效运行。 如其他抗疫一线单位需要我们的设备或者紧急检修维护服务,我们都将第一时间响应,支援一线,义不容辞。目前,我司德国MMM生物安全型灭菌柜在中国大陆地区有16台在生物安全三级实验室(BSL-3)使用,涉及十四家省级CDC和国家级生物安全三级(BSL-3)实验室,德国MMM BSL-3级脉动真空灭菌柜正在为奋战在一线的抗疫科研人员保驾护航,相对于普通灭菌柜,德国MMM脉动真空可以做到极高水平的生物安全防护,保护实验人员的安全。▌《新冠检测技术指南》要求2020年1月22日国家卫生健康委员会发布《新型冠状病毒感染的肺炎实验室检测技术指南(第二版)》中指出实验活动暂按照病原微生物危害程度分类中第二类病原微生物进行管理,有要求如下:1、病毒培养 在病毒的分离、培养、滴定、中和试验、活病毒及其蛋白纯化、病毒冻干以及产生活病毒的重组试验等操作应在具有开展相应活动资质的生物安全三级(Biological Safety Level 3,BSL-3)实验室进行;2、动物感染实验 指以活病毒感染动物的实验,应在具有开展相应活动资质的动物(Animal)BSL-3(ABSL-3)实验室进行操作。3、未经培养的感染性材料的操作 未经培养的感染性材料在采用可靠的方法灭活前进行的病毒抗原检测、血清学检测、核酸检测、生化分析等操作,应在生物安全二级(BSL-2)实验室操作,但个人防护装备参照生物安全三级(BSL-3)实验室的防护要求。WHO 和美国 CDC 等也发布了相关指南,指导实验室检测及临床诊治,指南建议核酸检测在生物安全第二等级(BSL-2)设施中进行。▌实验废弃物排除根据GB19484-2008《实验室安全通用要求》中规定,生物安全三级(BSL-3)实验室在防护区内需设置生物安全型的双扉高压蒸汽灭菌柜,试验过程中产生的固体废弃物和少量液体废物物需经过专用的高压蒸汽灭菌柜灭活后排出。 ▌极高水平的生物安全防护针对于生物安全实验室可以顺利安全的开展相应的研究工作,德国MMM sterivap BSL3级灭菌柜可以做到极高水平的生物安全防护,保护实验人员的安全,为奋战在一线的科研人员保驾护航。1 独有的生物密封技术(抗震级别)在实验室墙体埋如不锈钢边框,配合设备的密封边框和墙体的连接采用软性硅胶条进行可靠的密封,达到气密性隔离,有效隔绝实验室内气溶胶泄漏:2 高效率的脉动真空系统脉动体现在多次抽空再注入饱和蒸汽的过程,研究表明如果灭菌蒸汽中含有1%的空气,则灭菌蒸汽的传热系数将降低60%,直接导致灭菌温度达不到设计标准,因此必须将脉动真空灭菌柜内的空气完全排除。BMT sterivap BSL3级灭菌柜采用双级水循环泵,能节约70%的水消耗的同时,还能将腔体压力可以抽空至6kpa以下,达到到100%的空气移除能力,让饱和蒸汽进入待灭菌物品的内部,进行100%的有效灭菌。区别于普通固体多孔物品的脉动真空灭菌,对于液体的物品例如培养基等需要无脉动灭菌,BMT Sterivap BSL3级别灭菌柜采用重力移除方式进行灭菌。独有的设计会在灭菌过程中冷凝液收集在腔室内,一起和灭菌的物品进行灭菌。与常见的脉动真空灭菌柜区别如下3 进气过滤器方面的要求:按照灭菌设计要求需配置可更换滤芯的不锈钢外壳的空气过滤器。过滤后的空气用于灭菌循环结束后平衡腔体内外压力和对门加压密封,对0.2um过滤器过滤效率至少要到达99.9 % ,同时过滤器需带有批次在线灭菌功能,建议每年更换1次。 4 灭废过滤器要求 生物安全三级(BSL-3)实验室装载侧位于走廊侧门的污染区,在开门时可能会含有病原微生物的空气进入高压蒸汽灭菌柜腔体,同时被灭菌的废弃物中也会含有病原微生物,在开始灭菌抽真空时腔体内的空气必须经过高效过滤器过滤方可排出,高效过滤器在每个灭菌循环中都应该被灭菌,该过滤器建议每年更换1次。5 灭菌冷凝水处理 普通的高压蒸汽灭菌柜开始灭菌循环后产生的冷凝水直接通过排水口排入地漏,而生物安全型高压蒸汽灭菌柜在开始灭菌循环后产生的冷凝水则是会被收集灭菌,待灭菌完成后才会通过地漏排出。德国MMM集团脉动真空灭菌柜严格遵循各项法规要求进行设计、制造、测试和验收,对灭菌全过程进行温度和压力的在线监测和实时打印,整个过程均可被追溯。广泛应用于制药厂、实验室、科研单位、BSL-3实验室等,对物品进行消毒灭菌,满足6log的灭菌效果。德国MMM集团作为全球灭菌器品牌的领导者,通过不断的创新和优化制造的生物安全型灭菌器为奋斗在对抗疫病一线实验人员提供更佳的灭菌解决方案及生物安全保护。艾力特生命科学为MMM集团在中国的独家代理,在此疫情时期,我司仍会继续提供高效完善的售前咨询、方案设计、设备运输安装及售后服务,为抗疫一线单位提供我们最大的支持。
厂商
2020.03.05
浅谈气化过氧化氢灭菌的第三代干法闪蒸技术
引言发达国家已禁止在食品和药品生产车间使用甲醛熏蒸进行空间消毒,因为其毒性很大,长期接触会引发呼吸功能障碍和肝中毒性病变,选择既安全有效又卫生环保的消毒剂和消毒设备是卫生消毒领域发展的方向。过氧化氢因具有氧化还原作用而具有杀菌效果,汽化过氧化氢(VHP)灭菌技术,是利用过氧化氢在常温下气体状态比液体状态更具杀孢子能力的优点,通过复杂的化学反应解离具有强氧化性的羟基,用于攻击细胞的成分,包括破坏细胞膜、脂类、蛋白质和DNA,达到完全灭菌的要求的一种技术。图1.VHP灭菌技术原理干法VS湿法灭菌技术目前主要分为两大阵营,分别为干法VHP(Vaporized Hydrogen Peroxide)灭菌技术和湿法HPV(Hydrogen Peroxide Vapour)灭菌技术。干法VHP定义微冷凝是湿法的一种,通过一种亚微米级的微冷凝膜覆盖在物体表面,在凝结过程中使微生物失去活性。真正的干法闪蒸技术,过氧化氢完全气化,整个灭菌过程空气中和物体表面均看不见任何液滴,在空间做布朗运动,分布均匀。控制在气化过氧化氢冷凝点以下,灭菌浓度低于饱和浓度,并在整个灭菌工艺上控制不冷凝。工艺无需除湿,不控制湿度,高湿灭菌,会因为天气等原因而变化。最大可达600m3材料兼容性易腐蚀,对于彩板、设备等材质要求较高,高浓度的H2O2冷凝液在接触表面会使橡胶材料变坏,腐蚀和损坏电子产品。第三代干法闪蒸工艺灭菌技术主要利用高温闪蒸,将过氧化氢溶液滴加至加热到一定温度的光滑金属物体表面使其瞬间汽化,再喷射到环境中进行消毒灭菌。灭菌后产物为水分和氧气,环保无残留。随着时间发展和技术进步,干法闪蒸工艺也在不断发展完善,经历了不同的阶段,现在对市场上的工艺做以总结:第二代干法闪蒸工艺:突出代表是一些国产设备,相对于第一代工艺,在过氧化氢注入速率的问题上得到改善,不同的阶段以不同的速率喷射过氧化氢,如:快速注入阶段以较高速率喷射过氧化氢,迅速将环境中过氧化氢气体浓度拉升;慢速注入阶段以较低速率喷射过氧化氢,维持环境中过氧化氢气体浓度进行灭菌,完美解决了第一代工艺的弊端。但第二代工艺一般都是将闪蒸后的过氧化氢以灭菌设备为原点不断向空间进行喷射,其弊端也是显而易见的:空间气体分布不均匀,在灭菌设备近处,过氧化氢气体浓度极高,远端则浓度偏低;汽化不完全,工艺不稳定,有腐蚀的风险。图2.实现变速注入后灭菌周期中环境VHP浓度及相对湿度变化图3.PEA VHP灭菌技术为完整的闭环循环PEA VHP灭菌技术如下图所示,为某细胞治疗企业GMP车间待灭菌区域布局图,该区域面积125㎡,体积约为325m3,根据车间体积大小及布局情况,设置灭菌程序进行灭菌。图6.某细胞治疗企业GMP车间待灭菌B级区德国PEA自创立以来就一直专注于过氧化氢灭菌技术的优化,密切关注客户需求与技术创新,为实验室、制药工业、科研院所、医院、动物房、军队、公共场所等领域的用户提供全方位的灭菌技术和灭菌设备。以下为某抗体生产单位的PEA MLT17 zeta(专门用于制药行业空间灭菌)的PQ验证数据及生物指示剂(BI)和化学指示剂(CI)布点情况及最终的实验结果。图8.某抗体生产单位连续PQ验证环境中VHP浓度及相对湿度控制图9.GMP车间PQ验证现场BI及CI的布点情况图10.灭菌结束所有的CI变色明显,BI培养结果呈阴性灭菌技术用于空间的消毒灭菌,绿色、环保、安全可靠,是目前用于可密闭空间( 如GMP车间、医院病房、实验动物中心、小型仓库等) 和各种人造设备( 如隔离器、冷冻干燥机、孵化箱、传递窗、生物安全柜、压力蒸汽灭菌器、过滤器和各类风管及管道等) 的一种可靠的消毒灭菌方法,具有广阔的发展前景,是取代甲醛和臭氧等传统空间消毒灭菌的理想方法,也是今后空间消毒灭菌的发展趋势。
厂商
2020.02.24
法规热力灭菌相关名词解释
热力灭菌相关术语在各指南中有所不同,现在将常用热力灭菌常用术语进行解释,热力灭菌常用术语如下。1) Z值Z值表示使微生物的D值变化一个对数单位所需要升髙或下降的温度。常用于累计一个灭菌程序在加热和冷却阶段随温度变化的杀灭时间。--Z= (T1-T2)/(lgD2-lgD1) (2-7)3) F0是指Z取10℃时,一个湿热灭菌程序赋予被灭菌品121摄氏度下灭菌的等效灭 菌时间。新版灭菌指南十月一号生效后,建议f0启始计算温度为110℃5) FPHY物理杀灭时间(FPHY)指以灭菌程序的物理参数计算的杀灭时间。而 FPHY是灭菌率L对时间的积分值。FPHY = △t∑10(T-Tref)/Z (2-9)7) 无菌保证水平无菌保证水平(Sterility Assurance Level,SAL)是指产品/物品经 灭菌后微生物残存的概率,描述灭菌后非无菌单元概率。在制药工业中,预期的设计终点是 无菌保证水平≤10-6,即灭菌后微生物存活的概率不得大于百万分之一。9) 热穿透测试热穿透测试为评价灭菌柜腔室内传递给被灭菌品能量而进行的温度测试,测试用探头应放置于被灭菌物品中。11) 平衡时间平衡时间是指灭菌腔室(腔室参照温度通常是排水口探头温度)达到最低设定灭菌温度和装载达到最低设定灭菌温度之间的时间间隔,后者由加热最慢的热穿透 探头测得。它体现了灭菌柜去除装载中空气并对装载加热的能力。
厂商
2020.02.24
EN285法规与MMM BMT 灭菌柜
德国MMM集团是全球最大灭菌设备的专业制造商之一,成立于1954年,在德国、捷克和美国都有灭菌生产基地,经过几十年的发展和壮大, 德国MMM集团已在制药行业、实验室、医疗、工业等领域为全球众多客户提供高品质专业设备。EN285由CEN(英国标准化委员会)起草。根据CEN / CENELEC内部规定,以下国家的国家标准组织必须实施本欧洲标准:德国,捷克,法国,意大利,英国,波兰,西班牙,瑞典,瑞士,奥地利,比利时等。本欧洲标准在灭菌器的设计方面,制定了全面且详细的要求和规范,包括:设备的必要组件、管路系统及关键部件、监测系统、控制系统。除此之外,此标准还制定了细致的测试步骤和接受标准以检测设备的性能。正如CEN/CENELEC的内部规定:德国,捷克等国家必须完全贯彻并实施本标准。下面我们主要从设备的重要组件、关键部件、管路设计、监测系统等方面为大家概述介绍EN285的要求。材质要求与蒸汽接触的材质:;- 不会导致蒸汽质量下降- 双门不能同时打开(除维修等特殊需求)-(应按照下图设计,且标记a:螺纹管道-PT,ISO 228--G1/2A)管路系统及关键部件与蒸汽接触的管路的材质应不会污染蒸汽、能够抵抗蒸汽及冷凝水高于 腔室温度指示 腔室温度控制 腔室温度记录 腔室绝对压力指示;对于双门设备,此压力指示应该在每一侧都提供 腔室绝对压力控制 腔室绝对压力记录 夹套压力指示(如果设备配有夹套) 蒸汽压力指示(如果安装蒸汽发生器) 测量系统b)以及e)可以组合(见图j)a d g h 可以组合在一个显示系统中测量通道及计时器温度探头:要么使用符合2008的EN60584-1:2013的公差 0,9 ≤--50~150℃ 在1% 分辨率不超过-0.5 K 具有温度误差补偿,由环境温度引起的测量误差不超过a)bar或者公斤显示 范围为:绝对压力:c)1 kPa(d)5 kPa;计时器:测量误差不超过每个设定时间间隔的11年用于数据导出的软件应与用于控制循环的模块独立开控制系统灭菌柜应该由一个自动控制器操作,此自动控制器有+3K小于15s;800L的设备,平衡时间<-- 彼此之间温差不超过BD 测试:测试试纸应该显示出均一的颜色变化真空泄露测试:任何情况下不能超过0.13kpa/min除此之外,实验室和制药区域里所有MMM灭菌柜都能满足相关的质量需求(如pressure vessel directive、machinery directive、DIN58951、DIN58950、GMP、cGMP、GAMP、FDA CFR21 Part 11等)。MMM产品在整个完整的产品生命周期里因自身质量的可靠性而表现突出,这是通过“德国制造”的高精度的一流生产工艺和满足最高要求的成熟的控制系统来保证的。顶尖质量的材料,资深的技术人员和高标准的以工艺为导向的质量保证体系造就了MMM集团最高水准的设备。
厂商
2020.02.24
冠状病毒检测过程中涉及生物安全初探
2019 年 12 月底,武汉爆发新型冠状病毒(2019-nCoV)感染导致的肺炎,2020年1月22日国家卫生健康委员会发布《新型冠状病毒感染的肺炎实验室检测技术指南(第二版)》中指出实验活动暂按照病原微生物危害程度分类中第二类病原微生物进行管理,有要求如下:1、病毒培养 在病毒的分离、培养、滴定、中和试验、活病毒及其蛋白纯化、病毒冻干以及产生活病毒的重组试验等操作应在具有开展相应活动资质的生物安全三级(Biological Safety Level 3,BSL-3)实验室进行;2、动物感染实验 指以活病毒感染动物的实验,应在具有开展相应活动资质的动物(Animal)BSL-3(ABSL-3)实验室进行操作。3、未经培养的感染性材料的操作 未经培养的感染性材料在采用可靠的方法灭活前进行的病毒抗原检测、血清学检测、核酸检测、生化分析等操作,应在生物安全二级(BSL-2)实验室操作,但个人防护装备参照生物安全三级(BSL-3)实验室的防护要求。WHO 和美国 CDC 等也发布了相关指南,指导实验室检测及临床诊治,指南建议核酸检测在生物安全第二等级(BSL-2)设施中进行。 从目前掌握的新型冠状病毒的生物学性状、传播特性、致病性、临床资料等信息,考虑到新型冠状病毒感染聚集性发病且有重症病例,并有死亡病例的特点,实验活动暂按照病原微生物危害程度分类中第二类病原微生物进行管理,和口蹄疫、高致病性禽流感病毒、艾滋病毒(I型和II型)、SARS冠状病毒等大家常见病毒为同一类,这样就对实验室生物安全方面提出了挑战。本文将从试验废弃物处理、试验设备和空间消毒灭菌、标本运输安全等三个方面对潜在风险层面进行分析,以供相关专业人士参考。一、试验废弃物根据GB19484-2008《实验室安全通用要求》中规定,生物安全三级(BSL-3)实验室在防护区内需设置生物安全型的双扉高压蒸汽灭菌柜,试验过程中产生的固体废弃物和少量液体废物物需经过专用的高压蒸汽灭菌柜灭活后排出。因此,生物安全型的双扉高压蒸汽灭菌柜是生物安全三级(BSL-3)实验室不可或缺的设备,同时生物安全型的双扉高压蒸汽灭菌柜在制造和选型方面有着特殊的要求。1、生物安全密封方面的要求 生物安全型的双扉高压蒸汽灭菌柜横跨污染区和非污染区,这样就对灭菌柜和墙面的密封提出了较高的要求,正常情况下在装载侧进行生物安全密封,故在设备选型过程中需要注意灭菌柜腔体外侧至设备设备外侧装饰板内侧从上到下、从左到右需要至少用AISI 304不锈钢板满焊。同时在设备外层装饰板与墙壁的密封处需要用不锈钢板进行锚定并用优质硅胶进行密封。特别要注意的是在设备与墙壁密封处不用不锈钢板锚定只是简单的用硅胶进行密封在长时间运行后因硅胶老化发生病毒泄漏,造成生物安全事故。如1967德国马尔堡病毒实验室感染事件、1979年前苏联斯维尔德洛夫斯克炭疽菌泄漏事件、2003年新加坡国立大学实验室SARS感染事件、2004中国大陆中国疾病预防控制中心实验室SARS感染事件等等。 2、进气过滤器方面的要求 按照灭菌设计要求需配置可更换滤芯的不锈钢外壳的空气过滤器。过滤后的空气用于灭菌循环结束后平衡腔体内外压力和对门加压密封,对0.2um过滤器过滤效率至少要到达99.9 % ,同时过滤器需带有批次在线灭菌功能,建议每年更换1次。3、灭废过滤器 生物安全三级(BSL-3)实验室装载侧位于走廊侧门的污染区,在开门时可能会含有病原微生物的空气进入高压蒸汽灭菌柜腔体,同时被灭菌的废弃物中也会含有病原微生物,在开始灭菌抽真空时腔体内的空气必须经过高效过滤器过滤方可排出,高效过滤器在每个灭菌循环中都应该被灭菌,该过滤器建议每年更换1次。 4、进蒸汽的方式 相较与普通的高压蒸汽灭菌柜而言,生物安全型高压蒸汽灭菌柜进蒸汽的位置有较大的不同。普通的高压蒸汽灭菌柜的蒸汽由蒸气发生器产生纯蒸汽后通过不锈钢管路从腔体的侧面或顶部分布器在腔体内分布,灭菌循环开始后腔体内空气、空气蒸汽混合物通过腔体底部的排水口排出,而生物安全型高压蒸汽灭菌柜的蒸汽则由腔体底部进入腔体,灭菌循环开始后腔体内的空气、空气蒸汽混合物通过灭废过滤器过滤后排出,从而避免开始灭菌抽真空过程中腔体含有致病微生物的空气、空气蒸汽混合物被排出实验室。5、灭菌冷凝水处理 普通的高压蒸汽灭菌柜开始灭菌循环后产生的冷凝水直接通过排水口排入地漏,而生物安全型高压蒸汽灭菌柜在开始灭菌循环后产生的冷凝水则是会被收集灭菌,待灭菌完成后才会通过地漏排出。 二、试验设备和空间消毒灭菌 生物安全实验室是通过实验室设计建造、实验设备的配置、个人防护装备的使用,通过严格遵守预先制定的安全操作程序(SOP)和管理规范等综合措施,确保操作生物危险因子的工作人员不受实验对象的伤害,确保周围环境不受其污染,但往往在实验室中与各种病原微生物相关,所以做好安全防护和环境消毒灭菌是预防的重要手段。传统的方法多采用甲醛熏蒸和紫外灯照射的方法,由于甲醛具有刺激性气味,而且对眼睛、呼吸道、皮肤具有不良刺激,高浓度溶液可引起皮肤凝固性坏死,为A类致癌物质。在甲醛灭菌后需要进行中和,中和后白色会有结晶物产生,且很难完全清除。紫外灯照射照射方法灭菌因紫外线照射需要直接照射被消毒物体表面或空气才起作用,而对被遮挡的墙壁表面、地面和工作台面等则不起作用。随着大家对环境和人身安全的关注,气化过氧化氢空间灭菌技术越来越受到设备使用的喜爱,它是一种将液态过氧化氢转换成气态过氧化氢的灭菌方法,其主要特点是干燥、作用快速、无毒无残留等优越性。1、灭菌全过程控制 作用原理是将30%~35%浓度液体过氧化氢通过高温闪蒸板气化成气态过氧化氢,然后输送到实验室空间内,过氧化氢气体进行分子无规则布朗运动对空气和物体表面进行消毒。该技术普遍运用于生物安全实验室。过氧化氢消毒包括准备阶段(预热除湿)、调节阶段(过氧化氢气体快速注入)、灭菌阶段(过氧化氢气体慢速注入以维持其室内浓度)、降解通风4个阶段。 2、闪蒸温度控制 众所周知,35%浓度的液体过氧化氢沸点是108℃,传统的低温闪蒸技术无法实现过氧化氢完全气化,这样就会在灭菌全过程中有高浓度的过氧化氢液体被喷射到设备表面、彩钢板墙面及环氧地坪处,从而造成腐蚀气泡,而这些腐蚀气泡可能会给了气溶胶传播这一类致病微生物隐藏空间,无法运行气化过氧化氢空间灭菌技术进行完全灭菌,从而导致实验室发生感染,比如结核分枝杆菌。 3、数据传输 由于生物安全三级(BSL-3)实验室是密闭的负压实验室,无法像普通实验室一样进行数据的纸质数据的记录和直接传递,目前多采用实验数据记录与传输的计算机网络进行数据的传递,这样就需要对气化过氧化氢空间灭菌设备提出了要求,设备自身需带有存储功能和网络端口。4、对生物安全实验室环境保持的影响 生物安全三级(BSL-3)实验室正常状态下是负压状态,实验室的气流采用定向流动控制。在气化过氧化氢空间灭菌设备运行过程中实验室内温度、湿度变化均会对实验室负压状态有一定的影响,故在设备运行过程中需要监控设备闪蒸板和房间的温度、房间的湿度都是身份必要的。5、新型冠状病毒期间要注意的事宜根据国家卫生健康委员会发布《新型冠状病毒感染的肺炎实验室检测技术指南(第二版)》中未经培养的感染性材料的操作可在生物安全二级(BSL-2)实验室进行,实验室定期采用气化过氧化氢空间灭菌设备对实验室空间内、检测设备内外表面潜在病毒进行灭菌是十分必要,特别是肩负保护检测人员安全的生物安全柜因其HEPA过滤器、风道及排风管道更无法使用传统方法灭菌。目前已知的华中科技大学协和医院、武汉市金银潭医院、青岛一附院等医院检验科人员在未接触病人情况下发生感染。 三、标本运输安全根据国家卫生健康委员会发布《新型冠状病毒感染的肺炎实验室检测技术指南(第二版)》中国内运输要求:新型冠状病毒毒株或其他潜在感染性生物材料的运输包装分类属于A类,对应的联合国编号为UN2814,包装符合国际民航组织文件Doc9284《危险品航空安全运输技术细则》的PI602分类包装要求;环境样本属于B类,对应的联合国编号为UN3373,包装符合国际民航组织文件Doc9284《危险品航空安全运输技术细则》的PI650分类包装要求;通过其他交通工具运输的可参照以上标准包装。新型冠状病毒毒株或其他潜在感染性材料运输应按照《可感染人类的高致病性病原微生物菌(毒)种或样本运输管理规定》(原卫生部令第45号)办理《准运证书》。 在新型冠状病毒疫情期间,为保护检验人员安全,对用于样本运输的样本转运箱在进入实验室前尽可能采用紫外灯或臭氧传递窗灭菌对样本运转箱外表面进行灭菌,有条件的生物安全三级(BSL-3)实验室也可采用带有集成过氧化氢发生器的传递窗进行灭菌。笔者发现市面也有带过氧化氢接口的生物安全型高压蒸汽灭菌柜,以实现双扉高压蒸汽灭菌柜、过氧化氢传递窗双功能。
厂商
2020.02.20
重要!新型冠状病毒研究人员的生物安全防护
重要!新型冠状病毒研究人员的生物安全防护艾力特生命科学 艾力特生命科学 昨天中国工程院院士李兰娟指出:“疫苗成功研制至少还要三个月。”李兰娟随后解释说“三个月”仅是初期研发的时间,比如培养疫苗株、检测和验证等,新型肺炎疫苗真正走向市场还有很长的路。漫长的研究进程,极易扩散传播的病毒,这就对广大研究人员的生物安全防护提出了更高更严峻的要求,因为目前除了奋战在一线的医护人员被感染的案例见诸报端以外,已经有研究人员,甚至是检验技师被感染的报道出现。青岛新增1例患者详情公布!曾接触确诊病例的血液样本,现已对16名密切接触者开展医学观察-半岛都市报 病例44:48岁男性,现住市南区,为我市确诊病例32和病例35就诊医院的检验科技师,曾接触该院确诊病例的血液标本。2月5日出现发热等症状,2月6日前往李沧区某医院发热门诊就诊,经市疾控中心核酸检测和专家组评估,2月7日上午确诊。现已对16名密切接触者开展医学观察,目前无发热等异常情况。其他密切接触者正在进一步追踪和调查中。-青岛市卫生健康委员会2020年2月7日在入侵机制方面,据《中国科学报》日前报道,中科院的科学家已经发现新型冠状病毒入侵时的细胞受体跟SARS-CoV(SARS冠状病毒)受体一样,都是ACE2。 现在,初步还发现新病毒跟受体的结合力比SARS-CoV略强一些。破解病毒入侵宿主细胞的机制,对指导设计药物、抗体或疫苗进行防控至关重要。卫生防疫专家强调,目前可以确定的新冠肺炎传播途径主要有:直接传播、接触传播和潜在的气溶胶传播风险。直接传播是指患者喷嚏、咳嗽、说话的飞沫,呼出的气体直接沉积在易感染人员的鼻腔或口腔黏膜上,病原体进入人体从而导致感染;接触传播是指飞沫沉积在物品表面,接触污染手后,再接触口腔、鼻腔、眼睛等粘膜,导致感染;气溶胶传播是指飞沫混合在空气中,形成气溶胶,吸入后导致感染,此传播方式目前还未有直接证据证明,属于潜在风险。呼吸、咳嗽、说话、吐痰、呕吐、大小便(水冲洗)等,可产生气溶胶,造成潜在的风险。研究人员,乃至整个研究实验室的安全防护显得尤为重要,只有对整个实验室的空间环境进行彻底而有效的灭菌除染才能够保证大家的安全。“气化过氧化氢”消毒技术气化过氧化氢是一种先进的高水平绿色消毒技术20世纪80年代推出,首先应用于制药行业无菌隔离器的灭菌处理。21世纪初,美国将该项技术列入五角大楼国防部高级研究计划局计划,并应用于911事件后的炭疽粉末污染的消毒处理。作为一种高效的终末消毒方式,气化过氧化氢对各类空气传播的病原微生物均具有良好的杀灭效果,在SARS、MERS病毒、H7N9和埃博拉病毒等传染病疫情的防控中,均发挥过十分重要的作用。近年来,更广泛用于高等级生物安全实验室的灭菌处理,突发传染病现场密闭空间的消毒处理,医院超级耐药菌污染的消除,甚至密闭飞机机舱的消毒处理。实验证明,当气化过氧化氢达到一定浓度以上时,具有良好的杀灭微生物的性能,能够杀灭各种已知的病原微生物,达到灭菌水平。杀灭90%微生物的时间(D值),由几秒钟到几分钟不等,不同的微生物存在较大差异。D值由小到大,依次为脂质包膜病毒、细菌繁殖体、无包膜病毒、真菌、结核杆菌、细菌芽孢。德国PEA气化过氧化氢灭菌器第三代干法闪蒸技术德国PEA公司的气化过氧化氢发生器采用最先进的第三代干法闪蒸技术,能够使过氧化氢完全气化,产生均匀的粒径在亚微米级别的过氧化氢气体,在空间内通过布朗运动不断与病原微生物接触,从而有效杀灭密闭空间内的各种病原微生物,为广大科研人员提供一个安全的环境。不同于“湿法”工艺的过饱和凝结,真正的“干法”闪蒸更加安全,可以兼容多种材料,不会对救护车、净化舱、ICU病房以及科研实验室内的多种精密电子仪器设备以及医疗防护用品造成不良影响。同时更是因为气化完全,其消毒灭菌体积得到了极大的提升,单次灭菌体积即可达到1000m3。艾力特生命科学在过去已为国内多个疾控中心和BSL3(P3)实验室提供了高等级的双扉蒸汽脉动真空灭菌器和VHP空间灭菌器,积累了丰富的经验;我们还可以为奋战在一线的医护人员和病患提供病房空间灭菌服务,杜绝交叉污染的发生,如有需求,我司将无偿提供服务,为早日结束疫情贡献我们的一份力量。气化过氧化氢技术已经应用了20年之久,全球制药行业85%以上无菌隔离器使用此项技术作为生物去污染的选择。迄今,气化过氧化氢已经被广泛应用于隔离器、空气过滤器、无菌灌装线、高等级生物安全实验室、传染病病房、隔离担架、救护车等不同领域消毒处理。关于新型冠状病毒肺炎2月8日国务院联防联控机制发布会上,卫健委发布关于新冠病毒感染的肺炎暂命名的通知,统一称谓为“新型冠状病毒肺炎”(Novelcoronavirus pneumonia),简称“新冠肺炎”,英文简称为“NCP”。冠状病毒是一大类病毒,已知会引起疾病,患者表现为从普通感冒到重症肺部感染等不同临床症状,例如中东呼吸综合征(MERS)和严重急性呼吸综合征(SARS)。此次武汉发现的新型冠状病毒2019-nCov是一种以前尚未在人类中发现的新型病毒。2019-nCov呈球状,直径约为100~160nm。病毒颗粒由蛋白质和核酸组成:最外面的刺突蛋白(Spike,S)对维持病毒颗粒形态非常重要;再往里是E和M蛋白,这些是撑起病毒颗粒形状的重要蛋白;最里面是其遗传物质RNA,被N蛋白包裹并保护着。冠状病毒是现在已知的拥有最大基因组的RNA病毒,相对于人类用DNA作为遗传物质,其RNA基因组复制时的保真性相对较差,容易产生更多的变异。 中国医学科学院呼吸病学研究院常务副院长曹彬日前表示,目前从人体、环境中监测分离的病毒上看没有发现明显变异。 但是,流行期越长其变异的可能性越大。据媒体报道,香港大学研究人员于1月31日公布首批新型冠状病毒在细胞内复制过程的图像。研究人员表示,每个受病毒感染的细胞会衍生出逾千粒病毒粒子,从而继续感染新细胞。新型冠状病毒武汉株01 照片来源:国家病原微生物资源库 (中国疾病预防控制中心病毒病预防控制所)新型冠状病毒武汉株02 照片来源:国家病原微生物资源库(中国疾病预防控制中心病毒病预防控制所)
厂商
2020.02.13
抗击疫情丨艾力特生命科学助力生物安全实验室建设和研究
自2003年我国SARS疫情爆发以后,中国生物安全实验室的建设在我国取得长足的进步和快速的发展。在生物病毒研究、生物技术开发和遗传基因工程等诸多领域均会建设生物安全实验室。生物安全实验室相比较普通实验室具有其独特性。在不同的生物安全级别的实验室中,生物安全三/四级实验室(BSL-3/4)主要用于对人、畜有高度传染性的烈性传染病的研究和检测。2003年中国爆发流行重症急性呼吸综合症(SARS)后,中国政府启动BSL-4实验室建设。中国科学院武汉国家生物安全实验室由中国科学院和武汉市政府共同建设,于2015年1月31日竣工,是亚洲首个生物安全四级实验室(BSL-4实验室),2018年1月5日正式投入运行。中国科学院武汉国家生物安全实验室是构建中国公共卫生防御体系的重要环节之一,其建成为中国公共卫生科技支撑体系再添重器,标志着中国正式拥有了研究和利用烈性病原体的硬件条件,为带动中国建立国际先进的生物安全体系迈出关键一步,也意味着在新发和突发传染病防控方面有能力承担更多的责任。武汉国家生物安全(四级)实验室在“武汉新型病毒”前期鉴别阶段中,专家排除了SARS、中东呼吸综合征、禽流感等的可能,这些专家就包括武汉病毒研究所——中国最重要的生物安全实验室之一的研究人员。在此次“武汉新型病毒”的防疫中,我们已完全有能力对病毒的鉴别和诊断作出确认,武汉国家生物安全四级实验室将在对病毒的研究中起到越来越重要的作用。生物安全三/四级实验室(BSL-3/4)使用的安全性非常重要,如果实验材料或实验室空间防护不当,则可能造成实验人员的感染,甚至有可能病毒外泄。生物安全防护实验室的结构和设施、安全操作规程、安全设备能够确保工作人员在处理含有致病微生物及其毒素时,不受试验对象侵染,周围环境不受污染。艾力特生命科学作为全球专业的无菌风险控制方案和相关设备方案供应商,已为国内多地疾控中心、海关国家口岸生物安全实验室、传染病国家重点实验室等十余所生物安全实验室提供国际先进的无菌风险控制方案,对于环境空间及物品的灭菌效果都能达到SAL≤10-6无菌保证水平,杀死一切顽强抵抗的细胞、真菌、病毒等微生物。德国MMM脉动真空灭菌柜艾力特生命科学拥有欧美多家先进设备供应商合作伙伴。德国MMM集团生产的生物安全三/四级实验室大型灭菌柜采用防震级别生物安全密封、腔体底部进蒸汽设计、冷凝水收集再次灭菌、可在线灭菌的进排气过滤器装置、防泄漏特殊形状的密封圈等诸多特点,可大大降低实验人员感染和病毒外泄的可能。德国PEA气化过氧化氢空间灭菌由于生物安全三、四级实验室(BSL-3/4)试验的样本对人、畜有高度传染性的烈性传染,为了保证实验室时刻处于无致病菌随时待命状态,故在每次试验完成之后需对核心区实验室乃至整个实验室进行空间灭菌,以往采用甲醛进行灭菌时实验室会出现长时间的刺激性气味、难以清除的白色晶体及降低实验室被腐蚀的风险,故越来越多的生物安全三/四级实验室(BSL-3/4)采用干法过氧化氢方式进行灭菌,德国PEA公司的气化过氧化氢空间灭菌器采用第三代闪蒸技术,具有移动方便、灭菌环境(温度、湿度、过氧化氢浓度)可实时监控、150℃~160℃完全气化、符合各项法规标准、安全无残留等优点被中外各国生物安全三/四级实验室(BSL-3/4)广泛使用。德国PEA气化过氧化氢传递窗在进行小件物品传递时,为了减少打开安全门次数,大幅度的降低实验室和实验室外部空间被污染的风险,越来越多的新建实验室采用双扉过氧化氢传递窗进行小件物品传递。德国PEA公司可提供各种体积的双扉过氧化氢传递窗,过氧化氢发生器集成在设备内部,避免实验室空间浪费;内腔采用AISI 316L不锈钢制造,可长期耐30%~35%过氧化氢溶液腐蚀;采用德国西门子控制器以实现双门互锁和权限控制管理。德国MMM集团生产的生物安全三级实验室大型灭菌柜通过选配置H2O2接口外接移动式过氧化氢发生器实现临时双扉过氧化氢传递窗功能。
厂商
2020.02.04
countstar做为唯一的中国合作商亮相此次会议
the car-t congress gathers thought leaders from biotech, big pharma, academia and investment to address the challenges and opportunities of car-t therapies in both liquid and solid tumors. discussing the potential of cars in alternative cell types, mechanisms behind toxicity and tumor targeting, this event will provide an in depth view into this expansive area. exploring ground-breaking developments into car-t therapy, the event will provide the opportunity to collaborate to create a commercially viable, effective and safe therapy. key session topics include:alternative cell constructs: tcrs, gamma delta t cells, car-nk & car-tregscommercialisation, regulation & implementationsafety, control & the underlying mechanisms of toxicityscalability, automation & process developmenttarget identification & neoantigen discoverypatient access & strategic considerationsinvestment & partnering workshopscountstar®smart cell analysisintroducing countstar cell analysis systems, a line of instruments with an innovative combination of advanced technologies. countstar brings together the functionality of digital microscopes, cytometers and automated cell counters into its intuitively designed systems. by combining bright-field and fluorescent imaging with advanced image recognition technologies, extensive data on cell morphology, viability, concentration, cytotoxicity, apoptosis are generated in real time. countstar systems go further by generating high-resolution images, the essential basis for sophisticated data analysis. with more than 1,500 analyzers installed worldwide, countstar analyzers are proven to be valuable tools in research, process development, and validated production environments.the countstar brand was inspired by the endless possibilities a person experiences when counting stars in the night sky. with this approach, countstar explores the limits of technology. countstar was founded by alit life sciences, an emerging manufacturer of innovative equipment and consumables for the biological research community. headquartered in the high-tech district of shanghai, alit life sciences develops and produces the analytical equipment of the future.please meet us at the car-t congress in boston at the hilton boston/dedham on march 20th through 22nd.
厂商
2018.03.14
3月8-9日艾力特将亮相本届贸易生物产业大会
大会由易贸医疗主办、诸多行业协会、机构、企业支持协办的的生物产业高端千人峰会。大会聚焦精准医疗,覆盖诊断、治疗、用药全产业链,融合政策导向、市场投资、技术研发、临床应用等话题,已经成为国内外生物产业高层跨界交流与合作的标杆平台。艾力特将携公司产品作为参展方亮相此次展会。我们的位置酒店三楼 51号展位地点:苏州日航酒店 苏州虎丘区长江路368号欢迎各位业内人士莅临展位参观洽谈!
厂商
2018.03.07
艾力特诚邀您相约2017首届北京亦庄生物学术年会暨生物制药论坛
2017首届北京亦庄生物学术年会暨生物医药分析技术论坛以“技术创新,发展共赢”为主题,面向制药工业数字化工厂、制药现代化、生物制药、制药工业检测技术及相关领域,分享行业专家的最新创新理念和实践。 此次论坛旨在聚焦生物分析技术在药物研发与质量控制领域的应用,展示新技术、新进展、新经验。为国内外学者提供平等交流与合作的国际平台。以拓展思路、整合资源。推动生物制药检测技术水平的提升。完善医药行业全面、协调、可持续发展。本次大会以“技术创新,发展共赢”为主题,面向制药工业数字化工厂、制药现代化、生物制药、制药工业检测技术及相关领域,分享行业专家的最新创新理念和实践。 艾力特国际贸易有限公司是国内生物线领域最重要的仪器设备与技术服务供应商之一,致力于为生物制药提供全方位的解决方案。此次论坛艾力特将有样机现场展示,为您提供从生物工艺研发到质量控制的全方位解决方案。艾力特诚邀您莅临论坛现场进程咨询洽谈! 时间:2017年12月21日-22日地点:北京亦庄生物医药园形式:大会主题报告、分会场技术报告、新技术与产品展示;会议规模:500人展位号:14
厂商
2017.12.07
Countstar诚邀相约2017国际细胞治疗上海峰会
2017国际细胞治疗上海峰会将于11月17日在上海举办。本次峰会邀请了30多位国际顶级的CAR-T专家、行业资深人士和药监机构审评专家,将从技术、生产、监管、知识产权、企业融资发展等各个角度为大家带来精彩主题分享。作为国内重要的细胞分析仪器供应商,Countstar受邀参加此次会议,届时Countstar将携新一代全自动细胞荧光分析亮相此次会议,并展示它在CAR-T 细胞状态全程把控、AO/PI双荧光法活率检测等应用领域带给大家的全新体验。热忱欢迎各位新老客户莅临Countstar展位洽谈交流。地址:上海金茂君悦大酒店展位: NO 8演讲嘉宾:王刚 博士 CFDA药品审评中心首席科学家Xiaobin Victor Lu博士 FDA 生物制品评价和研究中心CMC评审专家Romaldas Maciulaitis教授 欧洲药品管理局CHMP委员会成员,立陶宛健康科学大学临床药理学教授Stephan Grupp教授 美国费城儿童医院肿瘤免疫治疗&细胞治疗主任,诺华CTL-019项目临床开发主要负责人Reiner Brentjens博士 纪念斯隆·凯特琳癌症中心细胞治疗主任Cassian Yee博士 美国德克萨斯州大学MD安德森癌症中心肿瘤免疫治疗研究/实体瘤细胞治疗中心主任Ghassan Abou-Alfa博士 纪念斯隆·凯特琳癌症中心消化道肿瘤专家Dan Kaufman教授 加州大学圣迭戈分校细胞治疗转化医学主任James Miskin博士,Oxford BioMedica首席技术官,FDA肿瘤药物咨询委员会CTL-019项目报告专家Jason Slingsby博士,Oxford BioMedica商务发展负责人Gregory I. Frost博士,F1 Oncology创始人 M. V. Peshwa博士,MaxCyte执行副总裁、首席科学官
厂商
2017.11.13
艾力特2017下游连续纯化工艺研讨会圆满结束
当前,未来制药工厂,包含了新的设备、现有药品生产设备的更新换代和技术改造,以满足更经济高效的生产需求,更小的产品生产批次,更高的灵活性以及新的监管需求。其中,连续生产工艺技术以及一次性生物技术设备解决方案都是当下讨论的热门话题,正在迅速成为得到业界认可的技术,现有工厂当中的可重用设备也正在为一次性系统所取代。以此为契机,为了促进生物制药领域客户更好的了解生物制药新技术,把握生物制药下游生产新工艺,获知最先进的应用案例,探讨行业发展新趋势。艾力特国际贸易有限公司携手美国Repligen公司于11月2日在上海举办了一场主题为“下游连续纯化工艺研讨会”的研讨会,来自国内许多知名药企的专家学者、企业代表参加了此次会议。会上,Repligen 副总裁Christine Gebski带来了主题为“下游纯化工艺”的精彩演讲,并为大家详细介绍了OPUS预装柱。而Repligen的TangenX产品总监Michael LaBreck则通过现场生动的样机演示,为大家形象地展示了一次性切向流过滤工艺膜包解决方案。
厂商
2017.11.07
PBMC检测新方法 ——Countstar助力免疫学研究发展
pbmc是指外周血中具有单个核的细胞,包含淋巴细胞、单核细胞等,常用于免疫学领域的科研活动(包括自身免疫性疾病),传染病,血液恶性肿瘤,疫苗开发,移植免疫学和高通量筛选。作为免疫学功能研究中最常用的细胞模型,pbmc在免疫学研究以及免疫治疗领域发挥至关重要的作用。传统的pbmcs血球计数板方法往往存在操作繁琐,耗费时间长等问题,再加上个体(如正常人和病人)和人工分离提取的差异,以及红细胞和血小板污染的程度差异,这都大大增加了准确计数pbmc和检测 pbmc活性的难度。近日countstar fl细胞荧光分析仪通过层层筛选,成功斩获了三家来自广东的细胞免疫学研究单位的订单。而 countstar fl之所以受到的青睐,除了它能对pbmc细胞进行准确稳定的检测,还可通过其独特的荧光图像成像系统,让您可以“看”到细胞。由于红细胞的存在,使得pbmcs测定的结果受到干扰。通常情况下需要通过2种方式去除红细胞的干扰:1. 将红细胞裂解去除红细胞;2. 密度梯度离心方法去除红细胞。countstar fl提供了一种更加简便和准确的pbmcs的分析方法,可是使用户在不裂解红细胞的情况下即可对pbmcs进行分析。活死单个核细胞可呈现荧光信号。而成熟的红细胞及血小板,因为没有细胞核,不能被ao/pi染色,因此可以完全被排除在外不被计数。可以精确计数分离后的pbmc以及活力分析。 虽然有研究者使用2种方法的组合来去除红细胞,但是同样被证明无法完全去除红细胞。现在的研究者在pbmcs研究中遇到的挑战:研究者们依然在使用传统的血球计数板分析pbmcs细胞;在分析的时候会pbmcs会受到红细胞的干扰;红细胞仅能用肉眼识别,并且需要有一定经验的实验者; 血细胞经pbs稀释后,在明场条件下,因为有大量的红细胞,血浆等干扰,无法进行计数,双荧光法可明显识别pbmc。梯度稀释后测定pbmcs浓度血细胞,用pbs稀释不同比例(1:5,1:10,1:15,1:20,1:25),使用ao/pi染色方法染色并在countstar仪器上进行检测。结果如图所示。经过稀释后,可以看到检测结果拥有良好的线性。 双荧光法对密度梯度离心法获得pbmc进行计数双荧光法可准确区分密度梯度离心后pbmc的死活,并有效排除干扰物质对细胞计数的影响 双荧光法对密度梯度离心法获得pbmc进行计数左图:对pbmc进行梯度稀释后,countstar对浓度的测试具有很好的线性;右图:对pbmc进行梯度稀释后,countstar®对活率的测定具有很好的一致性 countstar测试结果显示界面
厂商
2017.10.30
德国VHP过氧化氢传递窗
如果您想将材料安全地转移到或排出洁净室,我们向您推荐德国PEA传递窗。它们被集成到您的系统中,并在不同洁净室层级的房间之间提供货物转移服务。可应用于GMP洁净厂房、无菌处理流程 、生物制品 、生物医药 、生物安全/安保 、实验动物中心等。产品特点*具有净化功能,可消除物料从低洁净度区域传递至高洁净度区域时潜在的污染风险;*符合GMP洁净级别要求;*内置轨道操作便利,用于传递小批量物料;*对设备进行维护时不会对洁净室造成干扰;*可集成或连接过氧化氢发生器对设备进行灭菌过氧化氢灭菌优势:汽化过氧化氢无菌传递窗在欧美发达国家已成熟应用,汽化过氧化氢对对嗜热脂肪芽孢杆菌(MESA LABS /ATCC7953)的杀灭率达到6-log。低温、常压,适用于低温灭菌的产品,具有良好的物料兼容性,易分解,无有害残留,最终分解为水和氧气德国PEA集团简介德国PEA 创立于1991年,一直专注于过氧化氢灭菌技术的优化,以“使过氧化氢灭菌变得更安全、更简单、更精确、同时更经济”为目标,秉承“质量优先”的理念:产品的质量、员工的素质、服务的质量。PEA密切关注客户需求与技术创新,在与全球用户不断地交流和服务过程中,积累了大量的经验,同时结合技术创新、高品质的产品质量以及完善的技术服务,为实验室、制药工业、科研院所、医院、动物房、军队、公共场所等领域的用户提供全方位的无菌控制解决方案。
厂商
2017.10.30
艾力特2017生物制药新工艺研讨会感谢有您
2017年9月22 日艾力特携手美国repligen公司在美丽的苏州举办了一场关于抗体连续生产、上游连续灌流及下游连续纯化工艺的讨论盛会,旨在为大家提供一个了解最新生物制药技术与发展趋势,把握生物制药上下游生产新工艺及应用的交流平台。会上,来自repligen公司的亚洲区销售总监aidan audouy和国内用户代表与大家一起分享了基于xcellatf系统的灌流工艺及相关应用实例、抗体纯化下游解决方案等主题内容。另外,来自countstar应用研发部的王经理带来了主题为“countstar fl荧光细胞分析仪助力抗体从研发到生产”的精彩演讲。在接下来的活动中,艾力特产品经理们与现场嘉宾进行了互动答疑和充满欢笑的抽奖活动。
厂商
2017.09.28
Counstar2017(第九届)干细胞国际研讨会圆满结束
2017(第九届)干细胞国际研讨会于9月8日至9日在深圳圆满结束,本次会议围绕干细胞重编程与再生医学、干细胞技术规范等议题进行深入讨论。Countstar作为国内首家专业从事细胞分析仪器研发与生产的供应商受邀参加了此次会议。会上,Countstar向大家热情介绍了Countstar细胞荧光分析仪、Countstar 细胞计数仪等产品,吸引了众多干细胞研究专家学者驻足参观,这其中有不少是Countstar的老客户。Countstar细胞计数仪在日常细胞研究工作中稳定而准确的检测结果赢得了大家的信任和支持,而新一代Countstar细胞荧光分析仪在标准干细胞治疗质控体系的建立、细胞浓度及活率的精准测定等领域的应用再次引起了在场嘉宾的浓厚兴趣。
厂商
2017.09.18
Countstar 2017细胞治疗主题沙龙感谢有您
Countstar 2017细胞治疗主题沙龙于9月14日在上海客莱富诺富特酒店成功举办,此次会议得到了许多行业内的专家、企业代表的指导与支持。会上,Countstar与大家一起围绕“细胞检测技术的发展与应用”、“Car-T在胃癌方面的研究进展"、“干细胞制剂的制备与质量控制”等主题展开探讨和交流。与会嘉宾们正积极地对各个话题展开讨论现场气氛活跃,互动频频作为攻克癌症和退行性疾病最有希望的方式,细胞治疗俨然成为当前医学治疗领域最热门的研究领域之一。通过举办这次会议,Counstar希望可以提供出一套方案,用于解决当前国内的企业、政府监管等单位所面临的细胞制剂质量如何控制和监管的问题,助力未来中国细胞治疗行业的蓬勃发展。最后,Countstar再次感谢华东理工的陈教授、上海交大的郭教授、吉凯基因的袁博士、上海鸣大生物的刘博士以及各企业代表的莅临与支持。
厂商
2017.09.18
Countstar邀您相约2017细胞治疗主题沙龙
细胞治疗是攻克癌症和退行性疾病最有希望的方式。随着诺华首个CAR-T产品Kymriah获批上市,细胞治疗技术取得了里程碑式的突破。目前,细胞治疗不仅在血液病方面取得了重大进展,同时众多的先行者已开始使用细胞治疗手段挑战实体瘤。此外,众多干细胞产品已获批上市或进入临床实验阶段。在中国,细胞治疗行业在蓬勃发展,但相应的法规和监管制度还不够完善,活体细胞的细胞制剂的质量如何控制和监管,成为企业、政府监管部门及相关单位共同面临的挑战和难题。在行业内专家和学者的指导与支持下,Countstar特此举办这场细胞治疗主题沙龙,诚挚邀请您前来参加,并就机遇、挑战、质控等热点话题进行探讨和交流。会议时间:2017年9月14日 会议地址:客莱富诺富特酒店 康桥厅特邀嘉宾华东理工大学 郭美锦教授上海交通大学 陈彦田教授吉凯基因 副总裁/研发中心总监 袁纪军博士上海鸣大生物科技有限公司 细胞事业部总监 刘军博士上海睿钰生物科技有限公司研发应用部经理 颜海波 博士相关主题分享CAR-T在实体瘤(胃癌)方面的研究进展临床级干细胞制剂的制备及质量控制自然杀伤细胞的临床应用及制剂质量控制细胞检测技术的发展和应用
厂商
2017.09.07
第三届中国生物制药分离纯化技术创新发展论坛
8月30日-31日第三届中国生物制药分离纯化技术创新发展论坛圆满落幕,此次论坛汇集了国内外众多的纯化制药企业参加。作为国内重要的生物制药工艺解决方案供应商,艾力特受邀参加了此次盛会。会上,艾力特携ATF细胞截留系统、OPUS可定制预装纯化柱、Countstar细胞荧光分析仪等产品,向大家演示了从上游的细胞培养到下游的纯化工艺,再到cGMP生产的生物制药解决方案。来自Repligen公司的Stephen Tingley副总裁为大家带来了主题为“单克隆抗体ATF高密度细胞培养的下游纯化工艺开发”的精彩演讲。
厂商
2017.09.04
如何区别过氧化氢灭菌是干法还是湿法?
我们在面对客户的时候,发现很多客户都有这样一个疑问:是不是过氧化氢发生器带除湿功能就是干法,不带除湿功能就是湿法呢?显然答案是否定的,那干法和湿法究竟有怎样的区别呢?一、灭菌工艺 干法:干法的核心技术是闪蒸技术,可使过氧化氢完全气化,分子粒径级别在10-10m,可在空间做布朗运动,分布均匀,整个过程控制在冷凝点以下,因此是“干”工艺,从而避免结露和腐蚀。湿法:不管是微冷凝,干雾,或是其他电离方法总的概括起来属于简单加热法,不除湿,分子粒径在微米级别,分布不能保证均匀,单台设备最大可灭空间体积小于600m3,而且灭菌过程不控制湿度,很容易达到结露点,从而易对接触表面产生腐蚀。二、灭菌循环 干法:可以有效控制灭菌空间相对湿度,确保H2O2蒸汽不冷凝,保持低浓度高效杀菌能力的特性;每次灭菌前控制的相对湿度相同,开发出的参数代表所有工况;有很强的可重复验证性。 湿法:不控制相对湿度,注入的H2O2蒸汽要依据房间内原始的相对湿度确定注入量,否则很难控制冷凝点;故开发出的参数不能代表所有的工况,难于重复验证。 三、验证方法 干法: - 被灭菌空间内,先用化学指示剂模拟出该空间的气流模型,找出最不利点; - 依据化学指示剂验证结果,分高、中、低三个层面布置生物指示剂, - 重点关注最不利点,可达到完全的6log灭菌 - 验证方法科学,严谨;受到广大认证专家的高度认可。湿法: - 客户自己依照原有甲醛或臭氧方法验证; - 验证点少,结果无代表性,很难通过高标准、严要求的认证专家的认可; - 无法达到完全的6log的灭菌效果。 四、排放 干法: - VHP整个灭菌过程维持在汽化状态,与湿法工艺相比,汽化状态排放时间更短; - 相对于液体过氧化氢来讲,无残留;不需要做残留验证。湿法: - 在接触表面有很高浓度的H2O2冷凝液,如果接触表面要通过1ppm以下残留浓度的验证测试,要增加排放时间; - 需要残留验证,证明接触表面残留浓度在1ppm以下。 五、材料兼容性 干法:汽态过氧化氢灭菌工艺(干法工艺)通过欧美三十多年的实际应用,已经证实对于大多数的材料都是兼容的; 广泛应用于制药,航天,医疗、军事等领域,未发现腐蚀现象。湿法:高浓度的H2O2冷凝液在接触物体表面时可能会产生腐蚀,兼容性较差,对于彩钢板、设备等材质要求较高,已出现多例腐蚀现象;六、灭菌效能 干法: - 低浓度短时间的杀孢子能力; - 相比液体来讲,气态过氧化氢分布更好更均匀;可以达到完全的6log的杀菌效果,轻松通过FDA、WHO的认证。湿法: - 高浓度长时间接触的液态过氧化氢才会有较强的杀孢子能力;故浓度必须足够高、时间必须足够长,否则很难达到6log的杀菌效果; - 液体过氧化氢分布与气态相比较难达到均匀效果,故很多的点只能达到3log或4log. 七、客户使用效果反馈 干法:- 材料的兼容性好,无腐蚀现象;可频繁使用,无需任何担忧; - 被全球客户公认为到目前为止最安全、最高效、最环保的替代甲醛、臭氧的灭菌方法。湿法:- 部分客户在使用过程中出现腐蚀彩钢板,环氧地坪起泡现象;- 微雾化技术,对于很多关键设备的薄弱环节有不同程度的腐蚀,存在一定的使用风险;
厂商
2017.08.31