【安捷伦】USP <232>/<233> 和 ICH Q3D 制药行业元素杂质分析现场解决方案

美国药典通则 USP<232>(限度)和 <233>(方法)已于 2018 年 1 月 1 日起执行(FDA)。欧洲药典标准
在此形势下,制药企业都必须要根据 ICH Q3D 指导原则对所有药品中的元素杂质状况进行风险评估,而风险评估与常规测试所采用的所有分析方法,都必须进行方法验证。
新法规下,制药实验室的新痛点
执行法规缺乏经验可循,新手上路实验问题重重,人员培训,方法建立,大量的数据验证需求给制药企业带来了时间和资金的双重考验。
如何确定药品中可能存在的元素杂质?
如何评估其含量是否超过法规规定的每日限量?
如何设计最恰当的样品前处理方法保证样品溶解的同时不会带来金属元素的损失并减低后续验证步骤的风险?
如何在短时间内完成大量的方法学验证工作?
如何充分应对监管机构补充验证数据的要求以确保申报过程不会被延长?
如何控制实验室环境与实验耗材导致的元素背景干扰?
如何确认验证方法已满足 USP 232/233 法规的要求?
如何选择最合适的元素含量计算方法?风险评估选择产品法还是原料法?
安捷伦的“软”实力
安捷伦 ICP-MS 不仅具有优异的硬件性能指标,MassHunter 软件更是为制药用户量身定做了方法模板,装机预设了制药行业常用的 USP<232>、ICH Q3D 方法。
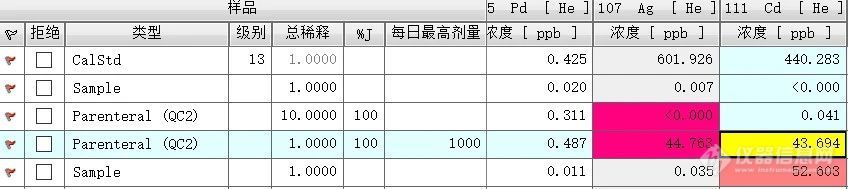
调用模板后即可得到优化后的 Q3D 中 24 元素仪器测量参数;相对常规功能,方法模板中增加了 ICH Q3D 中“每日最高剂量”的设置,“J 值”的计算,“口服、注射、吸入”三种剂型 QC 的设置;分析结束后还有 USP - ICH 分析报告模板供参考使用。

Agilent 7850 ICP-MS
安捷伦解决方案
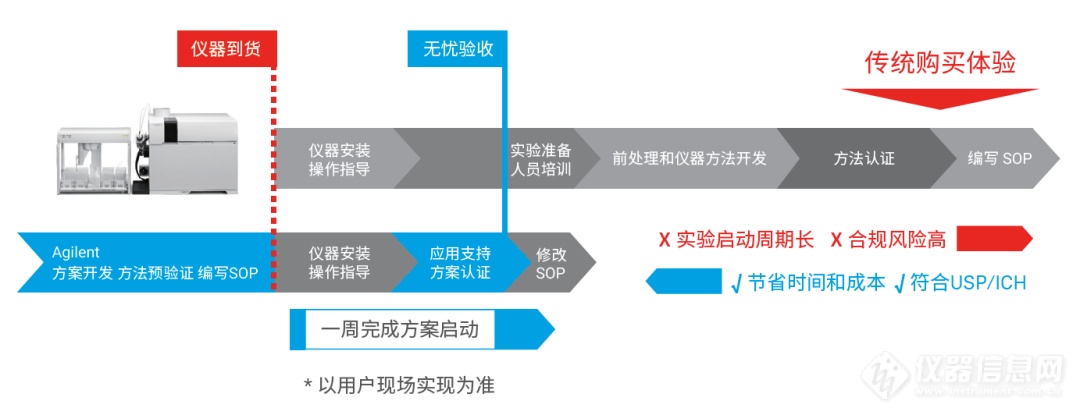
安捷伦制药行业元素分析全流程现场支持方案帮助您高质量、无风险、快速、准确的解决合规问题。
以客户样品为出发点,以预开发的应用方法为手段,一次解决前处理与上机分析的两步需求;
服务的设计基于方法验证相关通则 USP<1225> 与 ICH Q2(R1);
高效完成仪器分析和生成方法验证报告,简化步骤,提高效率;
基于实际样品提供符合法规要求的工作流程并现场完整验证;
缩短方法开发与验证周期,节省成本,降低风险;
方案附带可编辑的实验室 ICP-MS 元素分析 SOP 模板和安捷伦认证的 24 元素混合标准溶液组(符合 USP/ICH 口服限量)。
服务详情
现场服务基于 ICP-MS 仪器平台与客户实际样品提供符合 USP 通则 <232> 规定的元素列表与通则 <233> 性能要求的方法验证工作流程;
由安捷伦中国应用工程师针对中国制药市场的产品特点和用户需求设计开发;
提供样品前处理方案个体化定制咨询,操作流程标准化示范;
使用方案附带的安捷伦混合标样,完成标准曲线配制与样品加标;
附带一套 24 种元素和内标的安捷伦认证混合标样(完整包装),中文解决方案操作指南,可编辑的实验室 ICP-MS 元素分析 SOP 模板,帮助用户在日常实验和管理中实现方法的稳定运行。
安捷伦认证混合标样
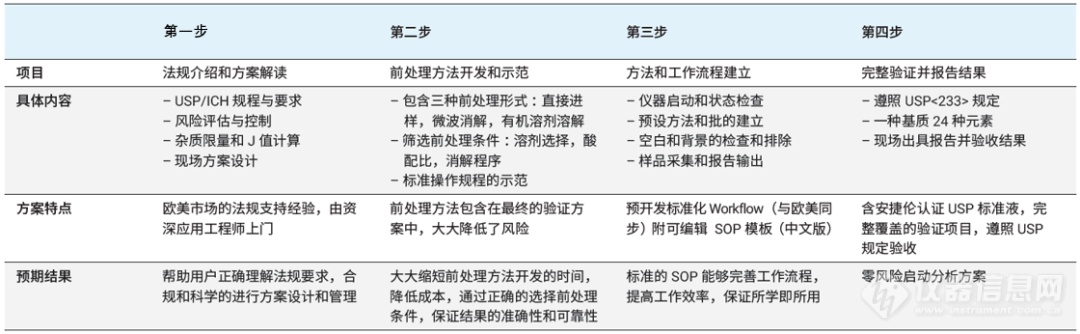
现场支持服务流程


关注安捷伦微信公众号,获取更多市场资讯

更多![]()
新品速递 | 全可拆卸炬管,便捷超乎想象
厂商
2024.08.08
中药质量安全检测技术新方向及实操培训班圆满落幕!
厂商
2024.08.07
突破一切极限 | 全新Agilent 7010D 三重四极杆气质联用系统
厂商
2024.08.07
创新50载 | 今朝又夺两金!超低流失气相色谱柱两大新品上市
厂商
2024.08.06













