PerkinElmer NGS整体解决方案助力新冠病毒的测序研究
2020/02/20 14:37
阅读:489
分享:方案摘要:
方案详情:
PerkinElmer NGS全流程解决方案
1、病毒RNA提取:Chemagen自动化核酸提取方案
2、病毒RNA质控及NGS文库质控:Labchip GX Touch
病毒RNA质控:由于不同样品之间病毒含量差异较大,不少样品病毒量稀少,在NGS文库构建需要进行RNA质控,了解RNA的提取质量情况对下游实验及数据分析等都有非常重要的意义。

我们创新的LabChip® GX Touch微流体技术提供了无与伦比的电泳分离效果。LabChip® RNA分析为大小介于100 至6000个核苷酸之间的RNA样品提供了一种快速简易的定量方法。利用RNA检测实验分析RNA样品,通过自动化步骤来进行样品定量和完整性分析,可以节省时间和金钱。LabChip的RNA分析能够为用户提供RNA浓度,以及核糖体RNA比值作为完整性检测的指标。RQS为一个介于0和10之间的质量评分,其中“10”表示样品完好无损。RQS与其它商业指标的相关度极好。
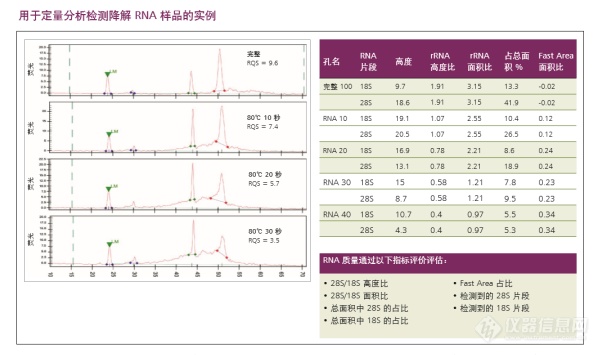
图示:RNA样品的降解过程,强制性的对完整的RNA通过加热一系列指定时间使之降解,以展示样品的降解过程。
NGS文库质控:构建好的NGS文库,可以利用NGS 3K试剂盒进行NGS文库的质控。LabChip DNA NGS 3K实验能够提供最灵敏的浓度检测范围(起始样品浓度5-500pg/μL),已远远超过其他的DNA荧光标记技术。无论是何种应用,LabChip DNA NGS 3K检测都只需要很低的样本量。这个实验尤其适合有稀缺文库样本的质控。
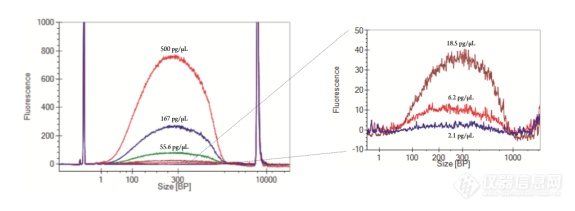
图示:DNA NGS 3K实验可达成的灵敏度。同一NGS文库样本进行6次3倍系列稀释,实验结果展示了LabChip DNA NGS 3K的灵敏度及检测下限。数据结果由LabChip GX Touch仪器生成。
除了以上RNA质控及高灵敏度的NGS 3k芯片试剂,Labchip可以在同一个平台上完成高灵敏度DNA/RNA样品分析、弥散性DNA样本分析, 以及RNA和基因组DNA样本的完整性分析,且每个样品耗时可低至28秒。本系统既有最大批处理能力为24个样品、帮助节约时间和试剂用量的型号LabChip GX Touch 24,又有适用于高通量实验室的型号LabChip GX Touch HT,可达成384的处理能力。您可根据具体的应用选择适合的数据输出:电泳峰图、虚拟胶图或数据表格。
3、NGS建库自动化方案:自动化文库构建工作站
NGS建库流程复杂,对液体处理精准度要求高,利用自动化工作站进行NGS文库构建,具有流程标准化、样品之间重复性好,精准度好,通量高等特点。根据通量大小、自动化程度的不同,珀金埃尔默提供了多款自动化NGS文库工作站供选择。
Sciclone G3 NGSx iQ高通量自动化建库工作站,通过整合协同工作, 自动化程度获得极大提高: 一个Twister III五维机器人手臂、可存放27盒枪头的储板栈、高通量精准移液的Sciclone G3 NGSx文库制备工作站、内嵌桌面式Inheco ODTC热循环仪、直观图示化的用户界面、经PKI 专业开发验证、兼容不同品牌供应商建库试剂盒的NGS自动化建库程序,确保高质量的DNA或RNA的NGS文库构建。大量已经 验证的NGS建库程序,确保NGS文库的快速制备。使用这套无人值守自动化建库系统,您可以空出更多时间去做更具智力挑战性的工作,分析实验数据、设计您的下一个实验方案等。
Sciclone G3 NGSx iQ HT 高通量自动化建库工作站,基于Sciclone G3 NGSx iQ工作站做进一步升级,配备384通道移液头,内置抓扳手及外置Twister III五维机器人手臂、内嵌桌面式Inheco ODTC热循环仪。是目前市场上唯一 一款提供从核酸到文库的微型化、标准化、测试应用的仪器。反应的微型化节约了宝贵的试剂,并允许研究人员以相同的成本运行更多的样品。
Sciclone® G3 NGSx工作站是我们的高通量解决方案,适用于文库制备、序列捕获及样品归一化。该系统每周可制备多达480个文库或192个外显子组捕获文库,且灵活性极强,每轮能处理8到96个样品。此外,Sciclone® G3 NGSx工作站的全封闭平台设计,可使交叉污染降至更低水平。该系统在针对前PCR工作流程设计优化之余,同样适用于后PCR工作流程。
Zephyr® G3 NGS工作站是一个简单易用的文库制备系统,经过专门的设计和预编程,可应对新一代测序样品制备工作流程中的后PCR步骤――磁珠纯化、qPCR体系构建、样品归一化、样品混合(多重)实验。同时也是追求性价比的中通量实验室的前PCR建库系统的好选择。
JANUS G3 NGS Express(PLUS)工作站配备直观的文库制备应用界面,可实现片段化文库、扩增子、靶向捕获等文库制备及样品归一化。它是中低通量台式测序系统的完美补充。
4、NGS建库试剂:NextFlex 文库构建试剂盒
新型冠状病毒是具外套膜的正链单股RNA病毒,利用NextFlex Directional RNA-seq kit 2.0 可以构建链特异性RNA文库,通过对病毒的测序来进行病毒变异、宿主溯源等深入研究。
珀金埃尔默提供了行业领先的二代测序文库构建试剂产品组合,包含DNA、RNA、Small建库试剂,扩增子/探针杂交捕获试剂以及建库流程中使用到的接头和纯化磁珠。同时珀金埃尔默提供相应的自动化试剂盒包装,可以直接应用于珀金埃尔默的NGS自动化文库构建工作站。
下载本篇解决方案:
更多![]()
HS-GCMS对聚醚多元醇中的氯氟烃和氢氯氟烃的测定分析
本文采用配有 PerkinElmer的TurboMatrix HS-40顶空自动进样器和Clarus 680-SQ8气相色谱-质谱联用仪对聚醚多元醇基体中的三氯氟甲烷(CFC-11)、二氟一氯甲烷(HCFC-22)和二氯一氟乙烷(HCFC-141b)进行了研究。文中给出了研究中所用的仪器方法参数,详细结果证明,该方法具有较好的精密度、线性度、灵敏度和回收率。
环保
2020/07/16
使用NexION 2000 ICP-MS 按照ICH Q3D 和USP <232>/<233>的规定检测和验证药用抗酸剂中的1 级和2A 级元素杂质
美国药典(USP) 宣布药品中元素杂质的新标准将于2018 年1月1日实施。通则<232> 和<2232> 基于给药途径规定了关注元素的列表及其允许的日接触(PDE)限值。此次标准更新使USP在关注元素杂质列表和PDE 方面与人用药品注册技术要求国际协调会(ICH)Q3D 第4 阶段文件相匹配。2016 年6月FDA发布了药品中涵盖ICH Q3D 的元素杂质的指导原则。随着元素杂质评估和监控期限的临近,制药厂商及其服务实验室必须立即开始执行新的法规,否则将承担违规风险。合规性要求分析方法应能准确地检测药品或(如有必要)其成分中较低的元素杂质含量,以确保患者的安全。USP 通则<232>概述了测定制成药品中元素杂质的两种分析方法:电感耦合等离子体质谱法(ICP-MS)或电感耦合等离子体发射光谱法(ICP-OES),以及相关的样品制备步骤。ICP-MS 的高性能最适合在低浓度水平下对1级元素进行常规性测定,尤其是日摄入剂量较大(>10g/ 天)的药品。在此类药品和营养品中,抗酸剂由于具有极高的钙含量,给分析造成了极大的挑战。本文旨在展示如何正确地制备样品、适当地考量各种仪器设计因素,就能轻松地克服这项挑战。在本文中, 我们展示了利用珀金埃尔默公司最新NexION® 2000 ICP-MS,依照USP 通则<233> 的规定,对抗酸剂中1级和2A级元素杂质进行验证的数据
制药/生物制药
2017/06/29
使用NexION 2000 ICP-MS 按照ICH Q3D 和USP <232>/<233>的规定检测和验证药用抗酸剂中的1 级和2A 级元素杂质Co
美国药典(USP) 宣布药品中元素杂质的新标准将于2018 年1月1日实施。通则<232> 和<2232> 基于给药途径规定了关注元素的列表及其允许的日接触(PDE)限值。此次标准更新使USP在关注元素杂质列表和PDE 方面与人用药品注册技术要求国际协调会(ICH)Q3D 第4 阶段文件相匹配。2016 年6月FDA发布了药品中涵盖ICH Q3D 的元素杂质的指导原则。随着元素杂质评估和监控期限的临近,制药厂商及其服务实验室必须立即开始执行新的法规,否则将承担违规风险。合规性要求分析方法应能准确地检测药品或(如有必要)其成分中较低的元素杂质含量,以确保患者的安全。USP 通则<232>概述了测定制成药品中元素杂质的两种分析方法:电感耦合等离子体质谱法(ICP-MS)或电感耦合等离子体发射光谱法(ICP-OES),以及相关的样品制备步骤。ICP-MS 的高性能最适合在低浓度水平下对1级元素进行常规性测定,尤其是日摄入剂量较大(>10g/ 天)的药品。在此类药品和营养品中,抗酸剂由于具有极高的钙含量,给分析造成了极大的挑战。本文旨在展示如何正确地制备样品、适当地考量各种仪器设计因素,就能轻松地克服这项挑战。在本文中, 我们展示了利用珀金埃尔默公司最新NexION® 2000 ICP-MS,依照USP 通则<233> 的规定,对抗酸剂中1级和2A级元素杂质进行验证的数据
制药/生物制药
2017/12/03
使用NexION 2000 ICP-MS 按照ICH Q3D 和USP <232>/<233>的规定检测和验证药用抗酸剂中的1 级和2A 级元素杂质Hg
美国药典(USP) 宣布药品中元素杂质的新标准将于2018 年1月1日实施。通则<232> 和<2232> 基于给药途径规定了关注元素的列表及其允许的日接触(PDE)限值。此次标准更新使USP在关注元素杂质列表和PDE 方面与人用药品注册技术要求国际协调会(ICH)Q3D 第4 阶段文件相匹配。2016 年6月FDA发布了药品中涵盖ICH Q3D 的元素杂质的指导原则。随着元素杂质评估和监控期限的临近,制药厂商及其服务实验室必须立即开始执行新的法规,否则将承担违规风险。合规性要求分析方法应能准确地检测药品或(如有必要)其成分中较低的元素杂质含量,以确保患者的安全。USP 通则<232>概述了测定制成药品中元素杂质的两种分析方法:电感耦合等离子体质谱法(ICP-MS)或电感耦合等离子体发射光谱法(ICP-OES),以及相关的样品制备步骤。ICP-MS 的高性能最适合在低浓度水平下对1级元素进行常规性测定,尤其是日摄入剂量较大(>10g/ 天)的药品。在此类药品和营养品中,抗酸剂由于具有极高的钙含量,给分析造成了极大的挑战。本文旨在展示如何正确地制备样品、适当地考量各种仪器设计因素,就能轻松地克服这项挑战。在本文中, 我们展示了利用珀金埃尔默公司最新NexION® 2000 ICP-MS,依照USP 通则<233> 的规定,对抗酸剂中1级和2A级元素杂质进行验证的数据
制药/生物制药
2017/12/03












