推荐厂家
暂无
暂无
 银牌9年
银牌9年
 400-860-5168转3750
400-860-5168转3750
 留言咨询
留言咨询
 白金10年
白金10年
 400-878-6829
400-878-6829
 留言咨询
留言咨询
 金牌19年
金牌19年
 400-633-0963
400-633-0963
 留言咨询
留言咨询

 400-895-0897
400-895-0897
 留言咨询
留言咨询

 400-860-5168转3181
400-860-5168转3181
 留言咨询
留言咨询

 400-860-5168转1545
400-860-5168转1545
 留言咨询
留言咨询






现在大多数对细胞超微结构的观察多采用化学染色法固定、染色、脱水、包埋的前处理,电镜观察。想请教一下各位大虾,有没有什么好的技术能实现对活细胞的超微结构的实时动态观察啊?最好不要染色什么的处理,直接在生理状态下就能观察。需要国内能够买到的仪器,谢谢大家了。目前查了一下文献,好像原子力显微镜、相差显微镜说可以,但我看了一下成像,感觉不如电镜的分辨率高啊。还有共聚焦显微镜,需要使用特定的荧光探针。
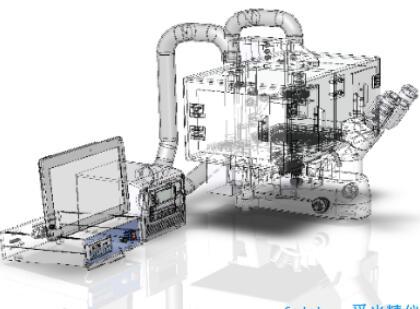
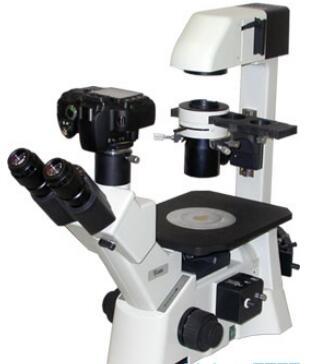
[url=http://www.f-lab.cn/microscope-incubators/mio.html][b]显微镜活细胞培养箱[/b]([b]Microscope Incubation Chamber[/b] )[/url]是欧盟专业为生物,生命科学,医学等科学实验而设计的[b]显微镜CO2培养箱[/b]和[b]显微镜活细胞培养系统[/b],它为科学家提供CO2浓度,O2浓度,温度和气流可调的环境用于显微镜观察实验。[img=显微镜活细胞培养箱]http://www.f-lab.cn/Upload/Mio2.jpg[/img][img=显微镜活细胞培养箱]http://www.f-lab.cn/Upload/MOFI-600_.jpg[/img][b]显微镜活细胞培养箱[/b]可匹配全世界所有品牌所有型号的商用显微镜,为实时活细胞实验提供理想可控的环境。科学家拥有这种显微镜活细胞培养箱可观察细胞内和细胞为发成的变化,以往,没有这种CO2显微培养箱时,科学家需要对死亡细胞染色后在显微镜下观察,现在, 这种显微镜CO2培养箱可以架设到显微镜上直接观察培养中的活细胞,它可以控制温度,气流,湿度,CO2浓度,氧气浓度等,为细胞实验创造出局部可控环 境[img=显微镜活细胞培养箱]http://www.f-lab.cn/App/Tpl/Home/Default/Public/images/grey.gif[/img]显微镜活细胞培养系统是全球唯一做到100%可控的封闭空间,其它同类显微镜活细胞培养箱的控制是被动的,随机的,热空气扩散从一个热源发出以维持设定 温度,而这套显微镜活细胞培养箱没有热空气回风口问题,加热空气从培养箱与显微镜结合处的预留缝隙中自然随机逸出,使得腔内的热空气和温度更加均匀,克服 了其它产品温度不均匀问题。即使电流不稳或振动干扰,热点也不漂移,规避了剧烈温度漂移对环境的干扰。[img=显微镜活细胞培养箱]http://www.f-lab.cn/Upload/Mio.jpg[/img][b][b]显微镜活细胞培养箱[/b]特色[/b]独特的热扩散机制,结合领先空气导入和回风机制,提供连续稳定的气流,腔内温度均匀,没有局部温度热点和冷点外部加热器可以远离这个显微镜CO2培养箱,消除电干扰和振动干扰超高温度精度控制和温度稳定性具有最小的温度漂移,达到缓解平衡点后,样品处的温度精度高达±0.1º C,腔内平均温度精度高0.2º C即使开门,领先的气流流型和温度均匀性控制能力也消除剧烈的环境温度变化人体工程学设计,操作方便,XY位移台和聚焦控制器外置于腔体外,大面积开门设计,更为方便操作操作样品,试管等超精密封闭温度探针实时探测内部温度CO2浓度和O2浓度可调高精度控制器控制气流,CO2,O2和温度,并显示当前监测到的浓度数据和温度数据显微镜活细胞培养箱:[url]http://www.f-lab.cn/microscope-incubators/mio.html[/url]
摘要激光扫描共聚焦显微镜作为80年代发展起来的一种高精度分子细胞生物学分析仪器,具有组织细胞断层扫描、活细胞动态荧光监测、三维图像重建、共聚焦图像定量分析等先进功能,在近年的细胞凋亡这一研究热点中得到了大量创造性的应用。本文拟就对激光扫描共聚焦显微镜在凋亡的形态学、分子水平变化及重要生理过程三方面研究中的应用及其成果做一综述。细胞凋亡(apoptosis)是不同于细胞坏死的一种细胞主动死亡方式,并由特定的基因控制。凋亡细胞在形态上出现变圆皱缩、染色质浓缩边集、核碎裂、凋亡小体形成等变化,并最终由非炎症过程清除。由于细胞凋亡独特地影响着机体的细胞发育和代谢,在监测和清除肿瘤细胞与突变细胞等方面也可能发挥重要的作用,近年来受到了细胞生物学、分子生物学、免疫学等多学科的广泛关注。激光扫描共聚焦显微镜(laser scaing confocal microscopy, LSCM)是80年代发展起来的一种高精度分子细胞生物学分析仪器,辅以各类免疫荧光探针或荧光染料与被测物质特异性结合,不仅可观察固定的细胞组织切片,还可对活细胞的结构、分子和离子进行实时动态地观察和检测。在细胞凋亡的研究中,激光扫描共聚焦显微镜已被广泛地应用于形态学、分子水平监测及重要生理改变等各方面,其中不乏新颖之处,并获得了大量成果,以下将就此做一简单的介绍。激光扫描共聚焦显微镜与凋亡的形态学激光扫描共聚焦显微镜用点光源扫描标本的光学横断面,以代替普通光学显微镜所使用的场光源,并用探测针孔滤去离焦光线,所以消除了来自焦平面以外的衍射或散射光的干扰,可实现高清晰、高分辨率的组织细胞断层扫描。并且由于激光扫描共聚焦显微镜采用数字化成像,因而辅以一定的软件就能对图像进行定量分析及三维重建等操作。过去对细胞凋亡的形态学研究方法局限于活性细胞和组织切片染色、荧光镜观察,或者石蜡切片原位末端标记法。由于普通光镜的分辨率和清晰度有限,而电镜又显然不适合对凋亡这一复杂动态过程的监测,激光扫描共聚焦显微镜的应用使人们对细胞凋亡的形态学观察分析提高到了一个前所未有的新水平。细胞核核膜的破坏对于染色质聚集并形成凋亡小体起重要作用。lamin是构成核片层的蛋白质,位于核膜的内表面,由caase-6介导的lamin裂解可影响核膜的完整性。在McCall等的研究中,对果蝇卵子发生晚期的细胞凋亡现象进行了动态观察。以单抗mAb101标记其哺育细胞核内膜的laminDm0(哺乳类laminB的同源体),用激光扫描共聚焦显微镜加以观察。正常哺育细胞到11期时,染色的lamin呈弥散的雾状分布并围绕核周,而dcp-1GLC哺育细胞即使到了较晚的14期时,仍然显示界线明确的染色。可见dcp-1突变体在核lamin蛋白的酶切或解聚方面存在缺陷。细胞器Li 等在对C(6)-酰基鞘氨醇诱导胞内囊泡产生的研究中,在不产生中毒效应的情况下,加入10microM C(6)-酰基鞘氨醇以诱导鼠纤维母细胞(3T3-L1和3T3-F442A)凋亡。观察到囊泡的形成与C(6)-酰基鞘氨醇的诱导呈时间依从和剂量依从关系。大量小泡在其加入后8小时内出现,并且随时间而增大;大泡最终分布在核周,而小泡分布在细胞边缘。用抗-溶酶体膜蛋白抗体和共聚焦免疫荧光显微分析,证明增大的囊泡为晚期内吞体/溶酶体。另外,胞内的细胞器都有其适用的荧光探针,如高尔基复合体常用的探针有Dceramide、BODIPY ceramide等,内质网常用的有Dil、DiOC6等,经标记均可进行精细的观察。当然,激光扫描共聚焦显微镜在形态学中的优势更在于其对图像的三维重建功能,从而揭示过去只能在平面上显现的凋亡细胞在三维空间中的结构;而对细胞凋亡的动态过程,它可以用三维加时间的四维方式进行观察,来获取最逼真的形态学资料。凋亡过程中一些特征性的三维形态变化正期待着进一步具体的工作去发现。激光扫描共聚焦显微镜对凋亡细胞的分子水平监测随着分子生物学突飞猛进的发展,关于细胞凋亡分子机制的研究已有了很大的突破。细胞凋亡的信号传递途径及其调控涉及到大量的酶级联反应、生物大分子的空间转移等。而激光扫描共聚焦显微镜以其定性、定量、定时的优点,结合众多荧光探针的应用,成为了研究细胞凋亡分子水平变化的有力手段。DNA大分子DNA断裂以及染色质的异常凝聚,是细胞凋亡的关键,同时也是细胞核在细胞凋亡中具有标志性的变化。Columbara等报道将激光扫描共聚焦显微镜与原位TdT和Poll免疫荧光技术相结合,进而确定双链和单链DNA的断裂点。而在对细胞凋亡和细胞坏死区别的研究中,Kreel等在培养的K562细胞中加入放线菌素D以诱导凋亡,并对细胞的DNA片段进行了3’-末端标记。经激光扫描共聚焦显微镜观察发现K562细胞凋亡早期有大量DNA片段出现,且DNA片段弥散分布于除核仁外的细胞核区。伴随着凋亡的进展,细胞核内出现大量高标记密度的圆形小体。而采用NaN3或快速冻融法使细胞坏死,经激光扫描共聚焦显微镜观察证实,在坏死开始阶段并无DNA片段的出现,至少在坏死发生24小时后才有DNA片段产生。Caase家族Caases是一组高度保守的半胱氨酸蛋白酶,目前发现有11个成员。多数细胞凋亡是以Caase家族蛋白的激活并作用于其关键底物而实现的,而caases激活的关键又在于该家族蛋白间的级联反应,因此caases被认为是细胞凋亡的中心环节和执行者,成为研究的热点。Mandal等用激光扫描共聚焦显微镜对细胞凋亡中激活的caase-3的重分布进行了研究。用丁酸处理细胞后,观察到DNA-PKcs的裂解与caase-3的激活成正相关,而Bcl-2的过度表达则可抑制上述两个过程。同时还证明(1)激活后的caase-3重分布到核区,(2)裂解局部的DNA-PKcs和PARP(polyADP-ribosepolymerase,聚腺苷二磷酸核糖多聚酶),(3)裂解产物又被释放到核外的细胞液。caase-3的抑制物四肽DEVD-CHO又可抑制上述的三个连续的步骤。该研究提示:激活的caase-3在核内的重分布构成了丁酸所诱导的细胞凋亡中的一个重要凋亡信号。另外,在用激光扫描共聚焦显微镜对Q79诱导大鼠神经元凋亡的研究中,Sanchez等发现了Q79对caase-8的聚集和激活,而对caase-8的抑制则阻止了被诱导的细胞凋亡;加以Westernblot分析,还建立了caase-8的激活和某些神经退行性疾病(如舞蹈病)的联系。Grazyme丝氨酸蛋白酶grazyme为另一种重要的凋亡信号分子,对某些caase家族蛋白也有激活作用。Trapani等就证明了杀伤淋巴细胞利用穿孔素和grazymeB的协同作用来诱导靶细胞的凋亡,在其研究中通过激光扫描共聚焦显微镜观察到(1)50%细胞的胞核内快速聚集了以FITC荧光标记的grazymeB(最长7分钟,t1/2为2分钟),然后发生凋亡;(2)其它的细胞只有细胞液内有FITC-grazyme B的摄取,避免了凋亡。此间至少在13分钟后才有DNA碎片的出现,说明核内的grazyme B聚集出现在凋亡的执行阶段之前。并且通过对核内液的处理(加入70KDa FITC-dextran),间接观察到grazyme B的转移并非是因为核膜受caases的作用而破损,而是由于穿孔素的协同。其它以上的介绍显示,激光扫描共聚焦显微镜在检测活细胞酶活性动态变化方面有着突出的优势。实际上,对于细胞凋亡的分子机制这样一个极其复杂的课题,激光扫描共聚焦显微镜的应用远不只限于上述的几种离子和大分子,而是渗透到了大量的分枝课题中去。如在对重要的凋亡负调控蛋白Bcl-2的研究中,Beham等利用基因毒性损害(genotoxic damage)诱导细胞凋亡,并以Bcl-2蛋白抑制其凋亡过程。用激光扫描共聚焦显微镜和Immunoblotting观察显示,Bcl-2的作用在于阻止了诱导产生的p53蛋白向核内的转运。而Ohsawa等对独立于caase家族的另一种重要蛋白酶—组织蛋白酶进行了研究,用血清剥夺法诱导PC12细胞凋亡,并用激光扫描共聚焦显微镜监测了其精细超微结构改变过程和细胞内组织蛋白酶B和D的免疫活度的对比变化。又如,在人胰岛淀粉样多肽(hIA)的研究中,Hiddinga等用表达hIA的质粒转染COS-1细胞诱导凋亡,辅以免疫组化染色,用激光扫描共聚焦显微镜证明了hIA在细胞的内质网和高尔基复合体内呈簇状沉积,并与细胞