推荐厂家
暂无
暂无
 留言咨询
留言咨询
 留言咨询
留言咨询
 留言咨询
留言咨询

 400-893-6099
400-893-6099
 留言咨询
留言咨询

 400-668-7609
400-668-7609
 留言咨询
留言咨询

 400-668-7609
400-668-7609
 留言咨询
留言咨询


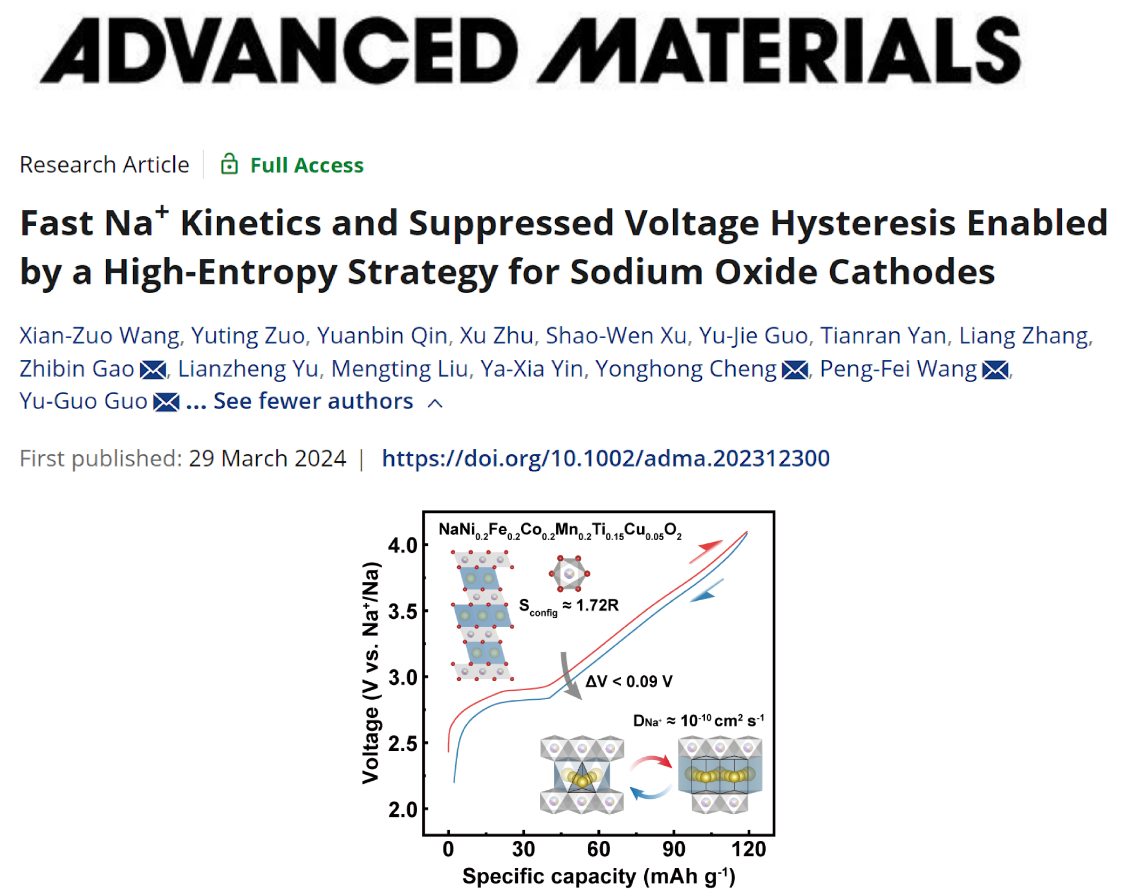




准备定量检测水中钠离子含量,但是条件有限,无法采取火焰原子吸收和离子色谱法,在论坛里看到有大侠提到了滴定法、紫外分光光度计法等,是否有大神知道具体方法步骤,如有其它方法,也请赐教,谢谢大家了!!!
如题,俺要用离子交换色谱测定样品中微量钠离子的含量(5ppm左右),在一个公司测得,仪器是Dionex, DX-120,色谱柱为IonPac CS16,进样量 0.05 mL ( 1 wt% in H20),谱图中除了钠离子的峰,还多出一个小峰,为何?开始通过标样测定,钠离子的保留时间在7.5 min,但是我的待测样IC谱上除了7.5 min 时出了一个峰外,11 min左右还有一个小峰,请问这个是其他杂质离子引起的吗?貌似测定的老师说我让他测定我样品中钠离子的含量,他就用了特异性的测量,测定电导率随时间变化啥的,貌似只能检测钠含量的。俺是离子色谱成分鉴定的外行,恳请专业的兄弟姐妹告知,IC谱中每一个峰是不是一定就代表一种存在的离子啊?非常感谢!!!
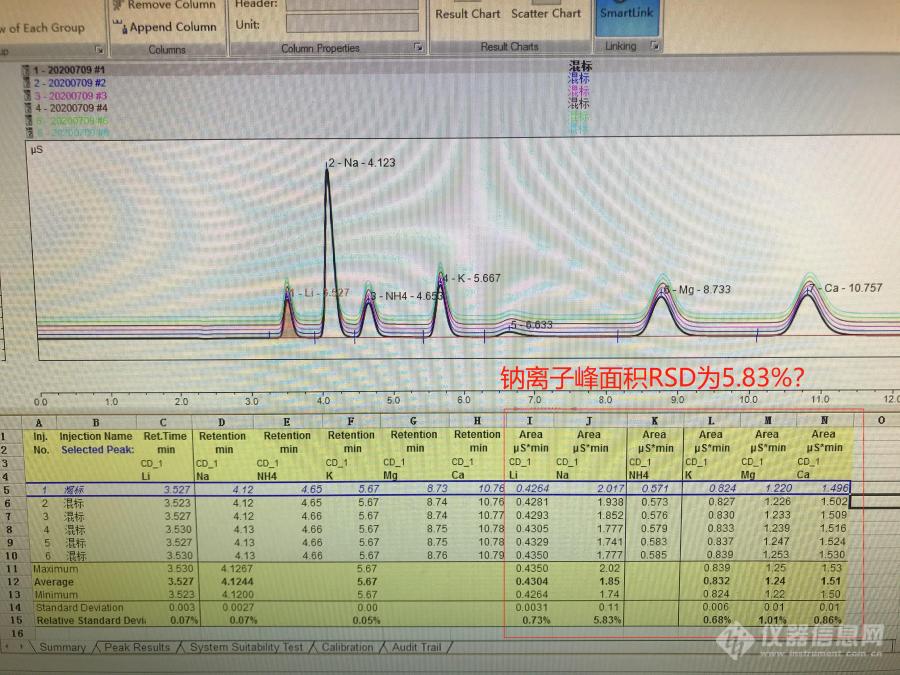
[font=宋体][size=10.5000pt][font=宋体]用阳离子混标测定[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]进样重复性的过程中,发现钠离子的峰面积[/font]RSD[font=宋体]偏大,为[/font][font=Calibri]5.83%[/font][font=宋体],超过[/font][font=Calibri]2.0%[/font][font=宋体],而其他各组分锂、铵、钾、镁、钙峰面积的[/font][font=Calibri]RSD[/font][font=宋体]均在[/font][font=Calibri]1.0%[/font][font=宋体]以内,针对钠离子含量异常进行排查。[/font][/size][/font][font=宋体][size=10.5000pt]阳离子测试色谱条件:[/size][/font][font=宋体][size=10.5000pt][font=宋体]流动相:[/font]20mM[font=宋体]甲磺酸; 流速:[/font][font=Calibri]1.0ml/min[/font][font=宋体];进样体积:[/font][font=Calibri]25[/font][font=宋体]微升;柱温:[/font][font=Calibri]30[/font][/size][/font][font=宋体][size=10.5000pt]℃[/size][/font][font=宋体][size=10.5000pt];[/size][/font][font=宋体][size=10.5000pt][font=宋体]色谱柱:[/font]Dionex IonPac GS12A[font=宋体]阳离子分析柱;[/font][font=Calibri]Dionex IonPac CG12A[/font][font=宋体]阳离子保护柱;[/font][/size][/font][font=宋体][size=10.5000pt]供试品:阳离子混合标准品。[/size][/font][font=宋体][size=10.5000pt]1. [/size][/font][font=宋体][size=10.5000pt][font=宋体]连续进样[/font]6[font=宋体]针阳离子混标,偏偏钠离子[/font][font=Calibri]RSD[/font][font=宋体]大于[/font][font=Calibri]2.0%[/font][font=宋体],钠离子的出峰位置不对?[/font][font=Calibri]RSD[/font][font=宋体]偏大的峰并非钠离子,而是其他成分?[/font][/size][/font][img=,690,517]https://ng1.17img.cn/bbsfiles/images/2020/07/202007212229289376_9858_3898318_3.jpg!w690x517.jpg[/img][font=宋体][size=10.5000pt]2. [/size][/font][font=宋体][size=10.5000pt][font=宋体]为了确认各组分的出峰位置,对各组分进行单独定位,结果发现钠离子出峰位置确实为[/font]4.1min[font=宋体]左右,且钠、钾、铵三个单独组分定位的钠离子位置都含有钠离子成分?钠离子来自于水中?配样中所用的水含有钠离子?[/font][/size][/font][font=宋体][size=10.5000pt][font=宋体][img=,690,517]https://ng1.17img.cn/bbsfiles/images/2020/07/202007212230003039_3767_3898318_3.jpg!w690x517.jpg[/img][/font][/size][/font][font=宋体][size=10.5000pt]3. [/size][/font][font=宋体][size=10.5000pt][font=宋体]分别运行超纯水、屈臣氏纯净水、钠离子定位溶液,发现均在[/font]4.1min[font=宋体]左右含有钠离子,且出峰位置高度重合。但无法解释的是屈臣氏空白水中含有的钠离子比定位溶液中的钠离子都要多,这有点匪夷所思。[/font][/size][/font][img=,690,517]https://ng1.17img.cn/bbsfiles/images/2020/07/202007212230453703_2671_3898318_3.jpg!w690x517.jpg[/img][font=宋体][size=10.5000pt]4. [/size][/font][font=宋体][size=10.5000pt][font=宋体]尝试采用手动进样超纯水空白溶剂,结果发现钠离子位置无明显峰,看来水的问题好像不大。回顾试验过程,采用的进样小瓶为新购买的玻璃小瓶,难道新买的玻璃小瓶中含有钠离子?问题的矛头越来越指向进样小瓶,采用清洗干净的进样小瓶进样,结果出峰正常,钠离子峰面积[/font]RSD[font=宋体]为[/font][font=Calibri]0.68%[/font][font=宋体],其他各组分峰面积的[/font][font=Calibri]RSD[/font][font=宋体]均在[/font][font=Calibri]1.0%[/font][font=宋体]以内[/font][/size][/font][img=,690,517]https://ng1.17img.cn/bbsfiles/images/2020/07/202007212231254039_8020_3898318_3.jpg!w690x517.jpg[/img]结论:[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]中采用的进样小瓶使用前需清洗干净,尽量采用塑料小瓶,以减少无关离子的引入。遇到问题后,要逐步排查,以找到其根本原因。


