推荐厂家
暂无
暂无



 400-622-8982
400-622-8982
 留言咨询
留言咨询

 400-860-5168转4826
400-860-5168转4826
 留言咨询
留言咨询

 400-860-5168转1587
400-860-5168转1587
 留言咨询
留言咨询



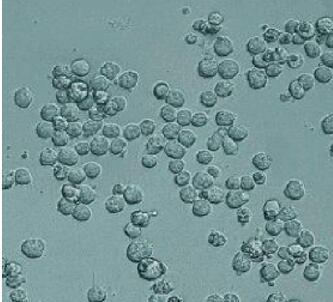
作者: 陈文庆 王建超 刘华杰 高飞 张韧 (北京清大天一科技有限公司 102200 ) (《中国兽药杂志》 2010.44 ( 10 ): 37-41 )【摘要】 采用反应器全悬浮培养BHK21细胞生产口蹄疫病毒与微载体悬浮培养Vero细胞生产狂犬病毒分别与相应的转瓶培养工艺生产案例对比分析,比较悬浮培养工艺与转瓶培养工艺的生产效益。分析显示,与转瓶培养工艺相比,反应器悬浮培养工艺获得的细胞密度、病毒效价、产品的产量和质量明显提高,生产时的能耗和劳动力需求明显降低。结果表明悬浮培养工艺的生产效益明显高于转瓶培养工艺,适宜于国内生物制品工业化生产的升级换代。【关键词 】 细胞培养;生物反应器;悬浮培养;微载体细胞悬浮培养技术是指细胞在生物反应器中自由悬浮于培养液内生长增殖的一种培养方法。根据细胞是否贴壁,又分为全悬浮细胞培养和贴壁细胞微载体培养。国际上该项技术发展较快,已趋向成熟,是疫苗、抗体等生物制品生产的普遍生产工艺模式。与转瓶培养技术相比,该工艺具有操作简单、产率高、容易放大等优点,本文结合口蹄疫病毒和狂犬病毒的生产,分别对细胞悬浮培养工艺与转瓶培养工艺的经济效益等进行了分析和分析。1. 全悬浮培养口蹄疫病毒与转瓶培养案例对比高效、安全的病毒性疫苗是防止口蹄疫情发生的最有效方法。BHK21细胞是繁殖FMDV的理想宿主,早在1962年Capstick PB等就实现FMDV的悬浮培养。1965年Telling, R.C.等实现在不锈钢发酵罐中悬浮培养BHK21细胞生产口蹄疫疫苗。目前国外(Intervet公司、Merial公司)普遍已经采用2000~5000L反应器悬浮培养BHK21细胞生产口蹄疫苗。本文就本公司自主研发的650L生物反应器和无血清培养基进行悬浮培养BHK21细胞生产口蹄疫疫苗与转瓶培养工艺进行比较和分析。1.1主要材料细胞株:BHK21贴壁细胞株(中国兽医药品监察所)毒 株:FMDV-O型(某兽用疫苗企业)培养基:低血清MEM培养基(产品代号MD611)、BHK21细胞无血清培养基(北京清大天一科技有限公司)血 清:特级新生牛血清(杭州四季青生物工程材料有限公司)仪 器:5 L反应器(德国贝朗),120L和650LCLAVORUS ® 生物反应器(北京清大天一科技有限公司)1.2实验方法1.2.1转瓶培养BHK21细胞生产口蹄疫病毒将复苏的BHK21细胞在T75培养瓶中使用低血清培养基(含5%牛血清)培养,连续传代扩增接种15L转瓶,37 ℃培养48小时,传代比例为1:8-1:10,按常规方法接种病毒及维持液,细胞病变90%左右收获病毒液。1.2.2反应器全悬浮无血清培养BHK21细胞生产口蹄疫病毒(1)贴壁细胞悬浮驯化培养:用BHK21细胞无血清培养基在恒温摇床或者方瓶中无血清驯化贴壁BHK21细胞,可采用直接驯化或者逐级降低血清驯化等方法,每代观察细胞数量和细胞活率,直至BHK21细胞在无血清培养基中的生长增殖速率正常,细胞活率达95%以上,并可连续稳定传代,说明细胞已适应无血清悬浮培养。(2)反应器用种子细胞扩增:采用反应器罐倒罐逐级放大技术,细胞从摇瓶→5 L反应器→120 L反应器→650 L反应器进行逐级放大培养。细胞培养方式为批培养,控制反应器各参数在正常范围:温度37.0 ℃、pH7.2~7.4、溶氧(DO)20~70%、搅拌转速50~150 r/min。(3)反应器培养口蹄疫病毒:待650 L反应器中细胞达到一定密度,提高培养pH至7.5左右,按一定比例直接接种口蹄疫病毒进行病毒维持培养,控制温度、pH、DO、搅拌转速等参数在合适范围,在线无菌间隔取样判断细胞病变情况并检测病毒毒价(LD50,TCID50),确定收获的最佳时间。1.3 细胞培养结果对比分别对低血清培养基15 L转瓶培养的贴壁BHK21细胞进行观察和细胞计数,反应器全悬浮培养的BHK21细胞取样进行数量和活率检测。培养条件和结果对比见表1。表1 转瓶培养和反应器全悬浮培养BHK21细胞对比http://img.dxycdn.com/trademd/upload/userfiles/image/2013/10/A1380442105_small.jpg http://img.dxycdn.com/trademd/upload/userfiles/image/2013/10/A1380442106_small.jpg http://img.dxycdn.com/trademd/upload/userfiles/image/2013/10/A1380442107_small.jpg 图1 转瓶BHK21细胞低血清培养48 hr,100X 图2 反应器全悬浮无血清培养48 hr,100X 结果显示,转瓶培养的BHK21细胞,培养48小时显微镜观察成致密单层,见图1,96小时细胞开始出现脱落死亡;反应器无血清全悬浮培养BHK21细胞48小时的细胞显微镜观察状态如图2,生长至96小时细胞密度可达5.4x106 cells/ml,活率维持在94%左右。从细胞数量比较,650L反应器培养一批的细胞数量相当于500~700个15 L转瓶培养的细胞总量。1.4 病毒培养效果对比两种不同培养工艺,细胞在满足活力要求的基础上,以同等条件分别接种FMDV病毒,取样测定病毒毒价,结果见表2。 表2 转瓶和反应器全悬浮培养BHK21细胞病毒毒价对比http://img.dxycdn.com/trademd/upload/userfiles/image/2013/10/A1380442112_small.jpg结果表明,无血清悬浮培养的口蹄疫病毒毒价(TCID50和LD50)检测不低于转瓶培养工艺。根据反应器低血清悬浮培养BHK21细胞生产口蹄疫完整病毒粒子(146S)检测较转瓶高10倍左右的情况,应用无血清悬浮培养工艺,杂蛋白含量更少,口蹄疫完整病毒粒子和口蹄疫疫苗质量均提高。1.5 反应器和转瓶经济效益估算对比依据培养BHK21细胞生产口蹄疫病毒工艺过程要求,从细胞密度、病毒毒价、产品效力、资源环境、劳动力等方面进行简单对比,借以一窥二者的经济效益差别(见表3)。 表3 反应器无血清悬浮培养与转瓶培养BHK21细胞经济效益对比http://img.dxycdn.com/trademd/upload/userfiles/image/2013/10/A1380442114_small.jpg*按照反应器无血清悬浮培养一条生产线(5L-120L-650L)、转瓶体积15 L进行对比按照目前培养BHK21细胞生产口蹄疫病毒质量要求,对悬浮无血清培养工艺的产能进行预估,一条5L-120L-650L的反应器生产线年生产病毒量约为2.1亿毫升,生产疫苗量约为4.2亿毫升。2. 人狂犬病毒微载体培养与转瓶培养的对比我国是受狂犬病危害最为严重的国家之一,近年报告狂犬病死亡人数均在2400人/年以上,一直位居我国各类传染病报告死亡数的前三位,根据有关国家成功控制狂犬病的经验,世界卫生组织提出倡议,到2020年消除人狂犬病。我国距此倡议目标还有大量工作要做,国内也对人用和兽用狂犬病疫苗的生产做了大量研究工作。下面就120L反应器微载体培养Vero细胞生产狂犬病毒效果与转瓶培养工艺和培养效果比较分析。2.1主要材料细胞株:Vero细胞株毒 株:aG株(细胞株和毒株均来自某人用疫苗企业)培养基:低血清199培养基(产品代号MD504)、 Vero细胞反应器培养用培养基(产品代号MD505), 均来自北京清大天一科技有限公司仪 器:5 L反应器(德国贝朗)、120LCLAVORUS ® 生物反应器(北京清大天一科技有限公司)血 清:特级新生牛血清(杭州四季青生物工程材料有限公司)微载体:Cytodex 1 (美国GE
张韧,王建超,陈文庆,刘华杰,高飞,徐舸辰,林龙飞(北京清大天一科技有限公司,北京102200) 反应器悬浮培养技术是目前国内外疫苗生产的热点之一,它可以极大提高疫苗的质量和生产率。介绍了该技术在国内外疫苗生产中的研发和应用现状,表明国内该技术目前已经在口蹄疫疫苗生产中获得成功应用,利用MDCK、Vero等细胞培养生产禽流感疫苗的技术也正在积极研发中,并将逐步替代传统的鸡胚生产工艺。积极推广和应用这一新型疫苗生产技术将是我国兽用生物制品行业升级换代的必然趋势。 生物反应器;悬浮培养;微载体培养;口蹄疫;禽流感 在我国,细胞反应器悬浮培养和微载体培养技术在动物疫苗生产领域的研发和应用正成为行业技术革新、产业升级的重要内容。农业部公告第1708号中明确规定,自2012年2月1日起,各省级兽医行政管理部门停止转瓶培养生产方式的兽用细胞苗生产线项目兽药GMP验收申请。该公告对动物疫苗生产技术升级做出了强制性规定。本文就反应器细胞悬浮培养和微载体培养技术在口蹄疫疫苗和禽流感疫苗生产中的国内外应用和发展进行了综述,分析了动物疫苗产业发展趋势和我国疫苗产业技术升级所面临的机遇和挑战。1 反应器悬浮培养技术在口蹄疫疫苗生产中的应用口蹄疫被认为家畜传染性疾病中传染性最强的一种疾病,国际兽医局(OIE)将之列为A类传染病。2010和2011年,在亚洲、非洲都有口蹄疫局部的爆发。接种安全、高效的疫苗是预防口蹄疫疫情发生的最有效策略之一。通常主要通过浓缩技术提高口蹄疫疫苗的有效抗原量来实现其高效性;通过病毒纯化工艺、有效的病毒灭活工艺来保证疫苗的安全性。反应器悬浮培养BHK21细胞生产口蹄疫病毒能显著提高口蹄疫病毒抗原浓度。国际上先进的口蹄疫疫苗的生产工艺都采用反应器悬浮培养BHK21细胞技术、有效的病毒纯化工艺及二次病毒灭活工艺。当前,面对国内外严峻的口蹄疫防控形势,高质量的口蹄疫疫苗必将在口蹄疫防控中发挥关键作用。1.1 国外应用现状和发展趋势 BHK21细胞是繁殖口蹄疫病毒的理想宿主。20世纪60年代,许多国家实验室建立起了转瓶培养BHK21细胞繁殖口蹄疫病毒的生产系统。1962年BHK21细胞悬浮培养成功,细胞增殖迅速,并成功应用于口蹄疫病毒的生产。反应器悬浮培养BHK21细胞生产口蹄疫病毒也就成为最普遍的口蹄疫疫苗生产方式,主要集中在印度、土耳其、巴西、阿根廷等国家(表1)。印度口蹄疫生产企业使用8000L反应器生产口蹄疫疫苗,南美口蹄疫疫苗生产企业一般采用3000~5000 L反应器生产口蹄疫疫苗,口蹄疫病毒抗原146S浓度大约在2 μg/mL。因为口蹄疫疫苗保护力与146S有正相关性,这些企业根据口蹄疫病毒146S来配制疫苗有效地保证了疫苗的质量。表1 国外部分悬浮培养BHK21细胞生产口蹄疫疫苗企业及其生产工艺http://img.dxycdn.com/trademd/upload/userfiles/image/2013/08/A1375859824_small.jpg*来自作者所属公司的客户信息调查但是,这种20世纪60年代开发的口蹄疫疫苗生产工艺延续至今,存在许多技术上的缺陷。国外口蹄疫疫苗生产使用的BHK21细胞培养液是添加磷酸肉汤(Tryptosephosphate broth, TPB)或水解乳蛋白(Lactalbumin hydrolysate, LAH)的GMEM及EMEM,再补加5%~10%牛血清(表1)。不同批次间血清质量差异引起细胞培养效果不稳定,导致影响疫苗生产工艺的稳定性和疫苗质量。疫苗中残留的血清蛋白使接种动物过敏反应升高,一定程度上影响疫苗的安全性。在口蹄疫强制免疫的国家,牛血清中存在含有抗口蹄疫病毒抗体的可能性,不仅影响病毒繁殖,而且可能导致口蹄疫病毒在抗体压力下选择性变异。牛血清中潜在污染朊病毒或疯牛病病毒可给动物疫苗带来潜在的生物危害,TPB或LAH等动物来源成份也存在安全隐患。为提升产品质量及安全性,目前国外多数口蹄疫疫苗生产厂家急于将现使用的含血清生产工艺升级为不含血清生产工艺。自从20世纪的80年代起,细胞培养基(液)发展迅速,低血清细胞培养基、无血清细胞培养基、无血清无动物来源成分细胞培养基已商品化,为疫苗生产中少使用或不使用血清奠定了物质基础。1.2 国内应用现状 默克密理博北京清大天一科技有限公司(以下简称“清大天一”)在国内较早开发了BHK21低血清细胞培养基和BHK21无血清无动物来源成分细胞培养基。2008年,清大天一开发了BHK21低血清细胞培养基及反应器悬浮培养BHK21技术,并于2009年成功应用到国内一家口蹄疫疫苗生产企业中。使用该工艺生产的口蹄疫抗原146S浓度可以达到3 μg/mL左右,工艺全过程管道化操作,产品内毒素含量低,口蹄疫疫苗生产和质量显著提高,同时生产成本下降30%。2009年,清大天一成功开发了BHK21无血清无动物来源成分培养基和反应器无血清悬浮培养BHK21细胞技术,并 2010年成功应用到国内某口蹄疫生产企业。相比于含血清悬浮培养工艺,无血清悬浮培养工艺具有巨大的技术优势。从种子库复苏BHK21细胞开始,到口蹄疫病毒繁殖、直至收获的全过程,不添加任何的血清和动物来源成分,消除了血清抗体对病毒繁殖的干扰,同时减轻了纯化压力。无血清悬浮培养BHK21细胞的细胞密度可以达到5×106~6×106/mL以上,为生产高浓度口蹄疫疫苗奠定了技术基础。图1是反应器无血清培养BHK21细胞生产口蹄疫病毒的工艺流程图,相比于含血清口蹄疫病毒生产工艺,因实现细胞无血清培养,工艺过程无需沉降换液。 http://img.dxycdn.com/trademd/upload/userfiles/image/2013/08/A1375859832_small.jpg 图1 4000L反应器无血清悬浮培养BHK21细胞生产口蹄疫病毒工艺流程目前国内某企业使用该工艺生产的口蹄疫疫苗正处于报批阶段,其他多家口蹄疫疫苗生产企业及研究单位也在研发或寻求无血清悬浮培养生产口蹄疫疫苗的工艺。
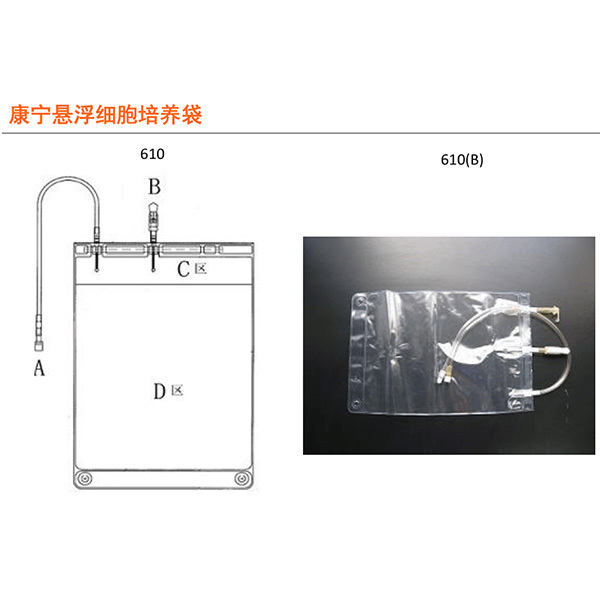
对于微生物培养,大家常用的是恒温培养箱、霉菌培养箱、震荡培养箱、恒温水浴箱、发酵罐等,满足了日常工作需要;当然,这都是针对好氧菌而言。 而对于厌氧菌和兼性好氧菌,则需要考虑选用合适的厌氧、微好氧/低氧培养装置(如厌氧培养盒/袋、厌氧罐以及专业的厌氧培养箱、厌氧工作站、微好氧/低氧培养箱、厌氧发酵罐/反应池等)。 常规的动物细胞培养,一般选用CO2培养箱、滚瓶培养装置、悬浮培养装置、生物反应器/细胞培养罐等。为更接近或模拟体内微环境,三气培养箱(即CO2培养箱加配O2传感器)逐渐为人们所熟知!当然,更专业的Biospherix 系列O2/CO2控制器加培养盒、H35微好氧/低氧细胞培养箱、X vivo 一体化细胞工作站等三气培养装置也给大家提供了更多的选择!