推荐厂家
暂无
暂无
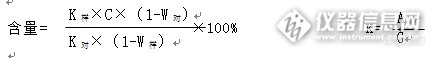
[align=left][b] 摘要 目的:[/b]近年来,国内外很多专家学者对甲钴胺在治疗领域中的作用展开了比较广泛研究。对甲钴胺原料药合成工艺进行研究发现这种制备工艺,甲钴胺的收率仅为80%。且合成过程中容易产生杂质,引起毒副作用,催化剂以及甲基化试剂对环境也有危害作用。针对上述工艺中的缺点及不足,本课题对甲钴胺制备工艺进行了全新的研究。[b]方法:[/b]经过一年多的小试工艺摸索,研制出了甲钴胺生产的工艺路线和控制参数,制备出高品质环境友好的合格产品。此工艺将氰钴胺、新型甲基化试剂、新型还原剂的催化剂及限制试剂用水在反应器中充分混合,用高纯氮气除氧后滴入硼氢化钠的稀碱溶液,该反应可一步生成甲钴胺。[b]结果:[/b]本课题确定了还原剂及其催化剂的工艺条件,有效控制了还原剂的还原速度,使得氰钴胺能够快速生成二价态的B12,减少了副反应的发生。由于在还原反应阶段使用了新型催化剂,它不仅能够让还原剂水解彻底,而且该催化剂能够重复利用,减少环保压力。本课题选取了新的甲基化试剂,该甲基化试剂具有溶于水、甲基化能力强、不产生异味物质等优点,这对实际生产益处多多。[b]结论:[/b]这种甲钴胺的新型制备方法中,以氰钴胺当作原料,生成过程中,甲钴胺一步合成,生产工艺简单,生产条件方便控制,对于设备没有过多要求,甲钴胺收率平均约93%,生产过程中污染物产生量小,拥有很高的实用价值。[/align][align=left][b]关键词:[/b]甲钴胺原料药;生产工艺;反应试剂与条件;环保; 甲钴胺属于辅酶型的一种维生素,甲钴胺甲基化官能团能够参与到体内甲基转移作用中,从而对体内神经组织核酸、蛋白质和脂肪的新陈代谢等都具有良好促进作用。在人体代谢中,甲钴胺和腺苷钴胺能够直接参与体内代谢,对疾病起到直接治疗作用。从甲钴胺的结构形式来说,甲基VB12要比普通氰钴VB12疗效更好,因此可以说甲基VB12未来将是氰钴VB12的一个更新换代产品。国内外学者在对甲钴胺临床作用研究中发现甲钴胺对于糖尿病的周围神经病变拥有良好治疗作用,能够改善糖尿病周围神经的形态,让神经损害得以修复。甲钴胺还在三叉神经痛、面神经炎治疗等领域有良好治疗作用。在这种情形下,开展甲钴胺原料药工艺技术研究开发与生产,生产出成本低、质量高、对环境污染小的产品,满足临床用药需求,具有重大现实意义,提高药品质量,降低成本,更方便国内患者用药。[b]1甲钴胺制备与质量控制的材料与方法1.1甲钴胺制备主要仪器与原料[/b]氰钴胺、硼氢化钠 、甲基化试剂 CH3-X、丙酮、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]、高压液相色谱仪、旋转蒸发器、电热恒温水浴锅、PHS-3C型酸度计、电子天平等。[b]1.2制备路线[/b]氰钴胺—→还原—→还原态氰钴胺—→甲基化—→ 甲基氰钴胺溶液—→树脂吸附—→洗脱液—→结晶—→干燥—→成品—→包装[b]1.3质量控制1.3.1鉴别[/b](1)避光操作,分别取本品和对照品各约5mg,置100ml容量瓶中,加水溶解,定容至刻度,摇匀备用。照紫外-可见分光光度计标准操作规程,进行波长扫描检测,供试品溶液在220~550nm的波长范围内的吸收光谱应与对照品溶液的一致。(在266nm、342nm、525nm处有最大吸收)。仪器:紫外-可见分光光度计,100ml容量瓶(2)本品经有机破坏后,加醋酸钠和稀醋酸使溶液pH值为6.0,Co[sup]3+[/sup][sup][/sup]离子与1-亚硝-2-萘酚-3,6-二磺酸钠(亚硝基R盐)配位化,生成红色的配位化合物。仪器:[b] [/b]坩埚、电炉、十万分之一电子天平。试剂:硫酸氢钾、酚酞指示液、氢氧化钠试液、醋酸钠、稀醋酸、0.2%1-亚硝基-2-萘酚-3,6-二磺酸钠、盐酸。(3)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与甲钴胺对照品溶液主峰的保留时间一致。(4)取本品照红外光谱测定法进行红外光谱测定,本品的红外光吸收图谱应与对照的图谱一致。[b]1.3.2水分仪器: [/b]自动水分滴定仪、十万分之一电子天平、称量舟。[b]试剂:[/b]卡尔费休试剂[b]偏差:[/b]同样方法同时测定三个平行样,三个数据的RSD应≤5.0%,取平均值报告。[b]1.3.3 HPLC含量测定仪器:[/b]高效液相色谱仪,紫外检测器,0.45μm微孔滤膜,针头式过滤器,溶剂过滤器,真空泵,超声波水浴,酸度计,50ml、1000ml容量瓶,漏斗,20*20mm的称量瓶,十万分之一电子天平。[b]试剂:[/b]乙腈(色谱纯),磷酸二氢钾(分析纯),磷酸(分析纯)。[b]流动相的配制:[/b]称取磷酸二氢钾4.1g,置1000ml容量瓶中,加纯化水溶解并稀释至刻度,摇匀,用磷酸调节PH值为4.5后,用0.45μm的水系微孔滤膜过滤,即得0.03mol/l磷酸二氢钾溶液。将乙腈与0.03mol/L磷酸二氢钾溶液按16:84的比例混合均匀,放入超声波水浴中脱气10分钟,即得。[b]供试品溶液的配制:[/b]称取本品25[u]+[/u]2.5mg于称量瓶内,将称量瓶放入漏斗中,将样品经漏斗倒入50ml容量瓶中,用流动相冲洗称量瓶及漏斗,洗液并入容量瓶中,加流动相稀释至刻度摇匀,再精密量取5ml,置50ml容量瓶中,加流动相稀释至刻度摇匀,作为供试品溶液。使用前经0.45μm的油系微孔滤膜过滤。[b]对照品溶液的配制:[/b]取甲钴胺对照品同供试品溶液配制方法,配制对照品溶液。[b]色谱条件:[/b]色谱柱:C[sub]18[/sub]柱;检测波长:342nm;柱温:40℃。流速:调节流速使甲钴胺峰的保留时间约为12分钟(11.5分钟至12.5分钟)。[b]测试过程:[/b]照液相色谱仪标准操作规程依法操作。取对照品溶液与供试品溶液各20μl注入液相色谱仪,记录色谱图。按外标法以峰面积计算,即得。[b]系统适用性:[/b]系统表现:取甲钴胺对照品25[u]+[/u]2.5mg,置50ml容量瓶中,加水溶解并稀释至刻度,摇匀,在自然光下放置5~10分钟,取20μl注入液相色谱仪,调节流速使甲钴胺峰的保留时间约为12分钟,记录色谱图,甲钴胺峰与羟钴胺峰(相对保留时间约为0.2)的分离度应大于20,甲钴胺峰与相邻杂质峰之间的分离度应>1.5。系统重现性:取对照品溶液20μl注入液相色谱仪,重复进样5针,所得5张图谱中主峰面积的RSD≤2.0%。[b]偏差:[/b]取对照品K值的平均值计算,同一方法同时测定两个平行样,RD应≤0.5%。[b]计算公式:[/b][img=,436,58]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141943_01_1626619_3.png[/img]K[sub]对[/sub]:对照溶液主峰面积/所称对照品的重量(g)K[sub]样[/sub]:供试品溶液主峰面积/所称供试品的重量(g)C:对照品百分含量W[sub]对[/sub]:对照品水分W[sub]样[/sub]:供试品水分A:对照溶液(供试品溶液)主峰面积G:所称对照品(供试品)的重量(g)[b]1.3.4有关物质仪器:[/b] 高效液相色谱仪,紫外检测器,C[sub]18[/sub]色谱柱,0.45μm的微孔滤膜,针头式过滤器,溶剂过滤器,真空泵,超声波水浴,酸度计,50ml、1000ml容量瓶,漏斗,20*20mm的称量瓶,十万分之一电子天平。[b]试剂:[/b] 乙腈(色谱纯),磷酸二氢钾(分析纯),磷酸(分析纯)。[b]流动相的配制:[/b] 称取磷酸二氢钾4.1g,置1000ml容量瓶中,加纯化水溶解并稀释至刻度,摇匀,用磷酸调节PH值为4.5后,用0.45μm的水系微孔滤膜过滤,即得0.03mol/l磷酸二氢钾溶液。将乙腈与0.03mol/L磷酸二氢钾溶液按16:84的比例混合均匀,放入超声波水浴中脱气10分钟,即得。[b]供试品溶液的配制: [/b] 取本品25[u]+[/u]2.5 mg于称量瓶内,将称量瓶放入漏斗中,将样品经漏斗倒入50ml容量瓶中,用流动相冲洗称量瓶及漏斗,洗液并入容量瓶中。加流动相稀释至刻度,摇匀,作为供试品溶液。使用前经0.45μm的油系微孔滤膜过滤。[b]对照液配制: [/b] 精密量取供试品溶液0.5ml,置50ml容量瓶中,加流动相稀释至刻度摇匀,作为对照液。使用前经0.45μm的油系微孔滤膜过滤。[b]色谱条件:[/b] 色谱柱:C[sub]18[/sub]柱;检测波长:342nm;柱温:40℃。流速:调节流速使甲钴胺峰的保留时间约为12分钟(11.5分钟至12.5分钟)[b]测试过程:[/b] 照液相色谱仪标准操作规程依法操作。取供试品溶液与对照溶液各20μl,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的3倍。记录供试品溶液的色谱图中最大单个杂质峰面积、杂质峰面积之和及对照液主峰面积。[b]偏差:[/b] 同一方法测定两个平行样,RD应≤5.0%,取两个结果的算术平均值报告。计算公式:[img=,361,112]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141945_01_1626619_3.png[/img][b]2 甲钴胺制备工艺研究2.1 还原反应的催化剂及限制试剂的选取[/b] 根据专利和文献报道[sup][/sup],国际上制备甲钴胺所采用的还原剂为硼氢化钠。硼氢化钠是一种强还原剂,使反应不易控制,它直接把维生素B12分子中的中心离子——三价钴离子还原成一价态,不仅把β位上氰根还原掉,而且也使得α位上的苯并咪唑键断裂,因此在产物中容易生成无咪唑基的钴啉醇酰胺类化合物;又因该反应以铁盐做催化剂,对环境造成污染。通过多年在甲钴胺制备的经验及文献资料[sup][/sup]与还原原理的掌握,选择了两种还原反应催化剂Por-A和Por-B,选取了一种限制试剂QAS。该两种催化剂都可迅速催化硼氢化钠水解,而且都可以经过再生后重复利用,不对环境造成固废污染。因在反应中加入了限制试剂,因此在还原过程中不会把氰钴胺分子中的三价钴还原成一价钴。为此,我们对以上两种催化剂进行了对比试验,试验数据见表2-2,由表2-2数据做出的甲钴胺的转化率随时间的变化曲线见图2-1。[/align][align=center]表2-2 不同催化剂的转化率(%) [/align][align=center][img=,553,115]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141947_02_1626619_3.png[/img] [/align][align=center][img=,592,270]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141948_01_1626619_3.png[/img][/align][align=center] 图2-1 不同还原反应催化剂的转化率[/align][align=center][/align] 由表2-2及图2-1可以看出,催化剂Por-A的催化能力优于催化剂Por-B,因此选择催化剂Por-A作为该工艺的还原反应催化剂,在30±2℃的温度下,其最佳还原时间为20分钟。[b]2.2选择新型甲基化试剂的原因和应用效果[/b] 目前甲钴胺的生产工艺中普遍采用的甲基化试剂是碘甲烷或三甲基碘化亚砜,碘甲烷是一种良好的亲核试剂,但是碘甲烷的沸点只有42℃,挥发性极强,而且毒性也很大,因此这种工艺用料对操作人员的健康与生命极具威胁性。尤其它不溶于水还要用甲醇或者乙醇作溶剂,为此在精制前还通过蒸发的方式除去溶剂,这一过程又会使甲钴胺受热破坏,从而降低收率并使产品质量下降。虽然三甲基碘化亚砜无毒又溶于水,但它甲基化后会生成具有恶臭的硫醇类物质随着尾气逸出到空气中,这又造成了大气污染。为此课题组根据文献[sup][/sup]及多年的生产经验,从反应机理选择了了一种全新的甲基化试剂M-S,该种试剂是一种固体,无毒无味,易溶于水,且甲基化后不产生异味物质。经试验证明其甲基化效果良好,可以使反应转化率达99%以上。[align=center]2-3新型甲基化试剂与三甲基碘化亚砜的对比效果[/align][align=center][img=,554,97]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141949_01_1626619_3.png[/img][/align] 根据表2-3的数据可知新型甲基化试剂M-S在同样条件下能够达到三甲基碘化亚砜的效果,同时达到了尾气对污染的减少。[b]2.3 反应温度、原料浓度及限制试剂加量反应时间对甲钴胺转化率的影响[/b] 在确定催化剂Por-A、限制试剂QAS和甲基化试剂M-S后,我们以原有的工艺条件为基础对其工艺条件进行优化。经分析[sup][/sup]我们认为反应温度、氰钴胺投料浓度及限制试剂的加量将是影响甲钴胺转化率的主要因素。反应温度越高,还原反应及甲基化反应的速度越快。反应温度过高会导致反应过于剧烈,使VB12分子降解,影响产品质量和收率;如果反应温度过低,导致还原及甲基化反应不完全,同样影响产品的质量与收率。在该反应中,还原剂水解速度的限制试剂加量也同样是一个重要参数,因此我们以反应温度、原料浓度及限制试剂C的加量为影响因素,以正交试验法来获得最佳反应条件(以甲钴胺的转化率为目标函数)。试验方案的因素水平见表2-4。[align=center]表2-4 因素水平表[/align][align=center][img=,570,118]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141950_01_1626619_3.png[/img][/align] 按照正交试验方案进行试验,试验结果见表2-5,根据试验结果对数据进行方差分析以确定最佳反应条件,方差分析表见表2-6。[align=center]表2-5 反应温度、原料浓度及甲基化时间的影响[/align][align=center][img=,563,366]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141952_01_1626619_3.png[/img][/align][align=center]表2-6 方差分析表[/align][align=center][img=,589,134]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141952_02_1626619_3.png[/img][/align] 表2-6数据可以看出: F[sub]A[/sub]=57.02, F[sub]B[/sub]=22.50大于F[sub]0.90[/sub](2,2)=9.0,也大于F[sub]0.95[/sub](2,2)=19.0,因此反应温度与甲基化时间两因子在显著性水平0.10与0.05上都是显著的。而F[sub]C[/sub]=2.47小于F[sub]0.9[/sub](2,2)=9.0,故物料浓度对其不显著,可忽略。表2-5、表2-6的计算结果显示: A[sub]3[/sub]水平为最佳温度条件,即40±2℃。B[sub]3[/sub]水平为最佳甲基化反应时间。对于不显著物料浓度项,参考原有氰钴胺的投料浓度,以2%为本研究的投料浓度。正交试验完成后,以选取的工艺条件进行验证,验证数据见表2-7。[align=center]表2-7三批甲钴胺数据[/align][align=center][img=,503,97]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141954_01_1626619_3.png[/img][/align] 从表2-7数据可以看出:以正交实验确定的工艺条件可以实现甲钴胺的高转化率。把该条件作为甲钴胺的合成条件。[b]3质量研究3.1 各国药典标准及产品内控标准[sup][/sup][/b][align=center] 表3-1 国内市场标准(CP)[/align][align=center][img=,648,312]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141954_02_1626619_3.png[/img][/align][align=center]表3-2 日本市场标准(JP)[/align][align=center][img=,623,261]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141957_01_1626619_3.png[/img][/align][align=center]表3-3印度等市场标准(JP)[/align][align=center][img=,616,251]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141957_02_1626619_3.png[/img][/align][align=center]表3-4美国市场标准(USP)[/align][align=center][img=,610,268]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141957_03_1626619_3.png[/img][/align][b]3.2 结构简单确认[/b] 把以本课题研究确定的制备工艺制得的甲钴胺与甲钴胺标准品进行红外光谱确认,以溴化钾压片法制备测试样品,图谱结果见图3-1,图3-2。[align=center]图3-1甲钴胺样品红外图谱[/align][align=center][img=,479,546]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142002_01_1626619_3.png[/img][/align][align=center]图3-2甲钴胺标准品红外图谱[/align][align=center][img=,513,526]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142002_02_1626619_3.png[/img][/align][b] 结论[/b]:甲钴胺样品的红外图谱与甲钴胺标准品的红外图谱基本一致。故从其红外光谱上可以证明以新工艺制备出的产品为甲钴胺。结果表明:(1)新工艺生产的甲钴胺产品的各项质量指标均符合内定的质量指标要求;(2)与工艺开发前的产品对比研究表明,新工艺生产的甲钴胺纯度高,质量明显优于工艺开发前的产品;(3)在已完成的加速稳定性考察过程中,产品重点质量指标均符合各相关药典规定;[b]4结果与讨论[/b] 本工艺研究取得的主要成果与结论简述如下:(1) 提高了还原反应转化率:本课题确定了新型催化剂及还原反应的工艺条件,该研究采用两种不同的还原反应催化剂,经过大量的对比试验,选出了适合甲钴胺合成反应中还原工序适宜的催化剂及相应的工艺条件,有效控制了还原剂的还原速度,使得氰钴胺能够快速生成二价态的B12,减少了副反应的发生。(2) 满足了清洁生产的要求:由于在还原反应阶段使用了新型催化剂,它不仅能够让还原剂水解彻底,减少了副产物的产生,提高了反应转化率,更为重要的是,在提倡可持续发展的今天,由于该催化剂能够重复利用,减少了原料药生产中三废的产生,有效的满足了清洁生产的要求。(3) 提高产品品质,降低三废:本课题选取了新的甲基化试剂,该甲基化试剂具有溶于水、甲基化能力强、不产生异味物质等优点,不仅可以生产出满足内控质量标准的产品,同时对员工身体健康、环境保护做出了贡献。 总之,以本课题研发的生产工艺生产的甲钴胺原料药具有收率高、质量好、成本低、清洁污染少等优点。在满足患者临床用药安全性、提高公司市场竞争力方面具有重大意义。[b] 参考文献[/b]Weiner,J.H.,Bilous,P.T.,Shaw,G.M.,Lubitz,S.P.,Frost,L.,Thomas,G.H.,Cole,J.A.,and Turner,R.J.(1998), Cell 93,93-101.Wikins,P.C.,Dalton,H.,Samuel, C.J., and Green,J.(1994),Eur.J.Biochem.226,555-560. Kaikov,Y.,Wadworth,L.D.,Hall,C.A.,and Rogers, Li, N., Rosenblatt,D.S.,Kamen,B.A.,Settharm,S., and Seetharam,B.(1994),Hum. M olec. GENET.3,1835-1840. Rothenberg, S.P. andQuadros, E.V.(1995), in Megaloblastic anemia(Wick-ramasinghe,S.N., ed.),pp.499-414,Bailliere Tindall, Lodon. Janata, J., Kogekar,N., andFenton,W.A.(1997), Hum.Molec. GENET.6,1457-1464. Mancia, F.,Keep,国家药典委员会.[color=#333333]《[/color]中国药典[color=#333333]》[/color]2015年版,北京,中国科技出版社,2015.

问题:2015中国药典要求甲钴胺峰与羟钴胺峰的分离度是?答案:药典要求甲钴胺峰与羟钴胺峰(相对保留时间约为0. 2)的分离度应大于20。【活动奖励】幸运奖(2钻石币):千层峰(注册ID:jxyan)sixingxing(注册ID:v2889187)ZHAOGUANGXI(注册ID:ZHAOGUANGXI)http://ng1.17img.cn/bbsfiles/images/2015/11/201511201512_574505_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/11/201511201513_574506_1610895_3.jpg积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================甲钴胺样品制备 制备方法含量测定系统适用性溶液:甲钴胺对照品(0.5 mg/mL),水溶解,自然光下放置10 min,即得。对照品溶液:取甲钴胺对照品适量,精密称定,加流动相溶解并定量稀释制成每1 mL中约含50 μg的溶液,即得。分析条件色谱柱Inspire C18 150 x 4.6 mm,5 μm (Cat#:81001)流动相0.03mol/L 磷酸二氢钾溶液(用0.2 mol/L 氢氧化钠溶液或磷酸调节pH 值至4.5):乙腈=84:16流速1.6 mL/min柱温30 ℃检测器UV 342 nm进样量20 μL色谱图含量测定对照品溶液http://ng1.17img.cn/bbsfiles/images/2015/11/201511201000_574453_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数 N USP拖尾因子 分离度 1 12.461 50544 2107 6070.328 0.972 -- 系统适用性溶液 http://ng1.17img.cn/bbsfiles/images/2015/11/201511201001_574454_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度* 1 1.158 880662 152634 712.423 1.086 -- 2 12.197 65167 2812 6186.804 0.975 27.812 *药典要求甲钴胺峰与羟钴胺峰(相对保留时间约为0. 2)的分离度应大于20,甲钴胺峰与相邻杂质峰之间的分离度应符合要求。本品种同时使用了DiamonsilC18、DiamonsilC18(2)两款色谱柱,在药典规定条件下进行检测,均满足药典要求。
求金刚烷胺对照品 批号、纯度、厂商







 留言咨询
留言咨询

 400-860-5168转4379
400-860-5168转4379
 留言咨询
留言咨询

 400-860-5168转5921
400-860-5168转5921
 留言咨询
留言咨询


