推荐厂家
暂无
暂无
研究不同基源及产地桑椹药材的品质差异。方法:建立桑椹药材的HPLC 分析方法,比较不同样品的HPLC 图谱相似度,并进行聚类分析。结果:16 批桑椹样品相似程度不高,不同基源及产地样品的化学成分在组成与数量上存在差异,桑椹药材的品质与产地无明显相关性,杂交桑的桑椹总峰面积大于法定品种的桑椹总峰面积,市购商品药材品质差异大。结论:桑椹药材的品质与原植物种质、药材加工及贮存有较密切的关系。
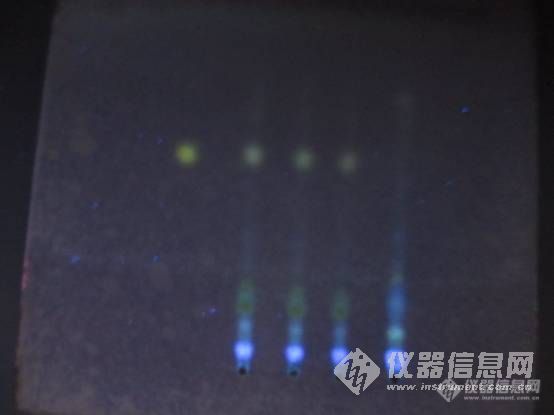
研究中药复方制剂中各味药材的鉴别药典中鉴别乌梅药材,选择“熊果酸”为对照乌梅含有熊果酸,大枣也含有熊果酸,请问那我做制剂中乌梅药材鉴别时,是不是就不能以熊果酸作对照了,因为怕大枣会有干扰?这种情况,乌梅该选择什么组分作为对照?实验结果显示,乌梅阴性并没有干扰,我能以“熊果酸”作为对照鉴别乌梅吗,虽然明知大枣也含熊果酸。乌梅阴性没有干扰,会不会是点样量少的问题?http://ng1.17img.cn/bbsfiles/images/2012/11/201211010017_400582_1872149_3.jpg1. 熊果酸;2-4. 样品;5. 阴性
在薄层色谱定性时,对照品、供试品和对照药材在相同的问题显相同颜色的斑点即可。对照品和对照药材定性有何区别?为什么两个要同时做呢?







 400-860-5168转3905
400-860-5168转3905
 留言咨询
留言咨询

 400-860-5168转2232
400-860-5168转2232
 留言咨询
留言咨询

 留言咨询
留言咨询


