推荐厂家
暂无
暂无
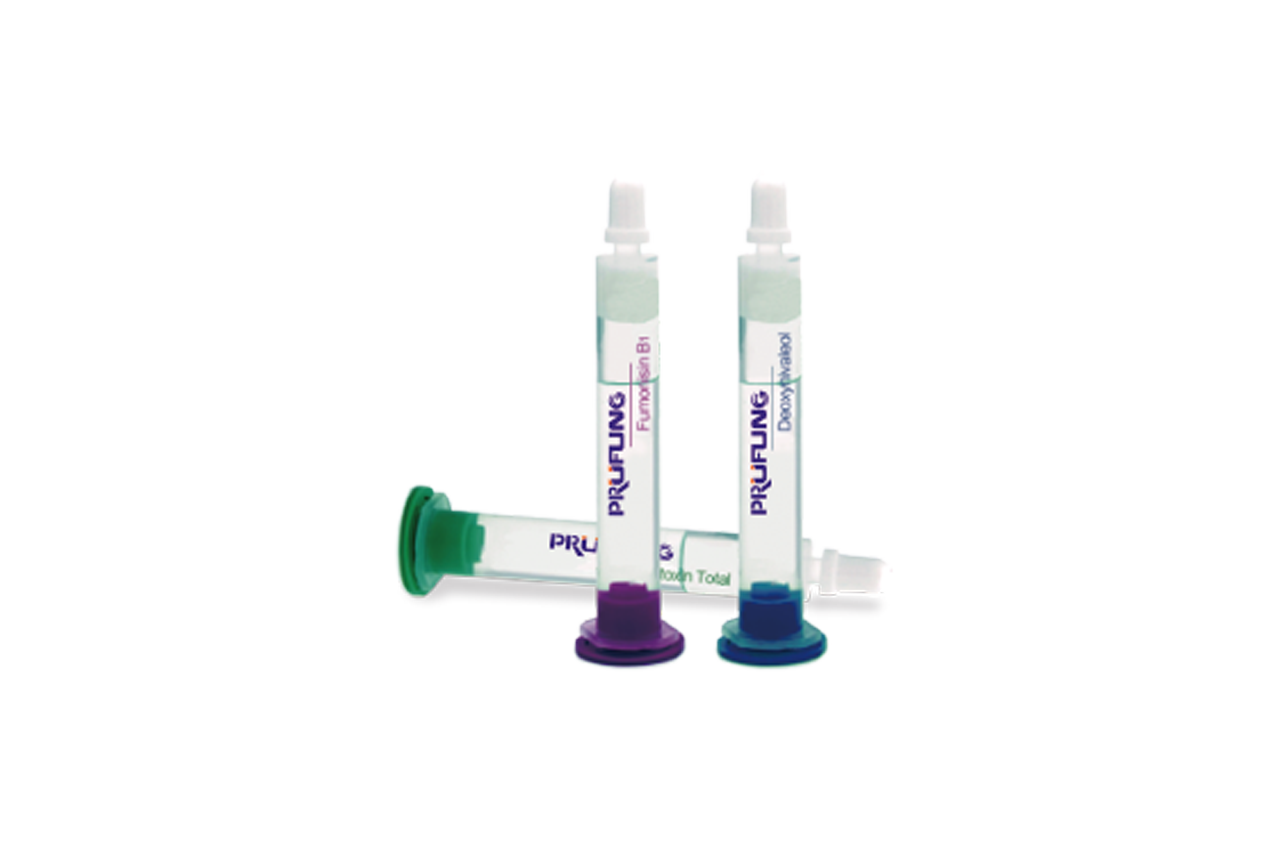
黄曲霉毒素是天然存在的霉菌产生的一种毒素,已经被证明对人体容易产生癌症,是一类致癌物质。美国联邦政府有关法律规定人类消费食品和奶牛饲料中的黄曲霉毒素含量不能超过20ppb,人类消费的牛奶中的含量不能超过0.5ppb。而其它动物饲料中的含量不能超过300ppb。黄曲霉毒素是一类真菌(如黄曲霉和寄生曲霉)的有毒的代谢产物,它们具有很强的致癌性,主要存在于谷物、坚果、棉籽以及一些与人类血液,动物饲料相关的产品中。黄曲霉毒素M1是黄曲霉毒素B1的羟基化代谢产物,也是一种强致癌物质。牛乳及其制品是易受到黄曲霉毒素M1污染的食品之一。黄曲霉毒素 M1的检测方法有高效液相色谱法(HPLC),薄层层析法(TLC),酶联免疫法(ELISA)等。而使用黄曲霉毒素M1 免疫亲和柱则能够快速而准确的提纯纯化并浓缩样品中黄曲霉毒素M1组分,使得后面的分析更加轻松简单。PriboFast黄曲霉毒素总量亲和层析柱可选择性吸附样品液中的黄曲霉毒素(B1,B2,G1,G2),从而对黄曲霉毒素总量(B1,B2,G1,G2)样品起到非常针对性的纯化作用,过柱净化后的样品液可直接用于液相进行黄曲霉毒素总量(B1,B2,G1,G2)含量的检测。亲和层析柱与HPLC配合使用可达到快速测定的目的,以改善信噪比,可提高检测方法的准确度。PriboFast黄曲霉毒素总量亲和柱用于定性、定量检测谷物、副食品、酒类等食品和饲料等样本中的黄曲霉毒素总量(B1,B2,G1,G2)时的样品前处理。柱容量:≥200ng 回收率:80-90%可用于快递纯化检测牛奶,奶粉等样本中的黄曲霉毒素M1。
外毒素与内毒素的主要区别: 区别要点 外毒素 内毒素 来源 革兰阳性菌与部分革兰阴性菌 革兰阴性菌存在部位 由活菌分泌到菌外,少数是细菌崩解后释出 细胞壁组分,菌裂解后释出 化学成分 蛋白质 脂多糖 稳定性 60~80℃,30分钟被破坏160℃,2~4小时才被破坏 外毒素与内毒素的主要区别:区别要点 外毒素 内毒素 来源 革兰阳性菌与部分革兰阴性菌 革兰阴性菌 存在部位 由活菌分泌到菌外,少数是细菌崩解后释出 细胞壁组分,菌裂解后释出 化学成分 蛋白质 脂多糖 稳定性 60~80℃,30分钟被破坏 160℃,2~4小时才被破坏 作用方式 与细胞的特异受体结合 刺激宿主细胞分泌细胞因子、血管活性物质 毒性作用 强,对组织器官有选择性毒害效应,引起特殊临床表现 较弱,各菌的毒性效应大致相同,引起发热、白细胞增多、微循环障碍、休克、DIC等 抗原性 强,刺激机体产生抗毒素;甲醛液处理脱毒形成类毒素 弱,刺激机体产生的中和抗体作用弱;甲醛液处理不形成类毒素
1 神经毒素神经毒素主要包括:鱼腥藻毒素如鱼腥藻毒素-a (Anatoxin-a)、鱼腥藻毒素-a(s) (Anatoxin-a(s))、高类鱼腥藻毒素-a (Homoanatoxin-a);麻痹性或瘫痪性贝毒素(Paralytic Shellfish Poisoning, PSP)如石房蛤毒素(Saxitoxin)、新石房蛤毒素(Neosaxitoxin)和膝沟藻毒素(Gonyautoxin)等;腹泻性贝毒素(Diarrhetic Shellfish Poisoning, DSP)如大田软海绵酸(Okadaic acid, OA)和鳍藻毒素1-3(Dinophysistoxin, DTX)等;记忆丧失性贝毒素(Amnesic Shellfish Poisoning, ASP);神经性贝毒素(Neurotoxic Shellfish Poisoning, NSP)及西加鱼毒素(Ciguatera Fish Poisoning, CFP)( 尹伊伟,2000)。鱼腥藻毒素-a是一种低分子质量的生物碱(图1-2),相对分子质量为165(Hitzfeld B C, 2000-II)。目前发现鱼腥藻、颤藻、束丝藻(Aphanizomenon)、柱孢藻(Cylindrospermum)和微囊藻可以产生鱼腥藻毒素-a。高类鱼腥藻毒素-a (图1-3)是从美丽颤藻(O. formosa)中分离到的一种鱼腥藻毒素-a的同系物,它用丙酰基替代了鱼腥藻毒素-a中C-2上的乙酰基。鱼腥藻毒素-a是神经递质乙酰胆碱的类似物,它可与乙酰胆碱受体结合,但乙酰胆碱酯酶或真核生物中的任何酶均不能降解它。它与乙酰胆碱受体结合后可使肌肉因过度兴奋而痉挛,如果动物的呼吸系统受到影响,动物会因窒息而死亡。鱼腥藻毒素-a(s)是N-羟基鸟嘌呤的单磷酸酯(图1-4),到目前为止仅从北美洲发现,由水华鱼腥藻(A.flos-aquae)和A.Lemmermannii产生。鱼腥藻毒素-a(s)可以阻止乙酰胆碱酯酶对乙酰胆碱的降解,使肌肉因过度兴奋而痉挛(Henriksen P, 1997)。 图1-2 鱼腥藻毒素-a分子结构图Figure 1-2 Structure of anatoxin-a 图1-3 高类鱼腥藻毒素-a分子结构图Figure 1-3 Structure of homoanatoxin-a 图1-4 鱼腥藻毒素-a(s)分子结构图Figure 1-4 Structure of anatoxin-a(s)麻痹性贝毒素是一类烷基氢化嘌呤化合物,形似三环化合物,是一种非蛋白质毒素。分子结构如图1-5所示。类似于具有两个胍基(guanidyl)的嘌呤核,为非结晶、水溶性、高极性、不挥发的小分子物质,在酸性条件下稳定,碱性条件下发生氧化,毒性消失;毒素遇热稳定,并不被人的消化酶所破坏。其中毒性最强的为STX、neoSTX、GTX1、GTX3和dcSTX(1300Mu• μmol-1),但其他几种毒素很容易水解成毒性成份。其来源生物均为甲藻,如有毒膝沟藻(Gonyaulax)、亚历山大藻(Alexandrum)和Pyrodinium等。麻痹性贝毒的强度是通过转换成STX的毒性来表达的。这些毒素主要是由海洋中的赤潮藻甲藻产生的,可在贝类中累积进而危害人类。由于这些毒素最早是从摄食有毒藻类的贝类体内发现,故被称作贝毒。在淡水中PSP主要存在于水华束丝藻(Aph. flos-aquae)、卷曲鱼腥藻(A.circinalis)、Lyngbyawollei和C. raciborskii中(Bialojan C, 1988)。麻痹性贝毒素也是到目前为止赤潮藻毒素中分布最广、危害最大的一类,主要包括石房蛤毒素及其四氢呋喃衍生物,发现的有近三十种(表1-1),由分子结构中R4基团的不同,可分为四类:氨基甲酸酯类、N-磺酰氨甲酰基类、脱氨甲酰基类和脱氧脱氨甲酰基类。其中石房蛤毒素(STX)已被收入《化学武器公约》中禁止化学品的第二类清单。我国也将PSP毒素列为贝类产品的常规检测指标之一。 图1-5 麻痹性贝毒素分子结构图Figure 1-5 Structures of Paralytic Shellfish Poisons (PSPs)麻痹性贝毒是一类神经肌肉麻痹剂,可以作用于细胞膜上的钠通道使之关闭,抑制动作电位的产生,使乙酰胆碱不能释放,从而导致神经麻痹。其毒理作用为阻断细胞钠离子通道,造成神经系统传输障碍而产生麻痹作用。对人体的中毒量为600~5000Mu,致死量为3000~30000Mu,目前尚无对症解毒剂。PSP的毒性为LD50=3.4×10-9。联合国卫生组织规定,100g贝类可食部分的PSP毒力超过80ug(400Mu)时不得食用(丘建文,1991)。海洋生物中,由于贝类对麻痹性贝毒具有极强的抵抗性,因此这种毒素就在贝类体内储存积累,人类或动物食用这些有毒贝类会产生一系列神经麻痹症状,严重的可能致命。由于其对人类健康造成危害,因此成为赤潮毒素中最受关注的一种,许多国家已在贝类生产、贸易过程中,对此毒素制订了严格的监测和管理条例。与贝类相比,鱼类对这种毒素却极为敏感。腹腔注射时,其对鱼类的半致死剂量(LD50)为(4~12)×10-6,口服为(100~750)×10-6,给药后5~15min,鱼类即失去平衡,0~60min就出现死亡。因此,在此类赤潮发生时,常出现鱼类大量死亡现象,欧洲的北海及北美的东北海岸都曾发生因麻痹性贝毒中毒的大规模死鱼事件,死亡的鱼类有玉筋鱼和鲱鱼等。值得注意的是,本来源于藻类的贝毒,许多是通过浮游动物的摄食而传递给鱼类,从而引起鱼类的死亡。因此,麻痹性贝毒对鱼类的危害,既可通过藻细胞本身的胞外分泌物也可通过摄食染毒的其他动物使鱼类中毒。不过由于麻痹性贝毒对鱼类的毒性很高,毒素不会在鱼体内大量残留,中毒死亡鱼体肌肉内的残留毒素含量很低。我国虽未有因麻痹性贝毒中毒而引起鱼类死亡的报道,但已有产生这类毒素的藻类赤潮发生,而且能产生麻痹性贝毒的藻类在我国海域普遍存在,因此,应高度警惕这类赤潮的发生(尹伊伟,王朝晖等,2000)。2 脂多糖内毒素脂多糖内毒素是蓝藻细胞壁的组成部分,由脂A、核心寡糖和O特异多糖组成,其中脂A分子结构式如图1-6所示。目前已从裂须藻(Schizothrix calcicola),颤藻,鱼腥藻,微囊藻和Anacystis中分离到。蓝藻脂多糖内毒素的脂A与格兰氏阴性细菌的脂多糖不完全相同,种类更多,而且往往含有少量的磷酸。脂多糖内毒素包括细胞毒性生物碱(Alkaloid)、皮肤毒性生物碱和刺激性毒物——脂多糖(Lipopolysaccharides, LPS) (Metcalf J S, 2004)。






 400-860-5168转6091
400-860-5168转6091
 留言咨询
留言咨询
 留言咨询
留言咨询
 400-860-5168转5075
400-860-5168转5075
 留言咨询
留言咨询