推荐厂家
暂无
暂无





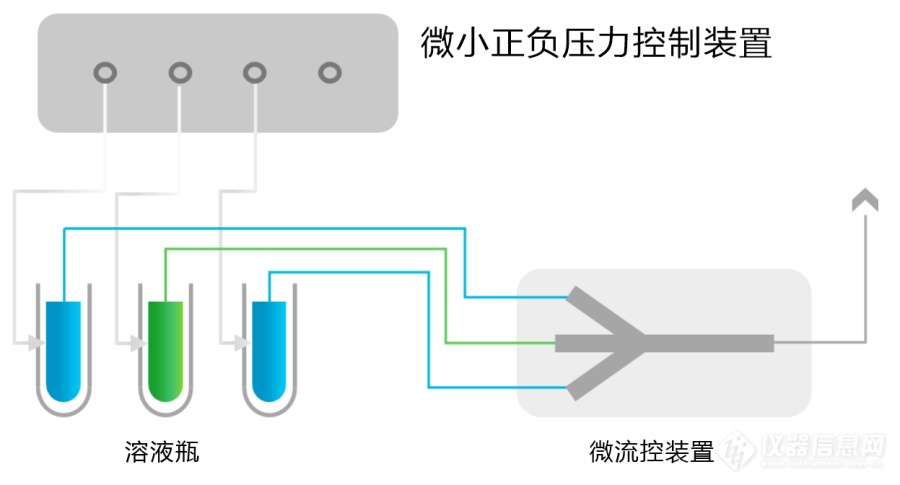
[align=center][img=压力驱动分选进样系统,690,371]https://ng1.17img.cn/bbsfiles/images/2022/06/202206231002395286_2664_3384_3.png!w690x371.jpg[/img][/align][color=#000099]摘要:在循环肿瘤细胞等细胞分选进样系统中,需要在一个标准大气压附近很小的正负压范围对压力进行精密控制,这就对控制方法、气体流量调节阀、压力传感器和控制器提出了更高的要求。本文将针对这些技术问题,提出高精度正负压精密控制解决方案,并详细介绍控制方法和其中软硬件的功能和技术指标,由此可实现0.5%的控制精度。[/color][align=center]~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~[/align][size=18px][color=#000099]一、问题的提出[/color][/size]循环肿瘤细胞(Circulating Tumor Cells,CTC)分选已被认为是癌症诊断和预后的有效工具,要求相应的检测装置能够执行所有实验过程而无需任何人工干预的自动、快速且灵敏。对于一些基于压力驱动液体流动原理的进样系统,要求通过精确控制气体的压力, 确保进样过程中流量稳定并实现自动反馈调节,并需要气压供应装置提供正压和负压以使检测装置中的泵及阀门动作。但在目前的CTC检测装置进样系统中,气压的精密控制还存在以下几方面的问题需要解决:(1)现有的气压供应装置无法提供微小的气压,常会导致泵的薄膜破损而无法使用,且现有的气压供应装置亦无法提供常压,使泵的薄膜在检测过程中无法回到平坦状态,造成细胞破损,故需要有可以提供微气压及常压至检测装置的气压供应装置。为了解决此问题,给微流道芯片提供正压、负压或常压,专利CN 216499436U“气压供应装置”中提出了一种非常复杂的概念性解决方案,标称正压气体的压力大小调节至 1~6psi,负压气体的压力大小调节至?1~6psi,正负压微调节阀可以精密至±0 .01psi。但这些指标恰恰是微压力调节阀的关键,如果没有能达到这种技术指标的调节阀,所述方案根本无法实现。(2)上海理工大学王固兵等人在2020年发表的“基于气压驱动的循环肿瘤细胞分选进样系统的设计与实现“一文中,提出了一种采用德国tecno PS120000 比例电磁阀的技术方案。但这种工业用比例阀主要是用于高压气体的压力控制,口径也较大,控制精度显然不能满足微小正负压的精密控制,而且无法外接高精度压力传感器来提升控制精度,根本无法实现文中提出的达到压力输出精度为1mbar(0.015psi)的指标,相对于1bar大气压这相当于达到0.1%的控制精度,这个指标显然不切合实际。从上述报道可以看出,细胞分选进样系统的压力控制需要在一个标准大气压附近很小的正负压范围对真空压力进行精密控制,这就对控制方法、气体流量调节阀、压力传感器和控制器提出了更高的要求。本文将针对这些技术问题,提出高精度正负压精密控制解决方案,并详细介绍控制方法和其中软硬件的功能和技术指标,由此可实现0.5%的控制精度。[size=18px][color=#000099]二、解决方案[/color][/size]本文所提出的解决方案是实现在一个标准大气压附近±10psi(或±700mbar)范围内的正负压精密控制,控制精度达到0.5%。即提供一个可控气压源解决方案,采用双向控制模式的动态平衡法,结合高精度步进电机和微小流量电动针阀、高精度压力传感器和双通道PID控制器,气压源可进行高精度的正压、负压和一个大气压的可编程输出。微小正负压精密控制的基本原理如图1所示,具体内容为:[align=center][img=气压驱动分选进样系统,690,377]https://ng1.17img.cn/bbsfiles/images/2022/06/202206231005336655_4666_3384_3.png!w690x377.jpg[/img][/align][align=center]图1 微小正负压精密控制原理框图[/align](1)控制原理基于密闭空腔进气和出气的动态平衡法。这是一个典型闭环控制回路,2通道PID控制器采集真空压力传感器信号并与设定值进行比较,然后调节进气和抽气调节阀的开度,最终使传感器测量值与设定值相等而实现真空压力的准确控制。(2)控制回路分别配备了抽气泵(负压源)和气源(正压源),以提供足够的负压和正压能力。(3)为了覆盖负压到正压的所要求的真空压力范围(如-10psi至+10psi),配置一个测试量程覆盖要求范围内的高精度绝对压力传感器,绝对压力传感器对应上述真空压力范围输出数值从小到大的直流模拟信号(如0~10VDC)。此模拟信号输入给PID控制器,由PID控制器调节进气阀和排气阀的开度而实现压力精确控制。采用绝对压力传感器的优势是不受当地大气气压变化的影响,无需采取气压修正,更能保证测试的准确性和重复性。(4)当控制是从负压到正压进行变化时,一开始的进气调节阀开度(进气流量)要远小于抽气调节阀开度(抽气流量),通过自动调节进出气流量达到不同的平衡状态来实现不同的负压控制,最终进气调节阀开度逐渐要远大于抽气调节阀开度,由此实现负压到正压范围内一系列设定点或斜线的连续精密控制。对于从正压到负压压的变化控制,上述过程正好相反。[size=18px][color=#000099]三、方案具体内容[/color][/size]解决方案中所涉及的微小正负压力发生器的具体结构如图2所示,主要包括高压气源、电动针阀、密闭空腔、压力传感器、高精度PID控制器和抽气泵。[align=center][img=气压驱动分选进样系统,690,465]https://ng1.17img.cn/bbsfiles/images/2022/06/202206231006045409_5247_3384_3.png!w690x465.jpg[/img][/align][align=center]图2 微小正负压精密控制的压力发生器结构示意图[/align]在图2所示的微小正负压控制系统中,密闭空腔上的工作压力出口连接检测仪器,密闭空腔左右安装两个NCNV系列的步进电机电动针阀,此电动针阀本身就是正负压两用调节阀,其绝对真空压力范围为0.0001mbar~7bar,最大流量为40mL/min,步进电机单步长为12.7微米,完全能满足小空腔的正负压精密控制。在图2所示的控制系统中使用了两个电动针阀来实现正负压任意设定点的精确控制,也可以从正压到负压的压力线性变化控制,也可以从负压到正压的压力线性变化控制。对于循环肿瘤细胞(CTCs)检测仪器进样系统中的微小正负压控制,要求是在标准大气压附近的真空压力精确控制,如控制精度为±0.5%甚至更小,一般都需要采用调节抽气阀的双向动态模式,即通过双通道PID控制器,一个通道用来恒定进气口处电动针阀的开度基本不变,另一个通道根据PID算法来调节排气口处的电动针阀开度。除了上述恒定进气流量调节抽气流量的控制方法之外,循环肿瘤细胞(CTCs)检测仪器进样系统中的微小正负压的控制精度,主要由压力传感器、PID控制器和电动针阀的精度决定。本方案中的PID控制器采用的是24位AD和16位的DA,电动针阀则是高精度步进电机,因此本解决方案的测试精度主要取决于压力传感器精度,一般至少要选择0.1%精度的压力传感器。对于进样系统中的微小压力控制,往往会要求密闭容器在正负压范围内进行多次往复变化,因此采用了可存储多个编辑程序的PID控制器,设定程度是一条多个折线段构成的曲线,由此可实现正负压往复变化的自动程序控制。在本文所述的解决方案中,为实现正负压的精密控制,如图2所示,针对负压的形成配置了抽气泵。抽气泵相当于一个负压源,但采用真空发生器同样可以达到负压源的效果,负压源采用真空发生器的优点是整个系统只需配备一个高压气源,减少了整个系统的造价、体积和重量,真空发生器连接高压气源即可达到相同的抽气效果。[size=18px][color=#000099]四、总结[/color][/size]本文所述解决方案,完全可以实现循环肿瘤细胞(CTCs)检测仪器进样系统中微小正负压的任意设定点和连续程序形式的精密控制,并且可以达到很高的控制精度和速度,全程自动化。本方案除了微小正负压的自动精密控制之外,另外一个特点是系统简单,正负压控制范围也可以比较宽泛,整个系统小巧和集成化,便于形成小型化的检测仪器。本文解决方案的技术成熟度很高,方案中所涉及的电动针阀和PID控制器,都是目前上海依阳实业有限公司特有的标准产品,其他的压力传感器、抽气泵、真空发生器和高压气源等也是目前市场上常见的标准产品。本文所述解决方案,同样可以适用于各种其他基于气压驱动的微流控进样系统。[align=center]~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~[/align]
各国争相发展的重点项目 iPS技术,即诱导性多能干细胞技术,是一种将成体成熟、分化的体细胞重编程获得类似胚胎干细胞的新兴技术。2007年11月美国和日本科学家分别独立宣布可将人类皮肤细胞转化为iPS细胞。这一发现被《自然》和《科学》杂志分别评为2007年第一和第二大科学进展。之后,iPS细胞研究迅猛发展,不同的国家和实验室纷纷报道了多种方法建立的iPS细胞系。就连世界第一只体细胞克隆动物多利羊的培育者伊恩·威尔莫特也宣布放弃人类胚胎干细胞克隆研究,转而进行 iPS 细胞研究,因为他认为这种细胞比胚胎干细胞更具潜在优势。 我国连续多年将干细胞研究列入“863”、“973”、国家自然基金重点项目。国务院2006年发布的《国家中长期科学和技术发展规划纲要(2006-2020年)》中,干细胞作为五项生物技术之一成为未来15年我国前沿技术的重点研究领域。 致瘤风险浮出水面 Yamanaka研究组在《自然·生物技术》上发表的文章显示,用iPS细胞诱导的神经干细胞,即使不含c-Myc(曾被认为是导致肿瘤的主要原因),在植入NOD/SCID免疫缺陷小鼠后仍有很强的致瘤性,甚至高于胚胎干细胞。 他们共研究了36个iPS细胞克隆,在诱导方式上,有些诱导剂配方中含有c-Myc基因,有些没有,因此具有较好的代表性。同时他们选择了3株胚胎干细胞作为对照。在45周的观察中,移植胚胎干细胞来源神经干细胞的34只小鼠有4只长出肿瘤。在100只移植胚胎成纤维细胞来源的iPS神经干细胞小鼠中34只发现肿瘤,概率和胚胎干细胞相当。在55只移植成人成纤维细胞来源的iPS神经干细胞小鼠中46只发现肿瘤,概率远高于胚胎干细胞。在36只移植肝细胞来源的iPS神经干细胞小鼠中10只发现肿瘤,概率高于胚胎干细胞。8只移植胃上皮细胞来源的iPS神经干细胞小鼠中未发现肿瘤。病理学检查证实肿瘤均为畸胎瘤,部分为恶性畸胎瘤。 研究还发现,以前认为致瘤性很强的c-Myc在去掉后并没有减少iPS神经干细胞的致瘤性,相反以前认为没有致瘤性的Nanog基因却可以明显增强iPS神经干细胞的致瘤性。 这次试验的另一个意外结果是并未发现在生成的肿瘤细胞中有c-Myc或其他基因的激活。以前的观点认为,转入的癌基因是iPS致瘤性的基础,只要在iPS细胞诱导成功后通过各种方法去除已完成使命的癌基因即可使iPS细胞免于致瘤性。这次试验的结果无疑给这些想法留下了阴影,而且使iPS致瘤的机制更加扑朔迷离。
http://www.bioon.com/biology/UploadFiles/201208/2012080216013081.jpg癌症研究人员可以测定肿瘤细胞基因组的序列,扫描其异常的基因活性,剖析其突变的蛋白质和研究它们在实验室培养皿中的生长,但研究者一直无法跟踪细胞形成肿瘤的过程。现在三个独立研究小组在小鼠体内做到了这一点。他们的研究结果支持这样的观点:一小部分细胞驱动肿瘤的生长,而想要治愈癌症可能需要将这些所谓肿瘤干细胞清除。目前还无法确认,这些从脑瘤,肠癌和皮肤癌研究的结论是否适用于其他类型肿瘤,但是得克萨斯大学西南医学中心的路易斯·帕拉达认为,如果它们适用于其他肿瘤,"将深刻地改变目前的化疗疗效评价和临床疗法的制定标准"。 不仅是看某种疗法是否缩小肿瘤,研究人员将更关注是否杀死了正确的细胞。帕拉达和他的同事们想检测是否特异性标识健康成人神经干细胞的一个遗传标记,也可标识神经母细胞瘤中的癌症干细胞。他们发现,所有神经母细胞瘤样本中至少有几个标记细胞 - 大概是干细胞。未标记细胞可被标准化疗杀死,但肿瘤可迅速恢复。进一步的实验表明,未标记细胞起源于标记的细胞祖先。当研究者把化疗与抑制标记细胞的遗传手段相结合进行治疗时,帕拉达说,肿瘤显著缩小到"残留遗迹"的水平。在另一项研究中,荷兰乌得勒支Hubrecht研究所的干细胞生物学家们把注意力瞄着了肠道。利用药物驱动的荧光素标志物表达系统,他们在小鼠体内证实,多种不同类型的肿瘤细胞,其实是来源于同一干细胞的。而且,这些干细胞是肿瘤发展的驱动力。对皮肤癌的研究,Blanpain和他的小组标记单个肿瘤细胞,而不是特异地标记干细胞。他们发现,细胞表现出两种不同的分工模式:它们要么在慢慢耗尽前分裂出少数细胞,或者产生许多细胞。这再次证实,一类独特的细胞亚群是肿瘤生长的驱动力。研究者说,下一步的研究计划将是,搞清楚这些实验所跟踪的细胞如何与通过多年移植实验所确定的,假定的癌症干细胞相联系的。研究人员已经紧锣密鼓地在寻找杀死这些细胞的方法;现在他们有更多的工具来测试这样的策略是否会奏效。

 400-805-0826
400-805-0826
 留言咨询
留言咨询

 400-860-5168转2623
400-860-5168转2623
 留言咨询
留言咨询

 留言咨询
留言咨询