推荐厂家
暂无
暂无
 留言咨询
留言咨询
 留言咨询
留言咨询
 留言咨询
留言咨询

 400-860-5168转4646
400-860-5168转4646
 留言咨询
留言咨询

 留言咨询
留言咨询

 留言咨询
留言咨询
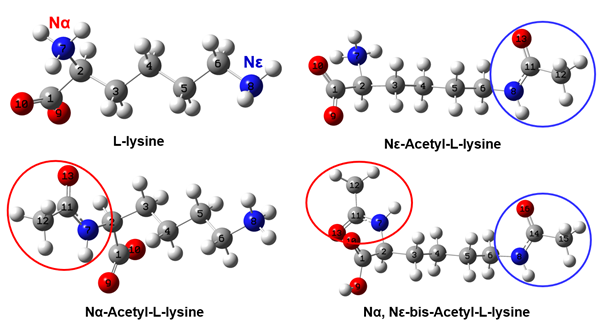



组蛋白乙酰化组蛋白修饰通过改变组蛋白与DNA的亲和性使染色质结构发生改变,进而影响转录因子与DNA序列的结合和基因表达,包括乙酰化、甲基化、磷酸化等,其中乙酰化是最重要的修饰方式之一,其主要发生在组蛋白H3赖氨酸(Lysine, Lys)的位点上,在癌症进展中发挥双重作用,既参与肿瘤抑制基因的沉默,又增强癌基因的表达[11],它受组蛋白乙酰转移酶(Histone acetyl transferase,HAT)和组蛋白去乙酰化酶(Histone deacetylase,HDAC)调控。HDAC可移去Lys残基上的乙酰基,增强组蛋白的正电性,DNA(本身带有负电荷)与组蛋白结合紧密,转录因子不易于DNA结合,抑制抑癌基因的转录,HAT作用则相反,二者动态平衡才能使组蛋白乙酰化维持在正常水平。表观遗传学改变通过调控基因转录平衡组蛋白乙酰化和去乙酰化,从而影响细胞周期、凋亡和分化相关蛋白的表达水平[12]。2.1 组蛋白乙酰化水平与SCLC发生发展密切相关 一项实验研究表明,乙酰化组蛋白H3在SCLC和NSCLC细胞中的表达有显著性差异,以前者表达较高。Notch信号通路是SCLC发生发展和化疗耐药的主要调节通路之一[13],具有肿瘤抑制作用。此研究中,Notch1在SCLC细胞系(除H69AR、SBC-3)中失活,其表达水平与组蛋白H3乙酰化有关。Notch1阳性表达的细胞系中乙酰化组蛋白H3富集在Notch1启动子区域,表达水平较高,Notch1阴性表达的细胞系中Notch1启动子周围的乙酰化组蛋白H3水平较低。这说明组蛋白去乙酰化是Notch1基因在SCLC中表观失活的原因[14]915-918。此外,组蛋白H3赖氨酸23(histone 3 lysine 23, H3K23)乙酰转移酶KAT6B在SCLC中失活,若其活性恢复可对SCLC产生抑制作用,它的乙酰化水平降低是SCLC发生的重要标志[15]。由此可见,组蛋白去乙酰化可以调控相关基因的表达从而促进SCLC发生发展。2.2 组蛋白去乙酰化酶抑制剂 HDAC在许多癌症中过表达,干扰其活性、抑制其功能是有效的治疗手段。组蛋白去乙酰化酶抑制剂(Histone deacetylase inhibitor, HDACI)是重要的表观调控药物,高效低毒,通过靶向阻断HDAC去乙酰化、促进组蛋白乙酰化发挥抗肿瘤作用。根据化学结构的不同,HDACIs分为异羟肟酸(异羟肟酸酯)、短链脂肪(脂肪族)酸、环状四肽、苯甲酰胺和Sirt抑制剂5类[16]。在单药和/或与传统化疗药物联合使用时,HDACI可阻滞细胞周期,抑制迁移和侵袭[17],诱导癌细胞分化、自噬[18]、凋亡,抗血管生成。当前,伏立诺他(Vorinostat ,SAHA)、罗米地辛(Romidepsin)、帕比司他(Panobinostat)等被批准用于血液系统恶性肿瘤的治疗[19]。丙戊酸(valproic acid ,VPA)作为HDACI可抑制SCLC细胞生长,诱导细胞凋亡,阻滞SCLC细胞周期于G1期。以上抑制作用是通过降低HDAC4表达,增加组蛋白H4乙酰化实现的。同时发现,VPA激活了SCLC中Notch1、Notch靶基因HES1和P21的Notch信号通路。此外,它还可以上调生长抑素受体II(somatostatinreceptor2,SSTR2)并增强受体靶向细胞毒素的抑制作用[20]。在经曲古抑菌素A (Trichostatin A ,TSA)处理后的SCLC细胞系中, Notch1启动子区域H3乙酰化水平增加,从而导致Notch1蛋白表达。此外,经TSA处理后,SCLC细胞黏附增加,上皮间质转化标志物表达减少,细胞增殖减少,细胞凋亡激活,可能与TSA诱导Notch1表达有关[14]916-918。这些研究成果为HDACI在 SCLC治疗中的应用提供了依据。为了达到最好治疗效果,药物用量、联合用药及使用顺序仍需深入研究。
[size=20px] [/size][size=20px]组蛋白乙酰化[/size][size=16px]组蛋白修饰通过改变组蛋白与[/size][size=16px]DNA[/size][size=16px]的亲和性使染色质结构发生改变,进而影响转录因子与[/size][size=16px]DNA[/size][size=16px]序列的结合和基因表达[/size][size=16px],[/size][size=16px]包括乙酰化、甲基化、磷酸化等,其中乙酰化是最重要的修饰方式之一,其主要发生在组蛋白[/size][size=16px]H3[/size][size=16px]赖氨酸([/size][size=16px]Lysine, Lys[/size][size=16px])的位点上,在癌症进展中发挥双重作用,既参与肿瘤抑制基因的沉默,又增强癌基因的表达[/size][font='times new roman'][size=16px][11][/size][/font][size=16px],它受组蛋白乙酰转移酶([/size][size=16px]Histone acetyl transferase[/size][size=16px],[/size][size=16px]HAT[/size][size=16px])和组蛋白去乙酰化酶[/size][size=16px](Histone deacetylase[/size][size=16px],[/size][size=16px]HDAC)[/size][size=16px]调控。[/size][size=16px]HDAC[/size][size=16px]可移去[/size][size=16px]Lys[/size][size=16px]残基上的乙酰基,增强组蛋白的正电性,[/size][size=16px]DNA[/size][size=16px](本身带有负电荷)与组蛋白结合紧密,转录因子不易于[/size][size=16px]DNA[/size][size=16px]结合,抑制抑癌基因的转录,[/size][size=16px]HAT[/size][size=16px]作用则相反,二者动态平衡才能使组蛋白乙酰化维持在正常水平。表观遗传学改变通过调控基因转录平衡组蛋白乙酰化和去乙酰化,从而影响细胞周期、凋亡和分化相关蛋白的表达水平[/size][font='times new roman'][size=16px][12][/size][/font][size=16px]。[/size][size=20px]1[/size][size=20px] [/size][size=20px]组蛋白乙酰化水平与[/size][size=20px]SCLC[/size][size=20px]发生发展密切相关[/size][font='黑体'][size=14px] [/size][/font][font='黑体'][size=14px] [/size][/font][size=14px] [/size][size=16px]一项实验研究表明,乙酰化组蛋白[/size][size=16px]H3[/size][size=16px]在[/size][size=16px]SCLC[/size][size=16px]和[/size][size=16px]NSCLC[/size][size=16px]细胞中的表达有显著性差异,以前者表达较高。[/size][size=16px]Notch[/size][size=16px]信号通路是[/size][size=16px]SCLC[/size][size=16px]发生发展和化疗耐药的主要调节通路之一[/size][font='times new roman'][size=16px][13][/size][/font][size=16px],具有肿瘤抑制作用。此研究中,[/size][size=16px]Notch1[/size][size=16px]在[/size][size=16px]SCLC[/size][size=16px]细胞系(除[/size][size=16px]H69AR[/size][size=16px]、[/size][size=16px]SBC-3[/size][size=16px])中失活,其表达水平与组蛋白[/size][size=16px]H3[/size][size=16px]乙酰化有关。[/size][size=16px]Notch1[/size][size=16px]阳性表达的细胞系中乙酰化组蛋白[/size][size=16px]H3[/size][size=16px]富集在[/size][size=16px]Notch1[/size][size=16px]启动子区域,表达水平较高,[/size][size=16px]Notch1[/size][size=16px]阴性表达的细胞系中[/size][size=16px]Notch1[/size][size=16px]启动子周围的乙酰化组蛋白[/size][size=16px]H3[/size][size=16px]水平较低。这说明组蛋白去乙酰化是[/size][size=16px]Notch1[/size][size=16px]基因在[/size][size=16px]SCLC[/size][size=16px]中表观失活的原因[/size][font='times new roman'][size=16px][14]915-918[/size][/font][size=16px]。此外,组蛋白[/size][size=16px]H3[/size][size=16px]赖氨酸[/size][size=16px]23(histone 3 lysine 23, H3K23)[/size][size=16px]乙酰转移酶[/size][size=16px]KAT6B[/size][size=16px]在[/size][size=16px]SCLC[/size][size=16px]中失活,若其活性恢复可对[/size][size=16px]SCLC[/size][size=16px]产生抑制作用,它的乙酰化水平降低是[/size][size=16px]SCLC[/size][size=16px]发生的重要标志[/size][font='times new roman'][size=16px][15][/size][/font][size=16px]。由此可见,组蛋白去乙酰化可以调控相关基因的表达从而促进[/size][size=16px]SCLC[/size][size=16px]发生发展。[/size][size=20px]2 [/size][size=20px]组蛋白去乙酰化酶抑制剂[/size][font='黑体'][size=14px] [/size][/font][font='黑体'][size=14px] [/size][/font][size=16px]HDAC[/size][size=16px]在许多癌症中过表达,干扰其活性、抑制其功能是有效的治疗手段。组蛋白去乙酰化酶抑制剂([/size][size=16px]Histone deacetylase inhibitor, HDACI[/size][size=16px])是重要的表观调控药物,高效低毒,通过靶向阻断[/size][size=16px]HDAC[/size][size=16px]去乙酰化、促进组蛋白乙[/size][size=16px]酰化发挥抗肿瘤作用。根据化学结构的不同,[/size][size=16px]HDACIs[/size][size=16px]分为异羟肟酸(异羟肟酸酯)、短链脂肪(脂肪族)酸、环状四肽、苯甲酰胺和[/size][size=16px]Sirt[/size][size=16px]抑制剂[/size][size=16px]5[/size][size=16px]类[/size][font='times new roman'][size=16px][16][/size][/font][size=16px]。在单药和[/size][size=16px]/[/size][size=16px]或与传统化疗药物联合使用时,[/size][size=16px]HDACI[/size][size=16px]可阻滞细胞周期,抑制迁移和侵袭[/size][font='times new roman'][size=16px][17][/size][/font][size=16px],诱导癌细胞分化、自噬[/size][font='times new roman'][size=16px][18][/size][/font][size=16px]、凋亡,抗血管生成。当前,伏立诺他([/size][size=16px]Vorinostat ,SAHA[/size][size=16px])、罗米地辛([/size][size=16px]Romidepsin[/size][size=16px])、帕比司他([/size][size=16px]Panobinostat[/size][size=16px])等被批准用于血液系统恶性肿瘤的治疗[/size][font='times new roman'][size=16px][19][/size][/font][size=16px]。[/size][size=16px]丙戊酸[/size][size=16px](valproic acid ,VPA)[/size][size=16px]作为[/size][size=16px]HDACI[/size][size=16px]可抑制[/size][size=16px]SCLC[/size][size=16px]细胞生长,诱导细胞凋亡,阻滞[/size][size=16px]SCLC[/size][size=16px]细胞周期于[/size][size=16px]G1[/size][size=16px]期。以上抑制作用是通过降低[/size][size=16px]HDAC4[/size][size=16px]表达,增加组蛋白[/size][size=16px]H4[/size][size=16px]乙酰化实现的。同时发现,[/size][size=16px]VPA[/size][size=16px]激活了[/size][size=16px]SCLC[/size][size=16px]中[/size][size=16px]Notch1[/size][size=16px]、[/size][size=16px]Notch[/size][size=16px]靶基因[/size][size=16px]HES1[/size][size=16px]和[/size][size=16px]P21[/size][size=16px]的[/size][size=16px]Notch[/size][size=16px]信号通路。此外,它还可以上调生长抑素受体[/size][size=16px]II[/size][size=16px]([/size][size=16px]somatostatinreceptor2[/size][size=16px],[/size][size=16px]SSTR2[/size][size=16px])并增强受体靶向细胞毒素的抑制作用[/size][font='times new roman'][size=16px][20][/size][/font][size=16px]。在经曲古抑菌素[/size][size=16px]A (Trichostatin A ,TSA)[/size][size=16px]处理后的[/size][size=16px]SCLC[/size][size=16px]细胞系中,[/size][size=16px] Notch1[/size][size=16px]启动子区域[/size][size=16px]H3[/size][size=16px]乙酰化水平增加,从而导致[/size][size=16px]Notch1[/size][size=16px]蛋白表达。此外,经[/size][size=16px]TSA[/size][size=16px]处理后,[/size][size=16px]SCLC[/size][size=16px]细胞黏附增加,上皮间质转化标志物表达减少,细胞增殖减少,细胞凋亡激活,可能与[/size][size=16px]TSA[/size][size=16px]诱导[/size][size=16px]Notch1[/size][size=16px]表达有关[/size][font='times new roman'][size=16px][14]916-918[/size][/font][size=16px]。这些研究成果为[/size][size=16px]HDACI[/size][size=16px]在[/size][size=16px] SCLC[/size][size=16px]治疗中的应用提供了依据。为了达到最好治疗效果,药物用量、联合用药及使用顺序仍需深入研究。[/size]
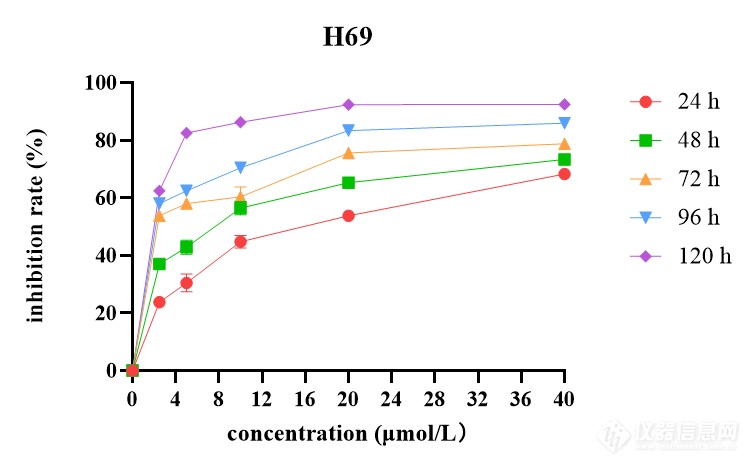
[align=left][size=18px]西达本胺促进[/size][size=18px]S[/size][size=18px]CLC[/size][size=18px]细胞系组蛋白乙酰化[/size][/align][align=left][size=18px] [/size][size=18px] [/size][size=16px]为验证西达本胺是否上调[/size][size=16px]SCLC[/size][size=16px]细胞系的乙酰化水平,我们使用[/size][size=16px]Western blot[/size][size=16px]检测了不同浓度([/size][size=16px]I[/size][size=16px]C10[/size][size=16px]、[/size][size=16px]IC20[/size][size=16px]、[/size][size=16px]IC50[/size][size=16px])西达本胺处理[/size][size=16px]4[/size][size=16px]8[/size][size=16px] [/size][size=16px]h[/size][size=16px]后,[/size][size=16px]S[/size][size=16px]CLC[/size][size=16px]细胞系中乙酰化组蛋白[/size][size=16px]H[/size][size=16px]3[/size][size=16px]、[/size][size=16px]H[/size][size=16px]4[/size][size=16px]表达水平,并以组蛋白[/size][size=16px]H[/size][size=16px]3[/size][size=16px]、[/size][size=16px]H[/size][size=16px]4[/size][size=16px]表达水平为对照。结果如图所示。在四种亚型细胞系中,总组蛋白[/size][size=16px]H[/size][size=16px]3[/size][size=16px]、[/size][size=16px]H[/size][size=16px]4[/size][size=16px]表达水平无变化,乙酰化组蛋白[/size][size=16px]H[/size][size=16px]3[/size][size=16px]、[/size][size=16px]H[/size][size=16px]4[/size][size=16px]表达量随加药浓度增大而增多,这证明了西达本胺对[/size][size=16px]S[/size][size=16px]CLC[/size][size=16px]细胞系组蛋白乙酰化的促进作用,这种作用呈剂量依赖性。[/size][/align][align=left][size=18px]A[/size][/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2022/11/202211302350400898_8640_5887180_3.png[/img][/align][align=left][/align][align=left][/align][align=left][/align][align=center][/align][align=left][size=18px] [/size][size=18px]西达本胺通过线粒体凋亡途径诱导[/size][size=18px]S[/size][size=18px]CLC[/size][size=18px]细胞系凋亡[/size][/align][align=left][size=16px]我们的功能实验表明,西达本胺[/size][size=16px]可剂量依赖的[/size][size=16px]促进[/size][size=16px]SCLC[/size][size=16px]细胞[/size][size=16px]系[/size][size=16px]凋亡[/size][size=16px],但其机制尚未明确。[/size][size=16px]依据国内外报道,西达本胺主要通过线粒体凋亡途径诱导细胞凋亡[/size][size=16px]。除此之外,[/size][size=16px]西达本胺[/size][size=16px]能[/size][size=16px]使[/size][size=16px]线粒体[/size][size=16px]DNA[/size][size=16px]双链断裂,发生损伤。[/size][size=16px]为探究其是否通过此途径在[/size][size=16px]S[/size][size=16px]CLC[/size][size=16px]细胞系中发挥作用,我们检测了加药[/size][size=16px]4[/size][size=16px]8[/size][size=16px] [/size][size=16px]h[/size][size=16px]后,[/size][size=16px]H69[/size][size=16px]、[/size][size=16px]H[/size][size=16px]446[/size][size=16px]、[/size][size=16px]H[/size][size=16px]526[/size][size=16px]、[/size][size=16px]DMS114[/size][size=16px]细胞中由线粒体介导的[/size][size=16px]C[/size][size=16px]aspase[/size][size=16px]信号通路相关蛋白[/size][size=16px]Bcl-2[/size][size=16px],[/size][size=16px]Bax[/size][size=16px],细胞色素[/size][size=16px]C[/size][size=16px],[/size][size=16px]Ca[/size][size=16px]spase 9[/size][size=16px],[/size][size=16px]c[/size][size=16px]leaved Caspase 9[/size][size=16px],[/size][size=16px]P[/size][size=16px]ARP[/size][size=16px],[/size][size=16px]c[/size][size=16px]leaved [/size][size=16px]PARP[/size][size=16px],[/size][size=16px]Ca[/size][size=16px]spase 3[/size][size=16px],[/size][size=16px]c[/size][size=16px]leaved Caspase 3[/size][size=16px]以及[/size][size=16px]D[/size][size=16px]NA[/size][size=16px]双链断裂标志物[/size][size=16px] [/size][size=16px]γH2AX[/size][size=16px]表达水平。[/size][size=16px]Western blot[/size][size=16px]结果显示,[/size][size=16px]Ca[/size][size=16px]spase 9[/size][size=16px],[/size][size=16px]P[/size][size=16px]ARP[/size][size=16px] [/size][size=16px],[/size][size=16px]Ca[/size][size=16px]spase 3[/size][size=16px]表达水平无明显变化,[/size][size=16px]Bcl-2[/size][size=16px]表达下调,其余蛋白表达均上调。这些结果表明,在[/size][size=16px]S[/size][size=16px]CLC[/size][size=16px]细胞中,西达本胺可以通过线粒体凋亡途径诱导细胞凋亡。[/size][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=left][size=16px]A[/size][/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2022/11/202211302350402755_79_5887180_3.png[/img][/align][align=left][size=18px] [/size][size=18px]西达本胺通过抑制[/size][size=18px]C[/size][size=18px]yclin-CDK[/size][size=18px]复合物活性阻滞[/size][size=18px]S[/size][size=18px]CLC[/size][size=18px]细胞系周期[/size][/align][align=left][font='宋体'][size=16px]据文献报道,[/size][/font][size=16px]不同[/size][size=16px]HDACI[/size][size=16px]对不同细胞阻滞时相不一致。为验证西达本胺对[/size][size=16px]SCLC[/size][size=16px]细胞周期的作用,我们检测了[/size][size=16px]经[/size][size=16px]西达本胺[/size][size=16px]处理[/size][size=16px]48[/size][size=16px] [/size][size=16px]h[/size][size=16px]后,[/size][size=16px]H69[/size][size=16px]、[/size][size=16px]H446[/size][size=16px]、[/size][size=16px]H526[/size][size=16px]、[/size][size=16px]DMS114[/size][size=16px]细胞中细胞周期相关蛋白的表达水平,如图所示。[/size][size=16px]在[/size][size=16px]H69[/size][size=16px]、[/size][size=16px]H526[/size][size=16px]、[/size][size=16px]D[/size][size=16px]MS114[/size][size=16px]细胞系中[/size][size=16px]P21[/size][size=16px]、[/size][size=16px]P27[/size][size=16px]表达上调,[/size][size=16px]C[/size][size=16px]yclin A2[/size][size=16px]与[/size][size=16px]C[/size][size=16px]DK[/size][size=16px]2[/size][size=16px]表达下调[/size][size=16px],[/size][size=16px]说明西达本胺阻滞[/size][size=16px]H69[/size][size=16px]、[/size][size=16px]H526[/size][size=16px]、[/size][size=16px]D[/size][size=16px]MS114[/size][size=16px]于[/size][size=16px]S[/size][size=16px]期。在[/size][size=16px]H446[/size][size=16px]细胞系中[/size][size=16px]C[/size][size=16px]yclin E1[/size][size=16px]与[/size][size=16px]C[/size][size=16px]DK2[/size][size=16px]表达下调[/size][size=16px],说明西达本胺阻滞其于[/size][size=16px]G[/size][size=16px]1[/size][size=16px]/S[/size][size=16px]期。[/size][/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2022/11/202211302350422585_1956_5887180_3.png[/img][size=16px] [/size][img]https://ng1.17img.cn/bbsfiles/images/2022/11/202211302350405804_8826_5887180_3.png[/img][/align][align=left][size=18px]小结[/size][/align][size=16px]1[/size][size=16px].[/size][size=16px]西达本胺可以增强[/size][size=16px]S[/size][size=16px]CLC[/size][size=16px]细胞系组蛋白乙酰化水平。[/size][size=16px]2.[/size][size=16px]西达本胺诱导[/size][size=16px]S[/size][size=16px]CLC[/size][size=16px]细胞凋亡的机制可能与其激活线粒体介导的[/size][size=16px]caspase[/size][size=16px]凋亡途径有关。[/size][size=16px]3[/size][size=16px].[/size][size=16px]西达本胺可阻滞[/size][size=16px]S[/size][size=16px]CLC[/size][size=16px]细胞周期,可能与其上调细胞周期蛋白激酶抑制剂表达、从而抑制[/size][size=16px]C[/size][size=16px]yclin-CDK[/size][size=16px]复合物活性有关。[/size]