









近日,恒瑞医药子公司苏州盛迪亚生物医药有限公司收到国家药品监督管理局(以下简称“国家药监局”)下发的《受理通知书》,公司注射用瑞康曲妥珠单抗(研发代号:SHR-A1811)的药品上市许可申请获国家药监局受理,并且近日该产品已被纳入优先审评程序,适应症为:用于既往接受过至少一种系统治疗的局部晚期或转移性HER2突变成人非小细胞肺癌患者的治疗。
关于HER2突变非小细胞肺癌原发性肺癌是世界范围内最常见的恶性肿瘤。根据GLOBOCAN 2022数据,肺癌发病率居恶性肿瘤第一位,死亡率居恶性肿瘤首位,全球每年新发肺癌病例数约为250万,死亡病例数约为180万,在肿瘤致死病因中居第一位。HER2突变在非小细胞肺癌(NSCLC)中是一种相对罕见的驱动基因变异,发生率大约为2%-4%。与其他驱动基因相比,HER2突变NSCLC总体生存期较短,预后差。我国该人群在一线标准治疗进展后仍以化疗为主,缺乏有效的治疗手段。
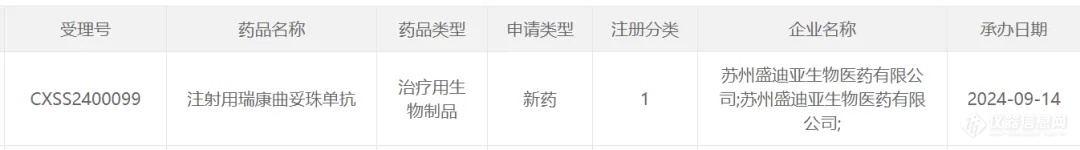
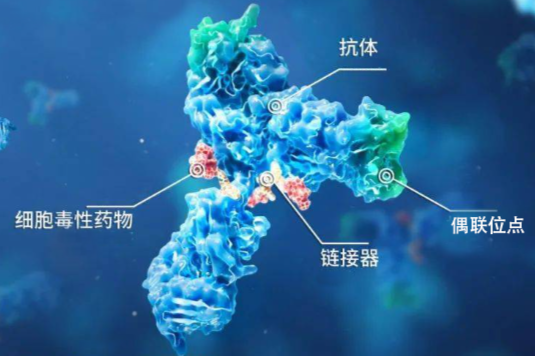
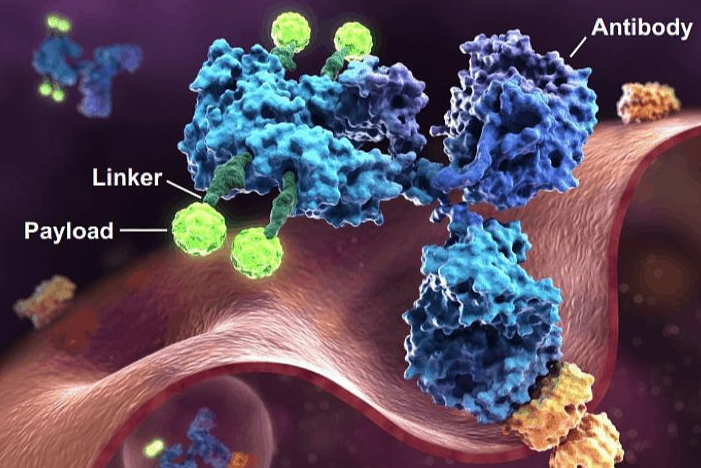
注射用瑞康曲妥珠单抗是恒瑞医药自主研发的、以HER2为靶点的抗体药物偶联物,拟用于HER2表达或突变的晚期实体瘤的治疗。瑞康曲妥珠单抗可特异性结合肿瘤细胞表面上的HER2,随后偶联物被内吞至细胞内并转运至溶酶体中,通过携带的载药在肿瘤细胞内产生药物作用,诱导肿瘤细胞的凋亡。瑞康曲妥珠单抗已获批开展多项临床研究,其中乳腺癌、胃癌或胃食管结合部腺癌、结直肠癌以及非小细胞肺癌均进入III期研发阶段,旨在为HER2基因异常的肿瘤患者提供新的治疗选择,为后续研究及药物惠及患者提供更多的临床证据。
2024年6月,瑞康曲妥珠单抗治疗HER2突变非小细胞肺癌(NSCLC)患者的II期临床试验(SHR-A1811-I-103)主要研究终点结果达到方案预设的优效标准。该研究旨在评估瑞康曲妥珠单抗治疗HER2突变的晚期NSCLC受试者的抗肿瘤疗效和安全性。由上海市胸科医院陆舜教授担任主要研究者,全国35家中心共同参与。主要研究终点为由独立影像评审委员会(IRC)基于RECIST v1.1评估的客观缓解率(ORR),次要研究终点包括研究者基于RECIST v1.1标准评估的ORR、IRC和研究者评估的缓解持续时间(DoR)、疾病控制率(DCR)、无进展生存期(PFS)以及总生存期(OS)等。研究结果表明,与预设的历史数据相比,瑞康曲妥珠单抗单药在HER2突变NSCLC患者中取得了显著的且有临床意义的改善。
多年来,恒瑞医药深刻关注中国HER2表达或突变肿瘤领域的治疗现状,持续探索更多有效的治疗方案。目前,基于恒瑞模块化ADC创新平台(HRMAP),经过10年的ADC研发积累,恒瑞成为国内在热门靶点上布局进展靠前、兼具诸多差异化ADC产品的企业,目前已有包括SHR-A1811在内的12个新型、具有差异化的ADC分子成功获批临床,6款产品实现国际同步开发,还有多个创新药产品布局各个实体肿瘤治疗领域,以期为患者带来更多的治疗选择。
[来源:药融圈]
2024.08.16

2024.09.14

2024.09.13
新疗法组合:ADC+Keytruda显著延长晚期癌症OS和PFS
2024.09.04
2024.08.22

2024.08.21
版权与免责声明:
① 凡本网注明"来源:仪器信息网"的所有作品,版权均属于仪器信息网,未经本网授权不得转载、摘编或利用其它方式使用。已获本网授权的作品,应在授权范围内使用,并注明"来源:仪器信息网"。违者本网将追究相关法律责任。
② 本网凡注明"来源:xxx(非本网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责,且不承担此类作品侵权行为的直接责任及连带责任。如其他媒体、网站或个人从本网下载使用,必须保留本网注明的"稿件来源",并自负版权等法律责任。
③ 如涉及作品内容、版权等问题,请在作品发表之日起两周内与本网联系,否则视为默认仪器信息网有权转载。
![]() 谢谢您的赞赏,您的鼓励是我前进的动力~
谢谢您的赞赏,您的鼓励是我前进的动力~
打赏失败了~
评论成功+4积分
评论成功,积分获取达到限制
![]() 投票成功~
投票成功~
投票失败了~