









01
研究背景
02
研究内容
2024年4月22日,苏州大学生物医学研究院周芳芳教授团队在 Cell 发表题为“Alanyl-tRNA synthetase, AARS1, is a lactate sensor and lactyltransferase that lactylates p53 and contributes to tumorigenesis” 的研究论文。
DOI: 10.1016/j.cell.2024.04.002IF: 45.5 Q1
在这篇研究中,课题组发现肿瘤源性乳酸是p53的天然抑制剂,可促进p53乳酸化,全基因组CRISPR筛选确定了AARS1是肿瘤细胞中全局赖氨酸乳酸化的介质。AARS1耗竭的肿瘤细胞中增殖、集落形成能力显著降低,并且AARS1的耗竭抑制了乳酸诱导的赖氨酸乳酸化。另外,β-丙氨酸在结构上类似于乳酸,研究者发现用其预处理的细胞赖氨酸乳酸化减少。这些生理表象背后的分子机制,研究者仍需要进行进一步探究。
借助NanoTemper公司的MST技术,研究者验证证实了AARS1蛋白(EcAlaRS细菌酶、HsAlaRS人源酶)在分子层面上与乳酸的结合,乳酸与EcAlaRS、乳酸与HsAlaRS的Kd值分别为13 μM和35 μM(图1A),表明EcAlaRS和HsAlaRS可以使用乳酸作为底物直接催化乳酸化。同时,通过MST实验,研究了β-丙氨酸与AARS1的互作,Kd值为2.7 μM(β-alanine与EcAlaRS) 和4.0 μM(β-alanine与HsAlaRS)(图1B), β-丙氨酸有着更强的亲和力。MST的结果在分子层面上非常直观地给出了β-丙氨酸可以抑制乳酸化的结果,从而阐明了生理上β-丙氨酸的拮抗乳酸化的机制(图1C、D)。
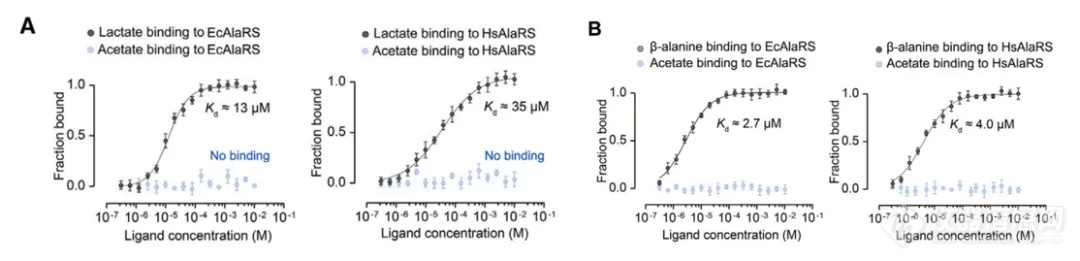
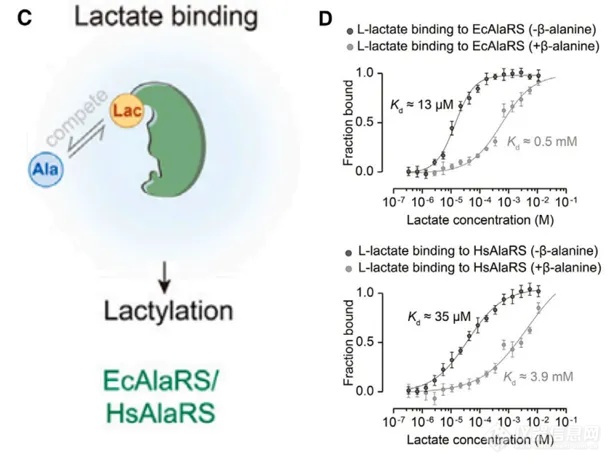
图1.AASR1与乳酸互作(A),AASR1与β-丙氨酸互作(B), β-丙氨酸与乳酸竞争结合机制(C), β-丙氨酸抑制乳酸结合AASR1(D)
但是,AARS1结合了乳酸其后续是如何靶向到p53上的呢?
为了寻找答案,研究人员进行了分子对接模拟及关键位点突变pull-down实验,采用质谱分析结合MST实验的方式,发现AARS1 通过 ATP 依赖的方式催化形成乳酸-AMP 中间体,随后将乳酸转移至目标蛋白的赖氨酸残基上,可实现共价结合。这一过程不仅在人类中,也在大肠杆菌中观察到,表明 AARS1 在物种间具有催化赖氨酸乳酸化的古老功能。
通过MST实验,研究者们得到了验证,HsAlaRS和EcAlaRS在体外直接与p53结合,p53与HsAlaRS和p53与EcAlaRS的Kd分别达到39 μM和21 μM,定量确认了pull-down实验的结果(图2A、B)。结合其他生化实验提出描述AlaRS介导的乳酸化的工作模型(图2C):AlaRS首先与乳酸结合,在ATP存在下形成乳酸AMP和PPi;在底物蛋白存在的情况下,AlaRS将丙酰基转移到底物蛋白上的赖氨酸残基上。
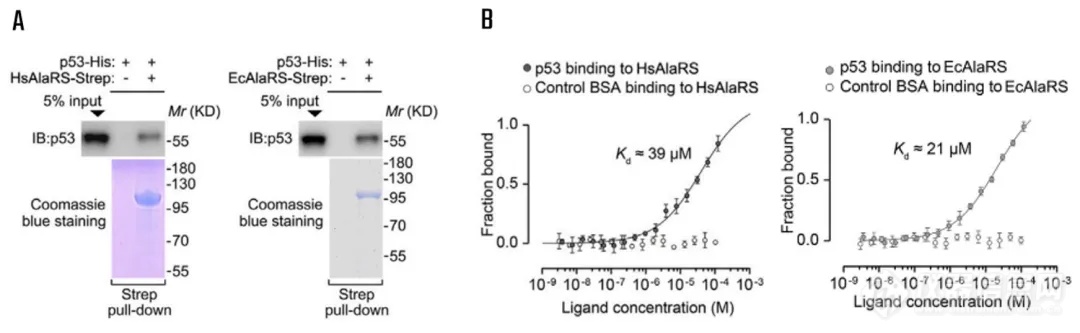
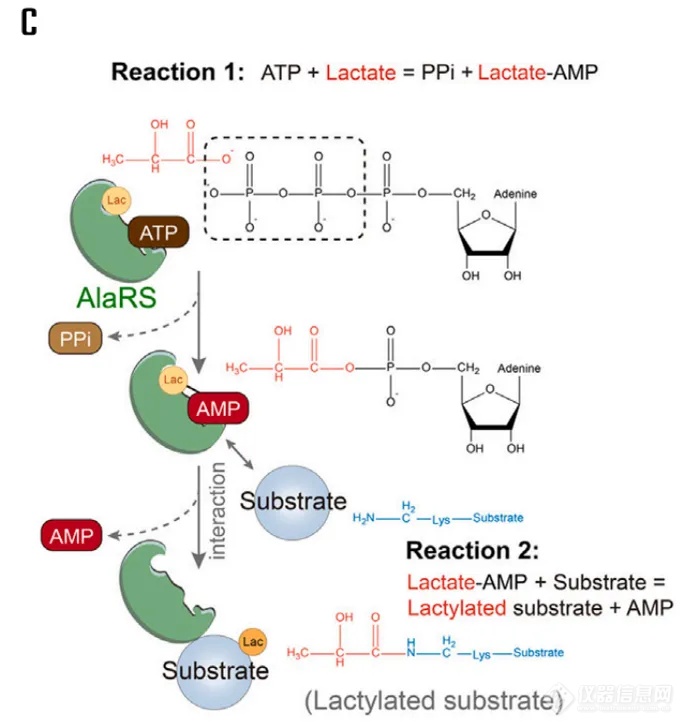
图2.p53与HsAlaRS和p53与EcAlaRS定性pull-down结果(A), p53与HsAlaRS和p53与EcAlaRS互作(B), AlaRS介导的乳酸化的工作模型(C)
后续进一步通过质谱分析和抗体识别确认了p53上乳酸化的残基是K120和K139。通过MST实验直接比较了乳酸化p53(p53Lac)与非乳酸化p53(p53Non-Lac)对含有p53应答元件的DNA(p53RE-DNA)的亲和力,乳酸化p53(p53K120-Lac、p53K139Lac和p53-Dual-Lac)对p53RE-DNA的亲和力分别降低了约100倍、10倍和1000倍(图3)。之后的生化生理实验进一步表明p53的位点特异性乳酸化减弱了它们的DNA结合和液-液相分离(LLPS),从而降低了p53的抑瘤作用。
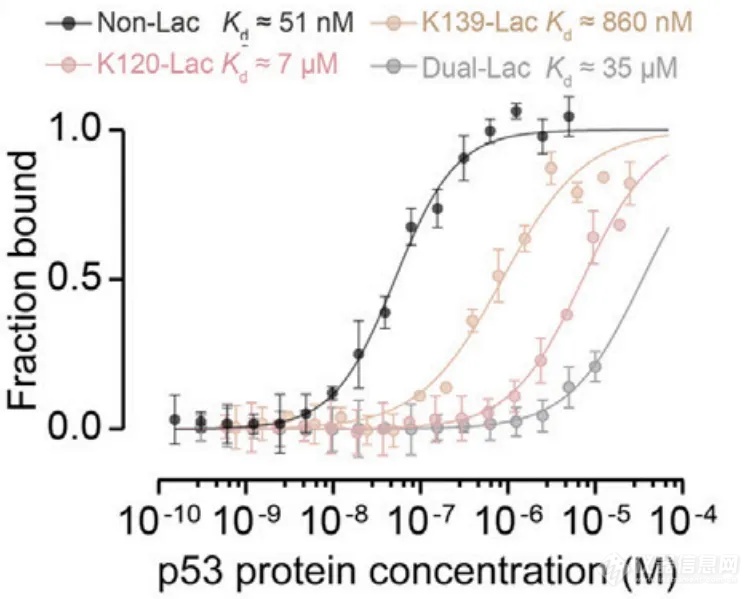
图3.p53乳酸化减弱了其与DNA结合
另外,对于p53上的位点K120和K139, 各种研究表明,p53-K120N可能是无功能的,这些乳酸化模拟变体可能有助于肿瘤发生。
研究者通过借助MST实验给出了有力的数据支持(图4),纯化的K120N/Q/E和K139 N/T/Q/E突变体对p53RE-DNA的结合亲和力降低。K120E和K139E的减少更为明显,表明K-to-E突变导致电荷减少更强。在进一步的生化活性实验中发现,K120N/Q和K139N/T/Q部分丧失了刺激p53反应基因表达的能力,而K120E和K139E几乎完全丧失了这种能力。K120、K139上的病理性突变(肿瘤发生)与p53乳酸化(肿瘤发展)都会导致其与DNA结合能力降低,从而活性丧失(图4)。
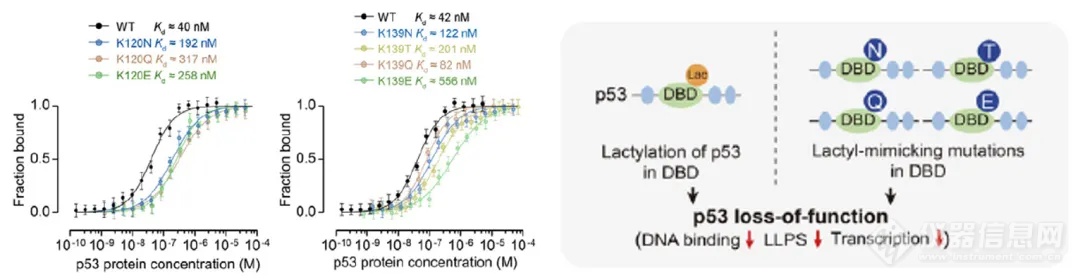
图4.Cy5-p53RE-DNA与p53 WT及其突变蛋白互作(左), p53中乳酸化与模拟突变(右)
本项研究中进行了大量的MST实验,通过MST技术,来验证测定AARS1蛋白与肿瘤代谢产物(乳酸)的互作,确认AARS1与p53(蛋白与蛋白)互作的行为, 表征蛋白突变体功能上改变。结合其他生理生化实验完整详细地阐述了关键酶AARS1与肿瘤代谢物(乳酸)在肿瘤发生和发展中重要作用,揭示了p53乳酸化失活机制,提供了一种利用β-丙氨酸阻止p53乳酸化的方法,β-丙氨酸与乳酸竞争结合AARS1,从而加强癌症治疗(图5)。
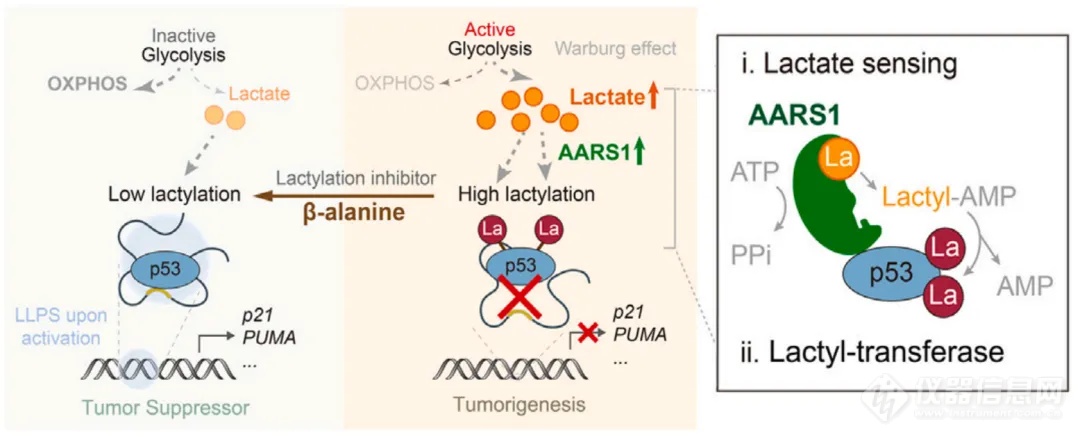
图5.AARS1在赖氨酸乳酸化组和p53乳酸化在肿瘤发生中的作用以及β-丙氨酸的抑制作用
03
技术优势
NanoTemper公司的专利MST技术不依赖于分子量的改变,蛋白用量少,可以轻松进行蛋白与小分子代谢产物实验。MST实验是在溶液中,无需固定蛋白的实验体系,可以便捷地设计多组分的实验方案,验证类似小分子的功能。在这篇研究中,除了采用标记蛋白的方式,在检测多种突变体蛋白与p53RE-DNA互作(蛋白与DNA)时,还选择了标记DNA的方式,使得实验内容设计更加简洁且高效。
Monolith系列分子互作平台可以更好的帮助科研人员简便地设计互作方案,在分子层面上直观验证生理机制上的互作结果,为您的实验研究提供强大助力。

Monolith 分子互作检测仪
· 直接在溶液中检测亲和力,无需固定
· 无惧分子量的变化,轻松检测各种类型小分子
· 检测一个Kd仅需10min
· 无微流控系统,无需清洗维护
[来源:诺坦普科技(北京)有限公司]

新品上市 | Andromeda X 全新蛋白质表达和功能快速筛选系统
2024.08.08

让痛风不再痛,NanoTemper专利MST技术精准助力小分子检测 !
2024.07.24

Eurofins Discovery | 片段药物发现新「组合拳」
2024.07.18


IF: 46.9 | 多元互作案例分享--首选NanoTemper的MST技术!
2024.06.21

2024.06.20
版权与免责声明:
① 凡本网注明"来源:仪器信息网"的所有作品,版权均属于仪器信息网,未经本网授权不得转载、摘编或利用其它方式使用。已获本网授权的作品,应在授权范围内使用,并注明"来源:仪器信息网"。违者本网将追究相关法律责任。
② 本网凡注明"来源:xxx(非本网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责,且不承担此类作品侵权行为的直接责任及连带责任。如其他媒体、网站或个人从本网下载使用,必须保留本网注明的"稿件来源",并自负版权等法律责任。
③ 如涉及作品内容、版权等问题,请在作品发表之日起两周内与本网联系,否则视为默认仪器信息网有权转载。
![]() 谢谢您的赞赏,您的鼓励是我前进的动力~
谢谢您的赞赏,您的鼓励是我前进的动力~
打赏失败了~
评论成功+4积分
评论成功,积分获取达到限制
![]() 投票成功~
投票成功~
投票失败了~