







我思故我在


2020年年初新冠肺炎全球爆发,为应对紧张的疫情,国家药品监督管理局(NMPA)、美国食品药品监督管理局(FDA)、世界卫生组织(WHO)开放了应急审批通道,加快了新型冠状病毒检测试剂盒的审批。
截至2020年4月26日,国家药品监督管理局已应急审批30个新型冠状病毒检测试剂。其中核酸检测试剂18个,抗体检测试剂11个。
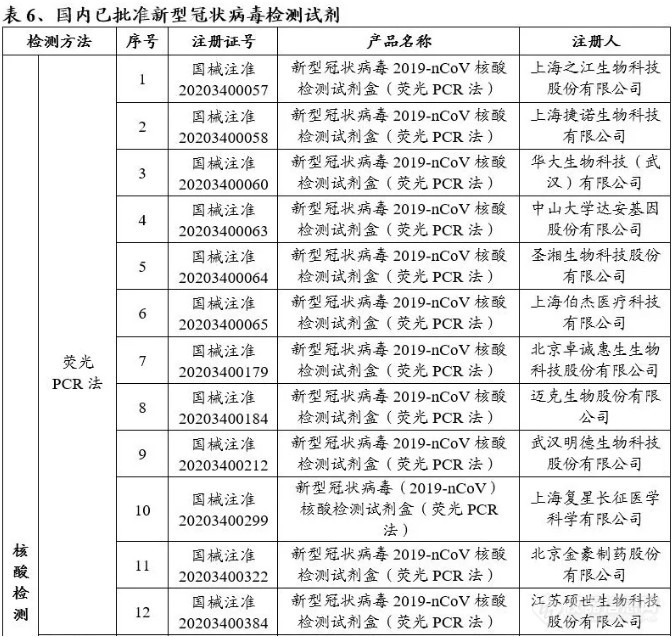
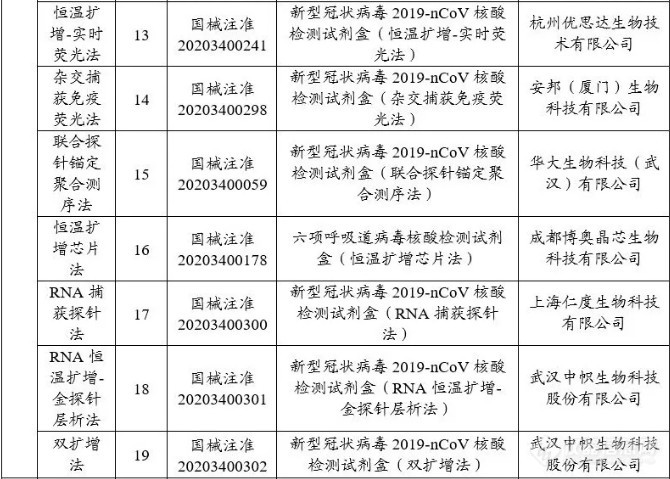
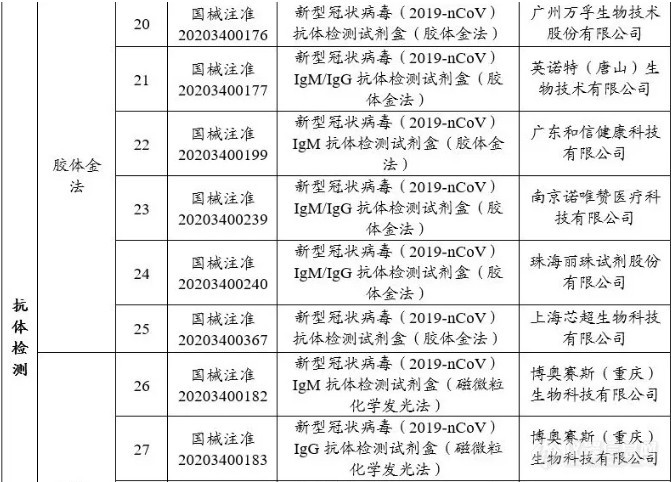
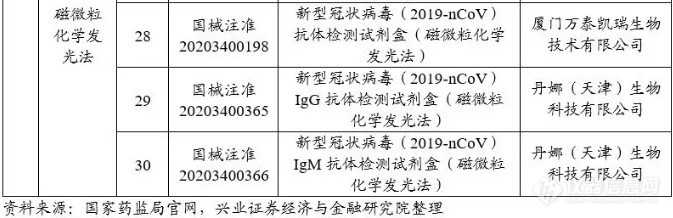
国外疫情日趋严峻,各国陷入试剂盒短缺的困境。国产试剂盒具有先发临床和成本优势,多家国内企业开始向世界各国出口试剂盒。3月开始,欧洲严峻疫情态势产生新冠检测的巨大需求,多家中国企业瞄准了欧洲庞大的新冠检测市场,并积极推动自主研发的新冠检测产品进入欧洲市场。截至4月22日,据不完全统计,国内从事新冠检测相关产品研发生产的企业近千家,其中产品已获得CE认证的企业超过160家。
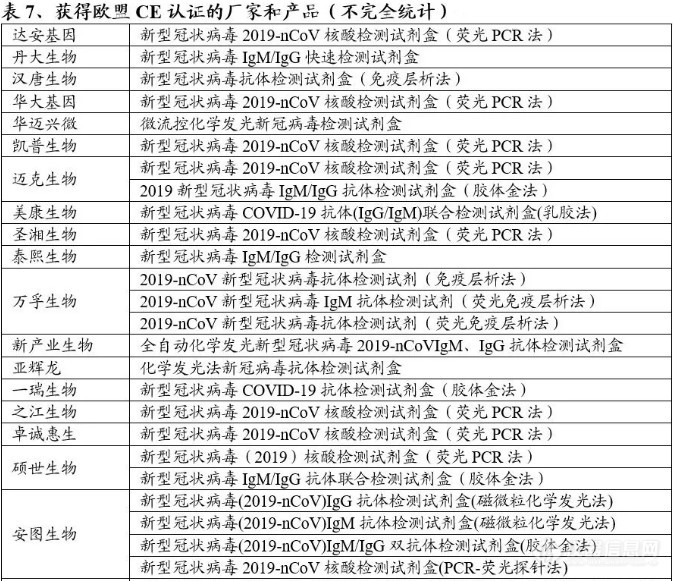



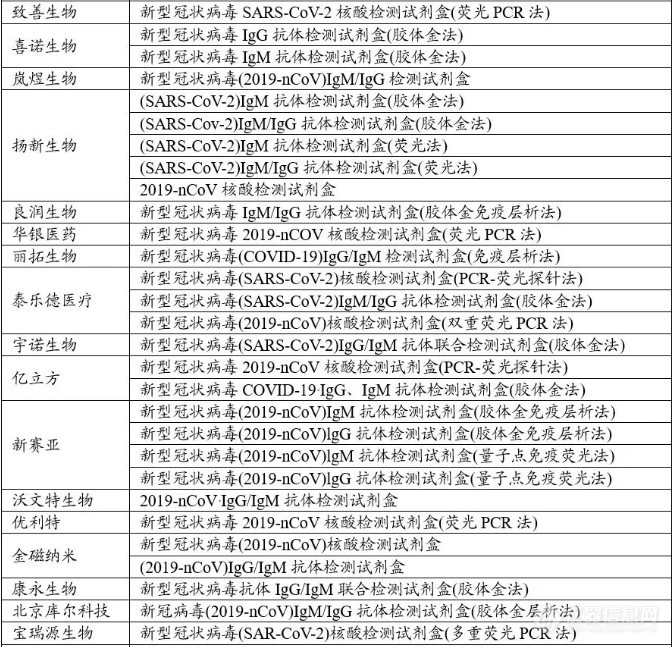

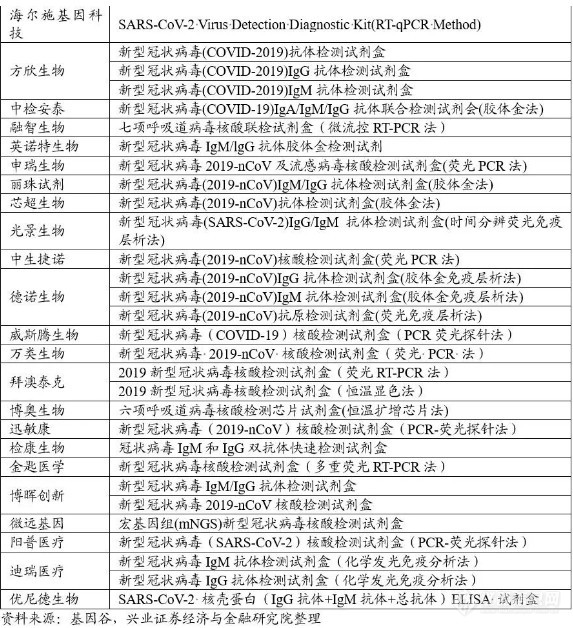
相比欧盟CE认证而言,美国市场的准入门槛更高。截止2020年4月27日,核酸检测产品已获得美国EUA的40余家企业中,多为业内知名的跨国巨头企业,其中有四家中国企业:华大基因、南京科维思、迈克生物、复星医药;而核酸检测产品已同时取得国内NMPA注册证书、欧盟CE认证和美国FDA EUA的国内企业只有华大基因、迈克生物、复星医药三家公司。
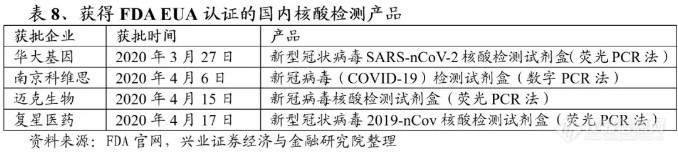
在抗体检测产品中,乐普医疗的新型冠状病毒(SARS-CoV-2)抗体检测试剂盒(胶体金免疫层析法)于3月27日取得FDA EUA准入,安图生物的新型冠状病毒抗体检测试剂盒(胶体金法,英文名称:Anti-SARS-CoV-2 Rapid Test)于2020年4月24日获得FDA EUA认证。此外,国内企业万孚生物、三诺生物等的抗体检测试剂盒也已按照FDA发布的《Policy for Diagnostic Tests for CoronavirusDisease-2019 during the Public Health Emergency》完成Notification程序,并且完成了公司注册和产品列名,标志着公司该产品具备了在美国上市销售的资格。
2020年4月25日,我国商务部发布公告,“自4月26日起,取得国外标准认证或注册的新型冠状病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计的出口企业,报关时须提交书面声明,承诺产品符合进口国(地区)质量标准和安全要求,海关凭商务部提供的取得国外标准认证或注册的生产企业清单验放”。这也就意味着新冠检测产品的出口只需要取得国外标准认证或注册,无需拥有国内注册证。但同时很重要的一点是出口企业必须进入中国医药保健品进出口商会企业清单才能被验放。目前,符合规定的企业都在积极申请加入,截至4月28日晚,已有51家企业进入清单。
而在此前2020年3月31日,国家商务部会同海关总署、国家药监局发布《关于有序开展医疗物资出口的公告》(2020年第5号),要求自4月1日起,同时获得NMPA注册证书和国外特定区域准入资格的企业可实现国内及获授权的国外地区新冠检测产品的销售。此次“双证”限制的放开,进一步促进国内IVD企业的新冠检测产品出口。
[来源:仪器信息网] 未经授权不得转载

3626.7万元!中华人民共和国广州海关10月拟采购超过40台/套仪器设备
2024.08.26

4821.56万元!厦门大学9月仪器采购意向公布:聚焦生命科学领域
2024.08.26

2024.08.21
2024.08.21

2024.08.20

涉及大量仪器设备,成都发布53.6亿预算大规模设备更新需求清单
2024.08.19
版权与免责声明:
① 凡本网注明"来源:仪器信息网"的所有作品,版权均属于仪器信息网,未经本网授权不得转载、摘编或利用其它方式使用。已获本网授权的作品,应在授权范围内使用,并注明"来源:仪器信息网"。违者本网将追究相关法律责任。
② 本网凡注明"来源:xxx(非本网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责,且不承担此类作品侵权行为的直接责任及连带责任。如其他媒体、网站或个人从本网下载使用,必须保留本网注明的"稿件来源",并自负版权等法律责任。
③ 如涉及作品内容、版权等问题,请在作品发表之日起两周内与本网联系,否则视为默认仪器信息网有权转载。
![]() 谢谢您的赞赏,您的鼓励是我前进的动力~
谢谢您的赞赏,您的鼓励是我前进的动力~
打赏失败了~
评论成功+4积分
评论成功,积分获取达到限制
![]() 投票成功~
投票成功~
投票失败了~