2× qPCR Green Fast Mixture
2× 预混实时荧光定量快速 PCR 反应体系
【产品简介】
本产品是采用 SYBR Green I 嵌合荧光法进行实时荧光定量 PCR 的专用 2×浓度预混液。产品含有
优化浓度的 HotStart Taq DNA Polymerase、SYBR Green I、dNTPs、Mg2+、反应缓冲液和稳定剂等
成分。主要用于基因组 DNA 靶序列和 RNA 反转录后 cDNA 靶序列的检测。HotStart Taq DNA
Polymerase 高温加热前,抗 Taq 单克隆抗体与 Taq 酶结合,抑制 Taq 酶的聚合酶活性,从而抑制在低
温条件下出现的由引物和模板 DNA 非特异性杂交或引物二聚体引起的非特异性扩增。抗 Taq 单克隆抗
体在 PCR 反应第一循环的变性步骤中已完全失活,不会阻碍之后的 Taq Polymerase 反应,大大提高
了 PCR 反应的灵敏度及特异性。优化浓度的 SYBR Green I 荧光染料,特异性地掺入 DNA 双链后,
荧光信号增强,而不掺入链中 SYBR Green I 染料分子荧光信号不变,从而保证荧光信号的增加与
PCR 产物的增加完全同步,荧光可以在退火或延伸阶段测定。
本产品为 2×预混荧光定量 PCR 反应体系,使用时只需加入模板、引物和水,使其工作浓度为 1×,
即可进行反应。具有快速简便、灵敏度高、特异性强、稳定性好等优点,可最大限度地减少人为误差、
节约 PCR 实验操作时间、降低污染几率。
【规格和组分】
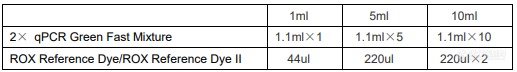
【保存】-20℃恒温避光保存两年,避免反复冻融。如经常使用,可置于 4℃保存至少六个月。
【注意事项】
1. 使用前请上下颠倒轻轻混匀,尽量避免起泡,并经短暂离心后使用。
2. 尽可能减少 qPCR Green Fast Mixture 在光下的曝露时间,长时间的曝光可导致荧光信号减弱。
3. 反应液的配制、分装请一定使用无污染的枪头、Microtube 等,尽量避免交叉污染。
4. 本品不能用于杂交探针法。
【使用方法】
用户需自备的试剂:cDNA 模板或 DNA 模板、引物
请按照不同品牌荧光定量 PCR 仪的使用说明书要求进行试验操作。
操作示例:分别以 20ul 和 50ul PCR 反应体系为例
1. PCR 反应体系的建立:
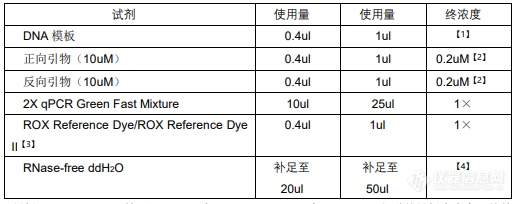
1. 模板量:10~100 ng 基因组 DNA,或 1~10 ng cDNA 为参照,因不同物种的模板中含有目的基因拷贝数不同,可对模板进行梯度稀释,以确定最佳的模板使用量。另外,two Step RT-PCR 反应的 cDNA(RT 反应液)作为模板时的添加量不要超过 PCR 反应液总体积的 10%。
2. 引物:通常引物浓度以 0.2uM 可以得到较好结果,可以终浓度 0.1~1.0uM 作为设定范围的参考。扩增效率不高的情况下,可提高引物的浓度;发生非特异性反应时,可降低引物浓度,由此优化反应体系,为了获得理想的去 PCR 的效果,扩增片段的长度建议为 80~200bp。
3. 不同仪器所需 ROX Reference Dye 不同,或需要添加或不需要添加,请根据仪器说明进行操作。
4. 按照各仪器推荐体系进行反应液配制。
2. PCR 反应条件的设置
本制品中使用的 HotStart Taq DNA Polymerase 是利用抗 Taq 抗体封闭的 Hot Start DNA 聚合酶,如果在 PCR 反应前进行模板的预变性,通常设定为 95℃、2min,复杂或高 GC 模板适当延长时间至 5min。该 DNA 聚合酶在 15 sec 内可完成至少 300bp 的扩增,可以满足绝大多数的 qPCR 实验;对于超过 350bp或者高 GC 含量的扩增子,建议增加延伸时间至 60sec 或者采用三步法以提高扩增效率。

注:以上举例为常规 qPCR 反应系统,仅供参考。实际反应条件因模板、引物等的结构不同而各异,需根据模板、引物、目的片段的特点设定最佳反应条件,并根据此比例放大或缩小反应体系
【备注】
本产品仅供科研使用。在确认产品质量出现问题时,本公司承诺为客户免费更换等量的质量合格产
品。在所有情况下,本公司对此产品所承担的责任,仅限于此产品的价值本身。
特别提示:本公司的所有产品仅可用于科研实验,严禁用于临床医疗及其他非科研用途!
![]()
![]()