搜全站
搜展位
使用超高效合相色谱分析人体尿液中的三环类抗抑郁药
使用超高效合相色谱(UPC2)分析人体尿液中的三环类抗抑郁药
Erin Chambers和Kenneth J. Fountain
沃特世公司(美国马萨诸塞州米尔福德市)
应用优势
1.环保、可持续(绿色)化学
2.分析速度快
3.定量准确
4.可与反相色谱进行正交实验
5.可使用SPE洗脱液直接进样
沃特世解决方案
ACQUITY UPC2™系统
ACQUITY UPC2色谱柱
Oasis® WCX 96孔µElution板(部件号186002499)
Xevo® TQ-S质谱仪
关键词
合相色谱,Oasis,样品制备,生物分析,三环类抗抑郁药,定量,UPC2
简介
三环类抗抑郁药(TCA)是较老的一类药物,但仍具有药理学作用。例如,对其它类抗抑郁药反应较差的药物受试者仍较常见,由此决定了TCA仍具有持续的生存空间。此外,这类药物比其它新型的抗抑郁药要便宜得多,因此在门诊中也有使用。过去,人们使用GC、1 UV、2 或LC/MS对TCA进行分析。3 UPC2™技术可对有机提取物进行分析,因此在生物分析测定领域备受青睐。有机提取物可通过此领域中最常见的样品制备方法,例如蛋白质沉淀(PPT)、液-液萃取(LLE)和固相萃取(SPE)法获得。反相色谱系统在进样前需对有机提取物进行蒸发和复溶,而非水溶剂系统则不需要此环节。UPC2技术具有主要溶剂(CO2)环保、可再生、可与反相色谱进行正交实验、以及可利用多种固定相的特点,使其具备了低溶剂消耗和低成本的优势,从而增加了生物分析方法开发的选择性和灵活性。因此,本实验以人体尿液中TCA的分析为例,进行了一项确证UPC2分离适用性的论证性研究。研究中所用特定TCA的结构见图1。虽然人们对GC和LC方法开发途径有很好的定义并在常规应用中使用,但UPC2分离的方法开发仍是一块较新的研究领域。本应用纪要中重点描述了某些关键的UPC2参数并提供了适用的筛选选项。例如,色谱柱化学性质、pH和进样溶剂由色谱柱管理器和四元溶剂切换系统进行系统化的自动筛选。在选择色谱柱、流动相和进样溶剂后,系统将使用通过筛选试验获得的最佳条件对梯度进行优化并分析尿样提取物。在尿液检测中,各抗抑郁药的定量下限(LLOQ)0.1 ng/mL可轻松达到,符合FDA针对生物分析方法制定的LLOQ测定标准。另外,简化的标准曲线(无内标物)在+/-1%至8%范围内的线性和准确度良好。
实验
UPC2条件
系统: ACQUITY UPC2
色谱柱:ACQUITY UPC2 BEH 2.1×50 mm,1.7 µm
流动相A:CO2
流动相B:含0.2% NH4OH的甲醇
清洗溶剂:60:40的乙腈/异丙醇+2%甲酸
分离模式:流动相B在2 min内从2.0%增加至40%;达到30%时保持1 min。
流速:1.4 mL/min
CCM反压:1750 psi
柱温:40 ℃
样品温度:10 ℃
进样体积:2.0 µL
运行时间:3.0 min
补液流速:0.25 mL/min含0.2% NH4OH的异丙醇
收集板: 沃特世(Waters®) 1 mL ACQUITY®收集板
MS条件
质谱仪:Xevo TQ-S
电离模式:ESI+
毛细管电压:1.0 kV
碰撞能量: 按组分优化(见表格1)
锥孔电压:按组分优化(见表格1)
数据管理
色谱软件:MassLynx®
定量软件:TargetLynx™
优化软件:IntelliStart™
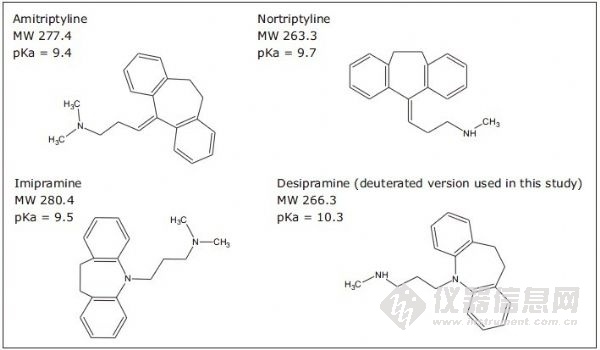
图1. 三环类抗抑郁药分析物的结构式。

实验
样品描述
采用Oasis WCX 96孔 µElution板制备尿样。首先,在200 µL样品中加入200 µL的4% H3PO4溶液,混匀;先用200 µL甲醇平衡萃取板中的各孔,然后用200 µL水平衡;将样品稀释液(400 µL)加载到板上;依次用200 µL 10 mM醋酸铵溶液(pH 6)、200 µL甲醇淋洗;用含2%甲酸的ACN/MeOH(60:40)溶液洗脱TCA,每次25 µL,洗脱2次,合并洗脱液。取洗脱液2 µL直接注入ACQUITY UPC2系统。
储备溶液和工作溶液均以甲醇为溶剂。向2 mL尿液中加入20 µL复合工作溶液(各化合物浓度为1 µg/mL)制成含5种抗抑郁药的尿样,此方法制成的尿样浓度为10 ng/mL。其它浓度的样品溶液通过使用对照人体尿液连续稀释高浓度的标准溶液制备而得。在本论证性研究中,制备并用于萃取的尿样最终浓度分别为:0.1、0.2、0.5、1.0、5.0和10.0 ng/mL。为确定定量下限(LLOQ),实验还对空白尿进行了萃取。
表1. 4种抗抑郁药物组的MS条件。
结果与讨论
Erin Chambers和Kenneth J. Fountain
沃特世公司(美国马萨诸塞州米尔福德市)
应用优势
2.分析速度快
3.定量准确
4.可与反相色谱进行正交实验
5.可使用SPE洗脱液直接进样
沃特世解决方案
ACQUITY UPC2™系统
ACQUITY UPC2色谱柱
Oasis® WCX 96孔µElution板(部件号186002499)
Xevo® TQ-S质谱仪
关键词
合相色谱,Oasis,样品制备,生物分析,三环类抗抑郁药,定量,UPC2
简介
三环类抗抑郁药(TCA)是较老的一类药物,但仍具有药理学作用。例如,对其它类抗抑郁药反应较差的药物受试者仍较常见,由此决定了TCA仍具有持续的生存空间。此外,这类药物比其它新型的抗抑郁药要便宜得多,因此在门诊中也有使用。过去,人们使用GC、1 UV、2 或LC/MS对TCA进行分析。3 UPC2™技术可对有机提取物进行分析,因此在生物分析测定领域备受青睐。有机提取物可通过此领域中最常见的样品制备方法,例如蛋白质沉淀(PPT)、液-液萃取(LLE)和固相萃取(SPE)法获得。反相色谱系统在进样前需对有机提取物进行蒸发和复溶,而非水溶剂系统则不需要此环节。UPC2技术具有主要溶剂(CO2)环保、可再生、可与反相色谱进行正交实验、以及可利用多种固定相的特点,使其具备了低溶剂消耗和低成本的优势,从而增加了生物分析方法开发的选择性和灵活性。因此,本实验以人体尿液中TCA的分析为例,进行了一项确证UPC2分离适用性的论证性研究。研究中所用特定TCA的结构见图1。虽然人们对GC和LC方法开发途径有很好的定义并在常规应用中使用,但UPC2分离的方法开发仍是一块较新的研究领域。本应用纪要中重点描述了某些关键的UPC2参数并提供了适用的筛选选项。例如,色谱柱化学性质、pH和进样溶剂由色谱柱管理器和四元溶剂切换系统进行系统化的自动筛选。在选择色谱柱、流动相和进样溶剂后,系统将使用通过筛选试验获得的最佳条件对梯度进行优化并分析尿样提取物。在尿液检测中,各抗抑郁药的定量下限(LLOQ)0.1 ng/mL可轻松达到,符合FDA针对生物分析方法制定的LLOQ测定标准。另外,简化的标准曲线(无内标物)在+/-1%至8%范围内的线性和准确度良好。
实验
UPC2条件
系统: ACQUITY UPC2
色谱柱:ACQUITY UPC2 BEH 2.1×50 mm,1.7 µm
流动相A:CO2
流动相B:含0.2% NH4OH的甲醇
清洗溶剂:60:40的乙腈/异丙醇+2%甲酸
分离模式:流动相B在2 min内从2.0%增加至40%;达到30%时保持1 min。
流速:1.4 mL/min
CCM反压:1750 psi
柱温:40 ℃
样品温度:10 ℃
进样体积:2.0 µL
运行时间:3.0 min
补液流速:0.25 mL/min含0.2% NH4OH的异丙醇
收集板: 沃特世(Waters®) 1 mL ACQUITY®收集板
MS条件
质谱仪:Xevo TQ-S
电离模式:ESI+
毛细管电压:1.0 kV
碰撞能量: 按组分优化(见表格1)
锥孔电压:按组分优化(见表格1)
数据管理
色谱软件:MassLynx®
定量软件:TargetLynx™
优化软件:IntelliStart™

图1. 三环类抗抑郁药分析物的结构式。
实验
样品描述
采用Oasis WCX 96孔 µElution板制备尿样。首先,在200 µL样品中加入200 µL的4% H3PO4溶液,混匀;先用200 µL甲醇平衡萃取板中的各孔,然后用200 µL水平衡;将样品稀释液(400 µL)加载到板上;依次用200 µL 10 mM醋酸铵溶液(pH 6)、200 µL甲醇淋洗;用含2%甲酸的ACN/MeOH(60:40)溶液洗脱TCA,每次25 µL,洗脱2次,合并洗脱液。取洗脱液2 µL直接注入ACQUITY UPC2系统。
储备溶液和工作溶液均以甲醇为溶剂。向2 mL尿液中加入20 µL复合工作溶液(各化合物浓度为1 µg/mL)制成含5种抗抑郁药的尿样,此方法制成的尿样浓度为10 ng/mL。其它浓度的样品溶液通过使用对照人体尿液连续稀释高浓度的标准溶液制备而得。在本论证性研究中,制备并用于萃取的尿样最终浓度分别为:0.1、0.2、0.5、1.0、5.0和10.0 ng/mL。为确定定量下限(LLOQ),实验还对空白尿进行了萃取。
| 分析物 | 母离子m/z | 子离子m/z | 锥孔电压(V) | 碰撞能量(eV) |
| 阿米替林 | 278.3 | 233.1 | 30 | 18 |
| 去甲替林 | 264.3 | 233.4 | 28 | 15 |
| 丙咪嗪 | 281.3 | 85.8 | 25 | 20 |
| 地昔帕明-D3 | 267.4 | 208.1 | 22 | 25 |
结果与讨论
之前已证明混合模式SPE是生物分析中最常选择的一类样品制备方法,4 这依赖于其分离分析物与内源性干扰物的双正交保留机制。因此,混合模式SPE是本次实验的首选。选用混合模式的弱阳离子交换剂基于以下两个方面的原因:分析物呈碱性,需要通过离子交换保留;此特定吸附剂的最终洗脱液实际呈酸性。进样溶剂的筛选结果表明,采用酸性进样溶剂可获得最佳的峰型和灵敏度(此处不作数据说明)。因此,Oasis WCX是不二之选。对通用的提取方法稍作修改,确保所有分析物通过离子交换可完全保留。人体尿液经SPE处理后,最终洗脱液中所有分析物的回收率为92%至104%,RSD为3%至6%。SPE洗脱液可直接进样,不需做进一步的稀释或蒸发,从而简化了整个工作流程,提高了分析通量。
系统性色谱筛选
方法开发过程对色谱柱、改性剂和改性添加剂进行了系统筛选,以获得最佳分离结果。经筛选的4种UPC2色谱柱如下:ACQUITY UPC2 BEH、BEH 2-EP、HSS C18 SB和 CSH™ Fluoro-Phenyl,所有色谱柱规格均为2.1×50 mm,填料粒径为1.7 μm。3种流动相B溶剂分别为甲醇、含0.2%甲酸的甲醇和含0.2% NH4OH的甲醇。筛选过程采用流动相B在3 min内从2%增加至45%,达到45%时保持1.5 min的常用梯度。当以添加有氢氧化铵的甲醇作流动相时,各色谱柱分析所得的峰形、灵敏度和分离度均为最佳。四种固定相使用此高pH流动相所得分析结果的对比情况如图2所示。除HSS SB色谱柱外,其它色谱柱的出峰顺序相似。但是,由HSS SB色谱柱得出的谱峰明显更宽,这将导致信噪比降低并影响低浓度样品的检测。峰变宽可能是由于分析物与固定相之间的次级相互作用所致。采用ACQUITY UPC2系统分析其它类化合物(本文未涉及此部分实验内容)时发现:使用具有缓冲作用的流动相改性剂(如,20至40 mM的甲酸铵)可以改善峰形。在本文的研究中,色谱分析的主要目标不是使分析物达到绝对的基线分离,而是获得最佳的峰形和最高灵敏度,因此我们对各色谱柱所得的峰面积进行了测定。在高pH改性剂条件下,使用各色谱柱得出的分析物峰面积如表2所示。
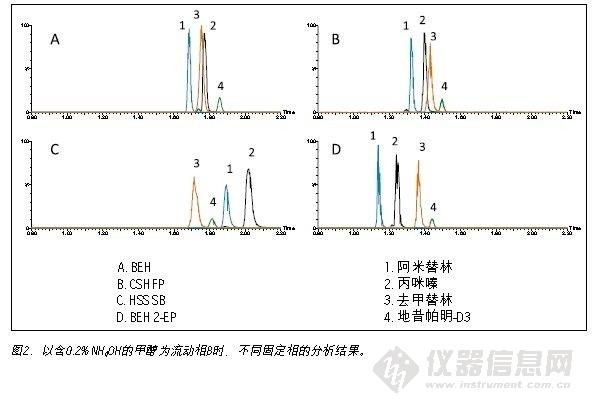
表2. 使用4种不同色谱柱所得的峰面积概览表。
系统性色谱筛选
方法开发过程对色谱柱、改性剂和改性添加剂进行了系统筛选,以获得最佳分离结果。经筛选的4种UPC2色谱柱如下:ACQUITY UPC2 BEH、BEH 2-EP、HSS C18 SB和 CSH™ Fluoro-Phenyl,所有色谱柱规格均为2.1×50 mm,填料粒径为1.7 μm。3种流动相B溶剂分别为甲醇、含0.2%甲酸的甲醇和含0.2% NH4OH的甲醇。筛选过程采用流动相B在3 min内从2%增加至45%,达到45%时保持1.5 min的常用梯度。当以添加有氢氧化铵的甲醇作流动相时,各色谱柱分析所得的峰形、灵敏度和分离度均为最佳。四种固定相使用此高pH流动相所得分析结果的对比情况如图2所示。除HSS SB色谱柱外,其它色谱柱的出峰顺序相似。但是,由HSS SB色谱柱得出的谱峰明显更宽,这将导致信噪比降低并影响低浓度样品的检测。峰变宽可能是由于分析物与固定相之间的次级相互作用所致。采用ACQUITY UPC2系统分析其它类化合物(本文未涉及此部分实验内容)时发现:使用具有缓冲作用的流动相改性剂(如,20至40 mM的甲酸铵)可以改善峰形。在本文的研究中,色谱分析的主要目标不是使分析物达到绝对的基线分离,而是获得最佳的峰形和最高灵敏度,因此我们对各色谱柱所得的峰面积进行了测定。在高pH改性剂条件下,使用各色谱柱得出的分析物峰面积如表2所示。

| BEH色谱柱 | BEH 2-EP色谱柱 |
HSS C SB色谱柱 18 |
CSH FP色谱柱 | |
| 阿米替林 | 1066581 | 940444 | 968946 | 940657 |
| 丙咪嗪 | 1291389 | 1180698 | 1690693 | 1145127 |
| 去甲替林 | 1586550 | 963422 | 1256074 | 1143857 |
| 地昔帕明 | 245922 | 149734 | 219268 | 208580 |
表2. 使用4种不同色谱柱所得的峰面积概览表。
在不同色谱柱的筛选实验中,阿米替林和丙咪嗪的峰面积无显著变化,但地昔帕明和去甲替林受固定相化学性质的影响,峰面积发生了明显改变。例如,地昔帕明在使用BEH色谱柱分析时所得峰面积较其它色谱柱增大了11%至40%。同样,去甲替林的峰面积在BEH色谱柱分析条件下较其它色谱柱增大了21%至40%。虽然BEH 2-EP色谱柱的总体分离效果较其它色谱柱稍有改善,但采用BEH色谱柱时信号强度更高。因此BEH色谱柱是进行TCA低浓度水平定量分析的最佳选择。
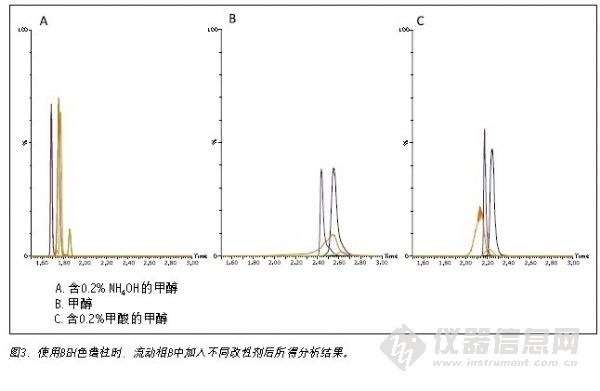
此外,BEH色谱柱所得色谱峰的平均基线峰宽<2 s,提高了低浓度样品测定的信噪比。运用各个色谱柱进行试验时观测到系统最大压力低于4200 psi,系统在此低于压力限值的条件下运行良好,可以灵活地根据需要提高流速,进一步缩短运行时间。除对固定相进行了筛选外,本实验还对不同的改性剂进行了评估。图3所示为不同流动相B改性
剂对ACQUITY UPC2 BEH色谱柱的影响,其它色谱柱受影响的趋势与此相似。使用NH4OH作为改性剂时常可获得最佳的分离度和峰形。单独用甲醇作流动相时,所得谱峰最宽,洗脱时间最迟,分离度最差。选择甲酸作为改性剂时,所得分析结果比使用NH4OH所得结果的保留时间增大,分离度降低且谱峰更宽。为缩短运行时间并提高样品分析通量,本实验对筛选梯度进行了“压缩”。结果表明,梯度压缩后所得峰形、分离度和灵敏度均未受负面影响。最终的整个运行时间确定为3 min。

灵敏度、线性和定量准确度
本实验还通过少量的研究对方法的准确度和线性进行了评估。使用浓度范围为0.1-10.0 ng/mL的对照人体尿液制备简化标准曲线(无内标物)。采用“实验”部分最后确定的分析条件进行测定,按照1/x的加权系数计算所得的曲线呈线性,R2>0.998,各标准曲线点理论浓度的平均偏差<8%。表3所示为阿米替林的典型标准曲线统计数据。对于所有分析物,0.1 ng/mL的LLOQ均可轻松实现。此浓度下,阿米替林、丙咪嗪、去甲替林和地昔帕明-D3的信噪比依次为334:1、292:1、590:1和66:1。各组分的信号强度是空白尿样提取物信号的5倍,符合FDA的LLOQ测定标
准。图4所示为0.1 ng/mL地昔帕明-D3和空白尿液的典型提取离子色谱图。
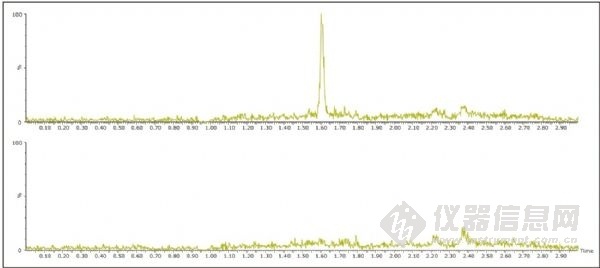
图4. 空白尿液提取物(下方色谱图)和含0.1 ng/mL地昔帕明-D3的尿液提取物(上方色谱图)。
表3. 阿米替林(从人体尿液中提取)的典型标准曲线统计数据。
结论

图4. 空白尿液提取物(下方色谱图)和含0.1 ng/mL地昔帕明-D3的尿液提取物(上方色谱图)。
| 标准溶液浓度(ng/mL) | 保留时间 | 峰面积 | 与理论值之间的偏差% | 准确度% |
| 0.1 | 1.48 | 16161 | -3.3 | 96.7 |
| 0.2 | 1.48 | 27061 | 2.7 | 102.7 |
| 0.5 | 1.48 | 60531 | 7.9 | 107.9 |
| 1.0 | 1.48 | 103149 | -3.6 | 96.4 |
| 5.0 | 1.48 | 467997 | -7.9 | 92.1 |
| 10.0 | 1.48 | 999886 | -0.9 | 99.1 |
结论
UPC2技术成功应用于人体尿液中TCA的分析和定量。主要参数的自动筛选功能为本研究组中的4种TCA提供了极
好的分离度和谱峰强度。对筛选出的梯度条件略作调整后,最终的总运行时间为3 min,尿液样品由Oasis WCX 96
孔μElution板进行提取处理。人体尿液中提取TCA的回收率范围为92%至104%。简化标准曲线溶液的浓度范围为0.1-10.0 ng/mL,曲线上各点呈线性分布,平均准确度为99%。各分析物的LLOQ均可达到0.1ng/mL,足以满足生物分析的要求。
总的来说,本应用纪要展现了UPC2 这种新型分离技术在生物分析这一重要应用领域中的实用性和应用优势。UPC2技术使用绿色环保的CO2 作为主要流动相、样品无需稀释或浓缩即可直接进样,另具公认的正交性(对反相色谱而言),使其在生物基质中药物的分析定量方面备受青睐。
参考文献
1. (a) Baker GB, Coutts RT, Holt A. Derivatization with acetic anhydride:Applications to the analysis of biogenic amines and psyc hiatric drugs by gas c hromatography and mass
spectrometry.Journal of Pharmacological and Toxicological Methods. 1994; 31(3):141-148. (b) Pujadas M, Pic hini S, Civit E, Santamariña E, Perez K, de la Torre R. A simple and reliable procedure for the determination of psyc hoactive drugs in oral fluid by gas c hromatography-mass spectrometry.Journal of Pharmaceutical and Biomedical Analysis. 2007; 44 (2): 594-601.
2. (a) Cantú M, Toso D, Lacerda C, Lanças F, Carrilho E, Queiroz M. Optimization of solidphase
microextraction procedures for the determination of tricyclic antidepressants
and anticonvulsants in plasma samples by liquid c hromatography.Analytical and
Bioanalytical Chemistry.2006; 386 (2): 256-263. (b) Frahnert C, Rao ML, Grasmäder
K. Analysis of eighteen antidepressants, four atypical antipsyc hotics and active
metabolites in serum by liquid c hromatography:a simple tool for therapeutic drug
monitoring.Journal of Chromatography B. 2003; 794 (1):35-47. (c) Hostette AL,
Stowe ZN, Cox M, Ritc hie JC.A Novel System for the Determination of Antidepressant
Concentrations in Human Breast Milk.T herapeutic Drug Monitoring.2004; 26(1): 47-
52. (d) Malfará W R, Bertucci C, Costa Queiroz ME, Dreossi Carvalho SA, de Lourdes
Pires Bianc hi M, Cesarino EJ, Crippa JA, Costa Queiroz RH.Reliable HPLC method
for therapeutic drug monitoring of frequently prescribed tricyclic and nontricyclic
antidepressants.Journal of Pharmaceutical and Biomedical Analysis.2007; 44(4):
955-962. (e) Ruiz-Angel MJ, Carda-Broc h S, Simó-Alfonso EF, Alvarez-Coque
MC.Optimized procedures for the reversed-phase liquid c hromatographic analysis
of formulations containing tricyclic antidepressants.Journal of Pharmaceutical and
Biomedical Analysis.2003; 32(1): 71-84. (f) T heurillat R, T hormann W. Monitoring
of tricyclic antidepressants in human serum and plasma by HPLC:c haracterization of
a simple, laboratory developed method via external quality assessment.Journal of
Pharmaceutical and Biomedical Analysis. 1998; 18(4-5): 751-760.
3. (a) Santos-Neto AJ, Bergquist, Lanças FM, Sjöberg PJ.Simultaneous analysis of five
antidepressant drugs using direct injection of biofluids in a capillary restrictedaccess
media-liquid c hromatography–tandem mass spectrometry system.Journal of
Chromatography A.2008; 1189(1-2):514-522. (b) Sauvage FL, Gaulier JM, Lac hâtre
G, Marquet P. A Fully Automated Turbulent- Flow Liquid C hromatography-Tandem Mass
Spectrometry Technique for Monitoring Antidepressants in Human Serum.T herapeutic
Drug Monitoring.2006; 28(1): 123-130. (c) Shinozuka T, Terada M, Tanaka E. Solidphase
extraction and analysis of 20 antidepressant drugs in human plasma by LC /MS
with SSI method.Forensic Science International.2006; 162(1-3): 108-112. (d) Titier
K, Castaing N, Le-Déodic M, Le-bars D, Moore N, Molimard M. Quantification of Tricyclic
Antidepressants and Monoamine Oxidase Inhibitors by High-Performance Liquid C
hromatography-Tandem Mass Spectrometry in W hole Blood.Journal of Analytical
Toxicology. 2007; 31(4): 200-207.
4. C hambers E, Wagrowski-Diehl DM, Lu Z, MazzeoJR.Systematic and comprehensive
strategy for reducing matrix effects in LC /MS/MS analyses.Journal of Chromatography
B. 2007; 852(1-2): 22-34.
最新动态
更多![]()
Xevo MRT新应用 | 火眼金睛,让PFAS无处遁形
厂商
2024.08.26
Arc GPC体验:PEO/PEG的SEC分析
厂商
2024.08.26
UPLC二十周年大咖说 | UPLC技术应用于复杂组分的分离分析
厂商
2024.08.26
“悟空”出马,PFAS无处遁形:Xevo MRT智斗污染妖魔
百态
2024.08.22
推荐产品
供应产品










