请问安捷伦[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]采用什么柱子检测食醋中含氮化合物如:四甲基吡嗪;2,3-二甲基吡嗪等吡嗪类化合物?
最近做一个三嗪二酮类化合物的检测,总有一个杂质峰不稳定,怀疑发生了烯醇互变,请教大家有没有什么好的[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]方法检测类似化合物的
有没有大神做车内空气全谱分析或者车内硫类和胺类化合物测试的??而且是用热脱附GCMS做的??想咨询这方面的问题,私信我,有偿咨询!!!
有没有人用HP-17的柱子做酚类化合物的
各位大神酚类化合物前处理都怎么做的?索氏提取器坐土壤中的酚类化合物条件是多少合适?HJ703-2014这个标准,净化那一步怎么我做的有机相在上层,标准是说在下层,求指点,最好能细致点的
各位大侠,大家做过酚类化合物吗?我的标准曲线做不出来,求救了!你们的标准曲线是什么样的?
在实际工作中我们会遇到这类化合物如,对甲基环己甲酸,对乙基环己甲酸等等,这类化合物都存在异构体,感兴趣的朋友,请交流下这类化合物分析的心得!
固体污染源排气中酚类化合物的测定四氨基安替比林分光光度法中做标准曲线时为什么吸光值会越来越小,请各位同仁前辈解惑
山葡萄酒中多酚类化合物酚类化合物是葡萄酒中的重要生理活性物质,对人体的健康起着重要保健作用。山葡萄酒中的多酚类化合物主要有:花色苷:是一种红色素化合物,有花青素、甲基花青素、牵牛花素、锦葵花素、花翠素、芍药素、栎皮黄素等,其含量是一般葡萄酒的2倍。黄酮类:是一种黄色素化合物,有堪非醇、槲皮素、山奈酚、杨梅素等,其黄铜醇的含量为1.43g/L,是一般葡萄酒的5~10倍。儿茶素类:主要有儿茶素、表儿茶素、表没食子儿茶素等,具有一定的苔味。原花色素类:主要有原花青素、原花翠素、原天竺葵素等。是葡萄籽与皮的主要成份,也是葡萄酒中多酚类化合物含量最多的一类。单宁类:是由花白素的多聚体组成的,有一定的涩味,具有重要的生理功能。山葡萄酒中单宁的含量是一般葡萄酒的2~3倍。白藜芦醇化合物:主要有顺式白藜芦醇、反式白藜芦醇、顺式白藜芦醇糖苷、反式白藜芦醇糖苷、顺式反式白藜芦醇异构体等。这些化合物主要来源于葡萄皮、籽中,是植物体具抗病毒的生理活性物质,也是对人体防治心脑血管疾病的重要药理成份。山葡萄酒中白藜芦醇的含量为5.86~8.20mg/L,高于国际标准,是一般葡萄酒的4~6倍。多酚类化合物是重要的保健功能成份,主要来源葡萄皮、籽中,因此吃葡萄带皮、籽一起吃掉是最有益身体健康的。酶类化合物:主要有超氧化物岐化酶(SOD),是一种自由基清除剂,具有破坏活性氧作用的自卫酶类化合物。山葡萄酒中含量为1.52×104—1.84×104mg/L,虽然含量极微小,但对人体健康有重要作用,也是其它葡萄中不具备的。
请教一下用紫外分光光度法测白油中的芳烃含量(NB/SH/0966-2017)中的标样c10~C13萘类化合物和C10-C20烷基苯类化合物哪里有卖吗?哪里能买到?C10~C13萘类化合物在285nm波长下的平均吸光系数33.7L/(g.cm)在270nm附近的平均吸光系数30.0L/(g.cm)C10~C20烷基苯类化合物在270nm附近的平均吸光系数3.01L/(g.cm),知道的朋友麻烦告知一下,好吗?谢谢
酚类化合物怎么做啊,我的为什么没有橙红色,是黄色。而且我试了一下,不加缓冲溶液,只加标液,显色剂,是橙红色。什么原因?[img]https://ng1.17img.cn/bbsfiles/images/2019/04/201904101027496813_99_3494685_3.png[/img]
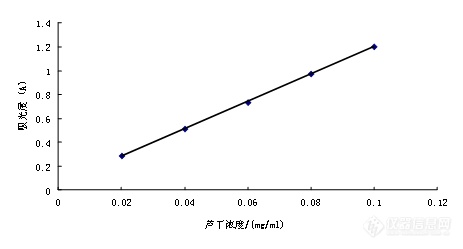
[align=center]从黄芩中提取黄酮类化合物的工艺研究[/align][align=center]西安国联质量检测技术股份有限公司[/align][align=center]食品事业部:李灿[/align][b]摘要:[/b]探讨超声波辅助法提取黄芩中总黄酮的最佳提取条件及对提取物的抗氧化性活性研究,这为黄芩作为天然抗氧化剂和功能性食品的开发利用提供理论基础和实验依据。[b][/b] 通过设计正交试验,采用超声波辅助法提取黄芩中总黄酮的最佳工艺条件条件,并通过对羟自由基、超氧自由基和DPPH自由基的清除效果研究其抗氧化活性。[b][/b]超声波辅助提取黄芩中总黄酮的最佳条件为:乙醇浓度为50%,时间为25min,料液比为1∶10,温度为30℃,黄芩总黄酮的提取率为3.25%。并且研究了黄芩提取物中的黄酮类物质对O[sub]2[/sub]-• 、• OH和DPPH自由基的抗氧化性能。研究结果表明洋葱提取物中黄酮类物质的抗氧化性较VC强。在浓度为0.0125mg/ml下,对羟基自由基的清除率为88.30%,对超氧基自由基的清除率为90.01%,对DPPH自由基的清除率为93.87%。[b]关键词[/b]:黄芩;超声波提取;总黄酮;抗氧化活性 [align=center][b] Study on extraction technology of flavonoids from Scutellaria[/b][/align][align=center]Li Can[/align][align=center] (Department of Chemistry and Chemical Engineering, Xi′an University of [/align][align=center]Arts and Science, Xi′an 710065)[/align][b]Abstract: [/b]To investigate the ultrasonic assisted extraction optimum extraction conditions of total flavonoids from Scutellaria and to extract antioxidant activity, which is a skullcap as a natural antioxidant and functional food development and utilization of theoretical and experimental evidence provided . [b][/b] Through orthogonal experiment, the optimum conditions using ultrasonic assisted extraction conditions of total flavonoids from Scutellaria, and to study its antioxidant activity by hydroxyl radicals, superoxide radicals and DPPH radical scavenging effect. Optimal conditions . [b] [/b]Ultrasonic assisted extraction of total flavonoids from Scutellaria: ethanol concentration of 50%, the time is 25min, solid-liquid ratio of 1:10, the temperature is 30 ℃, extraction of total flavonoids was 3.25%. And studied the extract of Scutellaria flavonoids on O2-• , • OH and DPPH radical antioxidant properties. The results show that the onion extract antioxidant flavonoids than VC strong. At a concentration of under 0.0125mg/ml, hydroxyl radical scavenging rate of 88.30% for super-group was 90.01% scavenging of DPPH radical scavenging rate was 93.87%.[b][color=#2b2b2b]Key Words[/color][/b][color=#2b2b2b]:[/color][color=#2b2b2b] [/color][color=#2b2b2b]Skullcap [/color][color=#2b2b2b]U[/color][color=#2b2b2b]ltrasonic extraction [/color][color=#2b2b2b]T[/color][color=#2b2b2b]otal flavonoids [/color][color=#2b2b2b]A[/color][color=#2b2b2b]ntioxidant activity[/color][b]1 前言[/b]黄岑主要生长在陕西秦岭,为常用中草药之一,性寒,味苦。具有清热燥湿,泻火解毒,止血安胎[sup][/sup]等功效,它的主要成分为黄酮类化合物[sup][/sup],黄酮类化合物主要存在于双子叶及裸子植物的叶、果、实、根、皮中,在植物中主要与糖结合成苷的形式存在[sup][/sup]。目前从黄酮类物质有很多种,黄酮类化合物的结构特点是具有 C[sub]6[/sub]- C[sub]3[/sub]- C[sub]6[/sub]的基本骨架,根据中间三碳链的氧化程度、B 环( 苯基) 连接位置( 2-或3-位) 以及三碳链是否呈环状等特点,主要有黄酮醇,二氢黄酮,二氢黄酮醇,黄烷,黄烷醇,异黄酮等,被广泛应用在医药、功能食品添加剂、兽药和农药等领域。在医药方面,根据其在心血管系统、内分泌系统、抗肿瘤方面的药理作用,很多以黄酮类成分为主的制剂已作为成药上市[sup][/sup]。在食品中它们应用于功能性食品添加剂,如天然甜味剂、天然抗氧化剂、天然色素等;应用于功能食品,如生物类黄酮口香糖、银杏叶袋泡茶等防衰、抗癌、提高免疫力食品;在兽药、农药等领域,现已开发出些具有特效功能的含有黄酮类化合物药品和驱虫、杀虫剂等[sup][/sup]。目前国内侧重于对黄酮类化合物的研究,但他们常被当作残渣而扔掉,因而就造成了黄芩的浪费,没有使黄芩得到充分利用,本文主要针对黄芩总黄酮的提取方法及其抗氧化能力测定方法进行研究,以期为黄芩黄酮类成分的进一步开发利用从黄岑中提取黄酮类化合物的方法有很多种,传统提取方法有煎煮法[sup][/sup]、有机溶剂提取法[sup][/sup]、浸渍法、渗漉法、回流提取法[sup][/sup]、水提法等,新的提取方法有超声波提取法、微波提取法、索氏提取法、超临界萃取法、大孔树脂吸附法、酶解法提取[sup][/sup]。黄芩黄酮的提取主要为溶剂萃取法,包括无机溶剂萃取法和有机溶剂萃取法。其主要原理是利用黄芩黄酮能溶于碱水或甲醇等有机溶剂的特性来提取黄芩中的黄酮[sup][/sup],考虑到该法提取时间长,提取率较低的缺点,我们采用超声波辅助提取法。因为超声波提取法是一种新型方法,它具有能耗低、效率高、不破坏有效成分的特点,在低温下可以强化水浸提效率,达到省时高效节能的目的,而且是目前广泛使用的方法。超声提取的主要理论依据是超声的空化效应、热效应和机械作用。当大能量的超声波作用于介质时,介质被撕裂成许多小空穴,这些小空穴瞬时闭合,并产生高达几千个大气压的瞬间压力,即空化现象。超声空化中微小气泡的爆裂会产生极大的压力,使植物细胞壁及整个生物体的破裂在瞬间完成,缩短了破碎时间,同时超声波产生的振动作用加强了胞内物质的释放、扩散和溶解,从而显著提高提取效率。因此本实验拟决定用超声波提取法来提取黄酮类化合物。黄酮类化合物的测定方法也多种多样,目前有薄层扫描法、紫外分光光度法、液相色谱法等[sup][/sup]。但是以上方法测定黄芩提取液中总黄酮的含量都比较繁琐,非黄酮类物质干扰比较大。由于Al[sup]3+[/sup]仅与黄酮类物质有特征反应,使用这种显色方法可以使黄酮类化合物溶液在510nm左右出现吸收峰,采用紫外分光光度法测定黄芩提取液中总黄酮含量,方法简单快速[sup][/sup]。对于黄酮类化合物的抗氧化性研究,国内外所做研究也比较多。方法可分为体外抗氧化与体内抗氧化,其中体外抗氧化运用较为广泛,体外抗氧化还可分为直接清除活性氧自由基、抑制油脂过氧化反应[sup][/sup]等;体内抗氧化是用受试物连续喂饲大鼠或小鼠1个月~3个月,然后处死动物,测定其血或组织(如肝、脑)中各物质的含量,同对照组进行比较,间接地说明受试物的抗氧化活性。采用体外抗氧化性研究,常用到的自由基有OH[sup] [/sup],O[sub]2[/sub][sup]-[/sup], DPPH等,由于直接清除活性自由基的方法易行且效果直观,本次实验采用该种方法。本实验将从两个方面研究黄芩黄酮类化合物。第一部分为黄芩总黄酮最佳提取方法的研究。本环节采取超声辅助提取法,采用料液比(A),乙醇浓度(B), 超声时间(C),超声温度(D)作为研究因素,采用四因素三水平,选择L[sub]9[/sub](3[sup]4[/sup])设计正交试验。用芦丁做标准曲线测定黄芩提取液中总黄酮的含量。第二部分为总黄酮类化合物抗氧化性的研究,采用对OH,O[sub]2[/sub][sup]-[/sup]自由基和DPPH自由基的清除作用研究其抗氧化性。[b]2 实验部分2.1 材料与仪器2.1.1 材料和试剂[/b] 黄芩(购于西安同仁堂大药房),芦丁(分析纯,上海试剂药品厂),亚硝酸钠(分析纯,成都市科龙化工试剂厂),硝酸铝(分析纯,成都市科龙化工试剂厂),氢氧化钠(分析纯,成都市科龙化工试剂厂),邻苯三酚(分析纯,成都市科龙化工试剂厂),盐酸(分析纯,天津市天力化学试剂有限公司),双氧水(天津市天力化学试剂有限公司),硫酸亚铁(分析纯,成都市科龙化工试剂厂),水杨酸(分析纯,天津市天力化学试剂有限公司),无水乙醇(分析纯,天津市天力化学试剂有限公司),三羟基甲基氨基甲烷(分析纯,天津市福晨化学试剂厂),邻二氮菲(分析纯,天津市福晨化学试剂厂),DPPH(购于阿拉丁试剂)。[b]2.1.2 仪器[/b] 高速粉碎机(FW80型,北京中兴伟业仪器有限公司);紫外可见分光光度计(722N,上海精密科学仪器有限公司) 电子天平(YP202W,上海精密科学仪器有限公司);循环水式多用真空泵(SHB-Ⅲ,郑州长城科工贸有限公司);超声波清洗机(11—1404,宁波新芝生物科技股份有限公司);智能型恒温鼓风干燥箱(CMD-20X型,上海琅轩试验设备有限公司);玻璃仪器气流烘干器(TH48SYBQ-1型,北京中兴伟业仪器有限公司)。[b]2.2实验方法2.2.1黄芩样品的制备[/b] 将黄芩在烘箱中60℃干燥8h,干燥后的黄芩用粉碎机粉碎成粉末,用分样筛(40目)筛分黄芩粉末,保证粉末均匀一致,密封保存,待用。[b]2.2.2 总黄酮的测定方法2.2.2.1 芦丁标准曲线的绘制[/b] 准确称取干燥至恒重的芦丁4.0mg 于小烧杯中,用50%乙醇溶解,并定容于25ml的容量瓶,摇匀,得浓度0.16mg/ml的标准液。准确吸取标准应用液0、1.0、2.0、3.0、4.0、5.0ml 于6 个10ml容量瓶中,与上述容量瓶中分别加入5% NaNO[sub]2[/sub]0.3ml,摇匀,放置6min后,分别加入10% Al(NO[sub]3[/sub])[sub]3[/sub] 溶液0.3ml,摇匀,放置6min后,再分别加入4% NaOH 溶液4ml,加50%乙醇定容至10ml,摇匀,以试剂空白为参比,放置10~15min,用紫外可见分光光度计进行全波长扫描,在最大吸收波长510nm处测定吸光度,得到吸光度Y与芦丁浓度X(mg/ml)间标准曲线回归方程。[b]2.2.2.2 提取液总黄酮含量的测定 [/b]准确称取1.00g黄芩粉末,在不同的提取条件下提取黄芩总黄酮,提取液用乙醇稀释定容至50ml。准确吸取提取液1.0ml于25ml容量瓶,按上述方法显色后测定吸光度,代入标准曲线回归方程中可以得到黄芩中黄酮类物质的含量(mg/ml),从而计算出黄芩中黄酮类物质的提取率,即:黄芩中黄酮类物质的提取率= ×100%[b]2.2.3 单因素试验[/b] 主要研究料液比、乙醇浓度、超声波时间、超声波温度4个因素,在保持其他因素相同的条件下分别进行单因素试验,研究各因素对黄芩总黄酮提取效果的影响,筛选最佳的提取条件。 准确称取黄芩粉末,在不同的条件下进行超声提取,提取液冷却后用乙醇定容,按照2.2.2的测定方法,计算黄芩中总黄酮的含量。[b]2.2.4 正交试验[/b]在单因素试验基础上,选择料液比、乙醇浓度、超声时间、超声温度4因素,设计L[sub]9[/sub](3[sup]4[/sup])正交试验,以总黄酮的含量为评价指标,确定黄芩总黄酮超声辅助法的最佳提取工艺。[b]2.2.5 总黄酮体外抗氧化性的研究2.2.5.1 对羟自由基清除作用的研究[sup][/sup][/b]原理:通过反应所产生的羟基自由基可将Fe[sup]2+[/sup]氧化为Fe[sup]3+[/sup], Fe[sup]2+[/sup]和邻二氮菲反应可产生有色络合物,向有色沉淀加入抗氧化剂后,其反应效果会相对减弱。羟基自由基对二价铁离子的氧化作用,会导致吸光值不断变化,从而评价样液消除羟基自由基的能力。步骤:取0.75 mmoL/L邻二氮菲溶液1 mL,加入不同浓度的样液,再加0.75 mmoL/L硫酸亚铁1 mL混匀,加0.75mmol/l的过氧化氢1 mL,于37 ℃ 水浴下,水浴60 min后,在536 nm处测其吸光度,所得吸光度A[sub]b[/sub]。 反应方程式:H[sub]2[/sub]O[sub]2[/sub] + Fe[sup]2+[/sup]=OH[sup]-[/sup] +OH + Fe[sup]3+ [/sup]清除率S(%)=「Ax- A[sub]b[/sub]]/[As- A[sub]b[/sub]] ×100% 其中 A[sub]b[/sub]:标准体系的吸光度 Ax:不含黄芩提取液的吸光度As:不含过氧化氢的标准体系吸光度本底吸光度[b]2.2.5.2 对超氧自由基清除作用的研究 [sup][/sup][/b] 原理:在碱性条件下,邻苯三酚能迅速发生自氧化反应,生成超氧阴离子自由和有色中间产物,且邻苯三酚自氧化速率与生成超氧阴离子自由基的浓度呈正相关,该有色中间产物在300nm处有一特征吸收峰。当加入抗氧化剂能催化超氧阴离子自由基与H[sup]+[/sup]结合生成O[sub]2[/sub]和H[sub]2[/sub]O[sub]2[/sub] ,从而阻止了中间有色产物积累,溶液在320nm 处的吸收减弱。因此可通过测定添加试样前后吸光度[i]A[/i]的变化来表示抗氧化剂对超氧阴离子自由基的清除效果。步骤:取0.05mol/L三羟甲基氨基甲烷盐酸缓冲液(pH =8.2)4.5mL,置于25℃水浴中预热20min,分别加入0.1mL试样和0.4mL2.5mmol/L邻苯三酚溶液,混匀后于25℃水浴中反应4min,加入8mol/L HCl溶液两滴终止反应,于波长299nm处测定吸光度As,空白对照组以相同体积的蒸馏水代替样品,并计算清除率。 清除率计算公式: S(%)=[(1-(As-A[sub]0[/sub] )/A[sub]b[/sub]]×100%其中 A[sub]b[/sub]:不含黄芩提取物的标准体系吸光度 As:标准体系的吸光度值 Ao:不含邻苯三酚的标准体系吸光度[b]2.2.5.3 对DPPH自由基清除作用的研究[sup][/sup] [/b]原理:DPPH 在有机溶液中是一种稳定的自由基,其乙醇溶液呈深紫色,当 DPPH 溶液中加入自由基清除剂时,其孤对电子被配对,溶液颜色变浅,可由此来检测自由基的清楚状况,从而评价物质的抗氧化能力。步骤:将样品储备液适当稀释得到不同浓度的黄芩黄酮溶液。 向一系列 10 mL比色管中加入 3.5 mL 1.0×10[sup]-4[/sup]mol/L 的 DPPH 溶液和 0.5 mL 样品液,摇匀避光反应30 min,与波长517 nm下测定吸光度 A s。空白对照组以无水乙醇代替样品,并计算清除率。清除率计算公式: 清除率S(%)=[(1-(As-A[sub]0[/sub] )/A[sub]b[/sub]]×100% 其中 A[sub]b[/sub]:不含黄芩提取物的标准体系吸光度 A[sub]s[/sub]:标准体系的吸光度值 A[sub]0[/sub]:不含DPPH的标准体系吸光度[b]3. 结果与分析 3.1 芦丁标准曲线[/b]由图可得,芦丁在0.02—0.10mg/ml浓度范围内与吸光度呈良好的线性关系,R[sup]2[/sup]= 0.9998。回归方程为Y= 11.47X+ 0.0554 [align=center]表1 芦丁浓度与吸光度的关系[/align][table][tr][td][align=center]序号[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][/tr][tr][td][align=center]芦丁浓度/(mg/ml)[/align][/td][td][align=center]0.02[/align][/td][td][align=center]0.04[/align][/td][td][align=center]0.06[/align][/td][td][align=center]0.08[/align][/td][td][align=center]0.10[/align][/td][/tr][tr][td][align=center]吸光度(A)[/align][/td][td][align=center]0.288[/align][/td][td][align=center]0.514[/align][/td][td][align=center]0.736[/align][/td][td][align=center]0.976[/align][/td][td][align=center]1.204[/align][/td][/tr][/table][align=center] [/align][align=center] [/align][align=center] [/align][align=center][img=,463,249]http://ng1.17img.cn/bbsfiles/images/2018/07/201807091813421003_7187_2904018_3.png!w463x249.jpg[/img] [/align][align=center]图1 芦丁标准曲[/align]Fig.1 Standard curve of rutin[b]3.2 总黄酮提取条件的优化3.2.1 料液比对黄酮类化合物提取效果的影响[/b]在料液比为1:6,1:8,1:10,1:12,1:14时,50%乙醇作为提取剂,超声波时间为20min,超声波温度为60℃,冷却后采用超声波提取法提取黄芩中黄酮类化合物含量,研究料液比对提取效果的影响。[align=center]表2 料液比与提取率的关系[/align][align=center][img=,394,250]http://ng1.17img.cn/bbsfiles/images/2018/07/201807091815178933_5515_2904018_3.png!w394x250.jpg[/img][/align][align=center] 图2 料液比对黄芩黄酮提取的影响[/align][align=center]Fig.2 Solid-liquid ratio on the extraction of flavonoids from Scutellaria impact[/align]由图2可见,随着料液比的增加,黄酮类化合物的提取率也逐渐升高,当料液比为1:10时,黄酮类化合物的提取率达到最高值,继续增加料液比,提取率会有一定的降低。在一定范围内料液比的增加有利于物料中黄酮类物质的溶出,但料液比过大的时候,会导致溶液浓度太小,从而影响到黄酮类物质对超声波能的吸收,导致黄酮得率下降。因此选定料液比在1:10的条件下进行实验。[b]3.2.2 乙醇浓度对黄酮类化合物提取效果的影响[/b]当乙醇浓度为30%,40%,50%,60%,70%时作为提取剂,超声波时间为20min,超声波温度为60℃,料液比为1:10的条件下,冷却后采用超声波提取法提取液中总黄酮含量,研究料液比对提取效果的影响。结果如图2所示[align=center]表3 乙醇浓度与提取率的关系[/align][table][tr][td][align=center]序号[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][/tr][tr][td][align=center]乙醇浓度(%)[/align][/td][td][align=center]30[/align][/td][td][align=center]40[/align][/td][td][align=center]50[/align][/td][td][align=center]60[/align][/td][td][align=center]70[/align][/td][/tr][tr][td][align=center]提取率(%)[/align][/td][td][align=center]2.08[/align][/td][td][align=center]2.44[/align][/td][td][align=center]3.18[/align][/td][td][align=center]2.15[/align][/td][td][align=center]1.28[/align][/td][/tr][/table][align=center][img=,457,289]http://ng1.17img.cn/bbsfiles/images/2018/07/201807091815413326_3128_2904018_3.png!w457x289.jpg[/img][/align]图3 乙醇浓度对黄芩总黄酮提取的影响[align=center] Fig.3 The effect of ethanol concentration on the extraction of flavonoids from Scutellaria[/align]由图3可见,随着乙醇浓度的增加,黄酮类化合物的提取率逐渐升高,在乙醇浓度为50%时提取率最高,再增加乙醇浓度,提取率逐渐降低。这主要是随着乙醇浓度的增加导致溶液极性的改变,使提取液中杂质含量增加,因此选择50%的乙醇溶液作为提取剂。[b]3.2.3 超声波时间对黄酮类化合物提取效果的影响[/b]当超声波时间为5min,10min,15min,20min,25min,料液比为1:10,乙醇浓度为50%,超声波温度为60℃的条件下,冷却后采用超声波提取法提取液中总黄酮含量,研究料液比对提取效果的影响。[align=center]表4 超声波时间与提取率的关系[/align][table][tr][td][align=center]序号[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][/tr][tr][td][align=center]超声波时间(min)[/align][/td][td][align=center]5[/align][/td][td][align=center]10[/align][/td][td][align=center]15[/align][/td][td][align=center]20[/align][/td][td][align=center]25[/align][/td][/tr][tr][td][align=center]提取率(%)[/align][/td][td][align=center]1.67[/align][/td][td][align=center]1.82[/align][/td][td][align=center]1.93[/align][/td][td][align=center]2.19[/align][/td][td][align=center]2.08[/align][/td][/tr][/table][align=center][img=,420,258]http://ng1.17img.cn/bbsfiles/images/2018/07/201807091815572952_9256_2904018_3.png!w420x258.jpg[/img][/align]图4 超声时间对黄芩总黄酮提取的影响[align=center]Fig.4 Ultrasonic time of total flavonoids extracted[/align]由图4可见,随着超声波时间的延长,黄酮类化合物提取率逐渐升高,在20min时提取率最高,继续延长超声波提取时间提取率几乎不变,主要是因为在初期,黄芩中黄酮类化合物没有完全浸提到溶剂中,而随着时间的增加,黄酮类化合物逐渐完全溶于提取剂中,因此提取率几乎不变。所以选择超声波时间为20min时进行实验。[b]3.2.4 超声波温度对黄酮类化合物提取效果的影响[/b]当超声波温度为20℃,30℃,40℃,50℃,60℃,料液比为1:10,乙醇浓度为50%,超声波时间为20min的条件下,冷却后采用超声波提取法提取液中总黄酮含,研究料液比对提取效果的影响。[align=center]表5 超声波温度与提取率的关系[/align][table][tr][td][align=center]序号[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][/tr][tr][td][align=center]超声波温度(℃)[/align][/td][td][align=center]20[/align][/td][td][align=center]30[/align][/td][td][align=center]40[/align][/td][td][align=center]50[/align][/td][td][align=center]60[/align][/td][/tr][tr][td][align=center]提取率(%)[/align][/td][td][align=center]1.87[/align][/td][td][align=center]2.34[/align][/td][td][align=center]2.44[/align][/td][td][align=center]2.25[/align][/td][td][align=center]2.31[color=#ff0000] [/color][/align][/td][/tr][/table][align=center][img=,360,256]http://ng1.17img.cn/bbsfiles/images/2018/07/201807091816171242_5784_2904018_3.png!w360x256.jpg[/img][/align][align=center] [/align][align=center] [/align]图5 超声温度对黄芩黄酮提取的影响[align=center]Fig.5 Skullcap ultrasonic extraction temperature on impact[/align] 由图5可见,随着超声波温度的升高,黄酮类化合物提取率逐渐升高,在40℃时提取率最高,继续升高超声波提取温度,提取率反而略有下降。高温提取的过程是先使物料升温,保持一定时间后,利用温度使细胞壁破碎,乙醇溶剂溶入细胞内部,黄酮充分溶解,再继续升高温度,反而使更多的杂质释放出来,导致黄酮提取率不再上升。所以选择超声波温度为40℃进行实验。[b]3.3 正交试验确定最佳工艺3.3.1 正交试验结果[/b]通过上述单因素试验,得出各个单因素的最佳条件,其中料液比为1:10,乙醇浓度为50%,超声时间为20min,超声温度为40℃。选择料液比、乙醇浓度、超声波时间、超声波温度4因素3水平,设计L[sub]9[/sub](3[sup]4[/sup])正交试验,因素与水平见表1,试验结果见表2为了进一步判断上述4类因素对试验结果的影响是否存在,将以正交试验数据进行方差分析,找出这些因素中起主导作用的来源。表1 正交试验因素及水平表Tab 1 Factors and levels of the orthogonal tests[table][tr][td=1,2]水平[/td][td] 因素[/td][/tr][tr][td]A B C D料液比(g/ml) 乙醇浓度(%) 超声时间(s) 超声温度(℃)[/td][/tr][tr][td=2,1]1 1:8 40 15 302 1:10 50 20 403 1:12 60 25 50[/td][/tr][/table]表2 正交试验结果及分析 Tab 2 The results and analysis of orthogonal tests [table][tr][td=1,2]试验号[/td][td] 因素[/td][td=1,2]提取量(%)[/td][/tr][tr][td]A B C D料液比(g/ml) 乙醇浓度(%) 超声时间(s) 超声温度(℃)[/td][/tr][tr][td=3,1]1 1:8 40 15 30 2.622 1:8 50 20 40 2.903 1:8 60 25 50 2.764 1:10 50 25 30 3.255 1:10 60 15 40 2.626 1:10 40 20 50 2.507 1:12 60 20 30 2.408 1:12 40 25 40 2.589 1:12 50 15 50 2.85K[sub]1[/sub]/3 2.76 2.57 2.70 2.76K[sub]2[/sub]/3 2.79 3.00 2.60 2.70K[sub]3[/sub]/3 2.61 2.59 2.86 2.70R 0.18 0.43 0.26 0.06[/td][/tr][/table]由表1、2可知,主次因素由极差大小确定:B>C>A>D,即影响黄芩总黄酮提取效率的因素贡献率为乙醇浓度>超声时间>料液比>超声温度。以总黄酮含量为评价指标,得最佳提取工艺条件为A[sub]2[/sub]B[sub]2[/sub]C[sub]3[/sub] D[sub]1[/sub],即乙醇浓度为50%、超声时间为25min、料液比为1∶10、超声温度为30℃。最佳条件为正交表中的第四组,因此测抗氧化性实验选择此组数据。[b]3.4 总黄酮的抗氧化性3.4.1 对羟自由基的清除作用[/b][align=center]表6 提取液浓度对羟基自由基清除率[/align][table][tr][td][align=center]序号[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][/tr][tr][td][align=center]提取液浓度/(mg/ml)[/align][/td][td][align=center]0.0025[/align][/td][td][align=center]0.0050[/align][/td][td][align=center]0.0075[/align][/td][td][align=center]0.0100[/align][/td][td][align=center]0.0125[/align][/td][/tr][tr][td][align=center]VC清除率(%)[/align][/td][td][align=center]20.54[/align][/td][td][align=center]42.88[/align][/td][td][align=center]59.39[/align][/td][td][align=center]74.44[/align][/td][td][align=center]79.09[/align][/td][/tr][tr][td][align=center]黄酮清除率(%)[/align][/td][td][align=center]40.39[/align][/td][td][align=center]67.21[/align][/td][td][align=center]78.42[/align][/td][td][align=center]85.29[/align][/td][td][align=center]88.30[/align][/td][/tr][/table][align=center][img=,360,256]http://ng1.17img.cn/bbsfiles/images/2018/07/201807091816376703_5430_2904018_3.png!w360x256.jpg[/img][/align]图6 黄芩总黄酮对羟自由基的清除Fig.6 Scutellaria Flavonoids on Scavenging of Hydroxyl Radicals黄芩总黄酮对羟自由基的清除作用,结果见图6。由图6可知,黄芩总黄酮对羟基自由基具有一定的清除作用。在相同的浓度范围下,清除能力大小为:提取物VC溶液。在0.0025—0.0125mg/ml浓度下,各溶液的清除能力都随浓度的增大而增大。当提取液浓度为0.0125mg/ml下,黄芩提取液的清除率达到了88.30%。3.4.2 [b]对超氧自由基的清除作用[/b][align=center]表7 提取液浓度对超氧基自由基清除率[/align][table][tr][td][align=center]序号[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][/tr][tr][td][align=center]提取液浓度/(mg/ml)[/align][/td][td][align=center]0.0025[/align][/td][td][align=center]0.0050[/align][/td][td][align=center]0.0075[/align][/td][td][align=center]0.0100[/align][/td][td][align=center]0.0125[/align][/td][/tr][tr][td][align=center]VC清除率(%)[/align][/td][td][align=center]26.77[/align][/td][td][align=center]43.09[/align][/td][td][align=center]61.73[/align][/td][td][align=center]78.69[/align][/td][td][align=center]80.20[/align][/td][/tr][tr][td][align=center]黄酮清除率(%)[/align][/td][td][align=center]49.81[/align][/td][td][align=center]75.29[/align][/td][td][align=center]84.38[/align][/td][td][align=center]89.21[/align][/td][td][align=center]90.01[/align][/td][/tr][/table]黄芩总黄酮对超氧自由基的清除作用,结果见图7。由图7可知,黄芩总黄酮对邻苯三酚自氧化产生的超氧自由基有一定的清除作用,其清除率随浓度的增大而增大。在相同的浓度范围下,清除能力大小为:提取物VC溶液。各溶液的清除能力都随浓度的增大而增大。当提取液浓度为0.0125mg/ml下,黄芩提取液的清除率达到了90.01%。3.4.3 [b]对DPPH自由基的清除作用[/b][align=center]表8 提取液浓度对DPPH自由基清除率[/align][table][tr][td][align=center]序号[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][/tr][tr][td][align=center]提取液浓度/(mg/ml)[/align][/td][td][align=center]0.0025[/align][/td][td][align=center]0.0050[/align][/td][td][align=center]0.0075[/align][/td][td][align=center]0.0100[/align][/td][td][align=center]0.0125[/align][/td][/tr][tr][td][align=center]Vc清除率(%)[/align][/td][td][align=center]27.36[/align][/td][td][align=center]52.41[/align][/td][td][align=center]79.98[/align][/td][td][align=center]80.49[/align][/td][td][align=center]81.31[/align][/td][/tr][tr][td][align=center]黄酮清除率(%)[/align][/td][td][align=center]55.7[/align][/td][td][align=center]82.3[/align][/td][td][align=center]89.78[/align][/td][td][align=center]93.74[/align][/td][td][align=center]93.81[/align][/td][/tr][/table][b] [/b]黄芩总黄酮对DPPH的清除作用,结果见图8。由图8可知,黄芩总黄酮对DPPH有一定的清除作用,其清除率随浓度的增大而增大。相同的浓度范围下,清除能力大小为:提取物VC溶液。各溶液的清除能力都随浓度的增大而增大。当提取液浓度为0.0125mg/ml下,黄芩提取液的清除率达到了93.81%。[b]4.总结[/b]1.通过单因素实验,得出各个单因素的最佳条件,其中料液比为1:10,乙醇浓度为50%,超声时间为20min,超声温度为40℃,为正交试验奠定了基础。然后用设计正交试验,确定了超声辅助法提取黄芩总黄酮的最佳工艺条件:乙醇浓度为50%、超声时间为25min、料液比为1∶10、超声温度为30℃。黄芩总黄酮的提取率为3.25%。2.本实验分别就黄芩提取物对羟基自由基,超氧阴离子自由基和DPPH自由基的抗氧化性进行了测定,并与VC进行了对比实验,得到如下结论:在0.0025—0.0125mg/ml浓度下,提取物对各自由基清除能力为:DPPH O[sub]2[/sub][sup]-[/sup]• • OH ,同浓度黄芩提取物清除能力普遍高于VC溶液,黄芩黄酮提取液和VC溶液对自由基清除率随其浓度的增大而增大。在浓度为0.0125mg/ml下,对羟基自由基的清除率为88.30%,对超氧基自由基的清除率为90.01%,对DPPH自由基的清除率为93.87%,由此可知黄芩总黄酮是一种天然有效的自由基清除剂。黄芩中黄酮类化合物的利用已经有一定的规模,但黄芩中黄酮化合物的提取方法和工艺尚未成熟,所以充分利用黄芩资源是我国药用研究的科学发展方向。基于提取率、成本等因素的影响,通过对各种因素的比较分析,从而探索开发出适合工业化生产应用的方案,提高黄芩利用率,仍是研究工作的重点之一。随着人们对健康的日渐重视,因黄芩中的黄酮化合物有着极高的药用营养及良好的保健作用,具有极为广阔的市场前景[b]。[/b]本文旨在研究黄芩中黄酮类物质的提取工艺及其体外抗氧化活性,为黄芩中黄酮类化合物作为天然抗氧化剂和功能性药品得到开发利用提供理论基础和实验依据。[align=center][b] [/b][/align] 刘雄,高建德.黄芩研究进展.甘肃中医学院,2007,24(2):46-50. 罗小文.黄芩中黄酮类成分提取工艺研究进展.中国现代中药.2010,12(7):5-8. 张睿,徐雅琴,时阳.黄酮类化合物提取工艺研究.食品与机械.2003,15(1):21-22. 梁丹,张保东.黄酮类化合物提取和分离方法研究进展.周口师范学院学报,2007,24(5):87-89. 龙春,高志强,陈凤鸣,等.黄酮类化合物的结构-抗氧化活性研究进展.重庆文理学院学报.2006,5(2):13-15. 刘雄,高建德.黄岑研究进展.甘肃中医学院学报,2007,24(2):46-50. 郭雪峰, 岳永德. 黄酮类化合物的提取-分离纯化和含量测定方法的研究进展. 安徽农业科学. 2007, 35(26): 8083- 8086.. 唐德智.黄酮类化合物的提取、分离、纯化研究进展.中药与天然产物,2009,21(12):101-104.. 张岩, 曹国杰, 张燕,等. 黄酮类化合物的提取以及检测方法的研究进展.天食品研究与开发,2008,29(1):154-157. 韩雅慧,陶宁萍.甘草黄酮提取及其抗氧化能力测定方法研究进展.山西农业科学,2010, 38(11):89- 93. 崔永明,余龙江,等. 甘草总黄酮的提取技术及其抑菌活性研究.中药材,2006, 29(8): 838-840. 孙墨珑, 宋湛谦, 方桂珍. 核桃楸总黄酮的提取工艺.东北林业大学学报, 2006, 34 (1) : 38 - 39. 徐清萍,钟桂,芳孟君. 抗氧化剂抗氧化方法研究进展.食品工程,2007,6(7):23-25. 安卓,贾昌喜.苦苣菜总黄酮提取、纯化工艺优化抗氧化活性研究.食品科学. 赵新淮.大黄醇提取物对三种自由基的清除能力的研究.东北农业大学学报.1998,29(3):284-288 杨立琛,李荣.花椒叶黄酮的微波提取及其成分分析.食品科学. CHI Ru-an,ZHOU Fang,HUANG Kun,ZHANG Yue-fei.Separation of baicalin form Scutellaria Baicalensis Georgi with polyamide.Key Laboratory for Green Chemical Process of Ministry of Education.2008,15(1):606-611.
[color=#333333]橄榄(Canarium album L.)为我国珍贵的药食两用资源,具有解酒护肝、抗菌消炎、抗病毒和解毒等药理功效,橄榄中酚类化合物是其主要的药效成分,但国内外有关橄榄酚类化合物组成的研究报道不多。本论文对我国橄榄果实中的酚类化合物进行提取、分离和纯化,并对酚类化合物单体的化学结构进行鉴定研究,以明确橄榄酚类的具体组成,对于橄榄资源的深加工利用和橄榄中药的药理研究具有重要的指导意义和应用价值。首先采用化学和仪器分析方法对福建闽侯檀香橄榄果实不同部分的化学组成进行了分析测定,[/color]
我是一个刚做定性的新手,想问下在GC-MS,酯类化合物的特征离子有哪些?
水质硝基苯类化合物的测定中,其他组分线性度能满足要求,为什么2,4,6三硝基甲苯曲线线性不好?
酚类化合物水溶性强,一般分离后极性较大又都在水部位,比如10%甲醇请问除了挥掉甲醇后冻干这个方法外,还有没有除水的方法。因为温度一高就变黄了,所以不方便用悬蒸。
[align=right][b]SGLC-GC/MS-020[/b][/align] [b]摘要:[/b]本文建立了12种硝基酚类化合物测定的[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GC-MS[/color][/url]方法。参照HJ 1150-2020中色谱方法,采用色谱柱 SH-I-5SilMS对12种硝基酚类化合物进行分析,岛津[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-TQ8050NX[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]-质谱联用仪进行检测。结果表明,12种硝基酚类化合物峰形对称,重现性好,满足标准要求。本方法可为12种硝基酚类化合物的测定提供参考。 [b]关键词:[/b]水质 硝基酚类 SH-I-5SilMS [url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GC-MS[/color][/url] [b]1. 实验部分 1.1 实验仪器及耗材[/b] 岛津[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-TQ8050NX[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]-质谱联用仪; 色谱柱:SH-I-5SilMS(30 m×0.25 mm×0.25μm;P/N:221-75954-30); 纯水机:PR-FP-0120α-MT1(+ 60L水箱 + 取水器); SHIMSEN Arc Disc HPTFE针式过滤器(P/N:380-00341-05); [url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GC-MS[/color][/url]认证样品瓶LabTotal Vial(P/N:227-34002-01); SHIMSEN Pipet[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url]:SHIMSEN Pipet PMII-10(P/N:380-00751-02); SHIMSEN Pipet PMII-100(P/N:380-00751-04); SHIMSEN Pipet PMII-1000(P/N:380-00751-06)。 [b]1.2 混合标准使用液的制备[/b] 取市售硝基酚类混合标准品适量,用二氯甲烷稀释定容至2.0mg/L,作为混合标准使用液。 [b]1.3 分析条件 GC条件[/b] 毛细管柱:SH-I-5Sil MS(30 m×0.25 mm×0.25μm;P/N:221-75954-30) 程序升温:初始温度50℃,保持5min,以8℃/min升温到250℃,保持4min 载气:He 载气控制模式:恒线速度 流速:1.0ml/min 进样口温度:220 ℃ 进样量:1μL 进样方式:不分流进样 [b]质谱条件[/b] 电离模式:电子轰击电离(EI) 电子轰击能量:70 eV 离子源温度:230 ℃ 接口温度:260 ℃ 溶剂延迟:3min 数据采集模式:SIM 各化合物SIM参数见下表 [img=SHIMSEN Styra HLB]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-020_01.png[/img][font=arial, &][size=12px][/size][/font] [b]2. 实验结果[/b] 按照上述色谱条件(1.3)进行采集,混合标准使用液色谱图如下: [b]混合标准使用液[/b] [img=SHIMSEN Styra HLB]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-020_02.png[/img][font=arial, &][size=12px][/size][/font] [b]重现性数据[/b] [img=SHIMSEN Styra HLB]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-020_03.png[/img] [b]3. 结论[/b] 本文建立了12种硝基酚类化合物测定的[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GC-MS[/color][/url]方法。参照HJ 1150-2020的方法,采用色谱柱SH-I-5SilMS对12种硝基酚类化合物进行分析,岛津[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GCMS[/color][/url]-TQ8050NX[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]-质谱联用仪进行检测。结果表明,12种硝基酚类化合物峰形对称,重现性好,满足标准要求。本方法可为12种硝基酚类化合物的测定提供参考。
[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]质谱仪联用分析硝基苯类化合物液液萃取前处理注意是想,新手上路,大侠们指点迷津
[color=#444444]萜烯类化合物可以冷凝么?[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用仪[/color][/url]可以测萜烯类化合物么?[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用仪[/color][/url]只能测可冷凝de挥发性有机化合物么[/color]
水质 苯胺类化合物的测定HJ822-2017 净化过程中分别用3次洗脱溶液洗脱,三次的洗脱溶液中分别是哪些物质,苯胺在第几次洗脱液中
hj638.[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]测酚类化合物,出峰不完全,只有10个,求各位大佬的帮助,用的是赛默飞u3000.怎么设置仪器条件[img]https://ng1.17img.cn/bbsfiles/images/2022/06/202206011036247875_8255_4245459_3.png[/img]
GB 5009.26-2016 食品中亚硝胺类化合物的测定,第一法中是只测一种亚硝胺化合物的含量吗?
不好意思,小弟是使用LC的,平时的工作就是检测碳水化合物样品,做一些糖类检测方面工作。因新购置一台GC,听说GC也可以测定糖类化合物,但是样品可能需要经过处理才行,特此向各位请教了,GC如何才能测定糖类化合物呢?我知道糖类最好还是使用LC测定,仅仅为了扩展知识而已,还望不吝赐教。
葡萄酒酚类化合物分为两大类:非类黄酮(羟基肉桂酸、羟基苯甲酸和二苯乙烯)和类黄酮(花青素、黄酮-3-醇和黄酮醇)。这些次生代谢产物对葡萄酒的苦味、色泽、涩味、香气等主要感官参数都有重要影响,而这些都是影响消费者接受度和喜好度的最重要因素。许多研究表明,影响葡萄酒中酚类化合物存在的主要因素之一是葡萄品种。因此,用特定的葡萄品种酿造的葡萄酒通常是根据感官品质来描述的,这至少可以部分反映其品种来源。

维权声明:本文为chuanxinlian原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。浅谈甾体类化合物的分离与结构鉴定 在植物环己烷或石油醚萃取部分,有很多小极性的化合物,并且这些化合物之间的极性差异也很小,分离时可能会遇到很多困难,即使分离得到了单体化合物,结构解析时也是一件很不容易的事,不管是氢谱还是碳谱中,都在高场区出来一堆信号,有时氢谱中的积分都不一定能积准,碳谱的高场区就像个小树林,密密麻麻的全是信号,看着就头疼。由于我曾从一植物的环己烷层中分离得到了多个甾体类化合物(主要为豆甾类),下面就我在实验过程中在分离和解析甾体类化合物的一点经验跟大家分享一下。1.甾体类化合物的分离纯化 由于我做的这一部分的成分极性很小,其中的甾体类化合物均不连糖,并且我所得到的化合物的结构很相似,有的只相差一个双键或只差一个羟基或羰基,总之,结构类似,极性也就相差不大,分离也就不容易了。由于极性小,我采用的分离手段只能局限在硅胶柱或板、凝胶柱(Sephadex LH-20)。首先把粗浸膏过一遍大的硅胶柱,已达到按照极性大致砍一下段的效果,由于环己烷萃取部分有很多色素,所以接下来采用过Sephadex LH-20柱将其中的色素除去,最后得到多种没有色素的流分,这里面的成分也是很杂的,有多种类型的化合物,如黄酮类、二萜内酯类、甾体类等,由于各类型化合物间的分子量有很大的差异,接下来就可以过一个又细又长的Sephadex LH-20柱,流速一定不能太快,并且流分要接的很细,我们一般用5ml的小瓶接,尽量避免不必要的交叉。这样就有可能将甾体类化合物与其他类型的化合物分开了,最后一步,在硅胶薄层板上看一下,如果成分简单,分离度良好,就采用制备薄层色谱,将单体化合物得到。 需要指出的是,制备薄层时,由于很多甾体类化合物在紫外灯下没有任何紫外吸收,这时千万不要认为没有紫外吸收的地方就没有化合物。比如这块板上的: http://ng1.17img.cn/bbsfiles/images/2010/10/201010220007_252894_1745326_3.jpg 此时,一定要在点小硅胶板时用通用显色剂显色,确定哪里有点,该流分总共有几个点,各个点之间的上下关系,有没有紫外吸收之类的,分析清楚了,最后再去做制备薄层,如果有没有紫外吸收的点,在刮板前可以先用玻璃或报纸将板的大部分挡住,在板的另一边显色,找到该点的具体位置,以免漏掉重要的点。2.豆甾类化合物的结构解析 因为我分到的甾体类化合物主要为豆甾类,所以我就只介绍此类化合物的结构解析了。下面是我在解析过程中总结的该类化合物的谱学上的特点:2.1 氢谱中最高场的信号为18-CH3,化学位移一般在0.7ppm左右。2.2 碳谱中最高场的信号同样为18-CH3,化学位移一般在12.0ppm左右。实例列举:http://ng1.17img.cn/bbsfiles/images/2010/10/201010220010_252897_1745326_3.jpg1H-NMRhttp://ng1.17img.cn/bbsfiles/images/2010/10/201010220011_252898_1745326_3.jpg13C-NMRhttp://ng1.17img.cn/bbsfiles/images/2010/10/201010220011_252899_1745326_3.jpg2.3 甾体母核上的羟基的取向不同,与其所连的碳的化学位移也会有所不同,一般情况下,α-OH连接的碳化学位移一般小于70.0ppm,而β-OH连接的碳化学位移一般大于70.0ppm。举例如下:http://ng1.17img.cn/bbsfiles/images/2010/10/201010220011_252900_1745326_3.jpg2.4 如果你拿到一套新的谱图,看到高场区有很多聚集在一起的碳氢信号,并且氢碳谱中最高场的化学位移值分别在12.0和0.7ppm左右,在你不确定它什么类型的化合物的时候,可以考虑一下是不是甾体类化合物(三萜类最高场的碳信号在18ppm左右,基本上没有12ppm左右的碳信号)。最后,希望我的原创能给某些人起到抛砖引玉的作用。
如果要分析一类化合物 比如塑化剂 ,总共有18种化合物, 用GC-MS,刚拿到手怎么确定程序升温的过程,是不是要每一个化合物要单独进一针,确定其保留时间,离子碎片啊

http://ng1.17img.cn/bbsfiles/images/2017/03/201703220908_01_3111730_3.png酚类化合物在酸碱中的分配比很不一样吗? 为什么在碱性条件下溶于水中,酸性条件下溶于有机试剂中,这里面机理什么呢?
本人参照GBZ/T 160.72-2007标准在做工作场所硝基苯类化合物检测时,由于使用的是ECD检测器,它的响应值不稳定,作出的标准曲线的线性很差,标准上的线性范围很窄,而且职业卫生的限值并不包括在内。有哪位同仁可以传授下经验,谢谢!!
植物黄酮类化合物的分离分析方法研究
我现在想分离黄铜类化合物,包括金丝桃苷,槲皮素,芦丁,山奈酚,看有文献缓冲液用的是硼砂和磷酸二氢钠的混合溶液,这种缓冲液如何调节PH啊,还有二者的比例对分离度有何影响啊,大家有做过的分享一下经验