化学蛋白质组学揭示高铁血红素-蛋白互作谱
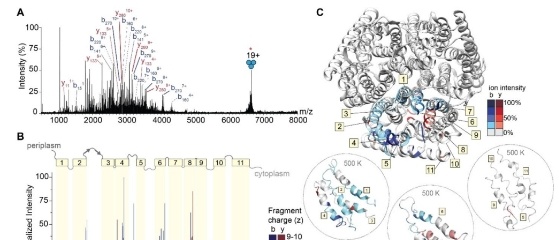
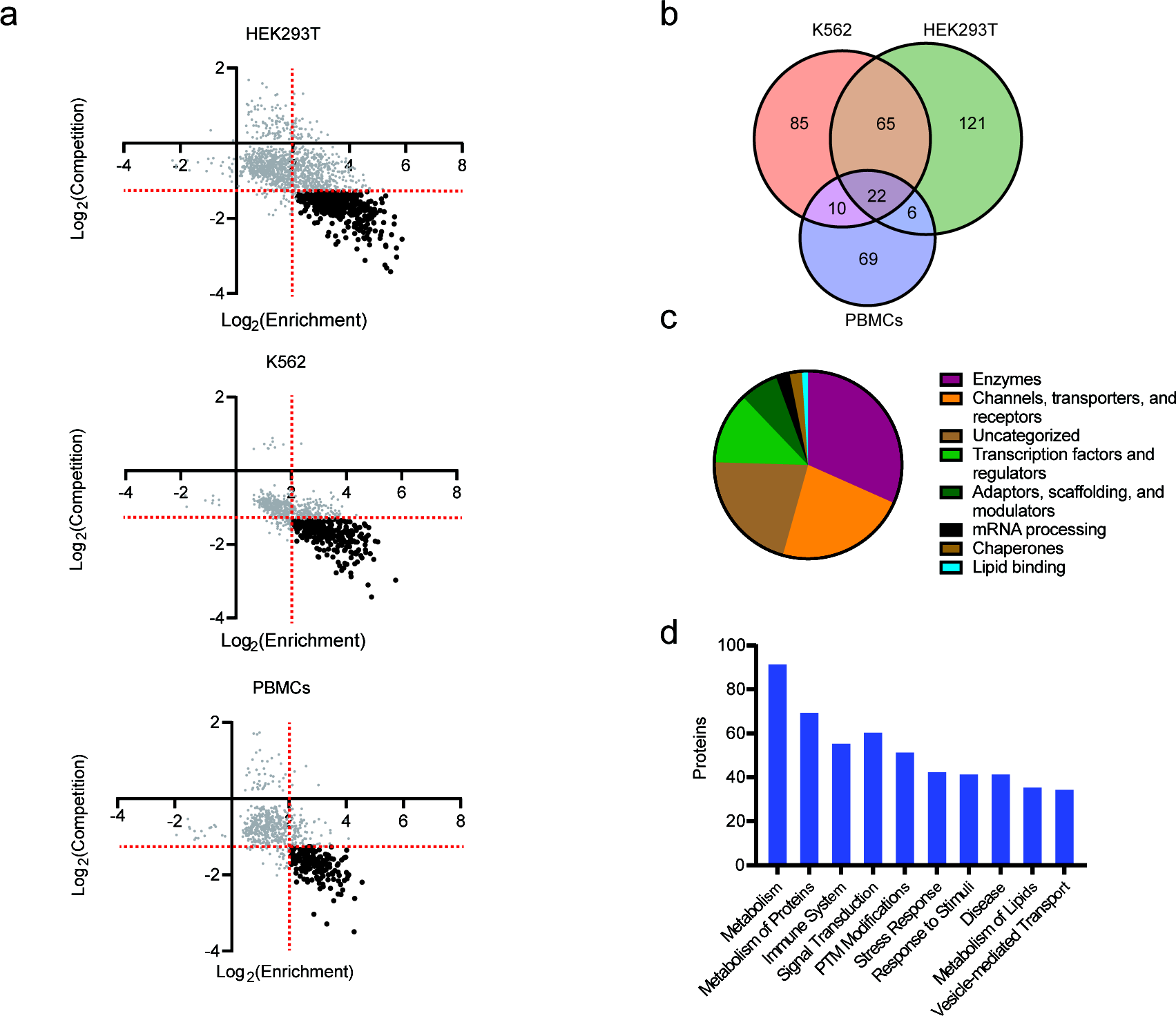
大家好,本周为大家分享一篇最近发表在Journal of The American Chemical Society上的文章,A Chemical Proteomic Map of Heme−Protein Interactions1。该文章的通讯作者是美国斯克利普斯研究所的Christopher G. Parker研究员。高铁血红素(heme)是人体中许多蛋白质的辅助因子,也是血液中氧气的主要转运体。最近的研究也证实了高铁血红素可以作为一种信号分子,通过与伴侣蛋白质结合而不是通过其金属中心反应来发挥其作用。然而,目前关于血红素结合蛋白的注释还不够完整。因此,本文采用化学蛋白质组学的方法去揭示人体中与高铁血红素发生互作的蛋白质谱。化学蛋白质组学是揭示蛋白质功能和发现药物靶标的重要工具。其中,最常用的是基于活性的蛋白质分析(Activity-based protein profiling,ABPP),通过结合活性分子探针标记及串联质谱分析,实现对靶标蛋白的鉴定。如图1b,本文设计了一个“全功能”活性分子探针(HPAP),共包含3个部分:1. Hemin母核,用于与靶蛋白非共价结合;2.光活化基团-双吖丙啶,可在UV光照下生成卡宾,促使分子探针与蛋白发生共价交联;3. 炔基,可在铜催化下与含有叠氮的试剂(荧光标签,生物素)发生点击化学反应,后两者组成FF-control。具体实验流程如下图1a所示,用HPAP处理不同细胞(In Situ)或不同细胞来源的蛋白质组(In vitro),HPAP中的hemin母核可与靶蛋白发生非共价结合,经UV光照,HPAP-蛋白间形成共价交联,再利用点击化学可将HPAP-蛋白与荧光素(TAMRA)或者生物素标签相连,用于后续的荧光成像(In-gel fluorescence)或者链霉亲和素纯化、LC-MS鉴别定量(MS-based I.D. and quantitation)。 图1. (a)使用基于高铁血红素的光亲和探针(HPAP)识别血红素结合蛋白的流程示意图。(b) HPAP、hemin和FF-control的结构;(c) HEK293T裂解物中与HPAP结合的蛋白的荧光成像;(d) hemin加入对HPAP与蛋白结合的影响。作者首先使用了SDS-PAGE去评估了HPAP标记蛋白的能力。如图1c所示,随着HPAP浓度的提高,胶图上条带颜色也逐渐加深,说明HEK293T细胞裂解液中与HPAP结合的蛋白在逐渐增加。如图1d所示,在10 μM HPAP的条件下,逐渐加入hemin,可以看到胶图上条带颜色逐渐变浅,说明hemin与HPAP之间发生了竞争,HPAP模拟了hemin与蛋白的结合过程。随后,作者又使用已知的hemin结合蛋白来确认HPAP捕获目标蛋白的能力。如图2所示,这些已知蛋白被HPAP成功的标记上,但由于hemin的加入,条带的颜色在逐渐变浅(TAMRA)。Western blot的结果显示,蛋白的总量并无太大变化,但hemin的竞争结合,导致与HPAP结合的蛋白量在下降。以上实验均说明,HPAP具有较好的选择性标记能力,能够模拟hemin与靶蛋白的结合,并以共价交联的方式标记在蛋白上。 图2. 用已知的高铁血红素结合蛋白确认HPAP捕获目标蛋白的能力。验证了方法的可行性后,作者将HPAP与定量蛋白质组学结合用于绘制高铁血红素-蛋白质互作谱。考察了多种细胞系,包括:人胚胎肾细胞(HEK293T)、人慢性髓系白血病细胞(K562)以及人原代外周血单个核细胞(PBMCs)。每种细胞系设置了两种实验形式:1)特异性结合实验(Enrichment):通过将HPAP识别出蛋白与FF-Control识别出的蛋白进行对比,排除非特异结合的干扰(图1b),如果同一蛋白通过HPAP富集到的量是FF-control富集到的量4倍以上,则认为该蛋白是HPAP特异性结合蛋白。2)竞争性结合实验(Competition):观察HPAP富集的蛋白在hemin和HPAP同时存在时富集到的量的变化,变化大于3倍且具有显著性差异(p<0.05)的蛋白被认为是HPAP与hemin竞争性结合的蛋白。最终确定的高铁血红素结合蛋白应满足以上两种实验的筛选标准(图3a)。如图3b-d所示,总共鉴定出378个的高铁血红素结合蛋白,其中214个来自HEK293T, 182个来自K562, 107个来自PBMC。尽管三种细胞类型之间的结合蛋白有一些重叠,但大多数靶点蛋白只存在于一种或两种细胞类型中(图3b),这暗示血红素在不同细胞中可能发挥不同的功能。其中,19个靶点蛋白是在UniProt上已经注释为高铁血红素的结合蛋白,剩余都是未揭示的结合蛋白。这些结合蛋白按照功能可划分为:转运蛋白,转录因子,支架蛋白和酶(图3c),根据代谢通路又可进一步划分(图3d)。作者最后对几个新发现的结合蛋白进行了验证,并选择IRKA1进行进一步的作用机制研究。IRKA1在调节炎症信号通路中起着关键作用,IRAK1被IRAK4磷酸化,然后自磷酸化,产生NFkB介导的炎症反应。经实验确认(图4),hemin是IRKA1的一种变构活化配体,可增强其酶活性,促进IRAK1的自磷酸化。 图3. 基于蛋白质组学的HPAP-蛋白互作分析。 图4. Hemin对IRKA1的调节作用。总之,本文设计开发了一种基于高铁血红素的光亲和探针,它可以与化学蛋白质组工作流程结合,以识别不同蛋白质组中的高铁血红素结合蛋白。利用该方法也可拓展至其他分子配体靶标蛋白的识别。 撰稿:刘蕊洁编辑:李惠琳原文:A Chemical Proteomic Map of Heme-Protein Interactions参考文献1. Homan, R. A., Jadhav, A. M., Conway, L. P., & Parker, C. G. (2022). A Chemical Proteomic Map of Heme-Protein Interactions. Journal of the American Chemical Society, 144(33), 15013–15019.