一锅法合成二硫醚的简便制备过程研究
谁有在线NIR在化学合成过程质量控制方面应用资料啊
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=126561]甲烷液相部分氧化合成甲醇过程研究[/url]

h、c谱、H谱、DEPT谱等结构确证证明合成的样品具有伏立康畔的结构,空可结构为2R/3S。在合成原料药的过程中选择适当的溶剂可提高产量或决定药物的性质如晶型、纯度和溶解性,因此有时溶剂是合成过程中十分关键的因素,然而由于残留溶剂没有疗效,会影响产品的安全性,故需对其进行研究。药物中的残留溶剂系指在原料药或辅料的生产中,以及制剂制备过程中使用的,但在工艺过程中未能完全去除的有机溶剂。按有机溶剂的毒性和对环境的危害,ICH将有机溶剂分为避免使用、限制使用、低毒和毒性依据尚不足四种情况。环境健康标准(EHC)和危险信息系统大全(IRIS)将苯、四氯化碳等几种生产过程中常用的残留溶剂列为有毒化合物,一些组织如国际化学品安全性纲要(IPCS)、美国环境保护机构(EPA)和美国食品药品监督管理局(FDA)制定了人体可接受水平,目的是防止长期接触化学品后可能对人体健康和整个环境造成危害。本论文详细研究了伏立康唑合成工艺及其理化性质,并对合成过程中的有机残留成分及检测方法进行了研究。采用顶空气相色谱法,以D~t-624毛细管柱(30m×0.53mm×3.0um,固定液为6%氰丙基苯基一94%聚二甲基硅氧烷)为分析柱;氢火焰离子检测器,程序升温,测得样品中甲醇小于O.004%,丙酮0.001%,异丙醇0.26%,乙醇、二氯甲烷、乙酸乙酯、四氢氟喃、乙二醇二甲醚未检出。关键词:伏立康唑 真菌 有机残留溶剂 顶空气相色谱法http://ng1.17img.cn/bbsfiles/images/2012/07/201207232354_379322_2355529_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/07/201207232354_379323_2355529_3.jpg
原料药合成过程中的中间体检测方法需要做方法学验证吗?是关键中间体的检测方法做方法验证,还是都要做?一般做哪几项?
我合成了一种新的加合物,因为在合成过程中使用了DMSO做溶剂,烘干后我想检测其中是否很有S?请问用什么测试方法合适??我目前考虑的是元素分析,不知是否可行??谢谢!!!
我们单位最近开展阴离子合成洗涤剂的检测项目,我们用二氮杂菲萃取分光光度法检测水质中的阴离子合成洗涤剂含量,可是怎么也做不好。请做过的老师给我详细的操作过程,最好有具体数值,我参考一下自己到底是哪地方出现问题?谢谢~~~~
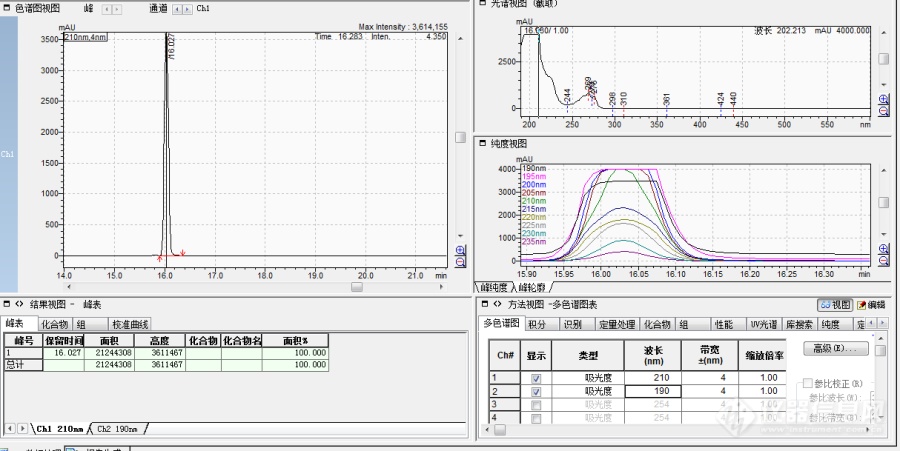
如题,在开发方法过程中,如何选择最佳吸收波长。问题1、使用全波长扫描(我们使用的是PDA)后,发现其吸收的最高波长很低,在190nm处吸收最高,最近遇到好几个这种情况, 那么此种情况下如何选择最佳的波长呢?附图,图中色谱图为210nm处的一个吸收,左边为光谱图和各吸收波长下的一个峰轮廓图。此图不算典型,至少在210nm 吸收也还客观,但也大概能说明问题。之前遇到的是在210nm处吸收只有190的一半甚至1/3,那么如此情况下,我们如何选择波长,难道选择190nm吗?[img=,690,345]https://ng1.17img.cn/bbsfiles/images/2019/04/201904181623375228_9656_3116636_3.png!w690x345.jpg[/img]问题2、当我们确定了产品的一个吸收波长后,可能会发现合成该产品的原料的吸收波长不一定在此波长下有较大吸收,可能在其他波长下吸收较大。 那么此种情况下,投料反应时,我们依然查看的是产品的吸收波长,而原料在此波长下的吸收并不明显, 导致无法判断原料是否有进行反应,也无法用此方法来进行中控, 有时候我们在这个波长下发现原料的吸收已降低到无法识别,产品纯度已达到了99% 但事实上在原料的波长下,原料可能还有20%未反应,因为尽管纯度达到了99%,但事实上含量却只有80%左右。 如此一来,很影响实验员在中控过程的一个判断,那么我们在此时又如何去选择最佳波长呢?(这只是刚开始的反应就有这个问题了,那么之后可能会出现不同的步骤,产生不同的中间体,如果每个中间体的吸收波长都有差异,如何进行判断呢?) 以上问题,望指教!
我现在要做一个微波合成实验,我想用抽真空的方式把多余的产物过滤出去,但是不知道如何能保证气密性?因为如果抽的不完全我的实验就白做了。
前段时间实验室试用了一家仪器公司代理的进口流动合成仪,效果蛮好的。就是类似于微管道反应器,反应液边流动边反应。之前做了两个实验,都是平时很迟钝的那种,一天一夜或者两天两夜那种,后来使用流动合成仪,增加了系统压力从而可以大大升高反应温度,实验进行了一个小时就达到甚至比之前的反应效果还好。正好我们实验室有一个才从国外回来的博后,他以前就用过流动合成,效率提高很多,也完成了一些平时烧瓶条件不好进行的反应,尤其是在新药研发和条件优化时具有很大的优势。大家有没有知道这款仪器的呢?想多交流交流。加上最近听到的关于流动化学的讲座,我觉得这样的仪器在国内市场上会有很大前景的哦,不过需要一个过程,不知道大家怎么看。
我想请问一下,用sephadex G25进行分离时,样品分子量大概需要相差多少才能分离开来?用它来除去样品中所含的盐(合成过程中所带入的)效果怎么样?
耶鲁研究学者成功地对细菌的蛋白质合成机制进行遗传学改造 随着合成生物学的发展,科学家们已经掌握了相当的遗传学工具,他们已能够修改有机物的天然遗传密码,甚至重新谱写生命。在昨天的《科学》杂志上,耶鲁大学的研究学者发表论文说,他们已成功对细菌中的蛋白质合成机制进行遗传学改造。该论文的作者,细胞及分子生理学系的杰斯·莱因哈特(Jesse Rinehart)介绍说:“从本质上来说,我们已经扩展了大肠杆菌的遗传密码,这让我们能够合成以特殊形式,例如模拟天然状态或者疾病状态的蛋白质。”耶鲁研究小组的理念是, 通过修改遗传密码,用新的方式影响蛋白质的行为,使之能实现大多数的生命功能。他们并没有创造自然界不存在的东西,而是诱发了磷酸化作用(phosphorylation)。磷酸化作用是生命体中最常见的基本生理过程,它能显著改变蛋白的功能。通常,蛋白的磷酸化作用并不直接由DNA编码指导合成,而是在蛋白质合成之后才开始,而这正是耶鲁的研究人员们想要改写的:他们希望把磷酸化过程添加到大肠杆菌的遗传密码中,通过DNA第一时间就能指导蛋白磷酸化。过去,科学家们缺乏研究磷酸化状态蛋白的能力,致使对某些疾病的研究停滞不前,例如蛋白活性极高的癌症。而这项新技术实现了人类蛋白质的天然磷酸化体系,这对于理解疾病的发展至关重要。莱因哈特解释说:“我们现在做的就是运用蛋白开关——把蛋白机制打开或关闭,这让我们能以全新的方式研究疾病状态,并有望引导新药的研发。”莱因哈特他们现在打算创建与癌症、糖尿病以及高血压相关的磷酸化蛋白质,不过他们强调说,这种技术能够实现处理任何种类的蛋白质。
化妆品原料的来源和安全性在目前崇尚天然的潮流中,普通民众有一种观点:天然的就是安全的,化学合成的就是有毒的、不安全的。这一观点在食品、保健品、化妆品行业都普遍存在。这一观点显然错误,天然的许多东西是有毒的,如:蓖麻、夹竹桃、野生蘑菇、断肠草等等。《化妆品卫生规范》也严禁将70多种植物提取物用于化妆品。我们来看看获取化妆品原料的路线有哪些?1 大部分化妆品原料是化学合成的,如:合成油脂、硅油、表面活性剂、大部分功能性添加剂、防腐剂、化学防晒剂、色素等。为保证安全性《化妆品卫生规范》对所有原料有严格的规定,防腐剂、杀菌剂、化学防晒剂、色素都是限定用量,部分还是禁用的; 功效性添加剂中一部分也是限量的。2 很多添加剂原来最先发现于大自然或人体,提取出来结构分析清楚后进行人工合成,质量更有保证、成本也大幅度降低,如:大部分维生素、尿囊素、水杨酸、α-硫辛酸等。具有良好祛斑美白作用的苯乙基间苯二酚也是最早发现于杨树,现在都是采用化学合成工艺。3 许多添加剂结构复杂而且特殊,合成的成本很高或很难合成得到高纯度,目前还是天然提取,如:积雪草甙、光甘草定、葛根素、四氢姜黄素、根皮素、胡萝卜素、茶多酚、γ-亚麻酸、薄荷等。4 发酵也是另外一条重要途径,但这类原料种类相对而言不多。酒精就是典型的发酵产品(当然也可以合成),添加剂中的L-乳酸、曲酸、α-熊果苷(而β-熊果苷以合成制取)等都通过发酵制取。5 有些原料合成和提取两条途径都可,如:白藜芦醇、咖啡因、α-红没药醇等,提取或合成都可以得到,具体选取那条途径,需要看成本对比。6 复合型路线,用于美白祛斑的曲酸二棕榈酸酯、维生素C、甘草酸二钾、薄荷乳酸酯等,先发酵或提取,后面合成或修饰(也是一合成过程)。从得到化妆品原料的路线可清楚看到:天然和化学合成不是对立的,而是相互补充、相互启发。来源于天然提取还是化学合成也不是安全性和质量的评价标准。即使是来源于天然的原料,生产过程必须经过化工处理:提取、浓缩、除去杂质、脱色、干燥等,还是一个化工过程。总之,化妆品原料有多种,化妆品原料的安全性来源和过程不是关键,严格的产品检验(尤其是含量、有害杂质等指标)才是化妆品安全性和温和性的关键。小编想说化学其实是一门是很实用的学科,化学在保证人类的生存并不断提高人类的生活质量方面起着重要作用。如:利用化学生产化肥和农药,以增加粮食产量;利用化学合成药物,以抑制细菌和病毒,保障人体健康;利用化学开发新能源、新材料,以改善人类的生存条件;利用化学综合应用自然资源和保护环境以使人类生活得更加美好。现在社会上的一个普遍误解就是觉得化学一定是不好的,有毒害的,这是对化学的不公平对待,我们不能因为一小部分人对化学的错误使用而抹杀了化学对人类社会的贡献,这也是我们“生活中的化学”所想要传达的宗旨,我们要科普化学知识,传递化学正能量,让更多的人能正确的认识化学这一门学科。希望大家能加入我们一起去做这件有意义的事,告诉身边的人化学并不恐怖,相反,它对于我们的生活还起到了非常重要的作用。
多肽合成是一个重复添加氨基酸的过程,固相合成顺序一般从C端(羧基端)向 N端(氨基端)合成。固相合成法,大大的减轻了每步产品提纯的难度。为了防止副反应的发生,参加反应的氨基酸的侧链都是保护的。羧基端是游离的,并且在反应之前必须活化。固相合成方法有两种,即Fmoc和tBoc。由于Fmoc比tBoc存在很多优势,现在大多采用Fmoc法合成。【详情请咨询合肥国肽生物】(1)具体合成由下列几个循环组成:1. 去保护:Fmoc保护的柱子和单体必须用一种碱性溶剂(piperidine)去 除氨基的保护基团。2. 激活和交联:下一个氨基酸的羧基被一种活化剂所活化。活化的单体与游离的氨基反应交联,形成肽键。在此步骤使用大量的超浓度试剂驱使反应完成。循环:这两步反应反复循环直到合成完成。3. 洗脱和脱保护:多肽从柱上洗脱下来,其保护基团被一种脱保护剂(TFA) 洗脱和脱保护。(2)树脂的选择及氨基酸的固定将固相合成与其他技术分开来的最主要的特征是固相载体,能用于多肽合成的固相载体必须满足如下要求:必须包含反应位点(或反应基团),以使肽链连在这些位点上,并在以后除去;必须对合成过程中的物理和化学条件稳定;载体必须允许在不断增长的肽链和试剂之间快速的、不受阻碍的接触;另外,载体必须允许提供足够的连接点,以使每单位体积的载体给出有用产量的肽,并且必须尽量减少被载体束缚的肽链之间的相互作用。用于固相法合成多肽的高分子载体主要有三类:聚苯乙烯-苯二乙烯交联树脂、聚丙烯酰胺、聚乙烯-乙二醇类树脂及衍生物,这些树脂只有导入反应基团,才能直接连上(第一个)氨基酸。根据所导入反应基团的不同,又把这些树脂及树脂衍生物分为氯甲基树脂、羧基树脂、氨基树脂或酰肼型树脂。BOC合成法通常选择氯甲基树脂,如Merrifield树脂;FMOC合成法通常选择羧基树脂如王氏树脂。氨基酸的固定主要是通过保护氨基酸的羧基同树脂的反应基团之间形成的共价键来实现的,形成共价键的方法有多种:氯甲基树脂,通常先制得保护氨基酸的四甲铵盐或钠盐、钾盐、铯盐,然后在适当温度下,直接同树脂反应或在合适的有机溶剂如二氧六环、DMF或DMSO中反应;羧基树脂,则通常加入适当的缩合剂如DCC或羧基二咪唑,使被保护氨基酸与树脂形成共酯以完成氨基酸的固定;氨基树脂或酰肼型树脂,却是加入适当的缩合剂如DCC后,通过保护氨基酸与树脂之间形成的酰胺键来完成氨基酸的固定。(3)氨基、羧基、侧链的保护及脱除要成功合成具有特定的氨基酸顺序的多肽,需要对暂不参与形成酰胺键的氨基和羧基加以保护,同时对氨基酸侧链上的活性基因也要保护,反应完成后再将保护基因除去。同液相合成一样,固相合成中多采用烷氧羰基类型作为α氨基的保护基,因为这样不易发生消旋。最早是用苄氧羰基,由于它需要较强的酸解条件才能脱除,所以后来改为叔丁氧羰基(BOC)保护,用TFA(三氟乙酸)脱保护,但不适用含有色氨酸等对酸不稳定的肽类的合成。chang Meienlofer和Atherton等人采用Carpino报道的Fmoc(9-芴甲氧羰基)作为α氨基保护基,Fmoc基对酸很稳定,但能用哌啶-CH2CL2或哌啶-DMF脱去,近年来,Fmoc合成法得到了广泛的应用。羧基通常用形成酯基的方法进行保护。甲酯和乙酯是逐步合成中保护羧基的常用方法,可通过皂化除去或转变为肼以便用于片断组合;叔丁酯在酸性条件下除去;苄酯常用催化氢化除去。对于合成含有半胱氨酸、组氨酸、精氨酸等带侧链功能基的氨基酸的肽来说,为了避免由于侧链功能团所带来的副反应,一般也需要用适当的保护基将侧链基团暂时保护起来。保护基的选择既要保证侧链基团不参与形成酰胺的反应,又要保证在肽合成过程中不受破坏,同时又要保证在最后肽链裂解时能被除去。如用三苯甲基保护半胱氨酸的S-,用酸或银盐、汞盐除去;组氨酸的咪唑环用2,2,2-三氟-1-苄氧羰基和2,2,2-三氟-1-叔丁氧羰基乙基保护,可通过催化氢化或冷的三氟乙酸脱去。精氨酸用金刚烷氧羰基(Adoc)保护,用冷的三氟乙酸脱去。我们主要提供:多肽合成、定制多肽、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。合肥国肽生物官网:http://www.bankpeptide.com欢迎咨询服务热线:0551-62626599
多肽化学合成方法,包括液相和固相两种方法。液相合成方法现在主要采用BOC和Z两种保护方法,现在主要应用在短肽合成,如阿斯巴甜,力肽,催产素等,其相对与固相合成,具有保护基选择多,成本低廉,合成规模容易放大的许多优点。【请移步百度搜“合肥国肽生物”即可】与固相合成比较,液相合成主要缺点是,合成范围小,一般都集中在10个氨基酸以内的多肽合成,还有合成中需要对中间体进行提纯,时间长,工作量大。固相合成方法现在主要采用FMOC和BOC两种方法,它具有合成方便,迅速,容易实现自动化,而且可以比较容易的合成到30个氨基酸左右多肽。1.氨基酸保护基 20种常见氨基酸,根据侧链可以分为几类:脂肪族氨基酸(Ala,Gly,Val,Leu,Ile,),芳香族氨基酸(Phe,Tyr,Trp,His),酰胺或羧基侧链氨基酸(Asp,Glu,Asn,Gln),碱性侧链氨基酸(Lys,Arg),含硫氨基酸(Cys,Met),含醇氨基酸(Ser,Thr),亚氨型基酸(Pro)。多肽化学合成中氨基酸的保护非常关键,直接决定了合成能够成功的关键。因为常见的20中氨基酸中有很多都是带有活性侧链的,需要进行保护,一般要求,这些保护基在合成过程中稳定,无副反应,合成结束后可以完全定量的脱除。合成中需要进行保护的氨基酸包括:Cys,Asp,Glu,His,Lys,Asn,Gln,Arg,Ser,Thr,Trp,Tyr。需要进行保护的基团:羟基,羧基,巯基,氨基,酰胺基,胍基,吲哚,咪唑等。其中Trp也可以不保护,因为吲哚性质比较稳定。当然在特殊的情况下,有些氨基酸也可以不保护,象,Asn,Gln ,Thr,Tyr。氨基酸侧链保护基团非常多,同一个侧链有多种不同的保护基,可以在不同的条件下选择性的脱除,这点在环肽以及多肽修饰上具有很重要的意义。而且侧链保护基和选择的合成方法有密切的关系,液相和固相不一样,固相中BOC和FMOC策略也不一样,从某种意义上看,多肽化学就是氨基酸保护基的灵活运用与搭配。关于侧链保护基的使用,请参考王德心的《固相有机合成——原理及应用指南》第四章,我们这里主要介绍Cys,Lys,Asp的几种保护基及其脱除方法。Cys最常见的保护基有三种,Trt,Acm,Mob,这三个保护基可以完成多对二硫键多肽的合成。Lys最常见的保护基有:Boc,Fmoc,Trt,Dde,Allyl,这对于固相合成环肽提供了很多正交的保护策略。Asp最常见的保护基有:Otbu,OBzl,OMe,OAll,OFm,同样也提供了多种正交的保护策略。2.多肽缩合试剂 目前多肽合成中,主要采用羧基活化方法来完成接肽反应,最早使用的是将氨基酸活化为酰氯,叠氮,对称酸酐以及混合酸酐的方法,但是由于这些条件下,存在氨基酸消旋,以及反应试剂危险以及制备比较复杂,逐渐被后来的缩合试剂取代,按照其结构可以分为两种:缩合试剂主要有:碳二亚胺型,鎓盐型(Uronium)。3.碳二亚胺型 主要包括:DCC,DIC,EDC.HCl等。采用DCC进行反应,由于反应中生成的DCU,在DMF中溶解度很小,产生白色沉淀,所以一般不用在固相合成中,但是由于其价格便宜,在液相合成中,可以通过过滤除去,应用仍然相当广泛。EDC.HCl因为其水溶解性的特点,在多肽与蛋白的连接中使用比较多,而且也相当成功。但是该类型的缩合试剂的一个最大的缺点,就是如果单独使用,会有比较多的副反应,但是研究表明如果在活化过程中添加HOBt,HOAt等试剂,可以将其副反应控制在很低的范围。多肽合成方法比较 1.液相多肽合成(solution phase synthesis) 液相多肽合成现在仍然广泛的使用,在合成短肽和多肽片段上具有合成规模大,合成成本低的显著优点,而且由于是在均相中进行反应,可以选择的反应条件更加丰富,象一些催化氢化,碱性水解等条件,都可以使用,这在固相中,使用却由于反应效率低,以及副反应等原因,无法应用。液相多肽合成中主要采用BOC和Z两种反应策略。2.固相多肽合成固相多肽合成现在使用的主要有两种策略:BOC和FMOC两种。BOC方法合成过程中,需要反复使用TFA脱BOC,而且在最后从树脂上切割下来需要使用HF,由于HF必须使用专门的仪器进行操作,而且切割过程中容易产生副反应,因此现在使用受到实验条件限制,使用也逐渐减少。FMOC方法反应条件温和,在一般的实验条件下就可以进行合成,因此,也得到了非常广泛的应用。[align=center][img=,770,348]https://ng1.17img.cn/bbsfiles/images/2019/03/201903151637572385_7105_3531468_3.jpg!w770x348.jpg[/img][/align]请移步百度搜“合肥国肽生物”即可我们主要提供:多肽合成、定制多肽、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。
苯片呐醇的光化学法合成过程是什么
生命活动与蛋白质的动态变化密切相关, 很多情况下某些蛋白质是通过各种翻译后修饰来完成或改变其功能。在数量众多的蛋白质翻译后修饰中,蛋白质磷酸化修饰无疑是最重要的一类,它是指通过蛋白激酶(Protein kinase,PK)介导的酶促反应把磷酸基团从一个化合物转移到另一个化合物上的过程(Figure 1所示),是生物体内存在的一种普遍的调节方式。现今发现的所有人类蛋白质中超过30%可被磷酸化修饰,这一修饰在细胞信号的传递过程中占有极其重要的地位,与生命活动的许多过程都密切相关,对此的研究已经成为蛋白质科学的热点之一。 http://img.dxycdn.com/trademd/upload/userfiles/image/2012/09/1346918444_small.jpg磷酸化多肽(主要指肽链中的酪氨酸、丝氨酸和苏氨酸残基的侧链羟基被磷酸化生成酸式磷酸酯的修饰多肽)是研究蛋白质磷酸化过程的必不可少的工具,它可作为磷酸酶模型底物,或作为可产生抗磷酸化蛋白抗体的抗原,也可以在确定磷酸化蛋白的物理参数时作为参考化合物等。因此磷酸化多肽的合成在过去的几年中吸引了相当大的兴趣,目前已确定了较为成熟的合成路线,使磷酸化多肽的合成趋于常规。目前磷酸化多肽的合成主要有两个策略:后磷酸化法(Global phosphorylation)和单体法(Building block approach),如Figure 2所示。前者是在多肽序列合成结束后再在固相载体上对丝氨酸、苏氨酸或酪氨酸的侧链羟基进行磷酸化,可以在同一次合成中同时得到带有和不带有磷酸化位点的多肽;而后者则将适当保护的磷酸化氨基酸直接引入到多肽序列中,操作较前者更为简单,现已成为磷酸化多肽合成的首选策略。在采用单体法构建磷酸化多肽时,目前广泛采用的原料为侧链单苄基保护的氨基酸:Fmoc-AA(PO(OBzl)OH)-OH (AA = Ser, Thr or Tyr)。这类保护的磷酸化位点由于侧链磷酸化基团的离子化而产生较大的位阻效应,并且磷酸化位点的引入往往能促进肽链二级结构的形成,故而磷酸化位点及其后的氨基酸的引入会比较困难。这些问题在合成含有多个磷酸化位点的多肽时将会变得尤为严重,往往会使最终产物的组成非常复杂,难以进行纯化,甚至直接导致合成的失败。http://img.dxycdn.com/trademd/upload/userfiles/image/2012/09/1346918477_small.jpg一般来讲,增加投料量和延长反应时间都能促使连接反应趋于完全,但增加投料量无疑会提高合成成本,对于较昂贵的带有保护的磷酸化氨基酸更是这样,而延长反应时间则可能增加其它副反应发生的风险,故而在合成磷酸化多肽时,需要对氨基酸投料量、反应方法以及反应时长等进行优化调整以期达到更理想、更经济的合成效果。我们有针对性地对磷酸化多肽合成条件进行了探索和调整,采用最终的优化条件成功合成了含有多达六个磷酸化丝氨酸残基的多肽:FAM-Ahx-X(pS)XX(pS)X(pS)X(pS)XX(pS)X(pS)-NH2(客户肽,详细序列未给出;其氨基端标记FAM以进行荧光检测),经过RP-HPLC纯化后最终纯品的纯度高达95%(见Figure 3)。http://img.dxycdn.com/trademd/upload/userfiles/image/2012/09/1346918493_small.jpg参考文献:1. P. Cohen, “The Role of Protein Phosphorylation in Neural and Hormonal Control of Cellular Activity”, Nature, 1982, 296 (5858): 613-620.2. From: http://en.wikipedia.org/wiki/Protein_kinase.3. L. A. Pinna, A. Donella-Deana, “Phosphorylated Synthetic Peptides as Tools for Studying Protein Phosphatases”, Biochim. Biophys. Acta., 1994, 1222 (3): 415-431.4. W. C. Chan, P. D. White, “Fmoc Solid Phase Peptide Synthesis-A Practical Approach” (2000), Oxford University Press.
我们第一次分析合成氨触媒中的SiO2含量,但比色测定中样品空白总是有颜色,希望请教大家样品处理过程中应注意哪些环节?
多肽合成又叫肽链合成,是一个固相合成顺序一般从C端(羧基端)向N端(氨基端)合成。过去的多肽合成是在溶液中进行的称为液相合成法。多肽的合成主要分为两条途径:化学合成多肽和生物合成多肽。请移步百度搜“合肥国肽生物”即可多肽合成的原理多肽合成就是如何把各种氨基酸单位按照天然物的氨基酸排列顺序和连接方式连接起来。由于氨基酸在中性条件下是以分子内的两性离子形式(H3+NCH(R)COO-)存在,因此,氨基酸之间直接缩合形成酰胺键的反应在一般条件下是难于进行的。氨基酸酯的反应活性较高。在100℃下加热或者室温下长时间放置都能聚合生成肽酯,但反应并没有定向性,两种氨基酸a1和a2的酯在聚合时将生成a1a2…、a1a1…、a2a1…等各种任意顺序的混合物。为了得到具有特定顺序的合成多肽,采用任意聚合的方法是行不通的,而只能采用逐步缩合的定向多肽合成方法。一般是如下式所示,即先将不需要反应的氨基或羧基用适当的基团暂时保护起来,然后再进行连接反应,以保证多肽合成的定向进行。式中的X和Q分别为氨基和羧基的保护基,它不仅可以防止乱接副反应的发生,还具有能消除氨基酸的两性离子形式,并使之易溶于有机溶剂的作用。Q在有的情况下也可以不是共价连接的基团,而是由有机强碱(如三乙胺)同氨基酸的羧基氢离子组成的有机阳离子。Y为一强的吸电子基团,它能使羧基活化,而有利于另一氨基酸的自由氨基,对其活化羧基的羧基碳原子进行亲核进攻生成酰胺键。由此所得的连接产物是N端和C端都带有保护基的保护肽,要脱去保护基后才能得到自由的肽。如果肽链不是到此为止,而是还需要从N端或C端延长肽链的话,则可以先选择性地脱去X或Q,然后再同新的N保护氨基酸(或肽)或C保护的氨基酸(或肽)进行第二次连接,并依次不断重复下去,直到所需要的肽链长度为止。对于长肽的多肽合成来说,一般有逐步增长和片段缩合两种伸长肽链的方式,前者是由起始的氨基酸(或肽)开始。每连接一次,接长一个氨基酸,后者则是用N保护肽同C保护肽缩合来得到两者长度相加的新的长肽链。对于多肽合成中含有谷氨酸、天冬氨酸、赖氨酸、精氨酸、组氨酸、半胱氨酸等等带侧链功能团的氨基酸的肽来说,为了避免由于侧链功能团所带来的副反应,一般也需要用适当的保护基将侧链基团暂时保护起来。多肽合成方法分类多肽的合成主要分为两条途径:化学合成多肽和生物合成多肽。化学合成主要是以氨基酸与氨基酸之间缩合的形式来进行。在合成含有特定顺序的多肽时,由于多肽合成原料中含有官能度大于2的氨基酸单体,多肽合成时应将不需要反应的基团暂时保护起来,方可进行成肽反应,这样保证了多肽合成目标产物的定向性。多肽的化学合成又分为液相合成和固相合成。多肽液相合成主要分为逐步合成和片段组合两种策略。逐步合成简洁迅速,可用于各种生物活性多肽片段的合成。片段组合法主要包括天然化学连接和施陶丁格连接。近年,多肽液相片段合成法发展迅速,在多肽和蛋白质合成领域已取得了重大突破。在多肽片段合成法中,根据多肽片段的化学特定性或化学选择性,多肽片段能够自发进行连接,得到目标多肽。因为多肽片段含有的氨基酸残基相对较少,所以纯度较高,且易于纯化。多肽的生物合成方法主要包括发酵法、酶解法,随着生物工程技术的发展,以DNA重组技术为主导的基因工程法也被应用于多肽的合成。多肽的固相合成多肽的合成是氨基酸重复添加的过程,通常从C端向N端(氨基端)进行合成。多肽固相合成的原理是将目的肽的第一个氨基酸C端通过共价键与固相载体连接,再以该氨基酸N端为合成起点,经过脱去氨基保护基和过量的已活化的第二个氨基酸进行反应,接长肽链,重复操作,达到理想的合成肽链长度,最后将肽链从树脂上裂解下来,分离纯化,获得目标多肽。1、Boc多肽合成法Boc方法是经典的多肽固相合成法,以Boc作为氨基酸α-氨基的保护基,苄醇类作为侧链保护基,Boc的脱除通常采用三氟乙酸(TFA)进行。多肽合成时将已用Boc保护好的N-α-氨基酸共价交联到树脂上,TFA切除Boc保护基,N端用弱碱中和。肽链的延长通过二环己基碳二亚胺(DCC)活化、偶联进行,最终采用强酸氢氟酸(HF)法或三氟甲磺酸(TFMSA)将合成的目标多肽从树脂上解离。在Boc多肽合成法中,为了便于下一步的多肽合成,反复用酸进行脱保护,一些副反应被带入实验中,例如多肽容易从树脂上切除下来,氨基酸侧链在酸性条件不稳定等。2、Fmoc多肽合成法Carpino和Han以Boc多肽合成法为基础发展起来一种多肽固相合成的新方法——Fmoc多肽合成法。Fmoc多肽合成法以Fmoc作为氨基酸α-氨基的保护基。其优势为在酸性条件下是稳定的,不受TFA等试剂的影响,应用温和的碱处理可脱保护,所以侧链可用易于酸脱除的Boc保护基进行保护。肽段的最后切除可采用TFA/二氯甲烷(DCM)从树脂上定量完成,避免了采用强酸。同时,与Boc法相比,Fmoc法反应条件温和,副反应少,产率高,并且Fmoc基团本身具有特征性紫外吸收,易于监测控制反应的进行。Fmoc法在多肽固相合成领域应用越来越广泛。多肽液相分段合成随着多肽合成的发展,多肽液相分段合成(即多肽片段在溶液中依据其化学专一性或化学选择性,自发连接成长肽的合成方法)在多肽合成领域中的作用越来越突出。其特点在于可以用于长肽的合成,并且纯度高,易于纯化。多肽液相分段合成主要分为天然化学连接和施陶丁格连接。天然化学连接是多肽分段合成的基础方法,局限在于所合成的多肽必须含半光氨酸(Cys)残基,因而限定了天然化学连接方法的应用范围。天然化学连接方法的延伸包括化学区域选择连接、可除去辅助基连接、光敏感辅助基连接。施陶丁格连接方法是另一种基础的片段连接方法,其为多肽片段连接途径开拓了更广阔的思路。正交化学连接方法是施陶丁格连接方法的延伸,通过简化膦硫酯辅助基来提高片段间的缩合率。其他多肽合成方法1、氨基酸的羧内酸酐法(NCA)氨基酸的羧内酸酐的氨基保护基也可活化羧基。NCA的原理:在碱性条件下,氨基酸阴离子与NCA形成一个更稳定的氨基甲酸酯类离子,在酸化时该离子失去二氧化碳,生成二肽。生成的二肽又与其他的NCA结合,反复进行。NCA适用于短链肽片段的多肽合成,其周期短、操作简单、成本低、得到产物分子量高,在目前多肽合成中所占比例较大,技术也较为通用。2、组合化学法20世纪80年代,以固相多肽合成为基础提出了组合化学法,即氨基酸的构建单元通过组合的方式进行连接,合成出含有大量化合物的化学库,并从中筛选出具有某种理化性质或药理活性化合物的一套多肽合成策略和筛选方案。组合化学法的多肽合成策略主要包括:混合-均分法、迭代法、光控定位组合库法、茶叶袋法等。组合化学法的最大优点在于可同时合成多种化合物,并且能最大限度地筛选各种新化合物及其异构体。3、酶解法酶解法是用生物酶降解植物蛋白质和动物蛋白质,获得小分子多肽。酶解法因其多肽产量低、投资大、周期长、污染严重,未能实现工业化生产。酶解法获得的多肽能够保留蛋白质原有的营养价值,并且可以获得比原蛋白质更多的功能,更加绿色,更加健康。4、基因工程法基因工程法主要以DNA重组技术为基础,通过合适的DNA模板来控制多肽的序列合成。有研究者通过基因工程法获得了准弹性蛋白-聚缬氨酸-脯氨酸-甘氨酸-缬氨酸-甘氨酸肽(VPGVG)。利用基因工程技术生产的活性多肽还有肽类抗生素、干扰素类、白介素类、生长因子类、肿瘤坏死因子、人生长激素,血液中凝血因子、促红细胞生成素,组织非蛋白纤溶酶原等。基因工程法合成多肽具有表达定向性强,安全卫生,原料来源广泛和成本低等优点,但因存在高效表达,不易分离,产率低的问题,难以实现规模化生产。5、发酵法发酵法是从微生物代谢产物中获得多肽的方法。虽然发酵法的成本低,但其应用范围较窄,因为现在微生物能够独立合成的聚氨基酸只有ε-聚赖氨酸(ε-PL)、γ-聚谷氨酸(γ-PGA)和蓝细菌肽。[align=center][img=,770,348]https://ng1.17img.cn/bbsfiles/images/2019/03/201903151633244062_8177_3531468_3.jpg!w770x348.jpg[/img][/align]请移步百度搜“合肥国肽生物”即可我们主要提供:多肽合成、定制多肽、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。
请大神解答:饮料中合成着色剂前处理采用安谱固相萃取柱方法提取.加标.标曲都用同一来源.但是回收率居高不下一直在120%左右.前处理过程包括去离子水超声提取.过柱子.氮吹.水复溶.过膜.严格按照说明书.回收率过高是什么原因造成的?
众所周知,有机化学特别是有机合成化学是一门发展得比较完备的学科。在人类文明史上,它对提高人类的生活质量作出了巨大的贡献.然而,不可否认,“传统”的合成化学方法以及依其建立起来的“传统”合成化学工业,对整个人类赖以生存的生态环境造成了严重的污染和破坏。以往解决问题的主要手段是治理、停产、甚至关闭,人们为治理环境污染花费了大量的人力、物力和财力。20世纪90年代初,化学家提出了与传统的“治理污染”不同的“绿色化学”的概念,即如何从源头上减少、甚至消除污染的产生。通过研究和改进化学化工过程及相应的工艺技术,从根本上降低、以至消除副产品或废弃物的生成,从而达到保护和改善环境的目的.“绿色化学”的目标要求任何一个化学的活动,包括使用的化学原料、化学和化工过程、以及最终的产晶,对人类的健康和环境都应该是友好的。因而,绿色化学的研究成果对解决环境问题是有根本意义的。对于环境和化工生产的可持续发展也有着重要的意义。十几年来,关于绿色化学的概念、目标、基本原理和研究领域等已经迈步明确,初步形成了一个多学科交叉的新的研究领域。具体来说,绿色化学的基本原理可以有以下几个方面:1)防止污染的产生优于治理产生的污染;2)原子经济性;3)只要可行,应尽量采用毒性小的化学合成路线:4)更安全的化学晶的设计应能保留其功效,但降低毒性;5)应尽可能避免使用辅助物质(如溶剂、分离剂等),如用时应是无毒的;6)应考虑到能源消耗对环境和经济的影响,并应尽量少地使用能源;7)原料应是可再生的,而非将耗竭的;8)尽量避免不必要的衍生化步骤;9)催化性试剂(有尽可能好的选择性)优于当量性试剂;10)化工产品在完成其使命后,不应残留在环境中,而应能降解为无害的物质:11)分析方法必须进一步发展,以使在有害物质生成前能够进行即时的和在线跟踪及控制:12)在化学转换过程中,所选用的物质和物质的形态应能尽可能地降低发生化学事故的可能性。1995年美国设立了总统绿色化学挑战奖,旨在奖励在创造性地研究、开发和应用绿色化学基本原理方面获得杰出成就的个人、集体或组织。共有五个奖项:学术奖(Academic Award)、中小企业奖(Small Business Award)、新合成路线奖(Alternative Synthetic Pathways Award)、新工艺奖(Alternative Solvent/Reaction Conditions Award)和安全化学品设计奖(Designing Safer Chemicals Award)。从设立的奖项和历届获奖的研究成果也可以大致了解绿色化学所涵盖的范围。从根本上说,绿色化学是要求化学家从一个崭新的角度来审视“传统”的化学研究和化工过程,并以“与环境友好”为基础和出发点提出新的化学问题,创造出新的化工技术。作为一个多学科交叉的新的研究领域,绿色化学尚有许多基本的科学问题需要深入研究。这里,仅就作者比较熟悉的绿色化学中的有机合成方面的问题提出看法,供大家参考和讨论。
请问:在氯硅烷合成过程中会产生哪些含碳化合物?分子式是什么?
在微波加热过程中,若设定的温度为60度,那么不管反应物质和介质的混合液的温度是40还是30,整个过程中受到微波辐射对合成的作用和影响是一样的还是有较大差别的?另外,假若混合液的温度加到60度以后,是否接受的微波辐射的效果相当于保温的辐射效果呢,如果是这样,是否该状态下的辐射强度和加热时的辐射强度有差别?哪位朋友能帮助我解答一下,万分感谢。
我是做合成中试工作。在工作中经常遇到产品检测项目不合格的问题,在分析、解决这些问题的过程中需要了解该项目的分析方法和一些理论知识,这个时候就会感觉比较乏力,希望能够系统的学习一下各种化学分析和仪器分析的理论知识,希望大家给推荐几本这方面的书!谢谢
概 述 从真核生物的组织或细胞中提取mRNA,通过酶促反应逆转录合成cDNA的第一链和第二链,将双链cDNA和载体连接,然后转化扩增,即可获得cDNA文库,构建的cDNA文库可用于真核生物基因的结构、表达和调控的分析;比较cDNA和相应基因组DNA序列差异可确定内含子存在和了解转录后加工等一系列问题。总之cDNA的合成和克隆已成为当今真核分子生物学的基本手段。自70年代中叶首例cDNA克隆问世以来,已发展了许多种提高cDNA合成效率的方法,并大大改进了载体系统,目前cDNA合成试剂已商品化。cDNA合成及克隆的基本步骤包括用反转录酶合成cDNA第一链,聚合酶合成cDNA第二链,加入合成接头以及将双链DNA克隆到于适当载体(噬菌体或质粒)。 一、RNA制备 模板mRNA的质量直接影响到cDNA合成的效率。由于mRNA分子的结构特点,容易受RNA酶的攻击反应而降解,加上RNA酶极为稳定且广泛存在,因而在提取过程中要严格防止RNA酶的污染,并设法抑制其活性,这是本实验成败的关键。所有的组织中均存在RNA酶,人的皮肤、手指、试剂、容器等均可能被污染,因此全部实验过程中均需戴手套操作并经常更换(使用一次性手套)。所用的玻璃器皿需置于干燥烘箱中200℃烘烤2小时以上。凡是不能用高温烘烤的材料如塑料容器等皆可用0.1%的焦碳酸二乙酯(DEPC)水溶液处理,再用蒸馏水冲净。DEPC是RNA酶的化学修饰剂,它和RNA酶的活性基团组氨酸的咪唑环反应而抑制酶活性。DEPC与氨水溶液混合会产生致癌物,因而使用时需小心。试验所用试剂也可用DEPC处理,加入DEPC至0.1%浓度,然后剧烈振荡10分钟,再煮沸15分钟或高压灭菌以消除残存的DEPC,否则DEPC也能和腺嘌呤作用而破坏mRNA活性。但DEPC能与胺和巯基反应,因而含Tris和DTT的试剂不能用DEPC处理。Tris溶液可用DEPC处理的水配制然后高压灭菌。配制的溶液如不能高压灭菌,可用DEPC处理水配制,并尽可能用未曾开封的试剂。除DEPC外,也可用异硫氰酸胍、钒氧核苷酸复合物、RNA酶抑制蛋白等。此外,为了避免mRNA或cDNA吸附在玻璃或塑料器皿管壁上,所有器皿一律需经硅烷化处理。 细胞内总RNA制备方法很多,如异硫氰酸胍热苯酚法等。许多公司有现成的总RNA提取试剂盒,可快速有效地提取到高质量的总RNA。分离的总RNA可利用mRNA 3'末端含有多聚(A)+ 的特点,当RNA流经oligo(dT)纤维素柱时,在高盐缓冲液作用下,mRNA被特异的吸附在oligo(dT)纤维素上,然后逐渐降低盐浓度洗脱,在低盐溶液或蒸馏水中,mRNA被洗下。经过两次oligo(dT)纤维素柱,可得到较纯的mRNA。纯化的mRNA在70%乙醇中-70℃可保存一年以上。

多肽合成方法分类多肽的合成主要分为两条途径:化学合成多肽和生物合成多肽。化学合成主要是以氨基酸与氨基酸之间缩合的形式来进行。在合成含有特定顺序的多肽时,由于多肽合成原料中含有官能度大于2的氨基酸单体,多肽合成时应将不需要反应的基团暂时保护起来,方可进行成肽反应,这样保证了多肽合成目标产物的定向性。多肽的化学合成又分为液相合成和固相合成。【合肥国肽生物】多肽液相合成主要分为逐步合成和片段组合两种策略。逐步合成简洁迅速,可用于各种生物活性多肽片段的合成。片段组合法主要包括天然化学连接和施陶丁格连接。近年,多肽液相片段合成法发展迅速,在多肽和蛋白质合成领域已取得了重大突破。在多肽片段合成法中,根据多肽片段的化学特定性或化学选择性,多肽片段能够自发进行连接,得到目标多肽。因为多肽片段含有的氨基酸残基相对较少,所以纯度较高,且易于纯化。多肽的生物合成方法主要包括发酵法、酶解法,随着生物工程技术的发展,以DNA重组技术为主导的基因工程法也被应用于多肽的合成。多肽的固相合成多肽的合成是氨基酸重复添加的过程,通常从C端向N端(氨基端)进行合成。多肽固相合成的原理是将目的肽的第一个氨基酸C端通过共价键与固相载体连接,再以该氨基酸N端为合成起点,经过脱去氨基保护基和过量的已活化的第二个氨基酸进行反应,接长肽链,重复操作,达到理想的合成肽链长度,最后将肽链从树脂上裂解下来,分离纯化,获得目标多肽。1、Boc多肽合成法Boc方法是经典的多肽固相合成法,以Boc作为氨基酸α-氨基的保护基,苄醇类作为侧链保护基,Boc的脱除通常采用三氟乙酸(TFA)进行。多肽合成时将已用Boc保护好的N-α-氨基酸共价交联到树脂上,TFA切除Boc保护基,N端用弱碱中和。肽链的延长通过二环己基碳二亚胺(DCC)活化、偶联进行,最终采用强酸氢氟酸(HF)法或三氟甲磺酸(TFMSA)将合成的目标多肽从树脂上解离。在Boc多肽合成法中,为了便于下一步的多肽合成,反复用酸进行脱保护,一些副反应被带入实验中,例如多肽容易从树脂上切除下来,氨基酸侧链在酸性条件不稳定等。2、Fmoc多肽合成法Carpino和Han以Boc多肽合成法为基础发展起来一种多肽固相合成的新方法——Fmoc多肽合成法。Fmoc多肽合成法以Fmoc作为氨基酸α-氨基的保护基。其优势为在酸性条件下是稳定的,不受TFA等试剂的影响,应用温和的碱处理可脱保护,所以侧链可用易于酸脱除的Boc保护基进行保护。肽段的最后切除可采用TFA/二氯甲烷(DCM)从树脂上定量完成,避免了采用强酸。同时,与Boc法相比,Fmoc法反应条件温和,副反应少,产率高,并且Fmoc基团本身具有特征性紫外吸收,易于监测控制反应的进行。Fmoc法在多肽固相合成领域应用越来越广泛。多肽液相分段合成随着多肽合成的发展,多肽液相分段合成(即多肽片段在溶液中依据其化学专一性或化学选择性,自发连接成长肽的合成方法)在多肽合成领域中的作用越来越突出。其特点在于可以用于长肽的合成,并且纯度高,易于纯化。多肽液相分段合成主要分为天然化学连接和施陶丁格连接。天然化学连接是多肽分段合成的基础方法,局限在于所合成的多肽必须含半光氨酸(Cys)残基,因而限定了天然化学连接方法的应用范围。天然化学连接方法的延伸包括化学区域选择连接、可除去辅助基连接、光敏感辅助基连接。施陶丁格连接方法是另一种基础的片段连接方法,其为多肽片段连接途径开拓了更广阔的思路。正交化学连接方法是施陶丁格连接方法的延伸,通过简化膦硫酯辅助基来提高片段间的缩合率。其他多肽合成方法1、氨基酸的羧内酸酐法(NCA)氨基酸的羧内酸酐的氨基保护基也可活化羧基。NCA的原理:在碱性条件下,氨基酸阴离子与NCA形成一个更稳定的氨基甲酸酯类离子,在酸化时该离子失去二氧化碳,生成二肽。生成的二肽又与其他的NCA结合,反复进行。NCA适用于短链肽片段的多肽合成,其周期短、操作简单、成本低、得到产物分子量高,在目前多肽合成中所占比例较大,技术也较为通用。2、组合化学法20世纪80年代,以固相多肽合成为基础提出了组合化学法,即氨基酸的构建单元通过组合的方式进行连接,合成出含有大量化合物的化学库,并从中筛选出具有某种理化性质或药理活性化合物的一套多肽合成策略和筛选方案。组合化学法的多肽合成策略主要包括:混合-均分法、迭代法、光控定位组合库法、茶叶袋法等。组合化学法的最大优点在于可同时合成多种化合物,并且能最大限度地筛选各种新化合物及其异构体。3、酶解法酶解法是用生物酶降解植物蛋白质和动物蛋白质,获得小分子多肽。酶解法因其多肽产量低、投资大、周期长、污染严重,未能实现工业化生产。酶解法获得的多肽能够保留蛋白质原有的营养价值,并且可以获得比原蛋白质更多的功能,更加绿色,更加健康。4、基因工程法基因工程法主要以DNA重组技术为基础,通过合适的DNA模板来控制多肽的序列合成。有研究者通过基因工程法获得了准弹性蛋白-聚缬氨酸-脯氨酸-甘氨酸-缬氨酸-甘氨酸肽(VPGVG)。利用基因工程技术生产的活性多肽还有肽类抗生素、干扰素类、白介素类、生长因子类、肿瘤坏死因子、人生长激素,血液中凝血因子、促红细胞生成素,组织非蛋白纤溶酶原等。基因工程法合成多肽具有表达定向性强,安全卫生,原料来源广泛和成本低等优点,但因存在高效表达,不易分离,产率低的问题,难以实现规模化生产。5、发酵法发酵法是从微生物代谢产物中获得多肽的方法。虽然发酵法的成本低,但其应用范围较窄,因为现在微生物能够独立合成的聚氨基酸只有ε-聚赖氨酸(ε-PL)、γ-聚谷氨酸(γ-PGA)和蓝细菌肽。[img=,457,333]https://ng1.17img.cn/bbsfiles/images/2019/04/201904221507346400_2482_3531468_3.jpg!w457x333.jpg[/img]我们主要提供:多肽合成、定制多肽、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。合肥国肽生物官网:http://www.bankpeptide.com欢迎咨询服务热线:17718122172;17718122684;17730030476;17718122397
合成肽技术用化学手段将氨基酸依次定向地缩合成多肽或蛋白质的技术。大多数天然多肽和蛋白质都由a-氨基酸构成。氨基酸分子内可有3个化学活泼的基团即侧链、氨基及羧基,与a-碳原子共价连接。请移步百度搜“[b]合肥国肽生物[/b]”即可化学合成肽有两类基本方法液相法即反应物在完全溶解状态下作均相缩合。由于每步缩合产物都可经结晶或洗涤过程去除副产物,故液相合成肽的质量较高,但耗时多,手续繁,产率较低。1965年中国科学家以此法合成了结晶牛胰岛素。目甑助产药物——催产素(一个九肽)的工厂生产流程仍采取液相法工艺。固相法反应物之一取固相状态。反应产物因共价连接于树脂而可被过滤法回收并洗涤除去未反应物,故操作简单,易于规范化和机械化,事实上,固相多肽合成仪已被广泛采用。此法缺点在于副反应物会在树脂上不断积累,难以去除。且反应次数越多即目标肽越长则副产物积累越多,最后至造成主产物被淹没在杂质中无法被分离出来。所以这个方法的创立虽然促使迈利菲尔特(R.B.Merrifield)获得了诺贝尔化学奖,但实用中仍限于30肽左右的合成水平上。为了克服这一缺点,有人利用液相法合成高纯度的小肽进行固相缩合,使总的固相缩合次数减少,这就成为固相片段缩合法。中国利用此法已成功地合成了结晶胰岛高血糖素和蛇毒膜毒素等大肽和蛋白质。除化学方法外,利用蛋白水解酶的逆反应也可酶促合成某些特定的肽键。
[b][font=微软雅黑]矿物油:[/font][/b][font=微软雅黑]通常是指经过开采和初加工的原油(或石油),mineral oil,石油是埋藏于地下的天然矿产物,经过勘探、开采出的未经炼制的石油也叫做原油。[/font][font=微软雅黑]在常温下,原油经过炼制后的成品叫做石油产品。依据习惯,把通过物理蒸馏方法从石油中提炼出的基础油称为矿物油基础油。提炼加工过程主要是将原油分成不同的部分以得到所需产品。主要的分离过程包括将原油分离成粗汽油、粗煤油、粗柴油、重柴油、各种润滑油馏分、裂化原料油及渣油(又称残油)的蒸馏分离和将各种润滑油提纯所使用的溶剂分离。生产过程基本以物理过程为主,不改变烃类结构,生产的基础油取决于原料中理想组分的含量与性质 矿物油在提炼过程中因无法将所含的杂质清除干净,因此得到的基础油流动点较高,不适合寒带作业使用 因此,矿物油类基础油在性质上受到一定限制。[/font][b][font=微软雅黑]合成油:[/font][/b][font=微软雅黑]通过化学合成或精炼加工的方法获得的,其工艺复杂,炼制成本高昂,拥有矿物油不可比拟的优势:合成油的黏度指数更高,所以黏温特性更好,高温时润滑更充足,低温下流动性好(室温条件下外观感觉比同级别矿物油稀)。同时用合成油调配的机油抗氧化性更强,大大地延长了换油周期,虽然在机油上增加了投入,但减少了更换机油和滤清器的次数。合成油因其蒸发损失小,所以机油消耗低,减少了添加机油的繁琐,并且能更好地保护三元催化器等昂贵的废气控制系统部件。[/font][font=微软雅黑]此外,合成油适应更高负荷的发动机,还拥有更强的抗高温抗剪切能力,在发动机高速运转下,机油也不会损失黏度,对发动机的保护更全面。 合成型基础油来自原油中的瓦斯气或天然气所分散出来的乙烯、丙烯,再经聚合、催化等繁复的化学反应(费托合成技术,即 GTL 技术)才炼制成大分子组成的基础油。在本质上,它使用的是原油中较好的成分,加以化学反应并通过人为控 制达到预期的分子形态,其分子排列整齐,抵抗外来变数的能力自然很强,因此合成油品质较好,其对热稳定、抗氧化反应、抗黏度变化的能力自然要比矿物油强得多。[/font]
第一节 类型衍生化与系列设计新药开发途径可分为两方面:一是寻求新的模型化合物,确定显效化学结构,获得新结构的化合物,称作类型衍化(Lead generation)。另一则在某一确定模型化合物基础上,寻求系列中最佳化合物,称作最佳化合物设计(Lead optimization)或系列设计(Series design)。系列设计为类型衍化的继续和发展;类型衍化则为系列设计开辟新的设计条件和领域,两者相辅相成,各有其重要作用。一、类型衍化:模型化合物,就是可以用来作为进行结构修饰和结构改造的模型,从中可获得预期药理作用的药物。随着多种模型化合物化学结构的剖析,选择可能的显效化学结构,确定合成对象,进行合成与药效筛选,进而确定显效结构及新的模型化合物。模型化合物有多种发掘途径,以代谢过程、生命基础过程研究、受体契合方法及现有药物结构的总结性研究最为瞩目。以某种或多种模型化合物为对象,从受体模式等药理作用、构效关系(SAR)一般规律及QSAR方法、分子特征分析与三维立体结构选择等方面进行显效的基本结构与三维立体构型和构象的诸种设想,采用计算机进行适当运算,拟定可能具有活性的不同结构类型,并从取代基选择拟定不同类型的有关化合物。在合成对象初步拟定后,由合成设计考查合成的可能性,然后进行合成。同时可拟定这些化合物的化学结构因素并赋值,再进行选择。此外,拟定生物活性测试的有关指标并测得数值。在此基础上,运用统计数学计算方法进行结构类型分类,选出有显著活性的化学结构类型,为系列设计奠定化学结构基础。二、系列设计:显著活性的化学结构类型确定后,即可进行最佳化合物的(系列)设计。基本内容有:(1)合成对象选择。以活性显著的结构类型为基础,结合药理作用,分子特征分析,SAR一般规律及QSAR结果,取代基聚类分析与三维立体结构研究,运用计算机进行恰当选择,确定基本结构、取代基、立体构型及构象,拟定应合成的化学结构与化合物。(2)由合成设计考查合成的可能性。(3)拟定生物活性测试指标及方法,并进行测定。(4)化学结构参数的选择。物化参数、量子化学参数、拓朴参数及化学结构标示符等均可用作参数,通过统计数学方法(聚类分析与因子分析)以选择和确定进入QSAR计算前的诸种参数。(5)QSAR方程的求得。采用逐步回归分析和逐步判别分析等等统计数学方法进行。(6)活性预计及新合成对象的确定。选择预计活性较强的化合物进行第二或第三轮的合成与试验。一般循环二至三轮即可获得最佳活性化合物。类型衍化中活性结构的选择也与QSAR有关。

[font=宋体][size=10.5000pt][font=宋体]多肽固相合成法是多肽合成化学的一个重大的突破。它的最大特点是不必纯化中间产物,合成过程可以连续进行,进而为多肽合成的自动化奠定了基础。目前全自动多肽的合成,基本都是固相合成。其基本过程如下:[/font] [/size][/font][font=宋体][size=10.5000pt][font=宋体]基于[/font]Fmoc[font=宋体]化学合成,先将所要合成的目标多肽的[/font][font=Calibri]C-[/font][font=宋体]端氨基酸的羧基以共价键形式与一个不溶性的高分子树脂相连,然后以这一氨基酸的氨基作为多肽合成的起点,同其它的氨基酸已经活化的羧基作用形成肽键,不断重复这一过程,即可得到多肽。【详情请咨询国肽生物】根据多肽的氨基酸组成不同,多肽后处理方式不同,纯化方式也有差异。 [/font][/size][/font][font=宋体][size=10.5000pt]1.[font=宋体]做免疫用的多肽多长为合适[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]一般约[/font]10-15[font=宋体]个氨基酸,当然长一些免疫效果好一些,不过合成费用也会增加。[/font][font=Calibri]MAP[/font][font=宋体]多肽则希望长度在[/font][font=Calibri]15aa[/font][font=宋体]以上,效果较好。另外,[/font][font=Calibri]10aa[/font][font=宋体]以下的多肽免疫效果比较差。 [/font][/size][/font][font=宋体][size=10.5000pt]2.[font=宋体]免疫用多肽的纯度需要很高吗[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]一般而言,免疫用[/font]Peptide[font=宋体],[/font][font=Calibri]70-85%[/font][font=宋体]即可。 [/font][/size][/font][font=宋体][size=10.5000pt]3.[font=宋体]我们合成的多肽溶解性不好,多肽就有问题对吗[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]很难准确预测一个多肽的溶解性及合适的溶剂是什么。如果多肽难以溶解就认为多肽合成有问题这个观念并不正确。[/font] [/size][/font][font=宋体][size=10.5000pt]4.[font=宋体]多肽状态是如何[/font][font=Calibri]?[/font][font=宋体]如何保存储存[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]我们提供的多肽是粉末状,一般为灰白色,组成不同,多肽粉末的颜色有差异,多肽一般长期保存需要避光保存,并应保存在[/font]-20[font=宋体]度,短期可以保存在[/font][font=Calibri]4[/font][font=宋体]度。可以短时间的话是以室温运输。 [/font][/size][/font][font=宋体][size=10.5000pt]5.[font=宋体]如何溶解多肽[/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]溶解多肽是非常复杂的事情,一般很难一下子确定合适的溶剂。通常是先取一点试验,在没有确定合适的溶剂前千万不要合部溶解。[/font] [font=宋体]下列方法有助于您选择合适的溶剂:[/font] [/size][/font][font=宋体][size=10.5000pt](1)[font=宋体]判定多肽的电荷特定,设定酸性氨基酸[/font][font=Calibri]Asp(D),Glu(E)[/font][font=宋体]和[/font][font=Calibri]C[/font][font=宋体]端[/font][font=Calibri]COOH[/font][font=宋体]为[/font][font=Calibri]-1[/font][font=宋体];碱性氨基酸[/font][font=Calibri]Lys(K),Arg(R),His(H)[/font][font=宋体]及[/font][font=Calibri]N[/font][font=宋体]端[/font][font=Calibri]NH2[/font][font=宋体]为[/font][font=Calibri]+1,[/font][font=宋体]其它氨基酸的电荷为[/font][font=Calibri]0[/font][font=宋体]。计算出将电荷数。 [/font][/size][/font][font=宋体][size=10.5000pt](2)[font=宋体]如果净电荷数[/font][font=Calibri]0[/font][font=宋体],多肽为碱性,用水溶解:如果不溶解或溶解性不大,加入醋酸[/font][font=Calibri](10%[/font][font=宋体]以上[/font][font=Calibri])[/font][font=宋体];如果多肽还不能溶解,加入少量[/font][font=Calibri]TFA(25ul)[/font][font=宋体]溶解,然后加入[/font][font=Calibri]500ul[/font][font=宋体]水稀释。 [/font][/size][/font][font=宋体][size=10.5000pt](3)[font=宋体]如果净电荷数[/font][font=Calibri]0[/font][font=宋体],多肽为酸性,用水溶解;如果不溶解或溶解性不大,加入氨水[/font][font=Calibri](25ul)[/font][font=宋体]溶解,然后加入[/font][font=Calibri]500ul[/font][font=宋体]水稀释。 [/font][/size][/font][font=宋体][size=10.5000pt](4)[font=宋体]如果净电荷数[/font][font=Calibri]=0[/font][font=宋体],多肽为中性,一般需要用有机溶剂如乙腈,甲醇或异丙醇,[/font][font=Calibri]DMSO[/font][font=宋体]等溶解。还有人建议需要尿素来溶解疏水性很大的多肽。[/font][/size][/font][font=宋体][size=10.5000pt]6.[font=宋体]非[/font][font=Calibri]HPLC[/font][font=宋体]纯化的多肽中有哪些杂质[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]粗品和脱盐级别的多肽中多肽和非多肽类杂质:如非全长多肽和多肽后处理的一些原料如[/font]DTT[font=宋体]、[/font][font=Calibri]TFA[/font][font=宋体]等。 [/font][/size][/font][font=宋体][size=10.5000pt]7.HPLC[font=宋体]纯化的多肽有哪些杂质[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]经过[/font]HPLC[font=宋体]纯化的多肽,仍会有一些一些杂质存在,其中的杂质主要是短肽和微量[/font][font=Calibri]TFA[/font][font=宋体]。 [/font][/size][/font][font=宋体][size=10.5000pt]8.[font=宋体]多长的多肽为合适[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]多肽合成需要考虑多肽的长度,电荷,亲疏水性等因素。长度越长,合成粗品的纯度和产率都随着降低,纯化的难度和无法合成的几率就会大些。当然多肽功能区的序列是无法改变的,但是为了多肽的顺利合成,有时不得不在功能取的上下游增加一些辅助氨基酸,以改善多肽的溶解性和亲疏水性。如果多肽太短,合成也可能有问题,主要问题是合成的多肽在后处理过程中有一定的难度,[/font]5[font=宋体]肽以下的多肽,一般要有疏水的氨基酸,否则后处理难度加大。[/font][font=Calibri]15[/font][font=宋体]个氨基酸残基以下的多肽一般都可以得到满意的产率和得率。 [/font][/size][/font][font=宋体][size=10.5000pt]9.[font=宋体]如何从多肽序列中判定多肽的溶解性[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt](1)[font=宋体]多肽中如果含有高比例的疏水性很强的氨基酸如和[/font][font=Calibri]Leu,Val,IIe,Met,Phe[/font][font=宋体]和[/font][font=Calibri]Trp[/font][font=宋体],多肽很难溶解与水性溶液中或根本不可能溶解。这些氨基酸无论是纯化或合成,都有可能有问题。 [/font][/size][/font][font=宋体][size=10.5000pt](2)[font=宋体]一般情况下疏水性氨基酸的比例[/font][font=Calibri]50%[/font][font=宋体],不能连续[/font][font=Calibri]5[/font][font=宋体]个连续[/font][font=Calibri]aa[/font][font=宋体]为疏水性,带电荷的氨基酸的[/font][font=Calibri]([/font][font=宋体]正电荷[/font][font=Calibri]K,R,H,N-terminus,[/font][font=宋体]负电荷[/font][font=Calibri]D,E,C- terminus)[/font][font=宋体]的比例达到[/font][font=Calibri]20%[/font][font=宋体],在多肽的[/font][font=Calibri]N[/font][font=宋体]或[/font][font=Calibri]C[/font][font=宋体]短如果能增加极性氨基酸,也可以改善溶解性。 [/font][font=Calibri]11.[/font][font=宋体]为什么含有[/font][font=Calibri]Cys,Met,[/font][font=宋体]或[/font][font=Calibri]Trp[/font][font=宋体]的多肽难合成[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]含有[/font]Cys,Met[font=宋体],或[/font][font=Calibri]Trp[/font][font=宋体]的多肽难以合成,同时难以获得高纯度的产品。主要因为这些基团不稳定,易氧化。这些多肽的使用和储存都需要特别注意,避免反复开启盖子。 [/font][/size][/font][font=宋体][size=10.5000pt]10.[font=宋体]为什么有些多肽的合成产率或纯度会比较低[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]多肽合成与引子合成有比较大的区别,不能合成的引子很少,但是不能合成的多肽经常有。如[/font]Val,Ile,Tyr,Phe,Trp,Leu,Gln,[font=宋体]和[/font][font=Calibri]Thr[/font][font=宋体]这些氨基酸比邻或重复时,多肽链在合成过程中不能完全舒展溶解,合成效率下降。以下几种情形,合成效率和产物的纯度都比较低,如:重复[/font][font=Calibri]Pro,Ser-Ser[/font][font=宋体],重复[/font][font=Calibri]Asp[/font][font=宋体],[/font][font=Calibri]4[/font][font=宋体]个连续[/font][font=Calibri]Gly[/font][font=宋体]等。 [/font][/size][/font][font=宋体][size=10.5000pt]11.[font=宋体]多肽是如何纯化的[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]多肽纯化一般使用反相柱[/font]([font=宋体]如[/font][font=Calibri]C8[/font][font=宋体],[/font][font=Calibri]C18[/font][font=宋体]等[/font][font=Calibri])[/font][font=宋体],[/font][font=Calibri]214nm[/font][font=宋体]。缓冲体系通常为含[/font][font=Calibri]TFA[/font][font=宋体]的溶剂,[/font][font=Calibri]pH2.0[/font][font=宋体]。[/font][font=Calibri]Buffer A[/font][font=宋体]为含[/font][font=Calibri]0.1%TFA in ddH2O[/font][font=宋体],[/font][font=Calibri]Buffer B[/font][font=宋体]为[/font][font=Calibri]1%TFA/ACN/pH2.0[/font][font=宋体]。纯化前用[/font][font=Calibri]Buffer A[/font][font=宋体]溶解;如果溶解不好,用[/font][font=Calibri]Buffer B[/font][font=宋体]溶解后,然后用[/font][font=Calibri]Buffer A[/font][font=宋体]稀释;对疏水性强的多肽,有时还需要加入少量的[/font][font=Calibri]Formic Acid[/font][font=宋体]或醋酸。[/font][font=Calibri]HPLC[/font][font=宋体]分析多肽粗产物,如果多肽不长[/font][font=Calibri](15aa[/font][font=宋体]以下[/font][font=Calibri])[/font][font=宋体],一般会有主峰,主峰通常为全长产物;对于[/font][font=Calibri]20aa[/font][font=宋体]以上的长肽,如果没有主峰,[/font][font=Calibri]HPLC[/font][font=宋体]需搭配[/font][font=Calibri]Mass[/font][font=宋体]来判定分子量,进而确定哪个峰是所要合成的多肽。[/font][/size][/font][font=宋体][size=10.5000pt][font=宋体][img=,690,143]https://ng1.17img.cn/bbsfiles/images/2020/07/202007091611507608_3379_3531468_3.jpg!w690x143.jpg[/img][/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]国肽生物主要提供:多肽合成、多肽定制、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、美容肽、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。详情请咨询国肽生物[/font][/size][/font]