有关水中多环芳烃痕量富集技术最新进展资料
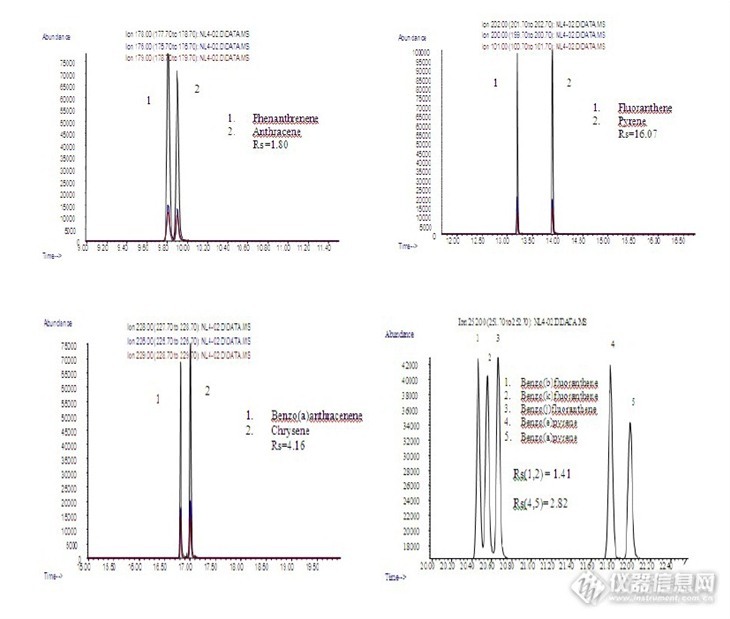
顶空固相微萃取-[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]串联质谱法检测石油样品中的痕量多环芳烃文章图片多环芳烃(polycyclic aromatic hydrocarbons, PAHs)是煤、石油、木材、烟草、有机高分子化合物等有机物不完全燃烧时产生的挥发性碳氢化合物, 广泛分布于天然环境中, 属于持久有机污染物, 具有极强的致癌毒性。迄今已发现有200多种PAHs, 有相当部分具有致癌性, 其中常见的有16种同类物质[sup][[url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226.html#b1-1008-3650-43-3-226]1[/url]][/sup]。石油是多环芳烃在自然界的主要存在源, 在与石油相关的案件中, 多环芳烃痕量组分的检测是石油检测的一个重点。近年来, 顶空固相微萃取(HS-SPME)技术逐渐被人们关注, 因其集取样、萃取及富集于一体, 萃取快速、操作简单, 便于实现自动化而广泛用于挥发性物质分析研究中。多采用固相微萃取-[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用[/color][/url]技术进行检测, 但单级质谱技术的分析灵敏度较低, 不能满足痕量组分的检测。本文在文献报道[sup][[url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226.html#b2-1008-3650-43-3-226]2[/url], [url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226.html#b3-1008-3650-43-3-226]3[/url], [url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226.html#b4-1008-3650-43-3-226]4[/url]][/sup]基础上, 利用顶空固相微萃取-[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]-三重四极杆串联质谱(GC/MS/MS)方法, 对石油中的16种多环芳烃, 采用多离子反应监测(MRM)技术, 选择适当的母离子进行二次质谱分析, 获得了比单级质谱选择离子检测(SIM)技术更多的碎片信息(母离子加子离子), 同时有效去除了基质离子和其它物质的干扰, 为石油样品中的多环芳烃痕量组分的检测提供了方法和依据。[color=#333333]1 材料与方法[/color][size=14px][color=#333333]1.1 仪器与试剂[/color][/size]Bruker SCION TQ-456GC 三重四极杆[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]/质谱联用仪及液体-顶空-固相微萃取三合一自动进样器(美国, 布鲁克公司) 固相微萃取装置:65 μ m PDMS/DVB、100 μ m PDMS和85 μ m PA 3种萃取头(美国, supelco公司)。16种 PAHs混合标准溶液40 mg/L(美国, sigma-Aldrich公司) 晕苯标准溶液0.5 mg/mL(美国, sigma-Aldrich公司)。尾油样品:原样稀释10倍, 主要测定晕苯的含量 QLH样品:齐鲁尾油原样, 稀释500倍, 含烷烃与芳烃 A样品:QLH里萃取出的芳烃, 稀释约50倍 PAHs混合标准溶液配制:取适当PAHs标准溶液与晕苯标准溶液混合, 配制成浓度为1 mg/L的17种PAHs混合标准溶液(含内标物氘代对三联苯)。所用溶剂均为二氯乙烷。[size=14px][color=#333333]1.2 实验条件[/color][/size]1.2.1 顶空固相微萃取条件SPME萃取头(65 μ m PDMS/DVB):首次使用前于300 ℃老化1 h 萃取方式:顶空自动 搅拌速度:500 r/min 样品预热平衡时间:20 min 样品平衡和萃取温度:40 ℃ 解析温度:300 ℃ 解析时间:100 s。1.2.2 [url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]条件进样口温度:300 ℃, 不分流进样 载气流速:1 mL/min 色谱柱:VF-5MS柱 柱温:柱起始温度为70 ℃, 保持1 min, 以25 ℃/min的速率升至140 ℃, 后以10 ℃/min的速率升至 240 ℃, 再以5 ℃/min 的速率升至300 ℃, 保持7.2 min。1.2.3 质谱条件EI源 离子源温度:250 ℃ 传输线温度:290 ℃ [i]m[/i]/[i]z[/i] 50-550 碰撞气:2 mTorr 溶剂延迟:4.5 min。[size=14px][color=#333333]1.3 样品制备[/color][/size]准确移取3.00 mL待测样品于20 mL规格的顶空样品瓶中, 压紧瓶盖放入自动进样盘中, 固相微萃取借助自动进样器完成。[color=#333333]2 结果与讨论[/color][size=14px][color=#333333]2.1 质谱条件的优化[/color][/size]为获得最佳分析结果, 保证对目标物定性定量的准确性, 对待测物的母离子、产物离子、碰撞能量等质谱参数进行了优化。首先采用全扫描模式获得待测物的母离子, 再用产物离子扫描模式通过优化碰撞能量获得产物离子, 最后采用优化的质谱参数在MRM模式对待测物进行定性定量分析。经过优化, 得到了较为理想的分析结果, 优化后的质谱条件见[url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226.html#outline_anchor_11]表1[/url]。图1为1 mg/L PAHs混合标准溶液直接进样, 全扫描测定得到的总离子流图。[table=657][tr][td=1,1,140][img]http://www.xsjs-cifs.com/html_resources/images/table-icon.gif[/img][/td][td][b]表1[/b] PAHs 的MRM质谱条件[b]Table 1[/b] MRM conditions for PAHs[/td][/tr][/table][table=657][tr][td] [/td][td][list][*][url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226.html#]Figure Option[/url][url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226/img_1.png]Fig.1 Total ion chromatograms of PAHs standard solution (1 mg/L)" style="margin: 0px padding: 5px 10px box-sizing: border-box transition: all 0.3s ease 0s color: rgb(40, 117, 222) font-family: "Microsoft YaHei", 微软雅黑, SimHei, 黑体, serif text-decoration-line: none font-variant-numeric: normal font-variant-east-asian: normal font-stretch: normal line-height: normal display: block width: auto background-image: initial background-position: initial background-size: initial background-repeat: initial background-attachment: initial background-origin: initial background-clip: initial text-align: left position: relative white-space: nowrap "[/url][/list][/td][/tr][tr][td][url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226/img_1.png]Fig.1 Total ion chromatograms of PAHs standard solution (1 mg/L)" style="margin: 0px padding: 0px box-sizing: border-box transition: all 0.3s ease 0s color: rgb(34, 34, 34) font-family: "Microsoft YaHei", 微软雅黑, SimHei, 黑体, serif text-decoration-line: none line-height: 24px "[img]http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226/thumbnail/img_1.png[/img][/url][/td][td][b]图1[/b] 1 mg/L PAHs混合标准溶液总离子流[b]Fig.1[/b] Total ion chromatograms of PAHs standard solution (1 mg/L)[/td][/tr][/table][size=14px][color=#333333]2.2 顶空固相微萃取条件的优化[/color][/size]2.2.1 萃取纤维涂层的选择本实验比较了常用的100 μ m PDMS、65 μ m PDMS/DVB(MW50-300)和85 μ m PA 3种固相微萃取纤维涂层对PAHs的吸附效果, 实验表明, 萃取率大小依次为65 μ m PDMS/DVB(MW50-300) 85 μ m PA 100 μ m PDMS。因此, 本文选择65 μ m PDMS/DVB(MW50-300)作为萃取纤维涂层。2.2.2 萃取温度和时间的优化分别在30、40、50、60 ℃下进行萃取和检测, 结果表明:随着萃取温度提高, 萃取率有相应的提高, 当温度超过40 ℃后, 样品的萃取量反而减少。本实验选择40 ℃作为萃取温度。固定温度为40 ℃, 对达到吸附平衡所需时间进行考察, 改变萃取时间分别为10、20、30、40 min, 结果表明:随着萃取时间增加, 萃取率相应增加, 20 min达到吸附平衡, 因此选择萃取时间为20 min[sup][5[/sup]-[sup][url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226.html#b7-1008-3650-43-3-226]7[/url]][/sup]。[size=14px][color=#333333]2.3 线性方程、相关系数及灵敏度的检测[/color][/size]分别配制浓度为1、4、20、100、1000 μ g/L的标准混合溶液, 根据本文建立的方法进行检测。以定量离子的质谱峰面积为纵坐标([i]y[/i]), 各目标物的含量为横坐标([i]x[/i], μ g/L), 进行线性回归, 用浓度0.1μ g/L的PAHs混合标准溶液, 以S/N=3确定检出限, 以S/N=10确定定量限, 结果见[url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226.html#outline_anchor_15]表2[/url]。[table=657][tr][td=1,1,140][img]http://www.xsjs-cifs.com/html_resources/images/table-icon.gif[/img][/td][td][b]表2[/b] 多环芳烃的线性方程、相关系数、检出限、定量限[b]Table 2[/b] Linear equation, correlation coefficient, LOD and LOQ of PHAs[/td][/tr][/table][size=14px][color=#333333]2.4 样品全扫描与MRM扫描结果比较[/color][/size]比较样品全扫描与MRM扫描结果可知, MRM扫描模式能够排除复杂石油样品的基质干扰, 提高了检测的灵敏度和准确度, 避免了假阳性结果的产生[sup][[url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226.html#b8-1008-3650-43-3-226]8[/url], [url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226.html#b9-1008-3650-43-3-226]9[/url]][/sup], 结果见图2~4。[table=657][tr][td] [/td][td][list][*][url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226.html#]Figure Option[/url][url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226/img_2.png]Fig.2 Total ion chromatograms of tail oil with full and MRM scanning" style="margin: 0px padding: 5px 10px box-sizing: border-box transition: all 0.3s ease 0s color: rgb(40, 117, 222) font-family: "Microsoft YaHei", 微软雅黑, SimHei, 黑体, serif text-decoration-line: none font-variant-numeric: normal font-variant-east-asian: normal font-stretch: normal line-height: normal display: block width: auto background-image: initial background-position: initial background-size: initial background-repeat: initial background-attachment: initial background-origin: initial background-clip: initial text-align: left position: relative white-space: nowrap "[/url][/list][/td][/tr][tr][td][url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226/img_2.png]Fig.2 Total ion chromatograms of tail oil with full and MRM scanning" style="margin: 0px padding: 0px box-sizing: border-box transition: all 0.3s ease 0s color: rgb(34, 34, 34) font-family: "Microsoft YaHei", 微软雅黑, SimHei, 黑体, serif text-decoration-line: none line-height: 24px "[img]http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226/thumbnail/img_2.png[/img][/url][/td][td][b]图2[/b] 尾油样品的全扫描与MRM扫描TIC图[b]Fig.2[/b] Total ion chromatograms of tail oil with full and MRM scanning[/td][/tr][/table][table=657][tr][td] [/td][td][list][*][url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226.html#]Figure Option[/url][url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226/img_3.png]Fig.3 Total ion chromatograms of QLH tail oil with full and MRM scanning" style="margin: 0px padding: 5px 10px box-sizing: border-box transition: all 0.3s ease 0s color: rgb(40, 117, 222) font-family: "Microsoft YaHei", 微软雅黑, SimHei, 黑体, serif text-decoration-line: none font-variant-numeric: normal font-variant-east-asian: normal font-stretch: normal line-height: normal display: block width: auto background-image: initial background-position: initial background-size: initial background-repeat: initial background-attachment: initial background-origin: initial background-clip: initial text-align: left position: relative white-space: nowrap "[/url][/list][/td][/tr][tr][td][url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226/img_3.png]Fig.3 Total ion chromatograms of QLH tail oil with full and MRM scanning" style="margin: 0px padding: 0px box-sizing: border-box transition: all 0.3s ease 0s color: rgb(34, 34, 34) font-family: "Microsoft YaHei", 微软雅黑, SimHei, 黑体, serif text-decoration-line: none line-height: 24px "[img]http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226/thumbnail/img_3.png[/img][/url][/td][td][b]图3[/b] QLH尾油样品全扫描与MRM扫描TIC图[b]Fig.3[/b] Total ion chromatograms of QLH tail oil with full and MRM scanning[/td][/tr][/table][table=657][tr][td] [/td][td][list][*][url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226.html#]Figure Option[/url][url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226/img_4.png]Fig.4 Total ion chromatograms of sample A with full and MRM scanning" style="margin: 0px padding: 5px 10px box-sizing: border-box transition: all 0.3s ease 0s color: rgb(40, 117, 222) font-family: "Microsoft YaHei", 微软雅黑, SimHei, 黑体, serif text-decoration-line: none font-variant-numeric: normal font-variant-east-asian: normal font-stretch: normal line-height: normal display: block width: auto background-image: initial background-position: initial background-size: initial background-repeat: initial background-attachment: initial background-origin: initial background-clip: initial text-align: left position: relative white-space: nowrap "[/url][/list][/td][/tr][tr][td][url=http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226/img_4.png]Fig.4 Total ion chromatograms of sample A with full and MRM scanning" style="margin: 0px padding: 0px box-sizing: border-box transition: all 0.3s ease 0s color: rgb(34, 34, 34) font-family: "Microsoft YaHei", 微软雅黑, SimHei, 黑体, serif text-decoration-line: none line-height: 24px "[img]http://www.xsjs-cifs.com/article/2018/1008-3650-43-3-226/thumbnail/img_4.png[/img][/url][/td][td][b]图4[/b] 样品A全扫描与MRM扫描TIC图[b]Fig.4[/b] Total ion chromatograms of sample A with full and MRM scanning[/td][/tr][/table][color=#333333]3 结论[/color]本文采用顶空固相微萃取-[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]串联质谱方法, 通过优化萃取条件和质谱条件, 建立了一种痕量检测石油样品中的多环芳烃的简单有效的方法, 检出限和定量限测定结果表明, 方法的灵敏度高, 各PAHs化合物在10~500 μ g/L浓度范围内相关系数在0.999以上, 线性关系良好。实验结果表明顶空固相微萃取-[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]串联质谱检测具有较高的排除基质干扰能力以及灵敏度优势, 完全能满足案件中有关石油样品中的多环芳烃痕量组分的检测需求

安谱公司推出Athena PAHs 多环芳烃专用柱,用于EPA16种多环芳烃的分析。该柱子在30分钟内,完成对16种多环芳烃的完美分离,性能媲美进口品牌,价格更具优势。色谱柱编号:LAEQ-462551 标准价格:4299.00描述:Athena PAHs 多环芳烃专用柱规格:4.6 × 250mm,5um柱温:30℃标准品:HJ 478-2009 16种多环芳烃混标(美国O2si,200ug/ml于乙腈,CDGG-110124-06-1ml)流动相梯度Time(min)A 水B 乙腈0 min60%40%25 min0%100%35 min0%100%45 min60%40%流速:2.0ml/min检测器:266nm进样体积:5ul(10ppm)http://ng1.17img.cn/bbsfiles/images/2014/06/201406171530_502328_1835694_3.jpg出峰编号保留时间(min)中文名称英文名称峰面积分离度理论塔板数110.308萘Naphthalene68432050295 211.296苊烯Acenaphthylene3052
GCMS分析塑料和橡胶制品中的多环芳烃摘要:新型的Agilent J&W DB-EUPAH 气相色谱柱是用于分离多环芳烃的专用色谱柱,本文采用此专用柱建立了对塑料和橡胶制品中 20种多环芳烃进行监测的GC/MS方法;其中20种多环芳烃包括 EPA要求监测的16种PAHs和欧盟要求监测的苯并(j)荧蒽, 苯并(e)芘, 1-甲基萘和2-甲基萘。为了确保结果的准确性,还在样品中添加了5个氘代多环芳烃(Naphthalene-d8, Acenaphthene-d10, Phenanthrene-d10, Chrysene-d12和Perylene-d12)和p-Terphenyl-d14作为内标和指示物标样。所有化合物在DB-EUPAH色谱柱上都获得良好的分离,方法可靠,分析时间短,符合法规要求。前言: 多环芳烃(简称PAH) 是指两个或两个以上苯环以稠环形式相连的一类化合物,通常存在于焦油、炼油、润滑油、防锈油、橡胶、塑料制品等石化产品中。多环芳烃脂溶性高, 不易降解且易在生物体内积累, 具有致癌、致畸和致突变的作用 , 对人类健康和生态环境具有巨大的潜在危害 。美国环保总署(EPA) 1979 年确定了16 种PAHs 作为首选监测污染物;2010年1月1日起生效的欧洲议会及欧盟理事会发布的2005/ 69/ EC 指令主要针对轮胎和添加油中的PAHs 作出规定 , 该规定要求苯并芘(BaP)含量应低于1 mg/kg,同时8种 PAHs(苯并(a)芘(BaP), 苯并(e)芘(BeP),苯并(a)蒽(BaA),屈(CHR),苯并(b)荧蒽(BbFA),苯并(j)荧蒽(BjFA),苯并(k)荧蒽(BkFA),二苯并(a,h)蒽(DBAhA)总含量应低于10 mg/kg。橡胶和塑料加工过程中需要加入大量的添加剂,包括防老剂,粘合增进剂等,例如PAHs主要作为软化剂被加入橡胶。目前,关于土壤、水和食品类样品中多环芳烃的检测已有大量报道,
做的是多环芳烃EPA16,目前有[font=&]氘代内标(菲-D10,芘-D12),想用菲-D10(3环)来校正2-3环的多环芳烃(在开始时加入,每次计算回收率校正数据),用芘-D12(4环)来校正4-6环多环芳烃,请问这种做法可以吗?各种氘代多环芳烃内标具体可以监测那些多环芳烃呢?有无明确要求呢?是每一个环数的多环芳烃都要有氘代内标吗?(高环数氘代内标太贵了)[/font]
求助:多环芳烃的ACCUracy PE sample 多环芳烃好做吗?
用多环芳烃的混标做标准曲线,其中16重组分分离度良好(未添加内标和替代物)。屈和苯并a蒽在285度左右出峰。用半挥发性有机物混标几十种的混标外加内标和替代物,进样。最后有两个多环芳烃,屈和苯并a蒽在245度左右出峰,但是降低出峰温度两种物质还是分不开。想请问还能怎么调整分析方式,使混标中这两个物质分开。。。
HJ 478-2009水质 多环芳烃的测定 高效液相色谱法中规定用紫外检测器,那如果用PDA检测器代替紫外检测器,灵敏度能达到吗?以前看到有的帖子中说UV的信号的响应值是DAD的10倍,那是不是说做痕量的有机物只能用UV检测器?
去年做过16中多环芳烃,分离度也不错。今天调用之前的方法标准品(10ug/ml)出的十几个峰特别小,因为时间关系没来的及做高浓度的,标准品是二氯甲烷中的多环芳烃,我拿已睛配置的浓度点,想知道这样有没有影响?剃度是甲醇水,紫外检测器。有做过多环芳烃的大侠可以指点一下吗?万分感激!!!
最近在做高效液相测多环芳烃的标曲,我用的是紫外检测器,C18柱子。但是方法上测水质,土壤,和空气的多环芳烃的洗脱梯度不同,诸位帮帮忙有没有优化的洗脱梯度方案提供一下
近期,德国在对消费品安全要求进行审查后,建议在GS(安全性认证(安全测试))控制列表中增加两种多环芳烃(PAH)致癌物。这将使GS 标志列表管控的多环芳烃总数达到18个。自愿性的德国GS标志认证基于美国环境保护署提出的技术指标列表对适用产品中的多环芳烃加以管控。目前,这份列表包含的 16种多环芳烃被分类为致癌物质。不过,最近由欧洲食品安全局(EFSA)和德意志研究联合会(DFG)参议院委员会认定的两种剧毒多环芳烃却未被列入表内。这两种物质——苯并荧蒽,苯并苝,都被列为第二类致癌物质,并被列入REACH法规附录XVII(第50项)。因此,德国倡议进一步控制消费品中的多环芳烃。这两种物质的加入将确保欧盟列出的所有八个第二类高致癌多环芳烃可通过GS标志进行管控。德国技术设备及消费品委员会(AtAV委员会)建议,申请GS标志应基于以下更新物质列表。在测试范围更新之后,ZEK 01.2-08规定的分析过程将是应用于GS标志认证的测试方法。经验交流中心(ZEK)第67次会议在德国德国技术设备及消费品委员会(ZEK-04-11号文件)的建议下同意了此次列表的扩大。从现在起,经过六个月的过渡期后,新的物质列表将应用于GS标志认证。
我要测定石油中多环芳烃的含量,这个我用标准SN-T 1877.3-2007矿石油中多环芳香烃的测定可以吗?也没有找到任何关于石油中PAHs测定的资料,希望大家赐教
多环芳烃污染物近年来受到人们的高度重视。美国EPA(国家环保总署) 确定了16种多环芳烃为代表检测物,并且推荐了检测方法。中国国标也给出了水中6种多环芳烃的检测方法。分别用乙腈/水或者甲醇/水梯度洗脱,都是用普通ODS柱。市场上很多品牌都有PAH检测专用柱,普通ODS柱检测问题在哪里呢?PAH检测专用柱有何优势呢?PAH专用柱特别的原因为何(比如是否可能是ODS填料键合一些芳基,瞎猜啊)?看了一些谱图,发现自来水或者土壤的PAH检测基线干扰挺严重的。或许是因为含量太少,萃取浓缩的原因吧。似乎针对水质土壤监控,有效的前处理方法更有意义。
多环芳烃(PAHs)是一类在环境中广泛存在的污染物,美国环保署和欧盟都将其列为优先控制污染物,目前通过的多环芳烃检测方法有[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]法(EPA Method 550、8310)、[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法(EPA Method 8100)、[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]-质谱法(EPA Method 610、625、8270)等 [url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]-三重四级杆串联质谱是一种选择性和灵敏度的检测技术,这种方法在检测基质干扰严重的样品中的痕量污染物时表现非常出色。近几年来,这种方法不断被用于检测环境和生物样品中的多环芳烃,被证明是一种非常有效的技术手段。 检测方法所需仪器:[b][url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url][/b]-三重四级杆串联质谱;快速溶剂萃取装置,配备12位100mL萃取池。 采用[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]-三重四级杆串联质谱作为检测仪器,并采用[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]-质谱联用仪作为对照。色谱条件如下:色谱柱为30m×0.25mm×0.25μm,进样口温度280℃,载气为高纯氦气,流速1ml/min,不分流进样。进样体积1μL。升温程序:70℃保持2min;15℃/min升温到180℃,保持2min;5℃/min生物呢到260℃,保持2min;3℃/min升到300℃,保持6min。 质谱采用电子轰击离子源(EI),多反映检测(MRM)模式和选择离子扫描模式扫描,碰撞气为高纯氩气。
多环芳烃,有测过得朋友没,我测的
本人在尝试建立水样中多环芳烃的GC-MS测定方法,参考的方法是国标HJ 646-2013《环境空气和废气 气相和颗粒物中多环芳烃的测定 气相色谱-质谱法》,其中遇到两个问题不是很清楚,特向各位前辈求助:1. 方法中采用2-氟联苯和对三联苯-d14作为替代物,在样品前处理之前加入已知的量,再利用前处理后样品的测定值计算出提取回收率,从而可以评价前处理过程产生的损失。那么,多环芳烃的测定值是否也要用这个提取回收率反算出原有值?还是直接用测定值作为最终结果呢?2. 方法要求制作硅胶层析柱进行样品的净化,请问用二氯甲烷/正己烷洗脱后的柱子还能重复用于净化另一个样品吗?还是要除掉填料重做层析柱?如果可以重复用,是不是也要进行一定的处理?用二氯甲烷或正己烷冲洗可以吗?可能这些问题在各位看来比较初级,不过作为初次接触此行的小弟来说还是比较头疼的,烦请您指点一二!谢谢~
GS标志物质列表中将新增两种多环芳烃 来源:技术壁垒资源网 时间:2011-11-09近期,德国在对消费品安全要求进行审查后,建议在GS安全性认证(安全测试)控制列表中增加两种多环芳烃(PAHs)致癌物质。这将使 GS 标志列表管控的多环芳烃总数达到 18个。 自愿性的德国GS标志认证基于美国环境保护署提出的技术指标列表对适用产品中的多环芳烃加以管控。目前,这份列表包含的 16种多环芳烃被分类为致癌物质。不过,最近由欧洲食品安全局(EFSA)和德意志研究联合会(DFG)参议院委员会认定的两种剧毒多环芳烃却未被列入表内。这两种物质——苯并荧蒽,苯并苝,都被列为第二类致癌物质,并被列入REACH法规附录XVII(第50项)。因此,德国倡议进一步控制消费品中的多环芳烃。这两种物质的加入将确保欧盟列出的所有八个第二类高致癌多环芳烃可通过GS标志进行管控。 德国技术设备及消费品委员会(AtAV 委员会)建议,申请GS标志应基于以下更新物质列表。在测试范围更新之后,ZEK 01.2-08规定的分析过程将是应用于GS标志认证的测试方法。 经验交流中心(ZEK)第67次会议在德国德国技术设备及消费品委员会(ZEK-04-11 号文件)的建议下同意了此次列表的扩大。从现在起,经过六个月的过渡期后,新的物质列表将应用于 GS 标志认证。如有疑问,请致电PONY谱尼测试零七五五二六零五零九零九
我最近在做关于某种细菌对多环芳烃降解率的摇瓶实验,只用了菲、芴、芘、荧蒽四种多环芳烃,在测溶液中多环芳烃残留量的时候,还需要加替代和内标吗?加的种类和测16种多环芳烃时一样吗?我们课题组以前都是做土壤重金属的,师兄师姐也不知道,文献里也没有说明白,很迷茫测16种多环芳烃时我用的替代是2-氟联苯和对三联苯混合液,内标是苊、菲、屈、苝的氘代物
[B][size=4]前段时间我用[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]做塑料中的多环芳烃,用的柱子是hp-5ms,刚开始做的头几天峰形很好的,后来就逐渐开始拖尾,越来越拖得厉害,大约1000针样品后就彻底不行了, 但我再把它拿来做农残又仍然跟新柱子一样。衬管,柱子都是天天换割的。 只要再做多环芳烃就不行,不知道原因,修改的各种条件还是不行 后来我就买了个新ht-8的柱子,装上后做多环芳烃,立马就好了,但也是没过多久就两个月,就也拖尾得一塌糊涂。 再后来我又买了个hp-5msui的,现在正在用,也是有和上两个柱子一样的现象,才10天不到,现在已经开始拖尾了 不知道是否有人碰到和我一样的现象。可否有解决问题的方法?[/size][/B]
我们实验室要开展多环芳烃项目,想请教一下AfPS-GS-2014-01-PAK和zek01-08有什么不一样,做多环芳烃有哪些需要注意的地方,查了一些资料说多环芳烃不好做对色谱柱损害大,最好买一根专用色谱柱,有人知道这专用色谱柱的型号吗,十分感谢
有谁知道美国优先控制的16种多环芳烃(PAHs)在地表水中的环境标准吗,特别是这些物质在US EPA and EU directives规定的地表水的最高允许含量吗?最好是单个PAH在地表水中的含量限制?我现在非常想知道这些数据,我在网上找了好多天都没得到满意的答案,所以向各位求助了,希望大家能帮帮我,非常感谢各位的帮助,谢谢。
PAHs主要包括16种同类物质。 16种常见多环芳香烃: 1、Naphthalene 萘 2、Acenaphthylene 苊烯 3、Acenaphthene 苊 4、Fluorene 芴 5、Phenanthrene 菲 6、Anthracene 蒽 7、Fluoranthene 荧蒽 8、Pyrene 芘 9、Benzo(a)anthracene 苯并(a)蒽 10、Chrysene 屈 11、Benzo(b)fluoranthene 苯并(b)荧蒽 12、Benzo(k)fluoranthene 苯并 (k)荧蒽 13、Benzo(a)pyrene 苯并(a)芘 14、Indeno(1,2,3-cd)pyrene 茚苯(1,2,3-cd)芘 15、Dibenzo(a,h)anthracene 二苯并(a, n)蒽 16、Benzo(g,hi)perylene 苯并(ghi)北(二萘嵌苯) 日前,价值超过8000万美元的中国电动工具被德国海关扣押,这是因为被检测出PAHs(多环芳烃,一种致癌物质)值超标。English:Polycyclic Aromatic Hydrocarbons (PAHs)也称为:Polyaromates, PolyaromaticHydrocarbons 共有100多种化学结构式的总称。 德国政府最新规定:多环芳烃PAHs 是一种高致癌的物质.现在德国政府强制规定所以在德国政府出售的电动工具必须经过检验其中不含有过量的PAHs,要进入德国市场的电动工具必须通过专业的检验机构的检测! 来源:有机物的不完全燃烧,煤/油/气/烟草/烤肉,木炭,原油,木馏油,焦油,药物,染料,塑料,橡胶,农药,发动机,发电机产生PAHsPAHs 多环芳烃 通常存在于石化产品、橡胶、塑胶、润滑油、防锈油、不完全燃烧的有机化合物中等。除了电动工具外,很多电器产品中都存在PAHs物质。常见的是:塑料粒子在挤塑的时候,和模具之间存在黏着,此时要加入脱模剂,而脱模剂中可能含有PAHs。 多环芳香烃可能存在的材料: 木炭,原油,木馏油,焦油 (天然),药物,染料,塑料,橡胶,农药 (人为),润滑油,脱膜剂,电容电解液,矿物油,柏油 (人为),杀虫剂、杀菌剂、蚊香、吸烟、汽油阻凝剂 (人为)其它。多环芳香烃的危害: 强致癌物质, 损伤生殖系统, 易导致皮肤癌,肺癌,上消化道肿瘤,动脉硬化,不育症。 多环芳香烃(PAHs)的法规要求 : 欧盟国家 76/769/EEC / German: LMBG / 美国US EPA, 中国 GB, GB/T, GHZ。 可能含有多环芳香烃的材料: 塑料手柄 / 塑料包装箱 / 橡胶手柄 / 有异味塑料、橡胶产品。
如题,公司要扩一个多环芳烃的液相方法,专家让测一个多环芳烃的盲样,我这边只有标液,没有质控样,怎么做能知道自己测的准不准?
为了适用于ZEK 01.4-08文件,最新的德国多环芳烃(PAHs)标准应上海安谱科学仪器有限公司的要求,美国o2si公司新推出18种多环芳烃混标,货号: CDGG-110064-01-1ml,18种多环芳烃混标 标准品规格:1000ug/mL于二氯甲烷,1mL报价:1242RMB 与 16种多环芳烃比 增加了以下2种:benzopyrene 苯并芘 192-97-2 benzo(j)fluoranthene 苯并(j)荧蒽 205-82-318种多环芳烃标准品组分信息:Component CAS Number Concentration Units benzofluoranthene 苯并(k)荧蒽 207-08-9 1000 mg/L acenaphthene 苊 83-32-9 1000 mg/L acenaphthylene 苊烯 208-96-8 1000 mg/L anthracene 蒽 120-12-7 1000 mg/L fluorene 芴 86-73-7 1000 mg/L naphthalene 萘 91-20-3 1000 mg/L phenanthrene 菲 85-01-8 1000 mg/L benzoanthracene 1,2-苯并蒽 56-55-3 1000 mg/L benzopyrene 苯并芘 50-32-8 1000 mg/L chrysene 屈 218-01-9 1000 mg/L fluoranthene 荧蒽 206-44-0 1000 mg/L indenopyrene 茚并(1,2,3-cd)芘 193-39-5 1000 mg/L pyrene 芘 129-00-0 1000 mg/L benzofluoranthene 苯并(b)荧蒽 205-99-2 1000 mg/L benzoperylene 1,12-苯并芘 191-24-2 1000 mg/L dibenzanthracene 二苯蒽 53-70-3 1000 mg/L benzopyrene 苯并芘 192-97-2 1000 +/- 50 mg/Lbenzo(j)fluoranthene 苯并(j)荧蒽 205-82-3 1000 +/- 50 mg/L
我打算制备多环芳烃污染土壤(代替污染场地土壤)老化多长时间比较合适呢?我认为,短了不合适,太长又耽误实验。所以请教大家。
多环芳烃用荧光检测器检测不到十氟联苯
我在检测多环芳烃的时候遇到两个问题,请教各位老师:1、我用DB-5MS的柱子,样品和标准溶液的溶剂都是二氯甲烷,有人说二氯甲烷会伤害柱子?是这样吗?是什么原理呢?2、我购买的多环芳烃的标准溶液都是二氯甲烷,工程师建议用正己烷做溶剂,可是如何用正己烷稀释呢?正己烷和二氯甲烷好像不互溶?
我想测定石油组分中多环芳烃的含量。一般是经过正庚烷展开、烘干;再用甲苯展开、烘干;这样就有饱和份、芳香份、胶质和沥青质三个族组成。如果将多环芳烃和单环芳烃分离的话,是不是经过正庚烷、甲苯的展开,再用二甲基亚砜展开?关于用极性不同的溶剂展开,这句话在这个分析中是否这样理解?
SH/T 0806-2008测柴油中的多环芳烃,请问怎么计算结果呀,看不太懂标准
求一个岛津LC-20A的多环芳烃方法,我根据478的方法做出来以后峰区分不出来。