甲醇钠溶解在甲醇溶液中我们知道能发生甲酯化反应。氢氧化钾的甲醇溶液也能发生甲酯化反应,但是氢氧化钠的甲醇溶液会生成部分水,或者说如果氢氧化钾的甲醇溶液中有水的话,那还是单纯的甲酯化反应吗,会不会有水参与的水解反应?还有我看有的标准甲醇钠是用去离子水配置的,这里面和单纯的用甲醇溶解是不是会多一个H2O的水解反应?
如题有人知道酯化反应条件么?如果强酸例如浓硫酸能直接和醇类反应么?
马兜铃酸和甲醇理论上会发生酯化反应,但是加过浓硫酸,加热至70℃左右和除水剂等都不发生反应,该怎么办

上篇简单讨论1 缩醛反应,本篇简单介绍酸和醇的酯化反应。(附上次的目录:香精是由多种香原料成分组成的复杂混合物,可能包含溶剂。既然是多种化合物在一起,在存放老化过程,不可避免的会产生某些反应,生产新的物质。这些新物质和原来香精的成分是有关联的,对这些新物质的测定,利用这些信息,就能对原香精的组分更好的还原,使香精剖析更全面准确。下面对一些常见反应做简单介绍。(注:前面GCMS线下活动和后来的帖子或短信中,有网友问我这个问题并希望有讲座或文章介绍,一直没时间做。)先粗略的介绍一下,给一个思考方向。香精一般有下列几种反应:1 缩醛反应2 缩酮反应3 酸和醇的酯化反应4 醛的氧化反应5 氧化反应6 酯交换反应7 皂化酯化反应8 聚合反应9 分解反应10 希夫(Schiff)反应)本篇内容:3 酸和醇的酯化反应酸和醇的酯化反应是香精在存放过程(陈化老熟)中最常见的化学反应之一,也是最简单、最容易理解的反应。只要有酸和醇同时存在,就有可能会发生酯化反应。不过有时候可能没留意到罢了或仔细考虑。3.1 丙二醇和酸的酯化反应丙二醇是食品香精里面最常用,也是用量最大的溶剂,日化香精也用到。如果香精里面加入各种酸的话,很容易生产丙二醇的酯。例如,丙二醇和乙酸生产乙酸的单丙二醇酯(两个异构体),双乙酸的丙二醇酯:CH3COOH + CH3-CH(OH)-CH2(OH) ----à CH3-CH2(OH)-CH2OOCCH3 + H2O或CH3COOH + CH3-CH(OH)-CH2(OH) ----à CH3-CH(OOCCH3)-CH2(OH)+ H2O或CH3COOH + CH3-CH(OH)-CH2(OH) ----à CH3-CH(OOCCH3)-CH2OOCCH3 + H2O丁酸和丙二醇的反应:http://ng1.17img.cn/bbsfiles/images/2012/12/201212301545_417345_1615838_3.jpg一般情况下都会有两个酸的丙二醇酯的异构体。注意有时候一个丙二醇可能和两个不同的酸同时反应生成不对称酯。丙二醇本身产生的聚丙二醇也可能与酸反应生产一些酯。下面是乙酸,双乙酸丙二醇酯,甲酸,单甲酸丙二醇1,单乙酯酸丙二醇酯1,丙二醇(PG),单乙酯酸丙二醇酯2,单甲酸丙二醇2在极性柱子上的TIC图:http://ng1.17img.cn/bbsfiles/images/2012/12/201212301557_417348_1615838_3.jpg图C2下面是异丁酸,单乙酸丙二醇酯1,丙二醇(PG),丁酸,单异丁酸丙二醇酯1,单异丁酸丙二醇
做的是环糊精与琥珀酸酯化反应,红外2330左右是什么峰?是不是CO2吸收峰?
细胞膜脂肪酸甲酯化要用什么反应容器?反应液大概有1.5ml,有文献说用反应样品瓶,具体是指什么容器?[img]https://ng1.17img.cn/bbsfiles/images/2019/03/201903291023427595_5464_3499435_3.png[/img]
反应原料是57%的混合物,反应是酯化反应,产物中可能混合有其他合成产物,但我只想要四种目标产物,如何进行分离纯化?求各位有机合成大佬指点!!!!
BF3作为催化剂催化酯化反应机理是什么?正丁醇和2,4-D的反应ROH+ R'COOH
关于游离脂肪酸检测,我将游离脂肪酸丁酯化处理,使用硫酸/正丁醇然后发现检测结果丁酸丁酯含量很高,我做了空白以及拿没有丁酸的标品做丁酯化都发现有丁酸丁酯,这丁酸丁酯是怎样产生的啊?有什么方法避免这种情况发生?丁酸是我很重要的目标分析物这样就很难对其定量。(我完成了丁酯化的[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GC-MS[/color][/url]方法开发换方法不可能了)急需大神解答。
各位大侠好:本人实验的内容是乳酸与乙醇酯化合成乳酸乙酯,所以反应后的体系为乳酸/乙醇/乳酸乙酯/水四元体系,比较好的分析方法应该是应用GC吧,想问问分析时应用什么样的柱子较好,应该注意一些什么问题?还望做过相同体系分析或知道的大侠给与指点~~
[color=#444444]高效液相色谱计算酯化率的问题[/color][color=#444444]现在在测试一种催化剂对酯化反应的效果,用HPLC测试,采用内标法计算产率,但是看到文献上是计算的酯化率,那么问题来了[/color][color=#444444]之前查到酯化率的计算是通过酸值,而酸值是通过酸碱滴定的方法,利用HPLC如何计算的酯化率呢[/color]
请教植物油甲酯化的方法(试剂以及反应条件,反应时间)
各位朋友,有人知道油酸甲酯化怎么做吗,想用比较常见的试剂做反应。谢谢大家了!!!
甲醇钠溶解在甲醇溶液中我们知道能发生甲酯化反应。氢氧化钾的甲醇溶液也能发生甲酯化反应,但是氢氧化钠的甲醇溶液会生成部分水,或者说如果氢氧化钾的甲醇溶液中有水的话,那还是单纯的甲酯化反应吗,会不会有水参与的水解反应?还有我看有的标准甲醇钠是用去离子水配置的,这里面和单纯的用甲醇溶解是不是会多一个H2O的水解反应?因为我做的甘油三酯分子量较大,要把分子量“拆碎”,所以甲酯化一下。过程中遇到一些疑问,问问各位老师。
用对甲苯磺酸做催化剂进行有机酸甲酯化,计算酯化率,添加丙酸苯乙酯(IS)做内标,GC-MS检测后发现酯化后检测不到IS,为什么?难道是发生反应了?如果不能用丙酸苯乙酯做IS,改用什么酯做内标呢?
小弟打算蛋中的脂肪酸及游离脂肪酸,需要先甲酯化在用GC检测。可是发现脂肪酸和游离脂肪酸测得的峰数基本相同,想请教一下大侠们这是什么原因呢,脂肪酸和游离脂肪酸是一回事么?还有想请教一下用三氟化硼-甲醇甲酯化时候需要加热么还是在常温下反应就行呀。看国标中测定肉里面的脂肪酸时先皂化以后才甲酯化,这里皂化是起什么作用呢?
[color=#444444]利用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]定量检测甲酸,溶剂为异丙醇、水、THF约5ml,甲酸有几十mg,甲酯化反应后进色谱检测,请教各位大虾该甲酯化反应的具体操作,最好能详细点。以及甲酸甲酯用何内标定量较好?[/color]
1。我想用酸化甲酯化的方法提取脂肪酸,用甲醇-HCL反应物,请问是直接将这两样东西配成体系么?有什么要求么?(不好意思,我是新手,看了很多资料,还是不太明白先后顺利)。请问加入正乙烷、正庚烷的原理是什么?[color=#00008B]谢谢水中月的帮忙,这个我已经弄明白了。[/color]2。有没有人用过微波消解的方法,就是将溶液、原料、内参都配好后,用微波加热,请问一定需要这个步骤么?我看到有人说微波有助于缩短反应时间,那我只要将体系作用的时间延长不就可以了么?[color=#00008B]谢谢sartre的帮忙,这个我也明白了[/color][B]谢谢 水中月 的 帮忙,我吧你的资料仔仔细细的看了一遍,对于我这个菜鸟是很大的帮助啊,真是太感谢了。[/B]Question:1.我用甲醇-盐酸的原因是我看到一篇文章,《脂肪和脂肪酸甲酯化方法的研究》说到:%硫酸一甲醇酯化的主要优点是适用面广,既适于游离脂肪酸,又适合于结合态脂肪酸(脂肪)。碱法甲酯化只适合于脂肪,但其反应时间短,水解、甲酯化一步完成,是一种快捷、简便的分析方法。而我测的是游离脂肪酸,所以我才选择甲醇-盐酸的方法。不知这样选择酸催化或者碱催化甲酯化的方法是否正确?2.请问过程中用到正己烷,有的资料上提到正庚烷,这两个有什么差别么?是一回事么?3.还有,氮气除了做[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]时用到,还有什么地方需要用到吗?请知道的帮帮忙,谢谢!我会继续督促自己好好跟上的,谢谢!
GC法分析脂肪酸时常需要进行甲酯化反应,常见的方法是用硫酸催化与甲醇反应,或者用NaOH与三氟化硼催化,哪位高手知道是否还有其他更好的方法?
有奖问答’对错题:纤维素纤维的酯化反应:纤维素硝酸酯、纤维素醋酸酯; 纤维素纤维的醚化:纤维素乙基醚、纤维素羧甲基醚。( )
脂肪酸甲酯化酸法优于碱法,不知道做过的人是否跟我一样的结论,油酸甲酯化后居然有4个以上较大成分峰,不知道是油酸不纯(化学纯)还是有其它的原因?
请问各位大佬,有机酸标准样品一开始用什么溶解,是用水还是甲醇呀?我做了好几次实验,实验步骤如下:称取有机酸标准样品,用甲醇溶解稀释,加入酯化剂(百分之14的BF3甲醇),放入烘箱100度1小时,等待冷却后,用1:1的正己烷:二氯甲烷萃取换相,去上层液用[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]测定。这个实验步骤每次做下来,[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]只出溶剂峰,其他什么都测不出来。有没有大佬看看我这个实验过程出了啥问题,求求了
各位大侠,请帮帮我吧。在此万分感谢啊!本人是大四本科生,正在做毕业设计,题目是油脂食品中反式脂肪酸的含量测定,选用的样品是奶油。在计算确切含量时要用到酯化率,请教各位下,酯化率怎么算啊?实验过程中如何操作啊?好像是要用到甘油三酯标样吧还有我选用的是三氟化硼甲醇酯化的方法,指导我的那位研究生说这种方法只适用于一定酸价的脂肪酸,不是普适的,应该先测一下奶油脂肪酸的酸价,怎么测酸价啊?酸价是PH值吗
细胞膜脂肪酸甲酯化要用什么作反应容器?反应液大概1.5ml,看了文献说用反应样品瓶,具体是什么容器?[img]https://ng1.17img.cn/bbsfiles/images/2019/03/201903282206509758_5524_3499435_3.png[/img]
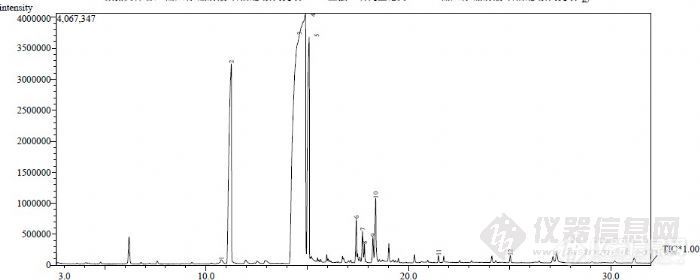
本人最近研究甜瓜籽油中脂肪酸成分时,采用氢氧化钠-甲醇发对所得油脂进行甲酯化,将甲酯化后的样品打进GC/MS后,发现所得的总离子流图中油酸与亚油酸的峰没有分开,且有些酸未能完全被甲酯化。请问各位大侠,有没有甲酯化效率高的方法,我应当如何改进我的实验?请不吝赐教。现将总离子流图附于下方,3号,4号峰位油酸和亚油酸的位置[img]http://ng1.17img.cn/bbsfiles/images/2010/07/201007092141_229734_1919819_3.jpg[/img]
每次用BF3-甲醇甲酯化试剂反应完以后烧瓶上都有很多白色的印子,怎么样可以洗去呢?
用[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用仪[/color][/url]测红细胞膜脂肪酸,参考文献里有20种脂肪酸,我只测出了7种脂肪酸,是不是甲酯化方法不好?我用的甲酯化方法是:取分离好的红细胞样本各50μL,依次加入已用BHT乙醇溶液抗氧化处理过的具塞玻璃试管中;在具塞玻璃试管中加入400μL3N盐酸-甲醇溶液,充分混匀3分钟,然后放置于90℃烘箱中避光反应3小时,反应完毕后取出冷却至室温;加入正己烷800μL到具塞玻璃试管中,充分混匀5分钟,4000rpm/min,2-8℃离心5min;将离心后的上层正己烷溶液尽量完全转移至另一个1.5ml离心管中,室温环境下,用氮气吹干仪吹干;在氮气吹干后的离心管中加入正己烷400μL溶解脂肪酸甲酯产物,充分混匀3分钟,然后转移100μL至样品瓶中,待测。
请问各位脂肪酸甲酯化大概有多少会被甲酯化啊??色谱柱上样不能有酸和水?那怎么判断酸和水的残留呢
有人问到 NHS化的染料蛋白标记我有跟帖简单回答 为了更清楚说明 并让更多人了解 NHS活化的荧光探针标记反应鉴于 荧光分析于毛细管电泳联用的广阔 前景单独发个主题帖 这大都是我的经验和理解 本人不是有机专业 有关合成方面 说错的地方还请拍砖 NHS化的荧光染料 是指 N-羟基琥珀酰亚胺 酯化的荧光染料标记 即N上的羟基与荧光探针上的羧基酯化反应[IMG]http://www.sigmaaldrich.com/structureimages/16/mfcd00005516.gif[/IMG]这些荧光探针与蛋白或者小分子胺偶联的原理很简单 都是 羧基与胺基反应生成酰胺键但是 一般的羧酸更倾向于 与胺基形成 铵盐因此引入个较好的离去基团就可以使羧基活化 促进羧基与胺基的共价键形成那么琥珀酰就是个很好的离去基团将荧光探针 用NHS进行酯化后 既可以相对稳定的保存,也可以直接用于与胺基分子的偶联,降低反应动力学壁垒与蛋白分子 或是 小分子胺 的偶联,原理相同 都是最终NHS基团离去,剩下的活化羧基与蛋白的胺基反应。在了解了原理的基础上,在进行NHS酯化的荧光探针标记策略上,应当着重注意以下几点:不用过多考虑蛋白的等电点,但需记住 胺基作为亲核基团的这个反应一般在 弱碱条件(pH=8~9)下进行 [B]![/B]考虑到蛋白的特殊性 配制缓冲液注意需要避免 1)极端pH (2)重金属污染 和(3)过大的离子强度 导致的蛋白变性 [B] ![/B]考虑到NHS酯化物的活泼程度,NHS化的荧光染料需要现配现加,不宜配制后静置过久。 [B] ![/B]考虑到 反应原理 ,选择缓冲液和反应容器 需要严格避免胺基或者氨基污染,避免与蛋白分子竞争反应掉荧光染料。 e.g. 常用缓冲液 有 borate buffer,NaHCO3,磷酸盐等等此外,还需注意: A.一般 的protocol都是针对 抗体的,抗体是比较 坚强的蛋白 B.虽说暴露在蛋白表面所有的侧链胺基都有可能跟羧基反应 但是 反应动力学最大的还是 Lys的那个长侧链上的e-伯胺基,因此富含lys的蛋白偶联有福啦。 C.一般来说,反应活性 伯胺>仲胺 D.别忘了 缓冲液选择也要考虑荧光探针自身特性,如果荧光探针自己带一个 很兴奋的胺基,那么由于自体的二聚反应,这个探针用于标记可能会效率很低当然NHS酯化的商品荧光探针有限,也可以用直接用 带油羧基的荧光探针偶联 蛋白,这时一般考虑使用 NHS EDC活化体系其原理就是 EDC先与 羧基形成个 不稳定的活化中间体然后 NHS接力 替代EDC形成 较稳定的 羧基活化体接下来的 就和上述原理一样了至于 标记上的蛋白 和未标记探针的蛋白 相互分离 每家公司各有法宝 我用过 BD公司的葡聚糖柱洗脱回收 也用CZE分离过小分子胺的标记产物其他更先进的方法就要看 论坛各位大神们的功夫啦附件上传的是 Pierce的NHS化荧光素的protocol 以及 Dynal beads羧基化表面偶联抗体的protocol 本文的 参考资料 有:http://en.wikipedia.org/wiki/N-hydroxysuccinimide[~185396~][~185397~]
做[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]乙酯化的时候安瓿瓶封口后静置6小时后,还要水浴一分钟的目的是啥,反应条件吗?为什么不直接水浴而是静置6h后呢?