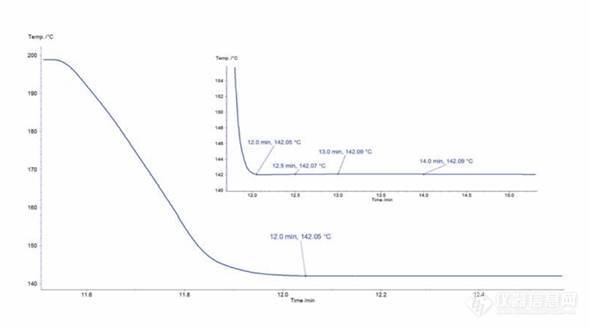
在聚合物行业中,注射模塑法是生产特定形状零件的主要方法。其过程为将熔融的高分子注入到一个相对较冷的模具中,冷却后即可得产品,此时模具的温度会直接影响最终产品的性能。等温结晶实验可以模拟模具中聚合物的行为,DSC等温结晶测试可以真正帮助注塑工艺的研究和优化。对于等温结晶测试,DSC实验必须满足两个要求。首先,样品必须快速冷却到指定的结晶温度,避免样品在冷却过程中结晶;其次,在指定的结晶温度下,温度控制必须稳定,不能波动。温度未到达目标温度会使结晶提早发生,有些高聚物(如聚烯烃)结晶很快,温度略低于目标温度几秒钟就会开始结晶。在DSC214出现之前,只有使用功率补偿型DSC才能够实现等温结晶测试所需的高冷却速率,这是因为功率补偿型DSC的炉体很小。耐驰DSC214 Polyma是第一个实现快速升降温的热流型DSC仪器,同时该仪器在恒温段具有极好的温控能力,这得益于它使用的具有低热质量的Arena炉体。[u][color=#00807a]案例分析:聚丙烯的等温结晶[/color][/u]在这个例子中,等温结晶实验使用耐驰DSC 214 Polyma对聚丙烯样品进行测试。进行适当的参数调节以优化快速冷却段到恒温段的过渡。将6.75mg样品以20K/min的速率加热到熔融温度,3分钟的恒温过程后,样品以程控速率200K/min冷却到142°C、140°C和138°C,整个实验过程在氮气气氛下进行。从冷却到142°C的温度曲线(图1)上可以看出,在达到目标结晶温度后,恒温段具有极好的温度稳定性,控温误差 0.1K。[img=,590,329]http://ng1.17img.cn/bbsfiles/images/2018/06/201806131429478899_7890_163_3.jpg!w590x329.jpg[/img][color=#000000] 图[/color][color=#000000] 1[/color][color=#000000]:冷却到[/color][color=#000000]142[/color][color=#000000]℃的温度曲线[/color][color=#000000]138°C、140°C和142°C恒温段下获得的DSC曲线如下图所示。[/color][color=#000000][img=,643,359]http://ng1.17img.cn/bbsfiles/images/2018/06/201806131430525844_7797_163_3.jpg!w643x359.jpg[/img][/color][color=#000000][color=#000000] 图 2:氮气气氛下使用DSC 214 Polyma测得的3个不同温度的聚丙烯的等温结晶曲线[/color][/color][color=#000000][color=#000000][/color][/color]由于DSC214在指定的温度下可以快速稳定,所以从冷却段到恒温段过渡造成的DSC曲线上的失稳效应足够短,这就可以观察到真正的结晶峰并测量结晶热焓。图2中获得的放热峰是由于聚丙烯的结晶造成的。正如预期,结晶热焓(峰面积)随着结晶温度的降低而增加,这表明最终产品具有更高的结晶度。同时,峰的斜率随着恒温温度的降低而变大,达到峰值更快,这表明结晶过程更快。耐驰DSC 214 Polyma可以对聚丙烯(一种以其快速结晶而闻名的聚烯烃)进行等温结晶测试。它可以用来帮助确定合适的工艺条件,例如模具温度和冷却时间,以便零件具有适当的性能。
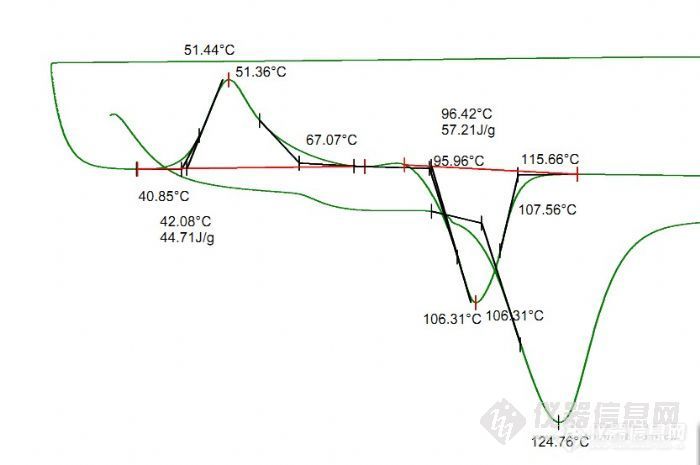
http://ng1.17img.cn/bbsfiles/images/2011/11/201111102221_329691_2325093_3.jpgDSC在测量过程中,第一次升温时没有结晶峰,有出现熔点,在第一次降温时也没有结晶峰,但是第二次升温时出现结晶峰 这是什么原因啊?
[font='Times New Roman'][font=宋体]结晶是指溶质自动从过饱和溶液中析出形成新相的过程,这一过程不仅包括溶质分子凝聚成固体,也包括这些分子有规律的排列在一定的晶格中。药物晶型的设计影响到药物的稳定性、纯度、溶出速率、流动性、压缩堆密度以及生物利用度,因此通过结晶控制实现对药物晶型形态的控制显得尤为重要。将近红外检测技术应用于药物结晶过程,可以实现在线结晶度的检测,确定多晶型,提供有关晶体结构的信息。[/font][/font]
想将手动调控的工业结晶过程改为自动控制,请DX们支招!
在做非等温结晶过程中发现某一组分共混物(尼龙共混物),在较快的降温速率时,降温过程中无结晶峰,然而在紧接着的升温过程中,却先出现放热峰,然后再出现熔点,请大家帮忙解释,谢谢了[em09505]
【网络讲座】:在线颗粒分析技术在结晶工艺优化方面的应用【讲座时间】:2016年04月19日 14:00【主讲人】:何禄,毕业于天津大学、大连理工大学,毕业后从事工艺研发工作多年,现任梅特勒-托利多自动化化学仪器部资深技术应用顾问,负责在线颗粒分析技术的应用支持。【会议简介】在线颗粒分析技术是一种在当前工艺条件下监测药物结晶的杰出方法,探头式测量技术能追踪整个结晶过程,无论是针对实验室小反应釜还是工业生产的大釜。实时在线测量工艺过程中晶体的粒径、数量和形状;利用在线颗粒分析技术实时原位进行药物结晶工艺的开发能帮助实现以下多方面的优化和改进:实现产量最大化、提高生产能力、确保晶体的质量和纯度、设计稳定的操作条件、消除后处理工艺的瓶颈、持续满足最终晶体的粒度要求、确保实验室到工业生产稳定放大的要求。-------------------------------------------------------------------------------1、报名条件:只要您是仪器网注册用户均可报名,通过审核后即可参会。2、报名截止时间:2016年04月19日 13:303、报名参会:http://www.instrument.com.cn/webinar/meeting/meetingInsidePage/18934、报名及参会咨询:QQ群—171692483http://ng1.17img.cn/bbsfiles/images/2017/01/201701191700_667383_2507958_3.gif
我的意思是出来吸热结晶峰后,随后的升温过程中没有熔融峰,这样的情况会是什么原因?
我师弟最近作了一个药物的DSC测试,好像是-30℃升温到190℃,在150℃附近出现了熔点峰,但是从190℃降温一直降到零下也没有结晶峰,这是什么原因?关键是我买了同一种药物,在降温的时候,就能出现结晶峰。还有一个问题就是降温的峰是分叉的,而升温的峰确实尖锐的峰,求教!
各位大侠, 请帮我恶补下知识。我现在混淆了!理论知识是 PE的结晶度比PP的结晶度低,那两者的结晶速率谁快谁慢啊。 还有PE/PP的复合物中,在降温过程中,结晶温度低的是谁?
在用王水溶解金属样品后,冷却,一些样品中出现结晶,会对铅有损失么,该怎么处理??我们这里领导说就这么过滤就行了,
氮吹至干,然后加0.5ml正己烷复溶。氮吹时瓶壁上出现白色结晶物了。0.5ml正己烷也不够把这些冲洗下去。大家一般怎么处理呢?
重结晶方法是利用固体混合物中各组分在某种溶剂中的溶解度不同而使其相互分离。进行重结晶的简单程序是先将不纯固体物质溶解于适当的热的溶剂中制成接近饱和的溶液,趁热过滤除去不溶性杂质,冷却滤液,使晶体自过饱和溶液中析出,而易溶性杂质仍留于母液小,抽气过滤,将晶体从母液中分出,干燥后测定熔点,如纯度仍不符合要求,可再次进行重结晶,直至符合要求为止。关于溶剂的选择选择适当的溶剂对于重结晶操作的成功具有重大的意义,一个良好的溶剂必须符合下面儿个条件:1、不与被提纯物质起化学反应2、在较高温度时能溶解多量的被提纯物质而在室温或更低温度时只能溶解很少量;3.对杂质的溶解度非常大或非常小,前一种情况杂质留于母液内,后一种情况趁热过滤时杂质被滤除;4.溶剂的沸点不宜太低,也不宜过高。溶剂沸点过低时制成溶液和冷却结晶两步操作温差小,团体物溶解度改变不大,影响收率,而且低沸点溶剂操作也不方便。溶剂沸点过高,附着于晶体表面的溶剂不易除去。5.能给出较好的结晶。在几种溶剂都适用时,则应根据结晶的回收率、操作的难易、溶剂的毒性大小及是否易燃、价格高低等择优选用 关于晶体的析出过滤得到的滤液冷却后,晶体就会析出。用冷水或冰水迅速冷却并剧烈搅动溶液时,可得到颗粒很小的晶体,将热溶液在空温条件下静置使之缓缓冷却,则可得到均匀而较大的品体。如果溶液冷却后晶体仍不析出,可用玻璃抹摩控液面下的容器壁,也可加入品种,或进一步降低溶液温度(用冰水或其它冷冻溶液冷却)。如果溶液冷却后不析出品体而得到油状物时,可重新加热,至形成澄清的热溶液后,任其自行冷却,并不断用玻璃棒搅拌溶液,摩擦器壁或投人品种,以加速品体的析出。若仍有油状物开始忻出,应立即剧烈搅拌使油滴分散。 结晶过程的确是一门学问,国内在结晶方面专家首推天津大学化工学院的王静康院士。关于这方面的理论书籍不少,但是真正具体到每一类物质或每个物质,他们又不完全相同。共性的东西可能是理论上的,具体到每一类化合物的结晶过程的讨论可能对大家最有帮助。溶剂的选择(单一或复合)、结晶温度,搅拌速度,搅拌方式,过饱和度的选择,养晶的时间,溶媒滴加的方式和速率等等,另外,在溶解、析晶、养晶这些过程中,上述温度、搅拌速度、时间多少、加入方式和速度还不完全一样。所以诸多因素叠加在一起,更是觉得难度大。一般说来,先应该选择主要的条件,使结晶过程能够进行下去,得到晶体,然后再优化上述条件。条件成熟后,才能进行中试和生产。如果是进行理论研究可能着重点就不一样了。如果是搞应用研究,那么溶剂相对来说不难选择,关键点在于使用这种溶剂能否找到过饱和点,过饱和点区间是不是好控制。如果过饱和点不好选,或过饱和度不够,很难析晶,更别提养晶了。这时可能要考虑复合溶媒,调整过饱和区间。所以我认为结晶过程最主要的是析晶过程,这时候各个条件的控制最为重要。控制好析晶过程,结晶过程大概完成60%。养晶过程相对来说好控制一些,主要是按照优化参数,控制好条件,一般问题不大,放大过程中也基本不会出问题。如果搞基础研究,物性还不是很清楚,结晶过程的研究可能花费的时间,精力较大。但一旦把整个过程搞明白,还是很有价值的。
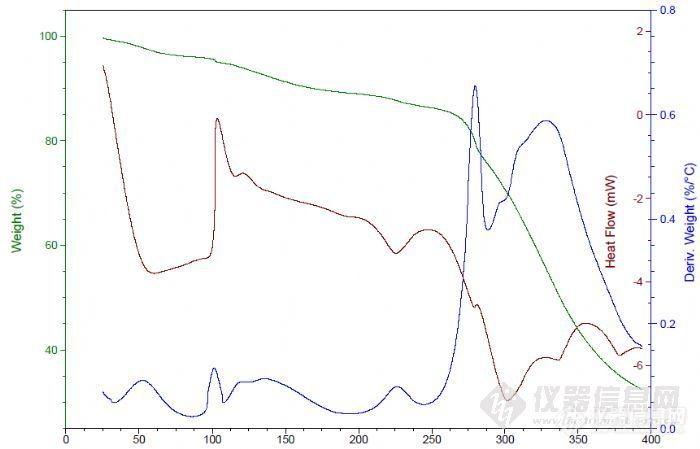
http://ng1.17img.cn/bbsfiles/images/2011/12/201112151443_338353_2415024_3.jpg如图,DSC曲线放热向上,请问是不是200-250度之间的失重为结晶水,200度以前的属于吸附水?
结晶和重结晶的操作步骤出自: http://emuch.net 结晶和重结晶的操作步骤结晶和重结晶包括以下几个主要操作步骤:1.将需要纯化的化学试剂溶解于沸腾或将进沸腾的适宜溶剂中;2.将热溶液趁热抽滤,以除去不溶的杂质;3.将滤液冷却,使结晶析出;4.滤出结晶,必要时用适宜的溶剂洗涤结晶。在实施结晶和重结晶的操作时要注意以下几个问题;1.在溶解预纯化的化学试剂时要严格遵守实验室安全操作规程,加热易燃、易爆溶剂时,应在没有明火的环境中操作,并应避免直接加热。因为在通常的情况下,溶解度曲线在接近溶剂沸点时陡峭地升高,故在结晶和重结晶时应将溶剂加热到沸点。为使结晶和重结晶地收率高,溶剂的量尽可能少,故在开始加入的溶剂量不足以将欲纯化的化学试剂全部溶解,在加热的过程中可以小心的补加溶剂,直到沸腾时固体物质全部溶解为止。补加溶剂时要注意,溶液如被冷却到其沸点以下,防爆沸石就不在有效,需要添加新的沸石。2.为了定量地评价结晶和重结晶地操作,以及为了便于重复,固体和溶剂都应予以称量和计量。3.在使用混合溶剂进行结晶和重结晶时,最好将欲纯化的化学试剂溶于少量溶解度较大的溶剂中,然后趁热慢慢地分小份加入溶解度较小的第二种溶剂,直到它触及溶液的部位有沉淀生成但旋即有溶解为止。如果溶液的总体积太小,则可多加一些溶解度大的溶剂,然后重复以上操作。有时也可用相反的程序,将欲纯化的化学试剂悬浮于溶解度小的溶剂中,慢慢加入溶解度大的溶剂,直至溶解,然后再滴入少许溶解度小的溶剂加以冷却。4.如有必要可在欲纯化的化学试剂溶解后加入活性炭进行脱色(用量约相当于欲纯化的物质重量的1/50~1/20),或加入滤纸浆、硅藻土等使溶液澄清。加入脱色剂之前要先将溶剂稍微冷却,因为加入的脱色剂可能会自动引发原先抑制的沸腾,从而发生激烈的、爆炸性的暴沸。活性碳内含有大量的空气,故能产生泡沫。加入活性碳后可煮沸5-10分钟,然后趁热抽滤去活性碳。在非极性溶剂,如苯、石油醚中活性碳脱色效果不好,可试用其他办法,如用氧化铝吸附脱色等。5.欲纯化的化学试剂为有机试剂时,形成过饱和溶液的倾向很大,要避免这种现象,可加入同种试剂或类质同晶物的晶种。用玻璃棒摩擦器壁也能形成晶核,此后晶体即沿此核心生长。6.结晶的速度有时很慢,冷溶液的结晶有时要数小时才能完全。在某些情况下数星期或数月后还会有晶体继续析出,所以不应过早将母液弃去。7.为了降低欲纯化试剂在溶液中的溶解度,以便析出更多的结晶,提高产率,往往对溶液采取冷冻的方法。可以放入冰箱中或用冰、混合制冷剂冷却。8.制备好的热溶液必须经过过滤,以除去不溶性的杂质,而且必须避免在抽滤的过程中在过滤器上结晶出来。若是一切操作正规,确实由于该试剂太易析出结晶而阻碍抽滤时,则可将溶液配制地稍微稀一些,或者采用保温或加热过滤装置(如保温漏斗)过滤。9.欲使析出地晶体于母液有效地分离,一般用布氏漏斗抽滤。为了更好地使晶体和母液分离,最好用清洁地玻璃塞将晶体在布氏漏斗上挤压,并随同抽气尽量地去除母液。晶体表面地母液,可用尽量少地溶剂来洗涤。这是应暂时停止抽气,用玻璃棒或不锈钢刀将已压紧地晶体挑松,加入少量地溶剂润湿,稍待片刻,使晶体能均匀地被浸透,然后再抽干,这样重复一、二次,使附于浸透表面地母液全部除去为止。10.晶体若遇热不分解时,可采用在烘箱中加热烘干的方法干燥。若晶体遇热易分解,则应注意烘箱的温度不能过高,或放在真空干燥器中在室温下干燥。若用沸点较高的溶剂重结晶时,应用沸点低的且对晶体溶解度很小的溶剂洗涤,以利于干燥。易潮解的晶体应将烘箱欲先加热到一定的温度,然后将晶体放入;但是极易潮解的晶体,往往不能用烘箱烘,必须迅速放入到真空干燥器中干燥。用易燃的有机溶剂重结晶的晶体在送入烘箱前,应预先在空气中干燥,否则可能引起溶剂的燃烧或爆炸。11.小量及微量的物质的重结晶:小量的物质的结晶或重结晶基本要求同前所述,但均采用与该物质的量相适应的小容器。微量物质的结晶和重结晶可在小的离心管中进行。热溶液制备后立即离心,使不容的杂质沉于管底,用吸管将上层清夜移至到另一个小的离心管中,令其结晶。结晶后,用离心的方法使晶体和母液分离。同时可在离心管中用小量的溶剂洗涤晶体,用离心的方法将溶剂与晶体分离.12.母液中常含有一定数量的所需要的物质,要注意回收。如将溶剂除去一部分后再让其冷却使结晶析出,通常其纯度不如第一次析出来的晶体。若经纯度检查不合要求,可用新鲜溶剂结晶,直至符合纯度要求为止。
在砖厂烟道采样过程中,发现厂家会添加氢氧化钠,与二氧化硫之后反映变成硫酸钠,硫酸钠会结晶到滤嘴滤膜上,这样在称重过程中会增加颗粒物含量,请问有什么办法能去掉结晶吗
化合物晶型的差异直接影响其稳定性/吸收的快慢/吸湿性/纯度等,不知大家这方面有什么心得?结晶溶剂选择的一般原则及判定结晶纯度的方法。结晶溶剂选择的一般原则:对欲分离的成分热时溶解度大,冷时溶解度小;对杂质冷热都不溶或冷热都易溶。沸点要适当,不宜过高或过低,如乙醚就不宜用。 或者利用物质与杂质在不同的溶剂中的溶解度差异选择溶剂判定结晶纯度的方法:理化性质均一;固体化合物熔距≤ 2℃;TLC或PC展开呈单一斑点;HPLC或GC分析呈单峰 现代结晶学主要包括以下几个分支:(1)晶体生成学(crystallogeny):研究天然及人工晶体的发生、成长和变化的过程与机理,以及控制和影响它们的因素。 (2)几何结晶学(gometrical crystallography):研究晶体外表几何多面体的形状及其间的规律性。 (3)晶体结构学(crystallology):研究晶体内部结构中质点排而的规律性,以及晶体结构的不完善性。 (4)晶体化学(crystallochemistry, 亦称结晶化学):研究晶体的化学组成与晶体结构以及晶体的物理、化学性质间关系的规律性。 (5)晶体物理学(crystallophysics):研究晶体的各项物理性质及其产生的机理。 溶剂方面:是制备结晶的关键所在。除yangdongyu提到的外,选择时可用少量各种不同溶剂试验其溶解度,包裹冷时和热时。一般首选乙醇。另外,尽可能选择单一溶剂,这样在大生产时也可较好的解决母液回收套用问题,降低成本。研究时,混合溶剂一般会有更好效果。还有安全,价廉也是考虑因素。结晶条件:主要指温度,压力,是否搅拌等。温度很重要,一般我们都是低温冷藏,其实有时还需要高温保温!这主要需摸清其溶解度的关系在确定结晶温度。搅拌也是一个影响因素,他对结晶的晶型,结晶的快慢都有影响。结晶纯度判定:都是一般的常规方法。不过都某些产品作的多了,可以凭经验的,如该样品经过多次重结晶后,看到应该出现的那种晶型,根据以往检测结果,其含量应该***不离十了,不信HPLC测去另外选择梯度降温的条件对晶型和收率影响也较大还有就是加晶种的时机:晶种加得过早,晶种溶解或产生的晶型一般较细;加的晚,则溶液里可能已经产生了晶核,造成结晶可能包裹杂质 重结晶方法是利用固体混合物中各组分在某种溶剂中的溶解度不同而使其相互分离。进行重结晶的简单程序是先将不纯固体物质溶解于适当的热的溶剂中制成接近饱和的溶液,趁热过滤除去不溶性杂质,冷却滤液,使晶体自过饱和溶液中析出,而易溶性杂质仍留于母液小,抽气过滤,将晶体从母液中分出,干燥后测定熔点,如纯度仍不符合要求,可再次进行重结晶,直至符合要求为止。关于溶剂的选择选择适当的溶剂对于重结晶操作的成功具有重大的意义,一个良好的溶剂必须符合下面儿个条件:1、不与被提纯物质起化学反应2、在较高温度时能溶解多量的被提纯物质而在室温或更低温度时只能溶解很少量;3.对杂质的溶解度非常大或非常小,前一种情况杂质留于母液内,后一种情况趁热过滤时杂质被滤除;4.溶剂的沸点不宜太低,也不宜过高。溶剂沸点过低时制成溶液和冷却结晶两步操作温差小,团体物溶解度改变不大,影响收率,而且低沸点溶剂操作也不方便。溶剂沸点过高,附着于晶体表面的溶剂不易除去。5.能给出较好的结晶。在几种溶剂都适用时,则应根据结晶的回收率、操作的难易、溶剂的毒性大小及是否易燃、价格高低等择优选用。关于晶体的析出过滤得到的滤液冷却后,晶体就会析出。用冷水或冰水迅速冷却并剧烈搅动溶液时,可得到颗粒很小的晶体,将热溶液在空温条件下静置使之缓缓冷却,则可得到均匀而较大的品体。如果溶液冷却后晶体仍不析出,可用玻璃抹摩控液面下的容器壁,也可加入品种,或进一步降低溶液温度(用冰水或其它冷冻溶液冷却)。如果溶液冷却后不析出品体而得到油状物时,可重新加热,至形成澄清的热溶液后,任其自行冷却,并不断用玻璃棒搅拌溶液,摩擦器壁或投人品种,以加速品体的析出。若仍有油状物开始忻出,应立即剧烈搅拌使油滴分散。 结晶过程的确是一门学问,国内在结晶方面专家首推天津大学化工学院的王静康院士。关于这方面的理论书籍不少,但是真正具体到每一类物质或每个物质,他们又不完全相同。共性的东西可能是理论上的,具体到每一类化合物的结晶过程的讨论可能对大家最有帮助。溶剂的选择(单一或复合)、结晶温度,搅拌速度,搅拌方式,过饱和度的选择,养晶的时间,溶媒滴加的方式和速率等等,另外,在溶解、析晶、养晶这些过程中,上述温度、搅拌速度、时间多少、加入方式和速度还不完全一样。所以疃嘁蛩氐釉谝黄穑蔷醯媚讯却蟆?br一般说来,先应该选择主要的条件,使结晶过程能够进行下去,得到晶体,然后再优化上述条件。条件成熟后,才能进行中试和生产。如果是进行理论研究可能着重点就不一样了。如果是搞应用研究,那么溶剂相对来说不难选择,关键点在于使用这种溶剂能否找到过饱和点,过饱和点区间是不是好控制。如果过饱和点不好选,或过饱和度不够,很难析晶,更别提养晶了。这时可能要考虑复合溶媒,调整过饱和区间。所以我认为结晶过程最主要的是析晶过程,这时候各个条件的控制最为重要。控制好析晶过程,结晶过程大概完成60%。养晶过程相对来说好控制一些,主要是按照优化参数,控制好条件,一般问题不大,放大过程中也基本不会出问题。如果搞基础研究,物性还不是很清楚,结晶过程的研究可能花费的时间,精力较大。但一旦把整个过程搞明白,还是很有价值的。
在连续动态再结晶过程中,位错胞薄壁平直化转变为亚晶,亚晶合并迁移,那么,位错胞是否也存在合并和扩展的过程呢?是否更大的位错胞更有利于演变为亚晶呢?
用的是空气回流装置。因为时间问题,回流两小时后,冷却了一会儿,打算将回流管里的水样倒到锥形瓶里,放在冷水中冷却。平常都是先从冷凝管端加些水进去,然后将冷凝管卸下,把水倒进锥形瓶里。今天因为拔不出冷凝管,就直接从冷凝管端倒出,却有白色结晶物出现。不知为何会出现这种现象?白色结晶物是什么呢?以及可以这样冷却吗?想请懂的人士,帮忙解答下O(∩_∩)O~
[em03] 我今天处理的米粉小料无论用干法灰化还是湿法消化都有结晶产生,怎么也溶不掉,怎么办/
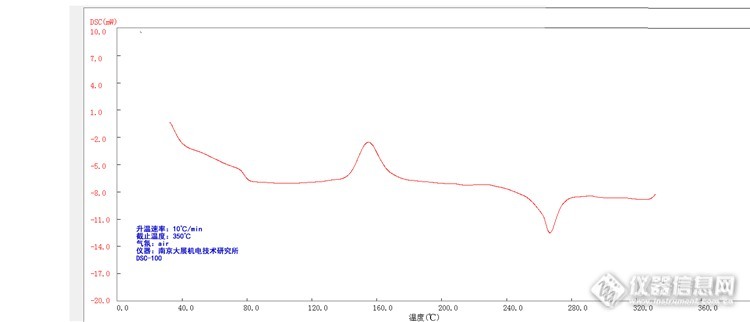
[color=#333333][img=第二个向上的峰,为冷结晶,690,296]http://ng1.17img.cn/bbsfiles/images/2017/06/201706161142_01_2781725_3.png[/img][/color][color=#333333]所有的晶体,结晶的过程方式是不一样的,熔融结晶是从熔融状态下开始结晶(起始设定温度高于熔点),而冷结晶是从玻璃态(相对熔融态而言是一种“冷”的状态)下开始结晶(起始设定温度低于玻璃化转变温度),可见这两者的区别在于起始的状态。由于起始状态决定成核的难易(聚合物结晶分成核和晶体生长两个阶段),一般而言,从玻璃态下成核较从熔融态下相对容易得多(低温成核容易,分子链不易扩散,晶体生长困难;高温成核困难,分子链易扩散,晶体生长容易),这就是为什么有的结晶慢的聚合物冷却过程中没有熔融结晶峰,而在升温过程中有冷结晶峰。[/color][color=#333333]一般而言,从玻璃态下成核较从熔融态下相对容易得多(低温成核容易,分子链不易扩散,晶体生长困难;高温成核困难,分子链易扩散,晶体生长容易),这就是为什么有的结晶慢的聚合物冷却过程中没有熔融结晶峰,而在升温过程中有冷结晶峰。[/color]
结晶溶剂选择的一般原则及判定结晶纯度的方法。 结晶溶剂选择的一般原则:对欲分离的成分热时溶解度大,冷时溶解度小;对杂质冷热都不溶或冷热都易溶。沸点要适当,不宜过高或过低,如乙醚就不宜用。 或者利用物质与杂质在不同的溶剂中的溶解度差异选择溶剂 判定结晶纯度的方法:理化性质均一;固体化合物熔距≤ 2℃;TLC或PC展开呈单一斑点;HPLC或GC分析呈单峰。 现代结晶学主要包括以下几个分支: (1)晶体生成学(crystallogeny):研究天然及人工晶体的发生、成长和变化的过程与机理,以及控制和影响它们的因素。 (2)几何结晶学(gometrical crystallography):研究晶体外表几何多面体的形状及其间的规律性。 (3)晶体结构学(crystallology):研究晶体内部结构中质点排而的规律性,以及晶体结构的不完善性。 (4)晶体化学(crystallochemistry, 亦称结晶化学):研究晶体的化学组成与晶体结构以及晶体的物理、化学性质间关系的规律性。 (5)晶体物理学(crystallophysics):研究晶体的各项物理性质及其产生的机理。 溶剂方面:是制备结晶的关键所在。除yangdongyu提到的外,选择时可用少量各种不同溶剂试验其溶解度,包裹冷时和热时。一般首选乙醇。另外,尽可能选择单一溶剂,这样在大生产时也可较好的解决母液回收套用问题,降低成本。研究时,混合溶剂一般会有更好效果。还有安全,价廉也是考虑因素。 结晶条件:主要指温度,压力,是否搅拌等。温度很重要,一般我们都是低温冷藏,其实有时还需要高温保温!这主要需摸清其溶解度的关系在确定结晶温度。搅拌也是一个影响因素,他对结晶的晶型,结晶的快慢都有影响。 结晶纯度判定:都是一般的常规方法。不过都某些产品作的多了,可以凭经验的,如该样品经过多次重结晶后,看到应该出现的那种晶型。 另外选择梯度降温的条件对晶型和收率影响也较大。 还有就是加晶种的时机:晶种加得过早,晶种溶解或产生的晶型一般较细;加的晚,则溶液里可能已经产生了晶核,造成结晶可能包裹杂质。 重结晶方法是利用固体混合物中各组分在某种溶剂中的溶解度不同而使其相互分离。 进行重结晶的简单程序是先将不纯固体物质溶解于适当的热的溶剂中制成接近饱和的溶液,趁热过滤除去不溶性杂质,冷却滤液,使晶体自过饱和溶液中析出,而易溶性杂质仍留于母液小,抽气过滤,将晶体从母液中分出,干燥后测定熔点,如纯度仍不符合要求,可再次进行重结晶,直至符合要求为止。 关于溶剂的选择 选择适当的溶剂对于重结晶操作的成功具有重大的意义,一个良好的溶剂必须符合下面儿个条件: 1、不与被提纯物质起化学反应 2、在较高温度时能溶解多量的被提纯物质而在室温或更低温度时只能溶解很少量; 3.对杂质的溶解度非常大或非常小,前一种情况杂质留于母液内,后一种情况趁热过滤时杂质被滤除; 4.溶剂的沸点不宜太低,也不宜过高。溶剂沸点过低时制成溶液和冷却结晶两步操作温差小,团体物溶解度改变不大,影响收率,而且低沸点溶剂操作也不方便。溶剂沸点过高,附着于晶体表面的溶剂不易除去。 5.能给出较好的结晶。 在几种溶剂都适用时,则应根据结晶的回收率、操作的难易、溶剂的毒性大小及是否易燃、价格高低等择优选用。 关于晶体的析出 过滤得到的滤液冷却后,晶体就会析出。用冷水或冰水迅速冷却并剧烈搅动溶液时,可得到颗粒很小的晶体,将热溶液在空温条件下静置使之缓缓冷却,则可得到均匀而较大的品体。 如果溶液冷却后晶体仍不析出,可用玻璃抹摩控液面下的容器壁,也可加入品种,或进一步降低溶液温度(用冰水或其它冷冻溶液冷却)。 如果溶液冷却后不析出品体而得到油状物时,可重新加热,至形成澄清的热溶液后,任其自行冷却,并不断用玻璃棒搅拌溶液,摩擦器壁或投人品种,以加速品体的析出。若仍有油状物开始忻出,应立即剧烈搅拌使油滴分散。 结晶过程的确是一门学问,国内在结晶方面专家首推天津大学化工学院的王静康院士。关于这方面的理论书籍不少,但是真正具体到每一类物质或每个物质,他们又不完全相同。共性的东西可能是理论上的,具体到每一类化合物的结晶过程的讨论可能对大家最有帮助。 溶剂的选择(单一或复合)、结晶温度,搅拌速度,搅拌方式,过饱和度的选择,养晶的时间,溶媒滴加的方式和速率等等,另外,在溶解、析晶、养晶这些过程中,上述温度、搅拌速度、时间多少、加入方式和速度还不完全一样。所以诸多因素叠加在一起,更是觉得难度大。 一般说来,先应该选择主要的条件,使结晶过程能够进行下去,得到晶体,然后再优化上述条件。条件成熟后,才能进行中试和生产。如果是进行理论研究可能着重点就不一样了。 如果是搞应用研究,那么溶剂相对来说不难选择,关键点在于使用这种溶剂能否找到过饱和点,过饱和点区间是不是好控制。如果过饱和点不好选,或过饱和度不够,很难析晶,更别提养晶了。这时可能要考虑复合溶媒,调整过饱和区间。所以我认为结晶过程最主要的是析晶过程,这时候各个条件的控制最为重要。控制好析晶过程,结晶过程大概完成60%。 养晶过程相对来说好控制一些,主要是按照优化参数,控制好条件,一般问题不大,放大过程中也基本不会出问题。 如果搞基础研究,物性还不是很清楚,结晶过程的研究可能花费的时间,精力较大。但一旦把整个过程搞明白,还是很有价值的。
我在用石油醚硅胶柱梯度洗脱过程中,发现一白色晶体,不过不纯。这个混合物在薄层板上有点拖尾,感觉难纯化,有没有高手指点一下用重结晶方法合适不,用什么溶剂,谢谢!
我是研究冷却过程中的活化能,但是我得到的活化能为负值,我想问下大家,活化能为负值表示什么意思,既然结晶活化能表示析出晶体需要克服的能量,但是它为什么为负值呢?还有就是用结晶活化能判断一种物质是否容易析晶时,是用它的负值大小去判断呢还是用它的绝对值去判断?谢谢大家了
实验室获得的固体有机物,经常含有少量杂质,除去这些杂质最常用的方法就是选择适当的溶剂进行重结晶。 重结晶方法的原理就是利用被提纯化合物和杂质在热和冷的溶剂中溶解度的不同,把杂质分离或留在溶液中,以达到分离提纯的目的。 重结晶操作的一般过程为:(1)选择合适的溶剂。(2)将待纯化的固体溶解在热溶剂中制成饱和溶液。若含有有色杂质时,应加适量活性炭脱色。(3)趁热过滤除去不溶性杂质。(4)冷却滤液使结晶析出。(5)减压过滤分出结晶并洗涤,以除去吸附的母液。(6)干燥结晶。1.溶剂的选择 选择合适的溶剂是重结晶时的首要问题。理想的溶剂应符合下列条件:(1)与被提纯化合物不起化学反应;(2)被提纯化合物在冷与热的溶剂中的溶解度应有显著的差别,一般高温时溶解度好而低温时溶解度差;(3)杂质的溶解度非常大或非常小;(4)溶剂的沸点不宜太高,以便容易从结晶中除去;(5)待提纯物在溶剂中能形成较好的结晶。此外,还要考虑溶剂的价格、易燃程度、毒性大小、操作与回收的难易等。 具体选择溶剂时,已知物的精制可查阅手册或参考类似化合物重结晶的条件。若是未知物,主要是通过实验进行选择,选择时应利用“相似相溶”的经验规律,并根据选择溶剂的条件要求,用少量样品反复试验来选择和决定合适的溶剂,即把少量(约0.1g)被提纯的样品研细放入试管中,用滴管慢慢滴入溶剂并不断振摇,待加入溶剂量约1 mL时,在水浴上加热至沸,观察加热和冷却时样品溶解的情况:(1)如样品在1 mL冷或热的溶剂中都溶解,表明溶解度太大。(2)如样品不溶于l mL沸腾的溶剂中,则要继续加热,慢慢再滴入溶剂,每次滴加 0.1 mL,并加热至沸。要是加入溶剂已达4 mL仍不能溶解,说明溶解度太小,该溶剂也不适用。(3)如化合物能溶于 1~4 mL沸腾的溶剂中,此时应将试管冷却,或在室温下静置。能自行析出结晶时,则可选择该溶剂为重结晶溶剂;如结晶不能析出,可让溶剂挥发,也可用玻棒摩擦试管壁或用冰水浴冷却,以促使结晶析出,如结晶仍不能析出,则该溶剂不能选用,此时应改用其它溶剂或选用混合溶剂。常用的重结晶溶剂有水、甲醇、95%乙醇、冰乙酸、丙酮、乙醚、石油醚、乙酸乙酯、苯、氯仿、四氯化碳等。 当一种物质在一些溶剂中的溶解度太大,而在另一些溶剂中的溶解度又太小,不能选择到一种合适的溶剂时,常可使用混合溶剂而得到满意的结果。所谓混合溶剂,就是把对此物质溶解度很大和溶解度很小的两种溶剂(能互溶,如水和乙醇)混合起来,这样可获得新的良好的溶解性能。用混合溶剂重结晶时,可先将待纯化物质在接近溶剂的沸点时溶于溶解度大的溶剂中。若有不溶物,趁热过滤除去;若有色,则用适量(大约l%~5%)活性炭煮沸脱色后趁热过滤。在热溶液中小心地加入溶解度小的溶剂,维持此温度,直至所出现的浑浊不再消失为止,再加入少量溶解度大的溶剂或稍加热使其恰好完全溶解。然后将混合物冷却,若得到的是油状物,则需重新调整比例进行试验。有时也可将两种溶剂按一定比例先行混合进行重结晶,其操作和用单一溶剂时相同。常用的混合溶剂有:乙醇—水,乙酸—水、丙酮—水、甲醇—乙醚、丙酮—乙醚、乙酸—石油醚、苯—石油醚等。
最近经常有人问到如何计算结晶度。1 利用JADE的峰强比计算结晶度是一种不怎么准确的方法。2 利用JADE的峰强比计算结晶度需要有一个明显的非晶峰和晶相峰。象分子筛结晶度计算就不能用这种方法。3 附件是一个结晶度计算的实例,包括例子文件和视频。4 注意:拟合是一个渐近的过程,需要不断地手工拟合,但是,可能会因为峰形不好而中断,因此,请注意在拟合过程中,保存了两次SAV文件,目的是如果出现不能再继续拟合下去的情况,可以直接打开这个SAV文件再继续拟合,而不需要从头再来。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=108735]视频[/url]
SH406全自动苯结晶点测定仪适用标准GB/T3145-1982苯结晶点测定,GB/T 3069.2-2005萘结晶点测定,GB/T 3710-2009工业酚、苯酚结晶点测定,GB/T7533-1993-2005有机化工产品结晶点测定、GB/T618-2006化学试剂结晶点测定。GB/T1663-2001增塑剂结晶点测定。(苯结晶点仪,酚结晶点仪,苯酚结晶点,凝固点仪,增塑剂结晶点仪)仪器特点 :采用嵌入式系统设计,试验全过程自动检测;彩色触摸屏;可以对试验结果进行存储;可以查看历史数据;仪器上打印结果,机械自动搅拌,实验结果可以通过U盘导出,存入电脑后可以多次试验对比。技术参数1、 工作电源: AC220V±10%;50Hz。2、 工作冷槽: 双层真空玻璃浴槽。3、 冷槽控温: +80℃~-10℃。4、 控温精度: ±0.1℃。5、 浴液搅拌: 搅拌电机自动搅拌,功率6W,1200r/min。6、 制冷系统: 新型制冷压缩机。7、 试样搅拌: 同步减速电机, 60次/分钟。8、 环境温度: ≤30℃。9、 相对湿度: ≤85%。10、整机功耗: 1500W左右。

在一次金相检测过程中,经过磨制、抛光、浸蚀后,在SEM下观察(一般应为金相显微镜)发现了一处结晶体的物质。样品采用的浸蚀剂为硝酸酒精。http://ng1.17img.cn/bbsfiles/images/2012/08/201208211802_385125_1623504_3.jpg
我做实验又出了一个意外现象。这次是处理含铬废液,加完沉淀剂静置一天后,烧杯出现了大量结晶,想和大家一起分析一下这结晶是什么成分?整个过程如下:废液来源:是按照GB15063-2009测试肥料中氮含量的废液。测试时所加试剂:1g肥料样品(通常为16-8-8),1.2g铬粉,7毫升浓盐酸,煮沸冷却后加22g混合催化剂(成分为硫酸钾和五水硫酸铜20:1混合),30毫升浓硫酸,消解一个小时,冷却后加水400毫升,加400g每升氢氧化钠溶液120毫升,蒸馏。所得废液倒入废液缸。另外这废液缸里还有我上次倒的重铬酸钾-硫酸溶液500毫升左右,测有机质用的。处理时我先测pH为1,取2000毫升废液,加了3药匙硫酸亚铁,搅拌,溶液由近黑色变成绿色,硫酸亚铁全部溶解后加氢氧化钠调pH为8,溶液渐渐变成泥浆状,静置后产生大量结晶。较大的一块有1*2*10厘米,无色,因为现在手里没相机,不能拍照传上来。大家帮忙分析一下这结晶是什么成分?我怀疑是硫酸钾和硫酸钠。
从液相中出现固相属新相的产生过程,是比较困难的(毕竟是从无到有),加入晶种相当于人为引入固相。引入固相这样会更容易形成结晶,分析化学中微量硫酸盐的测定,你有采用过这种预先加入少量的硫酸钡晶种促使其硫酸钡加快形成沉淀的方法吗
近日做材料的等温冷结晶动力学,仪器用的是TA Q2000,结晶温度120℃,升温速率150 ℃/min。测试发现材料结晶太快,升到设定温度后基线还没平就开始了,很难得到完整的结晶峰。请问有什么办法可以得到完整的结晶峰?提高升温速率?换其他型号的DSC?谢谢!