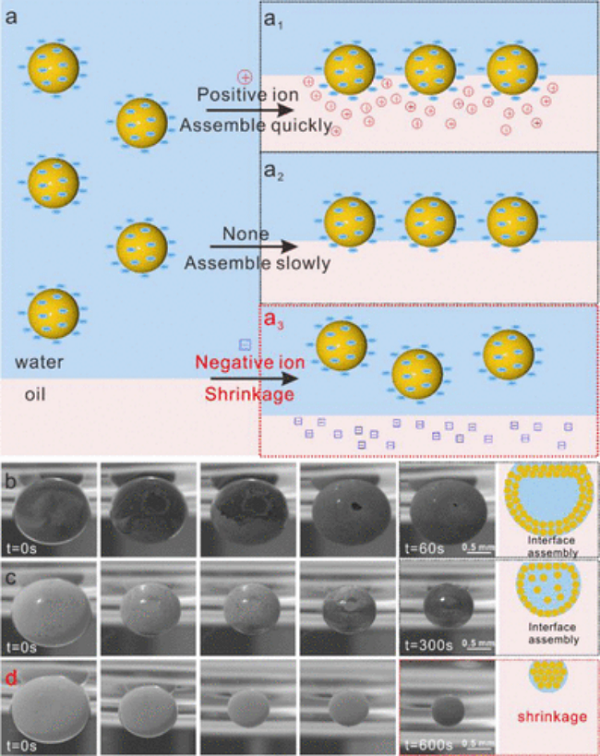
比较 2D 培养和 3D 生物打印肿瘤模型中的药物反应
导读在癌症生物学中,肿瘤微环境(TME)是肿瘤细胞和免疫系统之间的一个关键。TME是细胞外基质(ECM)、免疫细胞、信号分子、血管和成纤维细胞,它们包裹肿瘤并影响癌症进展。TME的成分通过分泌小信号分子相互作用,影响肿瘤行为的各个方面,包括细胞增殖、侵袭、转移和抗肿瘤治疗的耐药性(Bremnes,2011)。因此,重建TME对抗癌研究至关重要,但一个主要的痛点是无法开发出可预测的3D肿瘤模型用于高通量药物评估。3D肿瘤模型应再现肿瘤间质内细胞间的相互作用,并克服2D细胞培养系统的局限性。在这里,3D生物打印为预测体内结果、建模TME和评估药物反应提供了一个有前景的解决方案。肿瘤转移和化疗耐药性威胁着肿瘤患者的生存。在癌症治疗领域,化疗是一种很有效的治疗方式,它利用小的抗癌分子攻击特定的生长途径并杀死癌细胞。在这些分子中,顺铂(CIS)和吉非替尼(GEF)是FDA批准的靶向DNA和EGFR通路的抗癌药物。简而言之,CIS通过抑制细胞分裂和 mRNA的产生导致细胞凋亡,而GEF干扰癌细胞中EGFR信号的上调。有趣的是,虽然CIS和GEF都被用于治疗致命的胰腺癌和乳腺癌,但它们也与体外假阴性或假阳性预测有关,这表明它们在2D和3D中对细胞的影响不同(Reynolds, 2017)。为了进一步解决这一差异,我们使用两种乳腺癌(MCF7, MDA MB 231)和两种胰腺癌(BxPC3, Panc-1)细胞系,比较了CIS和GEF对2D单层细胞和3D生物打印类肿瘤模型的作用。材料和方法生物墨水制备和生物打印根据CELLINK方案制备3 mg/mL Coll 1 (CELLINK, Ref #IK4000002001)和5% GelMA (CELLINK, Ref #IK3051020303)用于生物打印。共3ml Coll 1或GelMA与5 x 106 cells/100µL培养基(10:1)混合,分别装入透明和琥珀色墨盒(CELLINK, Ref #CSO010311502),以~ 3kpa进行液滴打印。使用温度控制的打印头(TCPH, SKU #000000020346)设置为8℃,气动打印头分别在8℃的打印床上对Coll 1和GelMA液滴进行生物打印。使用BIO X (CELLINK, SKU #000000022222)上的液滴打印功能,将每种生物墨水打印在未经处理的96孔板(Thermo Fisher Scientific, Cat #267427)上。打印完成后,Coll 1液滴在37℃下热交联20分钟,GelMA液滴在365 nm下紫外交联6秒。每孔加100µL培养基,每2 ~ 3天更换一次。2D单层培养为了进行2D比较,将每个细胞株接种在处理过的96孔板上(Thermo Fisher Scientific, Cat #167425)。优化各细胞培养48小时后的细胞密度,达到90%的一致性。Panc-1细胞接种1.2 × 104个细胞/孔,BxPC3细胞接种1.7 × 104个细胞/孔,MCF7细胞接种2.0 × 104个细胞/孔,MDA MB 231细胞接种2.0 × 104个细胞/孔。药物治疗与分析生物打印类肿瘤细胞和2D细胞分别用不同浓度的吉非替尼(LC Laboratories,#G-4408)或顺铂(Cayman Chemical Company)处理96小时和48小时。MTS Assay(Sigma-Aldrich)和LIVE/DEAD染色试剂盒(Invitrogen)用于评估2D和3D条件下的细胞活力。所有的检测都是按照制造商的说明进行的。图1:该测定的优点显示了抗肿瘤药物对所有4种细胞系的强大作用,并描述了每种细胞类型和ECM的细胞形态变化。比例尺:1000m或650m。绿色:LIVE,红色:DEAD肿瘤根据细胞类型和培养条件适应不同的形态(Nath, 2016)。在GelMA和Coll 1中培养7天后,癌细胞聚集形成各种形态的球体。如图1所示,MDA MB 231细胞形成同心星形网络,MCF7细胞形成圆形椭球,BxPC3细胞形成葡萄状椭球,Panc-1细胞形成团块状椭球。使用GelMA和Coll 1作为肿瘤支架,由于孔隙度、刚度和成分的不同,也影响了球状体的形成。有趣的是,2D培养的癌细胞缺乏所描述的形态,可能是因为它们缺乏支持细胞间相互作用、紧密连接、营养和氧梯度的ECM(数据未显示)。3D模型的缺氧效应缺氧是药物反应的另一个变量,这是3D模型和体内组织所特有的。Warburg效应将缺氧描述为癌细胞的一种生存模式,它们从生产氧气和ATP转换为上调EGFR和AKT信号以促进增殖。这种转换增加了毒性、酸度和3D模型中的废物堆积,从而产生了一个三环低氧梯度。图1显示了低氧梯度,其中靠近球体中心的细胞呈死亡状态(红色),边缘的细胞呈存活状态(绿色)。最外面的环是一层增殖细胞,中间的环是一层活细胞,最里面的环是坏死细胞的核心,这是由于废物堆积和缺氧造成的(Nath, 2016)。顺铂在2D和3D模型的疗效分别在第2天和第7天,将低到高剂量的CIS添加到2D单层细胞和3D生物打印类肿瘤细胞中。2D细胞处理治疗48小时,3D生物打印类肿瘤治疗96小时。MTS试验显示,2D单层对所有细胞株的细胞毒性均呈剂量依赖性,3D乳腺癌类肿瘤细胞也是如此(图2A)。有趣的是,BxPC3和Panc-1细胞株在3D中比在2D中显示更高的IC50。换句话说,这两种胰腺癌细胞株在3D生物打印类肿瘤中基本上不受CIS的影响。这里,一种解释是胰腺癌细胞对CIS浓度的增加表现出了耐药性(Wang, 2016 凯兰,2007 Sangster-Guity, 2011)。针对药物治疗,胰腺癌细胞可能已经诱导了他们的生存途径,上调衰老、DNA损伤反应信号转导和跨损伤DNA合成(Gomes, 2019年)。吉非替尼在2D和3D模型的疗效EGFR癌蛋白常在乳腺癌和胰腺癌细胞系中表达。因此,药物抑制EGFR通路可导致细胞周期阻滞、衰老或凋亡(Jacobi, 2017)。如图2B所示,在3D和2D中,吉非替尼显著降低了细胞活力。对于所有细胞类型,3D Coll 1和GelMA的IC50均低于2D培养的IC50,这表明GEF在3D生物打印类肿瘤细胞中比在2D培养中造成更多的死亡。2D细胞培养的局限性2D细胞培养系统不能模拟体内肿瘤的内在特性,包括自然屏障、低氧梯度和紧密的细胞-细胞连接,这些都减缓了药物扩散。此外,它们缺乏支持3D生长和癌蛋白上调的组织特异性环境和ECM (Reynolds, 2017)。图2A的另一项研究显示,3D胰腺癌细胞比2D单层细胞对CIS的抗性更强。很明显,2D研究对于胰腺癌的体内治疗是一种误导和不准确的预测。结论使用CELLINK GelMA和Coll 1作为类肿瘤支架,为球状形成和药物扩散提供了稳定的肿瘤微环境(TME)。用GelMA和Coll 1构建的不同杀伤曲线模型表明,细胞外基质(ECM)在药物反应中起关键作用。未来的研究需要确定哪种支架适合特定的肿瘤模型。我们的研究结果显示,在2D和3D肿瘤模型中,顺铂(CIS)和吉非替尼(GEF)治疗具有剂量依赖性和细胞特异性反应。乳腺癌和胰腺癌细胞株在3D条件下比2D条件下对GEF更敏感。同样,乳腺癌细胞株3D对CIS治疗的敏感性高于2D,而胰腺细胞株对CIS治疗的敏感性则相反,提示3D模型的耐药水平升高。3D生物打印类肿瘤模型用于药物筛选,可用于减少假阴性和假阳性预测。未来的研究可以使用BIO X来扩大类肿瘤的生产,用于高通量药物测试。