有转子硫化仪和无转子硫化仪哪个好? 无转子硫化仪有哪些优点最近有客户问有转子硫化仪和无转子硫化仪哪个好,它们的优点缺点在哪?下面为您解答:无转子硫化仪的试验精度和使用时的方便程度都高于有转子硫化仪,无转子硫化仪更先进一些。 http://www.shfarui.com/zyzmxyhuayuweb2011/UploadFile/20149395034564.jpg橡胶硫化仪用于分析、测定橡胶性能指标,是国家规定的用于橡胶产品研制新产品、胶料配方检测及检定产品质量的检测仪器。橡胶硫化测试仪(简称硫化仪)通过测定对胶料往复摆动的模体或转子的作用转矩的大小,得到胶料的硫化特性曲线和特性参数,如焦烧时间,正硫化时间、模量及硫化平坦性等。 硫化仪主要有两大方面的功用:一方面可以用于进行各种橡胶配方设计开发、配方优化或新产品开发;另一方面用于对生产过程质量稳定性的控制,即通过胶料抽样检查或在线检测来监督检测产品质量,保证生产稳定性。在实际应用中,硫化仪能及时反映试样中各组分配比变化或组分成分改变等对硫化过程的影响,广大橡胶配方技术人员不可缺少的帮手。对于生产橡胶制品的厂家来说,可以用它来进行橡胶均匀性、重现性、稳定性的测试,以及橡胶配方的设计和检测。有一些厂家还用硫化仪进行生产在线检测。主要方法是对每一批橡胶进行硫化测定,检测每一批,甚至是每一时刻橡胶的硫化特性。通过特性曲线的最大转矩、最小转矩、焦烧时间、正硫化时间等特性参数来判断胶料是否满足制品的要求。 目前,按照硫化仪基本结构可分为有转子和无转子两种型号的设备。有转子硫化仪是最早的用于硫化检测的仪器。无转子硫化仪是在有转子硫化仪基础上开发出来的新一代硫化测试仪器。从先进性上讲,无转子硫化仪的试验精度和使用时的方便程度都高于有转子硫化仪,无转子硫化仪更先进一些。 1.基本原理 可硫化胶料在一定压力和一定温度下会发生化学交联作用,交联作用的结果使得胶料由混炼胶变成了硫化胶,强度和韧性大大加强。。硫化仪的工作原理就是测量在特定压力和温度下,测试胶料一些特性的变化过程。得到胶料转矩一时间的变化盐线,即硫化特性曲线。 2.两种硫化仪的性能要求及优缺点 上海发瑞仪器科技有限公司提示 硫化仪作为具有上述功能的检测仪器,必须具备如下性能要求:首先是设备整机使用稳定,故障率低。要求仪器机械调试稳定、软件使用稳定、电气安全稳定;其次是试验中要求多条曲线的重现性好、单条曲线的平滑性好。作为检测仪器,重现性和平滑性非常重要,在这两方面都稳定的前提下才能准确体现胶料本身的特性。就目前硫化仪技术的发展水平,无论是有转子硫化仪还是无转子硫化仪都可以达到很好的重现性和稳定性。试验中,使用无转子硫化仪时需要较精确地称量胶样重量。而有转子硫化仪的胶样重量要求不严,一般不用称量。这是因为无转子硫化仪是密闭模腔结构,如果胶样过多会挤压在模腔外环,影响下模体摆动,从而影响测量的转矩。而有转子硫化仪上下模体是固定的,多余的胶料会在上模压下的过程中自动挤出,对试验数据影响不大。上海发瑞仪器科技有限公司提示:但有转子硫化仪因为结构本身的原因,存在一些缺点。1)操作复杂:使用有转子硫化仪做试验时,试验完成后,熟胶样是裹在转子上的,需要人工卸胶。在胶样硬度和强度很大的情况下,经常需要利用钳子等工具卸胶,操作复杂。2)不易加玻璃纸:做硫化试验时,为了防止胶样粘模腔或其他考虑因素,经常需要加耐高温的玻璃纸,尤其是很粘的混炼胶。有转子硫化仪加玻璃纸时,需要把下片玻璃纸打一个小洞,转子上下放胶,再放人模腔内试验。即使这样,转子的上下表面还是会粘上胶,很难清理。而无转子硫化仪可以很方便的在胶样上下各加一片耐高温的玻璃纸,试验完成,只需用镊子轻轻取下即可。3)容易漏胶,造成数据异常:有转子硫化仪的下模体上有一个插转子的小孔。在实际操作中,经常会不慎把碎胶掉人孔中。如果不能及时清理,就会因为转子位置被垫高,影响试验数据。严重的话转子还会顶破上模体,造成仪器损坏。4)存在硫化曲线温度滞后的现象,使用有转子硫化仪做检测实验时,有一个很规律的现象:第一条硫化曲线存在温度滞后的现象。这一现象在参考文献里有详细研究,这里不再赘述。 3.机械结构比较 两种硫化仪的机械结构不同,无转子硫化仪的无转子硫化仪是通过测定对裹胁胶料往复摆动的模体的作用力矩的大小,得到胶料的硫化特性。模腔直径40士2mm,分离角为7。~18。,中心间距为0.5间隙值。有转子模腔直径42mm,模腔深度5.35mm。转子直径35.55mm,转子盘角度12.60(见图1)。 结构对转矩测试的影响:无转子硫化仪是通过测定对裹胁胶料往复摆动的下模体的作用转矩的大小,得到胶料的转矩特性。下模体的摆动对胶料产生剪切作用,剪切面为下模体表面。有转子依靠转子的摆动对胶料产生剪切作用,剪切面为转子的上下盘面。胶料在有转子硫化仪中受到两个面的剪切作用,产生的转矩应该大于无转子硫化仪的一个面的剪切作用,即无转子的转矩值会小于有转子的转矩值。 结构对吸热的影响:元转子硫化仪上下模体和加热片接触,作为热源对橡胶胶样加热。胶样的吸热面为整个无转子模腔内表面。有转子硫化仪除了有转子硫化仪是通过测定胶料对包复的往复摆动的转子的作用力矩的大小,得到胶料的硫化特性。模腔直径42mm,模腔深度5.35mm。转子直径35.55mm,转子盘角度12.6。依靠转子的摆动对胶料产生剪切作用,剪切面为转子的上下盘面。上下模体外,还有转子上下接触表面,但转子本身不产生热量,仅依靠空气和橡胶的热传导,一般温度比模腔低一些。所以有转子的吸热面为整个有转子模腔内表面以及温度稍低一些的转子上下表面。从模腔结构可以近似计算出胶料的吸热面积(见图2),无转子硫化仪的吸热面积约为S1—6744mm2,有转子硫化仪的吸热面积S2=5647mmz。无转子硫化仪的胶料重量约为4.89,有转子约为79。胶料单位重量对应的吸热面积可以用来反映吸热快慢。所以V1=sl/4.8,V2=s2/7。V1/V2=1.74,无转子的吸热速率大于有转予的,因此无转子的硫化时间一般要小于有转子的硫化时间。4.硫化特性数据 4.1最大转矩 试样充分硫化的剪切模量或刚度的测定值,包括平坦转矩、返原曲线的最大转矩,及在规定时间内没有出现平坦和返原曲线时的最大转矩。胶样硫化达到最大转矩时,胶料强度最大,从测力的角度来看,也表明胶料和模腔接触面的摩擦力达到最大。最大转矩越大,表明摩擦力越大。无转子硫化仪和有转子硫化仪的摩擦面构成是不同的。元转子的摩擦面积小于有转子的摩擦面积,所以无转子的最大转矩会小于有转子的最大转矩。 4.2最小转矩 未硫化试样粘度的测定值。该数值主要反映了胶料流动性的好坏和粘度的大小。流动性好ML小,粘度小ML小。一般而言,无转子硫化仪ML会比有转子的小。 4.3硫化时间 TS1:摆动角度为0.5(或1(时,转矩增加到ML+ldNm时所对应的时间,反映试件的焦烧时间。T10:转矩增加到ML+10(MH—ML)/100时所对应的时间,反映试件的焦烧时间。T50:转矩增加到ML+50(MH—ML)/100时所对应的时间。T90:转矩增加到ML+90(MH—ML)/100时所对应的时间,反映试件的正硫化时间。4个硫化时间所反映的是混炼胶开始吸热直到硫化基本完成的过程。吸热快的胶焦烧得就早,达到正硫化点的时间就越短。无转子硫化仪吸热快,对应的硫化时间比有转子的要短。 5.试验曲线及数据 由以上曲线及数据分析:有转子的ML、MH都大于无转子的;在正硫化点之前,有转子的硫化时间都比无转子长,验证了前面的分析结果。通过分析和实际数据可见,元转子和有转子测量的数据不能进行简单的比较,但二者有很好的相关性。例如一种配方的胶料在有转子中测量的硫化曲线和在无转子中测量的硫化曲线虽然不同,但硫化趋势相同。并且这两种曲线的对应关系不会改变。 从一定意义上来讲,硫化仪是用来作相对比较的设备。只有比较才能看出胶料配方的变化以及温度设定对硫化过程的影响等。用户可以把配料准确、操作工艺规范且混炼均匀的胶在任一种仪器上做实验,得到的特性曲线称为标准曲线。以后当配方发生变化或重新配置时,可用此标准曲线进行比较,判断配方的可行性。无转子有无转子的标准曲线,有转子有有转子的标准曲线,这样才能正确的分析胶料配方。 6.小结 目前,硫化仪在胶料配方研究领域的使用逐渐增强,并深入到助剂开发等其它开发领域。在实际应用中,两种硫化仪都占据着一定的市场。国内最早的无转子硫化仪生产厂家,大约98年才出现的,所以一些在线检测建立比较早的工厂,使用有转子硫化仪相对多一些。但近几年,随着无转子硫化仪技术的逐渐成熟和市场推广,已经有逐渐取代有转子硫化仪的趋势。,
空[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]量二硫化碳GB/T 14680-93各位大神 问下二硫化碳这个方法环境空气和排气筒的二硫化碳有固定时间的说法吗。因为方法上吗?只写到变色为终点,今天跟采样部讨论了很久他们认为是按照环境空气采样固定污染源采10min 环境空气采一小时!我这边认为是按照方法到变色为后停止(就是这样不同地方的采样,排气筒的时间和体积会发生变化)
硫化仪变温硫化模拟: 根据埋点硫化测温数据,取各位置相对应的胶料模拟实际工艺中温度-硫化时间关系进行变温硫化试验。部分位置在硫化初始阶段温度很低(<90℃),因此试验从硫化温度接近90℃时开始模拟。硫化过程中,随着硫化程度加深,胶料物理性能提高,但超过正硫化点后,继续硫化,胶料物理性能呈下降趋势,胶料的硫化曲线可以很明显地反映这一现象。在轮胎模拟硫化后期,即实际硫化过程开模后,胶料温度开始下降,根据弹性体的粘弹性对温度的响应,在相同形变下,高温时胶料变软,弹性转矩较小,低温时胶料较硬,弹性转矩较大。根据阿雷尼乌斯方程,温度下降10℃,硫化速度降低到原来的1/2,因此在温度较低时,胶料硫化速度很慢,在较短时间内可忽略不计。因此综合考虑硫化效应和温度效应,各位置变温硫化曲线的结束点可选在100℃。 本工作对埋点硫化测温数据进行分段处理,采用12~17个温度段,结果表明,模拟温度变化曲线与实测温度变化曲线较为接近。
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=52354]天然气、炼厂气和液化石油气中挥发性硫化物分析方法[/url]
橡胶硫化仪,FDR(平面圆盘硫化仪)是在规定的温度下,混合橡胶放在上下平板模腔之间并施以正弦波扭矩振动时,随着橡胶的硫化测定其扭矩的变化;可根据最大扭矩、最小扭矩、焦烧时间、硫化时间、粘弹性等其他因素的变化求出硫化特性的试验仪器。由于装有可达到正确的正弦波振动的圆锥回转驱动装置和四个加热器,实现了实验结果的优越的精度和再现性。 由于各个零配件彻底的总体设计,采用能适合各种测试场所的紧凑型结构的最先进的橡胶硫化仪。
在新建方法时,需要寻找合适的仪器的参数,如:功率、雾化器流量、泵速和读数时间等。版友们在做方法优化时,是以寻找被测元素的最佳强度还是最佳信背比呢?
摘要:厌氧发酵过程中,沼气组成成分及其含量不仅是判断厌氧发酵所处阶段的重要指标,也能直观地 反映厌氧发酵罐的运行情况。本试验用气相色谱优化方法对沼气三种主要成分CH4、CO2、H2S及其含量进行 检测,结果表明,沼气各成分出峰时间间隔清晰,容易识别;精密度较好,甲烷、二氧化碳、硫化氢的标准偏差分 别为0. 0109%、0 0966%、0. 1217% ,变异系数分别为0. 016%、0. 314%、0. 816%。该优化方法操作简单、方 便,定性、定量准确可靠,是一种检测沼气成分的实用方法。 关键词:气相色谱;厌氧发酵;沼气;甲烷;优化方法 随着能源短缺、环境污染问题日趋严重,环境 保护、资源回收、再生能源的开发利用已成为近年 来研究的重点。厌氧发酵产沼气法作为一种即可 处理废水和废物又能产生能源的工艺被环保行业 广泛应用。在厌氧发酵研究过程中,沼气组成 成分和含量是厌氧发酵过程的重要监控指标,不 但能够有效地反映厌氧发酵所处的阶段,亦能直 观地反映反应器运行情况。因此,在研究厌氧 发酵过程中,及时、快速和准确地监测沼气成分及 含量对研究厌氧发酵进行程度和发酵机理十分重 要。但沼气样品有它的特殊性,其保存时间有 限,普通气样袋只能保存几个小时,这就需要寻找 快速、准确的检测方法,气相色谱法是最常用的精 密测定方法。 本试验对气相色谱测定沼气成分进行了方法 优化,采用该优化方法对沼气主要成分甲烷和二氧化碳进行了检测,为了沼气工程中实际脱硫的 需要,同时对沼气中含量较少的硫化氢也进行了 测定。该优化方法操作快速、简单、方便,定性、定 量准确可靠,可用于厌氧发酵机理及发酵进行情 况的研究 1材料与方法 1. 1仪器与材料 气相色谱仪,热导检测器;联 想色谱工作站;氢气发生器(山东省化工研究所 研制);气体进样阀;100ml不锈钢定量环;无残 留绿色环保级硅胶软管;医用1 000引流袋;尾 气收纳瓶。 标准样品1:甲烷66. 3%、二氧化碳30. 8%、 氧气0. 97%,余为氢气,购自山东省半导体研究 所,下同。 标准样品2硫化氢14. 98%,余为氢气;氢氧 化钠溶液(收纳尾气);待测气样。 1. 2色谱条件 填充柱TDX01:薄膜厚度1 Pm,长度1 m,内 径3 mm,温度上限220°C;填充柱GDX- 502薄 膜厚度1 Pm,长度2 m,内径3 mm,温度上限 220°C。 1. 2. 1测定沼气中曱烷和二氧化碳的色谱条件 GDX- 502填充柱安装在右侧,TDX01填充柱 安装在左侧;左右路载气均为氢气(由氢气发生 器产生),电流为120mA;用标准混合气1作为标 样。 1. 2. 2测定沼气中硫化氢的色谱条件 GDX - 502填充柱安装在左侧,TDX01填充柱安装在右 侧;左右路载气均为氢气(由氢气发生器产生), 电流为100mA;用标准混合气2作为标样。 1. 3试验方法 1. 3.1定性的方法保留时间是定性的依据。 利用标样中已知各成分的保留时间,在同样的气 相色谱分析条件下,若样品峰与标样峰的保留时 间一样,则样品中的成分与标样中的成分相同。 1. 3.2定量的方法定量采用单点外标法。峰 面积(或者峰高)是定量的依据。利用标样中 各已知成分的浓度含量,在同样的气相色谱分析 条条!件下,样品含量与标样峰的峰面积比值等于样品图2标准样品2的GC峰[ 1.3.3测量步骤 (1)气相色谱仪最佳运行:按 优化条件设定好色谱测定条件;打开单次分析界 面,等待基线稳定。(2)标准样品测定:基线稳定 后,打开进样阀,开始进标准样品,多余的气体通 到氢氧化钠收纳瓶吸收。(3)实际样品测定:按 标准样品测定的程序方法进行。(4)标准曲线制 备:在色谱工作站,编组分表,进行标准样品和实 测样品的批处理,制备标准曲线。(5)结果计算: 在色谱工作站的数据分析中,查看各样品中各组 分的含量。 2结果与分析 2.1方法的优化 2. 1. 1测定沼气中曱烷和二氧化碳的优化方法 左右路载气流速均为40ml/min进样口温度为 100。C;柱温为95。C;检测器温度为100。C;前置温 度为100°C。 2. 1. 2测定沼气中硫化氢的优化方法左右路 载气流速均为30ml/mb;进样口温度为100。C; 柱温为50。C;检测器温度为100。C;前置温度为 100°C。 测量时气相色谱仪处于最佳运行状态且基线 稳定,在上述优化方法下,峰分离的好,没有拖尾 峰,测定时间短。测定的标准样品的峰图见图1、 图2i 图1标准样品1的GC峰
[color=#DC143C][B]微波橡胶硫化技术原理及优点[/B][/color] 1. 橡胶硫化的原理及微波橡胶硫化的优点 生橡胶受热变软,遇冷变硬、发脆,不易成型,容易磨损,易溶于汽油等有机溶剂,分子内具有双键,易起加成反应,容易老化。为改善橡胶制品的性能,生产上要对生橡胶进行一系列加工过程,在一定条件下,使胶料中的生胶与硫化剂发生化学反应,使其由线型结构的大分子交联成为立体网状结构的大分子,使从而使胶料具备高强度、高弹性、高耐磨、抗腐蚀等等优良性能。这个过程称为橡胶硫化。一般将硫化过程分为四个阶段,诱导-预硫-正硫化-过硫。为实现这一反应,必须外加能量使之达到一定的硫化温度,然后让橡胶保温在该硫化温度范围内完成全部硫化反应。 橡胶硫化可以采用各种方法。传统方法是将胶料采用蒸汽或远红外加热等硫化工艺。但由于加热温度是由介质外部向内部慢慢地热传导,因为橡胶物料是不良导热材料,对橡胶来说加热依靠物料表面向里层其传热速率是很慢的,大部分时间耗费在让橡胶达到硫化温度上。所以加热时间长、效率低、硫化均匀性不好。尤其旧工艺为消除橡胶粘连而使用硅酸镁(滑石粉),致使橡胶生产车间中粉尘弥漫,空气中粉尘含量远超过国家环保部门规定的标准。而且橡胶整体硫化状态并不理想,这是因为,常规热传导情况下,被硫化胶料表面升温与里层的时间不一,出现硫化不均匀的现象。 微波加热与传统加热方式完全不同,是将微波能量穿透到被加热介质内部直接进行整体加热,因此加热迅速,高效节能,大大缩短了橡胶硫化时间,使其加热均匀性更好,硫化质量较高。可以在较短的时间内越过橡胶极易发生粘连的诱导阶段进入预硫阶段,革除了旧工艺过程中使用滑石粉的操作,达到环保要求,该生产工艺可使大多数生产工序集中在一条生产线上完成,自动化程度高,能耗低,节省人力,生产稳定,产品质量均匀等,大大改善了生产劳动条件。2. 微波橡胶硫化技术的应用现状: 微波橡胶硫化技术自20世纪70年代问世以来得到迅速推广,特别是橡胶微波连续硫化生产线在橡胶挤出制品生产中的推广应用,其发展之迅速是史无前例的。日本是微波连续硫化技术发展较快的国家,至今已累计生产450多条微波连续硫化生产线,并向世界各国出口100余条。微波硫化技术在国外工业化国家已成为普遍的生产方式。不仅广泛用于各种挤压胶条、胶管的硫化预热,而且已用于各类轮胎的硫化预热。我国已从德国、日本、西班牙、英国等国家引进了几十条微波密封条连续硫化生产线。但进口的微波硫化生产线也存在很多问题,如价格高、维修成本高,微波箱体设计不合理、微波效率低,控制的自动化程度不够。随着国内微波能应用技术的发展,国内相继仿造和改造了多条采用微波硫化橡胶工艺的设备,有些引进设备的厂家与微波能应用厂家合作,开始着手对进口橡胶硫化设备所存在的问题进行改造,使其产品质量和产量有了较大提高。2000年以来随着多管型微波硫化设备的开发成功,使得设备成本及维修难度降低,目前橡胶的微波硫化技术已日益走向成熟,设备不断完善,向着高度自动化、省能源、减少环境污染方向努力,以满足广大用户不断提高的需求,有着巨大潜力和广阔的市场。[color=#00008B][font=楷体_GB2312]来源:网络[/font][/color]
[align=center][b]针对《GB5009.34-2016食品中二氧化硫的测定》方法的优化与总结[/b][/align]《GB5009.34-2016》中指出:对于样品的检测,碘标准滴定溶液的浓度为0.1000mol/L。但是由于标准滴定溶液浓度较大,在实际检测过程中,对于未检出二氧化硫的样品或实测值非常小的样品,滴定体积稍有差别,最终得到的双平行的数据的精密度便不符合国标中的要求。同时国标中规定用蒸馏烧瓶来蒸馏样品,蒸馏时间至少为15分钟才只能得到国标中的蒸馏题及。在实际检测过程中,这种方法不仅费时费力,还耗费水资源。所以针对本方法本人将实验过程进行了优化与改进,具体改动如下:[list=1][*]将样品的蒸馏过程由传统玻璃烧瓶改进为半自动凯氏定氮仪的蒸馏过程,,蒸馏7分钟即可得到国标中的蒸馏液,此方法不仅节约时间,还减少了水资源的浪费,通过人员比对证实,经过玻璃蒸馏烧瓶蒸馏过的样品的检测值与经半自动凯氏定氮仪蒸馏过的样品的检测值基本一致。[*]将滴定样品的碘标准滴定溶液的浓度由国标中给出的0.1000mol/L稀释成0.0050mol/L,进一步增大了滴定体积,减小滴定误差,确保实验的准确性;同时对于在检出限附近及实测值非常小的样品来说,读数精确度提高,更有力的保证检测结果的真实性、准确性。为确保实验的准确性,我们进行了人员比对,并通过多次人员比对发现最终结果基本一致。[/list]总结:通过对《GB5009.34-2016食品安全国家标准 食品中二氧化硫的测定》方法的优化,在检测过程中,既减少了资源的浪费,节省蒸馏时间及耗材的使用,又保证了结果的准确性,大大提高了实验效率。
分析含量大概是10%以下硫化氢的方法 。分析的是硫化氢燃烧制硫后的残余气体,关键问题是:有时候用标准气进色谱的出峰时间总是漂移不准,怎么回事儿?
有谁有做过固体酚醛树脂焦化时间(GT)测试的,能分享下您的测试方法或者经验么,谢谢
硫化橡胶中二硫化碳的测试有什么好的方法?是否有相关标准?
废水硫化物测定方法HJ1226-2021中,样品采集固定后于4d内测定。HJ91.1-2019规定硫化物加保存剂后保存期限24h,我们检测时,样品保存期限按照哪个标准?
最近单位要认证硫化物碘量法,接触检测行业时间不长,又是第一次做方法确认报告,不知道从何着手
如何让ECD老化时间最短?大家的方法都是什么样的?
请教各位老师,做MRM方法优化时,对各个物质的响应信号有没有要求
有谁知道在哪能查到硫化钠的分析方法,或者有谁知道分析方法可提供吗?谢谢!
油磷脂含量的测定 坩埚里炭化过程时间太长 有什么方法可以缩短炭化时间吗?
硫化碱应用的如此广泛使得在化工行业中如何快速的获得硫化碱越来越受人们关注,目前硫化碱生产常用的工艺方法有: 1.碳还原芒硝法 该方法是以煤炭作为还原剂,还原芒硝制得硫化碱。反应式: Na2SO4+2C=Na2S+2CO2-225.15KJ/mol Na2SO4+4C=Na2S+4CO-569.99KJ/mol Na2SO4+4CO=Na2S+4CO2-118.85KJ/mol CO2+C=2CO-172.42KJ/mol 2.硫化氢法 目前美国、英国、日本等国家多采用此方法生产硫化碱。该方法是以氢氧化钠溶液吸收工业硫化氢废气后,经蒸发后,制得硫化碱。反应式为: 2NaOH+H2S==Na2S+2H2O 3.硫酸钡副产品法 该方法用煤还原硫酸钡制取硫化钡,再加入硫酸钠溶液处理,生成硫化钠和沉淀硫酸钡,经抽滤分离,蒸发浓缩而得。 4.气体还原法 该方法是以气体作为还原剂,在沸腾炉中还原硫酸钠,以铁为催化剂催化,反应温度控制在600~640℃,可得优质无水颗粒状硫化钠(硫化钠含量达95~97%)。还原芒硝制得硫化碱,可作为还原剂的气体有:天然气、石油裂解气、焦炉煤气、工业氢气及合成氨生产中的原料气(即精炼气)和排空尾气等。以气体还原芒硝的反应式为: Na2SO4+4H2==Na2S+4H2O Na2SO4+CH4==Na2S+2H2O+CO2↑ Na2SO4+4CO==Na2S+4CO2↑
YS/T 349.1-2009 硫化钴精矿化学分析方法 第1部分:钴量的测定 电位滴定法YS/T 349.2-2010 硫化钴精矿化学分析方法 第2部分 铜量的测定 火焰原子吸收光谱法YS/T 349.3-2010 硫化钴精矿化学分析方法 第3部分 锰量的测定 火焰原子吸收光谱法YS/T 349.4-2010 硫化钴精矿化学分析方法 第4部分 二氧化硅量的测定 氟硅酸钾容量法镉化学分析方法
化工生产中产生的硫化氢气体污染环境,对人生生命安全有很大的威胁。且硫化氢在工艺中对催化剂类物质有很大的破坏力,因此检测化工生产中硫化氢含量是很重要的。硫化氢的检测有多种方法:检测管,[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法等。需要根据控制需要和硫化氢的浓度来选定方法。其中检测对催化剂损伤含量的硫化氢是痕量的。而酸气中硫化氢含量又是常量的。对于痕量的硫化氢检测(0.xppm)需要用毛细管柱[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法,PFPD检测器来测定。对于常量硫化氢(%)需要用填充柱[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法,TCD检测器来测定。当然如果要求快速的测定,还可以用硫化氢检测管来测定含量,不过要粗略一些。我们实验室就是根据不同的要求结合实验室仪器和试剂配置来控制生产中硫化氢含量的。下面就重点说一下微量H2S的测定:1适用于工艺气体中微量硫化氢和羰基硫(无机硫和有机硫)含量的测定。2载气(N2)携带含有硫化物的待检气体,在一定色谱条件下通过装有固定相的色谱柱经色谱柱分离后,由脉冲火焰光度检测器(PFPD)测定,以色谱峰保留时间定性、以色谱峰面积进行定量。3气体3.1 载气N2;纯度99.99%3.2 燃烧气H2;纯度99.99%3.3 助燃气Air;纯度99.9%3.4 标准气3.5 标准取样钢瓶或锡箔取样袋4 仪器4.1 Agilent6890N[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],脉冲火焰光度检测器 (OI5380)4.2 色谱柱:Gs-Gaspro,长度:30.0m,内径0.32mm,膜厚0.00mm。5 色谱条件5.1进样口,温度90℃,压力8.05psi5.2色谱柱,压力9.34psi5.3柱箱,温度50℃,时间,3.00min5.4 PFPD检测器,温度250℃,H2流量10.5ml/min,Air流量14.0ml/min,makeup流量10.0ml/min。6 分析步骤6.1 标准方法建立:在接通载气、燃气、助燃气后,接通电源,打开Agilent6890N,在色谱仪稳定后,将已配制好的标准气钢瓶上装上减压阀,将减压阀出口与色谱气体进样系统连接,采用旋转式六通阀切换进样,将六通阀旋至取样位置,打开减压阀置换10-20s,关闭减压阀,将六通阀切换至进样位置,同时按下“start”键,色谱仪开始分离检测,重复进样3-5次,误差范围不大于0.5%,即可选择一个标气样做为标准峰,然后根据第二章第二节中标准曲线制作一节可建立方法。6.2 样品测定:在色谱仪稳定后,在同建立方法的相同条件下,用标准钢瓶或锡箔袋取样,进样置换20S~30S,关闭出气口,使仪器气体进样系统瞬间达到压力平衡,迅速将六通阀切换至进样位置,同时按下“start”键,色谱工作站会自动记录出峰情况。7 结果计算7.1 根据标准气出峰保留时间定性。7.2 定量分析色谱工作站自动根据外标法,采用峰面积定量,在工作站上自动显示样品中H2S、COS、CS2的含量。保留时间 级别 含量 峰面积 含量/峰面积 参比 组 名称 [min] 信号 [ppm] -------|--|--|----------|----------|----------|---|--|--------------- 2.720 1 1 10.40000 6179.21057 1.68306e-3 总硫(COS+H2S)
有谁知道硫化氢的测定分析方法,多谢,最好是比较简单的
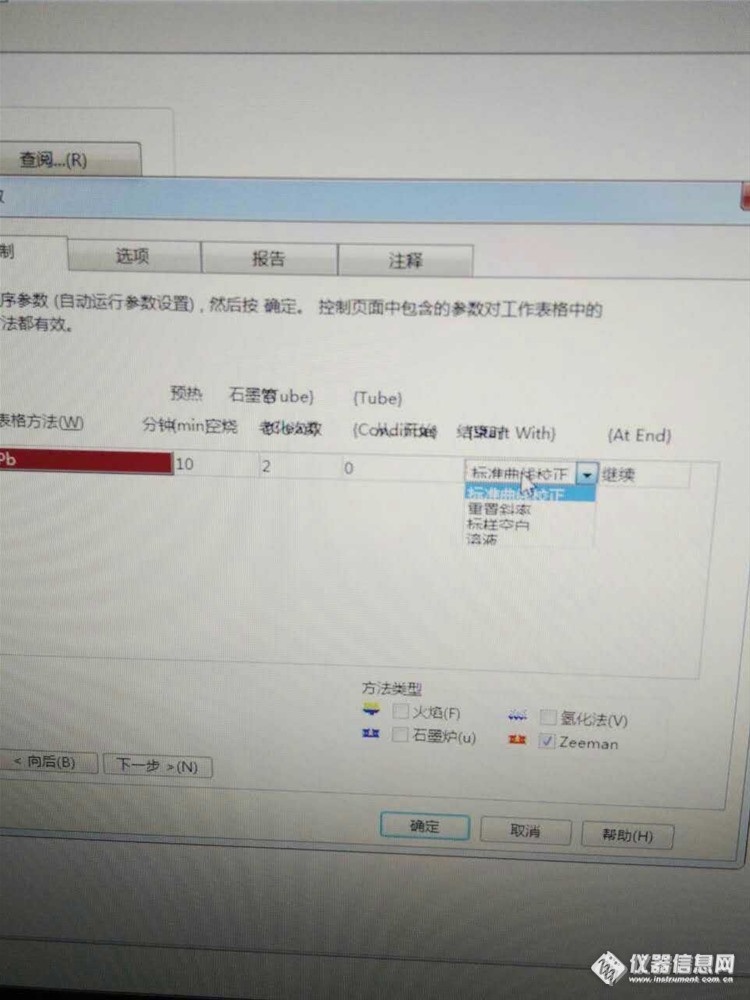
问题:方法建立后,点优化,元素灯会亮。它的那个预热倒计时时间会在那个界面右下端有显示,然后还有石墨管空烧的提示,今天操作时没有显示,是什么原因?点优化时出来一个提示,出现致命错误的提示,按确定又出现Timed move error这个提示。预热时间是在序列里设的,设了10分钟,点开始直接开始进样分析了。石墨管老化是2次。昨天好像就这样设的(第一张图),怎么选?方法建完后,点了优化,然后出来的这个(第二张图)重启过好几次,方法也设置了好几次。反正样品也正常分析呢。就是不显示预热倒计时还有石墨管空烧回复:建议打800咨询一下大家怎么看http://ng1.17img.cn/bbsfiles/images/2017/01/201701191701_669810_3114888_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/12/201612192344_01_3114888_3.jpg
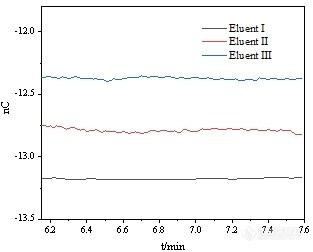
[b][font=宋体]摘要:[/font][/b][font=宋体]硫化氢([/font]H[sub]2[/sub]S[font=宋体])是生活中常见气体污染物,人体短时内吸入少量高浓度硫化氢便可导致死亡,也可对动植物、建筑设施等造成危害。针对离子色现有谱检测方法存在的问题,建立了一种准确、高效地测定微量硫化氢气体的[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url][/font]-[font=宋体]脉冲安培定量分析新方法。该法使用传统[/font]IonPac AS7 (250mm×4mm)[font=宋体]阴离子交换色谱柱,采用新型氢氧化钠[/font]-[font=宋体]草酸钠淋洗液组合,替代原有方法中氢氧化钠[/font]-[font=宋体]乙酸钠淋洗液组合,优化脉冲安培检测电位参数和积分时长。比较添加剂的种类和含量对硫化物稳定性的影响,探索了硫化物的最佳保存条件。实验结果表明,硫化物在[/font]0.01~0.20 mg/L[font=宋体]的范围内线性关系良好[/font]([font=宋体]相关系数[/font][i]r[sup]2[/sup][/i][font=宋体]可达到[/font]0.999)[font=宋体],检出限[/font]([i]S/N[/i]=3)[font=宋体]和定量限[/font]([i]S/N[/i]=10)[font=宋体]分别为[/font]1.03μg/L[font=宋体]和[/font]3.45 μg/L[font=宋体],硫化物的相对保留时间和相对峰面积的相对标准偏差[/font](RSD)[font=宋体]均小于[/font]0.2% ([i]n=6[/i])[font=宋体]。改进后方法稳定性好,基线噪音显著降低,淋洗液试剂成本只有原来的[/font]10%[font=宋体],[/font]100 μg/L[font=宋体]以下的硫化物也可检出,且峰型更为对称,更适用于实际样品中低浓度硫化物的检测。采用[/font]250 mmol/L[font=宋体]氢氧化钠[/font]-0.8%[font=宋体]乙二胺四乙酸二钠稳定液可使硫化物稳定保存[/font]10[font=宋体]小时以上,回收率和大批量、长时检测的可靠性大幅提高。将新建立的检测方法应用于学校垃圾处理站,结合被动采样法富集测定空气中硫化氢含量,检测结果均未超过国家规定限值,此法可满足硫化氢气体相关鉴定检测工作的要求。[/font][font=宋体]关键词:[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url];安培检测;硫化物;电位;草酸钠[/font][b][font=宋体]前言[/font][/b][font=宋体]硫化氢[/font](H[sub]2[/sub]S) [font=宋体]是人类生产生活中常见的气态污染物,低浓度即具有臭鸡蛋气味,且浓度足够高时能麻痹嗅觉反而不易被察觉。石油和天然气加工、采矿、造纸、废水处理、垃圾处理等均会产生硫化氢气体,来源广泛,控制困难。[/font]H[sub]2[/sub]S[font=宋体]对所有器官均有毒性,尤其是中枢神经和肺部系统,长期暴露于硫化氢环境中会出现头晕恶心,大量吸入还会造成呼吸衰竭而迅速死亡[/font][sup][1,2][/sup][font=宋体];[/font]H[sub]2[/sub]S[font=宋体]也是形成酸雨的原因之一,被氧化后形成硫酸腐蚀管道和植物根茎;对人类生产生活、自然环境产生严重影响[/font][sup][3,4][/sup][font=宋体]。[/font][font=宋体]近年来常用检测方法有分光光度法[/font][sup][5][/sup][font=宋体]、化学分析法[/font][sup][6][/sup][font=宋体]、[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法[/font][sup][7][/sup][font=宋体]、[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法[/font][sup][8][/sup][font=宋体]、现场快速检测法,如醋酸铅试纸、硫化氢报警法[/font][sup][9][/sup][font=宋体]等,以及使用气体检测器进行检测,如利用电化学、比色和光学方法进行定性定量,应用在工业环境中可对高浓度硫化氢起到警示作用[/font][sup][10,11][/sup][font=宋体]。上述方法虽能提供较可靠的检测结果,但存在灵敏度低、样品预处理较复杂、检测成本高,无法准确高效地定量低浓度的硫化氢气体等问题,即使是高浓度下,有些方法也只能半定量[/font][sup][12,13][/sup][font=宋体]。[/font][font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]高效、简便、灵敏度高等优点使其逐渐应用到测定硫化氢的工作中。已有研究是将采样的硫化氢氧化,电导检测器检测,此过程干扰众多,灵敏度较差[/font][sup][14][/sup][font=宋体];或利用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url][/font]-[font=宋体]安培检测法,将富集的硫化氢以离子形式分离,直流或脉冲安培法检测电流变化,反映出硫化氢的浓度[/font][sup][15,16][/sup][font=宋体]。但在日常检测中发现,硫化物在常规氢氧化钠碱性溶液中[/font]2h[font=宋体]就会有[/font]20%[font=宋体]左右的损失,保存困难,易被金属离子络合;且现有方法检出限高、灵敏度低,导致低浓度硫化物峰严重拖尾或不能检出,回收率仅有[/font]60%[font=宋体]左右,给实际应用带来重重困难。[/font][font=宋体]本文在原有[/font]Ag[font=宋体]电极测硫的基础上优化淋洗液条件,利用草酸钠金属络合剂的特性避免分析物损失,降低了基线噪音,分离效果更好,且成本大大降低;优化脉冲安培检测电位,在默认的硫化物电位基础上,针对低浓度硫化物优化电位参数,清洗电位中施加正向电压,探索积分时长的影响。最终线性范围拓宽,检出限、定量限更低,延长了[/font]Ag[font=宋体]电极使用寿命,建立了一套准确、可靠地测定低浓度硫化物的[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]方法;对比加入几种添加剂后硫化物稳定存在时间,得到硫化物的最佳保存条件,提高了硫化物的回收率。随后结合被动采样法将其应用于学校垃圾处理站进行实际样品检测。[/font][b]1 [font=宋体]实验部分[/font]1.1 [font=宋体]仪器[/font][font=宋体]、试剂及材料[/font][/b][font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url](美国[/font]Thermo Fisher [font=宋体]公司,[/font]ICS5000+[font=宋体])配备安培检测器和自动进样器([/font]AS-AP[font=宋体]);[/font]KQ5200DA[font=宋体]型数控超声波清洗器[/font][font=宋体](昆山市超声仪器有限公司);[/font]Milli-QA10[font=宋体]超纯水仪(美国[/font] Millipore [font=宋体]公司);[/font]50%[font=宋体]氢氧化钠溶液([/font]NaOH[font=宋体],分析纯)、乙二胺([/font]EDA [font=宋体]纯度[/font]99%[font=宋体])均购自赛默飞世尔科技中国有限公司;草酸钠([/font]Na[sub]2[/sub]C[sub]2[/sub]O[sub]4[/sub][font=宋体],纯度[/font]99.5%[font=宋体])、乙酸钠([/font]NaAc[font=宋体],纯度[/font]99%[font=宋体])均购自德国[/font]Sigma-Aldrich[font=宋体]公司;乙二胺四乙酸二钠([/font]EDTA[font=宋体],纯度[/font]99.99%[font=宋体])、硫化物标准溶液([/font]100 mg/L[font=宋体])购自上海麦克林生化科技公司[/font][b]1.2 [font=宋体]溶液的配制[/font]1.2.1 [font=宋体]稳定液的配置[/font] [/b][align=left]250mmol/L NaOH-0.8% EDTA[font=宋体]溶液:称取[/font]2.0 g 50%[font=宋体]氢氧化钠溶液、[/font]0.8 g [font=宋体]乙二胺四乙酸二钠于[/font]100 mL [font=宋体]容量瓶中,加入煮沸后冷却的超纯水,定容摇匀。[/font][/align][b]1.2.2 [font=宋体]标准溶液的配置[/font][/b][font=宋体]准确移取[/font]100 mg/L[font=宋体]的硫化物标准溶液,使用[/font]250 mmol/L NaOH-0.8% EDTA[font=宋体]溶液逐级稀释至[/font]1000[font=宋体]、[/font]500[font=宋体]、[/font]200[font=宋体]、[/font]100[font=宋体]、[/font]50[font=宋体]、[/font]20[font=宋体]、[/font]10 μg/L[font=宋体]。硫化物极易被氧化,应现配现用,避光、冷藏保存。(负二价态的硫在[/font]pH[font=宋体]>[/font]8[font=宋体]的碱性溶液中以[/font]HS[sup]-[/sup][font=宋体]状态存在,此后均用硫化物代称)[/font][b]1.2.3[font=宋体]淋洗液的配制[/font][/b][align=left][font=宋体]淋洗液(一)[/font]200 mmol/L NaOH-7.5 mmol/L Na[sub]2[/sub]C[sub]2[/sub]O[sub]4[/sub][font=宋体]溶液:称取[/font]2.0 g[font=宋体]草酸钠、[/font]32.0 g 50% [font=宋体]氢氧化钠溶液于流动相瓶中,加入超纯水至[/font]2 L[font=宋体],超声[/font]30 min[font=宋体]均匀溶液并除去气泡。淋洗液(二)[/font]100 mmol/L NaOH-500 mmol/LNaAc[font=宋体]溶液:称取[/font]41.0 g[font=宋体]乙酸钠、[/font]8.0 g 50% [font=宋体]氢氧化钠溶液于流动相瓶中,加入超纯水至[/font]1 L[font=宋体],超声[/font]30 min[font=宋体]均匀溶液并除去气泡。淋洗液(三)[/font]100 mmol/L NaOH-500 mmol/LNaAc-0.5% EDA[font=宋体]溶液:在淋洗液(二)的基础上添加[/font]5 mL[font=宋体]乙二胺溶液,加入超纯水至[/font]1 L[font=宋体]。[/font][/align][b]1.3 [font=宋体]色谱条件[/font][/b][font=宋体]色谱柱:[/font]IonPacAS7 (250mm×4mm)[font=宋体];保护柱:[/font]IonPacAG7 (50mm×4mm)[font=宋体];检测模式:安培检测;工作电极:[/font]Ag[font=宋体]电极;参比电极:[/font]Ag-AgCl[font=宋体]复合参比电极;电位波形见表[/font]5[font=宋体];淋洗液:[/font]200 mmol/L NaOH-7.5 mmol/L Na[sub]2[/sub]C[sub]2[/sub]O[sub]4[/sub][font=宋体],流速:[/font]1mL/min[font=宋体];柱温:[/font]30℃[font=宋体];进样量:[/font]25μL[font=宋体];[/font][font='Times New Roman',serif]2[/font]结果与讨论[b]2.1[font=宋体]色谱条件的优化[/font]2.1.1[font=宋体]色谱柱的选择[/font][/b] [font=宋体]硫化物分析常用[/font] IonPac AS7[font=宋体]色谱柱,该柱填料微粒较大,柱容量高,适合用于安培检测器测定高离子强度基质中的硫化物、氰化物。选取[/font]IonPac AS7[font=宋体]色谱柱使用[/font]Thermo[font=宋体]默认方法对硫化物进行分析。[/font]AS7[font=宋体]色谱柱说明书中色谱条件:色谱柱:[/font]IonPac AS7 (250mm[font=宋体]×[/font]4mm)[font=宋体];保护柱:[/font]IonPac AG7 (50mm[font=宋体]×[/font]4mm)[font=宋体];检测模式:脉冲安培检测;工作电极:[/font]Ag[font=宋体]电极;参比电极:[/font]Ag-AgCl[font=宋体]复合参比电极;电位波形见表[/font]1[font=宋体];淋洗液:[/font]100 mmol/L NaOH-500 mmol/LNaAc[font=宋体],流速:[/font]1mL/min[font=宋体];柱温:[/font]30 [font=宋体]℃;进样量:[/font]25 μL[font=宋体]。[/font][align=center][b][font=宋体]表[/font] 1 [font=宋体]默认电位波形[/font][/b][/align] [table][tr][td] [align=center]Time/s[/align] [/td][td] [align=center]Waveform/mV[/align] [/td][td] [align=center]Integration/s[/align] [/td][/tr][tr][td] [align=center]0.00[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]0.20[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center]Begin[/align] [/td][/tr][tr][td] [align=center]0.90[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center]End[/align] [/td][/tr][tr][td] [align=center]0.91[/align] [/td][td] [align=center]-1.0[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]0.93[/align] [/td][td] [align=center]-0.3[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]1.00[/align] [/td][td] [align=center]-0.3[/align] [/td][td] [align=center] [/align] [/td][/tr][/table][font=宋体]实验结果显示,硫化物峰存在拖尾现象,低于[/font]100 μg/L[font=宋体]硫化物不能检出,且信号基线较高、噪音较大,掩盖部分低浓度硫化物色谱峰[/font][sup][17][/sup][font=宋体]。[/font][b]2.1.2 [font=宋体]流动相类型的选择[/font][/b][font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]使用的专用乙酸钠等级较高,目前国内无法生产,全部依赖进口;此外,淋洗液中高浓度乙酸钠使基线高、噪音大且成本较高,不利于日常分析检测。尝试使用草酸钠替代乙酸钠降低基线噪音,且草酸能与硫化物样品中可能存在的金属离子形成络合物,以避免分析物的损失;乙二胺可作为掩蔽剂减小对硫化物测定的影响。使用淋洗液(一)、(二)(三)测定相同浓度硫化物,考察替换乙酸钠和加入乙二胺的影响。[/font][align=center][font=宋体][img=,313,252]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311053440504_285_1617661_3.jpg!w313x252.jpg[/img][/font][/align][font=宋体][/font][align=center][b][font=宋体]图[/font]1 [font=宋体]不同种淋洗液对基线噪音的影响[/font][/b][/align][font=宋体]实验发现乙二胺加入后硫化物峰形没有改善。低浓度草酸钠代替高浓度的乙酸钠,降低了约五倍噪音(见图[/font]1[font=宋体]),且有非常好的柱效和选择性,草酸钠成本仅是乙酸钠的[/font]0.2%[font=宋体],淋洗液总成本降低近九成,故选用[/font]200 mmol/L NaOH-7.5 mmol/L Na[sub]2[/sub]C[sub]2[/sub]O[sub]4[/sub][font=宋体]进行后续实验。[/font][b]2.1.3 [font=宋体]电位参数的选择[/font][/b][font=宋体]除在流动相中适当添加络合剂外,电位参数的改变可更好改善硫化物峰的突然消失和严重拖尾现象。常规方法分析时[/font]100 μg/L[font=宋体]以下硫化物的色谱峰消失,猜测原因一是部分硫化物被系统中残留的金属离子络合;二是安培检测电位参数不合理,导致部分硫化物未完全参与氧化还原反应;三是电位参数中清洗电位不合理,导致色谱峰拖尾且降低电极一次打磨后的使用寿命[/font][sup][18,19][/sup][font=宋体]。在默认电位波形(表[/font]1[font=宋体])的基础上,尝试改变清洗电位参数,对于低浓度硫化物,施加正向电位[/font]0.1 mV[font=宋体],积分电位[/font]-0.1 mV[font=宋体],仅积分[/font] 0.1 s[font=宋体]。改进电位波形如表[/font]2[font=宋体]所示[/font][sup][20][/sup][font=宋体]。[/font][align=center][b][font=宋体]表[/font]2 [font=宋体]硫化物改进电位波形[/font][/b][/align] [table][tr][td] [align=center]Time/s[/align] [/td][td] [align=center]Waveform/mV[/align] [/td][td] [align=center]Integration/s[/align] [/td][/tr][tr][td] [align=center]0.00[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]0.20[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center]Begin[/align] [/td][/tr][tr][td] [align=center]0.30[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center]End[/align] [/td][/tr][tr][td] [align=center]0.31[/align] [/td][td] [align=center]0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]0.40[/align] [/td][td] [align=center]0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][/table][align=center][img=,231,189]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311055220716_7826_1617661_3.jpg!w289x237.jpg[/img][/align][align=center][b][font=宋体]图[/font]2 [font=宋体]改进电位波形下[/font]10 μg/L[font=宋体]硫化物色谱图[/font][/b][/align][font=宋体]由图[/font]2[font=宋体]所示,低浓度[/font]10 μg/L[font=宋体]的硫化物也可检出,且拖尾问题得到明显改善。其中峰尾基线的减少是由于[/font]Ag[sub]2[/sub]S[font=宋体]沉淀后电极表面的电化学恢复,硫化银沉淀被还原,换言之,[/font]Ag[sub]2[/sub]S[font=宋体]沉淀通过产生总体负电流的电势循环而被消除[/font][sup][20][/sup][font=宋体]。[/font][b]2.1.4 [font=宋体]安培积分时长的选择[/font][/b][font=宋体]新改进电位峰面积较小,不利于降低检出限和应用于实际采样检测,尝试增加积分时长以增加积分定量的准确性,提高灵敏度。设置积分时间[/font]0.2[font=宋体]、[/font]0.3[font=宋体]、[/font]0.4[font=宋体]、[/font]0.5[font=宋体]、[/font]0.6[font=宋体]、[/font]0.7s[font=宋体],进样相同浓度的硫化物标准溶液。[/font][align=center][b][font=宋体]表[/font]3 [font=宋体]积分时长对峰面积的影响[/font][/b][/align] [table][tr][td] [align=center][color=black]Integration time[i]/[/i]s[/color][/align] [/td][td] [align=center][color=black]Peak area/(nCmin)[/color][/align] [/td][/tr][tr][td] [align=center][color=black]0.2[/color][/align] [/td][td] [align=center][color=black]9.4919[/color][/align] [/td][/tr][tr][td] [align=center][color=black]0.3[/color][/align] [/td][td] [align=center][color=black]18.8029[/color][/align] [/td][/tr][tr][td] [align=center][color=black]0.4[/color][/align] [/td][td] [align=center][color=black]28.3009[/color][/align] [/td][/tr][tr][td] [align=center][color=black]0.5[/color][/align] [/td][td] [align=center][color=black]37.4532[/color][/align] [/td][/tr][tr][td] [align=center][color=black]0.6[/color][/align] [/td][td] [align=center][color=black]47.9043[/color][/align] [/td][/tr][tr][td] [align=center][color=black]0.7[/color][/align] [/td][td] [align=center][color=black]57.3832[/color][/align] [/td][/tr][tr][td] [align=center][color=black]Linare equation[/color][/align] [align=center][i][color=black]r2[/color][/i][/align] [/td][td] [align=center][i][color=black]y = 8.307x[sup]2[/sup] + 88.50x - 8.526[/color][/i][color=black] 0.9998[/color][/align] [/td][/tr][/table][align=left][font=宋体]以积分时间([/font]x, s[font=宋体])为横坐标,色谱峰面积([/font]Y[font=宋体])为纵坐标进行线性拟合,表[/font]4[font=宋体]可以看出,满足二次线性方程[/font][i]y = 8.307x[sup]2[/sup] +88.50x - 8.526[/i][font=宋体],线性关系良好,[/font][i]r2[/i] = 0.9998[font=宋体]。但积分时间增加,清洗电位没有改变,硫化物在[/font] Ag [font=宋体]电极上与[/font] AgO [font=宋体]等银氧化物的反应时间延长,加剧银电极消耗,对后续硫化物在电极上响应有影响[/font][sup][21, 22][/sup][font=宋体]。尝试设置积分时长和清洗时长[/font]1[font=宋体]:[/font]1[font=宋体],[/font]3[font=宋体]:[/font]1[font=宋体]等电位波形,观察硫化物色谱峰均不理想,继续改进后选定四电位波形即加入默认电位中的反向清洗电位以期望得到最佳峰形和使用寿命。使用表[/font]4[font=宋体]所示电位检测[/font]100[font=宋体]、[/font]20[font=宋体]、[/font]10 μg/L[font=宋体]硫化物标准溶液,结果见图[/font]3[font=宋体]。[/font][/align][align=center][b][font=宋体]表[/font]4 [font=宋体]硫化物高浓度新电位波形[/font][/b][/align] [table][tr][td] [align=center]Time/s[/align] [/td][td] [align=center]Waveform/mV[/align] [/td][td] [align=center]Integration/s[/align] [/td][/tr][tr][td] [align=center]0.00[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]0.20[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center]Begin[/align] [/td][/tr][tr][td] [align=center]0.80[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center]End[/align] [/td][/tr][tr][td] [align=center]0.81[/align] [/td][td] [align=center]0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]0.90[/align] [/td][td] [align=center]0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]0.91[/align] [/td][td] [align=center]0.3[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]1.00[/align] [/td][td] [align=center]0.3[/align] [/td][td] [align=center] [/align] [/td][/tr][/table][align=center][img=,690,193]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311056125232_554_1617661_3.png!w690x193.jpg[/img][/align][align=center][b][font=宋体]图[/font] 3 [font=宋体]高浓度电位波形下[/font]100, 20, 10 μg/L[font=宋体]硫化物色谱图[/font][/b][/align][align=left][font=宋体]结果可见中等浓度的色谱峰峰形对称,[/font]100 μg/L[font=宋体]浓度的样品有较好峰形,而低浓度色谱峰出现拖尾现象,故认为表4中四电位波形应用到大于[/font]100 μg/L[font=宋体]较高浓度[/font][font=宋体]硫化物的检测中,能得到令人满意的峰形、灵敏度以及最佳电极使用寿命。 [/font][/align][align=left][font=宋体]而实际环境中能采集到的硫化氢较少,故以低浓度硫化物得到最佳色谱峰形为准,认为正向清洗电位下的色谱峰形最能接受。[/font][font=宋体]最后基于色谱峰形、整个安培电位循环时长、实际采集样品浓度以及[/font] Ag [font=宋体]电极一个打磨周期使用寿命的考虑,在表[/font]4[font=宋体]电位基础上延长积分时间为[/font] 0.7 s[font=宋体]。低浓度样品脉冲安培电位波形如表[/font]5[font=宋体]所示。[/font][/align][align=center][b][font=宋体]表[/font]5 [font=宋体]硫化物低浓度新电位波形[/font][/b][/align] [table][tr][td] [align=center]Time/s[/align] [/td][td] [align=center]Waveform/mV[/align] [/td][td] [align=center]Integration/s[/align] [/td][/tr][tr][td] [align=center]0.00[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]0.20[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center]Begin[/align] [/td][/tr][tr][td] [align=center]0.90[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center]End[/align] [/td][/tr][tr][td] [align=center]0.91[/align] [/td][td] [align=center]0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]1.00[/align] [/td][td] [align=center]0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][/table][align=center][img=,251,202]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311056231564_7993_1617661_3.jpg!w315x253.jpg[/img][/align][align=center][b][font=宋体]图[/font]4 [font=宋体]低浓度新电位波形下[/font]10 μg/L[font=宋体]硫化物色谱图[/font][/b][/align][font=宋体]图[/font]4[font=宋体]结果表明,此电位下低浓度峰型良好,可应用于实际样品中低浓度硫化物检测。[/font][b]2.2 [font=宋体]硫化物稳定性研究[/font][/b][font=宋体]为延长硫化物稳定存在的时间,尝试在溶剂中添加一定量[/font]EDTA[font=宋体]、[/font]EDA[font=宋体]和抗氧化剂(抗坏血酸([/font]AsA[font=宋体])、次亚磷酸钠([/font]SHP[font=宋体]))减少硫化物的损失[/font][sup][23,24][/sup][font=宋体]。[/font]5[font=宋体]种稳定液作为稀释溶剂,将[/font]100 mg/L[font=宋体]的硫化物标准溶液稀释后避光冷藏储存,于[/font] 0[font=宋体]、[/font]1[font=宋体]、[/font]2[font=宋体]、[/font]3[font=宋体]、[/font]4[font=宋体]、[/font]5[font=宋体]、[/font]8[font=宋体]、[/font]12[font=宋体]、[/font]16 h[font=宋体]后进样,根据色谱峰面积计算剩余浓度,得到不同保存时长下的硫化物含量。结果表明,抗坏血酸的加入,出现杂峰,其他溶液并未出现杂峰;除[/font]EDTA[font=宋体]外几种稳定液中硫化物含量[/font]8 h[font=宋体]即降到[/font]60%[font=宋体]以下,[/font]EDTA[font=宋体]稳定液[/font]3 h[font=宋体]内无明显变化,[/font]16 h[font=宋体]可保持在[/font]90%[font=宋体]以上。[/font][font=宋体]随后讨论加入[/font]EDTA[font=宋体]的最佳含量,选取种质量分数的[/font]250 mmol/L NaOH - EDTA[font=宋体]溶液作将硫化物稀释至[/font]1 mg/L[font=宋体],间隔[/font]0[font=宋体]、[/font]2[font=宋体]、[/font]4[font=宋体]、[/font]6[font=宋体]、[/font]8[font=宋体]、[/font]10 h[font=宋体]进样,各保存时间下硫化物的含量如图[/font]5[font=宋体]所示。[/font][align=center][img=,237,195]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311056308605_1960_1617661_3.jpg!w297x243.jpg[/img][/align][align=center][b][font=宋体]图[/font]5 [font=宋体]不同质量分数的[/font]EDTA [font=宋体]对硫化物稳定性的影响[/font][/b][/align][font=宋体]图[/font]5[font=宋体]结果表明,质量分数为[/font]0.8%[font=宋体]和[/font]1.0%[font=宋体]的[/font]EDTA[font=宋体]均能保证[/font]10 h[font=宋体]内损失[/font]2%[font=宋体]左右,从效果和使用量考虑,使用[/font]250 mmol/L NaOH-0.8% EDTA[font=宋体]作为稳定溶液。[/font][b]2.3 [font=宋体]方法学验证[/font]2.3.1 [font=宋体]线性范围、检出限和定量限[/font][/b][font=宋体]将[/font]100 mg/L[font=宋体]硫化物标准溶液逐级稀释为[/font]0.20[font=宋体]、[/font]0.10[font=宋体]、[/font]0.05 [font=宋体]、[/font]0.02[font=宋体]、[/font]0.01 mg/L [font=宋体]。选择新色谱条件,低浓度电位波形下对系列标准样品依次进样,平行测定[/font]3[font=宋体]次。[/font][align=center][b][font=宋体]表[/font]6 [font=宋体]硫化物的素的线性范围、线性方程、相关系数、检出限和定量限[/font][/b][/align] [table=554][tr][td] [align=center]Compond ([i]n[/i]=3[font=宋体])[/font][/align] [/td][td] [align=center]Linear range /(mg/L )[/align] [/td][td] [align=center]Linear equation[/align] [/td][td] [align=center][i]r2[/i][/align] [/td][td] [align=center]LOD/(μg/L)[/align] [/td][td] [align=center]LOQ/(μg/L)[/align] [/td][/tr][tr][td] [align=center]Sulfide[/align] [/td][td] [align=center]0.01~0.20[/align] [/td][td] [align=center][i]y = 28.99x - 0.467[/i][/align] [/td][td] [align=center]0.9997[/align] [/td][td] [align=center]1.03[/align] [/td][td] [align=center]3.45[/align] [/td][/tr][/table][align=left][font=宋体]以标准样品浓度([/font]x, mg/L[font=宋体])为横坐标,色谱峰面积([/font]Y[font=宋体])为纵坐标进行线性拟合。结果如表[/font]7[font=宋体]所示,在[/font]0.01~0.20 mg/L[font=宋体]范围内线性关系良好[/font][i]r[sup]2[/sup][/i][font=宋体]>[/font]0.999[font=宋体],以信噪比[/font][i]S/N[/i]≥[font=宋体]3确定检出限为[/font] 1.03 μg/L[font=宋体],以[/font][i]S/N[/i] ≥ 10[font=宋体]确定定量限为[/font]3.45 μg/L[font=宋体]。与原方法相比,新色谱条件可用于[/font]100 μg/L[font=宋体]以下硫化物的分析,检出限和定量限更低,对空气中微量硫化氢气体检测有重要意义。[/font][/align][b]2.3.2 [font=宋体]重复性[/font][/b][font=宋体]对配制好的[/font]0.1 mg/L[font=宋体]硫化物标准样品平行进样[/font]6[font=宋体]次。结果表明,硫化物的峰面积和保留时间均[/font]RSD%≤0.20%[font=宋体],说明该方法精密度高,重复性好且适用于实际样品检测。[/font][b]2.3.3 [font=宋体]回收率[/font][/b][font=宋体]使用徽章式被动采样器[/font][sup][25][/sup][font=宋体]采集硫化物,对回收率进行验证。向[/font]100 μL[font=宋体]硫化氢被动采样吸收液中加入[/font]0.2[font=宋体]、[/font]0.1 mg/L[font=宋体]硫化物标准溶液[/font]0.05 mL[font=宋体],[/font]30 min[font=宋体]后,加入[/font]250 mmol/L NaOH-0.8% EDTA [font=宋体]溶液[/font]5 ml[font=宋体]超声提取[/font]15 min[font=宋体]检测,获得被动采样方法回收率。向准备好的被动采样器中分别加入[/font]50 mg/L[font=宋体]硫化物标准溶液[/font]0.025[font=宋体]、[/font]0.05[font=宋体]、[/font]0.1 mL[font=宋体],得低、中、高三组加标采样器,与另一组不加标采样器相同条件下采样三天,加入[/font]250 mmol/L NaOH-0.8% EDTA [font=宋体]溶液[/font]5 ml[font=宋体]超声提取[/font]15 min[font=宋体]后检测,获得实际采样回收率。[/font][align=center][b][font=宋体]表[/font]7 [font=宋体]硫化物两个浓度下被动采样方法回收率和实际采样回收率[/font][/b][/align] [table=99%][tr][td] [color=black] [/color] [/td][td=3,1] [align=center][color=black]Method recovery[/color][sup][color=black]*[/color][/sup][/align] [/td][td=4,1] [align=center][color=black]Sampling recovery[/color][sup][color=black]*[/color][/sup][/align] [/td][/tr][tr][td] [align=center][color=black] [/color][/align] [/td][td] [align=center][color=black]Found[/color][/align] [align=center][color=black]mg/L[/color][/align] [/td][td] [align=center][color=black]Added[/color][/align] [align=center][color=black]mg/L[/color][/align] [/td][td] [align=center][color=black]Recovery[/color][/align] [align=center][color=black]%[/color][/align] [/td][td] [align=center][color=black]Background[/color][/align] [align=center][color=black] mg/L[/color][/align] [/td][td] [align=center][color=black]Added mg/L[/color][/align] [/td][td] [align=center][color=black]Found[/color][/align] [align=center][color=black]mg/L[/color][/align] [/td][td] [align=center][color=black]Recovery[/color][/align] [align=center][color=black]%[/color][/align] [/td][/tr][tr][td] [align=center][color=black]High concentration[/color][/align] [/td][td] [align=center][color=black]0.1910[/color][/align] [/td][td] [align=center][color=black]0.2000[/color][/align] [/td][td] [align=center][color=black]95.5[/color][/align] [/td][td] [align=center][color=black]0.9557[/color][/align] [/td][td] [align=center][color=black]0.2500[/color][/align] [/td][td] [align=center][color=black]1.1344[/color][/align] [/td][td] [align=center][color=black]80.7[/color][/align] [/td][/tr][tr][td] [align=center][color=black]Low concentration[/color][/align] [/td][td] [align=center][color=black]0.0988[/color][/align] [/td][td] [align=center][color=black]0.1000[/color][/align] [/td][td] [align=center][color=black]98.9[/color][/align] [/td][td] [align=center][color=black]0.5019[/color][/align] [/td][td] [align=center][color=black]0.5000[/color][/align] [/td][td] [align=center][color=black]0.9456[/color][/align] [/td][td] [align=center][color=black]91.2[/color][/align] [/td][/tr][/table] [font=宋体]*[/font] Method Recovery=Found/Added [font=Symbol]′[/font] 100%.[font=宋体]*[/font]SamplingRecovery=(Found[font=宋体]-[/font]Background)/Added[font=Symbol]′[/font] 100%.[align=left][font=宋体]结果表明(见表[/font]7[font=宋体]),两种浓度下方法回收率均大于[/font]95%[font=宋体],采样回收率均大于[/font]80%[font=宋体]。[/font][/align][b]2.4 [font=宋体]实际样品检测[/font][/b]垃圾站是日常生活场所中硫化氢含量较高的区域,由微生物在厌氧条件下分解有机物产生[sup][font='Times New Roman',serif][26][/font][/sup]。将组装好的被动采样器置于学校两处垃圾处理站,隔[font='Times New Roman',serif]12 h[/font]取出一批,加入[font='Times New Roman',serif]250 mmol/L NaOH-0.8% EDTA [/font]溶液[font='Times New Roman',serif]5 ml[/font]超声提取[font='Times New Roman',serif]15min[/font]后检测。根据如下公式[sup][font='Times New Roman',serif][25][/font][/sup]计算得到环境中的硫化氢气体含量,结果如表[font='Times New Roman',serif]9[/font]所示。[align=center]C=m[sub]s[/sub]/at[/align]式中[font='Times New Roman',serif]t[/font]为被动采样的时间[font='Times New Roman',serif]h[/font],[font='Times New Roman',serif]C[/font]为硫化氢气体在时间[font='Times New Roman',serif]t[/font]内空气中硫化氢的平均浓度[font='Times New Roman',serif]μg/m[sup]3[/sup][/font],[font='Times New Roman',serif]m[sub]s[/sub][/font]为采样器在时间[font='Times New Roman',serif]t[/font]小时内采集到硫化氢气体的总质量[font='Times New Roman',serif]μg[/font]。[font='Times New Roman',serif]a=1.1836×10[sup]-4[/sup][/font]为被动采样的吸收系数[font='Times New Roman',serif]m[sup]3[/sup]/h[/font]。[align=center][b][font=宋体]表[/font]8 [font=宋体]学校垃圾站点硫化氢浓度检测结果[/font][/b][/align] [table=631][tr][td=4,1] [align=center]Position[font=宋体]Ⅰ[/font][/align] [/td][td=4,1] [align=center]Position[font=宋体]Ⅱ[/font][/align] [/td][/tr][tr][td] [align=center]Time (h)[/align] [/td][td] [align=center]Concentration in the extract/(mg/L)[/align] [/td][td] [align=center]Adsorbed H[sub]2[/sub]S mass/(μg)[/align] [/td][td] [align=center]Concentration in the air (μg/m[sup]3[/sup])[/align] [/td][td] [align=center]Time (h)[/align] [/td][td] [align=center]Concentration in the extract/(mg/L)[/align] [/td][td] [align=center]Adsorbed H[sub]2[/sub]S mass/(μg)[/align] [/td][td] [align=center]Concentration in the air /(μg/m[sup]3[/sup])[/align] [/td][/tr][tr][td] [align=center]12[/align] [/td][td] [align=center]0.028[/align] [/td][td] [align=center]0.140[/align] [/td][td] [align=center]9.856[/align] [/td][td] [align=center]12[/align] [/td][td] [align=center]0.017[/align] [/td][td] [align=center]0.085[/align] [/td][td] [align=center]5.985[/align] [/td][/tr][tr][td] [align=center]24[/align] [/td][td] [align=center]0.036[/align] [/td][td] [align=center]0.180[/align] [/td][td] [align=center]6.337[/align] [/td][td] [align=center]24[/align] [/td][td] [align=center]0.026[/align] [/td][td] [align=center]0.130[/align] [/td][td] [align=center]4.576[/align] [/td][/tr][tr][td] [align=center]36[/align] [/td][td] [align=center]0.073[/align] [/td][td] [align=center]0.365[/align] [/td][td] [align=center]8.550[/align] [/td][td] [align=center]36[/align] [/td][td] [align=center]0.0563[/align] [/td][td] [align=center]0.280[/align] [/td][td] [align=center]6.571[/align] [/td][/tr][tr][td] [align=center]48[/align] [/td][td] [align=center]0.089[/align] [/td][td] [align=center]0.445[/align] [/td][td] [align=center]7.833[/align] [/td][td] [align=center]48[/align] [/td][td] [align=center]0.085[/align] [/td][td] [align=center]0.425[/align] [/td][td] [align=center]7.481[/align] [/td][/tr][tr][td] [align=center]72[/align] [/td][td] [align=center]0.126[/align] [/td][td] [align=center]0.630[/align] [/td][td] [align=center]7.393[/align] [/td][td] [align=center]72[/align] [/td][td] [align=center]0.097[/align] [/td][td] [align=center]0.485[/align] [/td][td] [align=center]5.691[/align] [/td][/tr][/table][font=宋体]表[/font]9[font=宋体]可以看出学校内两个垃圾站点中硫化氢含量均未超过国家规定居民区硫化氢的限值[/font]0.01 mg/m[sup]3[/sup] [sup][27][/sup][font=宋体]。[/font][font='Times New Roman',serif]3 [/font]结论[font=宋体]本文针对硫化物常规安培检测中灵敏度不高以及保存稳定性差的问题,对比不同环境下硫化物的保存效果,最终选定质量分数[/font]250 mmol/L NaOH-0.8% EDTA[font=宋体]作为稳定剂,可保证[/font]10 h[font=宋体]内测定结果稳定;在淋洗液中加入草酸钠替代醋酸钠,同时对安培积分电位、积分时长等条件进行优化。结果表明该分析方法试剂成本只有原来的[/font]10%[font=宋体],线性范围拓宽,拟合效果更好,检出限、定量限更低,采样回收率提高到[/font]80%[font=宋体]以上,[/font][font=宋体]更适用于日常微量硫化氢的实际检测。[/font][font=宋体] [/font][font=宋体] [/font][b][font=宋体]参考文献:[/font][/b][font='Times New Roman',serif][1] [/font][font='Times New Roman',serif]Czarnota J,Mas?oń A, Pajura R. Int. J. Environ. Res. Public Health, 2023, 20 (7): 5379[/font][font='Times New Roman',serif][2] [/font][font='Times New Roman',serif]Godoi A F L,Grasel A M, Polezer G, et al. Total Environ, 2018, 610-611: 583-590[/font][font='Times New Roman',serif][3] [/font][font='Times New Roman',serif] Zeng Z G, Lin T, Kang T. Guang Xi Journal ofLight Industry, 2008, (03): 89-90 [/font][font=宋体]曾志果,林铁,康媞[/font][font='Times New Roman',serif]. [/font][font=宋体]广西轻工业[/font][font='Times New Roman',serif], 2008, (3): 89-90[/font][font='Times New Roman',serif][4] [/font][font='Times New Roman',serif]Zhou W, PengM, Liang Q X, et al. Chin. J. Org. Chem, 2023, 43, 1-9[/font][font='Times New Roman',serif][5] [/font][font='Times New Roman',serif]He C T,Morden Chemical Research, 2022, (19):72-74[/font][font=宋体]何楚婷[/font][font='Times New Roman',serif]. [/font][font=宋体]当代化工研究[/font][font='Times New Roman',serif], 2022, (19): 72-74[/font][font='Times New Roman',serif][6] [/font][font='Times New Roman',serif]GB/T7714-2017, Soil and sediment - Determination of sulfide -Methylene bluespectrophotometric method:[s][/s][/font][s][font='Times New Roman',serif]GB/T 7714-2017, [/font][font=宋体]土壤和沉积物[/font][font=宋体]硫化物的测定[/font][font=宋体]亚甲基蓝分光光度法[/font][font='Times New Roman',serif]: [s][/s][/font][s][font='Times New Roman',serif][7] [/font][font='Times New Roman',serif]GB/T14678-1993, Air quality-Determination of sulfuretted hydrogen, methylsulfhydryl, dimethyl sulfide and dimethyl disulfide - Gas chromatography[s][/s][/font][s][font='Times New Roman',serif]GB/T 14678-1993, [/font][font=宋体]空气质量[/font][font=宋体]硫化氢、甲硫醇、甲硫醚和二甲二硫的测定[/font][font=宋体]气相色谱法[/font][font='Times New Roman',serif][s][/s][/font][s][font='Times New Roman',serif][8] [/font][font='Times New Roman',serif]Liu B, Liu JL, Wang R, et al. Chinese Journal of Inorganic Analytical Chemistry, 2023, 13(04):349-355[/font][font=宋体][color=#333333][back=white]刘[/back][/color][/font][font=宋体]冰,刘金蓉,王莹,等[/font][font='Times New Roman',serif]. [/font][font=宋体]中国无机分析化学[/font][font='Times New Roman',serif], 2023, 13(04): 349-355[/font][font='Times New Roman',serif][9] [/font][font='Times New Roman',serif]Liu H Y,Metrology & Measurement Technique, 2021, 48(11): 79-81[/font][font=宋体]刘红英[/font][font='Times New Roman',serif]. [/font][font=宋体]计量与测试技术[/font][font='Times New Roman',serif], 2021, 48 (11)[/font][font=宋体]:[/font][font='Times New Roman',serif]79-81[/font][font='Times New Roman',serif][10] [/font][font='Times New Roman',serif] Ba H S, Khir M H, Al-douri Y, et al. J PhysConf Ser, 2021, 1962(1): 012003[/font][font='Times New Roman',serif][11] [/font][font='Times New Roman',serif] Chen S W, Song T T, Yin X W, Electron Devices,2020, 43(4): 736-40[/font][font=宋体]陈书旺,宋彤彤,尹晓伟[/font][font='Times New Roman',serif]. [/font][font=宋体]电子器件[/font][font='Times New Roman',serif], 2020, 43(4): 736-40[/font][font='Times New Roman',serif][12] [/font][font='Times New Roman',serif]Jiang H,Morden Chemical Research, 2020, (20): 119-120[/font][font=宋体]蒋辉[/font][font='Times New Roman',serif]. [/font][font=宋体]当代化工研究[/font][font='Times New Roman',serif], 2020, (20): 119-120[/font][font='Times New Roman',serif][13] [/font][font='Times New Roman',serif] Zhou L L, Zhou C, Sun H X, Hunan NonferrousMetals, 2022, 38(4): 74-77[/font][font=宋体]周璐璐,周超,孙海侠[/font][font='Times New Roman',serif]. [/font][font=宋体]湖南有色金属[/font][font='Times New Roman',serif], 2022, 38(4): 74-77[/font][font='Times New Roman',serif][14] [/font][font='Times New Roman',serif]Jiao Y J, LiY J, Ningxia Journal of Agriculture and Forestry Science and technology, 2013, 54(03):100-102[/font][font=宋体]焦玉娟,李玉洁[/font][font='Times New Roman',serif]. [/font][font=宋体]宁夏农林科技[/font][font='Times New Roman',serif], 2013, 54(03): 100-102[/font][font='Times New Roman',serif][15] [/font][font='Times New Roman',serif]Zhang Y, FuJ, Cao J B, et al, Occupation and Health, 2017, 33(15): 2068-2070[/font][font=宋体]张妍,傅佳,曹建彪[/font][font='Times New Roman',serif]. [/font][font=宋体]职业与健康[/font][font='Times New Roman',serif], 2017, 33(15): 2068-2070[/font][font='Times New Roman',serif][16] [/font][font='Times New Roman',serif] Li R Y, Liang L N, Li J, Chinese Journal ofChromatography, 28(12): 1158-1161[/font][font=宋体]李仁勇,梁立娜,李静[/font][font='Times New Roman',serif]. [/font][font=宋体]色谱[/font][font='Times New Roman',serif], 2010, 28 (12): 1158-1161[/font][font='Times New Roman',serif][17] [/font][font='Times New Roman',serif]Jaszczak E,Koziol K, Kielbratowska B, et al. J Chromatogr B, 2019, 1110-1111: 36-42[/font][font='Times New Roman',serif][18] [/font][font='Times New Roman',serif] Liu X L, Wang J, Materials Protection, 2001,34(3): 1-3[/font][font=宋体]刘秀玲,王佳[/font][font='Times New Roman',serif]. [/font][font=宋体]材料保护[/font][font='Times New Roman',serif], 2001, 34(3): 1-3[/font][font='Times New Roman',serif][19] [/font][font='Times New Roman',serif]Jaszczak E,Narkowicz S, Namiesik J, et al. Monatsh Chem, 2017, 148(9): 1645-1649[/font][font='Times New Roman',serif][20] [/font][font='Times New Roman',serif] Caterina G, Silvano C, Alfredo G, et al. JChromatogr A, 2004, 1023(1): 105-112[/font][font='Times New Roman',serif][21] [/font][font='Times New Roman',serif] Inoue A, Earley R L, Lehmann M W, et al.Talanta, 1998, 46(6): 1507-1540[/font][font='Times New Roman',serif][22] [/font][font='Times New Roman',serif] Liang L, Cai Y, Mou S, et al. J Chromatogr A,2005, 1085(1): 37-41[/font][font='Times New Roman',serif][23] [/font][font='Times New Roman',serif]Hafer E,Holzgrabe U, Kraus K, et al. Magn Reson Chem, 2020, 58(7): 653-655[/font][font='Times New Roman',serif][24] [/font][font='Times New Roman',serif] Wang Y Z, Yu T X, Xing Y, Chemistry andAdhesion, 2011, 33(3): 77-79[/font][font=宋体]王玉芝,于天霞,邢宇[/font][font='Times New Roman',serif]. [/font][font=宋体]化学与黏合[/font][font='Times New Roman',serif], 2011, 33(3): 77-79[/font][font='Times New Roman',serif][25] [/font][font='Times New Roman',serif]Ni T,[/font][font=宋体][[/font][font='Times New Roman',serif]MSDissertation[/font][font=宋体]][/font][font='Times New Roman',serif]East China University of Science and Technology, 2023[/font][font=宋体]倪彤[/font][font='Times New Roman',serif].[/font][font=宋体][硕士学位论文][/font][font='Times New Roman',serif]. [/font][font=宋体]上海[/font][font='Times New Roman',serif]: [/font][font=宋体]华东理工大学[/font][font='Times New Roman',serif], 2023[/font][font='Times New Roman',serif][26] [/font][font='Times New Roman',serif]Murei A,Kamika I, Samie A, et al. Sci Rep, 2023, 13(1): 6250[/font][font='Times New Roman',serif][27] GBZ2.1-2019 Occupational exposure limits for hazardous agents in the workplace[/font][font=宋体]—[/font][font='Times New Roman',serif]Part 1: Chemical hazardous agents[/font][font='Times New Roman',serif]GBZ 2.1-2019 [/font][font=宋体]工作场所有害因素职业接触限值[/font][font=宋体]第[/font][font='Times New Roman',serif]1[/font][font=宋体]部分:化学有害因素[/font][font='Times New Roman',serif] [/font][font='Times New Roman',serif] [/font][/s][/s][/s][/s]
硫化物什么情况下需要吹气? 如果不需要吹气取样量为多少?方法按照国家地表水环境质量监测网作业指导书
[align=center][b]针对《GB5009.34-2016食品中二氧化硫的测定》方法的优化与总结[/b][/align]《GB5009.34-2016》中指出:对于样品的检测,碘标准滴定溶液的浓度为0.1000mol/L。但是由于标准滴定溶液浓度较大,在实际检测过程中,对于未检出二氧化硫的样品或实测值非常小的样品,滴定体积稍有差别,最终得到的双平行的数据的精密度便不符合国标中的要求。同时国标中规定用蒸馏烧瓶来蒸馏样品,蒸馏时间至少为15分钟才只能得到国标中的蒸馏题及。在实际检测过程中,这种方法不仅费时费力,还耗费水资源。所以针对本方法本人将实验过程进行了优化与改进,具体改动如下:1. 将样品的蒸馏过程由传统玻璃烧瓶改进为半自动凯氏定氮仪的蒸馏过程,,蒸馏7分钟即可得到国标中的蒸馏液,此方法不仅节约时间,还减少了水资源的浪费,通过人员比对证实,经过玻璃蒸馏烧瓶蒸馏过的样品的检测值与经半自动凯氏定氮仪蒸馏过的样品的检测值基本一致。2. 将滴定样品的碘标准滴定溶液的浓度由国标中给出的0.1000mol/L稀释成0.0050mol/L,进一步增大了滴定体积,减小滴定误差,确保实验的准确性;同时对于在检出限附近及实测值非常小的样品来说,读数精确度提高,更有力的保证检测结果的真实性、准确性。为确保实验的准确性,我们进行了人员比对,并通过多次人员比对发现最终结果基本一致。总结:通过对《GB5009.34-2016食品安全国家标准食品中二氧化硫的测定》方法的优化,在检测过程中,既减少了资源的浪费,节省蒸馏时间及耗材的使用,又保证了结果的准确性,大大提高了实验效率。
买的恶臭气体标准气体,用EPA TO-15方法做硫化氢,用SIM,一点都做不出来,如果是环境空气的话,还可以解释为硫化氢气体溶于空气中的水,在前处理过程中和水被吹掉了但是标气的话,一方面硫化氢浓度很大,另一方面水含量应该很低,可是还是做不出来不知道各位有没有做过这方面实验的,小弟在这里求助一下,有没有好的经验可以分享,谢谢各位!
YS/T 239.1~7 三硫化二锑化学分析方法
我们公司接到一份单,要检测有组织废气二硫化碳的,执行标准是GB 14554-93。执行标准推荐的方法是GB/T 14680-93,但是这个分析标准使用范围是恶臭厂界空气和环境空气,不适用有组织废气。然后再看了恶臭污染物排放标准新标准的意见稿,里面推荐的方法是GB/T 14680-93和HJ 759的,HJ 759-2015使用范围是环境空气的,也没有有组织废气的。请问有组织废气的二硫化碳是没有检测标准吗
[em05] [em21] [em05] [em05] [em05] [em05] GB/T6324.3—1986有机化工产品高锰酸钾氧化时间试验方法那位老师有?给一份