欧盟建议修改杀菌剂咪唑菌酮的最大残留限量2010年10月18日,欧盟建议修改杀菌剂咪唑菌酮(fenamidone)在荷兰芹中的最大残留量限量标准,由0.02 mg/kg(定量限)修改为2mg/kg。
美国环保署于7月24日发布通告,规定咪唑菌酮的许可限量。 规定以下作物内表咪唑菌酮残留许可限量为: l 芫荽叶: 60ppm l 黄秋葵: 3.5ppm l 绿萝卜: 55ppm及根茎蔬菜(甜菜除外), 亚洲组1B(胡萝卜除外):0.15ppm 制定葡萄内/表咪唑菌酮残留地区注册许可限量为1.0ppm 制定以下作物内/表咪唑菌酮及其代谢产物RPA 717879的混合残留限量: l田玉米草料:0.25ppm l 田玉米谷:0.02ppm l 田玉米秣草:0.40ppm l 甜玉米草料:0.15ppm l 带穗轴去皮甜玉米:0.02ppm l 甜玉米秣草:0.20ppm l 大豆草料:0.15ppm l 大豆干草:0.25ppm及大豆种:0.02ppm. 由于红萝卜(除甜菜外),亚组1B(除萝卜外)残留将包括在根茎植物新定许可限量内,因此取消红萝卜现定长久及时限许可限量。
近年来乳制品的质量安全问题时有发生,给消费者的生命安全和财产安全带来巨大损害。默克密理博作为色谱领域的鼻祖,一直在为广大消费者的食品安全分析检测贡献自己的一份力量。默克密理博的应用团队也不断为客户开发出安全可靠的分析检测方法。该贴将给大家分享牛奶中左旋咪唑残留量的测定方法。
求助1-乙酰基咪唑残留量的检测方法
最近要开展测烤鳗中甲苯咪唑残留的检测,请问有国标法或是SN法吗?我的Email:capinter@163.com,谁手头有能发一份给我吗?,先谢过了~~~
2013年10月16日,农业部网站发布消息称,《牛奶中左旋咪唑残留量的测定 高效液相色谱法》等29项标准业经食品安全国家标准审评委员会审定通过。并经农业部、卫生和计划生育委员会审查批准,发布为中华人民共和国食品安全国家标准,自2014年1月1日起实施。 迪马科技在国标基础上对牛奶中左旋咪唑残留量的测定方法进行了优化,取得了优异的回收率结果和重现性,下面为详细解决方案,与大家分享
NYT 1680-2009 蔬菜水果中多菌灵等4中苯并咪唑类农药残留量的测定 高效液相色谱法[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=174279]NYT 1680-2009 蔬菜水果中多菌灵等4中苯并咪唑类农药残留量的测定 高效液相色谱法.pdf[/url]
资料分享!!![img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=17973]甲苯咪唑有机溶剂残留的液固顶空毛细管[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定[/url]
1.分析目标化合物 恶唑菌酮 2、仪器设备 带紫外分光光度检测器的高效液相色谱仪(HPLC(UV)) 液相色谱--质谱仪(LC/MS) 3、试剂 丙酮 氯化钠溶液 正己烷 无水硫酸钠 乙腈:高效液相色谱用 甲醇:高效液相色谱用 恶唑菌酮标准品:含恶唑菌酮98%以上,熔点为140℃~143℃。 4.试验溶液的制备 1) 提取方法 豆类:称取10.0g样品,加入20mL水,放置2小时。 水果和蔬菜:称取20.0g样品。 加入100mL丙酮,均质后,抽滤。滤纸上的残留物中加入50mL丙酮,均质后,按上述同样操作,合并所得的滤液。40℃以下浓缩至约30mL。浓缩液中加入100mL 10%氯化钠溶液,分别用100mL和50mL正己烷振荡提取两次。提取液中加入无水硫酸钠脱水,滤去无水硫酸钠后,滤液在40℃以下浓缩,除去溶剂。残留物中加入5mL乙醚:正己烷(1:19)混合溶液溶解。 2)净化方法 ①硅胶柱色谱法 在硅胶小柱(690mg)中注入5mL正已烷,舍弃流出液,注入1)所得到的溶液,舍弃流出液。注入10mL乙醚:正己烷(1:19)混合溶液,舍弃流出液。再注入20mL乙醚:正己烷(3:7)混合溶液,溶出液40℃以下浓缩,除去溶剂。残留物中加入2mL丙酮:正己烷(1:19)混合溶液溶解。 ②酰胺丙基甲硅烷基化硅胶柱色谱法 在酰胺丙基甲硅烷基化硅胶小柱(500 mg) 中依次注入5mL丙酮:正已烷(1:19)混合溶液和5mL正已烷,舍弃各流出液。注入①所得的溶液,舍弃流出液。再注入8mL丙酮:正已烷(1:19)混合溶液,舍弃流出液。再注入20mL丙酮:正已烷(1:9)混合溶液,流出液40℃以下浓缩,除去溶剂。残留物中2.5mL甲醇溶解后,再加入2.5mL水。 ③ 十八烷基甲硅烷基化硅胶柱色谱法 在十八烷基甲硅烷基化硅胶小柱((500 mg ) 中依次注入5mL甲醇和5mL水,舍弃各流出液。注入②所得的溶液,舍弃流出液。再注入15 mL水:甲醇(1:1)混合溶液,舍弃流出液。再注入8mL乙腈:水(7:3)混合溶液,溶出液在45℃以下浓缩,除去溶剂。残留物溶解在乙腈:水(1:1)混合溶液中,准确至2mL(豆类为1 mL)作为试验溶液。
资料共享[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=17368]甲苯咪唑有机溶剂残留的液固顶空毛细管[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定[/url]
NY/T 1649-2008 水果、蔬菜中噻苯咪唑残留量的测定 高效液相色谱法
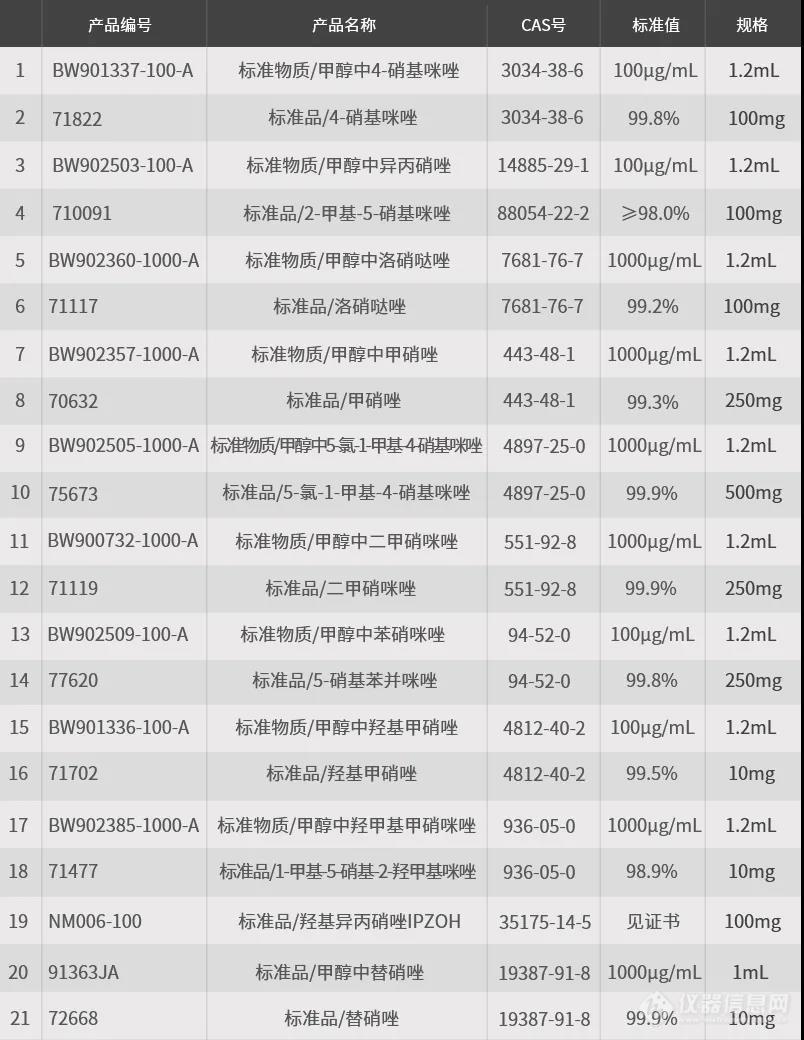
[b][font=宋体]硝基咪唑的危害及检测目的[/font][/b][font=Calibri][font=宋体]硝基咪唑类药物[/font][/font][font=宋体]([/font][font='Times New Roman']nitroimidazole,NMZs[/font][font=宋体])[/font][font=Calibri][font=宋体]是一类具有抗原虫感染和抗厌氧菌的硝基杂环类抗菌药物[/font][/font][font=宋体],[/font][font=Calibri][font=宋体]其具有抗菌和抗原虫作用[/font][/font][font=宋体]。[/font][font=Calibri][font=宋体]近年来作为饲料添加剂广泛应用于畜牧业生产中[/font][/font][font=宋体],[/font][font=Calibri][font=宋体]同时也是一种生长促进剂[/font][/font][font=宋体],[/font][font=Calibri][font=宋体]以促进畜禽的生长及改善饲料[/font][/font][font=宋体]的[/font][font=Calibri][font=宋体]转换率[/font][/font][font=宋体]。[/font][font=Calibri][font=宋体]由于这类化合物含有的硝基杂环类[/font][/font][font=宋体]物质[/font][font=Calibri][font=宋体]具有潜在致癌、致畸和致突变作用[/font][/font][font=宋体],[/font][font=Calibri][font=宋体]因此欧美等发达国家已禁止在食源性动物中使用硝基咪唑类药物[/font][/font][font=宋体]。[/font][font=Calibri][font=宋体]我国也对硝基咪唑类药物进行了严格的限制[/font][/font][font=宋体],[/font][font='Times New Roman']2020[/font][font=宋体]年[/font][font=Calibri][font=宋体]生效实施的[/font][/font][font='Times New Roman']GB 31650-2019[/font][font=Calibri][font=宋体]《食品安全国家标准[/font][/font][font=宋体] [/font][font=Calibri][font=宋体]食品中兽药最大残留限量》中仅规定了甲硝唑和地美硝唑[/font][/font][font=宋体]两[/font][font=Calibri][font=宋体]种物质允许作治疗[/font][/font][font=宋体]使[/font][font=Calibri][font=宋体]用[/font][/font][font=宋体],[/font][font=Calibri][font=宋体]但不得在动物性食品中检出[/font][/font][font=宋体];同年[/font][font=Calibri][font=宋体]农业[/font][/font][font=宋体]农村[/font][font=Calibri][font=宋体]部[/font][/font][font=宋体]公告第[/font][font=宋体]250[/font][font=宋体]号,[/font][font=Calibri][font=宋体]将[/font][/font][font=宋体]洛硝达唑、替硝唑[/font][font=Calibri][font=宋体]列入《食品动物中禁止使用的药品及其他化合物清单》中[/font][/font][font=宋体]。[/font][font=宋体]本文阐述了如何将[/font][font=宋体]硝基咪唑类化合物[/font][font=宋体]从样品基质中分离提取出来,并经过净化后,转化成[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用仪[/color][/url]可以检测的形式。以提取、净化为重点,依据国标[/font][font=宋体]GB/T 21318-2007[/font][font=宋体],为检测人员和相关领域研究人员提供一定的参考。[/font][b][font=宋体]检测项目:[/font][/b][font=宋体]硝基咪唑类原药及代谢产物[/font][b][font=宋体]应用范围:[/font][/b][font=宋体][font=宋体]猪肉[/font]/[font=宋体]鸡肉[/font][font=Calibri]/[/font][font=宋体]牛肉[/font][font=Calibri]/[/font][font=宋体]猪肝[/font][font=Calibri]/[/font][font=宋体]鸡肝[/font][font=Calibri]/[/font][font=宋体]牛肝[/font][font=Calibri]/[/font][font=宋体]猪肾[/font][font=Calibri]/[/font][font=宋体]牛肾[/font][font=Calibri]/[/font][font=宋体]鱼肉[/font][font=Calibri]/[/font][font=宋体]奶粉[/font][font=Calibri]/[/font][font=宋体]蜂蜜[/font][/font][b][b][font=宋体][font=宋体]液相色谱[/font]-质谱/质谱法[/font][font=宋体]方法原理:[/font][/b][font=宋体]样品中残留的[/font][font=宋体]8[/font][font=宋体]种硝基咪唑、[/font][font=宋体]2[/font][font=宋体][font=宋体]种代谢物用甲醇[/font]-[font=宋体]丙酮均质或超声波提取,经乙酸乙酯液液分配,以凝胶色谱([/font][/font][font=宋体]GPC[/font][font=宋体])净化,再经固相萃取([/font][font=宋体]SPE[/font][font=宋体][font=宋体])净化,采用液相色谱[/font]/[font=宋体]串联质谱确证,外标法定量测定。[/font][/font][font=宋体]前处理仪器:[/font][/b][font=宋体]凝胶色谱仪(配有馏份收集浓缩器);组织捣碎机;均质器;超声波发生器;旋转蒸发器;高速[/font][font=宋体]离心机;[/font][font=宋体]氮吹仪;固相萃取装置;具塞锥形瓶([/font][font='Times New Roman']250 mL[/font][font=宋体]);分液漏斗([/font][font='Times New Roman']250 mL[/font][font=宋体]);浓缩瓶([/font][font='Times New Roman']50 mL[/font][font=宋体]、[/font][font='Times New Roman']250 mL[/font][font=宋体])。[/font][b][font=宋体]检测仪器:[/font][font='Times New Roman'][url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS+ESI[/font][font=宋体]源[/font][font=Calibri] [/font][font=Calibri] [/font][font=Calibri] [/font][font=宋体]前处理方法[/font][font='Times New Roman']1.[/font][font=宋体]提取[/font][font=宋体]肌肉组织、脏器组织样品及水产品[/font][/b][font=宋体]准确称取约[/font][font=宋体]20 g[font=宋体]样品(精确至[/font][font=Times New Roman]0.1 g[/font][font=宋体])[/font][/font][font=宋体]于[/font][font='Times New Roman']250 mL[/font][font=宋体]具塞锥形瓶中,加入[/font][font=宋体]10 g[font=宋体]硅藻土([/font][font=Times New Roman]80[/font][font=宋体]目[/font][/font][font=宋体]~[/font][font=宋体]120[font=宋体]目)与样品充分混匀,再依次加入[/font][/font][font=宋体]5 mL[font=宋体]饱和氯化钠水溶液和[/font][font=Times New Roman]70 mL[/font][font=宋体]甲醇[/font][font=Times New Roman]-[/font][font=宋体]丙酮([/font][font=Times New Roman]3+1[/font][font=宋体]),高速均质提取[/font][font=Times New Roman]3 min[/font][font=宋体]。将提取液移入离心管中,于[/font][/font][font=宋体]10000 r/min[/font][font=宋体]离心[/font][font=宋体]2[/font][font=宋体] min[font=宋体],将上层[/font][/font][font=宋体]提取液移入[/font][font='Times New Roman']250 mL[/font][font=宋体][font=宋体]浓缩瓶中。残渣每次再用[/font]50 mL[font=宋体]甲醇[/font][font=Times New Roman]-[/font][font=宋体]丙酮([/font][font=Times New Roman]3+1[/font][font=宋体])重复提取两次,合并提取液。[/font][/font][b][font=Calibri] [/font][font=宋体]蜂蜜、乳及乳制品样品[/font][/b][font=宋体]准确称取约[/font][font=宋体]20 g[font=宋体]样品(精确至[/font][font=Times New Roman]0.1 g[/font][font=宋体])[/font][/font][font=宋体]于[/font][font='Times New Roman']250 mL[/font][font=宋体]具塞锥形瓶中,[/font][font=宋体]加入[/font][font=宋体]10 mL[font=宋体]饱和氯化钠水溶液和[/font][font=Times New Roman]70 mL[/font][font=宋体]甲醇[/font][font=Times New Roman]-[/font][font=宋体]丙酮([/font][font=Times New Roman]3+1[/font][font=宋体]),超声波提取[/font][font=Times New Roman]30 min[/font][font=宋体]。移入离心管中,于[/font][/font][font=宋体]10000 r/min[/font][font=宋体]离心[/font][font=宋体]2[/font][font=宋体] min[font=宋体],将上层[/font][/font][font=宋体]提取液移入[/font][font='Times New Roman']250 mL[/font][font=宋体][font=宋体]浓缩瓶中。残渣每次再用[/font]50 mL[font=宋体]甲醇[/font][font=Times New Roman]-[/font][font=宋体]丙酮([/font][font=Times New Roman]3+1[/font][font=宋体])重复提取两次,合并提取液。[/font][/font][b][font='Times New Roman'] [/font][font=宋体]2.[font=宋体]液液分配[/font][/font][/b][font=宋体]将提取液于[/font][font=宋体]40[/font][font=宋体] ℃水浴中旋转浓缩至只剩水相,并转移至[/font][font='Times New Roman']250 mL[/font][font=宋体][font=宋体]分液漏斗中,加入[/font]50 mL[font=宋体]饱和氯化钠水溶液和[/font][/font][font='Times New Roman']25 mL[/font][font=宋体][font=宋体]乙酸乙酯,振摇[/font]3 min[font=宋体],静置分层,收集乙酸乙酯相。水相再用[/font][/font][font=宋体]20 mL[font=宋体]乙酸乙酯重复提取两次,合并乙酸乙酯相。经无水硫酸钠柱脱水,收集于[/font][/font][font='Times New Roman']250 mL[/font][font=宋体]浓缩瓶中,[/font][font=宋体]于[/font][font=宋体]40[/font][font=宋体] ℃水浴中旋转浓缩至近干,加入[/font][font='Times New Roman']5 mL[/font][font=宋体][font=宋体]乙酸乙酯[/font]-[font=宋体]环己烷([/font][font=Times New Roman]1+1[/font][font=宋体])溶解残渣,并用[/font][font=Times New Roman]0.45 [/font][/font][font='Times New Roman']μm[/font][font=宋体]滤膜过滤,待净化。[/font][b][font='Times New Roman'] [/font][font=宋体]3[/font][font='Times New Roman'].[/font][font=宋体]净化[/font][font=宋体]凝胶色谱([/font][font='Times New Roman']GPC[/font][font=宋体])净化[/font][font=宋体]凝胶色谱净化条件如下:[/font][/b][font=宋体][font=宋体]净化柱:[/font]700 mm[font=宋体]×[/font][font=Times New Roman]25 mm[/font][font=宋体],[/font][font=Times New Roman]Bio Bcads S X3[/font][font=宋体],或相当者;[/font][/font][font=宋体][font=宋体]流动相:乙酸乙酯[/font]-[font=宋体]环己烷([/font][font=Times New Roman]1+1[/font][font=宋体]);[/font][/font][font=宋体][font=宋体]流速:[/font]4.7 mL/min[font=宋体];[/font][/font][font=宋体][font=宋体]样品定量环:[/font]5.0 mL[font=宋体];[/font][/font][font=宋体][font=宋体]预淋洗体积:[/font]50 mL[font=宋体];[/font][/font][font=宋体][font=宋体]洗脱总体积:[/font]210 mL[font=宋体];[/font][/font][font=宋体][font=宋体]开始弃去体积:[/font]90 mL[font=宋体];[/font][/font][font=宋体][font=宋体]收集体积:[/font]90 mL[font=宋体];[/font][/font][font=宋体][font=宋体]最后弃去体积:[/font]30 mL[font=宋体]。[/font][/font][b][font=宋体]凝胶色谱净化步骤如下:[/font][/b][font=宋体][font=宋体]将[/font]5 mL[font=宋体]待净化液按照凝胶色谱净化条件进行净化,合并馏份收集器中的收集液于[/font][/font][font='Times New Roman']250 mL[/font][font=宋体]浓缩瓶中,于[/font][font='Times New Roman']4[/font][font=宋体]0[/font][font=宋体] ℃水浴中旋转浓缩至近干,加入[/font][font=宋体]5 mL[font=宋体]甲醇以溶解残渣,待净化。[/font][/font][b][font=宋体] [/font][font=宋体]固相萃取([/font][font='Times New Roman']SPE[/font][font=宋体])净化[/font][/b][font=宋体]使用前用[/font][font=宋体]5 mL[font=宋体]甲醇预淋洗[/font][font=Times New Roman]C18[/font][font=宋体]固相萃取柱([/font][font=Times New Roman]1 g[/font][font=宋体],[/font][font=Times New Roman]6 mL[/font][font=宋体]),将[/font][font=Times New Roman]5 mL[/font][font=宋体]溶解液倾入[/font][font=Times New Roman]C18[/font][font=宋体]固相萃取柱中,以[/font][font=Times New Roman]1 mL/min[/font][font=宋体]的速度收集流出液,再用[/font][font=Times New Roman]10 mL[/font][font=宋体]甲醇进行洗脱。收集全部洗脱液于[/font][font=Times New Roman]50 mL[/font][font=宋体]浓缩瓶中,于[/font][/font][font='Times New Roman']4[/font][font=宋体]0[/font][font=宋体] ℃水浴中旋转浓缩至干。用甲醇溶解并定容至[/font][font=宋体]1.0 mL[font=宋体],经[/font][font=Times New Roman]0.45 [/font][/font][font='Times New Roman']μm[/font][font=宋体]滤膜过滤后,供[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]测定和确证。[/font][b][font=宋体] [/font][font=宋体]国标解读及注意事项[/font][/b][font='Times New Roman']1.[/font][font=宋体]硝基咪唑标准物质用甲醇配成[/font][font=宋体]1000[/font][font='Times New Roman'] μg/[/font][font=宋体]mL[font=宋体]的标准[/font][/font][font=宋体]储备液,在[/font][font='Times New Roman']0[/font][font=宋体] [/font][font=宋体]~[/font][font='Times New Roman']4[/font][font=宋体] ℃条件下避光保存,可使用[/font][font='Times New Roman']12[/font][font=宋体]个月。[/font][font=宋体]2.[/font][font=宋体]如果有条件,建议凝胶色谱净化系统中配合使用紫外检测器,准确监测目标化合物及杂质的流出情况。[/font][b][font=宋体]3[/font][font='Times New Roman'].[/font][font=宋体][font=宋体]固相萃取净化过程中,[/font]C18[font=宋体]柱作为净化柱使用,注意上样过程中就需要收集流出液,再和洗脱液进行合并。[/font][/font][font=宋体]4.[/font][font=宋体]国标方法中使用基质添加标准曲线,外标法进行回收率的校正。注意做肉类样品的基质添加标准曲线前,先进行洗涤,然后加标,再进行后续提取净化等流程。[/font][font='Times New Roman']5.[/font][font=宋体]建议使用硝基咪唑标准物质相对应的同位素内标,进行回收率的校正。[/font][font=Calibri] [/font][font=Calibri] [/font][font=宋体]参考文献[/font][/b][font=宋体]GB/T 21318-2007 [/font][font=宋体]动物源食品中硝基咪唑残留量检验方法[/font][align=center][font=Calibri] [/font][/align][align=center][img=,554,]https://ng1.17img.cn/bbsfiles/images/2020/10/202010301416299459_3472_3793_3.png!w554x415.jpg[/img][font=Calibri] [/font][/align][align=center][/align][align=center][/align][font=宋体][/font][align=center][font=宋体]图[/font][font=宋体]1 [/font][font=宋体]肌肉组织、脏器组织样品及水产品中硝基咪唑残留量测定的前处理流程图[/font][/align][align=center][/align][align=center][/align][align=center][img=,554,]https://ng1.17img.cn/bbsfiles/images/2020/10/202010301416169976_4411_3793_3.png!w554x415.jpg[/img][/align][font=宋体][/font][align=center] [/align][align=center][font=宋体]图[/font][font=宋体]2 [/font][font=宋体]蜂蜜、乳及乳制品样品中硝基咪唑残留量测定的前处理流程图[/font][/align][font=宋体][/font][font=宋体][/font][align=center][b][font='Times New Roman'][font=宋体]表[/font][/font][font='Times New Roman']1 [/font][font='Times New Roman'][font=宋体]硝基咪唑标准物质信息表[/font][/font][/b][/align][align=center][font=宋体][img=,690,]https://ng1.17img.cn/bbsfiles/images/2020/10/202010301416445861_6609_3793_3.jpg!w690x892.jpg[/img][/font][/align]
最近在做水果蔬菜中多菌灵等4种苯并咪唑类农药残留,完全按照标准做下来的,走标样出峰情况还不错,但是我做的3个添加样怎么走也不出峰,流动相流速、比例我都换试了,可是添加样还是不出峰
杀菌剂多残留分析方法 检测农产品中农药残留量是评价其是否超过MRL值的前提,因此农药残留分析方法得到各国的重视。无论是多残留分析(MRMs)还是单残留分析(SRMs),均基于相似的检测步骤,多残留分析由于可同时检测多种农药残留的存在,因此通常是首选方法。公职分析化学家协会(AOAC)的方法是国际公认的多残留分析方法,可用于多种农药残留的检测。该方法通常用水溶性的溶剂提取,紧接着的净化用不溶于水的溶剂进行分配,再用硅胶或弗罗里硅土净化,净化后的提取物用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]、高效液相色谱检测。尽管AOAC方法可以检测多达325种农药及相关化合物,但也存在一些不足之处,如效率低,不适于进行筛选分析;有些试剂有毒且用量大;不能分析一些新农药等。针对上述缺陷,一些新的提取、净化方法得到重视和发展,如固相萃取(solid-phase extraction,SPE)、固相净化(solid-phase cleanup,SPC)、基质固相分散萃取(matrix solid-phase dispersion,MSPD)、超临界流体萃取(supercritical fluid extraction,SFE)等。这些技术的突出特点是简便、样量小型化、萃取的广泛性。检测技术上,[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]及高效液相色谱仍然是主要的技术手段。[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]方面,采用微波诱导等离子(microwave induced plasma,MIP)-原子发射检测器(atomic emission detector,AED)及多级质谱的检测技术取得了快速的发展;离子及离子对色谱以及柱后衍生技术的应用是高效液相色谱检测的研究热点,激光诱导荧光检测器也已开始应用。超临界流体色谱(Supercritical fluid chromatography, SFC)在农药残留检测中的成功应用,实现了样品中农药残留的提取、净化、检测一步完成,是当前联用技术的典型代表。2.1 提取从样品中提取残留农药的效果,很大程度上决定于农药的极性及样品基质的类型。提取过程通常将样品置于匀浆瓶中,添加溶剂,利用匀浆器(homogeniser)、搅拌机(blender)或超声波发生器(sonicator)匀浆。常用的有机溶剂有丙酮、乙腈、甲醇、乙酸乙脂等,根据样品类型、含水量及目标农药,有时需要添加适量的水或调整pH值。多数情况下样品能均匀的分散在有机溶剂中,从而可提高被测残留物的回收率,减少共提的干扰物比率。经均化作用后,以过滤或离心的方法将溶剂和固体分开。2.1.1乙腈提取法乙腈提取法可应用于大多数农药和其它一些化合物的提取,然而在该方法中,许多水溶性(极性)化合物在石油醚从乙腈水中提取农药以及在弗罗里硅土柱层析或氧化镁/硅藻土柱进行层析净化时,水溶性化合物或部分或全部损失。尽管如此这种提取方法仍适用于许多杀菌剂的分析。在Liao等人的方法中采用乙腈进行提取,通过添加氯化钠使乙腈与水分离,上层部分(乙腈)浓缩至小体积后用[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用仪[/color][/url]检测。AOAC早期的方法及美国加州食品和农业部 (California Department of Food and Agriculture,CDFA)的MRSM (Multiresidue Screen Method) 方法多采用乙腈作为溶剂。2.1.2丙酮提取法由于丙酮具有无毒、易于纯化、与乙腈和其它一些溶剂相比挥发性好而且价格低廉等优点,因此也是一种常用的提取溶剂,许多方法采用它。此外,在样品中含糖时,丙酮不会象乙腈那样与水形成两相,故可用于高含糖量的样品。实验表明,丙酮具有广泛的化合物和样品基质适用性,已有的回收率数据包括400余种化合物,其中含杀菌剂40余种。理论上,丙酮可用于提取任何样品中除了带有永久离子之外的残留农药。因此,许多国家农药残留标准方法均采用丙酮作为主要溶剂,如德国的DFG S19方法,美国FDA MRMs方法等。在这些方法中,丙酮提取液用氯化钠或硫酸钠饱和之后,分配至二氯甲烷、己烷或石油醚中,从而可得到对不同化合物有利的分配特性和有机相的快速分离。2.1.3乙酸乙酯提取法乙酸乙酯极性相对丙酮、乙腈要弱,因此其对弱极性农药的提取回收率一般较好些,并且其共提物尤其是色素要显著少于丙酮,从而减少了净化时的压力。采用乙酸乙酯作提取溶剂的方法最早由Ross等提出,提取液采用凝胶渗透层析(GPC)净化(SX-3柱),杀菌剂的回收率超过90%。1989年,瑞典国家食品管理局将其列为国家多残留分析方法,替代了原来由Anderson和Ohlin建议的方法。现在该方法已能检测约160种农药、异构体及降解代谢产物。在荷兰的国家方法中,乙酸乙酯也作为主要的提取溶剂。由于省去净化步骤,乙酸乙酯提取方法也被称为在线提取法(on-line extraction methods),其理论基础是Gibbs三角,可用于在线提取的有机溶剂对还有正己烷/丙酮(8∶2)、乙酸乙酯/二甲苯、丙酮或乙腈/二氯甲烷或石油醚等。2.1.4其它提取方法固相萃取是近年发展较快的一种提取、净化方法,作为一种提取技术,主要应用于液体样品中农药的提取,用于农产品及土壤等固体或半固体样品中农药的提取,实质上是一种净化、富集过程。商品化的固相萃取装置很多,主要是固相萃取小柱、固相萃取盘等,其发展主要体现在填料方面,如石墨化炭黑、键合硅胶、弗罗里硅土、活性炭、硅胶等。基质固相分散萃取是类似于固相萃取的一种提取、净化、富集技术,其是将吸附剂或填料与样品一起研磨分散,然后装柱,用有机溶剂淋洗,使农药淋洗出来,淋洗液一般无需进一步净化,可直接进[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]或高效液相色谱检测。MSPD实际上将包括样品匀浆、细胞裂解、完全提取、分馏及纯化过程集于一个简单的过程。有些淋出杂质较多的样品,也可进行净化、分析。Kadenski等采用MSPD技术,研究了多种农药在一些蔬菜、水果中的回收。与传统方法相比,MSPD具有显著的优点,主要表现在,缩短了样品分析周期;减少了样品量,从而极大的降低了溶剂的用量,降低了环境污染的可能性并提高了操作安全性;适用于自动化操作等。
[size=1][size=3][font=Arial]SPE-HPLC[/font][/size][size=3][font=宋体]法测定土壤中咪唑乙烟酸的残留量[/font][/size][/size][size=1][font=宋体]摘要:建立了[/font][font=Times New Roman]SPE[/font][font=宋体]净化和[/font][font=Times New Roman]HPLC[/font][font=宋体]法测定土壤中常用除草剂咪唑乙烟酸的残留。土壤样品用[/font][font=Times New Roman]0.1 mol/L[/font][font=宋体]的醋酸铵与氨水缓冲液[/font][font=Times New Roman](pH 10)[/font][font=宋体]超声波提取,提取液经酸化后用[/font][font=Times New Roman]200 mg/3mL C18 SPE[/font][font=宋体]柱净化,浓缩,乙腈定容后,供反相高效液相色谱检测,外标法定量。[/font][font=Times New Roman] [/font][font=宋体]添加回收率为[/font][font=Times New Roman]77.2%~94.9%[/font][font=宋体],咪唑乙烟酸的最小检出量为[/font][font=Times New Roman]5.2×10[/font][font=宋体]-[/font][font=Times New Roman]5 mg[/font][font=宋体],经计算可知,咪唑乙烟酸在土壤中的最小检出质量分数为[/font][font=Times New Roman]0.2 mg/kg[/font][font=宋体]。[/font][font=Times New Roman] [/font][font=宋体]该方法大大减少了有机溶剂的使用,方便快速,结果准确可靠,适合一般实验室操作。[/font][/size][size=3][font=宋体][size=1]关键词:咪唑乙烟酸;固相萃取;高效液相色谱;土壤[/size][/font][/size]
分享一个检测标准,GB29681-2013 《食品安全国家标准 牛奶中左旋咪唑残留量的测定 高效液相色谱法》 。本标准适用于牛奶中左旋咪唑残留量检测,检测限为2.5μg/kg,定量限为5μg/kg。
GBT 20744-2006 蜂蜜中甲硝唑、洛硝哒唑、二甲硝咪唑残留量的测定 液相色谱-串联质谱法
SN/T 1623-2005 进出口卫生筷中噻苯咪唑、邻苯基苯酚、联苯和抑霉唑残留量的检验方法 液相色谱法2005-08-18发布,2006-02-01实施,现行有效。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=133655]SN/T 1623-2005 进出口卫生筷中噻苯咪唑、邻苯基苯酚、联苯和抑霉唑残留量的检验方法 液相色谱法[/url]
【关键词】国家标准物质 中华标准物质中 标物中心 国家标准物质网站 内容摘要:用丙酮从样品中提取恶唑菌酮,转溶到正己烷后,用硅胶小柱、酰胺丙基甲硅烷基化硅胶小柱和十八烷基甲硅烷基化硅胶小柱净化,HPLC(UV)测定、LC/MS确证。 1.分析目标化合物 恶唑菌酮 2、仪器设备 带紫外分光光度检测器的高效液相色谱仪(HPLC(UV)) 液相色谱--质谱仪(LC/MS) 3、试剂 丙酮 氯化钠溶液 正己烷 无水硫酸钠 乙腈:高效液相色谱用 甲醇:高效液相色谱用 恶唑菌酮标准品:含恶唑菌酮98%以上,熔点为140℃~143℃。 4.试验溶液的制备 1) 提取方法 豆类:称取10.0g样品,加入20mL水,放置2小时。 水果和蔬菜:称取20.0g样品。 加入100mL丙酮,均质后,抽滤。滤纸上的残留物中加入50mL丙酮,均质后,按上述同样操作,合并所得的滤液。40℃以下浓缩至约30mL。浓缩液中加入100mL 10%氯化钠溶液,分别用100mL和50mL正己烷振荡提取两次。提取液中加入无水硫酸钠脱水,滤去无水硫酸钠后,滤液在40℃以下浓缩,除去溶剂。残留物中加入5mL乙醚:正己烷(1:19)混合溶液溶解。 2)净化方法 ①硅胶柱色谱法 在硅胶小柱(690mg)中注入5mL正已烷,舍弃流出液,注入1)所得到的溶液,舍弃流出液。注入10mL乙醚:正己烷(1:19)混合溶液,舍弃流出液。再注入20mL乙醚:正己烷(3:7)混合溶液,溶出液40℃以下浓缩,除去溶剂。残留物中加入2mL丙酮:正己烷(1:19)混合溶液溶解。 ②酰胺丙基甲硅烷基化硅胶柱色谱法 在酰胺丙基甲硅烷基化硅胶小柱(500 mg) 中依次注入5mL丙酮:正已烷(1:19)混合溶液和5mL正已烷,舍弃各流出液。注入①所得的溶液,舍弃流出液。再注入8mL丙酮:正已烷(1:19)混合溶液,舍弃流出液。再注入20mL丙酮:正已烷(1:9)混合溶液,流出液40℃以下浓缩,除去溶剂。残留物中2.5mL甲醇溶解后,再加入 2.5mL水。 ③ 十八烷基甲硅烷基化硅胶柱色谱法 在十八烷基甲硅烷基化硅胶小柱((500 mg ) 中依次注入5mL甲醇和5mL水,舍弃各流出液。注入②所得的溶液,舍弃流出液。再注入15 mL水:甲醇(1:1)混合溶液,舍弃流出液。再注入8mL乙腈:水(7:3)混合溶液,溶出液在45℃以下浓缩,除去溶剂。残留物溶解在乙腈:水(1:1)混合溶液中,准确至2mL(豆类为1 mL)作为试验溶液。 5.标准曲线的制作 用乙腈:水(1:1)混合溶液将恶唑菌酮标准品配制成0.1~2 mg/L的溶液数点,分别注入50 μL于HPLC中,用峰高法或面积法绘制成标准曲线。 6.定量试验 注入50μL试验溶液于HPLC中,根据5的标准曲线求出恶唑菌酮的含量。 7.测定条件 HPLC 检测器:UV(波长230 nm) 柱:十八烷基甲硅烷基化硅胶(粒径5μm),内径4.6 mm、长150 mm 柱温:40℃ 流动相:乙腈:水(1:1)混合溶液。 保留时间标准:约16~17 分钟 8.定量限 0.01 mg/kg。 9.注意事项 1)检测方法概述 本方法用丙酮从样品中提取恶唑菌酮,转溶到正己烷后,用硅胶小柱、酰胺丙基甲硅烷基化硅胶小柱和十八烷基甲硅烷基化硅胶小柱净化,HPLC(UV)测定、LC/MS确证。。 2)注意点 ①要注意酰胺丙基甲硅烷基化硅胶小柱因制造厂商不同存在性能差异。用标准品进行预先溶出试验。 ②来自酰胺丙基甲硅烷基化硅胶小柱的溶出液的浓缩残留物,溶解在甲醇后,加入水。如直接加入水:甲醇(1:1)混合溶液,会出现残留物凝 固在玻璃表面不溶解的情况。
做克菌丹的残留检测分析需要用惰性衬管吗?
加拿大制定多项农药最高残留限量标准 加拿大近日发出G/SPS/N/CAN/362、364、365、368、369、370/Add.1号多项通报,对农药咪唑菌酮、稀禾定、甲霜灵、吡虫啉、氟酮磺隆以及赛座灭分别制定了最高残留限量。 上述法规均已生效。来源于:中国化工信息网
1.国产咪唑苯脲二丙酸盐在牛体内的药代动力学及组织残留沈春岚 吴弋麃 宋鲁敏 张金子 戴国华 【摘要】:给牛单剂量肌注咪唑苯脲二丙酸盐(2mg/kg)。用紫外分光光度计测出不同时间的血药浓度,并按有吸收一室模型=M(e~(-ket)—e~(-kat))公式,计算出咪唑苯脲的主要药代动力学参数:吸收速率常数(k_a)为2.027h~(-1) 清除速率常数(k_e)为0.419h~(-1),峰时间(T~(max))为1.18h 峰浓度(C~(max))为1.746μg/ml 吸收相半衰期(t1/2k_a)为0.342h,消除相半衰期(t1/2k_e)为1.165h 表观分布容积(Vd)为0.88L/kg 体清除率(BIC)为0.25L/kg/h。咪唑苯脲在牛的肝、肾、心,胆汁、脑、肌肉、脂肪中的残留【作者单位】: 兽医大学药理教研室 兽医大学药理教研室 兽医大学药理教研室 兽医大学药理教研室 兽医大学中心实验室 【关键词】: 咪唑苯脲 药代动力学 组织残留 牛 【DOI】:CNKI:SUN:ZSYX.0.1987-02-001【正文快照】: 咪哩苯脉(Imidocarb)具有抗巴贝斯梨形虫的作用,最早是schmidt等①在应用鼠骆氏巴贝西虫筛选一组均二苯脉类化合物时发现的,同年Beveridge②进一步证实了该药的LD:。低于其它通用的抗巴贝斯梨形虫药。随后,该药广泛用于世界各国,并证实其对各种巴贝斯梨形虫和无定形体(边虫)http://www.cnki.com.cn/Article/CJFDTOTAL-ZSYX198702001.htm2.国产咪唑苯脲对驽巴贝西虫病治疗试验李德昌 胡力生 阎仲堂 赵权 【摘要】:应用国产抗巴贝西虫新药咪唑苯脲(Imidocarb)二盐酸盐。对3匹马分别按每kg体重2、4、8mg剂量进行了安全性试验。结果,2、4mg剂量的马,间隔24h肌肉注射2次,临床、血液、肝功、肾功均未见明显变化 8mg剂量的马,仅注射1次就出现呼吸困难、流涎、腹痛和排稀粪等反应,30min后消失。对14例自然发病的驽巴贝西虫病马,按2mg/kg的体重剂量进行了试治,其中8例间隔24h共用药2次,6例仅用药1次,结果均获痊愈,且无任何副作用。【作者单位】: 兽医大学寄生虫病教研室 兽医大学寄生虫病教研室 兽医大学寄生虫病教研室 吉林农业大学兽医系 【关键词】: 咪唑苯脲 安全试验 驽巴贝西虫病 【DOI】:CNKI:SUN:ZSYX.0.1987-02-003【正文快照】: 3.咪哩苯脉(I midocarb)的抗巴贝西虫作用,最早为schmidt等(1969)①在应用鼠骆氏巴贝西虫筛选一组均二苯脉类化合物时发现。同年,Beveridge②进一步证实了该药的半数有效量(EDS。)低于其它通用的抗巴贝西虫药。随后,该药被广泛应用于非洲、拉丁美洲、北美洲、澳大利亚、爱尔兰咪唑苯脲——一种抗巴贝西虫新药李德昌 【摘要】:正 咪唑苯脲(Imidocarb)为均二苯脲(Carbanilide)类中的联脒(diamidine)的衍生物。商品名为 Imizol。化学名称为#结构式为#本药有两种盐类,即二盐酸盐和二丙酸盐,在10%(w/v)溶液时,后者 pH为6.5,前者 pH 为3.1,并且后者具有较前者易溶于水的优点。咪唑苯脲的抗巴贝西虫的作用最早为Schmidt 等(1969)在应用鼠骆氏巴贝西虫(Babesia rodhaini)筛选一组均二苯脲类化合物时发现,同年 Beveridge(1969)3,3′—双(2-咪唑啉)均二苯脲二盐酸[3,3′-his(2—imidozoline—2—yl)—Carbanil【作者单位】: 【关键词】: 巴贝西虫病 肌肉注射 咪唑苯脲 剂量 丙酸盐 二苯脲类 皮下注射 预防作用 静脉注射 衍生物 【DOI】:CNKI:SUN:JLXS.0.1986-03-031【正文快照】: 咪哩苯脉(Imidocarb)为均二苯脉(Carbanilide)类中的联眯(diamidine)的衍生物。商品名为I,nizol。化学名称为 #结构式为#3,3‘一双(2一咪哇琳)均二苯脉二盐酸 〔3,3/一1)15(2一imidozoline一2一yl)一Carbanilide dihydroehloride〕。 /‘一\一,,,。~、… \/一二、11—七L月—4.一种抗梨形虫药物咪唑苯脲及其盐的合成研究李光壁 【摘要】:抗梨形虫药物咪唑苯脲为均二苯脲类联脒衍生物,是一种重要的具有生物活性的化合物,一般以二盐酸盐和二丙酸盐最为常见。它们具有广谱、低毒、应用范围广、作用时间长、用药剂量小等优点,对家畜梨形虫病、无浆体病及猪犬等的附红细胞体病不仅有很好的治疗作用,也具有良好的预防效果,为新一代最佳的抗梨形虫药物,并且该药也是美国药典唯一收录的允许应用于梨形虫病治疗的药物。随着梨形虫病在世界各地的广泛传播,对该类药物的需求量越来越大。面对国内外的迫切需求,探求一条新的适宜工业化生产的路线,促进兽药行业的快速发展以及满足国内外的需求都具有重要的经济效益和社会效益。 本文合成了咪唑苯脲及其二盐酸盐和二丙酸盐。咪唑苯脲又称N,N’-双[3-(4,5,-2H-1H-咪唑啉-2-基)苯基)]脲。目前,据文献报道,有五种方法可以合成咪唑苯脲,如下所述: (1)3,3’-二氰二苯脲在乙醚-氢硫酸或乙醇-盐酸体系中与乙二胺反应: (2)3,3’-甲酸酯二苯脲与乙二胺在氯化铵溶液中反应(R与R’为含碳原子较少的烷烃基团): (3)将间硝基苯甲酸乙酯在三甲基铝存在下,与乙二胺反应得到2-(3-硝基苯基)咪唑啉,然后还原制得2-(3-氨基苯基)咪唑啉,最后在醋酸钠-水溶液中与光气发生缩合反应:【关键词】:咪唑苯脲 二盐酸盐 二丙酸盐 缩合 合成 【学位授予单位】:山东大学【学位级别】:硕士【学位授予年份】:2006【分类号】:TQ463.53【DOI】:CNKI:CDMD:2.2006.164426【目录】: 摘要6-9ABSTRACT9-12符号说明12-13第一章 前言13-351.1 梨形虫病及其治疗药物概述13-221.1.1 梨形虫病的种类14-171.1.2 抗梨形虫病药物国内外研究进展17-221.2 均二苯脲类联脒衍生物的生物活性及国内外研究进展22-281.2.1 均二苯脲类联脒衍生物的生物活性及国外研究进展22-271.2.2 国内研究进展27-281.3 课题的确立及应用价值28-291.4 咪唑苯脲的合成方法29-331.5 本文研究的主要内容33-351.5.1 2-(3-氨基苯基)咪唑啉二盐酸盐及其中间体的合成33-341.5.2 咪唑苯脲及其盐的合成34-35第二章 实验部分35-392.1 实验仪器与原料35-362.1.1 基本仪器352.1.2 基本原料35-362.2 合成部分36-392.2.1 间硝基苯甲腈的合成362.2.2 2-(3-硝基苯基)咪唑啉的合成36-372.2.3 2-(3-氨基苯基)咪唑啉二盐酸盐的合成372.2.4 N,N’-二-(3-(4,5-2H-1H-咪唑-2-基)苯基)脲的合成37-382.2.5 N,N’-二-(3-(4,5-2H-1H-咪唑-2-基)苯基)脲二盐酸盐的合成382.2.6 N,N’-二-(3-(4,5-2H-1H-咪唑-2-基)苯基)脲二丙酸盐的合成38-39第三章 结果与讨论39-683.1 间硝基苯甲腈的合成39-433.1.1 原料及工艺路线的选择393.1.2 反应条件的选择39-413.1.3 重结晶溶剂的选择413.1.4 结构分析与确定41-433.2 2-(3-硝基苯基)咪唑啉的合成43-483.2.1 结果433.2.2 讨论43-453.2.3 结构分析与确定45-483.3 2-(3-氨基苯基)咪唑啉二盐酸盐的合成48-523.3.1 结果483.3.2 讨论48-503.3.3 结构分析及确认50-523.4 N,N’-二-(3-(4,5-2H-1H-咪唑-2-基)苯基)脲的合成52-593.4.1 结果52-533.4.2 讨论53-543.4.3 结构分析及确认54-593.5 N,N’-二-(3-(4,5-2H-1H-咪唑-2-基)苯基)脲二盐酸盐的合成59-623.5.1 结果593.5.2 讨论59-603.5.3 结构分析及确认60-623.6 N,N’-二-(3-(4,5-2H-1H-咪唑-2-基)苯基)脲二丙酸盐的合成62-683.6.1 结果623.6.2 讨论62-643.6.2 结构分析及确认64-68第四章 实验结论68-69参考文献69-74致谢74-75[em09502]
现本人正在用HP6890N-5973i进行牛奶中左旋咪唑残留[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]检测,请教哪位做过请提供具体方法,谢谢!包括前处理,试剂,仪器条件,检测标准方法等。请email给我:yzbjm@163.com
[size=3]1、[/size] [size=3]NY/T 1279-2007 [/size][font=宋体][size=3]蔬菜、水果中硝酸盐的测定紫外分光光度法[/size][/font][size=3]2、[/size] [size=3]NY/T 1275-2007 [/size][font=宋体][size=3]蔬菜、水果中吡虫啉残留量的测定[/size][/font][size=3]3、[/size] [size=3]NY/T 1277-2007 [/size][size=3][font=宋体]蔬菜中异菌脲残留量的测定[/font][font=Times New Roman] [/font][font=宋体]高效液相色谱法[/font][/size][size=3]4、[/size] [size=3]NY/T 1382-2007 [/size][size=3][font=宋体]棉籽中棉酚旋光体的测定[/font][font=Times New Roman] [/font][font=宋体]高效液相色谱法[/font][/size][font=Times New Roman][size=3]5、[/size] [/font][size=3][font=宋体]农业部[/font][font=Times New Roman]783[/font][font=宋体]号公告[/font][font=Times New Roman]-1-2006 [/font][font=宋体]水产品中硝基呋喃类代谢物残留量的测定液相色谱[/font][font=Times New Roman]-[/font][font=宋体]串联质谱法[/font][/size][size=3]6、[/size] [size=3]DB33/T 598-2006 [/size][size=3][font=宋体]水产品中孔雀石绿及其代谢物残留量的测定[/font][font=Times New Roman]――[/font][font=宋体]液相色谱[/font][font=Times New Roman]-[/font][font=宋体]串联质谱法[/font][/size]7、 DB33/T 616-2006 [font=宋体]配合饲料中呋喃西林和呋喃唑酮的测定[/font][font=Times New Roman] [/font][font=宋体]液相色谱法[/font]8、 DB33/T 693-2008 [font=宋体]动物源性食品中硝基咪唑类药物残留量的测定[/font][font=Times New Roman] [/font][font=宋体]高效液相色谱法[/font]9、 DB33/T 691-2008 [font=宋体]水产品中土霉素[/font][font=Times New Roman],[/font][font=宋体]四环素[/font][font=Times New Roman],[/font][font=宋体]金霉素[/font][font=Times New Roman],[/font][font=宋体]强力霉素残留量的测定[/font][font=Times New Roman] [/font][font=宋体]高效液相色谱荧光检测法[/font]10、 GB/T 21928-2008 [font=宋体]食品塑料包装材料中邻苯二甲酸酯的测定[/font]11、 GB/T 5009.122-2003 [font=宋体]食品容器、包装材料用聚氯乙烯树脂及成型品中残留量[/font][font=Times New Roman]l[/font][font=宋体],[/font][font=Times New Roman]l-[/font][font=宋体]二氯乙烷的测定[/font]12、 GB/T 5009.60-2003 [font=宋体]食品包装用聚乙烯、聚苯乙烯、聚丙烯成型品卫生标准的分析方法[/font]13、 GB/T 5009.178-2003 [font=宋体]食品包装材料中甲醛的测定[/font]以上资料已经上传至资料库。
2011年3月16日,加拿大卫生部将丙硫菌唑在甜菜根中的最大残留限量修订为0.25mg/kg;将氟啶胺在干制小豆、豌豆、蚕豆、豇豆、四季豆、鹰嘴豆、瓜尔豆、花腰豆、羽扇豆等产品中的最大残留限量标准修改为0.02mg/kg;将噻苯咪唑在白蘑菇中的最大残留限量标准修改为55 mg/kg;将异丙甲草胺在甜菜根和甜菜叶中的最大残留限量标准分别修改为0.3mg/kg和0.08 mg/kg. 内容详见:http://www.hc-sc.gc.ca/cps-spc/pubs/pest/_decisions/emrl2011-10/index-eng.php
近日,欧盟发布COMMISSION REGULATION (EU) No 270/2012,对(EC) No 396/2005 Annex IIIA中的农药残留限量做了修订,新增对氟吡菌酰胺和甲咪唑烟酸的残留限量要求,该法规已于3月28日生效。 此次列入新增农药限量的产品包括水果,新鲜或冷冻蔬菜,豆类,含油种子与果实,谷类,茶、咖啡、草药制剂和可可,啤酒花,香料,糖料,陆地动物源性产品共十大类、370余种,其中对氟吡菌酰胺的限量从0.01mg/kg~2mg/kg不等,对甲咪唑烟酸的限量均为0.01mg/kg。 氟吡菌酰胺,是世界制药巨头拜耳作物科学公司推出的一种吡啶基乙基苯甲酰胺类的广谱型杀菌剂。主要用于阔叶作物上防治子囊菌引起的病害。可用于防治70多种作物如葡萄树、鲜食葡萄、梨果、核果、蔬菜以及大田作物等的多种病害,该农药是一种新农药,欧美各国对其风险评估尚处于初级阶段,此次欧盟增加其限量要求是在收到拜耳公司申请后进行了为期一年多的评估后作出的。美国EPA农药规划处将此种农药的登记决议期从2010年的第三季度推迟到了2012年度第一季度,于2012年2月24日,公布了对此种农药的残留限量要求。 甲咪唑烟酸,又名百垄通等,是一种咪唑啉酮类新型超高效除草剂,已得到较广泛应用,其内吸性强,对单、双子叶杂草均有良好防效,不仅能很好地杀死杂草地上部分,而且对杂草地下部的根与地下茎也有较强的防除效果。现主要被应用于花生田的除草剂,对多种杂草特别是香附子有较好的杀除效果。 欧盟此次新增这两种农药残留限量要求,涉及产品种类较多,主要为食品农产品。欧盟是我国食品农产品主要贸易地区,食品农产品出口企业应对其高度重视,特别是甲咪唑烟酸,目前主要应用于花生田除草。此两种农药限量要求将会对我国出口欧盟的水果、蔬菜、粮谷、花生等产品产生较大影响。
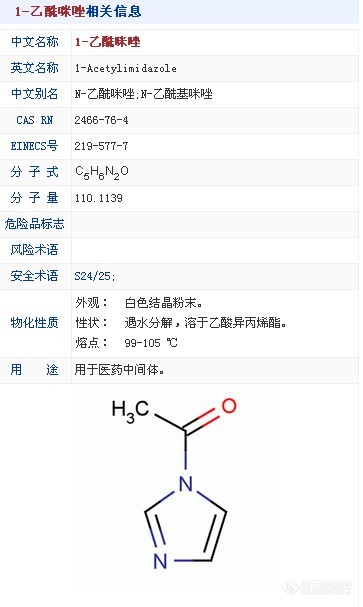
1-乙酰咪唑相关信息如图所示。水解产物是否为咪唑和乙酸?产品的体系为乙醇,水和多肽。乙酰咪唑是用来合成多肽时封闭和试剂,要求检测残留量,如果水解产物是咪唑的话,很想知道咪唑的检测方法(残留量),当然是越快速的越好。定性检测。谢谢各位!http://ng1.17img.cn/bbsfiles/images/2011/08/201108291337_312722_1665695_3.jpg
苯菌灵遇有机溶剂或水会分解成多菌灵和异氰酸丁酯,在液相分析中,也会发生柱上分离,使得两峰不能基线分离,所以苯菌灵的残留分析,我感到很困难,有老师做过这方面的工作吗,能给些建议吗[em46]
[求助]请教三唑锡、克菌丹、多菌灵、抗蚜威的液相色谱的多残留分析方法?? 我用反相柱做的,各种梯度、流速都试过了,但都在同一时间出峰左右,混标就是一个大峰,那位大虾有高招帮助解决以下 我用的zobax C18柱和AQ C18,各种条件梯度流速,醋酸缓冲液都试过了,就是分不开谁能帮助解决这个问题,或好的可行的建议或有北京的同行帮助做两针
使用 QuEChERS 预处理结合 Agilent 1260 第二代高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]建立了测定水稻水、土壤和大米中古维菌素残留的分析方法。样品用丙酮萃取,用C18吸收剂纯化,并通过0.2-μm有机滤膜过滤。稻田水、稻田和水稻中古维菌素的检测限(LODs)和定量限(LOQs)分别为0.0022、0.0041和0.0068 mg/kg和0.0073、0.0138和0.0227 mg/kg。在0.01~5 mg/L范围内线性关系良好,线性相关系数( R 2) 大于 0.9990。三个加标浓度(0.1、0.5 和 1.0 mg/kg)的平均回收率范围为 87.32% 至 112.53%,相对标准偏差 (RSD) 范围为 1.07% 至 2.48%。在 k = 2 的覆盖水平和大约 95% 的置信水平下,扩展的不确定性为 3.74-3.87%。结果表明,该方法简便、快速、准确、灵敏,能够满足稻田环境中古维菌素残留量的测定要求。这个方法的新颖处在于QuEChERS法粗净化的情况下,用紫外检测器能将稻田环境的古维菌素的定量限做到0.02 mg/kg以下,比较难得。详细信息见[url]https://doi.org/10.1016/j.jfca.2022.104644[/url]