用药典方法测定凝胶中的乙醇含量,但是要排除挥发油对乙醇的干扰,验证特异性。乙醇我用的溶剂是水,挥发油不溶于水,我用了甲醇和丙酮溶,但是单独甲醇或丙酮溶剂出的峰都很不好,应该怎么办?还需要换溶剂吗?
溶液聚合过程中,会生成一定量的聚合物凝胶,为考察工艺和设备对聚合物溶液中凝胶量的影响,需要对其含量进行测试,是否有相应的仪器和标准,请大家提供,谢谢!
HC-01162 交联聚乙烯塑料—交联度的测定—凝胶含量法

【作者】 蔡兴东; 刘新;【机构】 重庆医科大学药学院; 重庆医科大学药学院 重庆400016; 重庆400016;【摘要】 目的:建立生发凝胶中辣椒素含量测定的高效液相色谱方法。方法:采用Diamonsil C18色谱柱,以甲醇-0.1%磷酸(65∶35)为流动相,流速为1.0mL.min-1,检测波长为280nm,柱温为40℃。结果:辣椒素在5.0~100.0mg.L-1范围内与峰面积呈良好的线性关系(r=0.999 9),平均回收率为101.32%,RSD为1.72%(n=6)。结论:该方法简便、准确、重复性好,可作为生发凝胶中辣椒素的含量测定方法。 【谱图】 http://ng1.17img.cn/bbsfiles/images/2012/08/201208142055_383881_1609970_3.jpg
请问在凝胶色谱中,几个组分的峰面积之比与他们的含量之比是什么关系?是否相等?
[size=16px][color=#333333]点击链接查看更多:[color=#333333][url]https://www.woyaoce.cn/service/info-39756.html[/url][/color]服务背景[/color][/size]气凝胶是指通过溶胶凝胶法,用一定的干燥方式使气体取代凝胶中的[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]而形成的一种纳米级多孔固态材料。气凝胶检测范围气凝胶粉、气凝胶板、气凝胶毡、气凝胶隔热材料、气凝胶保温材料、气凝胶复合硅酸铝棉等。[size=16px][color=#333333]检测内容[/color][/size]气凝胶检测项目密度检测、憎水率检测、压缩强度检测、拉伸强度检测、导热系数检测、耐火极限检测、导热系数检测、压缩回弹率检测、振动质量损失率检测、热荷重收缩温度检测等。[size=16px][color=#333333]检测标准[/color][/size][table][tr][td]产品名称[/td][td]检测项目[/td][td]检测标准[/td][/tr][tr][td]气凝胶[/td][td]气凝胶绝热材料[/td][td]DB44/T 1455-2014[/td][/tr][tr][td]气凝胶[/td][td]疏水二氧化硅气凝胶粉体[/td][td]JC/T 2518-2019[/td][/tr][/table][size=16px][color=#333333]我们的优势[/color][/size]气凝胶检测流程1、沟通需求:了解待检测项目,确定检测范围;2、报价:根据检测项目及检测需求进行报价;3、签约:签订合同及保密协议,开始检测;4、完成检测:检测周期会根据样品及其检测项目/方法会有所变动,具体可咨询检测顾问;5、出具检测报告,进行后期服务;
哪位大侠能帮忙?GB/T 28601-2012 橡胶配合剂 沉淀水合二氧化硅 凝胶含量的测定
高效凝胶色谱法测定重组人白介素-l1的含量 来自《东方医药网》 摘要 目的:建立重组人白介素-11的高效凝胶色谱含量测定方法。方法:采用外标法,色谱柱:Biosep SEC-S2000 (300mm×7.8 mm),流动相:0.2mol/L 磷酸盐缓冲液(pH 6.8),流速:0.5 mL/min,检测渡长:280nm。结果:线性范围:2.5~30μg(r=0.9990),平均回收率101.1%~101.9%(RSD 1.8%,n=9) 精密度:RSD= 0.75%( n=5);最低检测限0.15μg。结论:该法用于测定重组人白介素-11的含量,简便,准确,重现性好。 关键词:重组人白介素-11;高效凝胶色谱法[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=21282]高效凝胶色谱法测定重组人白介素-l1的含量[/url]
凝胶色谱一般是在高分子方面应用的。有没有能用于小分子量化合物(分子量1000以下的)的凝胶色谱柱?上海哪所高校,研究所有呢?
奶粉蛋白质中乳清蛋白含量的测定 十二烷基硫酸钠-毛细管凝胶电泳法该标准还未正式发布

作者:陈丽娜; 李东; 谢燕贤; 温中明; 廖朝峰; 李惠民;(广东省深圳市宝安区人民医院; 广东省深圳市人民医院; 暨南大学医学院第二临床医学院; 广东省深圳市宝安区石岩医院; 广东省深圳市光明新区公明医院;)摘要:目的采用高效液相色谱法测定复方洛美沙星即型凝胶滴耳剂中地塞米松的含量。方法以Diamonsil C18柱为色谱柱,流动相为乙腈-水(40:60,pH为3.0~3.5),流速为1mL/min,柱温40℃,检测波长240nm,进样量20μL。以峰面积外标法计算。结果洛美沙星质量浓度在0.015~0.036mg/mL范围内与峰面积线性关系良好,r=0.9999(n=5),平均回收率为98.01%,RSD=2.95%(n=9)。结论该法操作简便、快速,结果准确可靠,重现性好,可用于测定复方洛美沙星即型凝胶滴耳剂中地塞米松的含量。谱图:http://ng1.17img.cn/bbsfiles/images/2012/08/201208271022_386296_1606903_3.jpg
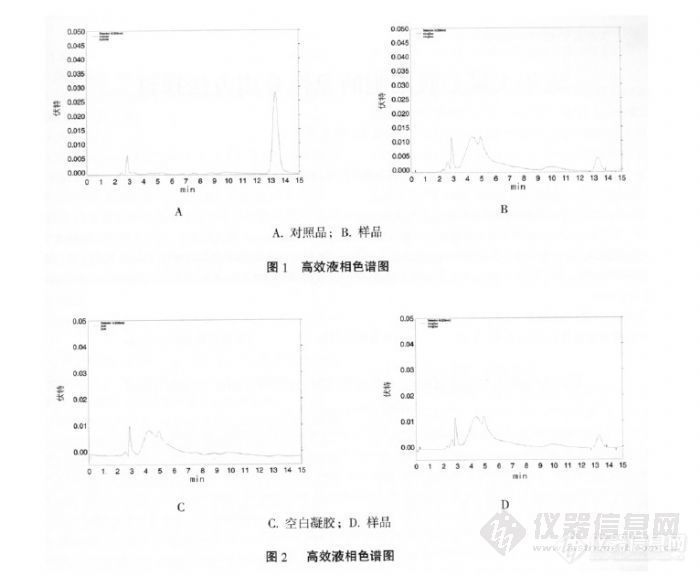
【作者】 李燕; 刘新;【Author】 LI Yan,et al (Department of Natural Medicinal Chemistry,College of Pharmacy,Chongqing Medical University)【机构】 重庆医科大学药学院天然药物化学教研室药物重庆市高校工程研究中心;【摘要】 目的:建立RP-HPLC法测定雷公藤外用凝胶中雷公藤甲素的含量。方法:采用Diamonsil C18色谱柱(250mm×4.6mmi.d,5μm),检测波长为220nm,流动相为甲醇∶水(46∶54),流速1ml/min,柱温为室温。结果:在10.24~51.20μg/ml间,雷公藤甲素的浓度与峰面积积分值呈良好的线性关系(r=0.9997),方法回收率为98.3%,RSD为0.23%(n=5)。结论:此方法准确、简便,可用于雷公藤甲素外用凝胶中雷公藤甲素的含量测定。 更多还原【Abstract】 Objective:To develop an HPLC method for the assay of the content of triptolide in triptolide gel. Methods:The content of triptolide was measured by HPLC on Diamonsil C18 column(250mm×4.6mm i.d,5μm)using methanol-water(46∶54,v/v)as mobile phase,at a flow rate of 1.0ml/min. The UV detection was set at 220nm. Results:The calibration curve was proved to be linear in the range of 10.24~51.20μg/ml with a regression coeficient of 0.999 7. The average recovery of the method was 98.3%;RSD was 0.23%(n=5).... 更多还原【关键词】 高效液相色谱法; 雷公藤甲素; 凝胶; 【Key words】 HPLC; Triptolide; Gel; http://ng1.17img.cn/bbsfiles/images/2012/08/201208061038_381720_2352694_3.jpg
凝胶成像定义 凝胶成像即:对DNA或RNA胶 进行切胶、拍照、观察、分析 ,的实验室类仪器, 凝胶成像系统可以应用于分子 量计算,密度扫描,密度定量, PCR定量等生物工程常规研究。凝胶成像应用范围 总体上来说凝胶成像可应用于:凝胶成像系统可以用于:蛋白质、核酸、多肽、氨基酸、多聚氨基酸等其他生物分子的分离纯化结果作定性分析 (1)分子量定量 对于一般常用的DNA胶片,利用分子量定量功能,通过对胶上DNA Marker条带的已知分子量注释,自动生成拟合曲线,并以它衡量得到未知条带的分子量。通过这种方法所得到的结果较肉眼观察估计要准确很多。 (2)密度定量 一般常用的测定DNA(脱氧核糖核酸)和RNA(核糖核酸)浓度的方法是紫外吸收法,但它只能测定样品中的总核苷酸浓度,而不能区分各个长度片段的浓度。利用凝胶成像系统和软件,先将DNA胶片上某一已知其DNA含量的标准条带进行密度标定以后,可以方便的单击其他未知条带,根据与已知条带的密度做比较,可以得到未知DNA的含量。此方法也适用于对PA GE蛋白胶条带的浓度测定。 (3)密度扫描 在分子生物学和生物工程研究中,最常用到的是对蛋白表达产物占整个菌体蛋白的百分含量的计算。传统的方法是利用专用的密度扫描,但利用生物分析软件结合现在实验室常规配备的扫描仪或者直接用白光照射的凝胶成像就能完成此项工作。 (4)PCR定量 PCR定量主要是指,如果PCR实验扩增出来的条带不是一条,那么可以利用软件计算出各个条带占总体条带的相对百分数。就此功能而言,与密度扫描类似,但实际在原理上并不相同。PCR定量是对选定的几条带进行相对密度定量并计算其占总和的百分数,密度扫描时并对选择区域生成纵向扫描曲线图并积分。
想搞个2%氯己定含量的透明凝胶,有大神搞过吗 ,怎么配,
思考了半天要把这个帖子发到哪里,确实有凝胶色谱的版块,却是GPC的,我要做的GFC也只是把凝胶柱装到普通液相上,而且这里专家也多,应该更能帮我解决问题,所以发到这里了。 言归正传,我是一个凝胶色谱的新手,之前只用葡聚糖凝胶做过分离,还是自己装的柱子,这次要做一种药的含量测定,美国药典已有方法,用了PolySep-GFC-P3000的柱子,打听了一下要8000多,有点贵,想找找有没有类似的柱子可能会便宜点,虽然有一点现成的资料,但我也要知道原理才行啊!这样问题就出来了,刚刚在网上找了半天,发现对于凝胶色谱的资料很少,而且大部分还是GPC的,图书馆也去了,没有收获。以下是我的问题: 1.用凝胶色谱测定分子量和质量分布的原理是什么呢?我知道凝胶色谱的分子排阻原理,这和测分子量有什么关系呢?色谱图的横坐标是时间吗?还是别的单位? 2.我要做的物质是含量测定,这是一种多取代混合物,其主成分的分子量范围是1000多到2000多(就是我要测含量的部分),当然也有一些小分子量的杂质,大部分不超过1000,那我在选择柱子(主要是排阻限)时有没有什么原则或依据呢?(虽然美国药典有明确的方法和柱子,我还是想知道) 3 对于GFC的凝胶应该也有好多种,他们之间只是在分离中分子量的差别吗?性质上有没有差别?拿我的情况为例吧,我要对一水溶性药物做含量测定,在选择柱子时只需考虑两点:1 用于水溶性的凝胶 2 选择合适的能分离的分子量。这就够了,也就是说如果有两种不同的凝胶,只要能满足上述两点,那我用哪种都能达到实验目的,这样理解对吗?先谢谢给位老师朋友不吝赐教!
凝胶是在直溜分柴油中加入一定含量的生物切片石蜡(5%-15%)形成的,需要测定蜡晶在凝胶中的形态和分布(单位体积内的蜡晶数量、大小分布),用偏光显微镜能观测到蜡晶,蜡晶最小能有几百个nm。求助各位大侠,用什么方法测定蜡晶在凝胶中的形态和分布?谢谢~~
请教下各位大神,怎么检测凝胶糖果中的死菌含量呢?急!!就是像QQ糖那种,要先融化吗?还是直接取样染色镜检?(问题是,融化是不是会把里面可能存在的活菌也灭了,直接染色镜检又不好固定,也不均匀。。。)
请教下各位大神,怎么检测凝胶糖果中的死菌含量呢?急!!就是像QQ糖那种,要先融化吗?还是直接取样染色镜检?(问题是,融化是不是会把里面可能存在的活菌也灭了,直接染色镜检又不好固定,也不均匀。。。)
想测定聚天冬氨酸的含量,问了好多个地方都不行,不知道哪里还能做水相的凝胶色谱,谢谢各位。。。
[color=#000000]我现在在用凝胶色谱柱检测甘油一酯、二酯、三酯及游离脂肪酸的含量。流动相是四氢呋喃,检测是ELSD。在检测过程中,分离效果不稳定,同样的条件,有时候分离度可以达到大于1.5,有时候完全分不开。而且跑四氢呋喃空白,也会在目标峰的位置有信号响应,响应值也不小。[/color]
电解液是锂离子电池关键材料之一,采用有机溶剂的电解液在极端情况下会出现漏液问题,并易燃。用聚合物电解质替代电解液被认为是解决上述问题的有效方案。聚合物电解质主要包括凝胶聚合物电解质(GPE)和全固态聚合物电解质(SPE)。全固态聚合物电解质由于常温离子电导率较低的问题一直没有解决,并且成本过高,尚未有商品上市。目前取得商业化应用的主要是凝胶聚合物电解质。凝胶聚合物电解质既有全固态聚合物电解质良好的安全性,又与有机溶剂电解液有相近的离子电导率,并且具有与电极材料间的反应活性低、质量轻、易成薄膜、黏弹性好的特点。因此采用凝胶聚合物电解质的电池可制成各种形状,并具有耐压、耐冲击、生产成本低和易于加工使用等优势。应用于高端数码产品的软包锂电池对轻薄和电池形状的灵活性有较高的要求,是凝胶聚合物电解质最适合的应用方向之一。传统制备凝胶聚合物电解质的原理是利用分子链间存在相互作用力而形成物理交联,再吸入电解液后制成凝胶聚合物电解质。需经过聚合物成膜、造孔剂萃出和电解液浸渍等复杂工序,制出凝胶聚合物电解质膜后再与正、负极按一定顺序组装成电池。随着制备工艺的发展,出现了凝胶聚合物电解质的现场聚合工艺。现场聚合工艺的原理是将聚合物单体和引发剂按一定比例加入电解液中混合均匀,在一定的外界条件下引发自由基聚合反应,单体聚合后即产生网状的立体骨架结构,将电解液均匀固化在网状结构的空隙当中,得到凝胶聚合物电解质。现场聚合工艺优点是电解液含量高,凝胶热稳定性好,电池成品质量稳定。但其未反应的残余单体对电池性能的影响不容忽视,并且聚合反应精确控制的难度较大。现场聚合工艺具体可分为热引发现场聚合工艺与非热引发现场聚合工艺,而前者更为常见。其中中国科学院物理研究所、比亚迪股份有限公司、三洋株式会社及三星SDI 株式会社等均有相关专利。相比传统制备工艺的繁琐,现场聚合工艺将电解质的制备与电池组装一步完成,有效降低了生产成本,提高了生产效率。
凝胶过滤色谱摘要:本文主要讲解了凝胶过滤色谱法(分子筛)在蛋白纯化实验中的应用,包括纯化原理、实验方案设计、技术操作以及相关案例介绍和问题分析。基本原理凝胶过滤色谱蛋白纯化法,又称为空间排阻色谱,分子筛等。其原理是应用蛋白质分子量或分子形状的差异来分离。当样品从色谱柱的顶端向下运动时,大的蛋白质分子不能进入凝胶颗粒从而被迅速洗脱;而较小的蛋白质分子能够进入凝胶颗粒中,且进入凝胶的蛋白在凝胶中保留时间也不同,分子量越大,流出时间就越早,最终分离分子大小不同的蛋白质。http://www.detaibio.com/assets/image/topics/gel-filtration-chromatography-theory.jpg通常,多数凝胶基质是化学交联的聚合物分子制备的,交联程度决定凝胶颗粒的孔径。常用的色谱基质有:葡聚糖凝胶(Sephadex)、琼脂糖凝胶(Sepharose)、聚丙烯酰氨凝胶(Bio-Gel P)等。高度交联的基质可用来分离蛋白质和其他分子量更小的分子,或是除去低分子量缓冲液成分和盐,而较大孔径的凝胶可用于蛋白质分子之间的分离。选用合适孔径的凝胶很大程度取决于目标蛋白的分子量和杂蛋白的分子量。实验方案设计凝胶介质的选择凝胶介质的选择主要是根据待分离的蛋白和杂蛋白的分子量选择具有相应分离范围的凝胶,同时还需要考虑到分辨率和稳定性的因素。比如,如果是要将目的蛋白和小分子物质分开,可以根据他们分配系数的差异,选用Sephadex G-25和 G-50;对于小肽和低分子量物质的脱盐,则可以选用Sephadex G-10、G-15以及Bio-Gel P-2或P-4;如果是分子量相近的蛋白质,一般选用排阻限度略大于样品中最高分子量物质的凝胶。具体凝胶过滤色谱介质应用如下:常用凝胶过滤色谱介质的分离范围凝胶介质蛋白质的分离范围/103凝胶介质蛋白质的分离范围/103Sephadex G25Sephadex G50Sephadex G100Sephadex G200Sepharose 6BSepharose 4B1~51.5~304~1505~60010~400060~20000Sepharose 2BBio-Gel P-4Bio-Gel P-10Bio-Gel P-60Bio-Gel P-150Bio-Gel P-30070~400000.5~45~1730~7050~150100~400凝胶介质的预处理凝胶在使用前应用水充分溶胀(胶:水=1:10),自然溶胀的耗时较长,可采用加热的方法使溶胀加速,即在沸水浴中将凝胶升温至沸,1~2h即可达到溶胀。在烧杯中将干燥凝胶加水或缓冲液,搅拌,静置,倾去上层混悬液,除去上清液中的凝胶碎块,重复数次,直到上清澄清为止。色谱柱的选择色谱柱的体积和高径比与色谱分离效果密切相关,凝胶柱床的体积、柱长和柱的直径以及柱比的选择必须根据样品的数量,性质和分离目的进行确定。组别分离时,大多采用2~30cm长的色谱柱,柱床体积为样品溶液体积的5倍以上,柱比一般在5~10之间;而分级分离一般需要100cm左右的色谱柱,并要求柱床体积大于样品体积25倍以上,柱比在20~100之间。凝胶柱的填装凝胶色谱柱与其它色谱方法不同,溶质分子与固定相之间没有力的作用,样品组分的分离完全依赖于他们各自的流速差异。装住时关住柱子下口,在柱内加入约1/3柱床体积的水或缓冲液,然后沿着柱子一侧将缓冲液中的凝胶搅拌均匀,缓慢并连续的一次性注入柱内。待凝胶沉积约5厘米左右时,打开柱子下口,控制流速在1ml/min。样品的处理与上样根据样品的类型和纯化分析,需要选择合适的缓冲液,为了达到良好的分析效果,上样量必须保持在较小的体积,一般为柱床体积的1%~5%,蛋白质样品上样前应进行浓缩,使样品浓度不大于4%(样品浓度与分配系数无关),但需要注意的是,较大分子量的物质,溶液粘度会随浓度增加而增大,使分子运动受限,影响流速。上样前,样品要经滤膜过滤或离心,除去可能堵塞色谱柱的杂质。洗脱与收集凝胶过滤色谱的缓冲液用单一缓冲液或含盐缓冲液作为洗脱液即可,主要考虑俩个方面的原因:蛋白的溶解性和稳定性。所用的缓冲液要保证蛋白质样品在其中不会变性或沉淀,PH应选在样品较稳定、溶解性良好的范围之内,同时缓冲液中要含有一定的盐(NaCL),对蛋白质起稳定和保护作用。洗脱过程中始终保持一定的操作压,流速不可过高,保持在0.5~3.0mL/min即可。案列介绍AKTA凝胶过滤色谱分离蛋白质材料色谱介质:Sephacryl S-200,蛋白质分离范围(5~250)×103 色谱柱:XK16/60预装柱色谱设备:AKTA Explorer混合样品:含单克隆抗体,分子量180000;牛血清白蛋白(68000),溶菌酶(14000)NaOH 0.5 mol/LNaCl 200 mmol/LPB 20 mmol/LPH7.0 缓冲液方法凝胶除菌处理超纯水冲洗柱子后,用0.5mol/L NaOH正向冲洗柱,流速3mL/min,冲洗3柱体积平衡NaOH处理完毕后,用超纯水冲洗2柱体积,接着用含200mmol/L NaCl和20mmol/L PB的7.0PH缓冲液冲洗5~10倍柱体积上样平衡完毕后,选择样品泵进行上样,上样流速3mL/min,上样体积为1mL洗脱上样结束后,用平衡缓冲液进行洗脱清洗与保存纯化结束后,用0.5mol/L NaOH反向冲洗2柱体积,冲洗时间30~60min,冲洗结束后,用超纯水正向冲洗5柱体积,再用20%乙醇冲洗3柱体积,然后拆下柱子,俩端封死,低温保存。问题分析和解决方案色谱分离前如何净化样品在色谱分离前,对样品进行离心和过滤,离心能除去大部分块状物,如果离心后样品仍不清澈,可用滤膜过滤。由醋酸纤维薄膜或PVDF材料制成的滤膜能够非特异性的结合少量蛋白。溶液交换不彻底严格控制上样体积,上样体积不超过柱体积30%。若样品溶液体积较多,可以分多次上样,注意每次上样时间间隔,可根据电导色谱峰确定下一次上样时间。分辨率不高1)提高装柱质量,使色谱柱装填匀实; 2)提高柱床高度; 3)控制上样体积,最大上样体积不超过柱床体积5%; 4)控制样品黏度与洗脱溶液黏度保持一致; 5)根据样品特点选择合适的洗脱溶液,调节洗脱溶液的离子强度或亲水性; 6)选择合适的凝胶柱(如何选择请参照上文)色谱峰对称性差1)提高装柱质量,装柱匀实——若柱装的太松,容易引起拖尾,装的太紧,会引起前沿;2)柱较脏,再生色谱柱肩峰出现的原因及解决方法1)柱床松动,重新装柱或反向冲洗柱2)柱筛板堵塞,超声清洗筛板3)柱干裂,重新装柱
我要测土壤中的抗生素含量,目前计划流程是这样的:提取——HLB固相萃取——凝胶层析——LC/MS/MS检测因为腐植酸会对色谱影响很大,所以有人建议我用分子排阻滤掉大分子,但是我能查到的资料都是用凝胶色谱测定大分子的,想知道如果我只是要层析分离不用测定,是不是也要用专门的凝胶色谱柱?还是买了填料自己做个层析柱就可以?自己做的话怎么控制洗脱时间?从来没接触过凝胶,还请大大们指点!
关键词:中检所网站 中检所标准品 中检所对照品 药检所标准品 药检所对照品 中检所标准物 质药检所标准物质摘要:凝胶色谱技术是六十年代初发展起来的一种快速而又简单的分离分技术,由于设备简单、操作方便,不需要有机溶剂,对高分子物质有很高的分离效果。目前已经被生物化学、分子生物学、生物工程学、分子免疫学以及医学等有关领域广泛采用,不但应用于科学实验研究,而且已经大规模地用于工业生产。 一、基本理论 (一)分子筛效益 一个含有各种分子的样品溶液缓慢地流经凝胶色谱柱时,各分子在柱内同时进行着两种不同的运动:垂直向下的移动和无定向的扩散运动。大分子物质由于直径较大,不易进入凝胶颗粒的微孔,而只能分布颗粒之间,所以在洗脱时向下移动的速度较快。小分子物质除了可在凝胶颗粒间隙中扩散外,还可以进入凝胶颗粒的微孔中,即进入凝胶相内,在向下移动的过程中,从一个凝胶内扩散到颗粒间隙后再进入另一凝胶颗粒,如此不断地进入和扩散,小分子物质的下移速度落后于大分子物质,从而使样品中分子大的先流出色谱柱,中等分子的后流出,分子最小的最后流出,这种现象叫分子筛效应。具有多孔的凝胶就是分子筛。各种分子筛的孔隙大小分布有一定范围,有最大极限和最小极限。分子直径比凝胶最大孔隙直径大的,就会全部被排阻在凝胶颗粒之外,这种情况叫全排阻。两种全排阻的分子即使大小不同,也不能有分离效果。直径比凝胶最小孔直径小的分子能进入凝胶的全部孔隙。如果两种分子都能全部进入凝胶孔隙,即使它们的大小有差别,也不会有好的分离效果。因此,一定的分子筛有它一定的使用范围。综上所述,在凝胶色谱中会有三种情况,一是分子很小,能进入分子筛全部的内孔隙;二是分子很大,完全不能进入凝胶的任何内孔隙;三是分子大小适中,能进入凝胶的内孔隙中孔径大小相应的部分。大、中、小三类分子彼此间较易分开,但每种凝胶分离范围之外的分子,在不改变凝胶种类的情况下是很难分离的。对于分子大小不同,但同属于凝胶分离范围内各种分子,在凝胶床中的分布情况是不同的:分子较大的只能进入孔径较大的那一部分凝胶孔隙内,而分子的可进入较多的凝胶颗粒内,这样分子较大的在凝胶床内移动距离较短,分子较小的移动距离较长。于是分子较大的先通过凝胶床而分子较小的后通过凝胶床,这样就利用分子筛可将分子量不同的物质分离。另外,凝胶本身具有三维网状结构,大的分子在通过这种网状结构上的孔隙时阻力较大,小分子通过时阻力较小。分子量大小不同的多种成份在通过凝胶床时,按照分子量大小“排队,凝胶表现分子筛效应。 (二)色谱柱的重要参数 ⑴柱体积:柱体积是指凝胶装柱后,从柱的底板到凝胶沉积表面的体积。在色谱柱中充满凝胶的部分称为凝胶床,因引柱体积又称“床”体积,常用Vt 表示。 ⑵外水体积:色谱柱内凝胶颗粒间隙,这部分体积称外水体积,亦称间隙体积,常用Vo表示。 ⑶内水体积:因为凝胶为三维网状结构,颗粒内部仍有空间,液体可进入颗粒内部,这就分间隙的总和为内水体积,又称定相体积,常用Vi表示。 不包括固体支持物的体积(Vg)。 ⑷峰洗脱体积:是指被分离物质通过凝胶柱所需洗脱液有体积,常用Ve 表示。当使用样品的体积很少时,(与洗脱体积比较可以忽略不计),在洗脱图中,从加样到峰顶位置所用洗脱液体积为Ve。 当样品体积与洗脱体积比较不能忽略时,洗脱体积计算可以从样品体积的一半到峰顶位置。当样品很大时,洗脱体积计算可以从应用样品开始到洗脱峰升高的弯曲点(或半高处)。 二、凝胶的种类及性质 (一)交联葡聚糖凝胶(Sephadex) ⑴Sephadex G交联葡聚糖的商品名为Sephndex,不同规格型号的葡聚糖用英文字母G表示,G后面的阿拉伯数为凝胶得水值的10倍。例如,G-25为每克凝胶膨胀时吸水2.5克,同样G-200克每克千胶吸水20克。交联葡聚糖凝胶的种类有G-10,G-15,G-25,G-50,G-75,G-100,G- 150,和G-200。因此,“G”反映,凝胶的交联程度,膨胀程度及分部范围。 ⑵Sephadex LH-20,是─Sephadex G-25的羧丙基衍生物, 能溶于水及亲脂溶剂,用于分离不溶于水的物质。 (二)琼脂糖凝胶: 商品名很多,常见的有,Sepharose(瑞典,pharmacia ),Bio-Gel-A(美国Bio-Rad)等。琼脂糖凝胶是依靠糖链之间的次级链如氢键来维持网状结构,网状结构的疏密依靠琼脂糖的浓度。一般情况下,它的结构是稳定的,可以在许多条件下使用(如水,pH4-9范围内的盐溶液)。琼脂糖凝胶在40℃以上开始融化,也不能高压消毒,可用化学灭菌活处理。 (三)聚丙烯酰胺凝胶: 是一种人工合成凝胶,是以丙烯酰胺为单位, 由甲叉双丙烯酰胺交联成的,经干燥粉碎或加工成形制成粒状,控制交联剂的用量可制成各种型号的凝胶。交联剂越多,孔隙越小。聚丙烯酰胺凝胶的商品为生物胶-P (Bio-Gel P),由美国Bio-Rod厂生产,型号很多,从P-2至P-300共10种,P 后面的数字再乘1000就相当于该凝胶的排阻限度。 (四)聚苯乙烯凝胶商品为Styrogel , 具有大网孔结构, 可用于分离分子量1600到40,000,000的生物大分子,适用于有机多聚物,分子量测定和脂溶性天然物的分级,凝胶机械强度好,洗脱剂可用甲基亚砜。 三、实验技术 (一)层析柱 层析柱是凝胶层析技术中的主体,一般用玻璃管或有机玻璃管。层析柱的直径大小不影响分离度,样品用量大,可加大柱的直径,一般制备用凝胶柱,直径大于2厘米,但在加样时应将样品均匀分布于凝胶柱床面上。此外, 直径加大,洗脱液体体积增大,样品稀释度大。分离度取决于柱高,为分离不同组分,凝胶柱床必须有适宜的高度,分离度与柱高的平方根相关,但由于软凝胶柱过高挤压变形阻塞,一般不超过1米。分族分离时用短柱,一般凝胶柱长20-30厘米,柱高与直径的比较5:1─10:1,凝胶床体积为样品溶液体积的 4-10倍。 分级分离时柱高与直径之线为20:1─100:1,常用凝胶柱有50×25厘米,10×25厘米。层析柱滤板下的死体积应尽可能的小,如果支掌滤板下的死体积大,被分离组分之间重新混合的可能性就大,其结果是影响洗脱峰形,出现拖尾出象,降低分辩力。在精确分离时,死体积不能超过总床体积的1/1000。 (二)凝胶的选择 根据所需凝胶体积,估计所需干胶的量。 一般葡聚糖凝胶吸水后的凝胶体积约为其吸水量的2倍,例如Sephadex G-20的吸水量为20,1 克Sephadex G─200吸水后形成的凝胶体积约40ml。凝胶的粒度也可影响层析分离效果。粒度细胞分离效果好,但阻力大,流速慢。一般实验室分离蛋白质采用 100-200号筛目的的Sephadex G-200效果好, 脱盐用Sephadex G-25、G-50,用粗粒,短柱,流速快。 (三)凝胶的制备 商品凝胶是干燥的颗粒使用前需直接在欲使用的洗脱液中膨胀。为了加速膨胀,可用加热法,即在沸水浴中将湿凝胶逐渐升温至近沸,这样可大大中速膨胀,通常在 1-2小时内即可完成。特别是在使用软胶时, 自然膨胀需24小时至数天,而用加热法在几小时内就可完成。这种方法不但节约时间,而且还可消毒,除去凝胶中污染的细菌和排除胶内的空气。 (四)样品溶液的处理 样品溶液如有沉淀应过滤或离心除去,如含脂类可高速离心或通过Sephadex G-15短柱除去。样品的粘度不可大,含蛋白为超过4%,粘度高影响分离效果。上柱样品液的体积根据凝胶床体积的分离要求确定。分离蛋白质样品的体积为凝胶床的1-4%(一般约0.5-2ml),进行分族分离时样品液可为凝胶床的10%,在蛋白质溶液除盐时,样品可达凝胶床的20-30%。 分级分离样品体积要小,使样品层尽可能窄,洗脱出的峰形较好。 (五)防止微生物的污染 交联葡
对于广大实验科研工作者来说大家在做PCR凝胶成像实验时应注意以下几个问题: 1.EB染料的安全使用EB(Ethidium bromide):即溴化乙锭是一种高度灵敏的荧光染色剂,广泛用于观察琼脂糖和聚丙烯酰胺凝胶中的核酸大分子。在302nm 紫外光激发下溴化乙锭能够放射出橙红色荧光信号,用Polaroid 底片或有CCD 成像头的凝胶成像处理系统可以捕捉拍摄这种信号。因此EB染料广泛用于分子生物学实验。但目前认为EB染料是一种强诱变剂,具有高致癌性。因此在实验过程中一定要注意安全。实验结束后要对EB染料净化处理,以免危害人身安全及污染环境。对于含有EB染料的溶液可做如下处理:EB含量超过0.5mg/ml:首先用水将其浓度稀释至0.5mg/ml以下;然后加入一倍体积的0.5mol/L KMnO4,混匀,再加入等量的25mol/L HCl,混匀,置室温下数小时;最后加入一倍体积的2.5mol/L NaOH,混匀并废弃。EB含量小于0.5mg/ml:首先按1mg/ml的量加入活性炭,轻摇混匀后置室温下1小时;然后用滤纸过滤溶液,并将活性碳与滤纸密封废弃。2.对于紫外线的防护虽然适量紫外线对人体具有一定的保健作用,但对于科学工作者来说往往要接触大量的紫外辐射,因此正确的防护尤为重要。过量过强紫外线作用于皮肤时,易引起皮肤出现红斑,水疱甚至水肿,严重的还可引起皮肤癌等。作用于眼睛可引起眼痛,流泪等进而引起各种炎症反应,严重的还可能诱发白内障。过量强紫外线作用于中枢神经系统,可引发头痛、头晕、体温升高等不适症状。
请问凝胶柱一般上样量多少比较合适?
凝胶糖果的还原糖分测定中含油该如何处理?内芯含大豆油,水溶不溶解,该如何处理?
[分享]凝胶色谱技术凝胶色谱技术是六十年代初发展起来的一种快速而又简单的分离分技术,由于设备简单、操作方便,不需要有机溶剂,对高分子物质有很高的分离效果。目前已经被生物化学、分子生物学、生物工程学、分子免疫学以及医学等有关领域广泛采用,不但应用于科学实验研究,而且已经大规模地用于工业生产。一、基本理论(一)分子筛效益 一个含有各种分子的样品溶液缓慢地流经凝胶色谱柱时,各分子在柱内同时进行着两种不同的运动:垂直向下的移动和无定向的扩散运动。大分子物质由于直径较大,不易进入凝胶颗粒的微孔,而只能分布颗粒之间,所以在洗脱时向下移动的速度较快。小分子物质除了可在凝胶颗粒间隙中扩散外,还可以进入凝胶颗粒的微孔中,即进入凝胶相内,在向下移动的过程中,从一个凝胶内扩散到颗粒间隙后再进入另一凝胶颗粒,如此不断地进入和扩散,小分子物质的下移速度落后于大分子物质,从而使样品中分子大的先流出色谱柱,中等分子的后流出,分子最小的最后流出,这种现象叫分子筛效应。具有多孔的凝胶就是分子筛。各种分子筛的孔隙大小分布有一定范围,有最大极限和最小极限。分子直径比凝胶最大孔隙直径大的,就会全部被排阻在凝胶颗粒之外,这种情况叫全排阻。两种全排阻的分子即使大小不同,也不能有分离效果。直径比凝胶最小孔直径小的分子能进入凝胶的全部孔隙。如果两种分子都能全部进入凝胶孔隙,即使它们的大小有差别,也不会有好的分离效果。因此,一定的分子筛有它一定的使用范围。综上所述,在凝胶色谱中会有三种情况,一是分子很小,能进入分子筛全部的内孔隙;二是分子很大,完全不能进入凝胶的任何内孔隙;三是分子大小适中,能进入凝胶的内孔隙中孔径大小相应的部分。大、中、小三类分子彼此间较易分开,但每种凝胶分离范围之外的分子,在不改变凝胶种类的情况下是很难分离的。对于分子大小不同,但同属于凝胶分离范围内各种分子,在凝胶床中的分布情况是不同的:分子较大的只能进入孔径较大的那一部分凝胶孔隙内,而分子的可进入较多的凝胶颗粒内,这样分子较大的在凝胶床内移动距离较短,分子较小的移动距离较长。于是分子较大的先通过凝胶床而分子较小的后通过凝胶床,这样就利用分子筛可将分子量不同的物质分离。另外,凝胶本身具有三维网状结构,大的分子在通过这种网状结构上的孔隙时阻力较大,小分子通过时阻力较小。分子量大小不同的多种成份在通过凝胶床时,按照分子量大小“排队,凝胶表现分子筛效应。(二)色谱柱的重要参数⑴柱体积:柱体积是指凝胶装柱后,从柱的底板到凝胶沉积表面的体积。在色谱柱中充满凝胶的部分称为凝胶床,因引柱体积又称“床”体积,常用Vt 表示。⑵外水体积:色谱柱内凝胶颗粒间隙,这部分体积称外水体积,亦称间隙体积,常用Vo表示。⑶内水体积:因为凝胶为三维网状结构,颗粒内部仍有空间,液体可进入颗粒内部,这就分间隙的总和为内水体积,又称定相体积,常用Vi表示。 不包括固体支持物的体积(Vg)。⑷峰洗脱体积:是指被分离物质通过凝胶柱所需洗脱液有体积,常用Ve 表示。当使用样品的体积很少时,(与洗脱体积比较可以忽略不计),在洗脱图中,从加样到峰顶位置所用洗脱液体积为Ve。 当样品体积与洗脱体积比较不能忽略时,洗脱体积计算可以从样品体积的一半到峰顶位置。当样品很大时,洗脱体积计算可以从应用样品开始到洗脱峰升高的弯曲点(或半高处)。 二、凝胶的种类及性质 (一)交联葡聚糖凝胶(Sephadex)⑴Sephadex G交联葡聚糖的商品名为Sephndex,不同规格型号的葡聚糖用英文字母G表示,G后面的阿拉伯数为凝胶得水值的10倍。例如,G-25为每克凝胶膨胀时吸水2.5克,同样G-200克每克千胶吸水20克。交联葡聚糖凝胶的种类有G-10,G-15,G-25,G-50,G-75,G-100,G-150,和G-200。因此,“G”反映,凝胶的交联程度,膨胀程度及分部范围。⑵Sephadex LH-20,是─Sephadex G-25的羧丙基衍生物, 能溶于水及亲脂溶剂,用于分离不溶于水的物质。(二)琼脂糖凝胶: 商品名很多,常见的有,Sepharose(瑞典,pharmacia ),Bio-Gel-A(美国Bio-Rad)等。琼脂糖凝胶是依*糖链之间的次级链如氢键来维持网状结构,网状结构的疏密依*琼脂糖的浓度。一般情况下,它的结构是稳定的,可以在许多条件下使用(如水,pH4-9范围内的盐溶液)。琼脂糖凝胶在40℃以上开始融化,也不能高压消毒,可用化学灭菌活处理。(三)聚丙烯酰胺凝胶: 是一种人工合成凝胶,是以丙烯酰胺为单位, 由甲*双丙烯酰胺交联成的,经干燥粉碎或加工成形制成粒状,控制交联剂的用量可制成各种型号的凝胶。交联剂越多,孔隙越小。聚丙烯酰胺凝胶的商品为生物胶-P (Bio-Gel P),由美国Bio-Rod厂生产,型号很多,从P-2至P-300共10种,P 后面的数字再乘1000就相当于该凝胶的排阻限度。(四)聚苯乙烯凝胶商品为Styrogel , 具有大网孔结构, 可用于分离分子量1600到40,000,000的生物大分子,适用于有机多聚物,分子量测定和脂溶性天然物的分级,凝胶机械强度好,洗脱剂可用甲基亚砜。三、实验技术(一)层析柱 层析柱是凝胶层析技术中的主体,一般用玻璃管或有机玻璃管。层析柱的直径大小不影响分离度,样品用量大,可加大柱的直径,一般制备用凝胶柱,直径大于2厘米,但在加样时应将样品均匀分布于凝胶柱床面上。此外, 直径加大,洗脱液体体积增大,样品稀释度大。分离度取决于柱高,为分离不同组分,凝胶柱床必须有适宜的高度,分离度与柱高的平方根相关,但由于软凝胶柱过高挤压变形阻塞,一般不超过1米。分族分离时用短柱,一般凝胶柱长20-30厘米,柱高与直径的比较5:1─10:1,凝胶床体积为样品溶液体积的4-10倍。 分级分离时柱高与直径之线为20:1─100:1,常用凝胶柱有50×25厘米,10×25厘米。层析柱滤板下的死体积应尽可能的小,如果支掌滤板下的死体积大,被分离组分之间重新混合的可能性就大,其结果是影响洗脱峰形,出现拖尾出象,降低分辩力。在精确分离时,死体积不能超过总床体积的1/1000。(二)凝胶的选择 根据所需凝胶体积,估计所需干胶的量。 一般葡聚糖凝胶吸水后的凝胶体积约为其吸水量的2倍,例如Sephadex G-20的吸水量为20,1 克Sephadex G─200吸水后形成的凝胶体积约40ml。凝胶的粒度也可影响层析分离效果。粒度细胞分离效果好,但阻力大,流速慢。一般实验室分离蛋白质采用100-200号筛目的的Sephadex G-200效果好, 脱盐用Sephadex G-25、G-50,用粗粒,短柱,流速快。(三)凝胶的制备 商品凝胶是干燥的颗粒使用前需直接在欲使用的洗脱液中膨胀。为了加速膨胀,可用加热法,即在沸水浴中将湿凝胶逐渐升温至近沸,这样可大大中速膨胀,通常在1-2小时内即可完成。特别是在使用软胶时, 自然膨胀需24小时至数天,而用加热法在几小时内就可完成。这种方法不但节约时间,而且还可消毒,除去凝胶中污染的细菌和排除胶内的空气。(四)样品溶液的处理 样品溶液如有沉淀应过滤或离心除去,如含脂类可高速离心或通过Sephadex G-15短柱除去。样品的粘度不可大,含蛋白为超过4%,粘度高影响分离效果。上柱样品液的体积根据凝胶床体积的分离要求确定。分离蛋白质样品的体积为凝胶床的1-4%(一般约0.5-2ml),进行分族分离时样品液可为凝胶床的10%,在蛋白质溶液除盐时,样品可达凝胶床的20-30%。 分级分离样品体积要小,使样品层尽可能窄,洗脱出的峰形较好。(五)防止微生物的污染 交联葡聚糖和琼脂糖都是多糖类物质,防止微生物的生长,在凝胶层析中十分重要,常用的抑菌剂有:⑴叠氨钠(NaN3)在凝胶层析中只要用0.02%叠氮钠已足够防止微生物的生长,叠氮钠易溶一水,在20℃时约为40%;它不与蛋白质或碳水化合物相互作用,因此叠氮钠不影响抗体活力;不会改变蛋白质和碳水化合物的层析我特性。叠氮钠可干扰荧光标记蛋白质。⑵可乐酮[Cl3C-C(OH)(CH3)2]在凝胶层析中使用浓度为0.01-0.02%。在微酸性溶液中它的杀菌效果最佳,在强碱性溶液中或温度高于60℃时易引起分解而失效。⑶乙基汞代巯基水杨酸钠 在凝胶层析中作为抑菌剂使用浓度为0.05-0. 01%。在微酸性溶液中最为有效。重金属离子可使乙基代巯基的物质结合,因而包含疏基的蛋白质可在不同程度上降低它的抑菌效果。⑷苯基汞代盐 在凝胶层析中使用浓度为0.001-0.01%。在微碱性溶液中抑效果最佳,长时间放置时可与卤素、硝酸根离子作用而产生沉淀;还原剂可引起此化合物分解;含疏基的物质亦可降低或抑制它的抑菌作用。
[color=#444444]目前正在实验室做课题需要用到凝胶色谱,请教大家,测酪蛋白溶液(里面还含有一些乳化剂)溶剂是纯水,凝胶色谱要用得流动相和柱子分别是什么?[/color]
含醋酸氯己定卡波姆基质凝胶剂浑浊问题的解决 最近在做一个含有中、西药的凝胶剂,由于西药成分与凝胶基质不能共存,导致加入后即产生浑浊沉淀,但由于西药成分与中药具有协同作用,能显著起到增强疗效的作用,故而还不得不加,于是漫长的工艺尝试过程展开了,好在黄天不负有心人,问题终于解决了,跟大家分享一下! 概念:凝胶剂是指药物与能形成凝胶的辅料制成均一、混悬或乳状液形的稠厚液体或半固体制剂。凝胶剂有油性和水性之分。水性凝胶剂基质一般由水、甘油或丙二醇与卡波姆、纤维素衍生物等构成。水性凝胶剂是近年来发展较快的剂型,因其具有美观、使用舒适、生物利用度高、稳定性好、不良反应少、不污染衣着等优点。卡波姆基质是水性凝胶剂最常用的基质,此基质对酸、碱、醇都有一定的耐受性;能耐受低温贮存和高压湿热灭菌,但不能耐受盐类;有良好的生物相容性,对眼睛和皮肤没有刺激。 仪器:烧杯、玻璃棒、电子天平、电热磁力搅拌器 配方:卡波姆(基质)、三乙醇胺(成胶碱)、甘油(保湿剂)、乙醇、水(溶剂)、吐温-80(增溶剂)、亚硫酸氢钠(抗氧化剂)、乙二胺四乙酸二钠、中药浸膏、醋酸氯己定。 最初制备工艺:取处方量亚硫酸氢钠、乙二胺四乙酸二钠溶解于适量水中,搅拌下加入处方量卡波姆,继续搅拌至溶胀均匀;取处方量的醋酸氯己定搅拌溶解于与乙醇中,加入处方量甘油、搅拌均匀,加入剩余量的水,搅拌均匀,将此溶液加入到卡波姆溶胀物中,搅匀,加入处方量的中药浸膏,加入处方量三乙醇胺,搅拌均匀。 最初的工艺中当醋酸氯己定溶液加入卡波姆中即刻会产生浑浊现象,为解决问题,我们查阅了大量的关于醋酸氯己定的卡波姆凝胶,但文献报道也不尽相同,有的文献的处方工艺加入顺序也是如此但未谈及沉淀问题,有的文献配方加入顺序有所不同,于是我们尝试了其他的加入顺序。 在配方工艺研究中我们按照文献的方法,先将三乙醇胺加入溶胀好的卡波姆基质中形成凝胶,然后再加入醋酸氯己定溶液,令人头疼的是,沉淀又产生了。没办法,接着尝试,我们将加入顺序重新组合…毫不夸张的说,我们已经将所有可能的加入顺序都尝试了,结果仍无济于事。 经一些专业论坛查询,这种情况不只发生在我们头上,挺多人都遇到了这种麻烦,但并未得到解决。卡波姆为交联聚丙烯酸树脂,显酸性,醋酸氯己定为胍类消毒剂,为碱性,两者混合后会发生反应。看来只有另辟蹊径了。 恰好实验室有人做挥发油的包合试验,因为挥发油气味比较刺激,影响口服效果,所以将其包合,掩盖不良气味。于是我们突发奇想,为什么不将醋酸氯己定包合上再加入卡波姆基质中呢,这样就可以避免两者的直接总接触了。 包合我们采用的是倍他环糊精,考虑到醋酸氯己定的分子量较大,包合比较困难,我们加大了环糊精的比例,摩尔比例为10:1,条件为40℃水浴加热2个小时。经包合后的醋酸氯定溶液再加入到卡波姆基质中,结果真的变好了。功夫不负有心人,问题最终得到了解决。 只是把这次试验的经历大致叙述了出来,描述有些拖沓,请大家见谅,试验总会有问题出现,只要大家不气馁,多思考,多尝试,总会找到解决的办法,可能试验对大家不会有什么帮助,但希望解决问题的思路会对大家有些启发。