一、实验目的1. 了解凝胶层析的原理及其应用。2. 通过测定蛋白质分子量的训练,初步掌握凝胶层析技术。二、实验原理凝胶层析又称排阻层析,凝胶过滤,渗透层析或分子筛层析等。它广泛地应用于分离、提纯、浓缩生物大分子及脱盐、去热源等,而测定蛋白质的分子量也是它的重要应用之一。凝胶是一种具有立体网状结构且呈多孔的不溶性珠状颗粒物质。用它来分离物质,主要是根据多孔凝胶对不同半径的蛋白质分子(近于球形)具有不同的排阻效应实现的。亦即它是根据分子大小这一物理性质进行分离纯化的。分离原理参见“理论部分的凝胶层析一节”。对于某种型号的凝胶,一些大分子不能进入凝胶颗粒内部而完全被排阻在外,只能沿着颗粒间的缝隙流出柱外;而一些小分子不被排阻,可自由扩散,渗透进入凝胶内部的筛孔,尔后又被流出的洗脱液带走。分子越小,进入凝胶内部越深,所走的路程越多,故小分子最后流出柱外,而大分子先从柱中流出。一些中等大小的分子介于大分子与小分子之间,只能进入一部分凝胶较大的孔隙,亦即部分排阻,因此这些分子从柱中流出的顺序也介于大、小分子之间。这样样品经过凝胶层析后,分子便按照从大到小的顺序依次流出,达到分离的目的。凝胶层析分离原理示意动画。对于任何一种被分离的化合物在凝胶层析柱中被排阻的范围均在0~100%之间,其被排阻的程度可以用有效分配系数Kav(分离化合物在内水和外水体积中的比例关系)表示,Kav值的大小和凝胶柱床的总体积(Vt)、外水体积(V0)以及分离物本身的洗脱体积(Ve)有关:Kav = (Ve-V0)/(Vt-V0) ----------- (1)在限定的层析条件下,Vt和V0都是恒定值,而Ve是随着分离物分子量的变化而改变。分子量大,Ve值小,Kav值也小。反之,分子量小Ve值大,Kav值大。有关凝胶层析柱中凝胶自身(基质)体积(Vg)、外水体积(V0)、内水体积(Vi)及柱床总体积(Vt)的参见示意图。凝胶层析柱中的几种层析峰。有效分配系数Kav是判断分离效果的一个重要参数,同时也是测定蛋白质分子量的一个依据。在相同层析条件下,被分离物质Kav值差异越大,分离效果越好。反之,分离效果差或根本不能分开。在实际的实验中,我们可以实测出Vt、V0及Ve的值,从而计算出Kav的大小。对于某一特定型号的凝胶,在一定的分子量范围内,Kav与logMw (Mw表示物质的分子量) 成线性关系:Kav =-b logMw + C --------- (2)其中 b,C为常数。同样可以得到:Ve =-b'logMw + C' --------- (3)其中 b', C'为常数。即 Ve 与 logMw 也成线性关系。我们可以通过在一凝胶柱上分离多种已知分子量的蛋白质后,并根据上述的线性关系绘出标准曲线,然后用同一凝胶柱测出其它未知蛋白的分子量。三、器材与试剂(一)器材1. 玻璃层析柱((20mm×60cm)2. 恒流泵(或下口恒压贮液瓶)3. 自动部分收集器4. 紫外分光光度计5. 100ml试剂瓶6. 1000ml量筒7. 250ml烧杯8. 50ml、100ml烧杯9. 10ml(或5ml)刻度试管(二)试剂1. 标准蛋白(1)牛血清白蛋白:Mw=67,000(上海生化所)(2)鸡卵清清蛋白:Mw=45,000(美国SIGMA公司)(3)胰凝乳蛋白酶原A:Mw=24,000(美国SIGMA公司)(4)溶菌酶:Mw =14,3002. 未知蛋白质样品:由实验室准备3. 0.025M KCl-0.1M HAC(乙酸)(洗脱液1000ml)4. 蓝色葡聚糖-2000
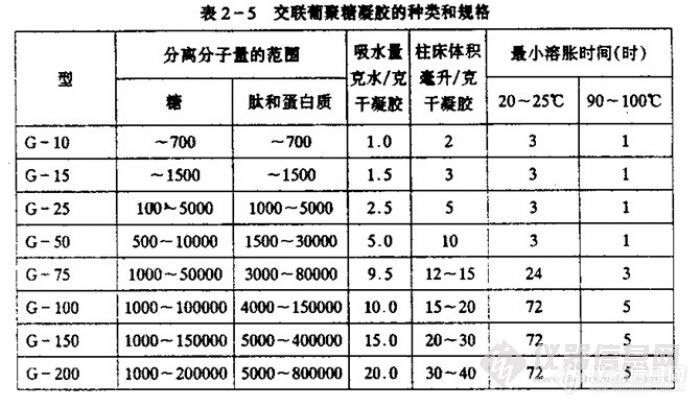
在一定的温度下,同一化学物质在不相混溶的两种介匝间分布达平街时.该物质在这两种介质中的浓度比是一常数.称分配系数。不同化学物质的分配系数不同。层析法即利用混合物中各组分的分配系数不同而崖其分离的方法。其两种介质,一为固定不动,称固定相,另一为可相对流动,称流动相。 层析法已广泛应用在生物化学领域中,无论是少量分析还是大量制备,都能体现出它的高效性,简便性等特点。在实脸室中的常用层析法有:凝胶过滤,纸层析.薄层层析,离子交换层析,亲和层析,高效液相层析等。 以下介绍几种常用的层析法凝胶过滤 凝胶过滤的别名很多,如凝皎扩散层析,分子筛层析,排阻层析等。这种技术具有操作简便,回收率高(近100%),条件缓和等特点,但它的分离操作速度较慢。该法常用于蛋白质,多糖,核酸的分离纯化。 凝胶过滤的分离过程是在装有多孔物质填料的柱中进行的。柱的总体积为VA,它包括填料的骨架体积VGM。,填料的孔体积Vi(内水体积)及填料颗粒间的体积VO(外水体积)。分布在填料的孔中的溶剂是固定相,分布的填料颗粒间的溶剂是流动相。填料颗粒含有许多不同大小的孔.如果待分离的物质分子大小合适,则可以不同程度地向孔中扩散,大分子物质只能占有较少的大孔,小分子则能占有大孔及另外一些小孔。所以当不同分子量物质的混合物流经凝胶柱时,较小的分子在柱中停留的时间比大分于停留的时间长,于是混合物中各组分即按分于大小分开,最先流出的是最大的分子。示意图如下所示,http://ng1.17img.cn/bbsfiles/images/2010/10/201010171831_251966_1638724_3.jpg用于生物材料分离的凝胶主要有交联葡聚糖凝胶(商品名为Sephadex),聚丙烯酰胺凝胶(商品名为Bio—Gel),琼脂糖凝胶(商品名Sepharose)等。如常用的交联葡聚糖是将葡聚糖(Dextran)悬浮于有机溶剂,加入交联剂表氯醇交联聚合而成多糖链的三维结构,这种聚合物为白色珠状微粒,是多孔性网状结构,凝胶的孔径大小与交联剂的量有关,交联剂多则交联度大,网状结构紧密,孔径小,反之交联剂少则孔径大。 将含有三种不同分子量物质的混合样品用某种规格的凝胶柱进行分离。首先将样品小心自柱顶端加入,洗脱,以分步收集器收集洗脱液,测定每管物质浓度,然后以洗脱体积为横坐标,各物质浓度为纵坐标即得如下的洗脱曲线:由图可见最先流出的物质是,A,它的分子量最大,大于该种凝胶的排阻限(A物质分子的直径大于凝胶的孔径),完全不能进入颗粒内部,只能从颗粒间隙流过,称“全排阻”。其流经体积最小,与外水体积VO相等。最后流出的物质是C,它的分子量最小,小于该种凝胶的渗入限,其分子可以自由进出凝胶颗粒,这叫“全渗入”。流经体积是外水体积VO与内水体积Vi的和。而物质B的分子量介于排阻限与渗入限之间,其分子能够部分地进入凝胶颗粒之中,不能全部地不受限制的通过,这叫做“部分排阻”或“部分渗入”。它的流经体积Ve是全部外水体积加上内水体积的一部分,即 Ve=VO+KdVi式中Kd称作“排阻系数”或“分配系数”。它反映了物质分子进入凝胶颗粒的程度。Kd=(Ve-VO)/Vi当Kd=1时,Ve=VO+Vi为全渗入。当Kd=0时,Ve=VO为全排阻。当0t,则说明该物质分子与凝胶有吸附作用。这三种物质的分离过程可见示意图如下:http://ng1.17img.cn/bbsfiles/images/2010/10/201010171832_251967_1638724_3.jpgVi也可通过计算求出:Vi=aWra=凝胶千重Wi=每克干凝胶吸水毫升数Vt=Vo+Vi+VgVg=凝胶骨架体积Vt=可通过测定层析柱内径及高度计算得出:Vt=1/4D2h下表为交联葡聚糖凝胶的种类和规格:http://ng1.17img.cn/bbsfiles/images/2010/10/201010171832_251968_1638724_3.jpg
[转贴]凝胶层析法技术简介凝胶层析法技术凝胶层析又称分子筛过滤、排阻层析等。它的突出优点是层析所用的凝胶属于惰性载体,不带电荷,吸附力弱,操作条件比较温和,可在相当广的温度范围下进行,不需要有机溶剂,并且对分离成分理化性质的保持有独到之处。对于高分子物质有很好的分离效果。 1. 凝胶的选择 根据实验目的不同选择不同型号的凝胶。如果实验目的是将样品中的大分子物质和小分子物质分开,由于它们在分配系数上有显著差异,这种分离又称组别分离,一般可选用Sephadex G-25和G-50,对于小肽和低分子量的物质(1000-5000)的脱盐可使用Sephadex G-10,G-15及Bio-Gel-p-2或4。如果实验目的是将样品中一些分子量比较近似的物质进行分离,这种分离又叫分级分离。一般选用排阻限度略大于样品中最高分子量物质的凝胶,层析过程中这些物质都能不同程度地深入到凝胶内部,由于Kd不同,最后得到分离。 2. 柱的直径与长度 根据经验,组别分离时,大多采用2-30cm长的层析柱,分级分离时,一般需要100cm左右长的层析柱,其直径在1-5cm范围内,小于1cm产生管壁效应,大于5cm则稀释现象严重。长度L与直径D的比值L/D一般宜在7-10之间,但对移动慢的物质宜在30-40之间。 3. 凝胶柱的制备 凝胶型号选定后,将干胶颗粒悬浮于5-10倍量的蒸馏水或洗脱液中充分溶胀,溶胀之后将极细的小颗粒倾泻出去。自然溶胀费时较长,加热可使溶胀加速,即在沸水浴中将湿凝胶浆逐渐升温至近沸,1-2小时即可达到凝胶的充分胀溶。加热法既可节省时间又可消毒。 凝胶的装填:将层析柱与地面垂直固定在架子上,下端流出口用夹子夹紧,柱顶可安装一个带有搅拌装置的较大容器,柱内充满洗脱液,将凝胶调成较稀薄的浆头液盛于柱顶的容器中,然后在微微地搅拌下使凝胶下沉于柱内,这样凝胶粒水平上升,直到所需高度为止,拆除柱顶装置,用相应的滤纸片轻轻盖在凝胶床表面。稍放置一段时间,再开始流动平衡,流速应低于层析时所需的流速。在平衡过程中逐渐增加到层析的流速,千万不能超过最终流速。平衡凝胶床过夜,使用前要检查层析床是否均匀,有无“纹路”或气泡,或加一些有色物质来观察色带的移动,如带狭窄、均匀平整说明层析柱的性能良好,色带出现歪曲、散乱、变宽时必须重新装柱。 4. 加样和洗脱 凝胶床经过平衡后,在床顶部留下数亳升洗脱液使凝胶床饱和,再用滴管加入样品。一般样品体积不大于凝胶总床体积的5%-10%。样品浓度与分配系数无关,故样品浓度可以提高,但分子量较大的物质,溶液的粘度将随浓度增加而增大,使分子运动受限,故样品与洗脱液的相对粘度不得超过1.5-2。样品加入后打开流出口,使样品渗入凝胶床内,当样品液面恰与凝胶床表面相平时,再加入数毫升洗脱液中洗管壁,使其全部进入凝胶床后,将层析床与洗脱液贮瓶及收集器相连,预先设计好流速,然后分部收集洗脱液,并对每一馏份做定性、定量测定。 5. 凝胶柱的重复使用、凝胶回收与保存 一次装柱后可以反复使用,不必特殊处理,并不影响分离效果。为了防止凝胶染菌,可在一次层析后加入0.02%的叠氮钠,在下次层析前应将抑菌剂除去,以免干扰洗脱液的测定。 如果不再使用可将其回收,一般方法是将凝胶用水冲洗干净滤干,依次用70%、90%、95%乙醇脱水平衡至乙醇浓度达90%以上,滤干,再用乙醚洗去乙醇、滤干、干燥保存。湿态保存方法是凝胶浆中加入抑菌剂或水冲洗到中性,密封后高压灭菌保存。 6. 凝胶层析的应用 ⑴ 脱盐:高分子(如蛋白质、核酸、多糖等)溶液中的低分子量杂质,可以用凝胶层析法除去,这一操作称为脱盐。本法脱盐操作简便、快速、蛋白质和酶类等在脱盐过程中不易变性。适用的凝胶为SephadexG-10、15、25或Bio-Gel-p-2、4、6。柱长与直径之比为5-15,样品体积可达柱床体积的25%-30%,为了防止蛋白质脱盐后溶解度降低会形成沉淀吸附于柱上,一般用醋酸铵等挥发性盐类缓冲液使层析柱平衡,然后加入样品,再用同样缓冲液洗脱,收集的洗脱液用冷冻干燥法除去挥发性盐类。 ⑵ 用于分离提纯:凝胶层析法已广泛用于酶、蛋白质、氨基酸、多糖、激素、生物碱等物质的分离提纯。凝胶对热原有较强的吸附力,可用来去除无离子水中的致热原制备注射用水。 ⑶ 测定高分子物质的分子量:用一系列已知分子量的标准品放入同一凝胶柱内,在同一条件下层析,记录每一分钟成分的洗脱体积,并以洗脱体积对分子量的对数作图,在一定分子量范围内可得一直线,即分子量的标准曲线。测定未知物质的分子量时,可将此样品加在测定了标准曲线的凝胶柱内洗肿后,根据物质的洗脱体积,在标准曲线上查出它的分子量。⑷ 高分子溶液的浓缩:通常将SephadexG-25或50干胶投入到稀的高分子溶液中,这时水分和低分子量的物质就会进入凝胶粒子内部的孔隙中,而高分子物质则排阻在凝胶颗粒之外,再经离心或过滤,将溶胀的凝胶分离出去,就得到了浓缩的高分子溶液。
实验七 葡聚糖凝胶层析脱盐一. 目的学习凝胶层析的工作原理和操作方法掌握利用葡聚糖凝胶层析进行蛋白质脱盐的技术二. 原理凝胶层析又称凝胶过滤或排阻层析。凝胶过滤的主要装置是填充有层析介质的层析柱。1. 层析介质的特点(1)遇水为不溶解的固相;(2)是化学惰性物质;(3)离子基团含量少;(4)颗粒大小和网眼均匀;(5)机械强度较强;(6)具有可选择的多种孔径。目前使用较多的是葡聚糖凝胶、聚丙烯酰胺凝胶、琼脂糖凝胶及其衍生物。尤其葡聚糖凝胶(商品名称Sephadex)是最常用的层析介质。它是由一定平均分子量的葡聚糖和交联剂1-氯-2,3-环氧丙烷( )交联成的具有三维结构不溶于水的高分子化合物。调节葡聚糖和交联剂配比,可以获得网眼大小不同,型号各异的凝胶。当葡聚糖分子量越小,交联剂用量越大,则交联度越大,凝胶网眼越小,吸水量越小,G值也越小。G值表示每克干胶吸水量(mL)的十倍。例如Sephadex G-25其吸水量应为2.5mL/g干胶。常用的葡聚糖凝胶有多种规格,如G-10、G-15、G-25、G-50、G-75、G-100等。实验中选用何种型号应根据被分离的混合物分子的大小及工作目的来确定(参见附录五)。2. 分离原理当混合样液加到凝胶柱上,随着洗脱剂而通过凝胶柱时,分子大小不同的物质受到不同的阻滞作用。颗粒接近或大于网眼的分子,不能进入凝胶的网眼中,在重力作用下它们随着溶剂在凝胶颗粒之间沿较短流程向下流动,受到的阻滞作用小,移动速度快,先出层析柱(此现象叫作被排阻。被排阻的最小分子量称为该规格凝胶的排阻极限);而颗粒小于网眼的分子可渗入凝胶网眼之中,它们被洗脱时不断地从一个网眼穿到另一个网眼,逐层扩散,阻滞作用大,流程长,移动速度慢,因而后出层析柱。在层析柱的出口处,我们用多个试管分步收集洗脱液,就可将混合物中各组分彼此分离。当我们从生物组织中用盐析法提取蛋白质后,常需要进行蛋白质的脱盐工作,我们可采用层析介质为葡聚糖凝胶G-25(或G-15、G-50),用适当的洗脱剂进行洗脱,经凝胶层析,就可以将大分子蛋白质与小分子盐类分离。三. 实验材料及设备1. 材料含硫酸铵盐的蛋白质溶液(参见附注3)2. 器材层 析 柱:内径×柱高=1.0cm×25cm滴定台架、螺丝夹:各1刻度试管:10mL×14移 液 管:1mL×1烧 杯:250mL×1 50mL×1滴 管:2洗 耳 球:2洗瓶、试管架、移液管架、玻棒:各1四. 试剂的配制1. 葡聚糖凝胶G-25(或G-15、G-50)溶胀凝胶方法:按每个层析柱约4g的量称取葡聚糖凝胶G-25于烧杯中,加过量蒸馏水于沸水浴中溶胀2小时或在室温下溶胀6小时以上。用倾泻法除去上层漂浮的细碎凝胶,重复3~4次。操作中避免剧烈搅拌,防止破坏其交联结构。2. BaCl2溶液(1%)3. 考马斯亮蓝G-250称取0.1g考马斯亮蓝G-250,先溶于50mL95%乙醇中,再加入85%的磷酸100mL,最后用蒸馏水定容到1000mL。暗处存放。4. 脲(6mol/L)5. 洗脱剂应依据被纯化的蛋白质的不同特性而选用不同的缓冲液。五. 操作步骤1. 层析柱的准备(1) 清洗:每组取一支层析柱,用清水冲洗干净。(若玻璃柱较脏,应卸去塑料装置,先入洗液中浸泡2小时。)(2) 安装与检查:检查出口装置中尼龙绸或烧结滤板是否完好干净。安装层析柱,让其垂直固定于滴定台架上。对准出口处,放一只250mL烧杯。向层析柱内灌洗脱剂,打开出口螺旋夹,检查有无渗漏、出口乳胶管是否通畅等情况。(3) 排气泡:保持柱内一定的水位,用手指弹击柱壁,部分气泡会从溶液中上浮排出。出口处的小气泡易停留在螺旋夹附近的乳胶管内,要想法排尽,否则会影响分离结果,排气完毕,保留柱内1~2cm高水位,关紧螺旋夹。(4) 标记高度:在距顶端8~10cm处做一标记,作为衡量灌装层析介质床体高度(15~17cm)的依据。2. 装柱每组用50mL烧杯取溶胀的凝胶悬浆25~30mL,静置片刻,观察凝胶沉淀与水的体积之比,约为1:1即可,否则应作调整。轻轻搅匀杯中凝胶,用玻璃棒引流入柱,打开出水口,并不断地向柱内补充凝胶,直到凝胶沉淀高度位于标记上方约2cm为止,凝胶柱内若有气泡和断层或柱床表面干水和歪斜,都将影响分离效果。必要时,需倒出凝胶,重新装柱。3. 平衡取15mL洗脱剂,用滴管沿柱内壁旋转着缓缓流下,不可冲动胶平面,打开出水口,经洗脱液的流动,一方面清洗内壁,另一方面使胶床收紧。洗脱平衡完毕,胶床上方保留约4cm高水位,关闭出水口。此时,胶床高度≥15cm为宜。4. 准备收集取6只干净的刻度试管(除净试管内残留的水),1~6编号,并在试管2mL处作一标记,插入试管架上,为收集洗脱样品作好准备。5. 上样与收集打开出口排水,当胶床与上方水层的弯月面相切时,关闭出口,用滴管将0.2mL混合样液沿柱内壁缓缓加入,勿冲动胶面。上样完毕,打开出水口,开始收集一号管。每管收集洗脱液2mL。当样液进入胶床,其弯月面与胶平面相切时,暂停排液,用滴管将洗脱剂沿柱内壁旋转着加入1cm高水位,然后排液,至其弯月面与胶平面相切,再缓缓注入3~5cm高的洗脱剂。6. 洗脱不断向柱内加洗脱剂,保持胶床上水位3~5cm。出口流速控制在每6秒1滴,直至收集到6号管达2mL时,关闭出口。7. 鉴定另取6只干净试管,按收集顺序将洗脱液一分为二,即每管1mL,依次在试管架上排成二排。第一排每管加2滴BaCl2,根据白色沉淀多少,判断SO42-在各管中的浓度。第二排每管加1mL考马斯亮蓝G-250试剂,根据蓝色情况,判断蛋白质在各管中的浓度。将结果记录于下表中。若鉴定的第6号管中,仍有样品,表明洗脱和收集不够,需增加7号、8号……试管继续洗脱与收集,同上法鉴定其蛋白质和盐浓度情况。管 号项 目1234567891011白色沉淀量蓝色深浅8. 再生鉴定完毕,打开出水口,继续用2~3倍床体积洗脱剂洗脱,洗脱后关闭出口,以备下次使用。六. 结果处理1. 根据实验结果,在同一坐标系中,以收集的管号为横坐标,颜色深浅程度为纵坐标,绘制二条(蛋白质及(NH4)2SO4)洗脱曲线。2. 分析混合样品分离效果。七. 思考题1. 利用凝胶层析分离混合物时,怎样才能得到较好的分离效果?2. 还有哪些方法可进行蛋白质脱盐?附注1. 凝胶的再生通常层析柱经洗脱剂再生、平衡后,就可反复使用。但使用过多次后凝胶床体积变小,流速降低,凝胶污染杂质过多,甚至变色,需经再生后才可使用。再生方法有多种:如(1)用水进行逆向冲洗,再用洗脱剂平衡,便可重新使用。又如(2)把凝胶倒出,用6mol/L脲浸泡凝胶半小时,抽滤,再用水漂洗数次,除净脲,必要时重复上述操作即可重新使用。2. 凝胶的保存(1) 湿法保存,可保存几个月至一年,有多种方法: 加入防腐剂硫柳汞,使其浓度为0.005%,下次使用前,水洗除去硫柳汞。 加入几滴氯仿,摇匀存放。下次使用前用热水浴除去氯仿。(沸点60℃)。 凝胶保存在60~70%乙醇溶液中,即凝胶以部分收缩状态保存。(2) 干法保存此法操作不及湿法简便,但处理得好,凝胶存放时间长。先抽取过量水分,再向凝胶逐步加入百分浓度递增的乙醇溶液,每次停留一段时间,使凝胶逐步脱水,最后加入95%乙醇,凝胶脱手收缩。抽干,铺与搪瓷盆中,60~80℃经常翻动烘烤。若有结块,在下次膨胀时会散开的,不可用力敲碎,否则会破坏颗粒结构。3. 用盐析法分离提取麦清蛋白取10g小麦种子,粉碎。转入250mL具塞磨口锥形瓶中。加100mL蒸馏水,在康氏震荡器上震荡1小时。静置半小时,上清液以3000转/分钟离心15分钟。将上清液在布氏漏斗上(铺3~4层滤纸)抽滤。滤液应透明。用醋酸酸化滤液至pH4.7。加等体积的饱和硫酸铵溶液,边加边搅动,即有白色絮状沉淀生成。置冰箱过夜,使麦清蛋白全部盐析沉淀出来,以3000转/分钟离心20分钟,弃去上清夜,加10mL无离子水使沉淀溶解,即得麦清蛋白和硫酸铵的混合液。
第一次做凝胶柱层析,想分离分子量 在100至5000之间的化合物,选择凝胶柱排阻范围为100-7000,因为没有在线检测器,上样以后,不知道什么时间段该收集样品,才能收集到分子量在100-7000之间的化合物,各位有经验的前辈指点我啊
我要测土壤中的抗生素含量,目前计划流程是这样的:提取——HLB固相萃取——凝胶层析——LC/MS/MS检测因为腐植酸会对色谱影响很大,所以有人建议我用分子排阻滤掉大分子,但是我能查到的资料都是用凝胶色谱测定大分子的,想知道如果我只是要层析分离不用测定,是不是也要用专门的凝胶色谱柱?还是买了填料自己做个层析柱就可以?自己做的话怎么控制洗脱时间?从来没接触过凝胶,还请大大们指点!
使用凝胶层析柱处理水产品,怎么做?凝胶用量?
[font=宋体]层析法无疑是下游处理中主要和常用的操作,因为层析法相比其他单元操作具有某些优势。例如层析法支持高分辨率的效率,可以分离分子性质非常相似的复杂粗制混合物。此外,层析法是生物工艺中遇到的稀释溶液中捕获分子的理想选择。[/font][font=宋体] [/font][font=宋体][font=宋体]柱色谱法[/font][font=Calibri]([/font][font=宋体]层析法[/font][font=Calibri])[/font][font=宋体]的原理是将一个大的蛋白池分离成许多小的蛋白池,其中一些富集了目标蛋白。虽然柱色谱法有昂贵的专业设备,但只需要基本的设备就可以了。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体]在所有色谱技术中,亲和层析法占主要地位。事实上,亲和层析是最特异、最有效的蛋白纯化技术,为靶蛋白纯化提供了合理的依据。它利用了生物分子识别的原理,即生物活性大分子与亲和配体形成特定的可逆复合物的能力。随着高价值蛋白的传统纯化方案被基于亲和色谱等先进的方法所取代,人们的关注重点转向了设计和选择具有高亲和力和特异性的配体。[/font][font=宋体] [/font][font=宋体]从用于生化表征的浓缩蛋白提取物的制备到治疗性重组蛋白的大规模生产,任何纯化过程都需要经济且足量地获得纯化蛋白。因此,下游处理面临的挑战是高产能、高分辨率和高成本效率。[/font][font=宋体] [/font][font=宋体]亲和层析法适用于基于高特异性相互作用的生化混合物的分离。在纯化过程中可以利用具有明确特性的靶蛋白。[/font][font=宋体] [/font][font=宋体][url=https://cn.sinobiological.com/resource/protein-review/protein-purification-by-iec][b]离子交换层析法[/b][/url]是一种常见的蛋白纯化方法,该方法基于与离子交换器的亲和力分离离子和极性分子。可溶性分子在通过色谱柱时与带相反电荷的不溶性固定相结合。[/font][font=宋体] [/font][font=宋体]尺寸排阻色谱法,根据分子的大小和分子量分离分子。[/font][font=宋体] [/font][font=宋体]疏水作用层析分离表面有疏水氨基酸侧链的靶蛋白,与疏水基团相互作用并结合在一起。[/font][font=宋体] [/font][font=宋体]蛋白纯化的原理为:不同蛋白质的氨基酸序列及空间结构不同,导致其在物理、化学、生物学等性质上存在差异,利用待分离蛋白质与其它蛋白质性质上的差异,即可以设计出一套合理的蛋白纯化方案。[/font][font=宋体] [/font][font=宋体][font=宋体]蛋白的纯化大致分为粗分离阶段和精细纯化阶段两个阶段。粗分离阶段主要将目的蛋白和其他细胞成分如[/font][font=Calibri]RNA[/font][font=宋体]、[/font][font=Calibri]DNA[/font][font=宋体]等分开,常用的方法为硫酸铵沉淀法。精细纯化阶段的目的是把目的蛋白与其他大小及理化性质接近的蛋白区分开来,[b]常用的方法有:凝胶过滤层析、离子交换层析、疏水层析、亲和层析等。[/b][/font][/font][font=宋体] [/font][font=宋体][b]凝胶过滤层析[/b][/font][font=宋体]凝胶过滤(也叫排阻层析或分子筛)是一种根据分子大小从混合物中分离蛋白质的方法。不同蛋白的形状及分子大小存在差异,在混合物通过含有填充颗粒的凝胶过滤层析柱时,由于各种蛋白的分子大小不同,扩散进入特定大小孔径颗粒内的能力也各异,大的蛋白分子会被先洗脱出来,分子越小,越晚洗脱,从而达到分离蛋白的目的。一般来说,凝胶过滤层析柱越细、越长纯化的效果越好。凝胶过滤层析详细介绍[/font][font=宋体] [/font][font=宋体]凝胶过滤层析所能纯化的蛋白分子量范围很宽,纯化过程中也不需要能引起蛋白变性的有机溶剂。缺点是所用树脂有轻度的亲水性,电荷密度较高的蛋白容易吸附在上面,不适宜纯化电荷密度较高的蛋白。[/font][font=宋体] [/font][font=宋体][b]离子交换层析[/b][/font][font=宋体][font=宋体]离子交换层析是一种依据蛋白表面所带电荷量不同进行蛋白分离纯化的技术。蛋白表面通常会带有一定的电荷,电荷的氨基酸残基均匀地分布在蛋白质的表面,在一定条件下可以与阳离子交换柱或阴离子交换柱结合。这种带电分子与固定相之间的结合作用是可逆的,在改变[/font][font=Calibri]pH[/font][font=宋体]或者用逐渐增加离子强度的缓冲液洗脱时,离子交换剂上结合的物质可与洗脱液中的离子发生交换而被洗脱到溶液中。由于不同物质的电荷不同,其与离子交换剂的结合能力也不同,所以被洗脱到溶液中的顺序也不同,从而达到分离的效果。[/font][/font][font=宋体] [/font][font=宋体][b]亲和层析[/b][/font][font=宋体][url=https://cn.sinobiological.com/resource/protein-review/protein-purification-by-ac][b]亲和层析纯化[/b][/url]是利用生物大分子物质具有与某些相应的分子专一性可逆结合的特性进行蛋白纯化的技术。该方法适用于从成分复杂且杂质含量远大于目标物的混合中提纯目标物,具有分离效果好、分离条件温和、结合效率高、分离速度快的优点。亲和层析技术可以利用配基与生物分子间的特异性吸附来分离蛋白,也可以在蛋白上加入标签,利用标签与配基之间的特异性结合来纯化蛋白。[/font][font=宋体] [/font][font=宋体][b]疏水作用层析[/b][/font][font=宋体][font=宋体]疏水作用层析是利用盐[/font][font=Calibri]-[/font][font=宋体]水体系中样品分子的疏水基团和层析介质的疏水配基之间疏水力的不同而进行分离的一种层析方法。该法利用了蛋白的疏水性,蛋白经变性处理或处于高盐环境下疏水残基会暴露于蛋白表面,不同蛋白疏水残基与固定相的疏水性配体之间的作用强弱不同,依次用从高至低离子强度洗脱液可将疏水用作由弱至强的组分分离。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]更多详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/chromatography-purification[/font][/font]
[b]1.凝胶的预处理[/b] 交联葡聚糖凝胶的市售商品多为干燥颗粒,使用前必须充分溶胀。方法是将欲使用的干凝胶缓慢地倾倒入5~10倍的去离子水中,参照相关资料中凝胶溶胀所需时间,进行充分浸泡,然后用倾倒法除去表面悬浮的小颗粒,并减压抽气排除凝胶悬液中的气泡,准备装柱。在许多情况下,也可采用加热煮沸方法进行凝胶溶胀,此法不仅能加快溶胀速率,而且能除去凝胶中污染的细菌,同时排除气泡。表 凝胶型号和层析柱大小与规格及凝胶用量[table][tr][td=3,1,236]层析柱规格[/td][td=4,1,285]凝胶的规格和用量(g)[/td][/tr][tr][td=1,1,70]直径(cm)[/td][td=1,1,70]高(cm)[/td][td=1,1,97]容量(ml)[/td][td=1,1,52]G[sub]25[/sub][/td][td=1,1,78]G[sub]50[/sub][/td][td=1,1,78]G[sub]100[/sub][/td][td=1,1,77]G[sub]200[/sub][/td][/tr][tr][td=1,1,70]0.9[/td][td=1,1,70]15[/td][td=1,1,97]9.5[/td][td=1,1,52]2.5[/td][td=1,1,78]1[/td][td=1,1,78]0.6[/td][td=1,1,77]0.3[/td][/tr][tr][td=1,1,70]0.9[/td][td=1,1,70]30[/td][td=1,1,97]19[/td][td=1,1,52]5[/td][td=1,1,78]2[/td][td=1,1,78]1.2[/td][td=1,1,77]0.6[/td][/tr][tr][td=1,1,70]0.9[/td][td=1,1,70]60[/td][td=1,1,97]38[/td][td=1,1,52]10[/td][td=1,1,78]4[/td][td=1,1,78]2.5[/td][td=1,1,77]1.2[/td][/tr][tr][td=1,1,70]1.6[/td][td=1,1,70]20[/td][td=1,1,97]40[/td][td=1,1,52]10[/td][td=1,1,78]4[/td][td=1,1,78]2.5[/td][td=1,1,77]1.2[/td][/tr][tr][td=1,1,70]1.6[/td][td=1,1,70]40[/td][td=1,1,97]80[/td][td=1,1,52]20[/td][td=1,1,78]8[/td][td=1,1,78]5.0[/td][td=1,1,77]2.4[/td][/tr][tr][td=1,1,70]1.6[/td][td=1,1,70]70[/td][td=1,1,97]140[/td][td=1,1,52]35[/td][td=1,1,78]14[/td][td=1,1,78]9.0[/td][td=1,1,77]4.4[/td][/tr][tr][td=1,1,70]1.6[/td][td=1,1,70]100[/td][td=1,1,97]200[/td][td=1,1,52]50[/td][td=1,1,78]20[/td][td=1,1,78]12.5[/td][td=1,1,77]6[/td][/tr][tr][td=1,1,70]2.6[/td][td=1,1,70]40[/td][td=1,1,97]210[/td][td=1,1,52]50[/td][td=1,1,78]20[/td][td=1,1,78]12[/td][td=1,1,77]7[/td][/tr][tr][td=1,1,70]2.6[/td][td=1,1,70]70[/td][td=1,1,97]370[/td][td=1,1,52]90[/td][td=1,1,78]35[/td][td=1,1,78]20[/td][td=1,1,77]12[/td][/tr][tr][td=1,1,70]2.6[/td][td=1,1,70]100[/td][td=1,1,97]530[/td][td=1,1,52]130[/td][td=1,1,78]50[/td][td=1,1,78]30[/td][td=1,1,77]17[/td][/tr][/table][b]2.装柱[/b] 层析柱的选择一般根据分离样品的种类和样品的数量而定。纯化蛋白质时,柱床体积应为样品体积的25~100倍。去除盐及游离荧光素约为样品体积的4~10倍。柱太短,影响分离效果。柱长一些,分离效果好,但柱太长,则延长分离时间,样品也稀释过度。层析柱的内径也要选择适当。内径过细,会发生“器壁效应”,即靠近管壁的流速要大于中心的流速影响分离效果。所以层析柱的内径和高度应有一定的比例。对于除盐来说应为1︰5~1︰25;对于纯化蛋白质来说应为1︰20~1︰100。 凝胶柱的装填方法和要求,基本上与离子交换柱的制备相同。一根理想的凝胶柱要求柱中的填料(凝胶)密度均匀一致,没有空隙和气泡。通常新装的凝胶柱用适当的缓冲溶液平衡后,将带色的兰葡聚糖–2000、细胞色素,或血红蛋白等物质配制成质量浓度为2g/L的溶液过柱,观察色带是否均匀下移,以鉴定新装柱的技术质量是否合格,否则,必须重新装填。
[font=宋体]在生物科学领域,蛋白质纯化是一项关键的技术,它对于研究生物分子的结构和功能至关重要。凝胶过滤层析是一种常用的蛋白质纯化技术,它具有分辨率高、分离效果好的优点。本文将介绍用凝胶过滤层析进行蛋白纯化的流程,包括实验准备、样品处理、层析柱的制作和上样、洗脱和收集等步骤。通过学习本文,读者可以了解凝胶过滤层析在蛋白纯化中的应用及其优缺点,为后续的实验和研究提供参考。[/font][font=宋体] [/font][b][font=宋体]用凝胶过滤层析进行蛋白纯化的流程,主要分为以下步骤:[/font][/b][font=宋体] [/font][font=宋体]准备凝胶柱:选择适当的凝胶材料和柱子,根据待纯化蛋白的分子大小选择合适的孔径。[/font][font=宋体]杂质去除:使用缓冲液预先洗脱凝胶,去除其中的杂质和阻塞物。[/font][font=宋体]样品加载:将待纯化的蛋白溶液加载到凝胶柱中,注意保持柱子的垂直姿势,防止样品泄漏。[/font][font=宋体]洗脱:使用缓冲液进行洗脱,以去除非目标蛋白和杂质。[/font][font=宋体]收集纯化蛋白:收集洗脱液,进行后续的分析或使用。[/font][font=宋体] [/font][font=宋体]以上步骤只是粗略的概述,实际操作时还需要注意许多细节和技巧。例如,选择合适的凝胶类型和柱子对纯化效果有很大影响;样品加载时需要防止样品泄漏;洗脱时需要选择合适的缓冲液等。因此,建议在进行实验前仔细阅读相关文献和资料,并请教有经验的实验人员。[/font][font=宋体] [/font][font=宋体][b][font=宋体]凝胶过滤层析([/font][font=Calibri]Gel Permeation Chromatography[/font][font=宋体],[/font][font=Calibri]GPC[/font][font=宋体])具有以下优点:[/font][/b][/font][font=宋体] [/font][font=宋体][font=宋体]①操作条件温和:[/font][font=Calibri]GPC[/font][font=宋体]不需要使用有机溶剂等强烈的条件,因此对样品的活性影响较小。[/font][/font][font=宋体][font=宋体]②高分离效果:[/font][font=Calibri]GPC[/font][font=宋体]可以分离不同分子量的蛋白质,且分辨率较高,能够实现样品的较纯分离。[/font][/font][font=宋体][font=宋体]③重复性好:[/font][font=Calibri]GPC[/font][font=宋体]的层析柱可以重复使用,分离效果稳定,有利于提高实验的可重复性和数据可靠性。[/font][/font][font=宋体][font=宋体]④适用范围广:[/font][font=Calibri]GPC[/font][font=宋体]可用于各种生化物质,如肽类、激素、蛋白质、多糖、核酸等的分离纯化、脱盐、浓缩以及分析测定等。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]在应用方面,[/font][font=Calibri]GPC[/font][font=宋体]被广泛应用于蛋白质和其他生物分子的分离纯化。例如,从混合物中分离纯化蛋白质、去除蛋白质中的盐和缓冲剂、脱去多糖和脂质等杂质、对蛋白质进行分子量测定等。此外,[/font][font=Calibri]GPC[/font][font=宋体]还可以用于分离合成多肽和基因克隆产物的纯度鉴定等。[/font][/font][font=宋体] [/font][font=宋体]总之,凝胶过滤层析具有温和的操作条件、高分离效果、重复性好等优点,被广泛应用于蛋白质和其他生物分子的分离纯化。[/font][font=宋体] [/font][font=宋体][font=宋体]详情可以关注:义翘神州[url=https://cn.sinobiological.com/resource/protein-review/chromatography-purification][b]蛋白层析纯化[/b][/url][/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/chromatography-purification[/font][/font]
请教凝胶层析介质biogel P系列和superdex 30 的区别我想请教一下各位高手,我想分离分子量在一万以内的几个寡糖,想用凝胶层析分离,用bio gel P 系列还是用superdex 30 效果更好呢?这两种凝胶层析介质各有什么特点吗。还请大家多多指教。
(一)原理凡盐析所获得的粗制蛋白质(盐析得到的IgG)中均含有硫酸铵等盐类,这类将影响以后的纯化,所以纯化前均应除去,此过程称为“脱盐”(desalthing)。脱盐常用透析法和凝胶过滤法,这两种方法各有利弊。前者的优点是透析后析品终体积较小,但所需时间较长,且盐不易除尽;凝胶过滤法则能将盐除尽,所需时间也短,但其凝胶过滤后样品体积较大。所以,要根据具体情况选择使用。前实验中样品体积较小,凝胶达滤后样品体积不会太增加,所以选用凝胶过滤法。(二)试剂与器材(1)Sephadex G-25。(2)0.0175mol/L,pH6.7磷酸盐缓冲液。(3)奈氏(Nessler)试剂:于500ml锥形瓶内加入碘化钾150g,碘110g,汞150g及蒸馏水100ml。用力振荡7~15min,至碘的棕色开始转变时,混合液温度升高,将此瓶浸于冷水内继续振荡,直到棕色的碘转变为带绿色的碘化钾汞液为止。将上清液倾入2000ml量筒内,加蒸馏水至2000ml,混匀备用。(4)20%(W/V)磺基水杨酸溶液。(5)1.5cm×20cm层析柱。(6)黑、白比色磁盘。
请问关于“离子交换层析”中的问题,在玻璃层析柱中阳离子交换层析剂——羧甲基纤维素是以什么状态存在?凝胶状还是颗粒状?其在装柱的时候容易产生气泡,请问如何除泡?
第一次做凝胶柱层析,想分离分子量 在100至5000之间的化合物,选择凝胶柱排阻范围为100-7000,因为没有在线检测器,上样以后,不知道什么时间段该收集样品,才能收集到分子量在100-7000之间,上样以后,不知道什么时间段该收集样品,才能收集到分子量在100-7000之间的化合物,各位有经验的前辈指点我啊

[color=#d801e5][color=#dc143c][size=2]维权声明:本文为lily002原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现的,均属侵权违法行为,我们将追究法律责任。[/size][/color]大家好,我是凝胶色谱一名新手,以前常常在咱们论坛中学习和下载资料,看到论坛中轰轰烈烈的第三届原创大赛开始了,还有各位达人们的攻略、帮助,心里有点小激动呢~~~于是就拿出自己的一些实验和研究的东东来与大家分享!!说实话拿出来有点小担心,毕竟自己的水平不高拿出来有点献丑了!本着分享第一荣誉第二的原则,就硬着头皮绣出来了!!也希望大家轻拍哦![/color][align=center][color=#d40a00]===================================Show Time========================================[/color][/align] 我在本次试验中研究的是金属硫蛋白(Metallothionein, MT)又名金属组氨酸甲基内盐,是分子量较小,富含半胱氨酸的非酶蛋白质,其内含有镉、铜、锌、汞等金属元素,不含芳香组胺酸残基。MT与微量元素代谢、重金属解毒、自由基清除以及应急反应有关。是一种广泛存在于各种组织的蛋白质。这些蛋白具有很高的结构稳定性。分析不同的动物和不同的组织器官,发现MT氨基酸组成差异很小。在真菌和动物体内,MT能够缓解镉、汞等有害元素的毒害并在不同应激条件保护机体,被认为是和生物体解毒有关的蛋白,在脊椎动物,MT则被更多地认为和锌的储藏和代谢有关。最显著的功能是可消除体内过量的自由基、重金属及有害物质的污染。在如今环境污染日趋严重的情况下,这种能增强自 身抗污染能力的产品,将越来越为人们所需要。香菇多糖、糖蛋白及 其衍生物具有较强的保肝、抗衰老、增食欲等功效,它是一种有效的免疫激活剂和调节剂,能通过提高机体免疫功能,抑制癌细胞的生长 和扩大。 聚丙烯酰胺是以丙烯酰胺和甲撑双丙烯酰胺聚合而成的具有三维网状结构的凝胶,其孔径可调,性质稳定,无色透明。用聚丙烯酰胺凝胶作为电泳的支持物分离蛋白,具有分辨力高、酶活性影响小、显带效果好等优点,因此应用广泛。 近年来,河流湖泊及近海海域不同程度受到重金属的污染,镉被美国毒理委员会列为第6位危及人体健康的有害物质。镉(Cd)是人体非必需元素,在自然界中常以化合物状态存在,一般含量很低,在正常环境下,不会影响人体健康。镉被人体吸收后在体内形成了镉硫蛋白,选择性地储存于肾、肝中,其中肾脏可吸收进入人体近1/3的镉,是镉 中毒的“靶器官”。其它如脾、胰、甲状腺和毛发等也有一定量的积蓄。镉在体内可与含羟基、氨基、硫基的蛋白质分子结合,使许多酶系统受到抑制,从而影响到肝、肾器官中酶系统的正常功能。由于镉损伤肾小管,病者出现糖尿、蛋白尿和氨基酸尿,特别是使骨骼的代谢受阻,造成骨质酥松,萎缩,变形等症状。 本实验通过体外暴露氯化镉染毒法处理长江华溪蟹,对华溪蟹的蛋白进行SDS-PAGE电泳,得到相应的分子量,并通过紫外分光光度计对华溪蟹体内的金属硫蛋白进行鉴定。 [b]一、实验材料和仪器[/b] 1.材料:华溪蟹于家门口的水场市场购回,先在实验室的饲养池中用清水驯养数天,不喂任何食物,选取大小均等、重量相似的个体进行染毒处理。 2.部分主要仪器:高速冷冻离心机Centrifuge 5804R(eppendorf),高速台式离心机 Centrifuge 5415D(eppendorf),恒温水浴锅,循环水式多用真空泵,超低温冰箱MDF-U50V(日本SANYO),国产凝胶柱(上海华美实验仪器厂,26*100),SephadexG-50(Amerchsham),AKTA Prime蛋白纯化系统(Amersham),UV-2102 PC型紫外可见分光光度计(UNICOTM) [b]二、 实验过程:[/b] 1.体外镉暴露法染毒 因为镉对金属硫蛋白有高度的诱导作用,所以在的、高镉环境中可以诱导华溪蟹的金属硫蛋白的产生。[14] 通过查阅资料及进行预实验,最终确定染毒的镉溶液浓度为58mg/l染毒时间为30h提取组织为肝胰腺。实验华溪蟹的解剖,用镊子将华溪蟹从染毒缸中取出,用清水冲洗干净,在解剖盘中先将其附肢剪掉,然后打开蟹壳,腮为半片状,分布在两侧,可以很轻易的取出,卵巢分布在中后部,颜色为亮黄色,颗粒状,用镊子可以方便取出,肝胰腺在卵巢和心脏的下面,将心脏剥离后向下夹入便可夹出整个肝胰腺,其呈暗黄色,絮状,从华溪蟹的螯中取出肌肉,先将其剪开,再用手术刀从螯壁上刮下肌肉组织,其半透明粘性大。 2. MT粗提取的制备 取染毒华溪蟹的肝胰腺,按每克湿组织用3ml0.02mol/lTris-Hcl缓冲液(pH8.6)在玻璃研钵中充分匀浆,将匀浆液放入-800C的冰箱中保存备用。 3. Sephadex G-50凝胶柱的制备 (1)凝胶柱的清洗 将购买国产凝胶柱(26*100)用70%浓盐酸浸泡过夜,用洗衣粉水浸泡,冲洗,最后用去离子水冲洗干净。 (2)凝胶填料的溶胀 商品凝胶是干燥的颗粒状固体,将凝胶均匀铺洒在干净并且干燥的烧杯内,缓缓家入超纯水,使其溶胀.待凝胶体积超过烧杯容积1/2后,将一般凝胶转移至另一干净烧杯,防止凝胶溢出.用封口膜封住烧杯放2d,然后将烧杯放入真空泵抽滤2d,排除凝胶中的气泡. (注意在凝胶溶胀和处理凝胶悬浮液的整个过程中,不能进行激烈的搅拌,这样会使凝胶颗粒破碎而产生碎片,以至影响层析的流速,在处理凝胶时,严禁使用电磁搅拌,它会象磨一样,在很短时间内把凝胶碾碎.) (3)凝胶柱的装填 把凝胶柱竖直固定好(有滤膜的一端为底部),用Ph8.6Tris-Hcl缓冲液润洗后加入柱体积1/3Tris-Hcl缓冲液,将少量凝胶转移至小烧杯中家Tris-Hcl缓冲液,用玻璃棒轻轻搅拌均匀,并观察凝胶是否有不均匀处(若有不均匀处,可将不均匀凝胶重新搅拌使重新沉降),然后用玻璃帮引流到凝胶柱内并不停地轻轻搅拌使凝胶均匀沉降,直至凝胶沉降至柱顶约10cm处,加Tris-Hcl缓冲液至柱顶,盖好柱顶螺帽,并将凝胶柱与蛋白纯化系统连接好,用Tris-Hcl缓冲液反复洗脱. (4)Sephadex G50 凝胶层析分离纯化MT 将装着已提取的染毒华溪蟹组织的EP管从冰箱中取出解冻,把组织倒入研钵加入1.5mlTris-Hcl缓冲液,充分研磨,将样品转至5mlEP管中,把EP管插在漂浮板上,放入80℃恒温水浴锅5min,取出后抽去表层脂肪,上样. (5)洗脱峰紫外光谱扫描分析 (6)洗脱峰SDS-PAGE分析 [b]三、实验结果与分析[/b] 1.SephdexG50凝胶层析分离纯化MT[img]http://ng1.17img.cn/bbsfiles/images/2010/07/201007291845_233096_1917139_3.jpg[/img] 图1为匀浆热沉淀处理上样经SephadexG-50凝胶柱层析图,洗脱液为0.01mol/L Tris-Hcl缓冲液,pH为8.60,洗脱速度为0.5ml/min,在254nm处检测吸光度,结果显示,层析后样品分为Ⅰ,Ⅱ两个峰. 2. 洗脱峰紫外光谱扫描分析 由于金属硫蛋白中不含有芳香族氨基酸,所以在紫外不能形成280nm特征光谱.但是由于金属硫蛋白在二级结构中形成特征性的巯基金属簇,而导致在紫外光谱中出现对应于金属簇结构的特殊吸收峰,吸收峰的位置主要决定于金属的种类,如:镉硫金属簇的吸收位于250nm附近,而锌硫金属簇的吸收峰位于225nm附近. 将接收峰Ⅰ,Ⅱ分别在190nm-300nm扫描。[img]http://ng1.17img.cn/bbsfiles/images/2010/07/201007291848_233097_1917139_3.jpg[/img] 图2,3分别为匀浆热沉淀处理上样洗脱峰Ⅰ,Ⅱ稀释8倍后在190nm-300nm间紫外吸收光谱.结果显示,洗脱峰Ⅰ在280nm处都有一个高的吸收峰,而洗脱峰Ⅱ在250nm附近具有一个高的吸收峰,在280nm处急剧下降,据此分析MT主要存在于峰Ⅱ中. 3.洗脱峰SDS-PAGE分析[img]http://ng1.17img.cn/bbsfiles/images/2010/07/201007291856_233100_1917139_3.jpg[/img] 图4,5为匀浆上样后洗脱峰SDS-PAGE电泳图谱,如图8所示峰2峰3蛋白浓度过低,经冷冻干燥浓缩再次上样,图9显示MT存在于峰Ⅱ中但未能得到完全纯化,还需进一步上离子交换柱层析分离.
我选用紫外分光光度仪测量溶液的吸收度,从200——400nm全程扫描。用A(混合液)和B(由A混合液通过凝胶层析柱按时间段分别收集)两个样品分别测试,发现,B的某个时间段里收集的样品在275nm时有个较明显的峰,而在A中却没有发现,我想请问一下这样的情况是正常的吗?为什么会有这样的情况呢(混合物里没有,而分离物里有,而且经过凝胶层析分离物质结构应该不会改变呀)?望能得到专家的指点。
基本原理凝膠過濾法(gel filtration)也稱為排阻層析(exclusion chromatography)、凝膠層析(gel chromatography)或分子篩層析(molecular sieve chromatofraphy),它是在1960年後發展出來的技術。凝膠是由膠體溶液凝結而成的固體物質,內部具有網狀篩孔,利用球狀凝膠內的篩孔,使分子流過填充凝膠的管柱時,大分子無法進入凝膠篩孔,而只流經凝膠及管柱間的孔隙,很快就可以流出管柱,較小的分子因為進入凝膠內的篩孔,故在管柱內的停留時間較長,由此區分大小不同的分子,亦可與已知大小的分子作比較而定出一分子的分子量。一般狀況下,凝膠不會吸附成份,所有欲分離物質都會被洗出,這是凝膠層析法與其它層析法不同的地方。目前常用的凝膠包括3個主要類型:1. PolydextranPolydextran的商品名稱是Sephadex,它幾乎不溶於溶劑中,親水性強,能迅速在水和電解質溶液中膨脹,在鹼性的環境中十分穩定,所以可以用鹼去除凝膠上的污染物。Sephadex依其吸水量有不同型號,如 G-25、G-75、G-100或是G-200,G 後面的數字為凝膠吸水量再乘以10,以G-25為例,表示1克乾燥的G-25凝膠可以吸水2.5 ml 。2. PolyacrylamidePolyacrylamide是一種合成凝膠,商品名Bio-Gel P,乾粉顆粒狀,在溶劑中自動溶成膠體,依膠的分離範圍不同,分成Bio-Gel P-2至Bio-Gel P-300,P後面的數字乘以1000為最大過濾限度。Polyacrylamide的化學性質不活潑,但它在極端的pH 下會被水解,水解後產生的COOH-具有離子交換的性質,因此pH 值應盡量控制在2-10之間。3. Agarose商品名Separose,屬於天然凝膠,依凝膠中乾膠的百分含量,分為Sepharose 2B,4B和6B。Agarose gel 是一種大孔凝膠,主要用於像核酸或病毒這些分子量400,000以上的物質,因其顆粒軟,在分離過程有時會阻塞管柱,造成流速減慢,又因其在攝氏50度以上會融化,故需於較低溫的環境中進行層析。Agarose 做成beads後不能再脫水乾燥,所以要在溼態中保存。凝膠和管柱的選擇凝膠的材質需為化學惰性,與分離物不能產生變性(denature)或是其它化學反應,最好具有能長期反覆使用的穩定性,並可以在較大的pH和溫度範圍內使用。由於凝膠上的離子交換基團會吸附帶電荷的物質,產生離子交換的效果,所以凝膠上最好不具有離子交換的基團。此外,凝膠要有一定的機械強度,在層析過程中才不會變形,增加機械強度也可使層析在較高壓力的環境進行,縮短分離時間。凝膠顆粒的粗細與分離效果有直接關係,顆粒細的分離效果好,但流速慢而費時,因此要依據實際的需要來選擇。對於分子量較小的物質,一般採用polydextran或polyacrylamide材質的凝膠,大分子物質則使用agarose。以Sephadex為例,Sephadex G-50可用於區分分子量1,500~30,000之分子,而Sephadex G-75 凝膠可區分分子量3,000~70,000之分子,所以若要分離分子量10,000及20,000之分子,兩種都適用。如果要分離的分子大小相差很多,則可選用柱高:直徑=5:1~15:1的管柱,且管柱體積要大於4~15倍的樣品體積;如果要分離的物質之間分子量差異不大,則要選用柱高:直徑=20:1~100:1的管柱,且管柱體積要大於25~100倍的樣品體積。凝膠的處理 商品凝膠一般是乾燥的顆粒,使用前要先泡在欲使用的沖洗液中,使它充份膨脹,否則有引起凝膠柱破裂的危險。熱脹法是常用的前處理法,即把浸於沖洗液中的凝膠加熱,讓它膨脹並除去氣泡,溫度夠高的話(加溫至近沸騰)也可消毒殺菌。凝膠處理過程不能劇烈攪拌,如此易使顆粒破裂,影響流速。將凝膠裝入管柱的方法有很多種,實驗室常用的方法是先在柱中加入約1/3 體積的沖洗液,邊輕輕攪伴邊將凝膠懸浮液倒入其中,等到底部沉積約1~2公分的凝膠後,打開下方出口讓水流出,上面不斷加入懸浮液,等到沉積到離頂部約3~5公分處停止,讓3~5倍柱床體積的緩衝液流過層析柱。若用polydextran的凝膠,可放入有顏色的蛋白質(如cytochrome c)流過管柱,看看色帶是否均勻下降,不均勻或出現氣泡,凝膠均需倒出重新填裝。衝洗緩衝液僅需留高於柱床2 公分左右,多餘的可用滴管吸去,再將出口打開使衝洗液流到距表面1~2公釐,關閉出口,用滴管緩緩加入樣品再打開出口,樣品完全滲入凝膠內後,加入約4公分衝洗液,出口處接上收集瓶開始層析。由於polydextran 和agarose都屬於多醣類,一旦微生物生長過多,分泌的酶會水解凝膠使其性質改變,為了防止這種情況發生,凝膠最好採用真空或低溫保存,但溫度不能過低使凝膠凍結。加入抑菌劑(chlohexidine, chlorbutol, phenylmercuric salts, NaOH等)也是常用的方法。長時間不用的凝膠可用乾燥保存法,也就是把使用過的凝膠用水除去碎顆粒和雜質,再用不同濃度的酒精,由70%、90%到95%逐步脫水,在攝氏60~80度下烘乾,不能加熱的Sepharose則用乙醚洗滌乾燥。
[分享]凝胶色谱技术凝胶色谱技术是六十年代初发展起来的一种快速而又简单的分离分技术,由于设备简单、操作方便,不需要有机溶剂,对高分子物质有很高的分离效果。目前已经被生物化学、分子生物学、生物工程学、分子免疫学以及医学等有关领域广泛采用,不但应用于科学实验研究,而且已经大规模地用于工业生产。一、基本理论(一)分子筛效益 一个含有各种分子的样品溶液缓慢地流经凝胶色谱柱时,各分子在柱内同时进行着两种不同的运动:垂直向下的移动和无定向的扩散运动。大分子物质由于直径较大,不易进入凝胶颗粒的微孔,而只能分布颗粒之间,所以在洗脱时向下移动的速度较快。小分子物质除了可在凝胶颗粒间隙中扩散外,还可以进入凝胶颗粒的微孔中,即进入凝胶相内,在向下移动的过程中,从一个凝胶内扩散到颗粒间隙后再进入另一凝胶颗粒,如此不断地进入和扩散,小分子物质的下移速度落后于大分子物质,从而使样品中分子大的先流出色谱柱,中等分子的后流出,分子最小的最后流出,这种现象叫分子筛效应。具有多孔的凝胶就是分子筛。各种分子筛的孔隙大小分布有一定范围,有最大极限和最小极限。分子直径比凝胶最大孔隙直径大的,就会全部被排阻在凝胶颗粒之外,这种情况叫全排阻。两种全排阻的分子即使大小不同,也不能有分离效果。直径比凝胶最小孔直径小的分子能进入凝胶的全部孔隙。如果两种分子都能全部进入凝胶孔隙,即使它们的大小有差别,也不会有好的分离效果。因此,一定的分子筛有它一定的使用范围。综上所述,在凝胶色谱中会有三种情况,一是分子很小,能进入分子筛全部的内孔隙;二是分子很大,完全不能进入凝胶的任何内孔隙;三是分子大小适中,能进入凝胶的内孔隙中孔径大小相应的部分。大、中、小三类分子彼此间较易分开,但每种凝胶分离范围之外的分子,在不改变凝胶种类的情况下是很难分离的。对于分子大小不同,但同属于凝胶分离范围内各种分子,在凝胶床中的分布情况是不同的:分子较大的只能进入孔径较大的那一部分凝胶孔隙内,而分子的可进入较多的凝胶颗粒内,这样分子较大的在凝胶床内移动距离较短,分子较小的移动距离较长。于是分子较大的先通过凝胶床而分子较小的后通过凝胶床,这样就利用分子筛可将分子量不同的物质分离。另外,凝胶本身具有三维网状结构,大的分子在通过这种网状结构上的孔隙时阻力较大,小分子通过时阻力较小。分子量大小不同的多种成份在通过凝胶床时,按照分子量大小“排队,凝胶表现分子筛效应。(二)色谱柱的重要参数⑴柱体积:柱体积是指凝胶装柱后,从柱的底板到凝胶沉积表面的体积。在色谱柱中充满凝胶的部分称为凝胶床,因引柱体积又称“床”体积,常用Vt 表示。⑵外水体积:色谱柱内凝胶颗粒间隙,这部分体积称外水体积,亦称间隙体积,常用Vo表示。⑶内水体积:因为凝胶为三维网状结构,颗粒内部仍有空间,液体可进入颗粒内部,这就分间隙的总和为内水体积,又称定相体积,常用Vi表示。 不包括固体支持物的体积(Vg)。⑷峰洗脱体积:是指被分离物质通过凝胶柱所需洗脱液有体积,常用Ve 表示。当使用样品的体积很少时,(与洗脱体积比较可以忽略不计),在洗脱图中,从加样到峰顶位置所用洗脱液体积为Ve。 当样品体积与洗脱体积比较不能忽略时,洗脱体积计算可以从样品体积的一半到峰顶位置。当样品很大时,洗脱体积计算可以从应用样品开始到洗脱峰升高的弯曲点(或半高处)。 二、凝胶的种类及性质 (一)交联葡聚糖凝胶(Sephadex)⑴Sephadex G交联葡聚糖的商品名为Sephndex,不同规格型号的葡聚糖用英文字母G表示,G后面的阿拉伯数为凝胶得水值的10倍。例如,G-25为每克凝胶膨胀时吸水2.5克,同样G-200克每克千胶吸水20克。交联葡聚糖凝胶的种类有G-10,G-15,G-25,G-50,G-75,G-100,G-150,和G-200。因此,“G”反映,凝胶的交联程度,膨胀程度及分部范围。⑵Sephadex LH-20,是─Sephadex G-25的羧丙基衍生物, 能溶于水及亲脂溶剂,用于分离不溶于水的物质。(二)琼脂糖凝胶: 商品名很多,常见的有,Sepharose(瑞典,pharmacia ),Bio-Gel-A(美国Bio-Rad)等。琼脂糖凝胶是依*糖链之间的次级链如氢键来维持网状结构,网状结构的疏密依*琼脂糖的浓度。一般情况下,它的结构是稳定的,可以在许多条件下使用(如水,pH4-9范围内的盐溶液)。琼脂糖凝胶在40℃以上开始融化,也不能高压消毒,可用化学灭菌活处理。(三)聚丙烯酰胺凝胶: 是一种人工合成凝胶,是以丙烯酰胺为单位, 由甲*双丙烯酰胺交联成的,经干燥粉碎或加工成形制成粒状,控制交联剂的用量可制成各种型号的凝胶。交联剂越多,孔隙越小。聚丙烯酰胺凝胶的商品为生物胶-P (Bio-Gel P),由美国Bio-Rod厂生产,型号很多,从P-2至P-300共10种,P 后面的数字再乘1000就相当于该凝胶的排阻限度。(四)聚苯乙烯凝胶商品为Styrogel , 具有大网孔结构, 可用于分离分子量1600到40,000,000的生物大分子,适用于有机多聚物,分子量测定和脂溶性天然物的分级,凝胶机械强度好,洗脱剂可用甲基亚砜。三、实验技术(一)层析柱 层析柱是凝胶层析技术中的主体,一般用玻璃管或有机玻璃管。层析柱的直径大小不影响分离度,样品用量大,可加大柱的直径,一般制备用凝胶柱,直径大于2厘米,但在加样时应将样品均匀分布于凝胶柱床面上。此外, 直径加大,洗脱液体体积增大,样品稀释度大。分离度取决于柱高,为分离不同组分,凝胶柱床必须有适宜的高度,分离度与柱高的平方根相关,但由于软凝胶柱过高挤压变形阻塞,一般不超过1米。分族分离时用短柱,一般凝胶柱长20-30厘米,柱高与直径的比较5:1─10:1,凝胶床体积为样品溶液体积的4-10倍。 分级分离时柱高与直径之线为20:1─100:1,常用凝胶柱有50×25厘米,10×25厘米。层析柱滤板下的死体积应尽可能的小,如果支掌滤板下的死体积大,被分离组分之间重新混合的可能性就大,其结果是影响洗脱峰形,出现拖尾出象,降低分辩力。在精确分离时,死体积不能超过总床体积的1/1000。(二)凝胶的选择 根据所需凝胶体积,估计所需干胶的量。 一般葡聚糖凝胶吸水后的凝胶体积约为其吸水量的2倍,例如Sephadex G-20的吸水量为20,1 克Sephadex G─200吸水后形成的凝胶体积约40ml。凝胶的粒度也可影响层析分离效果。粒度细胞分离效果好,但阻力大,流速慢。一般实验室分离蛋白质采用100-200号筛目的的Sephadex G-200效果好, 脱盐用Sephadex G-25、G-50,用粗粒,短柱,流速快。(三)凝胶的制备 商品凝胶是干燥的颗粒使用前需直接在欲使用的洗脱液中膨胀。为了加速膨胀,可用加热法,即在沸水浴中将湿凝胶逐渐升温至近沸,这样可大大中速膨胀,通常在1-2小时内即可完成。特别是在使用软胶时, 自然膨胀需24小时至数天,而用加热法在几小时内就可完成。这种方法不但节约时间,而且还可消毒,除去凝胶中污染的细菌和排除胶内的空气。(四)样品溶液的处理 样品溶液如有沉淀应过滤或离心除去,如含脂类可高速离心或通过Sephadex G-15短柱除去。样品的粘度不可大,含蛋白为超过4%,粘度高影响分离效果。上柱样品液的体积根据凝胶床体积的分离要求确定。分离蛋白质样品的体积为凝胶床的1-4%(一般约0.5-2ml),进行分族分离时样品液可为凝胶床的10%,在蛋白质溶液除盐时,样品可达凝胶床的20-30%。 分级分离样品体积要小,使样品层尽可能窄,洗脱出的峰形较好。(五)防止微生物的污染 交联葡聚糖和琼脂糖都是多糖类物质,防止微生物的生长,在凝胶层析中十分重要,常用的抑菌剂有:⑴叠氨钠(NaN3)在凝胶层析中只要用0.02%叠氮钠已足够防止微生物的生长,叠氮钠易溶一水,在20℃时约为40%;它不与蛋白质或碳水化合物相互作用,因此叠氮钠不影响抗体活力;不会改变蛋白质和碳水化合物的层析我特性。叠氮钠可干扰荧光标记蛋白质。⑵可乐酮[Cl3C-C(OH)(CH3)2]在凝胶层析中使用浓度为0.01-0.02%。在微酸性溶液中它的杀菌效果最佳,在强碱性溶液中或温度高于60℃时易引起分解而失效。⑶乙基汞代巯基水杨酸钠 在凝胶层析中作为抑菌剂使用浓度为0.05-0. 01%。在微酸性溶液中最为有效。重金属离子可使乙基代巯基的物质结合,因而包含疏基的蛋白质可在不同程度上降低它的抑菌效果。⑷苯基汞代盐 在凝胶层析中使用浓度为0.001-0.01%。在微碱性溶液中抑效果最佳,长时间放置时可与卤素、硝酸根离子作用而产生沉淀;还原剂可引起此化合物分解;含疏基的物质亦可降低或抑制它的抑菌作用。
凝胶色谱法简介 凝胶色谱技术是六十年代初发展起来的一种快速而又简单的分离分技术,由于设备简单、操作方便,不需要有机溶剂,对高分子物质有很高的分离效果。目前已经被生物化学、分子生物学、生物工程学、分子免疫学以及医学等有关领域广泛采用,不但应用于科学实验研究,而且已经大规模地用于工业生产。 一、基本理论 (一) 分子筛效益 一个含有各种分子的样品溶液缓慢地流经凝胶色谱柱时,各分子在柱内同时进行着两种不同的运动:垂直向下的移动和无定向的扩散运动。大分子物质由于直径较大,不易进入凝胶颗粒的微孔,而只能分布颗粒之间,所以在洗脱时向下移动的速度较快。小分子物质除了可在凝胶颗粒间隙中扩散外,还可以进入凝胶颗粒的微孔中,即进入凝胶相内,在向下移动的过程中,从一个凝胶内扩散到颗粒间隙后再进入另一凝胶颗粒,如此不断地进入和扩散,小分子物质的下移速度落后于大分子物质,从而使样品中分子大的先流出色谱柱,中等分子的后流出,分子最小的最后流出,这种现象叫分子筛效应。具有多孔的凝胶就是分子筛。各种分子筛的孔隙大小分布有一定范围,有最大极限和最小极限。分子直径比凝胶最大孔隙直径大的,就会全部被排阻在凝胶颗粒之外,这种情况叫全排阻。两种全排阻的分子即使大小不同,也不能有分离效果。直径比凝胶最小孔直径小的分子能进入凝胶的全部孔隙。如果两种分子都能全部进入凝胶孔隙,即使它们的大小有差别,也不会有好的分离效果。因此,一定的分子筛有它一定的使用范围。综上所述,在凝胶色谱中会有三种情况,一是分子很小,能进入分子筛全部的内孔隙;二是分子很大,完全不能进入凝胶的任何内孔隙;三是分子大小适中,能进入凝胶的内孔隙中孔径大小相应的部分。大、中、小三类分子彼此间较易分开,但每种凝胶分离范围之外的分子,在不改变凝胶种类的情况下是很难分离的。对于分子大小不同,但同属于凝胶分离范围内各种分子,在凝胶床中的分布情况是不同的:分子较大的只能进入孔径较大的那一部分凝胶孔隙内,而分子的可进入较多的凝胶颗粒内,这样分子较大的在凝胶床内移动距离较短,分子较小的移动距离较长。于是分子较大的先通过凝胶床而分子较小的后通过凝胶床,这样就利用分子筛可将分子量不同的物质分离。另外,凝胶本身具有三维网状结构,大的分子在通过这种网状结构上的孔隙时阻力较大,小分子通过时阻力较小。分子量大小不同的多种成份在通过凝胶床时,按照分子量大小“排队,凝胶表现分子筛效应。 二)色谱柱的重要参数 ⑴柱体积:柱体积是指凝胶装柱后,从柱的底板到凝胶沉积表面的体积。在色谱柱中充满凝胶的部分称为凝胶床,因引柱体积又称“床”体积,常用Vt 表示。 ⑵外水体积:色谱柱内凝胶颗粒间隙,这部分体积称外水体积,亦称间隙体积,常用Vo表示。 ⑶内水体积:因为凝胶为三维网状结构,颗粒内部仍有空间,液体可进入颗粒内部,这就分间隙的总和为内水体积,又称定相体积,常用Vi表示。 不包括固体支持物的体积(Vg)。 ⑷峰洗脱体积:是指被分离物质通过凝胶柱所需洗脱液有体积,常用Ve 表示。当使用样品的体积很少时,(与洗脱体积比较可以忽略不计),在洗脱图中,从加样到峰顶位置所用洗脱液体积为Ve。 当样品体积与洗脱体积比较不能忽略时,洗脱体积计算可以从样品体积的一半到峰顶位置。当样品很大时,洗脱体积计算可以从应用样品开始到洗脱峰升高的弯曲点(或半高处)。 二、凝胶的种类及性质 (一) 交联葡聚糖凝胶 ⑴Sephadex G交联葡聚糖的商品名为Sephndex,不同规格型号的葡聚糖用英文字母G表示,G后面的阿拉伯数为凝胶得水值的10倍。例如,G-25为每克凝胶膨胀时吸水2.5克,同样G-200克每克千胶吸水20克。交联葡聚糖凝胶的种类有G-10,G-15,G-25,G-50,G-75,G-100,G-150,和G-200。因此,“G”反映,凝胶的交联程度,膨胀程度及分部范围。 ⑵Sephadex LH-20,是─Sephadex G-25的羧丙基衍生物, 能溶于水及亲脂溶剂,用于分离不溶于水的物质。 (二) 琼脂糖凝胶: 商品名很多,常见的有,Sepharose(瑞典,pharmacia ),Bio-Gel-A(美国Bio-Rad)等。琼脂糖凝胶是依靠糖链之间的次级链如氢键来维持网状结构,网状结构的疏密依靠琼脂糖的浓度。一般情况下,它的结构是稳定的,可以在许多条件下使用(如水,pH4-9范围内的盐溶液)。琼脂糖凝胶在40℃以上开始融化,也不能高压消毒,可用化学灭菌活处理。 (三)聚丙烯酰胺凝胶:是一种人工合成凝胶,是以丙烯酰胺为单位, 由甲叉双丙烯酰胺交联成的,经干燥粉碎或加工成形制成粒状,控制交联剂的用量可制成各种型号的凝胶。交联剂越多,孔隙越小。聚丙烯酰胺凝胶的商品为生物胶-P (Bio-Gel P),由美国Bio-Rod厂生产,型号很多,从P-2至P-300共10种,P 后面的数字再乘1000就相当于该凝胶的排阻限度。 (四)聚苯乙烯凝胶商品为Styrogel , 具有大网孔结构, 可用于分离分子量1600到40,000,000的生物大分子,适用于有机多聚物,分子量测定和脂溶性天然物的分级,凝胶机械强度好,洗脱剂可用甲基亚砜。 三、实验技术 (一)层析柱 层析柱是凝胶层析技术中的主体,一般用玻璃管或有机玻璃管。层析柱的直径大小不影响分离度,样品用量大,可加大柱的直径,一般制备用凝胶柱,直径大于2厘米,但在加样时应将样品均匀分布于凝胶柱床面上。此外, 直径加大,洗脱液体体积增大,样品稀释度大。分离度取决于柱高,为分离不同组分,凝胶柱床必须有适宜的高度,分离度与柱高的平方根相关,但由于软凝胶柱过高挤压变形阻塞,一般不超过1米。分族分离时用短柱,一般凝胶柱长20-30厘米,柱高与直径的比较5:1─10:1,凝胶床体积为样品溶液体积的4-10倍。 分级分离时柱高与直径之线为20:1─100:1,常用凝胶柱有50×25厘米,10×25厘米。层析柱滤板下的死体积应尽可能的小,如果支掌滤板下的死体积大,被分离组分之间重新混合的可能性就大,其结果是影响洗脱峰形,出现拖尾出象,降低分辩力。在精确分离时,死体积不能超过总床体积的1/1000。 (二)凝胶的选择 根据所需凝胶体积,估计所需干胶的量。 一般葡聚糖凝胶吸水后的凝胶体积约为其吸水量的2倍,例如Sephadex G-20的吸水量为20,1 克Sephadex G─200吸水后形成的凝胶体积约40ml。凝胶的粒度也可影响层析分离效果。粒度细胞分离效果好,但阻力大,流速慢。一般实验室分离蛋白质采用100-200号筛目的的Sephadex G-200效果好, 脱盐用Sephadex G-25、G-50,用粗粒,短柱,流速快。 (三)凝胶的制备 商品凝胶是干燥的颗粒使用前需直接在欲使用的洗脱液中膨胀。为了加速膨胀,可用加热法,即在沸水浴中将湿凝胶逐渐升温至近沸,这样可大大中速膨胀,通常在1-2小时内即可完成。特别是在使用软胶时, 自然膨胀需24小时至数天,而用加热法在几小时内就可完成。这种方法不但节约时间,而且还可消毒,除去凝胶中污染的细菌和排除胶内的空气。 (四)样品溶液的处理 样品溶液如有沉淀应过滤或离心除去,如含脂类可高速离心或通过Sephadex G-15短柱除去。样品的粘度不可大,含蛋白为超过4%,粘度高影响分离效果。上柱样品液的体积根据凝胶床体积的分离要求确定。分离蛋白质样品的体积为凝胶床的1-4%(一般约0.5-2ml),进行分族分离时样品液可为凝胶床的10%,在蛋白质溶液除盐时,样品可达凝胶床的20-30%。 分级分离样品体积要小,使样品层尽可能窄,洗脱出的峰形较好。 (五)防止微生物的污染 交联葡聚糖和琼脂糖都是多糖类物质,防止微生物的生长,在凝胶层析中十分重要,常用的抑菌剂有: ⑴叠氨钠(NaN3)在凝胶层析中只要用0.02%叠氮钠已足够防止微生物的生长,叠氮钠易溶一水,在20℃时约为40%;它不与蛋白质或碳水化合物相互作用,因此叠氮钠不影响抗体活力;不会改变蛋白质和碳水化合物的层析我特性。叠氮钠可干扰荧光标记蛋白质。⑵可乐酮[Cl3C-C(OH)(CH3)2]在凝胶层析中使用浓度为0.01-0.02%。在微酸性溶液中它的杀菌效果最佳,在强碱性溶液中或温度高于60℃时易引起分解而失效。⑶乙基汞代巯基水杨酸钠 在凝胶层析中作为抑菌剂使用浓度为0.05-0. 01%。在微酸性溶液中最为有效。重金属离子可使乙基代巯基的物质结合,因而包含疏基的蛋白质可在不同程度上降低它的抑菌效果。⑷苯基汞代盐 在凝胶层析中使用浓度为0.001-0.01%。在微碱性溶液中抑效果最佳,长时间放置时可与卤素、硝酸根离子作用而产生沉淀;还原剂可引起此化合物分解;含疏基的物质亦可降低或抑制它的抑菌作用。 百特纯大分子(武汉)科技提供葡聚糖GPC标样
关键词:中检所网站 中检所标准品 中检所对照品 药检所标准品 药检所对照品 中检所标准物 质药检所标准物质摘要:凝胶色谱技术是六十年代初发展起来的一种快速而又简单的分离分技术,由于设备简单、操作方便,不需要有机溶剂,对高分子物质有很高的分离效果。目前已经被生物化学、分子生物学、生物工程学、分子免疫学以及医学等有关领域广泛采用,不但应用于科学实验研究,而且已经大规模地用于工业生产。 一、基本理论 (一)分子筛效益 一个含有各种分子的样品溶液缓慢地流经凝胶色谱柱时,各分子在柱内同时进行着两种不同的运动:垂直向下的移动和无定向的扩散运动。大分子物质由于直径较大,不易进入凝胶颗粒的微孔,而只能分布颗粒之间,所以在洗脱时向下移动的速度较快。小分子物质除了可在凝胶颗粒间隙中扩散外,还可以进入凝胶颗粒的微孔中,即进入凝胶相内,在向下移动的过程中,从一个凝胶内扩散到颗粒间隙后再进入另一凝胶颗粒,如此不断地进入和扩散,小分子物质的下移速度落后于大分子物质,从而使样品中分子大的先流出色谱柱,中等分子的后流出,分子最小的最后流出,这种现象叫分子筛效应。具有多孔的凝胶就是分子筛。各种分子筛的孔隙大小分布有一定范围,有最大极限和最小极限。分子直径比凝胶最大孔隙直径大的,就会全部被排阻在凝胶颗粒之外,这种情况叫全排阻。两种全排阻的分子即使大小不同,也不能有分离效果。直径比凝胶最小孔直径小的分子能进入凝胶的全部孔隙。如果两种分子都能全部进入凝胶孔隙,即使它们的大小有差别,也不会有好的分离效果。因此,一定的分子筛有它一定的使用范围。综上所述,在凝胶色谱中会有三种情况,一是分子很小,能进入分子筛全部的内孔隙;二是分子很大,完全不能进入凝胶的任何内孔隙;三是分子大小适中,能进入凝胶的内孔隙中孔径大小相应的部分。大、中、小三类分子彼此间较易分开,但每种凝胶分离范围之外的分子,在不改变凝胶种类的情况下是很难分离的。对于分子大小不同,但同属于凝胶分离范围内各种分子,在凝胶床中的分布情况是不同的:分子较大的只能进入孔径较大的那一部分凝胶孔隙内,而分子的可进入较多的凝胶颗粒内,这样分子较大的在凝胶床内移动距离较短,分子较小的移动距离较长。于是分子较大的先通过凝胶床而分子较小的后通过凝胶床,这样就利用分子筛可将分子量不同的物质分离。另外,凝胶本身具有三维网状结构,大的分子在通过这种网状结构上的孔隙时阻力较大,小分子通过时阻力较小。分子量大小不同的多种成份在通过凝胶床时,按照分子量大小“排队,凝胶表现分子筛效应。 (二)色谱柱的重要参数 ⑴柱体积:柱体积是指凝胶装柱后,从柱的底板到凝胶沉积表面的体积。在色谱柱中充满凝胶的部分称为凝胶床,因引柱体积又称“床”体积,常用Vt 表示。 ⑵外水体积:色谱柱内凝胶颗粒间隙,这部分体积称外水体积,亦称间隙体积,常用Vo表示。 ⑶内水体积:因为凝胶为三维网状结构,颗粒内部仍有空间,液体可进入颗粒内部,这就分间隙的总和为内水体积,又称定相体积,常用Vi表示。 不包括固体支持物的体积(Vg)。 ⑷峰洗脱体积:是指被分离物质通过凝胶柱所需洗脱液有体积,常用Ve 表示。当使用样品的体积很少时,(与洗脱体积比较可以忽略不计),在洗脱图中,从加样到峰顶位置所用洗脱液体积为Ve。 当样品体积与洗脱体积比较不能忽略时,洗脱体积计算可以从样品体积的一半到峰顶位置。当样品很大时,洗脱体积计算可以从应用样品开始到洗脱峰升高的弯曲点(或半高处)。 二、凝胶的种类及性质 (一)交联葡聚糖凝胶(Sephadex) ⑴Sephadex G交联葡聚糖的商品名为Sephndex,不同规格型号的葡聚糖用英文字母G表示,G后面的阿拉伯数为凝胶得水值的10倍。例如,G-25为每克凝胶膨胀时吸水2.5克,同样G-200克每克千胶吸水20克。交联葡聚糖凝胶的种类有G-10,G-15,G-25,G-50,G-75,G-100,G- 150,和G-200。因此,“G”反映,凝胶的交联程度,膨胀程度及分部范围。 ⑵Sephadex LH-20,是─Sephadex G-25的羧丙基衍生物, 能溶于水及亲脂溶剂,用于分离不溶于水的物质。 (二)琼脂糖凝胶: 商品名很多,常见的有,Sepharose(瑞典,pharmacia ),Bio-Gel-A(美国Bio-Rad)等。琼脂糖凝胶是依靠糖链之间的次级链如氢键来维持网状结构,网状结构的疏密依靠琼脂糖的浓度。一般情况下,它的结构是稳定的,可以在许多条件下使用(如水,pH4-9范围内的盐溶液)。琼脂糖凝胶在40℃以上开始融化,也不能高压消毒,可用化学灭菌活处理。 (三)聚丙烯酰胺凝胶: 是一种人工合成凝胶,是以丙烯酰胺为单位, 由甲叉双丙烯酰胺交联成的,经干燥粉碎或加工成形制成粒状,控制交联剂的用量可制成各种型号的凝胶。交联剂越多,孔隙越小。聚丙烯酰胺凝胶的商品为生物胶-P (Bio-Gel P),由美国Bio-Rod厂生产,型号很多,从P-2至P-300共10种,P 后面的数字再乘1000就相当于该凝胶的排阻限度。 (四)聚苯乙烯凝胶商品为Styrogel , 具有大网孔结构, 可用于分离分子量1600到40,000,000的生物大分子,适用于有机多聚物,分子量测定和脂溶性天然物的分级,凝胶机械强度好,洗脱剂可用甲基亚砜。 三、实验技术 (一)层析柱 层析柱是凝胶层析技术中的主体,一般用玻璃管或有机玻璃管。层析柱的直径大小不影响分离度,样品用量大,可加大柱的直径,一般制备用凝胶柱,直径大于2厘米,但在加样时应将样品均匀分布于凝胶柱床面上。此外, 直径加大,洗脱液体体积增大,样品稀释度大。分离度取决于柱高,为分离不同组分,凝胶柱床必须有适宜的高度,分离度与柱高的平方根相关,但由于软凝胶柱过高挤压变形阻塞,一般不超过1米。分族分离时用短柱,一般凝胶柱长20-30厘米,柱高与直径的比较5:1─10:1,凝胶床体积为样品溶液体积的 4-10倍。 分级分离时柱高与直径之线为20:1─100:1,常用凝胶柱有50×25厘米,10×25厘米。层析柱滤板下的死体积应尽可能的小,如果支掌滤板下的死体积大,被分离组分之间重新混合的可能性就大,其结果是影响洗脱峰形,出现拖尾出象,降低分辩力。在精确分离时,死体积不能超过总床体积的1/1000。 (二)凝胶的选择 根据所需凝胶体积,估计所需干胶的量。 一般葡聚糖凝胶吸水后的凝胶体积约为其吸水量的2倍,例如Sephadex G-20的吸水量为20,1 克Sephadex G─200吸水后形成的凝胶体积约40ml。凝胶的粒度也可影响层析分离效果。粒度细胞分离效果好,但阻力大,流速慢。一般实验室分离蛋白质采用 100-200号筛目的的Sephadex G-200效果好, 脱盐用Sephadex G-25、G-50,用粗粒,短柱,流速快。 (三)凝胶的制备 商品凝胶是干燥的颗粒使用前需直接在欲使用的洗脱液中膨胀。为了加速膨胀,可用加热法,即在沸水浴中将湿凝胶逐渐升温至近沸,这样可大大中速膨胀,通常在 1-2小时内即可完成。特别是在使用软胶时, 自然膨胀需24小时至数天,而用加热法在几小时内就可完成。这种方法不但节约时间,而且还可消毒,除去凝胶中污染的细菌和排除胶内的空气。 (四)样品溶液的处理 样品溶液如有沉淀应过滤或离心除去,如含脂类可高速离心或通过Sephadex G-15短柱除去。样品的粘度不可大,含蛋白为超过4%,粘度高影响分离效果。上柱样品液的体积根据凝胶床体积的分离要求确定。分离蛋白质样品的体积为凝胶床的1-4%(一般约0.5-2ml),进行分族分离时样品液可为凝胶床的10%,在蛋白质溶液除盐时,样品可达凝胶床的20-30%。 分级分离样品体积要小,使样品层尽可能窄,洗脱出的峰形较好。 (五)防止微生物的污染 交联葡
凝胶色谱技术 凝胶色谱法 凝胶色谱技术是六十年代初发展起来的一种快速而又简单的分离分技术,由于设备简单、操作方便,不需要有机溶剂,对高分子物质有很高的分离效果。目前已经被生物化学、分子生物学、生物工程学、分子免疫学以及医学等有关领域广泛采用,不但应用于科学实验研究,而且已经大规模地用于工业生产。一、基本理论(一)分子筛效益 一个含有各种分子的样品溶液缓慢地流经凝胶色谱柱时,各分子在柱内同时进行着两种不同的运动:垂直向下的移动和无定向的扩散运动。大分子物质由于直径较大,不易进入凝胶颗粒的微孔,而只能分布颗粒之间,所以在洗脱时向下移动的速度较快。小分子物质除了可在凝胶颗粒间隙中扩散外,还可以进入凝胶颗粒的微孔中,即进入凝胶相内,在向下移动的过程中,从一个凝胶内扩散到颗粒间隙后再进入另一凝胶颗粒,如此不断地进入和扩散,小分子物质的下移速度落后于大分子物质,从而使样品中分子大的先流出色谱柱,中等分子的后流出,分子最小的最后流出,这种现象叫分子筛效应。具有多孔的凝胶就是分子筛。各种分子筛的孔隙大小分布有一定范围,有最大极限和最小极限。分子直径比凝胶最大孔隙直径大的,就会全部被排阻在凝胶颗粒之外,这种情况叫全排阻。两种全排阻的分子即使大小不同,也不能有分离效果。直径比凝胶最小孔直径小的分子能进入凝胶的全部孔隙。如果两种分子都能全部进入凝胶孔隙,即使它们的大小有差别,也不会有好的分离效果。因此,一定的分子筛有它一定的使用范围。综上所述,在凝胶色谱中会有三种情况,一是分子很小,能进入分子筛全部的内孔隙;二是分子很大,完全不能进入凝胶的任何内孔隙;三是分子大小适中,能进入凝胶的内孔隙中孔径大小相应的部分。大、中、小三类分子彼此间较易分开,但每种凝胶分离范围之外的分子,在不改变凝胶种类的情况下是很难分离的。对于分子大小不同,但同属于凝胶分离范围内各种分子,在凝胶床中的分布情况是不同的:分子较大的只能进入孔径较大的那一部分凝胶孔隙内,而分子的可进入较多的凝胶颗粒内,这样分子较大的在凝胶床内移动距离较短,分子较小的移动距离较长。于是分子较大的先通过凝胶床而分子较小的后通过凝胶床,这样就利用分子筛可将分子量不同的物质分离。另外,凝胶本身具有三维网状结构,大的分子在通过这种网状结构上的孔隙时阻力较大,小分子通过时阻力较小。分子量大小不同的多种成份在通过凝胶床时,按照分子量大小“排队,凝胶表现分子筛效应。(二)色谱柱的重要参数⑴柱体积:柱体积是指凝胶装柱后,从柱的底板到凝胶沉积表面的体积。在色谱柱中充满凝胶的部分称为凝胶床,因引柱体积又称“床”体积,常用Vt 表示。⑵外水体积:色谱柱内凝胶颗粒间隙,这部分体积称外水体积,亦称间隙体积,常用Vo表示。⑶内水体积:因为凝胶为三维网状结构,颗粒内部仍有空间,液体可进入颗粒内部,这就分间隙的总和为内水体积,又称定相体积,常用Vi表示。 不包括固体支持物的体积(Vg)。⑷峰洗脱体积:是指被分离物质通过凝胶柱所需洗脱液有体积,常用Ve 表示。当使用样品的体积很少时,(与洗脱体积比较可以忽略不计),在洗脱图中,从加样到峰顶位置所用洗脱液体积为Ve。 当样品体积与洗脱体积比较不能忽略时,洗脱体积计算可以从样品体积的一半到峰顶位置。当样品很大时,洗脱体积计算可以从应用样品开始到洗脱峰升高的弯曲点(或半高处)。 二、凝胶的种类及性质 (一)交联葡聚糖凝胶(Sephadex)⑴Sephadex G交联葡聚糖的商品名为Sephndex,不同规格型号的葡聚糖用英文字母G表示,G后面的阿拉伯数为凝胶得水值的10倍。例如,G-25为每克凝胶膨胀时吸水2.5克,同样G-200克每克千胶吸水20克。交联葡聚糖凝胶的种类有G-10,G-15,G-25,G-50,G-75,G-100,G-150,和G-200。因此,“G”反映,凝胶的交联程度,膨胀程度及分部范围。⑵Sephadex LH-20,是─Sephadex G-25的羧丙基衍生物, 能溶于水及亲脂溶剂,用于分离不溶于水的物质。(二)琼脂糖凝胶: 商品名很多,常见的有,Sepharose(瑞典,pharmacia ),Bio-Gel-A(美国Bio-Rad)等。琼脂糖凝胶是依靠糖链之间的次级链如氢键来维持网状结构,网状结构的疏密依靠琼脂糖的浓度。一般情况下,它的结构是稳定的,可以在许多条件下使用(如水,pH4-9范围内的盐溶液)。琼脂糖凝胶在40℃以上开始融化,也不能高压消毒,可用化学灭菌活处理。(三)聚丙烯酰胺凝胶: 是一种人工合成凝胶,是以丙烯酰胺为单位, 由甲叉双丙烯酰胺交联成的,经干燥粉碎或加工成形制成粒状,控制交联剂的用量可制成各种型号的凝胶。交联剂越多,孔隙越小。聚丙烯酰胺凝胶的商品为生物胶-P (Bio-Gel P),由美国Bio-Rod厂生产,型号很多,从P-2至P-300共10种,P 后面的数字再乘1000就相当于该凝胶的排阻限度。(四)聚苯乙烯凝胶商品为Styrogel , 具有大网孔结构, 可用于分离分子量1600到40,000,000的生物大分子,适用于有机多聚物,分子量测定和脂溶性天然物的分级,凝胶机械强度好,洗脱剂可用甲基亚砜。三、实验技术(一)层析柱 层析柱是凝胶层析技术中的主体,一般用玻璃管或有机玻璃管。层析柱的直径大小不影响分离度,样品用量大,可加大柱的直径,一般制备用凝胶柱,直径大于2厘米,但在加样时应将样品均匀分布于凝胶柱床面上。此外, 直径加大,洗脱液体体积增大,样品稀释度大。分离度取决于柱高,为分离不同组分,凝胶柱床必须有适宜的高度,分离度与柱高的平方根相关,但由于软凝胶柱过高挤压变形阻塞,一般不超过1米。分族分离时用短柱,一般凝胶柱长20-30厘米,柱高与直径的比较5:1─10:1,凝胶床体积为样品溶液体积的4-10倍。 分级分离时柱高与直径之线为20:1─100:1,常用凝胶柱有50×25厘米,10×25厘米。层析柱滤板下的死体积应尽可能的小,如果支掌滤板下的死体积大,被分离组分之间重新混合的可能性就大,其结果是影响洗脱峰形,出现拖尾出象,降低分辩力。在精确分离时,死体积不能超过总床体积的1/1000。(二)凝胶的选择 根据所需凝胶体积,估计所需干胶的量。 一般葡聚糖凝胶吸水后的凝胶体积约为其吸水量的2倍,例如Sephadex G-20的吸水量为20,1 克Sephadex G─200吸水后形成的凝胶体积约40ml。凝胶的粒度也可影响层析分离效果。粒度细胞分离效果好,但阻力大,流速慢。一般实验室分离蛋白质采用100-200号筛目的的Sephadex G-200效果好, 脱盐用Sephadex G-25、G-50,用粗粒,短柱,流速快。(三)凝胶的制备 商品凝胶是干燥的颗粒使用前需直接在欲使用的洗脱液中膨胀。为了加速膨胀,可用加热法,即在沸水浴中将湿凝胶逐渐升温至近沸,这样可大大中速膨胀,通常在1-2小时内即可完成。特别是在使用软胶时, 自然膨胀需24小时至数天,而用加热法在几小时内就可完成。这种方法不但节约时间,而且还可消毒,除去凝胶中污染的细菌和排除胶内的空气。(四)样品溶液的处理 样品溶液如有沉淀应过滤或离心除去,如含脂类可高速离心或通过Sephadex G-15短柱除去。样品的粘度不可大,含蛋白为超过4%,粘度高影响分离效果。上柱样品液的体积根据凝胶床体积的分离要求确定。分离蛋白质样品的体积为凝胶床的1-4%(一般约0.5-2ml),进行分族分离时样品液可为凝胶床的10%,在蛋白质溶液除盐时,样品可达凝胶床的20-30%。 分级分离样品体积要小,使样品层尽可能窄,洗脱出的峰形较好。(五)防止微生物的污染 交联葡聚糖和琼脂糖都是多糖类物质,防止微生物的生长,在凝胶层析中十分重要,常用的抑菌剂有:⑴叠氨钠(NaN3)在凝胶层析中只要用0.02%叠氮钠已足够防止微生物的生长,叠氮钠易溶一水,在20℃时约为40%;它不与蛋白质或碳水化合物相互作用,因此叠氮钠不影响抗体活力;不会改变蛋白质和碳水化合物的层析我特性。叠氮钠可干扰荧光标记蛋白质。⑵可乐酮[Cl3C-C(OH)(CH3)2]在凝胶层析中使用浓度为0.01-0.02%。在微酸性溶液中它的杀菌效果最佳,在强碱性溶液中或温度高于60℃时易引起分解而失效。⑶乙基汞代巯基水杨酸钠 在凝胶层析中作为抑菌剂使用浓度为0.05-0. 01%。在微酸性溶液中最为有效。重金属离子可使乙基代巯基的物质结合,因而包含疏基的蛋白质可在不同程度上降低它的抑菌效果。⑷苯基汞代盐 在凝胶层析中使用浓度为0.001-0.01%。在微碱性溶液中抑效果最佳,长时间放置时可与卤素、硝酸根离子作用而产生沉淀;还原剂可引起此化合物分解;含疏基的物质亦可降低或抑制它的抑菌作用。
凝胶色谱技术是六十年代初发展起来的一种快速而又简单的分离分技术,由于设备简单、操作方便,不需要有机溶剂,对高分子物质有很高的分离效果。目前已经被生物化学、分子生物学、生物工程学、分子免疫学以及医学等有关领域广泛采用,不但应用于科学实验研究,而且已经大规模地用于工业生产。一、基本理论(一)分子筛效益 一个含有各种分子的样品溶液缓慢地流经凝胶色谱柱时,各分子在柱内同时进行着两种不同的运动:垂直向下的移动和无定向的扩散运动。大分子物质由于直径较大,不易进入凝胶颗粒的微孔,而只能分布颗粒之间,所以在洗脱时向下移动的速度较快。小分子物质除了可在凝胶颗粒间隙中扩散外,还可以进入凝胶颗粒的微孔中,即进入凝胶相内,在向下移动的过程中,从一个凝胶内扩散到颗粒间隙后再进入另一凝胶颗粒,如此不断地进入和扩散,小分子物质的下移速度落后于大分子物质,从而使样品中分子大的先流出色谱柱,中等分子的后流出,分子最小的最后流出,这种现象叫分子筛效应。具有多孔的凝胶就是分子筛。各种分子筛的孔隙大小分布有一定范围,有最大极限和最小极限。分子直径比凝胶最大孔隙直径大的,就会全部被排阻在凝胶颗粒之外,这种情况叫全排阻。两种全排阻的分子即使大小不同,也不能有分离效果。直径比凝胶最小孔直径小的分子能进入凝胶的全部孔隙。如果两种分子都能全部进入凝胶孔隙,即使它们的大小有差别,也不会有好的分离效果。因此,一定的分子筛有它一定的使用范围。综上所述,在凝胶色谱中会有三种情况,一是分子很小,能进入分子筛全部的内孔隙;二是分子很大,完全不能进入凝胶的任何内孔隙;三是分子大小适中,能进入凝胶的内孔隙中孔径大小相应的部分。大、中、小三类分子彼此间较易分开,但每种凝胶分离范围之外的分子,在不改变凝胶种类的情况下是很难分离的。对于分子大小不同,但同属于凝胶分离范围内各种分子,在凝胶床中的分布情况是不同的:分子较大的只能进入孔径较大的那一部分凝胶孔隙内,而分子的可进入较多的凝胶颗粒内,这样分子较大的在凝胶床内移动距离较短,分子较小的移动距离较长。于是分子较大的先通过凝胶床而分子较小的后通过凝胶床,这样就利用分子筛可将分子量不同的物质分离。另外,凝胶本身具有三维网状结构,大的分子在通过这种网状结构上的孔隙时阻力较大,小分子通过时阻力较小。分子量大小不同的多种成份在通过凝胶床时,按照分子量大小“排队,凝胶表现分子筛效应。(二)色谱柱的重要参数⑴柱体积:柱体积是指凝胶装柱后,从柱的底板到凝胶沉积表面的体积。在色谱柱中充满凝胶的部分称为凝胶床,因引柱体积又称“床”体积,常用Vt 表示。⑵外水体积:色谱柱内凝胶颗粒间隙,这部分体积称外水体积,亦称间隙体积,常用Vo表示。⑶内水体积:因为凝胶为三维网状结构,颗粒内部仍有空间,液体可进入颗粒内部,这就分间隙的总和为内水体积,又称定相体积,常用Vi表示。 不包括固体支持物的体积(Vg)。⑷峰洗脱体积:是指被分离物质通过凝胶柱所需洗脱液有体积,常用Ve 表示。当使用样品的体积很少时,(与洗脱体积比较可以忽略不计),在洗脱图中,从加样到峰顶位置所用洗脱液体积为Ve。 当样品体积与洗脱体积比较不能忽略时,洗脱体积计算可以从样品体积的一半到峰顶位置。当样品很大时,洗脱体积计算可以从应用样品开始到洗脱峰升高的弯曲点(或半高处)。 二、凝胶的种类及性质 (一)交联葡聚糖凝胶(Sephadex)⑴Sephadex G交联葡聚糖的商品名为Sephndex,不同规格型号的葡聚糖用英文字母G表示,G后面的阿拉伯数为凝胶得水值的10倍。例如,G-25为每克凝胶膨胀时吸水2.5克,同样G-200克每克千胶吸水20克。交联葡聚糖凝胶的种类有G-10,G-15,G-25,G-50,G-75,G-100,G-150,和G-200。因此,“G”反映,凝胶的交联程度,膨胀程度及分部范围。⑵Sephadex LH-20,是─Sephadex G-25的羧丙基衍生物, 能溶于水及亲脂溶剂,用于分离不溶于水的物质。(二)琼脂糖凝胶: 商品名很多,常见的有,Sepharose(瑞典,pharmacia ),Bio-Gel-A(美国Bio-Rad)等。琼脂糖凝胶是依靠糖链之间的次级链如氢键来维持网状结构,网状结构的疏密依靠琼脂糖的浓度。一般情况下,它的结构是稳定的,可以在许多条件下使用(如水,pH4-9范围内的盐溶液)。琼脂糖凝胶在40℃以上开始融化,也不能高压消毒,可用化学灭菌活处理。(三)聚丙烯酰胺凝胶: 是一种人工合成凝胶,是以丙烯酰胺为单位, 由甲叉双丙烯酰胺交联成的,经干燥粉碎或加工成形制成粒状,控制交联剂的用量可制成各种型号的凝胶。交联剂越多,孔隙越小。聚丙烯酰胺凝胶的商品为生物胶-P (Bio-Gel P),由美国Bio-Rod厂生产,型号很多,从P-2至P-300共10种,P 后面的数字再乘1000就相当于该凝胶的排阻限度。(四)聚苯乙烯凝胶商品为Styrogel , 具有大网孔结构, 可用于分离分子量1600到40,000,000的生物大分子,适用于有机多聚物,分子量测定和脂溶性天然物的分级,凝胶机械强度好,洗脱剂可用甲基亚砜。三、实验技术(一)层析柱 层析柱是凝胶层析技术中的主体,一般用玻璃管或有机玻璃管。层析柱的直径大小不影响分离度,样品用量大,可加大柱的直径,一般制备用凝胶柱,直径大于2厘米,但在加样时应将样品均匀分布于凝胶柱床面上。此外, 直径加大,洗脱液体体积增大,样品稀释度大。分离度取决于柱高,为分离不同组分,凝胶柱床必须有适宜的高度,分离度与柱高的平方根相关,但由于软凝胶柱过高挤压变形阻塞,一般不超过1米。分族分离时用短柱,一般凝胶柱长20-30厘米,柱高与直径的比较5:1─10:1,凝胶床体积为样品溶液体积的4-10倍。 分级分离时柱高与直径之线为20:1─100:1,常用凝胶柱有50×25厘米,10×25厘米。层析柱滤板下的死体积应尽可能的小,如果支掌滤板下的死体积大,被分离组分之间重新混合的可能性就大,其结果是影响洗脱峰形,出现拖尾出象,降低分辩力。在精确分离时,死体积不能超过总床体积的1/1000。(二)凝胶的选择 根据所需凝胶体积,估计所需干胶的量。 一般葡聚糖凝胶吸水后的凝胶体积约为其吸水量的2倍,例如Sephadex G-20的吸水量为20,1 克Sephadex G─200吸水后形成的凝胶体积约40ml。凝胶的粒度也可影响层析分离效果。粒度细胞分离效果好,但阻力大,流速慢。一般实验室分离蛋白质采用100-200号筛目的的Sephadex G-200效果好, 脱盐用Sephadex G-25、G-50,用粗粒,短柱,流速快。(三)凝胶的制备 商品凝胶是干燥的颗粒使用前需直接在欲使用的洗脱液中膨胀。为了加速膨胀,可用加热法,即在沸水浴中将湿凝胶逐渐升温至近沸,这样可大大中速膨胀,通常在1-2小时内即可完成。特别是在使用软胶时, 自然膨胀需24小时至数天,而用加热法在几小时内就可完成。这种方法不但节约时间,而且还可消毒,除去凝胶中污染的细菌和排除胶内的空气。(四)样品溶液的处理 样品溶液如有沉淀应过滤或离心除去,如含脂类可高速离心或通过Sephadex G-15短柱除去。样品的粘度不可大,含蛋白为超过4%,粘度高影响分离效果。上柱样品液的体积根据凝胶床体积的分离要求确定。分离蛋白质样品的体积为凝胶床的1-4%(一般约0.5-2ml),进行分族分离时样品液可为凝胶床的10%,在蛋白质溶液除盐时,样品可达凝胶床的20-30%。 分级分离样品体积要小,使样品层尽可能窄,洗脱出的峰形较好。(五)防止微生物的污染 交联葡聚糖和琼脂糖都是多糖类物质,防止微生物的生长,在凝胶层析中十分重要,常用的抑菌剂有:⑴叠氨钠(NaN3)在凝胶层析中只要用0.02%叠氮钠已足够防止微生物的生长,叠氮钠易溶一水,在20℃时约为40%;它不与蛋白质或碳水化合物相互作用,因此叠氮钠不影响抗体活力;不会改变蛋白质和碳水化合物的层析我特性。叠氮钠可干扰荧光标记蛋白质。⑵可乐酮[Cl3C-C(OH)(CH3)2]在凝胶层析中使用浓度为0.01-0.02%。在微酸性溶液中它的杀菌效果最佳,在强碱性溶液中或温度高于60℃时易引起分解而失效。⑶乙基汞代巯基水杨酸钠 在凝胶层析中作为抑菌剂使用浓度为0.05-0. 01%。在微酸性溶液中最为有效。重金属离子可使乙基代巯基的物质结合,因而包含疏基的蛋白质可在不同程度上降低它的抑菌效果。⑷苯基汞代盐 在凝胶层析中使用浓度为0.001-0.01%。在微碱性溶液中抑效果最佳,长时间放置时可与卤素、硝酸根离子作用而产生沉淀;还原剂可引起此化合物分解;含疏基的物质亦可降低或抑制它的抑菌作用。
凝胶色谱技术是六十年代初发展起来的一种快速而又简单的分离分技术,由于设备简单、操作方便,不需要有机溶剂,对高分子物质有很高的分离效果。目前已经被生物化学、分子生物学、生物工程学、分子免疫学以及医学等有关领域广泛采用,不但应用于科学实验研究,而且已经大规模地用于工业生产。 一、基本理论 (一) 分子筛效益 一个含有各种分子的样品溶液缓慢地流经凝胶色谱柱时,各分子在柱内同时进行着两种不同的运动:垂直向下的移动和无定向的扩散运动。大分子物质由于直径较大,不易进入凝胶颗粒的微孔,而只能分布颗粒之间,所以在洗脱时向下移动的速度较快。小分子物质除了可在凝胶颗粒间隙中扩散外,还可以进入凝胶颗粒的微孔中,即进入凝胶相内,在向下移动的过程中,从一个凝胶内扩散到颗粒间隙后再进入另一凝胶颗粒,如此不断地进入和扩散,小分子物质的下移速度落后于大分子物质,从而使样品中分子大的先流出色谱柱,中等分子的后流出,分子最小的最后流出,这种现象叫分子筛效应。具有多孔的凝胶就是分子筛。各种分子筛的孔隙大小分布有一定范围,有最大极限和最小极限。分子直径比凝胶最大孔隙直径大的,就会全部被排阻在凝胶颗粒之外,这种情况叫全排阻。两种全排阻的分子即使大小不同,也不能有分离效果。直径比凝胶最小孔直径小的分子能进入凝胶的全部孔隙。如果两种分子都能全部进入凝胶孔隙,即使它们的大小有差别,也不会有好的分离效果。因此,一定的分子筛有它一定的使用范围。综上所述,在凝胶色谱中会有三种情况,一是分子很小,能进入分子筛全部的内孔隙;二是分子很大,完全不能进入凝胶的任何内孔隙;三是分子大小适中,能进入凝胶的内孔隙中孔径大小相应的部分。大、中、小三类分子彼此间较易分开,但每种凝胶分离范围之外的分子,在不改变凝胶种类的情况下是很难分离的。对于分子大小不同,但同属于凝胶分离范围内各种分子,在凝胶床中的分布情况是不同的:分子较大的只能进入孔径较大的那一部分凝胶孔隙内,而分子的可进入较多的凝胶颗粒内,这样分子较大的在凝胶床内移动距离较短,分子较小的移动距离较长。于是分子较大的先通过凝胶床而分子较小的后通过凝胶床,这样就利用分子筛可将分子量不同的物质分离。另外,凝胶本身具有三维网状结构,大的分子在通过这种网状结构上的孔隙时阻力较大,小分子通过时阻力较小。分子量大小不同的多种成份在通过凝胶床时,按照分子量大小“排队,凝胶表现分子筛效应。 二)色谱柱的重要参数 ⑴柱体积:柱体积是指凝胶装柱后,从柱的底板到凝胶沉积表面的体积。在色谱柱中充满凝胶的部分称为凝胶床,因引柱体积又称“床”体积,常用Vt 表示。 ⑵外水体积:色谱柱内凝胶颗粒间隙,这部分体积称外水体积,亦称间隙体积,常用Vo表示。 ⑶内水体积:因为凝胶为三维网状结构,颗粒内部仍有空间,液体可进入颗粒内部,这就分间隙的总和为内水体积,又称定相体积,常用Vi表示。 不包括固体支持物的体积(Vg)。 ⑷峰洗脱体积:是指被分离物质通过凝胶柱所需洗脱液有体积,常用Ve 表示。当使用样品的体积很少时,(与洗脱体积比较可以忽略不计),在洗脱图中,从加样到峰顶位置所用洗脱液体积为Ve。 当样品体积与洗脱体积比较不能忽略时,洗脱体积计算可以从样品体积的一半到峰顶位置。当样品很大时,洗脱体积计算可以从应用样品开始到洗脱峰升高的弯曲点(或半高处)。 二、凝胶的种类及性质 (一) 交联葡聚糖凝胶 ⑴Sephadex G交联葡聚糖的商品名为Sephndex,不同规格型号的葡聚糖用英文字母G表示,G后面的阿拉伯数为凝胶得水值的10倍。例如,G-25为每克凝胶膨胀时吸水2.5克,同样G-200克每克千胶吸水20克。交联葡聚糖凝胶的种类有G-10,G-15,G-25,G-50,G-75,G-100,G-150,和G-200。因此,“G”反映,凝胶的交联程度,膨胀程度及分部范围。 ⑵Sephadex LH-20,是─Sephadex G-25的羧丙基衍生物, 能溶于水及亲脂溶剂,用于分离不溶于水的物质。 (二) 琼脂糖凝胶: 商品名很多,常见的有,Sepharose(瑞典,pharmacia ),Bio-Gel-A(美国Bio-Rad)等。琼脂糖凝胶是依靠糖链之间的次级链如氢键来维持网状结构,网状结构的疏密依靠琼脂糖的浓度。一般情况下,它的结构是稳定的,可以在许多条件下使用(如水,pH4-9范围内的盐溶液)。琼脂糖凝胶在40℃以上开始融化,也不能高压消毒,可用化学灭菌活处理。 (三)聚丙烯酰胺凝胶:是一种人工合成凝胶,是以丙烯酰胺为单位, 由甲叉双丙烯酰胺交联成的,经干燥粉碎或加工成形制成粒状,控制交联剂的用量可制成各种型号的凝胶。交联剂越多,孔隙越小。聚丙烯酰胺凝胶的商品为生物胶-P (Bio-Gel P),由美国Bio-Rod厂生产,型号很多,从P-2至P-300共10种,P 后面的数字再乘1000就相当于该凝胶的排阻限度。 (四)聚苯乙烯凝胶商品为Styrogel , 具有大网孔结构, 可用于分离分子量1600到40,000,000的生物大分子,适用于有机多聚物,分子量测定和脂溶性天然物的分级,凝胶机械强度好,洗脱剂可用甲基亚砜。 三、实验技术 (一)层析柱 层析柱是凝胶层析技术中的主体,一般用玻璃管或有机玻璃管。层析柱的直径大小不影响分离度,样品用量大,可加大柱的直径,一般制备用凝胶柱,直径大于2厘米,但在加样时应将样品均匀分布于凝胶柱床面上。此外, 直径加大,洗脱液体体积增大,样品稀释度大。分离度取决于柱高,为分离不同组分,凝胶柱床必须有适宜的高度,分离度与柱高的平方根相关,但由于软凝胶柱过高挤压变形阻塞,一般不超过1米。分族分离时用短柱,一般凝胶柱长20-30厘米,柱高与直径的比较5:1─10:1,凝胶床体积为样品溶液体积的4-10倍。 分级分离时柱高与直径之线为20:1─100:1,常用凝胶柱有50×25厘米,10×25厘米。层析柱滤板下的死体积应尽可能的小,如果支掌滤板下的死体积大,被分离组分之间重新混合的可能性就大,其结果是影响洗脱峰形,出现拖尾出象,降低分辩力。在精确分离时,死体积不能超过总床体积的1/1000。 (二)凝胶的选择 根据所需凝胶体积,估计所需干胶的量。 一般葡聚糖凝胶吸水后的凝胶体积约为其吸水量的2倍,例如Sephadex G-20的吸水量为20,1 克Sephadex G─200吸水后形成的凝胶体积约40ml。凝胶的粒度也可影响层析分离效果。粒度细胞分离效果好,但阻力大,流速慢。一般实验室分离蛋白质采用100-200号筛目的的Sephadex G-200效果好, 脱盐用Sephadex G-25、G-50,用粗粒,短柱,流速快。 (三)凝胶的制备 商品凝胶是干燥的颗粒使用前需直接在欲使用的洗脱液中膨胀。为了加速膨胀,可用加热法,即在沸水浴中将湿凝胶逐渐升温至近沸,这样可大大中速膨胀,通常在1-2小时内即可完成。特别是在使用软胶时, 自然膨胀需24小时至数天,而用加热法在几小时内就可完成。这种方法不但节约时间,而且还可消毒,除去凝胶中污染的细菌和排除胶内的空气。 (四)样品溶液的处理 样品溶液如有沉淀应过滤或离心除去,如含脂类可高速离心或通过Sephadex G-15短柱除去。样品的粘度不可大,含蛋白为超过4%,粘度高影响分离效果。上柱样品液的体积根据凝胶床体积的分离要求确定。分离蛋白质样品的体积为凝胶床的1-4%(一般约0.5-2ml),进行分族分离时样品液可为凝胶床的10%,在蛋白质溶液除盐时,样品可达凝胶床的20-30%。 分级分离样品体积要小,使样品层尽可能窄,洗脱出的峰形较好。 (五)防止微生物的污染 交联葡聚糖和琼脂糖都是多糖类物质,防止微生物的生长,在凝胶层析中十分重要,常用的抑菌剂有: ⑴叠氨钠(NaN3)在凝胶层析中只要用0.02%叠氮钠已足够防止微生物的生长,叠氮钠易溶一水,在20℃时约为40%;它不与蛋白质或碳水化合物相互作用,因此叠氮钠不影响抗体活力;不会改变蛋白质和碳水化合物的层析我特性。叠氮钠可干扰荧光标记蛋白质。 ⑵可乐酮[Cl3C-C(OH)(CH3)2]在凝胶层析中使用浓度为0.01-0.02%。在微酸性溶液中它的杀菌效果最佳,在强碱性溶液中或温度高于60℃时易引起分解而失效。 ⑶乙基汞代巯基水杨酸钠 在凝胶层析中作为抑菌剂使用浓度为0.05-0. 01%。在微酸性溶液中最为有效。重金属离子可使乙基代巯基的物质结合,因而包含疏基的蛋白质可在不同程度上降低它的抑菌效果。 ⑷苯基汞代盐 在凝胶层析中使用浓度为0.001-0.01%。在微碱性溶液中抑效果最佳,长时间放置时可与卤素、硝酸根离子作用而产生沉淀;还原剂可引起此化合物分解;含疏基的物质亦可降低或抑制它的抑菌作用。
国标5009.19中食品中有机氯农药多组分残留量的测定中,采用凝胶色谱层析纯化,用哪种固相萃取柱可替代?
背景知识:凝胶色谱技术是六十年代初发展起来的一种快速而又简单的分离分技术,由于设备简单、操作方便,不需要有机溶剂,对高分子物质有很高的分离效果。目前已经被生物化学、分子生物学、生物工程学、分子免疫学以及医学等有关领域广泛采用,不但应用于科学实验研究,而且已经大规模地用于工业生产。一、基本理论(一)分子筛效益 一个含有各种分子的样品溶液缓慢地流经凝胶色谱柱时,各分子在柱内同时进行着两种不同的运动:垂直向下的移动和无定向的扩散运动。大分子物质由于直径较大,不易进入凝胶颗粒的微孔,而只能分布颗粒之间,所以在洗脱时向下移动的速度较快。小分子物质除了可在凝胶颗粒间隙中扩散外,还可以进入凝胶颗粒的微孔中,即进入凝胶相内,在向下移动的过程中,从一个凝胶内扩散到颗粒间隙后再进入另一凝胶颗粒,如此不断地进入和扩散,小分子物质的下移速度落后于大分子物质,从而使样品中分子大的先流出色谱柱,中等分子的后流出,分子最小的最后流出,这种现象叫分子筛效应。具有多孔的凝胶就是分子筛。各种分子筛的孔隙大小分布有一定范围,有最大极限和最小极限。分子直径比凝胶最大孔隙直径大的,就会全部被排阻在凝胶颗粒之外,这种情况叫全排阻。两种全排阻的分子即使大小不同,也不能有分离效果。直径比凝胶最小孔直径小的分子能进入凝胶的全部孔隙。如果两种分子都能全部进入凝胶孔隙,即使它们的大小有差别,也不会有好的分离效果。因此,一定的分子筛有它一定的使用范围。综上所述,在凝胶色谱中会有三种情况,一是分子很小,能进入分子筛全部的内孔隙;二是分子很大,完全不能进入凝胶的任何内孔隙;三是分子大小适中,能进入凝胶的内孔隙中孔径大小相应的部分。大、中、小三类分子彼此间较易分开,但每种凝胶分离范围之外的分子,在不改变凝胶种类的情况下是很难分离的。对于分子大小不同,但同属于凝胶分离范围内各种分子,在凝胶床中的分布情况是不同的:分子较大的只能进入孔径较大的那一部分凝胶孔隙内,而分子的可进入较多的凝胶颗粒内,这样分子较大的在凝胶床内移动距离较短,分子较小的移动距离较长。于是分子较大的先通过凝胶床而分子较小的后通过凝胶床,这样就利用分子筛可将分子量不同的物质分离。另外,凝胶本身具有三维网状结构,大的分子在通过这种网状结构上的孔隙时阻力较大,小分子通过时阻力较小。分子量大小不同的多种成份在通过凝胶床时,按照分子量大小“排队,凝胶表现分子筛效应。(二)色谱柱的重要参数⑴柱体积:柱体积是指凝胶装柱后,从柱的底板到凝胶沉积表面的体积。在色谱柱中充满凝胶的部分称为凝胶床,因引柱体积又称“床”体积,常用Vt 表示。⑵外水体积:色谱柱内凝胶颗粒间隙,这部分体积称外水体积,亦称间隙体积,常用Vo表示。⑶内水体积:因为凝胶为三维网状结构,颗粒内部仍有空间,液体可进入颗粒内部,这就分间隙的总和为内水体积,又称定相体积,常用Vi表示。 不包括固体支持物的体积(Vg)。⑷峰洗脱体积:是指被分离物质通过凝胶柱所需洗脱液有体积,常用Ve 表示。当使用样品的体积很少时,(与洗脱体积比较可以忽略不计),在洗脱图中,从加样到峰顶位置所用洗脱液体积为Ve。 当样品体积与洗脱体积比较不能忽略时,洗脱体积计算可以从样品体积的一半到峰顶位置。当样品很大时,洗脱体积计算可以从应用样品开始到洗脱峰升高的弯曲点(或半高处)。二、凝胶的种类及性质 (一)交联葡聚糖凝胶(Sephadex)⑴Sephadex G交联葡聚糖的商品名为Sephndex,不同规格型号的葡聚糖用英文字母G表示,G后面的阿拉伯数为凝胶得水值的10倍。例如,G-25为每克凝胶膨胀时吸水2.5克,同样G-200克每克千胶吸水20克。交联葡聚糖凝胶的种类有G-10,G-15,G-25,G-50,G-75,G-100,G-150,和G-200。因此,“G”反映,凝胶的交联程度,膨胀程度及分部范围。⑵Sephadex LH-20,是─Sephadex G-25的羧丙基衍生物, 能溶于水及亲脂溶剂,用于分离不溶于水的物质。(二)琼脂糖凝胶: 商品名很多,常见的有,Sepharose(瑞典,pharmacia ),Bio-Gel-A(美国Bio-Rad)等。琼脂糖凝胶是依靠糖链之间的次级链如氢键来维持网状结构,网状结构的疏密依靠琼脂糖的浓度。一般情况下,它的结构是稳定的,可以在许多条件下使用(如水,pH4-9范围内的盐溶液)。琼脂糖凝胶在40℃以上开始融化,也不能高压消毒,可用化学灭菌活处理。(三)聚丙烯酰胺凝胶: 是一种人工合成凝胶,是以丙烯酰胺为单位, 由甲叉双丙烯酰胺交联成的,经干燥粉碎或加工成形制成粒状,控制交联剂的用量可制成各种型号的凝胶。交联剂越多,孔隙越小。聚丙烯酰胺凝胶的商品为生物胶-P (Bio-Gel P),由美国Bio-Rod厂生产,型号很多,从P-2至P-300共10种,P 后面的数字再乘1000就相当于该凝胶的排阻限度。(四)聚苯乙烯凝胶商品为Styrogel , 具有大网孔结构, 可用于分离分子量1600到40,000,000的生物大分子,适用于有机多聚物,分子量测定和脂溶性天然物的分级,凝胶机械强度好,洗脱剂可用甲基亚砜。三、实验技术(一)层析柱 层析柱是凝胶层析技术中的主体,一般用玻璃管或有机玻璃管。层析柱的直径大小不影响分离度,样品用量大,可加大柱的直径,一般制备用凝胶柱,直径大于2厘米,但在加样时应将样品均匀分布于凝胶柱床面上。此外, 直径加大,洗脱液体体积增大,样品稀释度大。分离度取决于柱高,为分离不同组分,凝胶柱床必须有适宜的高度,分离度与柱高的平方根相关,但由于软凝胶柱过高挤压变形阻塞,一般不超过1米。分族分离时用短柱,一般凝胶柱长20-30厘米,柱高与直径的比较5:1─10:1,凝胶床体积为样品溶液体积的4-10倍。 分级分离时柱高与直径之线为20:1─100:1,常用凝胶柱有50×25厘米,10×25厘米。层析柱滤板下的死体积应尽可能的小,如果支掌滤板下的死体积大,被分离组分之间重新混合的可能性就大,其结果是影响洗脱峰形,出现拖尾出象,降低分辩力。在精确分离时,死体积不能超过总床体积的1/1000。(二)凝胶的选择根据所需凝胶体积,估计所需干胶的量。 一般葡聚糖凝胶吸水后的凝胶体积约为其吸水量的2倍,例如Sephadex G-20的吸水量为20,1 克Sephadex G─200吸水后形成的凝胶体积约40ml。凝胶的粒度也可影响层析分离效果。粒度细胞分离效果好,但阻力大,流速慢。一般实验室分离蛋白质采用100-200号筛目的的Sephadex G-200效果好, 脱盐用Sephadex G-25、G-50,用粗粒,短柱,流速快。(三)凝胶的制备商品凝胶是干燥的颗粒使用前需直接在欲使用的洗脱液中膨胀。为了加速膨胀,可用加热法,即在沸水浴中将湿凝胶逐渐升温至近沸,这样可大大中速膨胀,通常在1-2小时内即可完成。特别是在使用软胶时, 自然膨胀需24小时至数天,而用加热法在几小时内就可完成。这种方法不但节约时间,而且还可消毒,除去凝胶中污染的细菌和排除胶内的空气。(四)样品溶液的处理 样品溶液如有沉淀应过滤或离心除去,如含脂类可高速离心或通过Sephadex G-15短柱除去。样品的粘度不可大,含蛋白为超过4%,粘度高影响分离效果。上柱样品液的体积根据凝胶床体积的分离要求确定。分离蛋白质样品的体积为凝胶床的1-4%(一般约0.5-2ml),进行分族分离时样品液可为凝胶床的10%,在蛋白质溶液除盐时,样品可达凝胶床的20-30%。 分级分离样品体积要小,使样品层尽可能窄,洗脱出的峰形较好。(五)防止微生物的污染 交联葡聚糖和琼脂糖都是多糖类物质,防止微生物的生长,在凝胶层析中十分重要,常用的抑菌剂有:⑴叠氨钠(NaN3)在凝胶层析中只要用0.02%叠氮钠已足够防止微生物的生长,叠氮钠易溶一水,在20℃时约为40%;它不与蛋白质或碳水化合物相互作用,因此叠氮钠不影响抗体活力;不会改变蛋白质和碳水化合物的层析我特性。叠氮钠可干扰荧光标记蛋白质。⑵可乐酮在凝胶层析中使用浓度为0.01-0.02%。在微酸性溶液中它的杀菌效果最佳,在强碱性溶液中或温度高于60℃时易引起分解而失效。⑶乙基汞代巯基水杨酸钠 在凝胶层析中作为抑菌剂使用浓度为0.05-0. 01%。在微酸性溶液中最为有效。重金属离子可使乙基代巯基的物质结合,因而包含疏基的蛋白质可在不同程度上降低它的抑菌效果。⑷苯基汞代盐 在凝胶层析中使用浓度为0.001-0.01%。在微碱性溶液中抑效果最佳,长时间放置时可与卤素、硝酸根离子作用而产生沉淀;还原剂可引起此化合物分解;含疏基的物质亦可降低或抑制它的抑菌作用。原理:选填项目主体内容:一、 实验室要求:凝胶色谱仪所使用流动相多为有毒的有机性试剂,实验室要保持良好的通风条件,试剂需专柜保存。实验室温度需保持在10℃~35℃,湿度小于80%。周围无腐蚀性气体,无尘土飞扬。二、实验台要求:实验台要求通水电良好,电源为220V±20 V,电源频率为50Hz±0.5 Hz,无剧烈震动。三、仪器摆放要求:仪器放在无阳光直射的地方,不要放在靠门、窗的地方,以减少空气、阳光对仪器带来的影响。四、仪器操作规范: 样品经充分溶解后,再用过滤器过滤后才可使用;流动相也需现配后,再过滤使用;所有选用试剂均需选用色谱纯试剂。新色谱柱初次使用流速设置为0.2ml/min,冲洗1小时后再接检测器
本人现在要做塑化剂,但没有GPC纯化系统,买了bio beads(s-x3)凝胶想自己装,该怎么装呢?装好后怎么活化啊?各位请帮帮忙,多谢了!此外,上样后的洗脱液要全部收集吗?单用正已烷洗脱行不?标准是收集5.5-16.5min的流出液的呀!
凝胶过滤填料的类型及性质 具有分子筛作用的物质很多,如浮石、琼脂、琼脂糖、聚乙烯醇、聚丙烯酰胺、葡聚糖凝胶等。层析用凝胶都是三维空间的网状高聚物,有一定的孔径和交联度。它们不溶于水,但在水中有较大的膨胀度,具有良好的分子筛功能。它们可分离的分子大小的范围广,相对分子质量在102~108范围之间。在柱层析分离中常用的凝胶有以下几类: 1.交联葡聚糖凝胶 交联葡聚糖凝胶的商品名称为Sephadex,由葡聚糖和3-氯-1.2-环氧丙烷(交联剂)以醚键相互交联而形成具有三维空间多孔网状结构的高分子化合物。交联葡聚糖凝胶,按其交联度大小分成8种型号如表3所示。交联度越大,网状结构越紧密,孔径越小,吸水膨胀就愈小,故只能分离相对分子质量较小的物质;而交联度越小,孔径就越大,吸水膨胀大,则可分离相对分子质量较大的物质。各种型号是以其吸水量(每g干胶所吸收的水的质量)的10倍命名,如,Sephadex G–25表示该凝胶的吸水量为每g干胶能吸2.5克水。在SephadexG–25及G–50中分别引入羟丙基基团,即可构成LH型烷基化葡聚糖凝胶。 表3 Sephadex1的种类与特性型号分离范围(分子量)吸水量(ml/g)最小溶胀时(h)床体积(ml)/(mg)20℃~25℃100℃G10<7001.0±0.1312~3G15<1 5001.5±0.2312.5~3.5G25<5 0002.5±0.2314~6G501500~20 0008.0±0.3319~11G753 000~70 0007.5±0.524112~15G1004 000~15 00010.0±1.072115~20G1505 000~800 00015.0±1.572120~30G2005 000~30 000020.0±2.072130~40 交联葡聚糖凝胶在水溶液、盐溶液、碱溶液、弱酸溶液和有机溶剂中较稳定,但当暴露于强酸或氧化剂溶液中,则易使糖甘键水解断裂。在中性条件下,交联葡聚糖凝胶悬浮液能耐高温,用120℃消毒10分钟而不改变其性质。如要在室温下长期保存,应加入适量防腐剂,如氯仿、叠氮钠等,以免微生物生长。 交联葡聚糖凝胶由于有羧基基团,故能与分离物质中的电荷基团(如碱性蛋白质)发生吸附作用,但可借助提高洗脱液的离子强度得以克服。因此在进行凝胶层析时,常用含有NaCl的缓冲溶液作洗脱液。交联葡聚糖凝胶可用于分离蛋白质、核酸、酶、多糖、多肽、氨基酸、抗菌素,也可用于高分子物质样品的脱盐及测定蛋白质的相对分子质量。 2.琼脂糖凝胶 琼脂糖的商品名称有Sepharose(瑞典)、Bio-gelA(美国)、Segavac(英国)、Gelarose(丹麦)等多种,因生产厂家不同名称各异。琼脂糖是由D-半乳糖和3,6位脱水的L-半乳糖连接构成的多糖链,在温度10O℃时呈液态,当下降至45℃以下时,它们之间相互连接成线性双链单环的琼脂糖;再凝聚即呈琼脂糖凝胶。商品除Segavac外,都制备成珠状琼脂糖凝胶。琼脂糖凝胶按其浓度不同,分为Sepharose 2B(浓度为2%)、4B(浓度为4%)及6B(浓度为6%)。Sepharose与1,3-二溴异丙醇在强碱条件下反应,即生成CL型交联琼脂糖,其热稳定性和化学稳定性均有所提高,可在广泛pH溶液(pH3~14)中使用。通常的Sepharose只能在pH4.5~9.0范围内使用。琼脂糖凝胶在干燥状态下保存易破裂,故一般均存放在含防腐剂的水溶液中。 琼脂糖凝胶的机械强度和筛孔的稳定性均优于交联葡聚糖凝胶。琼脂糖凝胶用于柱层析时,流速较快,因此是一种很好的凝胶层析载体。
生物分子下游纯化的对象一般包括蛋白、酶、重组蛋白、单抗、抗体及抗原、肽类、病毒、核酸等。纯化前首先需要测定生物分子的各物理和化学特性,然后通过实验选择出最有效的纯化流程。 1.测定------分子量、PI 当目标蛋白的物理特性如分子量、PI等都不清楚时,可用PAGE电泳方法或层析方法加以测定。分离范围广阔的Superose HR预装柱很适合测定未知蛋白的分子量。用少量离子交换介质在多个含不同PH缓冲液的试管中,可简易地测出PI,并选择纯化用缓冲液的最佳PH。 2.选择------层析方法 若对目标蛋白的特性或样品成分不太了解,可尝试几种不同的纯化方法: 一] 使用最通用的凝胶过滤方法,选择分离范围广阔的介质如Superose、Sephacryl HR依据分子量将 样品分成不同组份。 二] 用含专一配体或抗体的亲和层析介质结合目标蛋白。亦可用各种活化偶联介质偶联目标蛋白的底物、受体等自制亲和介质,再用以结合目标蛋白。一步即可得到高纯度样品。 三] 体积大的样品,往往使用离子交换层析加以浓缩及粗纯化。高盐洗脱的样品,可再用疏水层析纯化。疏水层析利用高盐吸附、低盐洗脱的原理,洗脱样品又可直接上离子交换等吸附性层析。两种方法常被交替使用于纯化流程中。 3.纯化------大量粗品 处理大量原液时,为避免堵塞柱子,一般使用sepharose big beads、sepharoseXL、sepharose fast flow等大颗粒离子交换介质。扩张柱床吸附技术利用多种STREAMLINE介质,直接从含破碎细胞或组织萃取物的发酵液中俘获蛋白。将离心、超滤、初纯化结合为一。提高回收率,缩短纯化周期。 4.纯化------硫酸氨样品 硫酸氨沉淀方法常被用来初步净化样品,经处理过的样本处于高盐状态下,很适合直接上疏水层析。若作离子交换,需先用Sephadex G-25脱盐。疏水层析是较新技术,随着介质种类不断增多,渐被融入各生产工艺中。利用Hitrap HIC Test Kit 和RESOURCE HIC Test Kit可在八种疏水介质中选择最适合介质及最佳的纯化条件。低盐洗脱的样品可稍加稀释或直接上其它吸附性层析。 5.纯水-----糖类分子 固化外源凝订素如刀豆球蛋白、花生、大麦等凝集素,可结合碳水化合物的糖类残基,很适合用作分离糖化细胞膜组份、细胞、甚至亚细胞细胞器,纯化糖蛋白等。两种附上外源凝集素的Sepharose 6MB亲和层析介质,专为俘获整个细胞或大复合物,如膜囊等。 6.纯化------膜蛋白 膜蛋白分离常使用去污剂以保持其活性。离子性去污剂应选用与目标蛋白相反电荷者,避免在作离子交换时和目标蛋白竞争交换介质,籍此除去去污剂。非离子性去污剂可以疏水层析除去。 7.纯化------单抗、抗原 *单抗多为IgG。来源主要是腹水和融合瘤培养上清液。腹水有大量白蛋白、转铁蛋白和宿主抗体等。Mabselect、Protein G和Protein A对IgG的Fc区有专一性亲和作用,能一步纯化各种不同源的IgG。血清互补剂如小牛血清可先用蛋白G预处理,在培养前除去IgG。重组蛋白A介质Mabselect和rProtein A Sepharose FF对IgG有更高的载量和专一性,基团脱落更少。脱落的rProtein A用离子交换Q Sepharose HP或凝胶过滤Superdex 200,很容易去除。 *疏水层析Phenyl Sepharose HP亦很适合纯化IgG。宿主抗体和污染IgG可用凝胶过滤Superdex 200在精细纯化中去除。 *纯化IgG抗原最有效的方法是用活化偶联介质如CNBr、NHs activated Sepharose FF偶联IgG,再进一步获取IgG抗原。 *HiTrap IgM是用来纯化融合瘤细胞培养的单抗IgM,结合量达5mg IgM。HiTrap IgY是专门用来纯化IgY,结合量达100mg纯IgY。 8.纯化------重组蛋白 重组蛋白在设计、构建时应已融入纯化构想。样品多夹杂了破碎细胞或溶解产物,扩张柱床吸附技术STREAMLINE便很适合做粗分离。Amersham biosciences提供三个快速表达、一步纯化的融合系统。 一] GST融合载体使要表达的蛋白和谷胱甘肽S转移酶一起表达,然后利用Glutathione Sepharose 4B作亲和层析纯化,再利用凝血酶或因子Xa切开。 2. 蛋白A融合载体使要表达的蛋白和蛋白A的IgG结合部位融合在一起表达,以IgG Sepharose 6 FF纯化。 二] 含组氨酸标记(Histidine-tagged)的融合蛋白可用Chelating Sepharose FF螯合Ni2+金属,在一般或变性条件(8M尿素)下透过组氨酸螯合融合蛋白。HisTrap试剂盒提供整套His-Tag蛋白的纯化方法。 9.纯化------包涵体蛋白 包涵体蛋白往往需溶于6M盐酸胍或8M尿素中。高化学稳定性的Superose 12及Sepharose 6FF凝胶过滤介质很适合在变性条件下做纯化。变性纯化后的蛋白需要复性至蛋白的天然构象。Superdex 75、Q Sepharose FF和Phenyl Sepharose FF分别被发现有助包涵体蛋白的复性。一般包涵体蛋白样品的纯度越高,复性效果越好。SOURCE 30 RPC反相层析介质很适合纯化复性前的粗品,并可以1MnaOH重生。此方法纯化后的包涵体蛋白,复性回收率明显提高。 10.包涵体蛋白固相复性 *近年许多文献报导将包涵体蛋白在变性条件下固定(吸附)在层析介质上,一般用各种Sepharose FF离子交换层析介质。去除变性剂后,蛋白在介质上成功复性,再将复性好的蛋白洗脱下来。固相复性避免了一般复性过程中蛋白质聚体的形成,所以复性得率更高,而且无需大量稀释样品,并将复性和初纯化合二为一,大大节省时间及提高回收率。 *固相复性方法也被用于以HiTrap Chelating金属螯合层析直接复性及纯化包涵体形式表达的组氨酸融合蛋白;以HiTrap Heparin肝素亲和层析直接复性及纯化包涵体形式表达的含多个赖氨酸的融合蛋白。两种亲和层析预装柱均可反复多次重复使用,比一般试剂盒更方便、耐用。 11.纯化------中草药有效成分 中药的化学成分极其复杂。传统中药多是煎熬后服用,有效成份多较为亲水,包括生物碱、黄酮、蒽醌、皂甙、有机酸、多糖、肽和蛋白质。灵活及综合性地利用多种层析方法。如离子交换、分子筛、反相层析,更容易分离到单一活性成分。Sephadex LH-20葡聚糖凝胶同时具备吸附性层析和分子筛功能,例:如用甲醇分离黄酮甙,三糖甙先被洗下来,二糖甙其次,单糖甙随后,最后是甙元。Sephadex LH-20可使用水、醇、丙酮、氯仿等各种试剂,广泛用于各种天然产物的分离,包括生物碱、甙、黄酮、醌类、内脂、萜类、甾类等。 *生物碱在酸性缓冲液中带正电,成为盐,HiTrap SP阳离子交换层析柱可以分离许多结构非常近似的生物碱。相反,黄酮、蒽醌、皂甙、有机酸等可溶于偏碱的缓冲液中,在HiTrap Q阴离子交换柱上分离效果良好。 *一般多糖纯化大多使用分子筛如Sephadex,Sephacryl。若分子量在600KD以下,并需更高分辨率,可选择新一代的Superdex。一般植物可能含水溶性、酸溶性、碱溶性多种多糖。综合利用分子筛及离子交换层析有助进一步获各组份纯品。另外,多糖药物需去除可引起过敏的蛋白质,传统Sevag方法用丁醇脱蛋白需反复数十次。阴阳离子交换法可以一、两步快速去除多糖中残存的蛋白质。SOURCE5、15、30RPC反相层析也很适合各种中药有效成分的检测、分离和放大制备。由于中药的成分非常复杂,SOURCE反相层析可用范围为PH1-14 ,并可用1M NaOH,1M HCL清洗、再生。比传统硅胶反相层析更易于工艺优化及在位清洗,寿命也更长。
简介:生物分子下游纯化的对象一般包括蛋白、酶、重组蛋白、单抗、抗体及抗原、肽类、病毒、核酸等。纯化前首先需要测定生物分子的各物理和化学特性,然后通过实验选择出最有效的纯化流程。内容:1.测定------分子量、PI 当目标蛋白的物理特性如分子量、PI等都不清楚时,可用PAGE电泳方法或层析方法加以测定。分离范围广阔的Superose HR预装柱很适合测定未知蛋白的分子量。用少量离子交换介质在多个含不同PH缓冲液的试管中,可简易地测出PI,并选择纯化用缓冲液的最佳PH。 2.选择------层析方法 若对目标蛋白的特性或样品成分不太了解,可尝试几种不同的纯化方法:一 使用最通用的凝胶过滤方法,选择分离范围广阔的介质如Superose、Sephacryl HR依据分子量将 样品分成不同组份。二 用含专一配体或抗体的亲和层析介质结合目标蛋白。亦可用各种活化偶联介质偶联目标蛋白的底物、受体等自制亲和介质,再用以结合目标蛋白。一步即可得到高纯度样品。三 体积大的样品,往往使用离子交换层析加以浓缩及粗纯化。高盐洗脱的样品,可再用疏水层析纯化。疏水层析利用高盐吸附、低盐洗脱的原理,洗脱样品又可直接上离子交换等吸附性层析。两种方法常被交替使用于纯化流程中。3.纯化------大量粗品 处理大量原液时,为避免堵塞柱子,一般使用sepharose big beads、sepharoseXL、sepharose fast flow等大颗粒离子交换介质。扩张柱床吸附技术利用多种STREAMLINE介质,直接从含破碎细胞或组织萃取物的发酵液中俘获蛋白。将离心、超滤、初纯化结合为一。提高回收率,缩短纯化周期。 4.纯化------硫酸氨样品 硫酸氨沉淀方法常被用来初步净化样品,经处理过的样本处于高盐状态下,很适合直接上疏水层析。若作离子交换,需先用Sephadex G-25脱盐。疏水层析是较新技术,随着介质种类不断增多,渐被融入各生产工艺中。利用Hitrap HIC Test Kit 和RESOURCE HIC Test Kit可在八种疏水介质中选择最适合介质及最佳的纯化条件。低盐洗脱的样品可稍加稀释或直接上其它吸附性层析。5.纯水-----糖类分子 固化外源凝订素如刀豆球蛋白、花生、大麦等凝集素,可结合碳水化合物的糖类残基,很适合用作分离糖化细胞膜组份、细胞、甚至亚细胞细胞器,纯化糖蛋白等。两种附上外源凝集素的Sepharose 6MB亲和层析介质,专为俘获整个细胞或大复合物,如膜囊等。6.纯化------膜蛋白 膜蛋白分离常使用去污剂以保持其活性。离子性去污剂应选用与目标蛋白相反电荷者,避免在作离子交换时和目标蛋白竞争交换介质,籍此除去去污剂。非离子性去污剂可以疏水层析除去。7.纯化------单抗、抗原 *单抗多为IgG。来源主要是腹水和融合瘤培养上清液。腹水有大量白蛋白、转铁蛋白和宿主抗体等。Mabselect、Protein G和Protein A对IgG的Fc区有专一性亲和作用,能一步纯化各种不同源的IgG。血清互补剂如小牛血清可先用蛋白G预处理,在培养前除去IgG。重组蛋白A介质Mabselect和rProtein A Sepharose FF对IgG有更高的载量和专一性,基团脱落更少。脱落的rProtein A用离子交换Q Sepharose HP或凝胶过滤Superdex 200,很容易去除。*疏水层析Phenyl Sepharose HP亦很适合纯化IgG。宿主抗体和污染IgG可用凝胶过滤Superdex 200在精细纯化中去除。*纯化IgG抗原最有效的方法是用活化偶联介质如CNBr、NHs activated Sepharose FF偶联IgG,再进一步获取IgG抗原。*HiTrap IgM是用来纯化融合瘤细胞培养的单抗IgM,结合量达5mg IgM。HiTrap IgY是专门用来纯化IgY,结合量达100mg纯IgY。8.纯化------重组蛋白 重组蛋白在设计、构建时应已融入纯化构想。样品多夹杂了破碎细胞或溶解产物,扩张柱床吸附技术STREAMLINE便很适合做粗分离。Amersham biosciences提供三个快速表达、一步纯化的融合系统。一 GST融合载体使要表达的蛋白和谷胱甘肽S转移酶一起表达,然后利用Glutathione Sepharose 4B作亲和层析纯化,再利用凝血酶或因子Xa切开。蛋白A融合载体使要表达的蛋白和蛋白A的IgG结合部位融合在一起表达,以IgG Sepharose 6 FF纯化。二 含组氨酸标记(Histidine-tagged)的融合蛋白可用Chelating Sepharose FF螯合Ni2+金属,在一般或变性条件(8M尿素)下透过组氨酸螯合融合蛋白。HisTrap试剂盒提供整套His-Tag蛋白的纯化方法。9.纯化------包涵体蛋白 包涵体蛋白往往需溶于6M盐酸胍或8M尿素中。高化学稳定性的Superose 12及Sepharose 6FF凝胶过滤介质很适合在变性条件下做纯化。变性纯化后的蛋白需要复性至蛋白的天然构象。Superdex 75、Q Sepharose FF和Phenyl Sepharose FF分别被发现有助包涵体蛋白的复性。一般包涵体蛋白样品的纯度越高,复性效果越好。SOURCE 30 RPC反相层析介质很适合纯化复性前的粗品,并可以1MnaOH重生。此方法纯化后的包涵体蛋白,复性回收率明显提高。
净化食用油苯并芘的凝胶渗透色谱仪、凝胶柱填料如何选择?Biologic LP的凝胶层析仪能用吗?