体内药物分析方法的设计与评价 一、分析方法的设定依据:(一)重视并做好文献总结、整理工作;(二)充分了解待测药物的特性及体内存在状况;(三)明确测定的目的要求;(四)实验室条件。二、方法建立的一般实验步骤:(一)以纯品进行测定:以一定量纯品按拟定方法进行测定。求得浓度与测定响应值之间(如吸收度、色谱峰高或面积等)的关系,浓度线性范围,最适测定浓度,检测灵敏度,测定的最适条件(pH、温度、反应时间)等等。(二)以经过纯化处理过的空白样品进行测定;(三)空白样品添加标准后的测定:血样等样品中添加一定量标准品后进行测定,求得样品回收率数据,检验生物样品对测定有无干扰等。(四) 体内实际样品测定:有时用体外建立的方法去测定体内取得的实样时,会得出错误的结论。故要强调对药物体内过程有一定程度的了解。有时也采用专属性强、已证明适用于体内实样测定的步骤和方法作为对照测定,并以此来检验所建立的方法的实际可行性。三、方法的评价:(一)准确度(Accuracy):测定结果与真值的符合程度。常用回收率(Recovery)数值间接反映测定的准确程度;也可通过与其他已建立的方法进行比较的办法(参比方法)来加以反映。回收率100%当然好,但很难达到。重要的是每次测定要保持稳定。(二)精密度(Precision):测定结果与平均值的偏离程度。测定间偏差越小,对测定的要求也越高(花费大);浓度与RSD值间存在反比关系,RSD在10%以内的方法可认为是可接受的。(三)灵敏度(Sensitivity):“一种方法可以检测出有关化合物的最小量”。常用最低检测限(Limit of detection,LOD)或最低检测量(Limit of quantification;LOQ)来表示。LOD范围在ng(10-9g)~10-18g。(四)专属性或选择性(Specificity or Selectivity):是指测定的信号(响应)是属于被测药物所特有的。若有干扰就需改进测定方法或改用具有分离能力(如色谱法的专属性较吸收光度法为高)的方法或专属性较强的方法进行。(五)不同方法测得结果的相关程度(Degree of correlation)的比较:用一有相当专属性和可靠性的方法与新建方法同量测定,以相关系数γ(Correlation coefficient)表示相关程度。γ一般要求在0。95以上。此外,还应从方法的可靠性、每个样品测定耗时多少、操作的难易及技术要求及仪器、设备要求、费用多少等等方面加以考虑。
作者:罗浩题目:长春新碱靶向缓释微球的制备及其体内外研究期刊:天津大学年份:2008链接:http://www.cnki.net/KCMS/detail/detail.aspx?dbcode=CMFD&QueryID=4&CurRec=283&dbname=CMFDLAST2010&filename=2009072195.nh&urlid=&yx=
题目:注射用载雌二醇m PEG-PLA缓释微球的制备及体内外释放研究作者:李静期刊:山东大学,2012链接:http://www.cnki.net/KCMS/detail/detail.aspx?dbcode=CMFD&QueryID=0&CurRec=1&dbname=CMFDTEMP&filename=1012462466.nh&urlid=&yx=
在参考国内外饮用水水质标准的基础上,建立了饮用水水质综合评价体系,通过专家咨询法获得判断矩阵,利用层次分析法计算各水质指标的权重,结合国内外饮用水水质标准的指标进行层次总排序,根据总排序结果对国内外饮用水水质标准的特点进行了综合评价。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=102669]国内外饮用水水质标准的综合评价.pdf[/url]
【序号】:1【作者】:杨涛【题名】:不同层软骨细胞与骨髓间充质干细胞在体内外三维共培养时细胞外基质特点的实验研究【期刊】:大连医科大学【年、卷、期、起止页码】:2017【全文链接】:https://kns.cnki.net/kcms2/article/abstract?v=3uoqIhG8C447WN1SO36whLpCgh0R0Z-ifBI1L3ks338rpyhinzvy7Kt4RMGSMaxxH2WkQVeTlx_sUqdJWIk0PB_cP8FsBxdg&uniplatform=NZKPT
我想请教一下:在国内外有没有关于通风厨抽风效果的评价标准,就是评价抽风效果等级,保证在通风厨内反应产生的有害气体大部分被抽出去不会对人体造成健康危害,不知道哪里有这种标准?
评价了国内外电站的脱硫技术
【序号】:6【作者】: 余俊1余兰1贺骏【题名】:壳聚糖和透明质酸纳米聚电解质复合物吸附动脉粥样硬化特异抗体CD47的合成及体内外靶向实验【期刊】:中国动脉硬化杂志.【年、卷、期、起止页码】: 2019,27(04)【全文链接】:https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=CJFD&dbname=CJFDLAST2019&filename=KDYZ201904009&uniplatform=NZKPT&v=rTNnNcbjMaG-Y7w8mlYACwBzqKoXNr4XcgkrmvtjNA6KPoYrPuFsaQJSSD8JNRpw
【技术视频】DOW化学品安全评价之:采用QSAR/PBPK预测化合物在体内暴露量导读:2016年6月16日,美国毒理学会生物建模组组织了“化学品安全评价之:采用QSAR/PBPK预测化合物在体内暴露量”Saying I do to the QSAR/PBPK marriage in GastroPlus to predict chemical exposure for safety evaluation的网络研讨会。会议邀请了美国Simulations Plus公司和Dow Chemical(陶氏化学)的专家讲解如何预测化学品在体内的暴露量。 报告人:John DiBella, Simulations PlusFagen Zhang and Leah Luna,The Dow Chemical Company http://player.youku.com/player.php/sid/XMTYyNjQxMjE2MA==/v.swf 视频下载链接: http://pan.baidu.com/s/1c1HBb4O 密码:aqi4 课件PDF课件下载链接:http://pan.baidu.com/s/1bNeIRW 关于Dow Chemical:陶氏是一家多元化的化学公司,运用科学和技术的力量,不断创新,为人类创造更美好的生活。公司通过化学、物理和生物科学的有机结合来推动创新和创造价值,全力解决当今世界的诸多挑战,如满足清洁水的需求、实现可再生能源的生产和节约、提高农作物产量等。陶氏以其一体化、市场驱动型、行业领先的特种化学、高新材料、农业科学和塑料等业务,为全球约180个国家和地区的客户提供种类繁多的产品及服务,应用于包装、电子产品、水处理、涂料和农业等高速发展的市场。2014年,陶氏年销售额超过580亿美元,在全球拥有约53,000名员工,在35个国家和地区运营201家工厂,产品达6,000多种。早在上世纪30年代,陶氏就已经在中国开展业务。目前,大中华区是陶氏全球第二大国际市场,陶氏在这里的总投资额达12亿美元,2014年销售额为43亿美元。 关于Simulations Plus:专注于为制药、生物技术领域提供加速药物研发进程、节省成本及提高效率的解决方案。主要产品--ADMET Predictor, GastroPlus,MedChem Studio, DDDPlus得到业界高度推崇。FDA, CFDA, EMA, 日本厚生省,美国EPA欧盟化学品管理局ECHA, 美国国家癌症研究所NCI。全球TOP20的制药企业都是Simulations Plus的用户,如Roche, GSK, Novartis, Eli Lilly, Pfizer, Johnson & Johnson, Merck等。 关于SOT:Founded in 1961, the Society of Toxicology (SOT) is a professional and scholarly organization of scientists from academic institutions, government, and industry representing the great variety of scientists who practice toxicology in the US and abroad. The Society’s mission is to create a safer and healthier world by advancing the science and increasing the impact of toxicology.SOT operates under the guiding principles of:Serving the needs of the scientific discipline and our members to enhance human, animal, and environmental healthLife-long learning and intellectual scientific stimulationDiversity of representation in all activities of the Society[*
视频课件:体内药物分析。共十一章二十五课,总容量超过1GB。因为每课都超过论坛规定的50M限量,所以分节上传。注意:用RAR解压时必须把每课的分节全部下载后合在一起做。执行文件:content.htm体内药物分析课件目录:第一章:绪论(1-3)第二章:药物在体内的存在状态与生物转化(4)第三章:生物样品与样品前处理(5-8)第四章:体内药物分析方法及方法的设计与评价(9-12)第五章:光谱分析法(13-14)第六章:免疫分析法(15-16)第七章:色谱法(17-20)第八章:手性色谱法(21-22)第九章:毛细管电泳法(23)第十章:联用技术(24)体内药物分析总复习(25)下载地址:http://www.instrument.com.cn/download/search.asp?searchType=admin%5Fname&keywords=wsy18&page=4
[img=小动物体内荧光成像系统]http://www.f-lab.cn/Upload/FluorVivo-system.jpg[/img][b][url=http://www.f-lab.cn/vivo-imaging/fluorvivo.html]小动物体内荧光成像系统fluorvivo[/url]应用[/b]表达荧光标记的小动物荧光筛选;肿瘤转移负担评价;药效试验内化物质的药代动力学;荧光物质的定量测量,如肿瘤负荷;连续或时间推移监测。小动物体内荧光成像系统:[url]http://www.f-lab.cn/vivo-imaging/fluorvivo.html[/url]
视频课件:体内药物分析。共十一章二十五课,总容量超过1GB。因为每课都超过论坛规定的50M限量,所以分节上传。注意:用RAR解压时必须把每课的分节全部下载后合在一起做。执行文件:content.htm体内药物分析课件目录:第一章:绪论(1-3)第二章:药物在体内的存在状态与生物转化(4)第三章:生物样品与样品前处理(5-8)第四章:体内药物分析方法及方法的设计与评价(9-12)第五章:光谱分析法(13-14)第六章:免疫分析法(15-16)第七章:色谱法(17-20)第八章:手性色谱法(21-22)第九章:毛细管电泳法(23)第十章:联用技术(24)体内药物分析总复习(25)下载地址:http://www.instrument.com.cn/download/searchuser.asp?admin_name=wsy18
年底了,大家实验室是否开展质量考核打分和评价?针对资质能力维持指标?扩项加分?内外部质控结果?科研课题等?
体内药物分析 :是通过分析的手段了解药物在体内(包括实验动物等机体)数量与质量的变化,获得各种药物代谢动力学的各种参数和转变、代谢的方式、途径等信息。从而有助于药物生产、实验、研究、临床等各个方面对所研究的药物作出估计与评价,以及对药物的改进和发展作出贡献。 体内药物分析任务和对象的特点: 1、被测定的药物和代谢物的浓度或活性极低;2、样品中存在各种直接或间接影响测定结果的物质,大多需要分离和净化;3、样品量少,尤其是连续测定时,很难再度获得完全相同的样品;4、工作量较大,随着工作的深入开展,会成倍地甚或按指数级数增加;5、往往要求很快地提供结果,尤其在毒物检测工作中;6、实验室应有多种检测手段,可进行多项分析工作;7、测定数据的处理和阐明有时不太容易。 样品的种类、采集和储存一、样品的种类和选取原则:(一)血样:血浆(plasma)和血清(serum)是体内药物分析最常采用的样本,其中选用最多的是血浆。因血浆中的药浓可反映药物在体内(靶器管)的状况。而且血浆中药物浓度的数据报道较多,可供借鉴。血浆是全血(whole blood)在加肝素、枸橼酸、草酸盐等抗凝剂的全血经离心后分取,量约为全血的一半。血清则是在血液中纤维蛋白元等影响下,引起析出血块,离心取得。血块凝结时往往易造成药物吸附损失。全血也应加入抗凝剂混匀,以防凝血。对大多数药物来说血浆浓度与红细胞中的浓度成正比,所以测定全血也不能提供更多的数据,而全血的净化较血浆与血清麻烦,尤其是溶血后,血色素等可能会给测定带来影响。但是一些可与红血球结合或药物在血浆和血球的分配比率因不同病人而异的情况下,则宜采用全血。血样采取量会受到一定的限制,血样取样时间间隔问题也常随测定目的不同而异。目前大都是测定原型药物总量。当药物与血清蛋白结合率稳定时,血药总浓度可以有效表示游离药物的浓度。但对低蛋白症或尿毒症患者,药物结合率降低,则在通常安全有效的血药总浓度中,游离型药物浓度可显著增加。(二)尿样(urine):尿样测定主要用于药物剂量回收研究、药物肾清除率和生物利用度等研究,以及测定代谢物类型等。体内药物清除主要是通过尿液排出,药物可以原型(母体药物)或代谢物及其缀合物形式排出。尿液药物浓度较高,收集量可以很大,但尿液浓度通常变化较大,所以宜测定一定时间内尿中药物的总量(如8、12、24小时内的累计量),需记录排出尿液体积及尿药浓度。尿药浓度改变不直接反映血药浓度,受试者肾功能将影响药物的排泄。尿中药物大多呈缀合状态,测定前要将缀合的药物游离。此外,采集尿液不可能在较短时间内多次取样,排尿时间较难掌握(尤其是婴儿),同时也具有不易采集完全的缺点。(三)唾液(saliva):唾液中的药物浓度通常与血浆浓度相关。样品易得,取样无损害,尤易为儿童接收。有些可从药物唾液浓度推定血浆中游离药物浓度。但有些蛋白结合率较高的药物在唾液中的浓度比血浆浓度低得多,需高灵敏度的方法才能检测。唾液pH值6.9±0.5,每日分泌量1~1.5L,含有的主要电解质有Na+、K+、Cl-、HCO3 -等,主要有机成分是粘液质和淀粉酶。采样一般是在漱口后15分钟,收集口内自然流出或经舌在口内搅动后流出的混合唾液(吸管内吸附的少量唾液用稀释液洗出),用2000~3000rpm离心15分钟,小心吸取上清液,进一步分离、净化。也可采用物理(嚼石蜡片、小块聚四氟乙烯或玻璃大理石)或化学(酒石酸、维生素C)的方法刺激,在短时间内可得到大量唾液,但药浓也可能会受到影响。(四)其它:乳汁、动物脏器组织匀浆等。二、样品储存和稳定性考察:取样后最好立即进行分析,冷藏(4℃)、冰冻(-20℃)有时也不能完全保证样品不起变化。尿液是很好的细菌生长液,若需收集24小时或更长时间的样品或不能立即测定的,应置冰箱冷藏或加防腐剂(1%甲苯、过饱和氯仿)保存。分析样品贮存时应考虑:储存条件;样品在贮存中会对分析结果产生什么影响;评述样品稳定性时会发生什么问题;如何预防或校正不稳定样品的分析结果。 测定前样品的制备 除少数体液经简单处理后直接测定外,通常在最后一步测定前要采取适当的样品制备,即进行分离、净化、浓集、必要时尚需对待测组分进行化学改性,为测定创造良好条件。一、样品的制备要考虑:药物的理化性质、待测物的浓度范围、药物测定的目的、选用的生物体液和组织的类型、样品制备与分析技术的关系。二、蛋白质的处理:是测定血浆、血清、全血及组织匀浆等样品中药物时的最先处理步骤。(一)加入沉淀剂和变性试剂:硫酸铵是经典的蛋白质沉淀剂,它与蛋白质分子竞争系统中水分子,而使蛋白质析出。阴离子型沉淀剂(三氯醋酸、高氯酸、钨酸、焦磷酸)与带电荷的蛋白质在氏于等电点的pH时形成不溶性盐;反之,阳离子型沉淀剂(含锌盐、铜盐)与蛋白质分子中带阴电荷的羧基,在高于蛋白质等电点时,形成不溶性盐。有关机制不十分清楚。(二)加入可与水混合的有机溶剂:乙醇过量存在时,能使与蛋白结合状态的药物释放可将混合物离心,取上清液(含药),但这不能解决样品的净化问题。蛋白沉淀法对于与蛋白结合力强的药物的回收率较差。也有采用酸消化法(Acid digestion)使药物自蛋白结合处释出,但常导致药物的分解。
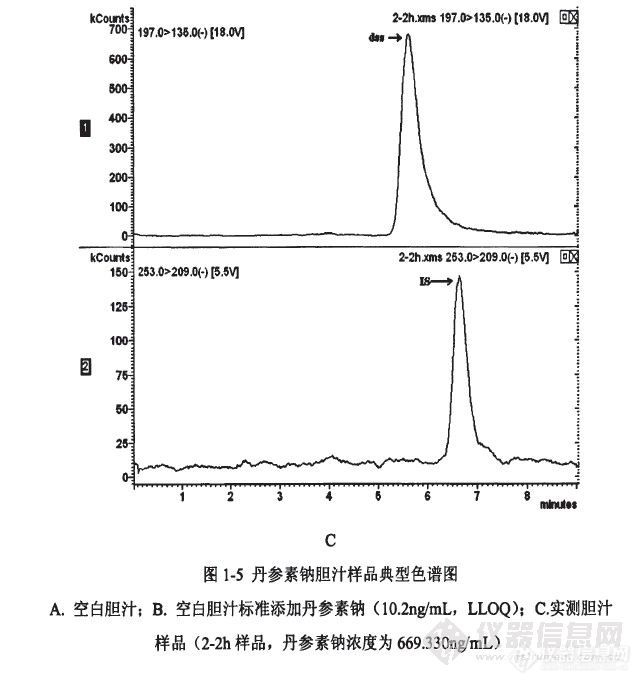
【作者】魏华 【摘要】:药物代谢动力学旨在通过测定生物样本中的药物或者代谢产物的浓度,定量描述药物进入体内以后的吸收、分布、代谢、排泄过程,进而阐明药物的药效或者毒性,为新药研究的代谢筛选和临床用药的疗效评价提供重要依据。丹参素为从唇形科植物丹参Salvia miltiorrhiza Bunge的干燥根中提取出的单体化合物,具有明显的药理活性。作为丹参的主要活性成分之一,有必要对丹参素进行药代动力学研究,探讨其体内过程。本文建立的LC-MS/MS法测定血浆、尿液、胆汁等多种生物样本中的丹参素钠浓度,满足临床前药代动力学研究对高灵敏度、高选择性检测的技术要求。此外,本文还进行了丹参素钠的体内、体外代谢研究,初步建立了体外代谢筛选研究平台,为进一步开展临床用药及剂型开发提供参考依据。 一、生物样品中丹参素钠定量分析方法的建立与确证 在临床前药代动力学研究中,定量分析方法的建立与确证占有举足轻重的地位,只有建立可靠、专一、灵敏、快速的生物样品分析方法,才能保证药代动力学研究的顺利进行。本文采用高灵敏度的LC-MS/MS方法检测生物样品中丹参素钠的浓度,生物样品以盐酸酸化后用乙酸乙酯提取其中的丹参素钠。色谱分析采用迪马Diamonsil C-18,5μm,200×4.6mm,柱温25℃;流动相组成为甲醇:水=80:20(含0.01‰甲酸),采用等梯度洗脱方式,流速0.80mL/min,3:2分流入质谱的流速为0.32mL/min,进样量20μl。质谱检测采用ESI离子源、负离子检测模式,选择MRM工作方式进行质谱分析。经完整的方法学确证,所有测定生物样品的线性、准确度、精密度、回收率、基质效应、稀释效应、稳定性等均满足生物样品的定量分析要求。该方法成功用于SD大鼠的药代动力学研究及尿液和胆汁的排泄研究。 二、丹参素钠在SD大鼠体内的临床前药代动力学研究 本试验设计SD大鼠单剂量尾静脉注射给药丹参素钠15mg/kg、30mg/kg、60mg/kg三个剂量组进行药代动力学研究。采用LC-MS/MS测定方法分别测定了给药后不同时间的体内丹参素钠血药浓度。按血浆样品预处理操作,测得数据代入相应样品随行标准曲线中求得含量。经非房室模型法估算药代动力学参数。结果表明,大鼠单剂量静注给药丹参素钠15mg/kg、30mg/kg、60mg/kg三个剂量组药代动力学药时曲线末端相消除半衰期(t1/2)分别为2.73h、2.37h、1.95h;AUC0~∞分别为15.29μg·h/mL、34.58μg·h/mL和58.49μg·h/mL,AUC与给药剂量基本呈正相关,相关系数r~2为0.9836。 SD大鼠单剂量尾静脉注射给药丹参素钠30mg/kg后,于给药后收集0~96h的尿液,按尿液样品预处理操作,测得数据代入相应样品随行标准曲线中求得含量。结果表明,丹参素钠在SD大鼠体内主要经尿液排泄,96h药物累积排泄量为46.99%。SD大鼠单剂量尾静脉注射给药丹参素钠30mg/kg后,于给药后0~24h取其胆汁,按胆汁样品预处理操作,测得数据代入胆汁样品随行标准曲线中求得含量。结果表明,丹参素钠在SD大鼠体内经胆汁排泄量少,24h内胆汁累积排泄量为给药剂量的0.82%。综上所述,丹参素钠在SD大鼠体内主要以原型药的形式直接由尿排出体外。 三、丹参素钠体内外代谢的初步研究 丹参素钠给药后大鼠胆汁和尿液样品的分析结果显示,其进入体内后,主要发生II相代谢反应,主要代谢物为:甲基化丹参素~-、硫酸酯结合物~-、甲基化硫酸酯结合物-、经尿液排出体外;胆汁中主要存在着甲基化丹参素。丹参素钠经在体肠灌流、原位肝灌流等实验后,主要产生甲基化代谢产物,说明这些器官组织中存在着参与其甲基化反应的酶。经过体外肝匀浆、肝微粒体、肾匀浆、肾微粒体温孵后,主要代谢产物为甲基化丹参素。丹参素钠在大鼠肝微粒体酶中代谢的酶动力学结果显示,它在大鼠肝微粒体酶中代谢的Vmax为185.19ng/(mL·min·mg)蛋白,Km为98940.74ng/mL,即5.0×10~(-4)mol/L,内在代谢清除率Clint为1.87×10~(-3)mL/(min·mg)蛋白。此外,本章还进行了丹参素钠在COMT单一酶中的酶促反应动力学研究。与肝微粒体酶相比,丹参素钠与COMT有较大的亲和力,Vm、Km与Clint均偏大:Vmax为243.90ng/(mL·min·mg)蛋白,Km为102156.1ng/mL,即5.16×10~(-4)mol/L,内在代谢清除率Clint为2.34×10~(-3)mL/(min·mg)蛋白。说明催化丹参素发生甲基化反应的主要酶是COMT。【关键词】:丹参素 LC-MS/MS 药代动力学 排泄 大鼠 代谢产物 肝微粒体 酶促反应动力学 COMT 【学位授予单位】:第二军医大学【学位级别】:硕士【学位授予年份】:2010【分类号】:R96http://ng1.17img.cn/bbsfiles/images/2012/08/201208210834_384889_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210834_384890_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210834_384891_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210834_384892_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210834_384893_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210835_384894_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210835_384895_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210835_384896_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210835_384898_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210835_384899_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210835_384900_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210836_384901_2352694_3.jpg
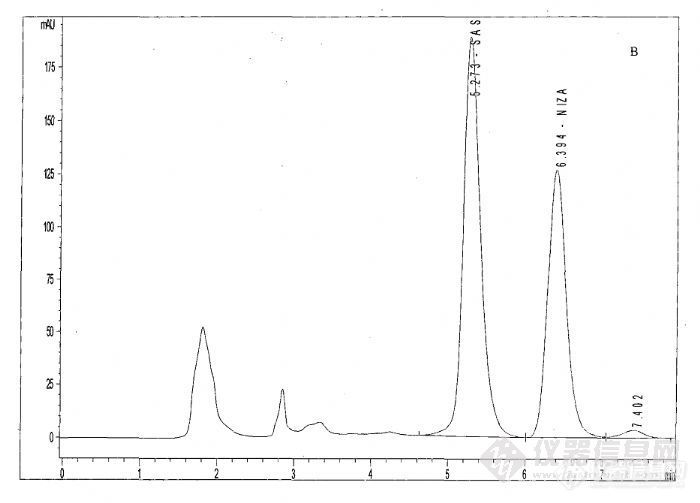
【作者中文名】张玲;【导师】王婷;【学位授予单位】兰州大学;【中文摘要】目的:建立高效液相色谱法测定人血浆和尿样中尼扎替丁浓度的方法。研究健康受试者单次和多次静脉滴注尼扎替丁注射液(100mg)后的血药和尿药药代动力学特征,计算其在健康人体内的药代动力学参数,描述其在体内的分布、代谢、排泄规律,并对该剂量静脉滴注后的安全性进行初步评价,为制定Ⅱ期临床试验方案及临床用药提供依据。 方法:本试验采用平行设计,筛选10名健康志愿受试者(男女各半),按体重随机排序,单次(100mg)和多次(100mg/次,3次/日,连续用药6天)静脉滴注尼扎替丁后,采集血样和尿样。色谱柱为Diamonsil C18 (150×4.6mm,5μm);流动相:V:V=L腈:0.05mol/LK2HPO4(含三乙胺1.0%v/v,用85%磷酸调pH至6.5)=17:83,流速为0.9mL/min;柱温:40℃;DAD检测器,检测波长320nm。采用RPHPLC-UV法,以水杨酸为内标测定尼扎替丁血药及尿药浓度,DAS软件计算药动学参数。 结果:1、尼扎替丁血药浓度在0.0117-6μg/mL范围内具良好线性关系(r=0.9999,权重W=1/C),方法回收率在96.2%~105.2%之间,提取回收...http://ng1.17img.cn/bbsfiles/images/2012/08/201208131811_383608_2379123_3.jpg
体内药物分析是通过分析的手段了解药物在体内(包括实验动物等机体)数量与质量的变化,获得各种药物代谢动力学的各种参数和转变、代谢的方式、途径等信息。从而有助于药物生产、实验、研究、临床等各个方面对所研究的药物作出估计与评价,以及对药物的改进和发展作出贡献。 体内药物分析任务和对象的特点:1、被测定的药物和代谢物的浓度或活性极低;2、样品中存在各种直接或间接影响测定结果的物质,大多需要分离和净化;3、样品量少,尤其是连续测定时,很难再度获得完全相同的样品;4、工作量较大,随着工作的深入开展,会成倍地甚或按指数级数增加;5、往往要求很快地提供结果,尤其在毒物检测工作中;6、实验室应有多种检测手段,可进行多项分析工作;7、测定数据的处理和阐明有时不太容易。样品的种类、采集和储存一、样品的种类和选取原则:(一)血样:血浆(plasma)和血清(serum)是体内药物分析最常采用的样本,其中选用最多的是血浆。因血浆中的药浓可反映药物在体内(靶器管)的状况。而且血浆中药物浓度的数据报道较多,可供借鉴。血浆是全血(whole blood)在加肝素、枸橼酸、草酸盐等抗凝剂的全血经离心后分取,量约为全血的一半。血清则是在血液中纤维蛋白元等影响下,引起析出血块,离心取得。血块凝结时往往易造成药物吸附损失。全血也应加入抗凝剂混匀,以防凝血。对大多数药物来说血浆浓度与红细胞中的浓度成正比,所以测定全血也不能提供更多的数据,而全血的净化较血浆与血清麻烦,尤其是溶血后,血色素等可能会给测定带来影响。但是一些可与红血球结合或药物在血浆和血球的分配比率因不同病人而异的情况下,则宜采用全血。血样采取量会受到一定的限制,血样取样时间间隔问题也常随测定目的不同而异。目前大都是测定原型药物总量。当药物与血清蛋白结合率稳定时,血药总浓度可以有效表示游离药物的浓度。但对低蛋白症或尿毒症患者,药物结合率降低,则在通常安全有效的血药总浓度中,游离型药物浓度可显著增加。(二)尿样(urine):尿样测定主要用于药物剂量回收研究、药物肾清除率和生物利用度等研究,以及测定代谢物类型等。体内药物清除主要是通过尿液排出,药物可以原型(母体药物)或代谢物及其缀合物形式排出。尿液药物浓度较高,收集量可以很大,但尿液浓度通常变化较大,所以宜测定一定时间内尿中药物的总量(如8、12、24小时内的累计量),需记录排出尿液体积及尿药浓度。尿药浓度改变不直接反映血药浓度,受试者肾功能将影响药物的排泄。尿中药物大多呈缀合状态,测定前要将缀合的药物游离。此外,采集尿液不可能在较短时间内多次取样,排尿时间较难掌握(尤其是婴儿),同时也具有不易采集完全的缺点。(三)唾液(saliva):唾液中的药物浓度通常与血浆浓度相关。样品易得,取样无损害,尤易为儿童接收。有些可从药物唾液浓度推定血浆中游离药物浓度。但有些蛋白结合率较高的药物在唾液中的浓度比血浆浓度低得多,需高灵敏度的方法才能检测。唾液pH值6.9±0.5,每日分泌量1~1.5L,含有的主要电解质有Na+、K+、Cl-、HCO3-等,主要有机成分是粘[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]和淀粉酶。采样一般是在漱口后15分钟,收集口内自然流出或经舌在口内搅动后流出的混合唾液(吸管内吸附的少量唾液用稀释液洗出),用2000~3000rpm离心15分钟,小心吸取上清液,进一步分离、净化。也可采用物理(嚼石蜡片、小块聚四氟乙烯或玻璃大理石)或化学(酒石酸、维生素C)的方法刺激,在短时间内可得到大量唾液,但药浓也可能会受到影响。(四)其它:乳汁、动物脏器组织匀浆等。
人体内的毒素,排出不彻底,将影响人的健康,对于女性朋友来,显得更加重要,世面上有很多排毒的药物,那么他们能起到排毒养颜的效果吗,那这些毒素是通过食物直接带入体内还是在体内转化的?
鱼体内有机氯农药的测定
近两年,中国涌现出一批有发展潜力的新药候选物,这些候选物在人体内的PK行为会是怎样?制药企业、临床试验机构、政府法规部门、科研单位都面临着巨大的发展机遇和挑战。FDA、EMA等法规部门、TOP20制药企业近年来都引入和推荐采用Modeling & Simulation的方法,对药物体内药动行为进行合理的预测,有效地将体外的数据转化成为体内的PK参数。美国生理药动模拟软件GastroPlus是基于模型的药物开发方法的模拟工具,可整合众多的体外数据和信息去模拟药物的体内行为,从而进行有效的种属间外推。
请问我建好了一种牛兽药残留检测方法,想做体内验证,可以5.6只牛注射后一段时间后采样检测吗?并不测这个方法在牛体内的残留消除规律,只是验证方法的可行性
Bioanalytical method validation英文资料,希望对做体内药物分析的人有帮助。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=16082]体内分析方法验证[/url]
采购的工作有哪些具体内容?
有谁做过体内乳酸的分析,介绍一下方法或给予研究思路
如果你体内的重金属超标,可能会有头疼、胃口不好、浑身乏力的症状,但均不明显,有可能与其它的病症混淆。而毛发检验是目前最有效的检测人体内各项微量元素含量的方法,只要检验0.2克的头发,就可以知道体内26种微量元素(包括6种有害元素)的均衡状况。人体血液中的微量元素通过与蛋白质结合的形式,被排泄积蓄于毛发中.毛发反映了人体内微量元素的长期积累状况。 而血液检查和尿液检查反映的是排泄速度较快的短期状况。另外,由于体内平衡的缘故,血液检查有时很难准确反映微量元素含量。
有了解各种兽药在奶牛体内的代谢过程的吗?可否分享一下?
体内药物分析 体内药物分析是通过分析的手段了解药物在体内(包括实验动物等机体)数量与质量的变化,获得各种药物代谢动力学的各种参数和转变、代谢的方式、途径等信息。从而有助于药物生产、实验、研究、临床等各个方面对所研究的药物作出估计与评价,以及对药物的改进和发展作出贡献。 体内药物分析任务和对象的特点:1、被测定的药物和代谢物的浓度或活性极低;2、样品中存在各种直接或间接影响测定结果的物质,大多需要分离和净化;3、样品量少,尤其是连续测定时,很难再度获得完全相同的样品;4、工作量较大,随着工作的深入开展,会成倍地甚或按指数级数增加;5、往往要求很快地提供结果,尤其在毒物检测工作中;6、实验室应有多种检测手段,可进行多项分析工作;7、测定数据的处理和阐明有时不太容易。 样品的种类、采集和储存一、样品的种类和选取原则:(一)血样:血浆(plasma)和血清(serum)是体内药物分析最常采用的样本,其中选用最多的是血浆。因血浆中的药浓可反映药物在体内(靶器管)的状况。而且血浆中药物浓度的数据报道较多,可供借鉴。血浆是全血(whole blood)在加肝素、枸橼酸、草酸盐等抗凝剂的全血经离心后分取,量约为全血的一半。血清则是在血液中纤维蛋白元等影响下,引起析出血块,离心取得。血块凝结时往往易造成药物吸附损失。全血也应加入抗凝剂混匀,以防凝血。对大多数药物来说血浆浓度与红细胞中的浓度成正比,所以测定全血也不能提供更多的数据,而全血的净化较血浆与血清麻烦,尤其是溶血后,血色素等可能会给测定带来影响。但是一些可与红血球结合或药物在血浆和血球的分配比率因不同病人而异的情况下,则宜采用全血。血样采取量会受到一定的限制,血样取样时间间隔问题也常随测定目的不同而异。目前大都是测定原型药物总量。当药物与血清蛋白结合率稳定时,血药总浓度可以有效表示游离药物的浓度。但对低蛋白症或尿毒症患者,药物结合率降低,则在通常安全有效的血药总浓度中,游离型药物浓度可显著增加。 (二)尿样(urine):尿样测定主要用于药物剂量回收研究、药物肾清除率和生物利用度等研究,以及测定代谢物类型等。体内药物清除主要是通过尿液排出,药物可以原型(母体药物)或代谢物及其缀合物形式排出。尿液药物浓度较高,收集量可以很大,但尿液浓度通常变化较大,所以宜测定一定时间内尿中药物的总量(如8、12、24小时内的累计量),需记录排出尿液体积及尿药浓度。尿药浓度改变不直接反映血药浓度,受试者肾功能将影响药物的排泄。尿中药物大多呈缀合状态,测定前要将缀合的药物游离。此外,采集尿液不可能在较短时间内多次取样,排尿时间较难掌握(尤其是婴儿),同时也具有不易采集完全的缺点。 (三)唾液(saliva):唾液中的药物浓度通常与血浆浓度相关。样品易得,取样无损害,尤易为儿童接收。有些可从药物唾液浓度推定血浆中游离药物浓度。但有些蛋白结合率较高的药物在唾液中的浓度比血浆浓度低得多,需高灵敏度的方法才能检测。唾液pH值6.9±0.5,每日分泌量1~1.5L,含有的主要电解质有Na+、K+、Cl-、HCO3-等,主要有机成分是粘[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]和淀粉酶。采样一般是在漱口后15分钟,收集口内自然流出或经舌在口内搅动后流出的混合唾液(吸管内吸附的少量唾液用稀释液洗出),用2000~3000rpm离心15分钟,小心吸取上清液,进一步分离、净化。也可采用物理(嚼石蜡片、小块聚四氟乙烯或玻璃大理石)或化学(酒石酸、维生素C)的方法刺激,在短时间内可得到大量唾液,但药浓也可能会受到影响。 (四)其它:乳汁、动物脏器组织匀浆等。 二、样品储存和稳定性考察:取样后最好立即进行分析,冷藏(4℃)、冰冻(-20℃)有时也不能完全保证样品不起变化。尿液是很好的细菌生长液,若需收集24小时或更长时间的样品或不能立即测定的,应置冰箱冷藏或加防腐剂(1%甲苯、过饱和氯仿)保存。分析样品贮存时应考虑:储存条件;样品在贮存中会对分析结果产生什么影响;评述样品稳定性时会发生什么问题;如何预防或校正不稳定样品的分析结果。 测定前样品的制备除少数体液经简单处理后直接测定外,通常在最后一步测定前要采取适当的样品制备,即进行分离、净化、浓集、必要时尚需对待测组分进行化学改性,为测定创造良好条件。一、样品的制备要考虑:药物的理化性质、待测物的浓度范围、药物测定的目的、选用的生物体液和组织的类型、样品制备与分析技术的关系。二、蛋白质的处理:是测定血浆、血清、全血及组织匀浆等样品中药物时的最先处理步骤。 (一)加入沉淀剂和变性试剂:硫酸铵是经典的蛋白质沉淀剂,它与蛋白质分子竞争系统中水分子,而使蛋白质析出。阴离子型沉淀剂(三氯醋酸、高氯酸、钨酸、焦磷酸)与带电荷的蛋白质在氏于等电点的pH时形成不溶性盐;反之,阳离子型沉淀剂(含锌盐、铜盐)与蛋白质分子中带阴电荷的羧基,在高于蛋白质等电点时,形成不溶性盐。有关机制不十分清楚。 (二)加入可与水混合的有机溶剂:乙醇过量存在时,能使与蛋白结合状态的药物释放可将混合物离心,取上清液(含药),但这不能解决样品的净化问题。蛋白沉淀法对于与蛋白结合力强的药物的回收率较差。也有采用酸消化法(Acid digestion)使药物自蛋白结合处释出,但常导致药物的分解。 (三)组织的酶消化法:蛋白水解酶(Proteolytic enzyme)中的枯草菌溶素(Subtilisin Carlsberg)不仅可使组织酶解,且可使药物析出。优点:1、因是在平稳条件下进行的,可避免某些药物在酸中水解及较高温度时降解;2、可显著改善对蛋白结合率强的药物的回收率;3、可用有机溶剂直接提取消化液而无乳化生成的危险;4、在用HPLC时,无需再进行过多的净化操作。缺点是不适用于一些在高pH时易水解的药物。三、提取:(一)溶液的pH调节:最佳pH选择主要与药物的pKa值有关。pH与pKa相当时,50%的药物以非电离形式存在。碱性药物最佳pH值要高于pKa值1~2个pH单位;反之,则低1~2个单位。可使90%药物以非电离开形式存在,易为溶剂提取。而对于碱性很强的药物往往采用“离子对”技术进行提取和定量。体内酸性物质较多,在碱性条件下不会被萃取出来,故在pH值偏高的情况下进行提取较好。 (二)提取溶剂的极性:选好第一个提取溶剂可减少以后的净化操作,在液-液提取中多采用极性小的溶剂。加入少量醇类可克服极性小溶剂提取能力弱和减小药物在容器表面的吸附损失的不足。也有利用不同极性的混合溶剂来提取药物和净化脂肪酸类。 (三)提取技术:由于体液样品量少且药物含量低,一次分析的样品数量较多。与常量和微量分析相比,提取时通常不采用反复提取的方法,多半进行一次(至多二次)提取,在改变pH后,从有机相回提至水相也只进行一次。一般并不考虑“提尽药物”,测定含量时则应精确加入提取溶剂,提取液也要定量分出。为避免进样时带来的误差,多采用提取前加入等量内标,以待测组分峰高(或峰面积)与内标峰高(或峰面积)之比对浓度作标准曲线。这样,即使在一系列操作过程中有微量损失,对比值影响也较小。混合时可在密塞情况下将试管平置于振荡器内振荡,振荡时间与强度视情况而定。可采用以“药物转入溶剂中量”与“混合时间”作图法,选取理想和符合实际的提取方式和时间。 (四)提取溶剂的蒸发:提取液常为数ml,往往不能直接供GC或HPLC测定,需采取浓集办法,常用真空蒸发(注意暴沸)或吹氮气流使溶剂挥散。四、固相分离:以固相分离方法进行样品预处理,从水相中分离出所需测定的组份,通常以柱分离方式进行操作,故有时这种方法又称为固相提取柱(Solid-phase extraction column)法。这类柱分两类:一种是阻留全部样品在柱上;一种则仅阻留药物及其相关物质。常用于填充柱的固相分离物质有氧化铝、活性碳、硅藻土、离子交换树脂及非离子型的树脂及凝胶等。在第一类柱中,常使用亲水性装填物,如硅藻土,可捕集全部样品。样品全部吸附在固相颗粒表面,形成一薄层,即使样品中含水也能如此。采用一种与水不相混溶的有机溶剂如氯乙烷倾入柱中,即可洗提药物。第二类柱则较有选择性,可装填疏水物或离子交换树脂,对药物及其相关物质进行滞留。常用的疏水物有活性碳、聚苯乙烯或C18化学键合硅胶。这种疏水柱可从样品中吸附亲脂性药物,然后用有机溶剂将药物洗提分离。离子交换柱适用于高极性、可电离的药物。五、利用分子大小进行分离—供血浆中游离药物的测定:采用超速离心、平衡透析、限外过滤(超滤)以及凝胶过滤方法等。以上方法也可用于药物蛋白结合率的测定。六、导致待测物损失的因素:(一)吸附:玻璃表面或橡胶塞会吸附药物,特别是脂肪胺类及含硫化合物。可采用硅烷化减少玻璃表面的吸附性,非极性提取溶剂中加入少量极性溶剂可减少器皿对药物的吸附。 血样中红血球和纤维蛋白元凝块的形成,常能引起待测物的共沉淀。所以宜将全血样品加入缓冲液后再行提
海带:含胶质成分能促进体内的放射性物质随同尿液排出体外。 绿豆汤:常饮用则能帮助排泄体内的毒素,促进机体的正常代谢。 胡萝卜:可与重金属汞结合,生成新物质排出体外。 大蒜:大蒜中的特殊成分能让体内铅的浓度下降。 蘑菇:能帮助排泄体内毒素,促进机体的正常代谢。 草莓:能帮助清洁胃肠道,并强固肝脏。对阿司匹林过敏和肠胃功能不好的人,不宜食用。 樱桃:能去除毒素和不洁的体液,因而对肾脏排毒具有相当的辅助功效,同事还有温和的通便作用。 葡萄:能帮助肠内粘液组成,清除肝、肠、胃、肾的垃圾。唯一的缺点是热量有点高,40颗葡萄相当于两个苹果的热量。 苹果:含半乳糖,醛酸,能帮助排毒,而果胶则能避免食物在肠内腐化。热量也很低。
[font=宋体][size=17px][color=rgba(0, 0, 0, 0.901961)]姜黄素为姜黄中的有效成分,具有抗炎[/color][/size][/font][font=宋体][size=17px][color=rgba(0, 0, 0, 0.901961)]、抗氧化[/color][/size][/font][font=宋体][size=17px][color=rgba(0, 0, 0, 0.901961)]、调节脂质代谢[/color][/size][/font][font=宋体][size=17px][color=rgba(0, 0, 0, 0.901961)]、抗肿瘤[/color][/size][/font][font=宋体][size=17px][color=rgba(0, 0, 0, 0.901961)]、抗纤维化[/color][/size][/font][sup][color=black]][/color][/sup][font=宋体][size=17px][color=rgba(0, 0, 0, 0.901961)]、器官保护[/color][/size][/font][font=宋体][size=17px][color=rgba(0, 0, 0, 0.901961)]等功效。虽然姜黄素的药效得到了国内外的普遍认可,但是其溶解性低、稳定性低和生物利用率低等缺点,限制了姜黄素的临床应用。[/color][/size][/font] [font=宋体]一般而言,姜黄素类化合物是姜黄素、[color=var(--weui-LINK)]去甲氧基姜黄素[i][/i][/color]和双去甲氧基姜黄素的混合物,这些物质具有相同的庚烷长链和双苯环结构,区别在于苯环上的甲氧基[/font][b][color=#ffffff][back=#7b0c00][/back][/color][/b][font=宋体]数目不同。在姜黄提取物中,姜黄素占[/font]61.69%[font=宋体],去甲氧基姜黄素占[/font]16.06%[font=宋体],双去甲氧基姜黄素占[/font]12.32%[font=宋体]。姜黄素分子中含有[/font]α,β-[font=宋体]不饱和二酮基,且在[/font]2[font=宋体]个苯环上分别含有酚羟基和甲氧基[/font][font=宋体],酮[/font]-[font=宋体]烯醇部分可与金属螯合,能够清除由金属离子产生的活性自由基,使姜黄素可以成为氢离子的供体或受体,这是姜黄素抗氧化、抗炎症、抗凋亡能力的来源[/font][font=宋体]。[/font] [font=宋体]姜黄素在水中的溶解度小于[/font]50 μmol/L[font=宋体],但极易溶于有机溶剂[/font][font=宋体],其溶解度和稳定性与溶剂的种类和[/font]pH[font=宋体]值相关。在高相对[color=var(--weui-LINK)]介电常数[i][/i][/color]或极性的溶液中以[/font]β-[font=宋体]二羰基形式存在,在低相对介电常数的溶液如环己烷和四氯化碳中以烯醇形式存在。在姜黄素的[/font]β-[font=宋体]二酮链上存在分子内氢原子转移,导致其在溶剂中存在酮和烯醇互变异构的构象:在酸性和中性溶液中稳定存在,呈亮黄色;而在碱性条件下姜黄素无法保持稳定,分解反应的产物中四氢二阿魏酰甲烷会迅速形成缩合产物,呈现棕红色或棕褐色[/font][font=宋体]。姜黄素还是一种光敏性物质,将姜黄素溶于乙醇,在[/font]24 h[font=宋体]强光照射后会被完全降解,溶液由黄色转变为无色[/font][font=宋体]。[/font] [font=黑体][/font][font=宋体]生物制药分类系统按照水溶性和肠道渗透性将药品归为[/font]4[font=宋体]类,而姜黄素因其水溶性差、通过胃肠上皮的渗透性可忽略不计的特点被归于第[/font]4[font=宋体]类药物。虽然各种动物模型和临床试验都证实了姜黄素的安全性[/font][font=宋体],但过去[/font]30[font=宋体]年来,与姜黄素吸收、分布、代谢和排泄相关的研究表明,血药浓度低、组织分布局限、转化速度快和代谢周期短等因素限制了其应用[/font][font=宋体]。姜黄素的最高口服耐受剂量可达[/font]12 g/d[font=宋体],有报道指出,即使摄入姜黄素[/font]10[font=宋体][color=black]~[/color][/font]12 g[font=宋体],人体内姜黄素最高血浆浓度仍然低于[/font]160 nmol/L[font=宋体]。[/font][font=宋体]目前临床姜黄素剂型主要为注射液及原料药,给药途径主要为[/font][i]po[/i][font=宋体]、[/font]iv[font=宋体]及[/font]ip[font=宋体]。姜黄素在体内的吸收代谢及分布情况一直以来被广泛研究,研究对象包括小鼠、大鼠及人体[/font][font=宋体]。绝大部分姜黄素未经小肠消化直接进入结肠部位,只有少量姜黄素可以被上皮细胞吸收,并在肝脏和血浆中分布。汪小珍[/font][font=宋体]对比了姜黄素不同给药方式在大鼠体内生物利用度的变化,结果显示[/font]ip[font=宋体]姜黄素的生物利用度([/font]35.07%[font=宋体])比[/font]ig[font=宋体]([/font]4.13%[font=宋体])更高,表明姜黄素在肠道内的吸收效率较低。[/font] [font=宋体] [/font]

[img]http://ng1.17img.cn/bbsfiles/images/2008/05/200805121951_89037_1626751_3.jpg[/img]这是2005年1月18日拍摄的生活在南极洲阿德利岛上的企鹅。美国研究人员5月9日说,在全球大部分国家禁用杀虫剂DDT数十年后,南极阿德利企鹅体内仍检测出这种有毒物质,且含量多年来始终不降。他们认为,这是因为DDT被“储存”在冰川中,持续影响南极生态环境。(新华社/路透) 美国研究人员5月9日说,在全球大部分国家禁用杀虫剂DDT数十年后,南极阿德利企鹅体内仍检测出这种有毒物质,且含量多年来始终不降。 他们认为,这是因为DDT被“储存”在冰川中,持续影响南极生态环境。 美国弗吉尼亚州海洋科学研究所的海鸟研究专家海迪盖兹说,研究人员早在20世纪60年代初就从阿德利企鹅的脂肪内检测出DDT。但令研究人员感到惊奇的是,尽管这种有毒农药已在大多数国家被禁用数十年,它在企鹅体内的含量却一直没有下降。 盖兹解释说,这可能是因为DDT等化学物质被蒸发后经大气层传播到南极,然后冷凝,“储存”到冰川中。证据之一是研究人员在冰川融化后的水中检测出DDT。 尽管南极企鹅体内的DDT含量不降,但盖兹领导的这项研究发现,在过去数十年内,北极野生动物体内的DDT含量大幅下降。盖兹说,目前在企鹅体内检测出的DDT含量还不足以伤害它们。 这项研究结果发表在美国《环境科学与技术》(Environmental Science & Technology)月刊上。[em0812] [em0815] 中国心