
Venusil XBP C18(L)分析头孢噻肟钠的分析报告摘要:本实验按照头孢噻肟钠2010版中国药典方法进行测定,以含量测定和有关物质检测方法共同进行色谱柱的筛选。在选定的色谱柱上,进一步考察了该色谱柱用于头孢噻肟钠系统适用性、含量、有关物质等项测试的结果,并初步考察了色谱柱的使用寿命,结果表明VenusilXBP C18(L)适用于头孢噻肟钠的分析:(1)系统适用性溶液中共检出7个杂质,分离度均符合标准要求;(2)对照品平行进样6针RSD为0.13%,保留时间17.039分钟,柱效5068,拖尾因子1.116,均符合标准要求;(3)含量测定中,头孢噻肟钠保留时间16.936分钟,柱效4779,拖尾因子1.118,符合标准要求;(4)有关物质测定中共检出6个杂质,分离度均符合标准要求;(5)用于头孢噻肟钠含量测试时,连续进样300针,保留时间、柱效和拖尾因子均无显著变化,表明VenusilXBP C18(L)对该样品和流动相有较好耐受性。关键词:头孢噻肟钠;VenusilXBP C18(L);2010版药典;液相色谱法前言头孢噻肟钠为中国药典2010版二部收录品种,本实验按照该标准进行测试,通过测试得出VenusilXBP C18(L)适用于头孢噻肟钠分析,其测试结果令人满意。实验部分试剂材料超纯水、甲醇、无水磷酸氢二钠、磷酸高效液相色谱柱:Venusil XBP C18(L);5 μm,150 Å,4.6 × 150mm样品制备系统适用性溶液制备:取头孢噻肟对照品适量,加流动相溶解并稀释制成每1 ml约含1 mg的溶液,作为系统适用性试验溶液。实验结果系统适用性测定结果表1. Venusil XBP C18(L)用于头孢噻肟钠系统适用性溶液测定结果http://ng1.17img.cn/bbsfiles/images/2017/10/2015082410220596_01_2864683_3.png表2.Venusil XBP C18(L)用于头孢噻肟钠对照品溶液测定结果http://ng1.17img.cn/bbsfiles/images/2017/10/2015082410251562_01_2864683_3.png含量测定结果表3. Venusil XBP C18(L)用于头孢噻肟钠含量测定结果http://ng1.17img.cn/bbsfiles/images/2017/10/2015082410281917_01_2864683_3.png有关物质测定结果表4.Venusil XBP C18(L)用于头孢噻肟钠有关物质测定结果http://ng1.17img.cn/bbsfiles/images/2017/10/2015082410305808_01_2864683_3.png色谱柱批次验证结果表5. Venusil XBP C18(L)批次验证结果http://ng1.17img.cn/bbsfiles/images/2017/10/2015082410355084_01_2864683_3.png色谱柱寿命测试结果表6.Venusil XBP C18(L)用于头孢噻肟钠寿命测试结果http://ng1.17img.cn/bbsfiles/images/2015/08/201508241038_562414_2864683_3.png
[color=#444444]本人做了头孢噻呋钠的样品,想用高效液相色谱分析一下,但是不知道具体的分析方法,想求助一下分析方法,谢谢[/color]
[align=right][b]SGLC-LC-338[/b][/align][b]摘要:[/b]本文建立了头孢呋辛钠有关物质分析的HPLC方法。参照2020版《中国药典》中色谱条件,采用色谱柱ShimNex HE C8分析头孢呋辛钠有关物质,结果显示,去氨甲酰头孢呋辛与头孢呋辛分离度大于3.0,且主峰与后相邻杂质峰基线分离,满足《中国药典》要求。此方法可为头孢呋辛钠有关物质分析提供参考。。[b]关键词:[/b]头孢呋辛钠 有关物质 ShimNex HE C8 HPLC[b]1. 实验部分1.1 实验仪器及耗材[/b]Shimadzu LC-40D高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url];色谱柱:ShimNex HE C8 (5 μm,4.6×250 mm;P/N:380-01241-09);纯水机:PR-FP-0120α-MT1(+ 60L水箱 + 取水器)SHIMSEN Arc Disc HPTFE针式过滤器(P/N:380-00341-05);[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]认证样品瓶LabTotal Vial(P/N:227-34001-01);SHIMSEN Pipet[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url]:SHIMSEN Pipet PMII-10(P/N:380-00751-02);SHIMSEN Pipet PMII-100(P/N:380-00751-04);SHIMSEN Pipet PMII-1000(P/N:380-00751-06)。[b]1.2 系统适用性溶液的制备[/b]取头孢呋辛对照品适量,加水溶解并稀释制成每1 mL含0.5 mg的溶液,置60℃水浴放置30分钟,放冷,使头孢呋辛部分转化为去氨甲酰头孢呋辛。[b]1.3 分析条件[/b]色谱柱:ShimNex HE C8 (5 μm,4.6×250 mm;P/N:380-01241-09)柱温:30℃检测波长:273 nm流速:1.0 mL/min进样量:20 μL流动相:A: 醋酸盐缓冲液(取醋酸钠0.68 g,冰醋酸5.8 g,加水稀释成 1000 mL,用冰醋酸调节pH值至3.4) B:乙腈梯度程序如下:[img]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-LC-338-01.png[/img][b]2. 实验结果[/b]按照上述色谱条件(1.3)进行采集,系统适用性溶液色谱图如下:[b]系统适用性溶液[/b][img]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-LC-338-02.png[/img][b]系统适用性放大图[/b][img]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-LC-338-03.png[/img][img]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-LC-338-04.png[/img][img]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-LC-338-05.png[/img][b]重现性[/b]系统适用性溶液重现性[img]https://img.shimadzumall.com/Storage//userfiles/images/Img_articles/SGLC-LC-338-06.png[/img][b]3. 结论[/b] 本文建立了头孢呋辛钠有关物质分析的HPLC方法。参照2020版《中国药典》中色谱条件,采用色谱柱ShimNex HE C8分析头孢呋辛钠有关物质,结果显示,去氨甲酰头孢呋辛与头孢呋辛分离度大于3.0,且主峰与后相邻杂质峰基线分离,满足《中国药典》要求。此方法可为头孢呋辛钠有关物质分析提供参考。
[color=black]头孢哌酮钠(Cefoperazone Sodium)为第三代头孢菌素,属β-内酰胺类抗生素。[/color][align=left][img=,297,163]https://ng1.17img.cn/bbsfiles/images/2019/03/201903120919066287_2141_2222981_3.jpg!w297x163.jpg[/img][/align][align=left][color=black]头孢哌酮钠 (M.W.667.65)Cefoperazone Sodium[/color][/align][color=black]CAPCELLPAK C18 MG[/color][color=black]和C18 UG120使用聚合物包被技术,抑制残留硅醇基的二次效应,同时采用超高纯硅胶,金属杂质更低,峰形更尖锐,非常适合具有配位结构、易与金属离子鳌合进而导致峰形拖尾的配位性化合物的分析。[/color][color=black]CAPCELLPAK C18 UG120[/color][color=black]的表面极性非常低,因此极性化合物可以以尖锐峰形快速溶出,同时也能取得良好的分离效果,具有独特的分离特性。而CAPCELL PAK C18 MG的整体保留能力较UG120更强,从极性化合物到疏水性化合物,对应各种极性的化合物都具有高保留能力和高柱效,适合大多数的一般分析。[/color][img=,400,231]https://ng1.17img.cn/bbsfiles/images/2019/03/201903120924348057_9069_2222981_3.jpg!w900x522.jpg[/img][img=,400,289]https://ng1.17img.cn/bbsfiles/images/2019/03/201903120924401677_8334_2222981_3.jpg!w900x651.jpg[/img][align=left][b][color=#0070c0][/color][/b][/align][align=left][b][color=#0070c0][/color][/b][/align][align=left][b][color=#0070c0]实验方法[/color][/b][/align][color=black]按照2015年版《中国药典》头孢哌酮钠含量测定项下方法对头孢哌酮钠原料药进行分析。[/color][color=black][/color][img=,400,236]https://ng1.17img.cn/bbsfiles/images/2019/03/201903120930296387_4566_2222981_3.jpg!w735x435.jpg[/img][img=,400,251]https://ng1.17img.cn/bbsfiles/images/2019/03/201903120930391737_1789_2222981_3.jpg!w755x474.jpg[/img][align=left][color=black] 图1 CAPCELL PAK C18 UG120分析结果 [/color][color=black][color=black]图2 CAPCELL PAK C18 MG分析结果[/color][/color][/align][color=black][/color][align=center][color=black] [/color][/align][align=left][color=black] [img=,400,117]https://ng1.17img.cn/bbsfiles/images/2019/03/201903120933467027_8088_2222981_3.jpg!w900x264.jpg[/img][img=,400,134]https://ng1.17img.cn/bbsfiles/images/2019/03/201903120933567447_2275_2222981_3.jpg!w900x303.jpg[/img][/color][/align][align=left][color=black] 表1 CAPCELL PAK C18 UG120结果详表 [/color][color=black]表2 CAPCELLPAK C18 MG 结果详表[/color][/align][align=left][color=black][img=,400,185]https://ng1.17img.cn/bbsfiles/images/2019/03/201903120934501237_9662_2222981_3.jpg!w900x418.jpg[/img][/color] [/align][color=black]综上所述,CAPCELL PAK C18 MG和C18 UG120两款色谱柱均能实现头孢哌酮钠的良好分离,头孢哌酮主峰不对称因子分别为1.23和1.38;其中,MG色谱柱的保留能力相对较强,而UG120可使极性物质快速溶出,用户可结合实际情况进行选择。[/color]
请教各位老师,在分析头孢曲松钠时,分析它的头孢曲松聚合物时,药典规定用柱色谱法,但它的项下的却是高效液相的方法,请问这是怎么一回事
求头孢西丁钠、头孢泊肟钠红外图谱
求头孢西丁钠、头孢泊肟钠红外图谱
头孢西丁钠有关杂质 头孢西丁钠有关杂质
谁有头孢西酮钠的检验方法,分离度尽量好点的,求帮助。

1、样品信息 样品名称结构式分子式分子量CAS号贮藏条件头孢羟氨苄 (Cefadroxil)http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_647856_2891022_3.jpgC16H17N3O5S,H2O381.4150370-12-2遮光,密封,在阴凉处保存2、色谱条件流动 相:0.02mol/L的磷酸二氢钾溶液(1mol/L氢氧化钾调pH至5.0)-甲醇(98:2), 等度洗脱检测波长:230 nm柱 温:30℃进样 量:10μl流 速:1.0 ml/min色谱 柱:Innoval AQ C18, 5μm,100Å,4.6×150mm3[back=#fbfbf9

1、样品信息 样品名称结构式分子式分子量CAS号贮藏条件头孢羟氨苄 (Cefadroxil)http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_647663_2891019_3.jpgC16H17N3O5S,H2O381.4150370-12-2遮光,密封,在阴凉处保存2、色谱条件流动 相:0.02mol/L的磷酸二氢钾溶液(1mol/L氢氧化钾调pH至5.0)-甲醇(98:2), 等度洗脱检测波长:230 nm柱 温:30℃进样 量:10μl流 速:1.0 ml/min色谱 柱:Innoval AQ C18, 5μm,100Å,4.6×150mm3[back=#fbfbf9
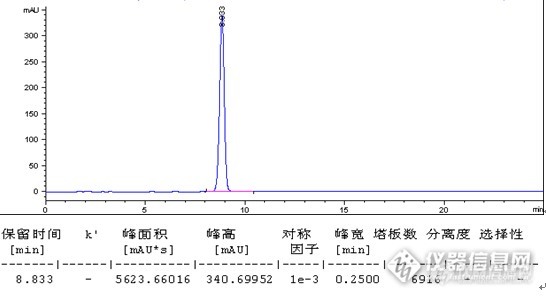
1、样品信息 样品名称结构式分子式分子量CAS号贮藏条件头孢羟氨苄 (Cefadroxil)http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_647835_2891022_3.jpgC16H17N3O5S,H2O381.4150370-12-2遮光,密封,在阴凉处保存2、色谱条件流动 相:0.02mol/L的磷酸二氢钾溶液(1mol/L氢氧化钾调pH至5.0)-甲醇(98:2), 等度洗脱检测波长:230 nm柱 温:30℃进样 量:10μl流 速:1.0 ml/min色谱 柱:Innoval AQ C18, 5μm,100Å,4.6×150mm3[back=#fbfbf9

1、样品信息样品名称结构式分子式分子量CAS号贮藏条件注射用头孢拉定(Cefradine for Injection)http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_647936_2891022_3.jpgC16H19N3O4S349.4038821-53-3密闭,在凉暗处保存2、色谱条件流动相:以含0.027mol/L辛磺酸钠的磷酸氢二钠溶液(磷酸调pH至8.0)-甲醇(75:25), 等度洗脱检测波长:206 nm柱温:30℃进样量:10μl流速:1.0 ml/min色谱柱:Durashell C18-AM,5μm,100Å,4.6×250mm3、测定结果3.1 样品测定结果样品测定图谱 http://ng1.17img.cn/bbsfiles/images/2014/06/201406251145_502961_801_3.pnghttp://ng1.17img.cn/bbsfiles/images/2014/06/201406251146_502962_801_3.png样品测定结果主峰名称保留时间(min)理论塔板数拖尾因子头孢拉定6.69595010.9393.2 不同批次色谱柱验证结果第1[/fon

1、样品信息样品名称结构式分子式分子量CAS号贮藏条件注射用头孢拉定(Cefradine for Injection)http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_647829_2891022_3.jpgC16H19N3O4S349.4038821-53-3密闭,在凉暗处保存2、色谱条件流动相:以含0.027mol/L辛磺酸钠的磷酸氢二钠溶液(磷酸调pH至8.0)-甲醇(75:25), 等度洗脱检测波长:206 nm柱温:30℃进样量:10μl流速:1.0 ml/min色谱柱:Durashell C18-AM,5μm,100Å,4.6×250mm3、测定结果3.1 样品测定结果样品测定图谱 http://ng1.17img.cn/bbsfiles/images/2014/06/201406251145_502961_801_3.pnghttp://ng1.17img.cn/bbsfiles/images/2014/06/201406251146_502962_801_3.png样品测定结果主峰名称保留时间(min)理论塔板数拖尾因子头孢拉定6.69595010.9393.2 不同批次色谱柱验证结果

头孢西丁钠有关杂质
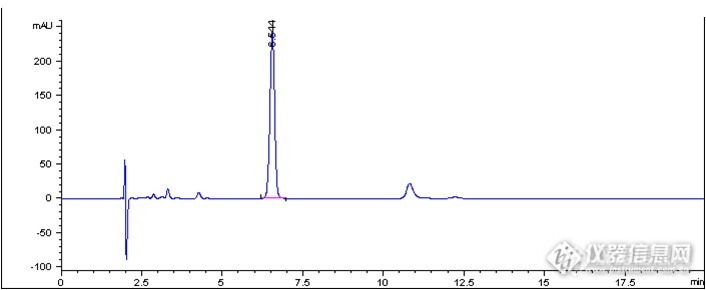
1、样品信息样品名称结构式分子式分子量CAS号贮藏条件注射用头孢拉定(Cefradine for Injection)http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_647675_2891019_3.jpgC16H19N3O4S349.4038821-53-3密闭,在凉暗处保存2、色谱条件流动相:以含0.027mol/L辛磺酸钠的磷酸氢二钠溶液(磷酸调pH至8.0)-甲醇(75:25), 等度洗脱检测波长:206 nm柱温:30℃进样量:10μl流速:1.0 ml/min色谱柱:Durashell C18-AM,5μm,100Å,4.6×250mm3、测定结果3.1 样品测定结果样品测定图谱 http://ng1.17img.cn/bbsfiles/images/2014/06/201406251145_502961_801_3.pnghttp://ng1.17img.cn/bbsfiles/images/2014/06/201406251146_502962_801_3.png样品测定结果主峰名称保留时间(min)理论塔板数拖尾因子头孢拉定6.69595010.9393.2 不同批次色谱柱验证结果第1批次色谱柱测定图谱http://ng1.17img.cn/bbsfiles/images/2014/06/201406251146_502963_801
注射用头孢西丁钠生产工艺验证方案[~74687~]
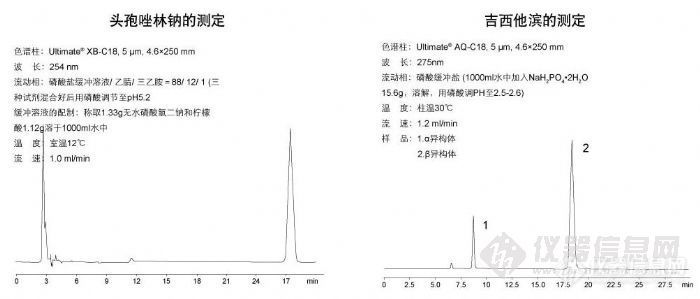
头孢唑林钠和吉西他滨的测定http://ng1.17img.cn/bbsfiles/images/2009/11/200911021830_180176_1896702_3.jpg
头孢泊肟酯的有关物质的分析,请问各路高人做过没有,色谱条件是什么,提前感谢了
[align=left][color=black]头孢克肟(Cefixime)是β-内酰胺类抗生素,为口服用的第三代头孢菌素类抗生素,适用于治疗敏感菌所致的呼吸、泌尿和胆道等部位的感染。[/color][/align][img=,619,248]https://ng1.17img.cn/bbsfiles/images/2019/03/201903271729327584_7997_2222981_3.jpg!w619x248.jpg[/img][color=black] [/color][color=black]ADME(adamantane)[/color][color=black]是笼状结构的金刚烷基团,通过“新型官能团”和特有的包被型填料表面“控制技术”,使该款色谱柱兼具疏水性和高极性的特点;由于金刚烷特有的笼状结构所带来的立体选择性,还赋予了ADME分离结构类似化合物的能力。头孢克肟极性较强,故选用键合金刚烷基团的高表面极性色谱柱CAPCELL PAK ADME进行分析。[/color][align=left][img=,400,222]https://ng1.17img.cn/bbsfiles/images/2019/03/201903271729553114_5586_2222981_3.jpg!w744x413.jpg[/img][/align][align=left][color=black]金刚烷基ADME填料表面示意图[/color][/align][color=black]使用CAPCELL PAK ADME色谱柱在0.1%甲酸水/乙腈体系下对混合对照品和血浆样品进行分析,头孢克肟峰形良好,保留时间为1.66 min。在混合对照品中,阿莫西林在该检测离子下显示为两个峰,头孢他美保留时间1.71,峰形正常,可考虑选做内标物。血浆样品能够正常检测目标物质峰。[/color][align=left][img=,500,310]https://ng1.17img.cn/bbsfiles/images/2019/03/201903271730190277_4380_2222981_3.jpg!w877x545.jpg[/img][/align][align=left][color=black]图1 混合对照品[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]分析图[/color][/align][align=left][img=,500,311]https://ng1.17img.cn/bbsfiles/images/2019/03/201903271730350327_5592_2222981_3.jpg!w879x547.jpg[/img][/align][align=left][color=black]图2 血浆样品[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]分析图[/color][/align][align=left][img=,500,261]https://ng1.17img.cn/bbsfiles/images/2019/03/201903271730528955_449_2222981_3.jpg!w818x427.jpg[/img][/align][color=black]综上所述,使用CAPCELL PAK ADME S3 2.1 mm i.d. × 100 mm色谱柱对头孢克肟混合对照品和血浆样品进行分析,可得到良好的分析结果。[/color]

抗生素头孢喹肟的动物体内药动学分析 头孢喹肟是目前唯一一个动物专用第四代头孢类抗生素,具有抗菌谱广,抗菌活性强的特点,适用于非肠道用药;源于基本头孢菌素结构的化学修饰提供了头孢喹肟的两性离子性质。头孢喹肟的这一特性可以促进其迅速跨生物膜渗透作用(包括细菌细胞壁的孔蛋白),从而增强生物利用度,较第二代和第三代头孢菌素抗菌谱更广。它对临床重要细菌的染色体和质粒编码的β-内酰胺酶高度稳定。被用于治疗动物呼吸道的疾病,牛的急性乳腺炎和腐蹄病,小牛败血症,猪子宫炎,乳房炎,无乳综合征,马驹败血病,其也是治疗羊的各类疾病的药物。 材料和方法: 头孢喹肟,、色谱乙腈、色谱甲醇、三氟乙酸(TFA)、去离子水。 岛津高效液相色谱仪、SPD-10AVP UV-VIS检测器268纳米处进行检测、柱温箱40°C、Phenomenex Gemini C18色谱柱 (250 mm ×4.6 mm; 5u m)。 流动相为乙腈和0.1%三氟乙酸水溶液,以0.9 ml/min的流速进行洗脱。 标准溶液配制: 头孢喹肟的储备溶液通过直接称量干燥后的标准物质溶解于水中,浓度1mg/ ml,并将该溶液保存于-70℃。头孢喹肟标准溶液通过加入空白血浆配制成溶度为0, 0.02, 0.04, 0.10, 0.40, 1, 2, 4, 10,和 12 ug/ml的溶液。 样品制备:200ul血浆中加入1.5毫升微量离心管中,加入等体积的甲醇使蛋白质沉淀,离心(4000转/min)10分钟后,300ul的上清离心液移入新鲜小瓶中,加入150ul去离子水混合,再吸取50ul上清液进样分析。 液相方法的验证: 选择性-选择性通过分析空白血浆、加入头孢喹肟的血浆、从羊服用头孢喹肟药代动力学研究中获得的血浆样品进行评价,无内源性化合物对目标化合物的干扰。 线性标准曲线-本方法的线性通过在0.02-12ug/ml的范围内的校正曲线评价。 灵敏度-通过进样 0.01ug/ml-0.1 ug/ml评价其信噪比。 精密度和准确度-头孢喹肟样品分低中高浓度分别进样分析,每个浓度分别进样六次日间、日内测定。 回收率-为了计算头孢喹肟的绝对回收率分别加入 0.4ug/ml, 2ug/ml, 和10ug/ml浓度样品,每个浓度分别重复6次进行加入和提取。 稳定性-标准
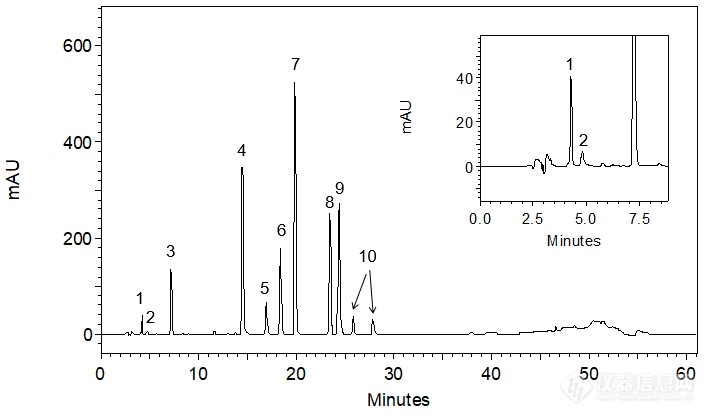
[align=center][b]头孢克洛有关物质——与9种杂质的共同分析[/b][/align]头孢克洛(cefaclor)为白色至微黄色粉末或结晶性粉末的化学品,微臭,本品在水中微溶,在甲醇、乙醇、三氯甲烷或二氯甲烷中几乎不溶,分子式:C15H14ClN3O4S。头孢克洛是β-内酰胺类抗生素,头孢菌素类药,是第二代头孢菌素,主要适用于敏感菌所致的急性咽炎、急性扁桃体炎、中耳炎、支气管炎、肺炎等呼吸道感染、皮肤软组织感染和尿路感染等。[align=center][img=,144,171]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140859582934_5220_2222981_3.gif!w144x171.jpg[/img][/align][align=center]头孢克洛[/align][align=center]M.W.: 367.81[/align]本实验对客户提供的头孢克洛原料药以及9种杂质(杂质A、B、C、D、E,7-ACCA,头孢克洛δ-3异构体,α-苯甘氨酸,苯甘氨酸甲酯盐酸盐)进行分析,希望得到杂质混合对照溶液及供试品溶液中各杂质的良好分离。客户反馈,将流动相磷酸盐体系的pH值由4.0提高到4.5可得到杂质混合对照溶液中7-ACCA和α-苯甘氨酸之间的良好分离,但头孢克洛与其相邻杂质E峰之间分离较难。客户前期使用了CAPCELL PAK C[sub]18 [/sub]MGII S3 4.6 mm i.d. × 250 mm色谱柱进行分析,在此基础上,我们尝试了其他填料的几款色谱柱进行分离尝试,分别为CAPCELL PAK C[sub]18[/sub] AQ(S3& S5)、CAPCELL PAK ADME(金刚烷基)、SUPERIOREX ODS、CAPCELL PAK PFP(五氟苯基)、CAPCELL PAK CN(氰基)。首先,参考客户提供的液相条件,使用高极性色谱柱[b]CAPCELL PAK C[sub]18 [/sub]AQ[/b]对杂质混合对照溶液进行分析尝试;为了得到杂质间的更好分离,粒径选择3 μm,如图1,[color=#2F5496]各杂质间均能得到良好的分离结果,头孢克洛与杂质[/color][color=#2F5496]E[/color][color=#2F5496]的分离度为[/color][color=#2F5496]2.70[/color][color=#2F5496],达到基线分离。[/color][color=#2F5496][/color][align=center][img=,690,405]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140902184290_9307_2222981_3.png!w690x405.jpg[/img][/align][align=center]图1 AQ S3 分析杂质混合对照溶液结果[/align][align=center] [/align][align=center]1.α-苯甘氨酸 2. 7-ACCA 3. 杂质A 4. 杂质B 5. 苯甘氨酸甲酯盐酸盐 6.杂质C[/align][align=center]7. 头孢克洛δ-3异构体 [color=#ff0000]8. 头孢克洛 9. 杂质E [/color]10.杂质D[/align][color=#2F5496][img=,555,311]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140902187828_2715_2222981_3.png!w555x311.jpg[/img][/color]进一步分析供试品溶液,如图2,由于样品浓度较高,导致头孢克洛主峰向后展宽,进而将杂质E包于其中。[color=#2F5496][/color][align=center][color=#2F5496][img=,659,441]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140915544228_5404_2222981_3.png!w659x441.jpg[/img][/color][/align][align=center]图2 AQ S3 分析供试品溶液结果[/align][align=center][/align][align=left]为使头孢克洛和杂质E之间得到更好的分离,我们尝试对色谱条件进行调整。[/align][align=left][/align][align=left][b]1.调整柱温[/b][/align][align=left][b][/b]首先对温度进行调整:实验过程中发现柱温对头孢克洛与杂质E的出峰行为有较大影响——当柱温设置为20 ℃时,头孢克洛和杂质E之间能够得到良好分离;将温度提高到30℃时,杂质E向前移动趋势较大。为使杂质E峰出在头孢克洛峰前,避免由于供试品中头孢克洛峰的展宽而使杂质E被包于其内,进一步将柱温提高到40℃,发现头孢克洛与杂质E峰重合;最终,将柱温提高到45℃,此时杂质E峰移至头孢克洛峰前,但未能得到理想的分离结果。[/align][align=left][/align][align=center][img=,659,430]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140916597550_373_2222981_3.png!w659x430.jpg[/img][/align][align=center]图3 不同柱温条件下AQ S3分析杂质混合对照溶液结果[/align][align=center][/align][align=left][b]2.调整流动相[/b][/align][align=left][b][/b][/align][align=left]考虑到提高柱温对色谱柱寿命的影响,仍选择初始使用的20℃,对流动相梯度条件进行调整。在增强整体保留时间的同时,发现[color=#538135]头孢克洛和杂质[/color][color=#538135]E[/color][color=#538135]的出峰顺序发生了颠倒[/color],且[color=#538135]分离良好[/color],进而有效避免了杂质E被包于头孢克洛主峰中的问题;而在主峰后出峰的杂质D与头孢克洛之间分离度亦较高,即使供试品溶液中的头孢克洛峰展宽,也不会出现将杂质D包于其中的问题。[/align][align=left]因此我们在此梯度条件下进一步对供试品溶液进行分析,如图4,头孢克洛与各杂质峰之间均能得到良好的分离结果。[/align][align=left][/align][align=center][img=,679,417]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140917450308_6331_2222981_3.png!w679x417.jpg[/img][/align][align=center]图4 AQ S3分析杂质混合对照溶液及供试品溶液结果(调整梯度)[/align][align=center] [/align][align=center]1.α-苯甘氨酸 2. 7-ACCA 3. 杂质A 4. 杂质B 5. 苯甘氨酸甲酯盐酸盐 6.杂质C[/align][align=center]7. 头孢克洛δ-3异构体 [color=#ff0000]8. 杂质E 9. 头孢克洛[/color] 10.杂质D[/align][align=left][img=,587,335]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140918136074_9375_2222981_3.png!w587x335.jpg[/img][/align][align=left][/align][align=left]为使客户有更多的色谱柱选择,本实验室也尝试使用键合金刚烷基的高极性色谱柱CAPCELL PAK ADME分析杂质混合对照溶液和供试品溶液,如图5,在分析杂质混合对照溶液时,能够得到各组分的良好分离,同时发现杂质E和头孢克洛出峰顺序发生颠倒,但同时也发现头孢克洛峰与其后相邻杂质D峰之间分离度较低(Rs=1.71);因此,如图6,在分析供试品溶液时,由于色谱峰向后展宽,使得杂质D被包于头孢克洛主峰中,未能得到理想分离结果。[/align][align=left][/align][align=center][img=,690,426]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140918484278_6616_2222981_3.png!w690x426.jpg[/img][/align][align=center]图5 ADME 分析杂质混合对照溶液结果[/align][align=center] [/align][align=center]1.α-苯甘氨酸 2. 7-ACCA 3. 杂质A 4. 杂质B 5. 苯甘氨酸甲酯盐酸盐 6.杂质C[/align][align=center]7. 头孢克洛δ-3异构体 [color=#ff0000]8. 杂质E 9. 头孢克洛[/color] 10.杂质D[/align][align=left][/align][align=center][img=,689,417]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140918485898_9906_2222981_3.png!w689x417.jpg[/img][/align][align=center]图6 ADME 分析杂质混合对照溶液结果[/align][align=left][img=,585,336]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140919331328_5070_2222981_3.png!w585x336.jpg[/img][/align][align=left][/align][align=left][/align][align=left]之后,我们也尝试使用了CN(氰基柱)和PFP(五氟苯基)以及高碳载量的SUPERIOREX ODS色谱柱,在客户提供的色谱条件下对杂质混合对照溶液进行分析,均未能得到更理想的分离结果。[/align]
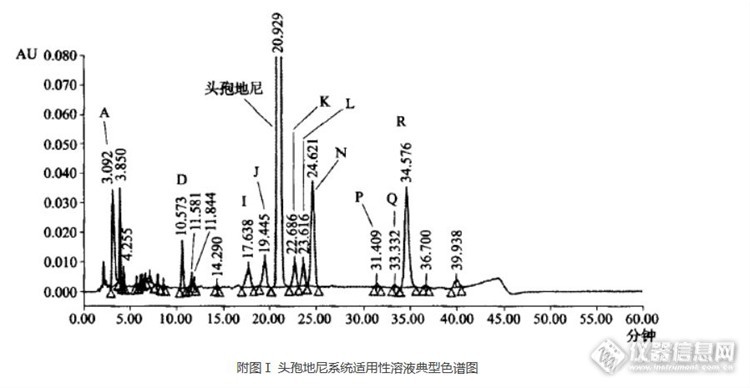
本数据依据2015年版《中国药典》二部头孢地尼项下方法,对头孢地尼原料药进行分析。客户反映主峰前后杂质与主峰分离度较难达到药典标准,需求合适C18柱进行分析以达到药典分离要求;因此分别尝试使用资生堂CAPCELL PAK MGII,SUPERIOREX ODS, AQ, BB等C18色谱柱对客户所提供样品进行分析,最终发现高极性的C18 AQ柱分析结果最佳,如图1。http://ng1.17img.cn/bbsfiles/images/2016/10/201610250907_615006_2222981_3.jpg头孢地尼主峰保留时间为20.73min,同药典头孢地尼系统适用性溶液的典型色谱图基本相符(如附图 I);药典要求头孢地尼峰与杂质J峰之间分离度不小于1.2,杂质I峰与杂质J峰、头孢地尼峰与杂质K峰及杂质K峰与杂质L峰之间分离度应符合要求,此时头孢地尼峰与杂质J峰分离度为1.21,杂质I峰与杂质J峰分离度为2.19,头孢地尼峰与杂质K峰分离度为2.77,杂质K峰与杂质L峰分离度为1.70,均符合药典规定。 药典要求使头孢地尼保留时间约为22min,因此进一步降低流速进行分析,结果如图2。http://ng1.17img.cn/bbsfiles/images/2016/10/201610250909_615008_2222981_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/10/201610250907_615005_2222981_3.jpg此时头孢地尼主峰保留时间为22.18min,符合药典要求;头孢地尼峰与杂质J峰分离度为1.23,杂质I峰与杂质J峰分离度为2.35,头孢地尼峰与杂质K峰分离度为2.68,杂质K峰与杂质L峰分离度为1.84,均符合药典规定。在该分析条件下对按药典方法配制的供试品溶液进行分析,分析结果如图3。http://ng1.17img.cn/bbsfiles/images/2016/10/201610250907_615007_2222981_3.jpg对供试品分析的结果中,我们发现AQ柱能够使供试品中各杂质均能够得到良好的基线分离。当然,为了有更多的色谱柱选择,在同样的分析条件进一步尝试使用中等极性的MGII柱、高碳载量的SUPERIOREX ODS、强耐碱性的BB柱分别对系统适用性溶液进行分析,但头孢地尼峰与其前杂质J峰的分离度分别为0.95,1.02,0.66,均未能符合药典分离要求。

[align=center][b]2015年版《中国药典》数据:头孢氨苄有关物质的分析[/b][/align]客户提供了头孢氨苄工作对照品、杂质7-氨基去乙酰氧基头孢烷酸、α-苯甘氨酸、△-2-头孢氨苄对照品和80℃条件下破解供试品溶液所得的分离度溶液。现要求本实验室选择合适的C[sub]18[/sub]色谱柱,实现头孢氨苄的有关物质分析。在头孢氨苄有关物质分析中,流动相为高水相条件,故本实验室首先尝试使用能在高水相下稳定使用的高极性色谱柱CAPCELL PAK C[sub]18 [/sub]AQ S5 4.6 mm i.d. × 250 mm(柱号:A6AD04229),对80℃破解所得分离度溶液进行分析,结果见图1。[align=center][img=,567,357]http://ng1.17img.cn/bbsfiles/images/2017/11/201711161024_01_2222981_3.png!w567x357.jpg[/img][/align][align=center]图1 80℃破解溶液及空白溶液分析所得色谱图(C[sub]18 [/sub]AQ色谱柱)[/align][align=left]*注:峰上所标数字为分离度,下同。[/align][img=,581,192]http://ng1.17img.cn/bbsfiles/images/2017/11/201711161024_02_2222981_3.png!w581x192.jpg[/img]如图1,头孢氨苄主峰保留时间为21.09min,主峰与前后杂质分离度分别为2.42和3.37,达到药典要求的基线分离。进一步分析杂质对照品溶液和供试品溶液,如图2,杂质7-氨基去乙酰氧基头孢烷酸(7-ADCA)和α-苯甘氨酸的分离度为11.19,符合药典要求。[align=center][img=,566,359]http://ng1.17img.cn/bbsfiles/images/2017/11/201711161025_01_2222981_3.png!w566x359.jpg[/img][/align][align=center]图2 杂质对照品溶液分析所得色谱图(C[sub]18[/sub] AQ色谱柱)[/align][img=,684,231]http://ng1.17img.cn/bbsfiles/images/2017/11/201711161025_02_2222981_3.png!w684x231.jpg[/img]如图3,对供试品溶液进行分析,各杂质间分离度良好。[align=center][img=,554,362]http://ng1.17img.cn/bbsfiles/images/2017/11/201711161026_01_2222981_3.png!w554x362.jpg[/img][/align][align=center]图3 头孢氨苄供试品溶液分析所得色谱图(C[sub]18 [/sub]AQ色谱柱)[/align][img=,585,192]http://ng1.17img.cn/bbsfiles/images/2017/11/201711161026_02_2222981_3.png!w585x192.jpg[/img]客户要求考察低浓度(10 μg/mL)下头孢氨苄与其异构体△-2-头孢氨苄的分离情况,在客户允许调整柱温(30℃~40℃)的前提下进行分析,如图4,当柱温设定为30℃时,头孢氨苄与△-2-头孢氨苄的分离度最佳,为1.17。[align=center][img=,566,371]http://ng1.17img.cn/bbsfiles/images/2017/11/201711161028_01_2222981_3.png!w566x371.jpg[/img][/align][align=center]图4 头孢氨苄及△-2-头孢氨苄混合溶液分析所得色谱图(C[sub]18[/sub] AQ色谱柱)[/align][img=,583,193]http://ng1.17img.cn/bbsfiles/images/2017/11/201711161028_02_2222981_3.png!w583x193.jpg[/img]为使客户有更多色谱柱选择,本实验室又进一步尝试了资生堂中等极性色谱柱CAPCELL PAK C[sub]18 [/sub]MGII以及高碳载量色谱柱SUPERIOREX ODS进行分析。使用CAPCELL PAK C[sub]18[/sub] MGII色谱柱在30℃条件下对头孢氨苄及其异构体△-2-头孢氨苄进行分离,分离度为1.05,分离效果不及CAPCELL PAK C[sub]18 [/sub]AQ;使用SUPERIOREX ODS色谱柱进行分析,分离度为1.18,分离效果略优于AQ柱,但在分析破解所得分离度溶液时,杂质峰形及分离效果不佳。在对头孢氨苄及其异构体△-2-头孢氨苄的分离中,本实验室也尝试使用键和金刚烷基团的高表面极性色谱柱CAPCELL PAK ADME和键合五氟苯丙基、对同分异构体有良好分离能力的CAPCELL PAK PFP色谱柱进行尝试。由于ADME色谱柱保留较强,在原梯度条件下未得到待测物洗脱,提高梯度条件中有机相比例后,亦未得到理想的分离效果;而使用CAPCELL PAK PFP S5 4.6 mm i.d. × 250 mm(TQAD01002)色谱柱进行分析,能得到4.84的分离度(见图5)。表1为各色谱柱分离度结果对比。[align=center][img=,554,357]http://ng1.17img.cn/bbsfiles/images/2017/11/201711161030_01_2222981_3.png!w554x357.jpg[/img][/align][align=center]图5 头孢氨苄及△-2-头孢氨苄混合溶液结果(PFP色谱柱)[/align][img=,582,190]http://ng1.17img.cn/bbsfiles/images/2017/11/201711161030_03_2222981_3.png!w582x190.jpg[/img][align=center]表1 各色谱柱分离度结果对比(色谱柱规格S5 4.6 mm i.d. × 250 mm)[/align][align=center][img=,471,160]http://ng1.17img.cn/bbsfiles/images/2017/11/201711161030_04_2222981_3.png!w471x160.jpg[/img][/align][align=center][/align][align=left]进一步,使用PFP色谱柱在原色谱条件下对供试品溶液、杂质对照溶液、△-2-头孢氨苄对照溶液、高温破解溶液及空白溶液进行分析。供试品溶液中各杂质能得到良好分离,主峰头孢氨苄与杂质△-2-头孢氨苄分离度为1.78(见图6),杂质对照品溶液中7-ADCA和α-苯甘氨酸的分离度为[b]7.28[/b](见图7)。[/align][align=left][/align][align=center][img=,568,372]http://ng1.17img.cn/bbsfiles/images/2017/11/201711161031_02_2222981_3.png!w568x372.jpg[/img][/align][align=center]图6 供试品溶液、空白及△-2-头孢氨苄溶液分析所得色谱图(PFP色谱柱)[/align][align=center][img=,572,376]http://ng1.17img.cn/bbsfiles/images/2017/11/201711161031_01_2222981_3.png!w572x376.jpg[/img][/align][align=center]图7 80℃破解溶液及杂质对照溶液分析所得色谱图(PFP色谱柱)[/align][align=center] [/align][align=left]综上实验结果,在C[sub]18[/sub]系列色谱柱中,使用资生堂CAPCELL PAK C[sub]18 [/sub]AQ S5 4.6 mm i.d. × 250 mm(A6AD04229)色谱柱分析头孢氨苄有关物质结果最优,能够实现杂质对照溶液及高温破解所得分离度溶液的分离。在供试品溶液分析中,由于浓度较高,△-2-头孢氨苄被包于主峰中,客户反馈属正常现象,单独考察低浓度头孢氨苄与其异构体△-2-头孢氨苄的混合溶液分离情况,能够达到1.17的分离度结果。[/align][align=left]在头孢氨苄及其异构体△-2-头孢氨苄的分离中,相比C[sub]18[/sub]柱,资生堂CAPCELL PAK PFP S5 4.6 mm i.d. × 250 mm(TQAD01002)色谱柱能够达到分离度为4.84的良好分离结果,在杂质对照溶液及供试品溶液的分析中,能够得到满足药典分离要求的良好结果,供客户参考。[/align]
有关物质检查方法参照USP-34:有关物质 取装量差异项下的细粉适量(相当于头孢地尼75mg),置50ml量瓶中,加0.1mol/L磷酸缓冲液30ml溶解,并用0.1%四甲基氢氧化铵溶液稀释至刻度,制成每1ml约含头孢地尼1.5mg的溶液,滤过,取续滤液作为供试品溶液。精密称取头孢地尼对照品适量,加0.1mol/L磷酸缓冲液溶解并定量稀释制成每1ml中约含头孢地尼0.75mg的溶液,精密量取适量,加0.1%四甲基氢氧化铵溶液并定量稀释至每1ml约含头孢地尼15μg的对照品溶液。照高效液相色谱法(中国药典2010版二部附录V D)测定,用十八烷基硅烷键合硅胶为填充剂(粒径:5um,规格:4.6mm×250mm);流动相A为0.1%四甲基氢氧化铵溶液(用磷酸调节pH值至5.5)1000ml,加入0.1mol/L乙二胺四醋酸二钠溶液0.4ml,流动相B为0.1%四甲基氢氧化铵溶液(用磷酸调节pH值至5.5)-乙腈-甲醇(500:300:200),加入0.1mol/L乙二胺四醋酸二钠溶液0.4ml;按表Ⅰ进行线性梯度洗脱。柱温为40℃,检测波长为254nm。精密称取头孢地尼对照品约37.5mg,置25ml量瓶中,加0.1mol/L磷酸缓冲液10ml溶解,并加入头孢地尼杂质A对照品溶液(取头孢地尼杂质A对照品适量,加0.1%四甲基氢氧化铵溶液溶解并稀释制成每1ml含0.04mg的溶液)5.0ml、头孢地尼杂质B对照品溶液(取头孢地尼杂质B对照品适量,加0.1%四甲基氢氧化铵溶液溶解并稀释制成每1ml含0.04mg的溶液)5.0ml,用0.1%四甲基氢氧化铵溶液稀释至刻度,摇匀,作为系统适应性溶液,取10μl注入液相色谱仪,记录色谱图;头孢地尼峰保留时间约为20分钟,头孢地尼杂质A有四个峰,相对头孢地尼主峰保留时间分别约为0.85、0.94、1.11和1.14;头孢地尼杂质B峰相对头孢地尼主峰保留时间约为1.28;头孢地尼峰与头孢地尼杂质A第三个峰之间的分离度应不小于1.5;头孢地尼杂质B峰的拖尾因子不大于1.5。取对照品溶液10μl注入液相色谱仪,调节检测灵敏度,使主成分色谱峰的峰高约为满量程的20%,精密量取对照品溶液和供试品溶液各10μl,注入液相色谱仪中,记录色谱图。供试品溶液色谱图中如有杂质峰,均采用以下公式按外标法以峰面积计算,杂质的限度见表Ⅱ。(供试品溶液中任何小于头孢地尼对照品溶液主峰面积0.05倍的峰可忽略不计)。表Ⅰ时间(分钟)流动相A(%)流动相B(%)095529552275253250503750503895548955杂质的含量采用以下公式计算:(rU/rS)×(Cs/CU)×(100/F)Cs为头孢地尼对照品溶液中头孢地尼的浓度(mg/ml);CU为供试溶液中头孢地尼的浓度(mg/ml);rU为供试溶液中杂质峰面积;rS为头孢地尼对照品溶液中头孢地尼峰面积;F为表Ⅱ中各杂质的相对响应因子;表Ⅱ 有关物质相对保留时间相对响应因子限值(%)杂质Ⅷ[/siz
求购头孢地尼E-异构体对照品头孢地尼做分析方法验证,其中有关物质头孢地尼E-异构体标准品买不到。很多销售公司都有但是资质不全我不能买他们的。请教各位大侠们,帮个忙吧。急用!!谢谢!!!!
头孢类抗生素在食用动物中的有效分析一直是热点。分享一种分子印迹固相萃取联合高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url]紫外检测器(MISPE-HPLC-UV)检测食品样品中头孢噻呋钠(CTFS)的方法。在该方法中,首先合成了一种环保的分子印迹聚合物(MIP)并用作吸附剂,它对水中的CTFS表现出优异的选择性,并且可以在1小时内达到吸附平衡。在优化的条件下,CTFS 在 0.005–1.0 mg L -1范围内获得了良好的线性,定量限为 0.0015 mg L -1,在牛奶、鸡肉、猪肉和牛肉样品的三个加标水平下,平均回收率高于 91.9%(RSD 小于 8.5%)。20个循环后,用于CTFS的MISPE小柱的回收率仍高于95%,证明了MISPE-HPLC-UV方法对食品样品中CTFS的分析具有较高的灵敏度和选择性。相关研究详见https://doi.org/10.1016/j.foodchem.2021.129013
[font=SimSun][color=#d40a00]维权声明:本文为[font=Times New Roman]luxw(小卢)[/font]原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。[size=5][b][marquee]恭喜luxw本作品被《分析试验室》杂志收录,接收在《分析试验室》2010年12月刊上发表[/marquee] [/b][/size][/color] [size=3] [b]HPLC法测定头孢曲松钠聚合物[size=2][font=SimSun]摘要:[/font][/size][/b][/size][size=2][font=宋体]目的:建立测定头孢曲松钠聚合物测定的高效液相色谱方法,并寻找减少样品分析时间的方法。方法:采用安捷伦1100高效液相色谱仪、不锈钢色谱柱(填料:Sephadex G-10,尺寸:10.0mm×300mm)、进样量100ul、检测波长254nm、流速1.5ml/min,在不同的流动相A和B中分析,并寻找梯度洗脱的比例来减少基线稳定时间。结果:方法满足检测要求,得到减少样品分析时间的梯度洗脱方法。[/font][b]关键词:[/b]聚合物、高效液相、谱图、基线、梯度洗脱[/size][size=2][b]正文:[/b][font=宋体]β-[/font][font=宋体]内酰胺类抗生素高分子杂质(中国药典称为“聚合物”,本文亦称聚合物)是引起临床过敏反应的一种杂质,往往是在生产、储存中降解得到或变大。为了保证临床用药安全,必须严格控制其含量,中国药典2010版也加大了对此类药品的聚合物检测。[/font]头孢曲松钠为头孢类无菌原料药,其聚合物是杂质检测中重要的一项。在以往的实验中,一般采用高分子杂质仪进行测定其含量,仪器一般是由泵、检测器、数据处理器、色谱柱等在实验室组合而成,[color=black]其柱为内径1.0-1.4cm的玻璃柱,填料为葡聚糖凝胶G-10,溶于水后在常压环境下手动填装而成。此仪器组装不方便,对其进行3Q验证困难,对国外认证来说比较困难。而仪器本身采用手动进样、色谱柱用前填装,因此实验过程繁琐、样品运行时间较长。为了适应国外验证的需要、减少样品分析时间,现采用高效液相色谱仪和高压填装的不锈钢色谱柱进行测定。[/color][/size][font=SimSun][/font][font=SimSun][size=2][b]1 色谱条件:[/b]仪 器:agilent1100色谱柱:Sephadex G-10, 10.0mm×300mm流动相:A:pH7.0的0.1mol/L磷酸盐缓冲液, B:水流 速:1.5ml/min波 长:254nm进样量:100ul[b]2 系统适应性:[/b]2.1蓝色葡聚糖2000在流动相A、B中的理论塔板数应大于400,拖尾因子小于应2.0,两种流动相中保留时间比应在0.93-1.07之间;2.2对照液主峰和供试品溶液中聚合物峰与相应色谱系统中蓝色葡聚糖2000峰保留时间的比值均应在0.93-1.07之间;2.3系统配制溶液测得高聚体的峰高与单体与高聚体之间的谷高比应大于2.0;2.4对照品连续进样5次,峰面积的RSD应不大于5.0%[/size][/font][/font]

头孢曲松钠的测定和泼尼松龙和氢化可的松的测定http://ng1.17img.cn/bbsfiles/images/2009/11/200911021846_180184_1896702_3.jpg
为什么可以利用红外光谱分析法来区分不同的氨噻肟类头孢菌素药物