各位老师大家好,我现在遇到一个很棘手的问题,就是一对烯烃的异构体没有办法分离,大家有没有什么烯烃异构体分析的经验啊,请指点迷津啊! 这对烯烃的碳原子在20个左右,就是烯烃的双建的位置不一样,很难分离,液相气相能想到的方法差不多都试过了,还是没有分开。
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=105317]同分异构体[/url]大家帮我看看,同分异构体,只是双键的位置不同,怎么分离啊。用了C18的柱子,试了很多条件都是分不开。
有哪位高手做过液相拆分同分异构体。玉米黄素和叶黄素的分离,找了好多条件就是分不开,这两种物质在结构上只有一个双键的位置不同。好难啊 哪位高手指点一下啊 谢谢了
如题,异构体有很多种,官能团异构、位置异构、立体异构等等。实际工作中你都用过哪些柱子分离异构体?有图谱分享的有额外奖励啊!欢迎分享!
亲们,现遇到一个棘手的问题向大家请教下。 目前手头有一混合物,其中部分组分分子式和分子量(小数点后四位)相同,结构上存在基团位置异构或双键位置异构。如:总共有15种组分,其中有3种组分为分子式1,2种组分为分子式2,2种组分为分子式3,3种组分为分子式4,2种组分为分子式5,其余3种均不相同,采用C18柱分离获得8个色谱峰,大部分峰分离度大于1.0,[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url](低分辨质谱)结果显示8峰中各峰分子量与理论分析所得化合物分子量基本一致,其中分子量相同的峰未实现分离,但其理论结构存在基团位置异构或双键异构等现象。更换C30后增加为9个峰,个别峰分离度增大,但同分子量峰仍未实现分离。 针对以上情况,需尽可能提高各峰分离度和增加峰分离个数(针对同分异构体)以确定每批物质种类分布一致,请问可以采用哪些途径去进行分离方法考察? 目前调研到C18-PFP柱和多孔石墨碳可能对这类型结构有一定改善,但因此2种色谱柱均不提供试用,暂无法确定其分离情况;针对流动相,拟对色谱柱进行初筛后进行考察。请问大家是否遇到过类似情况或对此类情况有建议解决措施,望不吝赐教,万分感谢!
最近看了一篇文献Graphene oxide and reduced graphene oxide as novel stationary phases via electrostatic assembly for open-tubular capillary electrochromatography(Electrophoresis2013,34,1869–18760)文中以氧化石墨烯为电色谱固定相来分离邻、间、对硝基苯酚,其pKa分别为8.39, 7.15, 和7.22 文中选择pH7.0的磷酸缓冲液为流动相,说是可以得到基线分离。但是,pH7.0下间硝基苯酚(7.15)和对硝基苯酚(7.22)都是以负离子和中性分子两种形式存在,邻硝基苯酚以分子形式存在,最后得到的邻硝基苯酚的峰中会不会掺杂有间硝基苯酚和对硝基苯酚的分子形式??? 这和氧化石墨烯有关吗? 氧化石墨烯在试验中的作用?对硝基苯酚的三种位置异构体的作用大小不一样吗? 谢谢各位
最近在做醛酮化合物,质谱出峰很难分离,怀疑有同分异构体。应该怎么分离
同分异构体分离,求助。。??水:甲醇=35:65等度分离,同分异构体分离效果一般,请大虾帮助,如何分离效果更好一些?跑梯度请给出条件,谢谢??
TDI样品,分离异构体,按照国标进行,分离不好,在这基础之上调整流量和温度,达不到要求的效果。还有什么办法吗
水:甲醇=35:65等度分离,同分异构体分离效果一般,请大虾帮助,如何分离效果更好一些?跑梯度请给出条件,谢谢??
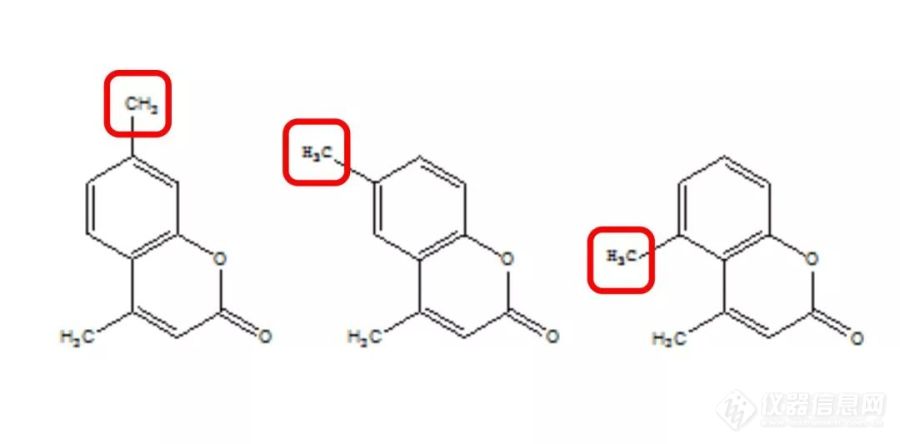
异构体是结构上彼此相似的化合物,这类化合物趋于拥有近似的K值,对于色谱分离来说,是一个非常具有挑战性的工作。特别是苯环上的间位和对位异构体的分离。常规分析我们会选择一些空间作用力的色谱柱来进行尝试,比如UltimateXS-C18、UltimatePFP、UltimatePAH以及UltimateXB-C30、来进行分离。如果这些色谱柱经过尝试均达不到分离要求时,不妨试试手性柱。月旭科技的Ultimate系列Cellu-D、Cellu-J、Amy-D和Amy-S四款手性柱,这里列举其中一款UltimateCellu-D分离异构体的案例:[b]1、邻、间、对位异构体分离结构式:[/b][align=center][b][img=,690,340]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091350181142_3359_932_3.jpg!w690x340.jpg[/img][/b][/align][b]色谱条件:[/b]流动相:正己烷:异丙醇=95:5检测波长:210nm;柱温:25℃流速:1.0ml/min[align=center][img=,600,289]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091352566692_7963_932_3.png!w626x302.jpg[/img][/align][b]2、邻、对位异构体的分离结构式:[/b][align=center][img=,600,413]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091353228860_4144_932_3.jpg!w690x476.jpg[/img][/align][b]色谱条件:[/b]流动相:甲醇检测波长:210nm;柱温:30℃流速:0.8ml/min[align=center][img=,600,316]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091353429412_7932_932_3.jpg!w690x364.jpg[/img][/align][b] 3、不同基团异构体的分离结构式:[/b][align=center][img=,600,326]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091354094367_1575_932_3.jpg!w690x375.jpg[/img][/align][align=center][/align][b]色谱条件:[/b]流动相:甲醇检测波长:210nm;柱温:30℃流速:0.8ml/min[align=center][b][img=,600,317]https://ng1.17img.cn/bbsfiles/images/2019/09/201909091355362882_3559_932_3.jpg!w690x365.jpg[/img][/b][/align][b]结论:[/b]在异构体分离的方法尝试过程中,当现有色谱柱均无法达到良好分离的情况下,不妨试试您手头上的手性柱。如果您有异构体分离的问题,可以关注月旭科技公众号,点击[b]“技术支持”[/b],在线咨询月旭工程师。[b]2、邻、对位异构体的分离结构式:[/b]
分离结构异构体,最适当的选择是( A )。A、吸附色谱 B、反相离子对色谱 C、亲和色谱 D、空间排阻色谱这题的答案为什么选择A啊
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=71348]应用自动内循环技术分离异构体[/url]应用自动内循环技术分离异构体旋光异构体药物在全世界50中主要药物中占了50%。对旋光异构体的分离一直是液相色谱分离中的一个难点。本文描述了应吉尔森制备色谱系统结合内循环分离技术对旋光异构体的分离。
[color=#444444]本人正在用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]器分析混合物质,混合物中有三对同分异构体,改变程序升温的条件,分离有所改善,但是三个同分异构体之间的分离度达不到1.5以上,请问该怎么做呢。谢谢![/color]
有谁做过酮类物质同分异构体的分离?想请教一下,谢谢!
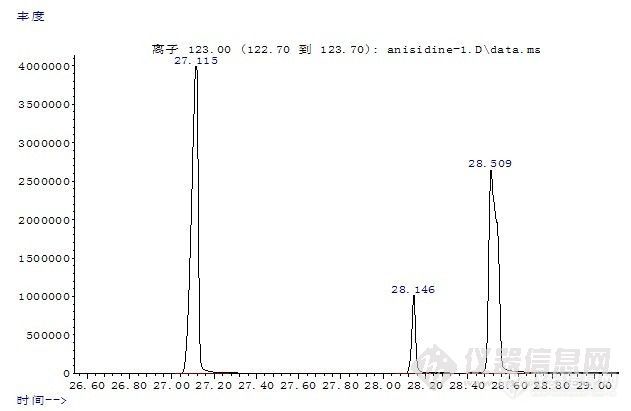
邻氨基苯甲醚同分异构体的分离摘要:为了实现邻氨基苯甲醚同分异构体的完全分离,作者采用气相色谱-质谱联用方法,通过改进色谱条件,使其取得了完全分离。试验表明采用气-质联用方法可以实现邻氨基苯甲醚同分异构体的完全分离。关键词:邻氨基苯甲醚;分离;异构体The Separation of O-Anisidine and Its isomersAbstract: In order to achieve the complete separation of o-anisidine and its isomers, the authors used gas chromatography - mass spectrometry methods, by improving the chromatographic conditions, so as to achieve their complete separation. The results showed that the gas-chromatography-mass spectrometry method can achieve the complete separationof o-anisidine and its isomers. Keywords: o-Anisidine; separation; isomers 1 前言采用气相色谱-质谱联用方法检测染料产品中23种有害芳香胺含量,按照现行国家标准GB/T17592-2006《纺织品禁用偶氮染料的测定》中提供的色谱条件,不但检测时间很长,而且大多数同分异构体保留时间相同或非常接近,同时这些异构体的质谱图又非常相似,从而造成无法使用特征离子对其进行定性和定量。如采用其它分析手段共同鉴别,如薄层色谱、液相色谱等,需要重新寻找条件,而且更换仪器费时费力,且多数实验室不一定同时具备这些设备。作者对芳香胺邻氨基苯甲醚及其异构体分离的问题进行了研究,其中,邻氨基苯甲醚属于有害芳香胺,而其同分异构体不属于有害芳香胺。作者通过改进色谱条件,使以上化合物达到很好的分离,提高了检测效率,减少了检测过程中的假阳性检出。2 试验2.1 仪器与试剂气相色谱-质谱联用仪(GC-MS):Agilent 7890A/5975C,美国Agilent公司毛细管柱:DB-17MS柱(30m×0.25mm×0.25μm)乙醚、硫酸亚铁等以上试剂均为分析纯;甲醇 色谱纯 美国Fisher公司旋转蒸发仪 上海亚荣生化仪器厂邻氨基苯甲醚及其同分异构体均为德国Dr.Ehrenstorfer公司。2.2 仪器操作条件色谱柱:DB一17MS 30m×0.25mm×0.25μm;温度:进样口220℃ ;辅助器280℃;离子源230℃ ;四极杆温度:150℃;柱温:40℃保持2分钟,以15℃/分钟升温至85℃ ,保持20分钟,再以30℃/分钟升至280℃,保持0分钟;载气:He;流速:1.0ml/分钟;离子化方式:EI;质量扫描范围:35—350;进样方式:不分流进样;进样0.2μL。2.3 执行标准试样处理按国标GB/T17592-2006执行。3 结果与讨论http://ng1.17img.cn/bbsfiles/images/2010/11/201011021932_256750_1604317_3.jpg图1 邻(间、对)氨基苯甲醚总离子流图由图1可以看出,邻氨基苯甲醚及其异构体在本实验条件下,可以得到很好的基线分离。保留时间分别为:邻氨基苯甲醚(27.115分钟);间氨基苯甲醚(28.509分钟);对氨基苯甲醚(28.146分钟)。在对染料产品中23种有害芳香胺含量的测定过程中,由于异构体的存在,并且多数异构体的质谱图很相似,如果保留时间相同,往往会形成假阳性结果的产生。当前针对有害芳香胺的气相色谱/质谱检测方法,大多采用非极性或极性较弱的色谱柱,如HP-5MS,DB-5MS,DB-35MS,这些色谱柱普遍存在的缺点是对常见的芳香胺异构体不能很好的分离。本方法通过使用中等极性色谱柱DB-17MS(固定相等同于50%苯甲基聚硅氧烷),同时使用三阶程序升温,很好的解决了这个问题。通过上面的数据与国标GB/T17592-
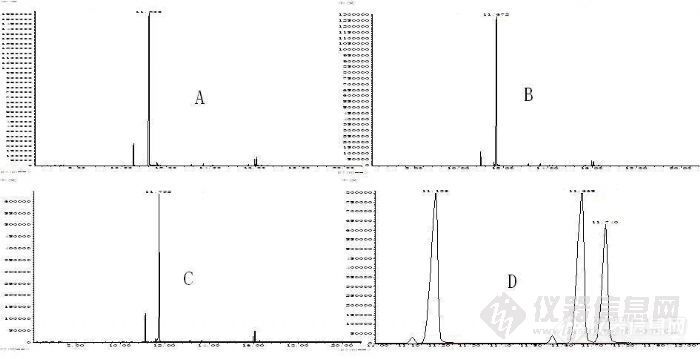
邻甲苯胺及其同分异构体的分离The Separation of O-Toluidine and Its isomers摘要:为了实现邻甲苯胺及其同分异构体的完全分离,首先,作者将邻甲苯胺及其同分异构体乙酰化,然后采用气相色谱-质谱联用方法,通过改进色谱条件,使其取得了完全分离。试验表明采用气-质联用方法可以实现邻甲苯胺及其同分异构体的完全分离。关键词:邻甲苯胺;分离;异构体;乙酰化Abstract: In order to achieve the complete separation of o-toluidine and its isomers, firstly, o-toluidine and its isomers were acetylation, and then the authors used gas chromatography-mass spectrometry methods, by improving the chromatographic conditions, so as to achieve their completely separation. The results showed that the gas-chromatography-mass spectrometry method can achieve the completely separation of o-toluidine and its isomers.Keywords: o-toluidine; separation; isomers; acetylation1 前言在禁用偶氮染料检测过程中,邻甲苯胺是经常被检出者之一。邻甲苯胺有两个同分异构体,分别是间甲苯胺和对甲苯胺。其中,邻甲苯胺属于禁用芳香胺,而间甲苯胺和对甲苯胺则不属于禁用芳香胺。三个化合物的沸点非常接近,分别为:邻甲苯胺(200±2℃)、间甲苯胺(203±3℃)、对甲苯胺(201±1℃)。而且三者的质谱图很相似,只是分子极性上略有差别,故造成在用气相色谱-质谱联用方法检测到邻甲苯胺时经常出现假阳性结果。如不采用薄层色谱、液相色谱等其它分析手段共同鉴别,是无法判断是否假阳性结果的。但是要排除假阳性结果,就需要重新寻找条件,而且更换仪器费时费力,且多数实验室不一定同时具备这些设备,这就给我们的日常检测工作带来了很多的麻烦和不便。本文作者结合自身知识和经验,对常见的邻甲苯胺及其异构体分离问题进行了研究。通过查阅相关资料,作者发现邻甲基乙酰苯胺(296℃)、间甲基乙酰苯胺(303℃)和对甲基乙酰苯胺(307℃)三者的沸点相差较大,所以作者首先通过试验将邻甲苯胺及其异构体分别乙酰化,然后通过改进色谱条件,使以上化合物达到了完全分离,提高了检测效率,减少了检测过程中的假阳性检出。 2 试验2.1 仪器与试剂气相色谱-质谱联用仪(GC-MS):Agilent 7890A/5975C,美国Agilent公司毛细管柱:DB-17MS柱(30m×0.25mm×0.25μm)叔丁基甲醚、乙酸酐、无水碳酸钠和无水碳酸钾均为分析纯 旋转蒸发仪 上海亚荣生化仪器厂邻甲苯胺及其同分异构体均为德国Dr.Ehrenstorfer公司。2.2 试剂配制标准品溶液:用叔丁基甲醚为溶剂,分别称取适量邻甲苯胺、间甲苯胺和对甲苯胺标准品配成合适浓度的单标溶液及混合溶液。碳酸钾溶液:0.1mol.L-1水溶液,取13.8g[font
我现在在做邻氟苯甲酸的液相检测,可是做了很多尝试都无法分离出邻、间、对位,他们始终都是一个峰,像这种高效液相检测中分离同分异构体的检测有哪位老师做过,请指教一下!
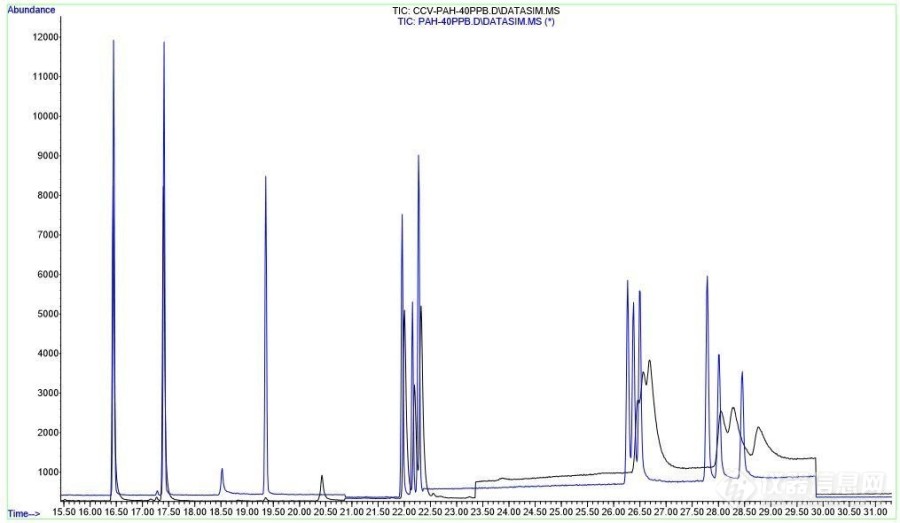
最近实验室测试多环芳烃PAH项目,遇到一个非常规的异常:后出峰的几种同分异构体(BbF,BjF,BkF等,见下图红色圈)突然无法分离,有做进样系统的维护(进样口,衬管,分流平板,柱子切割)以及MS的维护(离子源,EM,HED清洗),故障依旧。补充说明:1. MS调谐结果OK,更换新的色谱柱后,同分异构体分离正常,但维持几天后,分离变差直至无法分离,2. 分离变差的色谱柱更换到另一台仪器测试,同分异构体谱图分离正常(由此基本可排除柱子受污染的可能),3. 有检查柱箱升温正常,4. 方法参数未变。[img=,690,400]https://ng1.17img.cn/bbsfiles/images/2021/01/202101041914116980_2549_3151876_3.jpg!w690x400.jpg[/img]
C18的柱子可以分离脂溶性维生素类的顺反异构体吗
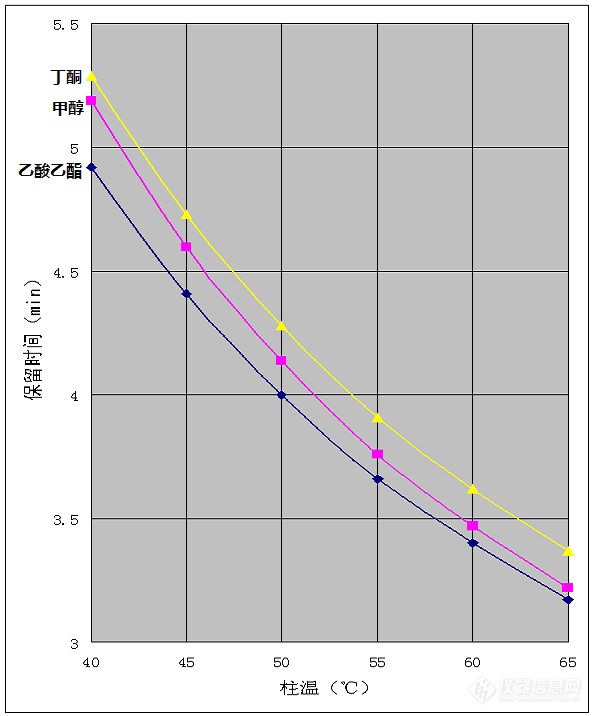
溶剂残留分析是[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]的重要应用之一,在药品、食品、包装等领域都是必测的项目。常见溶剂中涉及到的检测目标物经常有乙酸乙酯、甲醇、丁酮,以及二甲苯异构体这几项。最近看到 @m3091333、@p3109800、@Insm_c1196d2b 等多人发帖子讨论相关问题,我从原理上进行了一些解释,但终究纸上谈兵,于是找别的实验室要了这几种试剂,用实践检验了一下。首先,如果二甲苯异构体不要求分离,用624柱可以很容易的解决问题,这里就不讨论了。如果要求乙苯、对二甲苯、间二甲苯、邻二甲苯四种异构体分离,用624柱是无法完成的。因为二甲苯异构体色散力差异非常小,只能靠诱导力的差异分离,不同异构体在强极性柱上的极化率不同,乙苯极化率最低,其次是对二甲苯、间二甲苯,邻二甲苯极化率最大,出峰时间也随极化率的增加而延长。而624柱的极性比较弱,不能产生足够的极化作用,特别是对二甲苯与间二甲苯的极化差异非常小,无法实现分离。这个问题是由分子结构决定的,无论怎么调节色谱条件都不能解决。要想解决只能换强极性柱,常见的就是聚乙二醇柱,包括各种wax柱和FFAP柱等。三氟丙基柱也是强极性的,可以分离二甲苯异构体,但是这种柱很少使用。在聚乙二醇类的色谱柱上,乙酸乙酯、甲醇、丁酮三种目标物分离困难,各种类型的聚乙二醇柱选择性略有差异,但这三种物质都是较为接近的,想要分离是不太容易的。但是这三种物质与聚乙二醇固定相之间的作用力存在本质上的差异,因此通过调整柱温条件是可以分离的。下面三幅图是用60米*0.53mm*1um的INNOWAX柱分离乙酸乙酯、甲醇、丁酮的效果,柱温分别是40℃、50℃、60℃。[img=,690,796]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022157168864_5041_2204387_3.png!w690x796.jpg[/img][img=,690,796]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022157170984_7926_2204387_3.png!w690x796.jpg[/img][img=,690,796]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022157172914_736_2204387_3.png!w690x796.jpg[/img]图中很明显,柱温低时甲醇与丁酮出峰时间接近分不开,高温时甲醇与乙酸乙酯出峰时间接近分不开,温度适中时三者可以实现分离。虽然未达到基线分离,但分离度都超过1,用来定量是完全可以的。这是找别人借的一根旧柱子,柱效只有4万塔板,如果是新柱子柱效应该能达到七八万塔板,分离度肯定更高,如果是0.32mm口径的柱子分离就更没问题了。要强调的是,能够实现分离的条件并不是完全靠盲目尝试获得的。我们看一看三种目标物的保留时间随柱温的变化就能发现其中的规律,见下图:[img=,594,716]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022156374904_6999_2204387_3.png!w594x716.jpg[/img]图中可以看出,三种目标物的保留时间都是随温度升高而减小的,但是减小的幅度却并不相同。甲醇的保留时间随温度升高而减小的幅度明显大一些。这是因为甲醇具有羟基,与聚乙二醇固定相的相互作用力以氢键为主,氢键的强度随温度升高而迅速减弱。而乙酸乙酯、丁酮与聚乙二醇固定相的作用力都是以诱导力和取向力为主,这种力是由分子偶极矩决定的,受温度的影响要小一些。甲醇峰位置在乙酸乙酯与丁酮之间,温度升高时保留时间都减小,但甲醇减小更多,于是甲醇与乙酸乙酯靠的更近,与丁酮的分离度提高。温度降低时保留时间都增大,但甲醇增大更多,于是甲醇与丁酮靠的更近,与乙酸乙酯的分离度提高。用其他的柱子,如DB-wax或者FFAP时,各组分之间的相对位置会有差别,甚至有时出峰顺序都会变,但是保留时间随温度变化的这种规律仍然是适用的。所以遇到分不开的情况,一定不要盲目的乱试一通,也不用盲目的换柱子,一定要把问题想明白,有针对性的优化条件。最后要强调的是,这里虽然是以溶剂检测为例讨论了如何只用一根柱子就实现分离,但实际样品很复杂,并不是每次都能通过这种优化实现全部分离目的。所以色谱实验室配备多种不同极性的色谱柱是非常重要的。特别是做复杂样品时,即使谱图上看起来分离不错,最好也能用另外一种柱子进行一次验证,以免实际样品中有干扰物共流出,造成假阳性。
RT,似乎听说LC可以分离同分异构体,但昨天听到一个讲座说两个同分异构体是一个峰,有些糊涂了,请教各位大侠! 谢谢!
[size=3][b]DAD检测器可以分离手性异构体吗[/b][/size]最近做一个化学药,发现其有手性异构体,老板要求检测是否存在,又不给专门买手性柱。原来都是用DAD检测器判断峰的纯度,不知道能不能分辨出手性异构体?如果不行,还有什么其他的方法吗?
我做单糖的分析,所用标样是右旋的,这影响我分析吗,另同分异构体之间分离的相互干扰大不大?
蛋白质的翻译后修饰常常会影响蛋白质的结构和功能,反映在生物制药工业上,会对药品的安全性和有效性产生重大影响。翻译后修饰常常表现为电荷变异体,因此电荷异构体的分析成为了质量控制的一个关键项。目前常见的电荷异构体分析方法为IEF/cIEF或iCIEF,可以鉴别生物药,对生物药的纯度进行分析,测定电荷异构体的等电点以及各种异构体的分布。但是,等电聚焦或者毛细管等电聚焦存在很多短板,最明显的就是无法大规模制备异构体。美国基因泰克公司的科学家曾经用一种叫做自由流电泳的工具,高分辨率高通量大规模对单抗的电荷异构体进行分离制备,并结合各种分析手段,对每一个异构体进行了深度表征。现分享论文如下,欢迎大家讨论!
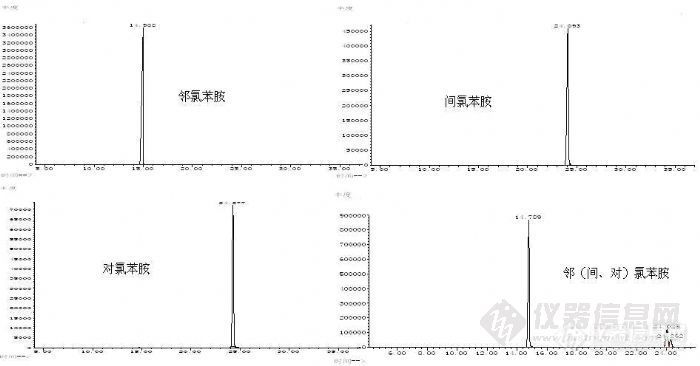
对氯苯胺及其同分异构体的分离对氯苯胺(106-47-8)为禁用芳香胺,而它的两种同分异构体间氯苯胺(108-42-9)、邻氯苯胺(91-51-2)则不是禁用芳香胺。如果仅仅靠GC-MSD无法确认该样品是否使用禁用偶氮染料,遇到这种情况时GB/T17592-2006推荐使用其他色谱手段对样品进行定性分析。如薄层色谱、液相色谱等,但这需要重新寻找条件,而且更换仪器费时费力,且多数实验室不一定同时具备这些设备。作者利用气相色谱-质谱联用方法(GC-MSD)对常见的对氯苯胺及其异构体分离进行了研究,通过改进色谱条件,使以上化合物达到很好的分离,减少了检测过程中的假阳性检出。1 实验部分4.3.1.1 仪器与试剂气相色谱-质谱联用仪(GC-MS):Agilent 7890A/5975C,美国Agilent公司毛细管柱:DB-17MS柱(30m×0.25mm×0.25μm)甲醇 色谱纯 美国Fisher公司旋转蒸发仪 上海亚荣生化仪器厂对氯苯胺及其同分异构体均为德国Dr.Ehrenstorfer公司。4.3.1.2 试剂配制用色谱纯级甲醇为溶剂,分别称取适量对氯苯胺、邻氯苯胺和间氯苯胺标准品配成合适浓度的混合溶液。4.3.1.3 仪器操作条件色谱柱:DB-17MS 30m×0.25mm×0.25μm;温度:进样口220℃ ;辅助器280℃;离子源230℃ ;四极杆温度:150℃;柱温:40℃保持2分钟,以20℃/分钟升温至100℃ ,保持25分钟,再以40℃/分钟升至280℃,保持0分钟;载气:He;流速:1.0mL/分钟;离子化方式:EI;质量扫描范围:35-350amu;进样方式:不分流进样;进样0.2μL。2 结果与讨论2.1 试验结果http://ng1.17img.cn/bbsfiles/images/2011/10/201110011241_320594_1606903_3.jpg虽然对氯苯胺及其异构体质谱图非常相似,但是由图4.3可以看出,在本实验条件下,对氯苯胺及其异构体无论是单标还是混标都实现了很好的分离。单标保留时间分别为:邻氯苯胺(14.988min);间氯苯胺(24.097min);对氯苯胺(24.277min)。混标保留时间分别为:邻氯苯胺(14.789min);间氯苯胺(24.029min);对氯苯胺(24.262min)。在混标样品中间氯苯胺和对氯苯胺虽然有部分峰是重叠的,未实现两者的基线分离,但是两者保留时间相差0.233min,基本上达到了有效分离,可以满足检测的要求。此外,如果样品遇到间氯苯胺和对氯苯胺异构体无法确认的时候,可以利用本文试验条件,通过向样品中加入一定量的间氯苯胺或对氯苯胺,观察样品加标前后哪个峰的面积显著增大,从而进一步确定该样品是否
想用YMC的C18AQ亲水柱梯度分离同分异构体Isobutyryl-CoA和Butyryl-CoA,流动相A是20mM 乙酸铵,0.3%乙酸的水,B是纯ACN含0.5%乙酸,但是梯度洗脱始终无法分开,请问达人有何改进方法能分开这两物质。
各位版友,小弟我最近在开发一个拥有4个手性中心的化合物的HPLC,目前已经购买了这个化合物的5个杂质对照品了,其中一个杂质是对映异构体,准备买大赛璐的手性柱进行分离,其他4个杂质均为非对映异构体,目前分别采用了0.1%的三氟乙酸作为流动相与乙腈梯度洗脱,5mM磷酸二氢钾(PH7.0)/(PH2.5)与乙腈梯度洗脱,采用前一个流动相峰宽有点宽,后一个流动相峰形很好,但是无法分开,想请教有分离非对映异构体的版友们支招啊!兄弟我不甚感激!
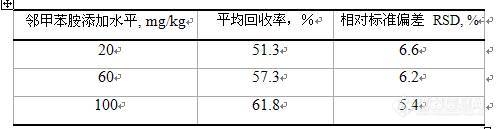
看见同行(看着这话题,绝对是同行,多交流)发着文章http://bbs.instrument.com.cn/shtml/20101012/2857370/,我这把手上的东西整整,算是补充吧。大家多多提意见吧!摘要 针对纺织品偶氮染料检验中常检出的禁用邻甲苯胺及其异构体,结合气相色谱-质谱和高效液相色谱-二极管阵列检测器(HPLC/DAD),摸索了以气相色谱-质谱进行初期定性筛选、以高效液相色谱进行确证和定量的芳香胺异构体检测方法,避免了检验中其异构体造成的假阳性检出。本方法在2 μg/mL~100 μg/mL浓度范围内线性关系良好,线性相关系数可达到0.9999;回收率为51%~62%。关键词 纺织品;检测;禁用邻甲苯胺;异构体1 前言采用气相色谱-质谱联用方法检测染料产品中24种有害芳香胺含量,按照现行国家标准中提供的气相色谱条件,会有多种异构体保留时间相同或非常接近,而且这些异构体的质谱图又非常相似,从而造成无法使用特征离子对其进行定性和定量,往往会形成假阳性结果的产生。当前针对有害芳香胺的气相色谱/质谱检测方法,大都采用非极性或极性较弱的色谱柱,如HP-5MS、DB-5MS、DB-35MS,这些色谱柱普遍存在的缺点是对常见的异构体不能很好的分离。有文献报道采用中等极性色谱柱DB - 17MS(固定相等同于50%苯甲基聚硅氧烷),对芳香胺异构体有一定的分离能力,但没能实现禁用芳香胺的基线分离,造成定量上的偏差。高效液相色谱法(HPLC)可同时测定多种芳香胺,在分离异构体上是强有力的确证方法,准确定性和定量,分析方法易于推广。本方法采用气相色谱-质谱联用对异构体进行初期定性筛选、以高效液相色谱进行确证并外标定量,对常检出的的禁用邻甲苯胺及其异构体检测进行了研究。本方法通过进一步摸索优化高效液相色谱条件,使邻甲苯胺及其异构体达到基线分离,有效避免了检测过程中的假阳性检出。2 实验材料与方法2.1 仪器和设备气相色谱/质谱联用仪:美国Agilent 公司7890A /5975 C,带自动进样器,四极杆质谱检测器;气相色谱柱:HP-5MS 5% Phenyl Methyl Silox,325 °C:30 m x 250 μ[size=
请问各位HPLC能分离番茄红素的异构体么?如果能的话,操作条件是什么?有适合的文献参考一下么。谢谢大家。