如何用普通生物显微镜拍清楚非小细胞肺癌细胞的细胞膜呢
我想用液相色谱法测定红细胞膜脂肪酸,想请教一下样品前期怎么处理?哪位高手可以提供具体的步骤,感激不尽!
将在药物开发进程中发挥重要作用2011年03月26日 来源: 科技日报 作者: 常丽君 本报讯 据每日科学网近日报道,美国范德堡大学研究人员开发出一种新型激光技术,可检测细胞膜上的蛋白质和其它多种生物分子之间的相互反应。这种检测将在药物开发进程中发挥重要作用。 人类细胞中约有7000种蛋白质,其中30%在细胞膜上,控制细胞分子运作机制的信号有60%—70%由这些膜蛋白产生,因此当前市场上约一半的药物都是瞄准细胞膜蛋白。但因为膜蛋白很难提纯,科学家在研究它们的结构时面临很多困难。现有的检测膜手段大多是将膜蛋白从其所处环境中分离,或用不同方式如荧光标签加以修改,以分析它们的活性。这些方法不仅昂贵耗时,还可能会影响目标膜蛋白的功能。 范德堡大学化学生物研究院化学教授达里尔·波恩霍普领导的研究小组和斯克里普斯研究院合作,开发了一种名为“后向散射干涉仪”(BSI)的新型激光技术,能精确检测出膜蛋白和自然界中各种分子之间的结合力。 BSI操作起来很简单,只要把两种分子混合装入一个充满液体的显微镜小盒中,用一束类似于条形码扫描仪的红色激光照射,就能测出它们之间的结合力。小盒的几何形状调整合适后,激光就会产生干涉图案,而这种干涉图案对分子之间的反应非常敏感。如果分子开始互相作用,图案就开始变换。 为了检验BSI的准确性,研究人员制造了一种含有GM1小蛋白质的合成膜,霍乱毒素要进入细胞,主要结合对象就是这种小蛋白质。他们把霍乱毒素B和这些膜混合,检测出的结合力结果与用其他方法所得到的结果一致。为了进一步确认,他们还用了一种和胸腺癌相关的天然分离膜和3种分别与疼痛、发炎和神经传导素GABA(用于放松、睡眠和调节紧张)相关的蛋白质膜进行检验,把包含这些蛋白质的膜和对应结合分子相混合,用BSI技术测得的值也和用其他方法得到的结果一样。 此外,该技术进入商业化也前景广阔,范德堡大学对新型激光检测技术已申请了专利,并已获得3项批准。他们还专门成立了一家分子传感公司对新技术进行独家开发。
【序号】:1【作者】:马宏1邢飞1项舟【题名】:干细胞膜片在骨与软骨修复中的应用【期刊】:华西医学. 【年、卷、期、起止页码】:2023,38(10)【全文链接】:https://kns.cnki.net/kcms2/article/abstract?v=Eo9-C_M6tLk9uZm4IkSK1syfkr0KDbFTcR0617hZuaOO2RfuHSxVbqaoIynt7ZcTvLJt5-3SIRpa86mQX1e7IjPPmI8GtcsVZ8ywUEJunoyVxXNl-EZ7vjp8_-Gb8KPo9lovkvfL5A4=&uniplatform=NZKPT&language=CHS
细胞膜脂肪酸甲酯化要用什么作反应容器?反应液大概1.5ml,看了文献说用反应样品瓶,具体是什么容器?[img]https://ng1.17img.cn/bbsfiles/images/2019/03/201903282206509758_5524_3499435_3.png[/img]
细胞膜脂肪酸甲酯化要用什么反应容器?反应液大概有1.5ml,有文献说用反应样品瓶,具体是指什么容器?[img]https://ng1.17img.cn/bbsfiles/images/2019/03/201903291023427595_5464_3499435_3.png[/img]
测红细胞膜表面DHA DHA的分离度不是很好 怎么解决?
请问有没有人做过红细胞膜脂肪酸的检测啊?例如检测其中反式脂肪酸,用什么方法比较好?可以用液相色谱么?
用[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用仪[/color][/url]测红细胞膜脂肪酸,参考文献里有20种脂肪酸,我只测出了7种脂肪酸,是不是甲酯化方法不好?我用的甲酯化方法是:取分离好的红细胞样本各50μL,依次加入已用BHT乙醇溶液抗氧化处理过的具塞玻璃试管中;在具塞玻璃试管中加入400μL3N盐酸-甲醇溶液,充分混匀3分钟,然后放置于90℃烘箱中避光反应3小时,反应完毕后取出冷却至室温;加入正己烷800μL到具塞玻璃试管中,充分混匀5分钟,4000rpm/min,2-8℃离心5min;将离心后的上层正己烷溶液尽量完全转移至另一个1.5ml离心管中,室温环境下,用氮气吹干仪吹干;在氮气吹干后的离心管中加入正己烷400μL溶解脂肪酸甲酯产物,充分混匀3分钟,然后转移100μL至样品瓶中,待测。
美国科学家彼得阿格雷博士因找到了允许水分子出入的细胞膜蛋白“水通道”,而荣获2003年度诺贝尔化学奖,但该通道的具体工作机制却一直是未解之谜。记者近日从中科院上海应用物理研究所获悉,我国科学家在此基础上续写下文,发现这种纳米级水通道上具有两把“锁”,分别通过力学和电学开关机制控制着水分子进出。该研究成果已发表在国际权威学刊《美国科学院院刊》(PNAS)在线版上。 在生物体内,蛋白水通道和周围的水溶液中都存在电荷。在纳米和分子尺度上,这些通道因为热噪音效应引起力学形变和电荷移位,这会否影响水通道的开或关?上海应用物理所方海平课题组与浙大、浙江师大、IBM公司研究所和哥伦比亚大学科研人员合作,采用纳米级“碳管”作为生物膜蛋白水通道的简化模型开展研究,结果发现,水分子在通过水通道时,不仅对作用在水通道管壁上的力学响应具有开关特性,对管壁上的电荷响应也有极好的开关特性。研究表明:有效力学信号会导致管壁产生足够大的形变,由此带来开或关的状态变化;而只有在水分子与外界电荷的作用距离非常接近时,通道才会响应,迅速开或关。 专家认为,这一新发现的机制不仅对生物化学有意义,对设计人工分子机器也具有一定启示性。来源:解放网-解放日报
[align=left][font='times new roman'][size=16px]动植物膜脂和膜蛋白提取方法[/size][/font][/align][align=left][font='times new roman'][size=16px]大豆卵磷脂和肺腺癌细胞膜脂提取物的制备[/size][/font][/align]对于大豆卵磷脂样品,首先去除胶囊,将100 mg大豆卵磷脂样品用10 mL正己烷/异丙醇(1:1,v/v)稀释溶解,样品在4℃下超声10 min,样品再经0.45 μm微孔膜过滤,以备后续使用。肺腺癌细胞膜脂的提取方法参照Folch法。首先裂解肺腺癌细胞,向细胞液中加入18 mL已经配好的氯仿-甲醇(2:1,v/v)混合溶剂,摇匀后置于高速低温离心机4℃,3000 r/min离心10 min(摇匀过程中时刻注意溶液的温度,尽量避免温度过高)。然后向该体系中加入约2 mL的超纯水,摇匀后离心。上清液移除后用少量的甲醇-水(1:1,v/v)小心清洗上表面,得到肺腺癌磷脂提取物,过0.45 μm滤膜后,N[font='times new roman'][sub][size=16px]2[/size][/sub][/font]吹干,备用。冰箱-20℃保存,临用时现配溶液。[align=left][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]肝脏膜蛋白质的制备[/size][/font][/align]参考试剂盒提取小鼠肝脏膜蛋白质的步骤如下:,试剂准备和组织预处理:取148 mg小鼠肝脏组织,用手术剪刀剪碎,移入4 mL离心管中,加入1 mL的膜蛋白提取剂A,冰浴15 min,之后将离心管中液体移入冰浴预冷玻璃匀浆器中,匀浆70次。去除未破碎的细胞:在4℃下将样品于900 g离心10 min,为了确保上清液的纯度应尽量避免接触沉淀。收集肝脏浆蛋白和细胞膜碎片:将上清液继续在4℃下1400 g离心40 min,获得细胞膜碎片。上清液(肝脏浆蛋白)应置于-70℃下保存备用。提取肝脏膜蛋白质:尽量将上一步骤中上清液吸取干净,避免肝脏浆蛋白的干扰。加入300 μL膜蛋白提取剂B,高速涡旋10 s后立即进行冰浴10 min,重复上述步骤三次。随后立即4℃下14,000 g离心15 min,吸取上清肝脏膜蛋白溶液,-70℃下保存备用。
细胞是如何出口和嵌入蛋白于细胞膜Grenoble, 12 December 2010 How cells export and embed proteins in the membraneEMBL scientists first to visualise crucial stephttp://www.embl.de/aboutus/communication_outreach/media_relations/2010/101212_Grenoble/index.htmlLike an overprotective parent on the first day of school, a targeting factor sometimes needs a little push to let go of its cargo. Scientists at the European Molecular Biology Laboratory (EMBL) in Grenoble, France, have visualised one such hand-over. They were the first to determine the structure of a ribosome-protein complex involved in carrying nascent proteins out of the cell. Their work, published online today in Nature Structural and Molecular Biology, could increase understanding of illnesses such as cystic fibrosis and some forms of Parkinson’s disease, in which improper protein targeting leads proteins to harmfully accumulate inside cells.In most organisms, proteins destined to cross or be embedded in a membrane contain a polypeptide sequence that is recognized during translation by a targeting factor known as the signal recognition particle (SRP). SRP binds to the ribosome synthesizing the polypeptide, and subsequently also binds an SRP receptor, located next to the machinery that transfers proteins across the membrane and out of the cell. EMBL scientists have now generated the first-ever structural image of this important step in the process.“The SRP receptor acts as a switch between the cargo binding and the release,” says Christiane Schaffitzel, who led the research at EMBL, “Now we have seen for the first time how the release can happen at a molecular level.”Schaffitzel’s group is taking structural snapshots of entire pathways by which proteins are synthesized and targeted to their final positions. To capture this hand-over step, the scientists had to overcome the fact that the link between SRP and its receptor is usually transient, chemically unstable. They engineered the SRP receptor so that it would bind more stably to SRP, then introduced ribosomes and observed the resulting complexes using cryo-electron microscopy (cryo-EM).Cryo-EM can be performed in roughly physiological conditions, providing a picture that closely resembles what happens in living cells. This picture can then be combined with higher-resolution crystallography data and biochemical studies – an exciting hybrid approach the EMBL scientists will further exploit to follow protein targeting all the way from start to finish.A particular asset for success in this project was the close collaboration with Guy Schoehn at the Institut de Biologie Structurale (IBS). IBS and EMBL are part of the Partnership for Structural Biology (PShttp://i.0dxy.cn/images_new/smiles/smile_blackeye.gif in Grenoble, France.Source ArticleEstrozi, L.F., Boehringer, D., Shan, S., Ban, N., Schaffitzel, C.. Cryo-EM structure of the E. coli translating ribosome in complex with SRP and its receptor. Nature Structural and Molecular Biology, Advance Online Publication 12 December 2010. DOI: 10.1038/nsmb.1952.
科罗索酸产品名称: 科罗索酸 产品类别: 主打产品 产品用途: 用于减肥原料及治疗糖尿病 点击次数: 1249 发布时间: 2010-03-02 产品介绍 产品名称:科罗索酸别 名:2α-羟基熊果酸(2-alpha- hydroxyursolic acid)商品名称:植物胰岛素.提取物名:巴拉巴提取物、大花紫薇提取物 规格: 科罗索酸1% 科罗索酸2% 科罗索酸10% 科罗索酸20%-98% 科罗索酸标准品CAS 号:4547-24-4分子式及分子量:C30H48O4 结 构式: 来 源:大花紫薇(俗称巴拿巴,盛产于菲律宾群岛)的提取物。 科罗索酸(corosolic acid),又名2α-羟基熊果酸,是存在于大叶紫薇中的一种三萜化合物。近年来研究发现其具有降血糖、减肥、抗肿瘤、抗炎、抗病毒和抗心血管疾病作用,尤其是其较好的降血糖活性,具有类似胰岛素的生理作用,被称为“植物胰岛素”,受到人们广泛关注,目前在国内外已被开发出多种保健品。为更好地开发利用科罗索酸,下面就科罗索酸降血糖活性进行相关介绍。 1 科罗索酸的理化性质科罗索酸为白色无定型粉末(甲醇),可溶于石油醚、苯、氯仿、吡啶等有机溶剂,不溶于水,可溶于热乙醇、甲醇。在无水条件下,与强酸(硫酸、磷酸、高氯酸)、中强酸(三氯乙酸)或Lewis氏酸(氯化锌、三氯化铝、三氯化锑)作用,会出现颜色反应或萤光。科罗索酸属α-香树脂醇型或乌斯烷型五环三萜类化合物,其基本骨架为多氢蒎的五环母核。科罗索酸在植物体内可游离存在,也可以皂甙的形式存在。在植物体内,其常常与其同分异构体山楂酸(2α-羟基齐墩果酸)共同存在,结构和化学性质相似,分离较难。 2 降血糖作用的研究科罗索酸降血糖作用的研究源于对菲律宾、马来西亚等东南亚国家传统降血糖保健饮料原料大叶紫薇叶的研究。1940年,Garcia采用以1~2g大叶紫薇干叶/kg体重的剂量喂养普通家兔,发现每24h家兔的血糖水平平均下降16~49mg/L。1956年,Garcia又采用大叶紫薇叶提取物进行临床实验,发现其具有降低糖尿病病人血糖的效果。1993年,Murakami等从大叶紫薇的叶中分离出2种三萜酸科罗索酸和山楂酸,发现科罗索酸具有降血糖的效果。目前,对科罗索酸降血糖的作用,已从体外细胞实验、体内动物实验和临床实验等方面进行了系统的研究。 在体外实验中,1993年,Murakami等以肿瘤细胞进行体外培养,发现大叶紫薇提取物可刺激细胞膜的葡萄糖运输通道,增强细胞对葡萄糖的利用,进而降低血糖含量,此作用与胰岛素降糖作用机理相似。体内动物实验中,1999年,Hamamoto等制备了一种含1%(w/w)科罗索酸的大叶紫薇提取物胶囊,将其喂养小鼠,喂养后90min,小鼠的血糖水平比对照组明显下降。此外,在兔子体内也进行了科罗索酸降糖作用实验。对禁食24h正常的兔子喂食科罗索酸,考察喂食一段时间后血糖含量,结果表明,大剂量服用科罗索酸引起的血糖降低与服用两个单位的胰岛素相似。大剂量服用科罗索酸可以带来57mg/ml的血糖降低。正常兔子口服科罗索酸会带来16~49mg/ml的血糖降低。2个多小时后再次给药会使血糖保持在低水平上,甚至略微有所下降,此过程会保持5个多小时。大剂量服用克罗索酸会带来40~58mg/ml的血糖降低。血糖降低的峰值期出现在服药后2~4h,6~10h后血糖恢复到正常水平。血糖下降明显和科罗索酸摄入量有关。临床实验中,1999年Ikeda等采用含大叶紫薇提取物的胶囊对糖尿病病人进行临床实验,发现其具有治疗糖尿病的作用。William等将含1%(w/w)科罗索酸的大叶紫薇甲醇提取物制备为软胶囊和硬胶囊,对56名II型糖尿病人进行了临床观察,结果表明,每人每天供给剂量32mg和48mg的两组,两周后,他们的血糖水平有明显下降,服用软胶囊组的病人,其血糖水平平均下降30%,服用硬胶囊组的病人,其血糖水平平均下降20%,表明两种胶囊都具有降血糖的效果,且软胶囊的降糖效果优于硬胶囊。 科罗索酸还有减肥作用,临床研究发现服用该药后能够调节体内胰岛素和血糖含量,具有明显的的减肥趋势(月平均减重0.908-1.816Kg),该过程比较缓且无需节食。 目前该天然产物已在美国作为营养补充剂上市,同时进行治疗糖尿病的三期临床试验,近期将通过FDA认证。其用于治疗糖尿病的作用效果与注射胰岛素相比较,具有口服效果显著、毒副作用小、使用方便等优点,作用效果与注射胰岛素相当。 应用展望: 科罗索酸作为防治肥胖症和II型糖尿病植物新药和功能性天然保健食品医药原料,目前已经成为市场的热门产品,产品供不应求。但目前在提取、制备上还存在一定的问题,随着研究的不断深入,该产品将具有非常广阔的市场前景。
[align=center][font='times new roman'][size=16px]超速离心法[/size][/font][font='times new roman'][size=16px]富集[/size][/font][font='times new roman'][size=16px]细胞分泌的外[/size][/font][font='times new roman'][size=16px]泌[/size][/font][font='times new roman'][size=16px]体[/size][/font][/align][align=left][font='times new roman'][size=16px]引言[/size][/font][/align]本章利用超速离心法富集细胞分泌的外泌体。采用透射电子显微镜,Western Blot实验,纳米颗粒示踪分析等表征了外泌体的形态结构及分布特征。最后,用增殖实验和划痕实验测试了富集得到的外泌体的生物完整性[font='宋体']。[/font][align=left][font='times new roman'][size=16px]细胞分泌的[/size][/font][font='times new roman'][size=16px]外[/size][/font][font='times new roman'][size=16px]泌[/size][/font][font='times new roman'][size=16px]体表征[/size][/font][/align][img]" style="max-width: 100% max-height: 100% [/img]利用透射电子显微镜对超速离心法得到的外泌体进行了表征。如图(a)所示,洗脱后的外泌体具有典型的杯状结构。纳米颗粒示踪分析技术显示富集的外泌体粒径分布较窄,平均粒径为115.3 nm(图 b)。Western blot方法验证了富集方法的有效性。如图(c)所示,经超速离心法富集后,典型的低丰度外泌体标记物HSC70、TSG101、CD63和CD9可得到有效检测。以上结果证明,基于超速离心法对外泌体的富集可行性。[align=center][font='黑体'][size=14px]图[/size][/font][font='黑体'][size=14px] (a)重悬液中外[/size][/font][font='黑体'][size=14px]泌[/size][/font][font='黑体'][size=14px]体的透射电子显微镜表征,(b)[/size][/font][font='黑体'][size=14px]纳米颗粒示踪分析技术[/size][/font][font='黑体'][size=14px]表征外[/size][/font][font='黑体'][size=14px]泌[/size][/font][font='黑体'][size=14px]体的尺寸分布,(c)[/size][/font][font='黑体'][size=14px]Western blot方法[/size][/font][font='黑体'][size=14px]表征[/size][/font][font='黑体'][size=14px]外[/size][/font][font='黑体'][size=14px]泌[/size][/font][font='黑体'][size=14px]体标记物HSC70、TSG101、CD63和CD9[/size][/font][font='黑体'][size=14px]蛋白条带[/size][/font][/align][align=left][font='times new roman'][size=16px][color=#000000] [/color][/size][/font][font='times new roman'][size=16px][color=#000000] [/color][/size][/font][font='times new roman'][size=16px]完整性验证[/size][/font][/align][img]" style="max-width: 100% max-height: 100% [/img]首先用细胞增殖用于评估超速离心法分离的外泌体的生物完整性。不同浓度(10[font='times new roman'][sup][size=16px]6[/size][/sup][/font]、10[font='times new roman'][sup][size=16px]8[/size][/sup][/font]、10[font='times new roman'][sup][size=16px]10[/size][/sup][/font]颗粒/孔)的H1299细胞外泌体分别与H1299细胞共培养24、48和72小时。如图(a)所示,H1299细胞来源的外泌体以剂量依赖性方式显著促进细胞增殖。此外,伤口愈合实验显示,H1299细胞来源的外泌体加速了伤口愈合速度,并以剂量和时间依赖的方式提高了伤口愈合质量(图 b)。上述结果表明,通过超速离心法富集的外泌体具有完整性,可以促进细胞增殖、分化和迁移。[align=center][font='黑体'][size=14px]图[/size][/font][font='黑体'][size=14px](a)H[/size][/font][font='黑体'][size=14px]1299[/size][/font][font='黑体'][size=14px]细胞来源的外[/size][/font][font='黑体'][size=14px]泌[/size][/font][font='黑体'][size=14px]体对细胞增殖的影响结果,(b)[/size][/font][font='黑体'][size=14px]H1299细胞来源的外[/size][/font][font='黑体'][size=14px]泌[/size][/font][font='黑体'][size=14px]体对细胞[/size][/font][font='黑体'][size=14px]划后伤口愈合[/size][/font][font='黑体'][size=14px]的影响结果[/size][/font][/align][align=left][font='times new roman'][size=16px]小结[/size][/font][/align]本章利用超速离心法富集了细胞来源的外泌体,并对富集得到的外泌体进行了一系列表征表征。通过透射电子显微镜和纳米颗粒示踪分析技术分析表明得到的外泌体具有典型的杯状结构和小的粒径分布,证明了富集方法的可行性。Western Blot结果表明,富集后得到的外泌体溶液经裂解后,特征蛋白HSC70、CD63、TSG101和CD81,其含量比富集前显著提高。利用细胞增殖实验和划痕实验证明超速离心法富集得到的外泌体具有良好的生物学活性,可应用于下游的实验研究。
[font=宋体][font=宋体]无细胞蛋白表达系统([/font][font=Calibri]Cell-Free Protein Expression System[/font][font=宋体])是一种基于原核和真核细胞提取物构建的体外蛋白表达系统。它具有许多优点,例如可以在短时间内生产大量的蛋白质,同时避免了细胞内的复杂调控机制和翻译后修饰等繁琐过程。因此,无细胞蛋白表达系统在生物制药、生物材料、生物燃料等领域具有广泛的应用前景。本文将详细介绍无细胞蛋白表达系统的优缺点。[/font][/font][font=宋体][b]一、无细胞蛋白表达系统的优点[/b][/font][font=宋体] [/font][font=宋体][font=Calibri]1.[/font][font=宋体]高效性:无细胞蛋白表达系统具有高表达效率的优点,这是由于体外体系中不存在靶蛋白累积所需的细胞分裂和细胞复杂代谢反应。此外,由于无细胞蛋白表达系统不受到细胞毒性和免疫反应的限制,可以实现大规模的蛋白质表达。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2.[/font][font=宋体]灵活性:无细胞蛋白表达系统可以使用一系列不同的原核和真核细胞提取物作为反应体系,例如[/font][font=Calibri]E.coli[/font][font=宋体]、小麦胚芽和人类细胞等。这意味着可以根据不同的实验目的和需求进行合理的选择,以适应多样化的研究需要。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3.[/font][font=宋体]易操作性:无细胞蛋白表达系统非常容易操作。与传统的细胞表达系统相比,无细胞蛋白表达系统不需要细胞培养、生长和繁殖。此外,无细胞蛋白表达系统可以快速进行,通常只需要数小时至几天即可完成目标蛋白的表达。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]4.[/font][font=宋体]简单纯化:由于无细胞蛋白表达系统可以避免有机溶剂和离子交换剂等复杂的步骤,从而使目标蛋白的纯化工作更加简便和迅速。例如,可以使用亲和柱、凝胶过滤和电泳分析等方法来快速分离和纯化蛋白质。[/font][/font][font=宋体] [/font][font=宋体][b]二、无细胞蛋白表达系统的缺点[/b][/font][font=宋体] [/font][font=宋体][font=Calibri]1.[/font][font=宋体]成本较高:尽管无细胞蛋白表达系统可以大规模进行蛋白质表达,但是所需的原核和真核细胞提取物通常需要较高的成本。此外,涉及到的一些试剂和设备也比较昂贵,使得无细胞蛋白表达系统在应用过程中存在一定的经济压力。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2.[/font][font=宋体]表达限制:由于无细胞蛋白表达系统缺乏复杂的代谢反应和细胞分化机制,因此它不适用于某些特定类型的蛋白。例如,它无法表达复杂的膜蛋白和困难的药物蛋白等。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3.[/font][font=宋体]不稳定性:无细胞蛋白表达系统通常具有一定的稳定性问题。由于缺乏细胞膜的保护,无细胞蛋白表达体系会更容易受到外部条件的影响,如温度、[/font][font=Calibri]pH[/font][font=宋体]、离子浓度等,从而导致蛋白质的不稳定性、聚集和降解等现象。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]4.[/font][font=宋体]不适合复杂蛋白结构:无细胞蛋白表达系统对于复杂蛋白结构的模拟效果不佳。例如,膜蛋白、多肽和糖蛋白等复杂蛋白质可能会被无细胞蛋白表达系统无法很好地复制,从而限制了其应用范围。[/font][/font][font=宋体] [/font][font=宋体]无细胞蛋白表达系统具有高效、灵活、易操作、简单纯化等优点,但同时也存在着成本较高、表达限制、不稳定性和不适合复杂蛋白结构等缺点。在实际应用中,需要根据具体的研究目的和需求进行选择,并结合其他技术手段来弥补其不足之处。[/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供[url=https://cn.sinobiological.com/services/cell-free-protein-synthesis-service][b]无细胞蛋白表达服务[/b][/url],服务优势:[/font][font=宋体]①快速、高效 ②高成功率 ③一致性 ④高难度抗体表达[/font][/font][font=宋体] [/font][font=宋体][font=宋体]详情可以咨询,具体[/font][font=Calibri]https://cn.sinobiological.com/services/cell-free-protein-synthesis-service[/font][/font]
原标题 “纳米生物间谍”技术能进入活细胞取样 可用于深入揭示线粒体基因组变异的重要性 科技日报讯 据物理学家组织网近日报道,美国加利福尼亚大学圣克鲁兹分校(UCSC)研究人员开发出一种机器人式的“纳米生物间谍”系统,能从单个活细胞内提取出微量样本,进行RNA或DNA测序,而不会杀死细胞。研究人员表示,这种单细胞“纳米生物间谍”技术是一种了解活细胞内部动态过程的有力工具。相关论文发表在最近出版的美国化学协会《纳米》杂志上。 “我们能从活细胞中拿走一个‘生物间谍’,再把它送回该细胞,在几天内这样重复多次而不会杀死细胞。如果用其他技术,你不得不牺牲这个细胞才能分析它。”该生物传感与生物电技术小组负责人、UCSC巴斯金工程学院生物分子工程教授内德·波曼德说。 “纳米生物间谍”平台是研究小组用纳米吸液管开发的最新设备。纳米吸液管是一种小玻璃管,取液端越来越细,至尖端直径仅50到100纳米。波曼德说:“我能在实验室造出纳米吸液管,这不需要昂贵的纳米制造设备。但要进入一个细胞,问题是即使在高倍显微镜下,你也看不见吸液管尖端,不知道它偏离了细胞有多远。” 实验室博士后研究员亚当·赛格尔解决了这一问题。他基于在一台改造过的扫描离子电导显微镜(SICM),开发出一种反馈控制系统。该系统能利用通过纳米吸液管尖端的离子流作为反馈信号,在尖端接近细胞表面时探测其中的液滴。在尖端进入细胞之前,一种自动控制系统能定位它在细胞上面的位置,然后尖端很快插入穿透细胞膜,通过操控电压有控制地提取一小点细胞内物质。由于吸液管尖端极精细,对细胞造成的损害极微小。 研究小组用这种系统从活细胞中提取的微量细胞物质,估计只有50毫微微升(千万亿分之一升),约一个人体细胞百分之一的量。他们从单个人体癌细胞中提取物质并进行RNA测序,还从人类成纤维细胞中提取了线粒体并对其进行了DNA测序。“人们已经知道,线粒体和多种神经退化疾病有关。该技术可用于深入揭示线粒体基因组变异的重要性。”波曼德说。 该技术应用前景广阔。波曼德希望能与其他研究人员合作,探索其更多用途。“对于癌症生物学家、干细胞生物学家等想要了解细胞内部情况的科学家来说,这是一种多功能的平台。”(常丽君)来源:中国科技网-科技日报 2014年01月20日
随着分子生物学的快速发展,许多实验的目标物质都是细胞内物质,要进行实验研究或产物收集就必须将细胞破壁,使产物得以释放,才能进一步提取,因此细胞破碎就变成了提取胞内产物的关键步骤,破碎方法的得当与否,直接影响到所提取产品的产量、质量和生产成本。现将常用的几种细胞破碎方法介绍如下。1.超声波破碎 利用超声波高强度声能产生的空化现象引起冲击波和剪切力进行细胞破碎。超声破碎的效率与超声频率、超声功率、处理时间、细胞浓度及处理量等因素有关。 不足及须加强的问题:超声波破碎在实验室规模应用较普遍,处理少量样品时操作简便,液量损失少,但超声波产生的化学自由基团可能使某些敏感性活性物质变性失活影响实验结果。且大容量装置声能利用率低,装置散热性差。2.生物酶溶法 就是用生物酶将细胞壁和细胞膜消化溶解的方法。常用的溶酶有溶菌酶β-1.3-葡聚糖酶、蛋白酶等。 不足:易造成产物抑制作用,这可能是导致胞内物质释放率低的最主要因素。而且溶酶价格高,限制了大规模利用。若回收溶酶,则又增加分离纯化溶酶的操作。另外酶溶法通用性差,不同菌种需选择不同的酶。3.物理珠磨法 微生物细胞悬浮液与极细的研磨剂在搅拌浆作用下充分混合,珠子之间以及珠子和细胞之间和互相剪切、碰撞,使细胞壁破碎,释出内容物,在珠波分离器的协助下,珠子被滞留在破碎室内,浆液流出,从而实现连续操作,破碎中产生的热量由夹套中的冷却液带走。缺陷:效能利用率仅为1%左右,且破碎过程产生大量的热能无法利用。4.化学渗透法 某些有机溶剂(如苯、甲苯)、抗生素、表面活性剂、金属螯合剂、变性剂等化学药品都可以改变细胞壁或膜的通透性从而使细胞内容物物有选择地渗透出来。其作用机理;化学渗透取决于化学试剂的类型以及细胞壁和膜的结构与组成。 不足:时间长,效率低;化学试剂毒性较强,同时对产物也有毒害作用,进一步分离时需要用透析等方法除去这些试剂;通用性差。
鸡蛋,在如今的社会里,更多时候是作为一种营养丰富的食品出现在我们的餐桌上。现代化大型养殖场如生产产品般输出鸡蛋的方式颠覆了人们对鸡蛋的认识,或许已经很少有人能够联想到从蛋黄蛋白到一个小生命的奇迹升华。但在人类漫长的历史中,农业是文明的核心。就在不太遥远的过去,大多数人还可以在家中目睹鸡生蛋、蛋生鸡的奇迹。这种神秘的现象让古时的人们感到好奇、困惑,甚至产生莫名的崇拜。我们华夏文明由雏鸡的诞生联想到世界的起源,“天地混沌如鸡子,盘古生其中”,看来在我们祖先的眼中,鸡蛋的孵化犹如天地诞生般神秘。这种“卵生崇拜”在史籍中屡见不鲜,如《史记·殷本纪》记述商朝人先祖契的来历时提到有娀氏的女儿简狄“见玄鸟坠其卵,简狄取吞之,因孕生契”,同样,在《史记·秦本纪》中,文章伊始就记载了颛顼的孙女女修织布时“玄鸟陨卵,女修吞之,生子大业”,而这位大业就是秦人的先祖。不得不佩服古人的想象,这玄鸟蛋孵化出了两个重要朝代。在漫长的历史中,这种对蛋朦胧而浪漫的崇拜逐渐融入了我们的文化中,直到如今,染红壳的鸡蛋依旧是新婚、生子、满月时,人们表达祝福的重要载体。随着科技的进步,人们对蛋的理解逐渐清晰,现在很多人都知道蛋和卵细胞有千丝万缕的关系。可是鸡蛋到底是否就是一个细胞?答案可谓五花八门,有人说整个鸡蛋就是一个放大的卵细胞,蛋壳内的那层膜是细胞膜,蛋清是细胞质,蛋黄是细胞核;也有人说蛋黄是卵细胞,卵黄膜就是细胞膜,蛋黄就是细胞质,而蛋黄上面的小白点是细胞核;还有人认为鸡蛋本就是由很多细胞构成的。
[size=3][font=宋体]基本原理[/font][font=Times New Roman] [/font][/size][size=3][font=宋体]细胞凋亡早期改变发生在细胞膜表面,目前早期识别仍有困难。这些细胞膜表面的改变之一是磷脂酰丝氨酸([/font][font=Times New Roman]PS[/font][font=宋体])从细胞膜内转移到细胞膜外,使[/font][font=Times New Roman]PS[/font][font=宋体]暴露在细胞膜外表面。[/font][font=Times New Roman]PS[/font][font=宋体]是一种带负电荷的磷脂,正常主要存在于细胞膜的内面,在细胞发生凋亡时细胞膜上的这种磷脂分布的不对称性被破坏而使[/font][font=Times New Roman]PS[/font][font=宋体]暴露在细胞膜外。[/font][font=Times New Roman]Annexin V[/font][font=宋体]是一种[/font][font=Times New Roman]Ca+[/font][font=宋体]依赖的磷脂结合蛋白,最初发现是一种具有很强的抗凝血特性的血管蛋白,[/font][font=Times New Roman]Annexin V[/font][font=宋体]具有易于结合到磷脂类如[/font][font=Times New Roman]PS[/font][font=宋体]的特性。对[/font][font=Times New Roman]PS[/font][font=宋体]有高度的亲和性。因此,该蛋白可充当一敏感的探针检测暴露在细胞膜表面的[/font][font=Times New Roman]PS[/font][font=宋体]。[/font][font=Times New Roman]PS[/font][font=宋体]转移到细胞膜外不是凋亡所独特的,也可发生在细胞坏死中。两种细胞死亡方式间的差别是在凋亡的初始阶段细胞膜是完好的,而细胞坏死在其早期阶段细胞膜的完整性就破坏了。因此,可以建立一种用[/font][font=Times New Roman]Annexin V[/font][font=宋体]结合在细胞膜表面作为凋亡的指示并结合一种染料排除试验以检测细胞膜的完整性的检测方法。[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman] [/font][/size][size=3][font=Times New Roman] [/font][/size][size=3][font=宋体]试剂与仪器[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman] [/font][font=宋体]孵育缓冲液:[/font][font=Times New Roman]10mmol/L HEPES/NaOH[/font][font=宋体],[/font][font=Times New Roman]PH 7.4[/font][font=宋体],[/font][font=Times New Roman]140mmol/L NaCl[/font][font=宋体],[/font][font=Times New Roman]5mmol/L CaCl2 [/font][/size][size=3][font=Times New Roman] [/font][font=宋体]标记液:将[/font][font=Times New Roman]FITC- Annexin V[/font][font=宋体](宝灵曼公司产品)和[/font][font=Times New Roman]PI[/font][font=宋体]加入到孵育缓冲液中,终浓度均为[/font][font=Times New Roman]1ug/ml [/font][/size][size=3][font=Times New Roman] [/font][font=宋体]流式细胞仪[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman] [/font][/size][size=3][font=Times New Roman] [/font][/size][size=3][font=宋体]实验步骤[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman]1. [/font][font=宋体]细胞收集:悬浮细胞直接收集到[/font][font=Times New Roman]10ml[/font][font=宋体]的离心管中,每样本细胞数为([/font][font=Times New Roman]1~5[/font][font=宋体])×[/font][font=Times New Roman]106[/font][font=宋体],[/font][font=Times New Roman]/mL[/font][font=宋体] [/font][font=Times New Roman]500~1000r/min[/font][font=宋体]离心[/font][font=Times New Roman]5min[/font][font=宋体],弃去培养液。[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman]2. [/font][font=宋体]用孵育缓冲液洗涤[/font][font=Times New Roman]1[/font][font=宋体]次,[/font][font=Times New Roman]500~1000r/min[/font][font=宋体]离心[/font][font=Times New Roman]5min[/font][font=宋体]。[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman]3. [/font][font=宋体]用[/font][font=Times New Roman]100ul[/font][font=宋体]的标记溶液重悬细胞,室温下避光孵育[/font][font=Times New Roman]10~15min[/font][font=宋体]。[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman]4. 500~1000r/min[/font][font=宋体]离心[/font][font=Times New Roman]5min[/font][font=宋体]沉淀细胞孵育缓冲液洗[/font][font=Times New Roman]1[/font][font=宋体]次。[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman]5. [/font][font=宋体]加入荧光([/font][font=Times New Roman]SA-FLOUS[/font][font=宋体])溶液[/font][font=Times New Roman]4[/font][font=宋体]℃下孵育[/font][font=Times New Roman]20min[/font][font=宋体],避光并不时振动。[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman]6. [/font][font=宋体]流式细胞仪分析:流式细胞仪激发光波长用[/font][font=Times New Roman]488nm[/font][font=宋体],用一波长为[/font][font=Times New Roman]515nm[/font][font=宋体]的通带滤器检测[/font][font=Times New Roman]FITC[/font][font=宋体]荧光,另一波长大于[/font][font=Times New Roman]560nm[/font][font=宋体]的滤器检测[/font][font=Times New Roman]PI[/font][font=宋体]。[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman]7. [/font][font=宋体]结果判断:凋亡细胞对所有用于细胞活性鉴定的染料如[/font][font=Times New Roman]PI[/font][font=宋体]有抗染性,坏死细胞则不能。细胞膜有损伤的细胞的[/font][font=Times New Roman]DNA[/font][font=宋体]可被[/font][font=Times New Roman]PI[/font][font=宋体]着染产生红色荧光,而细胞膜保持完好的细胞则不会有红色荧光产生。因此,在细胞凋亡的早期[/font][font=Times New Roman]PI[/font][font=宋体]不会着染而没有红色荧光信号。正常活细胞与此相似。在双变量流式细胞仪的散点图上,左下象限显示活细胞,为([/font][font=Times New Roman]FITC-/PI-[/font][font=宋体]);右上象限是非活细胞,即坏死细胞,为([/font][font=Times New Roman]FITC+/PI+[/font][font=宋体]);而右下象限为凋亡细胞,显现([/font][font=Times New Roman]FITC+/PI-[/font][font=宋体])。[/font][/size]
目前,细胞冻存最常用的技术是液氮冷冻保存法,主要采用加适量保护剂的缓慢冷冻法冻存细胞。细胞在不加任何保护剂的情况下直接冷冻,细胞内外的水分会很快形成冰晶,从而引起一系列不良反应。如细胞脱水使局部电解质浓度增高,pH值改变,部分蛋白质由于上述原因而变性,引起细胞内部空间结构紊乱,溶酶体膜由此遭到损伤而释放出溶酶体酶,使细胞内结构成分造成破坏,线粒体肿胀,功能丢失,并造成能量代谢障碍。胞膜上的类脂蛋白复合体也易破坏引起细胞膜通透性的改变,使细胞内容物丢失。如果细胞内冰晶形成较多,随冷冻温度的降低,冰晶体积膨胀造成细胞核DNA空间构型发生不可逆的损伤,而致细胞死亡。因此,细胞冷冻技术的关键是尽可能地减少细胞内水分,减少细胞内冰晶的形成。采用甘油或二甲基亚砜作保护剂,这两种物质分子量小,溶解度大,易穿透细胞,可以使冰点下降,提高细胞膜对水的通透性,且对细胞无明显毒性。慢速冷冻方法又可使细胞内的水分渗出细胞外,减少胞内形成冰结晶的机会,从而减少冰晶对细胞的损伤。二、细胞冻存操作步骤:(1)选择处于对数生长期的细胞,在冻存前一天最好换液。将多个培养瓶中的细胞培养液去掉,用0.25%胰蛋白酶消化。适时去掉胰蛋白酶,加入少量新培养液。用吸管吸取培养液反复吹打瓶壁上的细胞,使其成为均匀分散的细胞悬液。悬浮生产细胞则不要消化处理。然后将细胞收集于离心管中离心(1000r/min,10分钟)。(2)去上清液,加入含20%小牛血清的完全培养基,于4℃预冷15分钟后,逐滴加入已无菌的DMSO或甘油,用吸管轻轻吹打使细胞均匀,细胞浓度为3×106~1×107/mL之间。(3)将上述细胞分装于安瓿或专用冷冻塑料管中,安瓿装1~1.5mL在火焰喷灯上封口,封口处要完全封闭,圆滑无勾。冷冻管要将盖子盖紧,并标记好细胞名称和冻存日期,同时作好登记(日期、细胞种类及代次、冻存支数)。(4)将装好细胞的安瓿或冻存管装入沙布袋内;置于液氮容器颈口处存放过夜,次日转入液氮中。采用控制降温速度的方法也可采用下列步骤:先将安瓿置入4℃冰箱中2~3小时,再移至冰箱冷冻室内3~4小时(此步可省略),再吊入液氮容器颈气态部分存放2小时,最后沉入液氮中。细胞冻存在液氮中可以长期保存,但为妥善起见,冻存半年后,最好取出一只安瓿细胞复苏培养,观察生长情况,然后再继续冻存。
[size=3][font=宋体]基本原理[/font][font=Times New Roman] [/font][/size][size=3][font=宋体]细胞凋亡早期改变发生在细胞膜表面,目前早期识别仍有困难。这些细胞膜表面的改变之一是磷脂酰丝氨酸([/font][font=Times New Roman]PS[/font][font=宋体])从细胞膜内转移到细胞膜外,使[/font][font=Times New Roman]PS[/font][font=宋体]暴露在细胞膜外表面。[/font][font=Times New Roman]PS[/font][font=宋体]是一种带负电荷的磷脂,正常主要存在于细胞膜的内面,在细胞发生凋亡时细胞膜上的这种磷脂分布的不对称性被破坏而使[/font][font=Times New Roman]PS[/font][font=宋体]暴露在细胞膜外。[/font][font=Times New Roman]Annexin V[/font][font=宋体]是一种[/font][font=Times New Roman]Ca+[/font][font=宋体]依赖的磷脂结合蛋白,最初发现是一种具有很强的抗凝血特性的血管蛋白,[/font][font=Times New Roman]Annexin V[/font][font=宋体]具有易于结合到磷脂类如[/font][font=Times New Roman]PS[/font][font=宋体]的特性。对[/font][font=Times New Roman]PS[/font][font=宋体]有高度的亲和性。因此,该蛋白可充当一敏感的探针检测暴露在细胞膜表面的[/font][font=Times New Roman]PS[/font][font=宋体]。[/font][font=Times New Roman]PS[/font][font=宋体]转移到细胞膜外不是凋亡所独特的,也可发生在细胞坏死中。两种细胞死亡方式间的差别是在凋亡的初始阶段细胞膜是完好的,而细胞坏死在其早期阶段细胞膜的完整性就破坏了。因此,可以建立一种用[/font][font=Times New Roman]Annexin V[/font][font=宋体]结合在细胞膜表面作为凋亡的指示并结合一种染料排除试验以检测细胞膜的完整性的检测方法。[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman] [/font][/size][size=3][font=Times New Roman] [/font][/size][size=3][font=宋体]试剂与仪器[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman] [/font][font=宋体]孵育缓冲液:[/font][font=Times New Roman]10mmol/L HEPES/NaOH[/font][font=宋体],[/font][font=Times New Roman]PH 7.4[/font][font=宋体],[/font][font=Times New Roman]140mmol/L NaCl[/font][font=宋体],[/font][font=Times New Roman]5mmol/L CaCl2 [/font][/size][size=3][font=Times New Roman] [/font][font=宋体]标记液:将[/font][font=Times New Roman]FITC- Annexin V[/font][font=宋体](宝灵曼公司产品)和[/font][font=Times New Roman]PI[/font][font=宋体]加入到孵育缓冲液中,终浓度均为[/font][font=Times New Roman]1ug/ml [/font][/size][size=3][font=Times New Roman] [/font][font=宋体]流式细胞仪[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman] [/font][/size][size=3][font=Times New Roman] [/font][/size][size=3][font=宋体]实验步骤[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman]1. [/font][font=宋体]细胞收集:悬浮细胞直接收集到[/font][font=Times New Roman]10ml[/font][font=宋体]的离心管中,每样本细胞数为([/font][font=Times New Roman]1~5[/font][font=宋体])×[/font][font=Times New Roman]106[/font][font=宋体],[/font][font=Times New Roman]/mL[/font][font=宋体] [/font][font=Times New Roman]500~1000r/min[/font][font=宋体]离心[/font][font=Times New Roman]5min[/font][font=宋体],弃去培养液。[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman]2. [/font][font=宋体]用孵育缓冲液洗涤[/font][font=Times New Roman]1[/font][font=宋体]次,[/font][font=Times New Roman]500~1000r/min[/font][font=宋体]离心[/font][font=Times New Roman]5min[/font][font=宋体]。[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman]3. [/font][font=宋体]用[/font][font=Times New Roman]100ul[/font][font=宋体]的标记溶液重悬细胞,室温下避光孵育[/font][font=Times New Roman]10~15min[/font][font=宋体]。[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman]4. 500~1000r/min[/font][font=宋体]离心[/font][font=Times New Roman]5min[/font][font=宋体]沉淀细胞孵育缓冲液洗[/font][font=Times New Roman]1[/font][font=宋体]次。[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman]5. [/font][font=宋体]加入荧光([/font][font=Times New Roman]SA-FLOUS[/font][font=宋体])溶液[/font][font=Times New Roman]4[/font][font=宋体]℃下孵育[/font][font=Times New Roman]20min[/font][font=宋体],避光并不时振动。[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman]6. [/font][font=宋体]流式细胞仪分析:流式细胞仪激发光波长用[/font][font=Times New Roman]488nm[/font][font=宋体],用一波长为[/font][font=Times New Roman]515nm[/font][font=宋体]的通带滤器检测[/font][font=Times New Roman]FITC[/font][font=宋体]荧光,另一波长大于[/font][font=Times New Roman]560nm[/font][font=宋体]的滤器检测[/font][font=Times New Roman]PI[/font][font=宋体]。[/font][font=Times New Roman] [/font][/size][size=3][font=Times New Roman]7. [/font][font=宋体]结果判断:凋亡细胞对所有用于细胞活性鉴定的染料如[/font][font=Times New Roman]PI[/font][font=宋体]有抗染性,坏死细胞则不能。细胞膜有损伤的细胞的[/font][font=Times New Roman]DNA[/font][font=宋体]可被[/font][font=Times New Roman]PI[/font][font=宋体]着染产生红色荧光,而细胞膜保持完好的细胞则不会有红色荧光产生。因此,在细胞凋亡的早期[/font][font=Times New Roman]PI[/font][font=宋体]不会着染而没有红色荧光信号。正常活细胞与此相似。在双变量流式细胞仪的散点图上,左下象限显示活细胞,为([/font][font=Times New Roman]FITC-/PI-[/font][font=宋体]);右上象限是非活细胞,即坏死细胞,为([/font][font=Times New Roman]FITC+/PI+[/font][font=宋体]);而右下象限为凋亡细胞,显现([/font][font=Times New Roman]FITC+/PI-[/font][font=宋体])。[/font][/size]
摘要:细胞凋亡与坏死是两种完全不同的细胞凋亡形式,根据死亡细胞在形态学、生物化学和分子生物学上的差别,可以将二者区别开来。细胞凋亡的检测方法有很多,下面介绍几种常用的测定方法。一、细胞凋亡的形态学检测根据凋亡细胞固有的形态特征,人们已经设计了许多不同的细胞凋亡形态学检测方法。1. 光学显微镜和倒置显微镜(1) 未染色细胞:凋亡细胞的体积变小、变形,细胞膜完整但出现发泡现象,细胞凋亡晚期可见凋亡小体。贴壁细胞出现皱缩、变圆、脱落。(2) 染色细胞:常用姬姆萨染色、瑞氏染色等。凋亡细胞的染色质浓缩、边缘化,核膜裂解、染色质分割成块状和凋亡小体等典型的凋亡形态。2. 荧光显微镜和共聚焦激光扫描显微镜一般以细胞核染色质的形态学改变为指标来评判细胞凋亡的进展情况。常用的DNA特异性染料有:HO 33342 (Hoechst 33342),HO 33258 (Hoechst 33258), DAPI。三种染料与 DNA的结合是非嵌入式的,主要结合在DNA的A-T碱基区。紫外光激发时发射明亮的蓝色荧光。Hoechst是与DNA特异结合的活性染料,储存液用蒸馏水配成1mg/ml的浓度,使用时用PBS稀释成终浓度为2~5mg/ml。DAPI为半通透性,用于常规固定细胞的染色。储存液用蒸馏水配成1mg/ml的浓度,使用终浓度一般为0.5 ~1mg/ml。结果评判:细胞凋亡过程中细胞核染色质的形态学改变分为三期:Ⅰ期的细胞核呈波纹状(rippled)或呈折缝样(creased),部分染色质出现浓缩状态;Ⅱa期细胞核的染色质高度凝聚、边缘化;Ⅱb期的细胞核裂解为碎块,产生凋亡小体(图1)。 http://img.dxycdn.com/trademd/upload/userfiles/image/2013/08/A1376376278_small.jpg3 透射电子显微镜观察结果评判:凋亡细胞体积变小,细胞质浓缩。凋亡Ⅰ期(pro-apoptosis nuclei)的细胞核内染色质高度盘绕,出现许多称为气穴现象(cavitations)的空泡结构(图2);Ⅱa期细胞核的染色质高度凝聚、边缘化;细胞凋亡的晚期,细胞核裂解为碎块,产生凋亡小体。 http://img.dxycdn.com/trademd/upload/userfiles/image/2013/08/A1376376295_small.jpg二、磷脂酰丝氨酸外翻分析(Annexin V法)磷脂酰丝氨酸(Phosphatidylserine, PS)正常位于细胞膜的内侧,但在细胞凋亡的早期,PS可从细胞膜的内侧翻转到细胞膜的表面,暴露在细胞外环境中(图3)。Annexin-V是一种分子量为35~36KD的Ca2+依赖性磷脂结合蛋白,能与PS高亲和力特异性结合。将Annexin-V进行荧光素(FITC、PE)或biotin标记,以标记了的Annexin-V作为荧光探针,利用流式细胞仪或荧光显微镜可检测细胞凋亡的发生。碘化丙啶(propidine iodide, PI)是一种核酸染料,它不能透过完整的细胞膜,但在凋亡中晚期的细胞和死细胞,PI能够透过细胞膜而使细胞核红染。因此将Annexin-V与PI匹配使用,就可以将凋亡早晚期的细胞以及死细胞区分开来。http://img.dxycdn.com/trademd/upload/userfiles/image/2013/08/A1376376296_small.jpg方法1. 悬浮细胞的染色:将正常培养和诱导凋亡的悬浮细胞(0.5~1×106)用PBS洗2次,加入100 ul Binding Buffer和FITC标记的Annexin-V(20ug/ml)10 ul,室温避光30 min,再加入PI(50 ug/ml)5 ul,避光反应5 min后,加入400 ul Binding Buffer,立即用FACScan进行流式细胞术定量检测(一般不超过1 h), 同时以不加AnnexinV-FITC及PI的一管作为阴性对照。2. 贴壁培养的细胞染色:先用0.25%的胰酶消化,洗涤、染色和分析同悬浮细胞。3. 爬片细胞染色:同上,最后用荧光显微镜和共聚焦激光扫描显微镜进行观察。结果 http://img.dxycdn.com/trademd/upload/userfiles/image/2013/08/A1376376298_small.jpg http://img.dxycdn.com/trademd/upload/userfiles/image/2013/08/A1376376300_small.jpg
美国俄亥俄州立大学李巨研究小组首次在分子层面上设计一种模型,能够描述血红细胞是如何从正常的扁圆形缩成子弹形,穿过比它们的正常直径还小的血管。该研究结果在线发表在3月12日的《美国科学院院刊》上。 研究血红细胞如何从柔软的物体变成几乎液化的形态,能够帮助科学家们更好地了解疟疾、镰状细胞贫血症以及球形红细胞贫血症等。 人类血红细胞在其4个月的生命中,要成百万次地挤过细小的毛细血管,以便输送氧气,运走二氧化碳等废物。这是生命必需的过程。血红细胞的直径约为8微米,它们在流动过程中,常常穿过直径只有2微米的血管。血红细胞会拉长成子弹形状,然后在穿过血管后,恢复成本来的扁圆形。 李巨研究小组设计的这种模型显示,血红细胞的细胞骨架在这个变形过程中起到了重要作用。每个血红细胞都有一个细胞骨架,它由一种名为“血影蛋白”的蛋白分子构成,以一种类似毛刷的结构附着在细胞膜内侧。当这层蛋白质结构之间的键接破裂,或者这层结构与细胞膜之间的附着破裂,细胞就会变得更加柔软,从而能够穿过狭窄的通道。 研究人员发现这种变化或者是由于两个血影蛋白分子之间的键被断开,或者是由于血影蛋白与一种细胞膜中的肌动蛋白的键被断开。而加诸机械力(如挤压或者切断)或者化学能(如ATP),都足以断开这些化学键,进而引起细胞骨架的变形。 研究人员将利用该模型进一步研究几种血液疾病,包括疟疾、镰状细胞贫血症以及球形红细胞贫血症等。在疟疾患者中,细胞里的寄生虫会改变细胞膜和细胞骨架,从而使细胞失去原有的弹性,无法穿过血管。在镰状细胞贫血症中,红细胞会变成镰刀状,而在球形红细胞贫血症中,红细胞会变成球形,因而都无法正常地通过血管。 李巨博士1994年毕业于中国科学技术大学少年班。2000年获得麻省理工学院核工程技术系博士学位,之后在该系从事博士后研究工作,2002年成为俄亥俄州立大学助理教授。曾获美国材料学会2006年度青年科学家奖。
[b][font=微软雅黑][size=10.5pt]一、机械破碎法:[/size][/font][/b][font=微软雅黑][size=10.5pt][font=微软雅黑]是指利用捣碎机、研磨器或匀浆器[/font] [font=微软雅黑]等将细胞破碎开来[/font] [font=微软雅黑]。[/font][/size][/font][font=微软雅黑][size=10.5pt]1. 高速组织捣碎:将材料配成稀糊状液,放置于筒内约1/3体积,盖紧筒盖,将调速器先拨至最慢处,开动开关后,逐步加速至所需速度。此法适用于动物内脏组织、植物肉质种子等。[/size][/font][font=微软雅黑][size=10.5pt]2. 玻璃匀浆器匀浆:先将剪碎的组织置于管中,再套入研杆来回研磨,上下移动,即可将细胞研碎,此法细胞破碎程度比高速组织捣碎机为高,适用于量少和动物脏器组织。[/size][/font][b][font=微软雅黑][size=10.5pt]二、物理破碎法:[/size][/font][/b][font=微软雅黑][size=10.5pt]指利用温度差、压力差或超声波等将细胞破碎开来。[/size][/font][font=微软雅黑][size=10.5pt]1.用一定功率的超声波处理细胞悬液,使细胞急剧震荡破裂(借助超声的震动力破碎细胞壁和细胞器)。[/size][/font][font=微软雅黑][size=10.5pt]机制:可能与强声波作用溶液时,气泡产生、长大和破碎的空化现象有关,空化现象引起的冲击波和剪刀力使细胞裂解。[/size][/font][font=微软雅黑][size=10.5pt]超声波破碎的效率取决于声频、声能、处理时间、细胞浓度和细胞类型等。(使用时注意降温,防止过热)。[/size][/font][font=微软雅黑][size=10.5pt]2. 高压破碎:细胞悬浮液从高压室的环状隙喷射到静止的撞击环上,被迫改变方向经出口管流出。此过程中细胞经历了高速造成的剪切的碰撞及高压到常压的变化,从而破碎释放内含物。[/size][/font][font=微软雅黑][size=10.5pt]这是一种温和的、彻底破碎细胞的较理想的方法。[/size][/font][font=微软雅黑][size=10.5pt]3. 反复冻融法:将细胞在-20度以下冰冻,室温融解,反复几次,由于细胞内冰粒形成和剩余细胞液的盐浓度增高引起溶胀,使细胞结构破碎。[/size][/font][b][font=微软雅黑][size=10.5pt]三、化学破碎法:[/size][/font][/b][font=微软雅黑][size=10.5pt][font=微软雅黑]指利用甲醛、丙酮等有机溶剂或表面活性剂作用于细胞膜,使细胞膜的结构遭到破坏或透性发生改变[/font] [font=微软雅黑]。[/font][/size][/font][font=微软雅黑][size=10.5pt][font=微软雅黑]有些动物细胞,例如肿瘤细胞可采用十二烷基磺酸钠([/font]SDS)、去氧胆酸钠等细胞膜破坏。浓度一般为1mg/ml。[/size][/font][font=微软雅黑][size=10.5pt][font=微软雅黑]四、酶学破碎法[/font] [font=微软雅黑]:[/font][/size][/font][font=微软雅黑][size=10.5pt]选用合适的酶,使细胞壁遭到破坏,进而在低渗溶液中将原生质体破碎开来。[/size][/font][font=微软雅黑][size=10.5pt]细菌细胞壁较厚,可采用溶菌酶处理效果更好。[/size][/font][font=微软雅黑][size=10.5pt][font=微软雅黑]裂解液标准配方[/font]: :50mM Tris-HCl(pH8.5~9.0), 2mM EDTA, 100mM NaCl, 0.5% Triton X-100, 1mg/ml溶菌酶。(溶菌酶在这个pH范围内比较好发挥作用) 。[/size][/font][font=微软雅黑][size=10.5pt][font=微软雅黑]综合叙述:无论用哪一种方法破碎组织细胞,都会使细胞内蛋白质或核酸水解酶释放到溶液中,使大分子生物降解,导致天然物质量的减少,加入二异丙基氟磷酸([/font]DFP)可以抑制或减慢自溶作用;加入碘乙酸可以抑制那些活性中心需要有疏基的蛋白水解酶的活性,加入PMSF也能清除蛋白水解酶活力,但不是全部,而且应该在破碎的同时多加几次;另外,还可通过选择pH、温度或离子强度等,使这些条件都要适合于目的物质的提取。[/size][/font]
大家好,我初次接触TEM准备看细胞的精细结构,完全没有经验,想做一个关于在细胞膜上看到5nm量子点,我看文献主要涉及到为了制备TEM样品,将裸露的的细胞固定在戊二醛(2.5%)溶液中。 然后将细胞样品用1%四氧化锇后固定。 用二甲胂酸盐缓冲液(0.1M)洗涤后,用一系列乙醇溶液(30,50,70,90和100%)使细胞脱水。 所有这些处理均在4℃下进行。 之后,将细胞用环氧丙烷处理,渗透并包埋在液体树脂中。 使用超薄切片机切割树脂块,并在网格上收集切片。 使用TEM和STEM模式在FEI Talos F200X高分辨率透射电子显微镜下进行成像。我目前能做到的就是用戊二醛溶液把细胞固定,其他试剂或者仪器暂时都没有,所以想联系老师是否可以帮忙测试。价格可以协商,手机号:15122625693
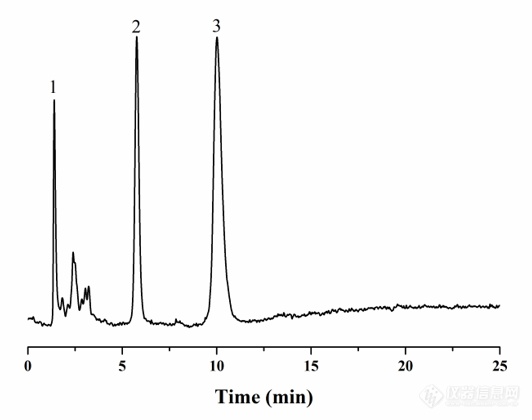
[align=left][font='times new roman'][size=16px]SiO[/size][/font][font='times new roman'][sub][size=16px]2[/size][/sub][/font][font='times new roman'][size=16px]-DMOA[/size][/font][font='times new roman'][size=16px]色谱柱分离磷脂[/size][/font][/align][align=left][font='times new roman'][size=16px]标准品[/size][/font][/align]不同类别的磷脂结构上的差异主要表现为头部基团极性的差异,在分离时主要采用正相色谱模式。基于SiO[font='times new roman'][sub][size=16px]2[/size][/sub][/font]-DMOA色谱柱具有反相/亲水混合模式保留特性,首先采用不同类别的磷脂标准品考察SiO[font='times new roman'][sub][size=16px]2[/size][/sub][/font]-DMOA色谱柱对混磷脂样品的分离选择性。如图示,以具有相同烷基侧链的磷脂DPPG、DPPE和DPPC为样品,能够在10 min内实现共洗脱,其出峰顺序依次为DPPG、DPPE和DPPC。[align=center][img]https://ng1.17img.cn/bbsfiles/images/2022/11/202211302316003138_968_5887186_3.png[/img][/align][align=center][size=13px]图[/size][size=13px] [/size][size=13px]混磷脂标准品在[/size][size=13px]SiO[/size][font='times new roman'][sub][size=13px]2[/size][/sub][/font][size=13px]-DMOA[/size][size=13px]色谱柱上的色谱分离图[/size][/align]进一步将SiO[font='times new roman'][sub][size=16px]2[/size][/sub][/font]-DMOA色谱柱应用于不同PC种类的分离。如图所示,以甲醇/乙腈(40/60,v/v)为流动相,DMPC、DPPC和DSPC在17 min内实现基线分离,且峰形良好,并没有明显拖尾现象。DMPC、DPPC和DSPC的差异主要表现为两条酰基侧链含碳数目的不同,它们尾部含碳数目分别为13、15和17。因此3种PC在SiO[font='times new roman'][sub][size=16px]2[/size][/sub][/font]-DMOA色谱柱上的洗脱顺序依次为DMPC、DPPC和PSPC。[align=center][img]https://ng1.17img.cn/bbsfiles/images/2022/11/202211302316021382_7179_5887186_3.png[/img][/align][align=center][size=13px]图[/size][size=13px] [/size][size=13px]混[/size][size=13px]PC[/size][size=13px]在[/size][size=13px]SiO[/size][font='times new roman'][sub][size=13px]2[/size][/sub][/font][size=13px]-DMOA[/size][size=13px]色谱柱中的分离谱图[/size][/align][align=left][font='times new roman'][size=16px] SiO[/size][/font][font='times new roman'][sub][size=16px]2[/size][/sub][/font][font='times new roman'][size=16px]-DMOA[/size][/font][font='times new roman'][size=16px]色谱柱分离大豆卵磷脂和肺腺癌细胞膜磷脂提取物[/size][/font][/align]基于SiO[font='times new roman'][sub][size=16px]2[/size][/sub][/font]-DMOA色谱柱对磷脂大类和磷脂类别的良好分离性能,以大豆卵磷脂提取物为实际样品,进一步探究SiO[font='times new roman'][sub][size=16px]2[/size][/sub][/font]-DMOA色谱柱对复杂磷脂样品的分离性能。以A/甲醇(50:50,v/v)为流动相的色谱分离图,大豆卵磷脂的分离是采用正相色谱条件下进行,从图中可以观察到在12 min内,可以观察到10个色谱峰,显示了良好的分离性能。[align=center][img]https://ng1.17img.cn/bbsfiles/images/2022/11/202211302316006230_4359_5887186_3.png[/img][/align][align=center][size=13px]图[/size][size=13px] [/size][size=13px]大豆卵磷脂在[/size][size=13px]SiO[/size][font='times new roman'][sub][size=13px]2[/size][/sub][/font][size=13px]-DMOA[/size][size=13px]色谱柱上的色谱分离图[/size][/align]此外,以肺腺癌细胞膜磷脂提取物为样品,对其分离的色谱条件与大豆卵磷脂一致,考察了SiO[font='times new roman'][sub][size=16px]2[/size][/sub][/font]-DMOA色谱柱对肺腺癌细胞膜磷脂提取物的分离性能。如图所示,肺腺癌细胞膜磷脂提取物在12 min内大致可观察到11个色谱峰。上述结果证实SiO[font='times new roman'][sub][size=16px]2[/size][/sub][/font]-DMOA色谱柱对复杂磷脂样品也同样具有良好的分离选择性。[align=center][img]https://ng1.17img.cn/bbsfiles/images/2022/11/202211302316024767_1277_5887186_3.png[/img][/align][align=center][size=13px]图[/size][size=13px] [/size][size=13px]肺腺癌细胞磷脂提取物在[/size][size=13px]SiO[/size][font='times new roman'][sub][size=13px]2[/size][/sub][/font][size=13px]-DMOA[/size][size=13px]色谱柱上的色谱分离图[/size][/align]
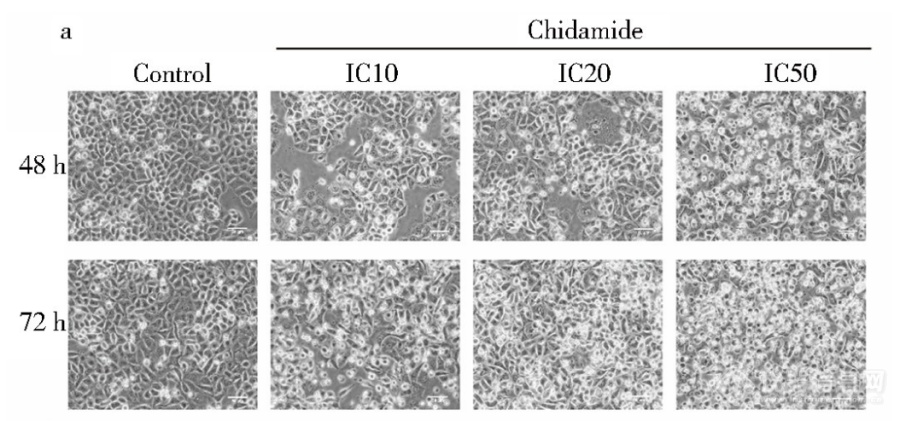
显微镜下西达本胺影响HCT-15细胞形态细胞经不同浓度药物处理后形态发生变化(图),随着药物浓度及作用时间的增加,细胞形态变为长 梭形,触角增多,细胞内颗粒物增多,并且可见空泡 同时相邻细胞之间连接疏松,细胞膜折光度下降,细胞数 量也随之减少[img]https://ng1.17img.cn/bbsfiles/images/2023/06/202306302200230901_4314_5389809_3.png[/img]
β分散频率范围内,生物量容积率与培养液中介电系数有关。在一定电场频率范围内,生物量容积与细胞大小无关,只与细胞浓度成线性关系。在外界交变电场的影响下,培养基中的离子向电极靠近,带有完整细胞膜的细胞(活细胞)在培养基中发生极化现象,形成一个极小的电容,这些小的“电容”可以被传感器两端的检测器检测到,从而得到实时的细胞浓度不知道这种仪器在学术研究上作用如何?请大家给点建议!
激光扫描共聚焦显微镜是近十年发展起来的医学图像分析仪器,与传统的光学显微镜相比,大大地提高了分辨率,能得到真正具有三维清晰度的原色图像。并可探测某些低对比度或弱荧光样品,通过目镜直接观察各种生物样品的弱自发荧光。能动态测量Ca2+ 、pH值,Na+、Mg2+等影响细胞代谢的各种生理指标,对细胞动力学研究有着重要的意义。同时激光扫描共聚显微镜可以处理活的标本,不会对标本造成物理化学特性的破坏,更接近细胞生活状态参数测定。可见激光扫描共聚焦显微镜是普遍显微镜上的质的飞跃,是电子显微镜的一个补充,现已广泛用于荧光定量测量,共焦图像分析,三维图像重建、活细胞动力学参数分析和胞间通讯研究等方面,在整个细胞生物学研究领域有着广阔的应用前景。1. 定量荧光测量ACAS可进行重复性极佳的低光探测及活细胞荧光定量分析。利用这一功能既可对单个细胞或细胞群的溶酶体,线粒体、DNA、RNA和受体分子含量、成份及分布进行定性及定量测定,还可测定诸如膜电位和配体结合等生化反应程度。此外,还适用于高灵敏度快速的免疫荧光测定,这种定量可以准确监测抗原表达,细胞结合和杀伤及定量的形态学特性,以揭示诸如肿瘤相关抗原表达的准确定位及定量信息。2. 定量共聚焦图像分析借助于ACAS激光共焦系统,可以获得生物样品高反差、高分辨率、高灵敏度的二维图像。可得到完整活的或固定的细胞及组织的系列及光切片,从而得到各层面的信息,三维重建后可以揭示亚细胞结构的空间关系。能测定细胞光学切片的物理、生物化学特性的变化,如DNA含量、RNA含量、分子扩散、胞内离子等,亦可以对这些动态变化进行准确的定性、定量、定时及定位分析。3. 三维重组分析生物结构ACAS使用SFP进行三维图像重组,SFP将各光学切片的数据组合成一个真实的三维图像,并可从任意角度观察,也可以借助改变照明角度来突出其特征,产生更生动逼真的三维效果。4. 动态荧光测定Ca2+、pH 及其它细胞内离子测定,利用ACAS能迅速对样品的点,线或二维图像扫描,测量单次、多次单色、双发射和三发射光比率,使用诸如Indo-1、BCECF 、Fluo-3等多种荧光探针对各种离子作定量分析。可以直接得到大分子的扩散速率,能定量测定细胞溶液中Ca2+对肿瘤启动因子、生长因子及各种激素等刺激的反应,以及使用双荧光探针Fluo-3和CNARF进行Ca2+和pH的同时测定。5. 荧光光漂白恢复(FRAP)——活细胞的动力学参数荧光光漂白恢复技术借助高强度脉冲式激光照射细胞某一区域,从而造成该区域荧光分子的光淬灭,该区域周围的非淬灭荧光分子将以一定速率向受照区域扩散,可通过低强度激光扫描探测此扩散速率。通过ACAS可直接测量分子扩散率、恢复速度,并由此而揭示细胞结构及相关的机制。6. 胞间通讯研究动物细胞中由缝隙连接介导的胞间通讯被认为在细胞增殖和分化中起非常重要的作用。ACAS可用于测定相邻植物和动物细胞之间细胞间通讯,测量由细胞缝隙连接介导的分子转移,研究肿瘤启动因子和生长因子对缝隙连接介导的胞间通讯的抑制作用,以及胞内Ca2+、PH和cAMP水平对缝隙连接的调节作用。7. 细胞膜流动性测定ACAS设计了专用的软件用于对细胞膜流动性进行定量和定性分析。荧光膜探针受到极化光线激发后,其发射光极性依赖于荧光分子的旋转,而这种有序的运动自由度依赖于荧光分子周围的膜流动性,因此极性测量间接反映细胞膜流动性。这种膜流动性测定在膜的磷脂酸组成分析、药物效应和作用位点,温度反应测定和物种比较等方面有重要作用。8. 笼锁-解笼锁测定许多重要的生活物质都有其笼锁化合物,在处于笼锁状态时,其功能被封闭,而一旦被特异波长的瞬间光照射后,光活化解笼锁,使其恢复原有活性和功能,在细胞的增值、分化等生物代谢过程中发挥功能。利用ACAS可以人为控制这种瞬间光的照射波长和时间,从而达到人为控制多种生物活性产物和其它化合物在生物代谢中发挥功能的时间和空间作用。9. 粘附细胞分选ACAS是目前唯一能对粘附细胞进行分离筛选的分析细胞学仪器,它对培养皿底的粘附细胞有两种分选方法: ① Coolie-CutterTM法,它是Meidian公司专利技术,首先将细胞贴壁培养在特制培养皿上,然后用高能量激光的欲选细胞四周切割成八角形几何形状,而非选择细胞则因在八角形之外而被去除,该分选方式特别适用于选择数量较少诸如突变细胞、转移细胞和杂交瘤细胞,即使百万分之一机率的也非常理想。 ② 激光消除法,该方法亦基于细胞形态及荧光特性,用高能量激光自动杀灭不需要的细胞,留下完整活细胞亚群继续培养,此方法特别适于对数量较多细胞的选择。10. 细胞激光显微外科及光陷阱技术借助ACAS可将激光当作“光子刀”使用,借此来完成诸如细胞膜瞬间穿孔、切除线粒体、溶酶体等细胞器、染色体切割、神经元突起切除等一系列细胞外科手术。通过ACAS光陷阱操作来移动细胞的微小颗粒和结构,该新技术广泛用于染色体、细胞器及细胞骨架的移动。
[align=center][size=18px][b]细胞信号通路那些事儿[/b][/size][/align][align=center][size=14px]会议时间[/size][size=14px]:[/size][size=14px]2020年[/size][size=14px]5[/size][size=14px]月[/size][size=14px]2[/size][size=14px]8[/size][size=14px]日1[/size][size=14px]4[/size][size=14px]:00[/size][/align][size=16px][b]内容[/b][/size][size=16px][b]介绍:[/b][/size]信号通路(signal pathway)的提出最早可以追溯到1972年,信号通路是指能将细胞外的分子信号经细胞膜传入细胞内发挥效应的一系列酶促反应通路。这些细胞外的分子信号(称为配体,ligand)包括激素、生长因子、细胞因子、神经递质以及其它小分子化合物等。配体特异性地结合到细胞膜或细胞内的受体(receptor)后,在细胞内的信号又是如何传递的呢?细胞内各种不同的生化反应途径都是由一系列不同的蛋白组成的,执行着不同的生理生化功能。各个信号通路中上游蛋白对下游蛋白活性的调节(包括激活或抑制作用)主要是通过添加或去除磷酸基团,从而改变下游蛋白的立体构象完成的。所以,构成信号通路的主要成员是蛋白激酶和磷酸酶。受体蛋白将细胞外信号转变为细胞内信号,经信号级联放大、分散和调节,最终产生一系列综合性的细胞应答,包括下游基因表达的调节、细胞内酶活性的变化、细胞骨架构型和DNA合成的改变等。这些变化并非都是由一种信号引起的,也可以通过几种信号的不同组合产生不同的反应。本次讲座将为大家介绍几种常见的信号通路及酶标仪在其中的应用。[size=16px][b]讲师[/b][/size][size=16px][b]介绍:[/b][/size] [size=14px][b]田华[/b][/size][size=14px][b]:[/b][/size][size=14px]现任[/size][size=14px]MolecularDevices[/size][size=14px]高级应用科学家,在[/size][size=14px]MolecularDevices[/size][size=14px]公司从事酶标仪的售前售后技术支持工作,熟悉酶标仪的原理及各种应用。毕业于南京农业大学遗传学专业,曾就职于中国科学院植物生理生态研究所和生物公司,拥有8年生物技术公司工作经验,熟悉各种分子和细胞生物学实验[/size][size=14px]。[/size]报名地址:[url]https://www.instrument.com.cn/webinar/meeting_13687.html[/url]