药用辅料是指生物药品和调剂处方时所用的赋形剂与附加剂,即除主要活性成分以外的一切物料的总称。在注射剂制备过程中,为确保安全、有效、稳定,除主药和溶剂之外常加入辅料以增加溶解度、提高稳定性等。常用的助溶剂和增溶剂有苯甲醇、乙醇、丙二醇、聚山梨醇酯80、环糊精等。现对常用的助溶剂和增溶剂存在的不良反应以及所涉及的药物进行总结,提高临床用药安全性。1. 苯甲醇:可与红细胞膜表面结合,产生溶血,其他还可能导致低血压、局部刺激、过敏反应、臀肌挛缩症等。禁止用于儿童肌肉注射。可引起婴儿致命性喘息综合征,禁用于婴儿。2. 乙醇:有刺激性,与头孢菌素类药物或甲硝唑、替硝唑等联合应用时,要注意药源性双硫仑样反应。3. 丙二醇:可能导致患者出现接触性皮炎、渗透压升高、乳酸酸中毒、中枢神经系统抑制、溶血、局部静脉炎、心脏毒性反应等不良反应。4. 聚山梨酯80:可能导致过敏反应、外周神经毒性、肝毒性等不良反应。5. 环糊精:主要不良反应为肾毒性,易引起环糊精蓄积。中至重度肾功能不全(肌酐清除率<50mL/min)者可能导致体内蓄积,不宜选用。
盐酸是药物辅料,我最近发现几家公司盐酸含量测定方法却不一样,比如指示剂,有的用甲基红、有的用甲基橙、有的用溴甲酚绿、有的用酚酞。都是用氢氧化钠标准溶液滴定。我查阅法规:国家药典2010版用甲基红,国家标准《GB 320-2006 工业用合成盐酸》和《GB 1897-2008 食品添加剂 盐酸》和化工行业标准《HG/T 2778-2009 高纯盐酸》用溴甲酚绿,电力行业标准《DL 422.2-91 工业盐酸含量的测定——容量法》用甲基橙,酚酞的使用没有找到法规依据。请问:①药用辅料比如盐酸的检测方法必须按照国家药典方法检测吗,可以用国家标准或行业标准吗?②没有法规依据的检测方法,比如使用酚酞检测,是不是要做药用辅料的方法验证,并报主管部门备案?③电力行业标准是否适应化工行业和化工制药的检测标准。
http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_647464_2507958_3.gif【网络讲堂第214期】最新便携式拉曼光谱在药物原辅料现场快速检定中的应用主讲人:李宇 海洋光学亚洲分公司技术中心经理 活动时间:2012年8月30日 下午 14:30http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_647464_2507958_3.gif1、报名条件:只要您是仪器网注册用户均可报名参加。2、参加及审核人数限制:限制报名人数为120人,审核人数100人。3、报名截止时间:2012年8月30日下午14:304、报名参会:http://simg.instrument.com.cn/meeting/images/20100414/baoming.jpg5、参与互动:本次讲座采取网络讲堂直播模式,欢迎大家积极发言提问。 *参会期间您还可以将有疑问的数据通过上传的形式给老师予以展示,并寻求解答* 每次会议从提问的用户中随机抽取出一名幸运之星,奖励一个价值150元的耳机。6、环境配置:只要您有电脑、外加一个耳麦就能参加。建议使用IE浏览器进入会场。7、提问时间:现在就可以在此帖提问啦,截至2012年8月29日8、会议进入:2012年8月30日14:00点就可以进入会议室9、开课时间:2012年8月30日14:3010、特别说明:报名并通过审核将会收到1 封电子邮件通知函(您已注册培训课程),请注意查收,并按提示进入会议室!为了使您的报名申请顺利通过,请填写完整而正确的信息哦~http://simg.instrument.com.cn/webinar/20110223/images/zb_11.gif注意:由于参会名额有限,如您通过审核,请您珍惜宝贵的学习交流机会,按时参加会议。如您临时有事无法参会,请您进入报名页面请假。无故不参会将会影响您下一次的参会报名。快来参加吧:我要报名》》》快来提问吧:我要提问》》》
http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_646767_2507958_3.gif【在线讲座190期】手持式拉曼光谱在药物原辅料现场快速检定中的应用主讲人:叶菲 B&W Tek公司应用工程师 活动时间:2012年6月20日 上午 10:00http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_646767_2507958_3.gif1、报名条件:只要您是仪器网注册用户均可报名参加。2、参加及审核人数限制:限制报名人数为120人,审核人数100人。3、报名截止时间:2012年6月20日上午10:004、报名参会:http://simg.instrument.com.cn/meeting/images/20100414/baoming.jpg5、参与互动:本次讲座采取网络讲堂直播模式,欢迎大家积极发言提问。 *参会期间您还可以将有疑问的数据通过上传的形式给老师予以展示,并寻求解答*6、环境配置:只要您有电脑、外加一个耳麦就能参加。建议使用IE浏览器进入会场。7、提问时间:现在就可以在此帖提问啦,截至2012年6月19日8、会议进入:2012年6月20日9:30点就可以进入会议室9、开课时间:2012年6月20日10:0010、特别说明:报名并通过审核将会收到1 封电子邮件通知函(您已注册培训课程),请注意查收,并按提示进入会议室!为了使您的报名申请顺利通过,请填写完整而正确的信息哦~http://simg.instrument.com.cn/webinar/20110223/images/zb_11.gif注意:由于参会名额有限,如您通过审核,请您珍惜宝贵的学习交流机会,按时参加会议。如您临时有事无法参会,请您进入报名页面请假。无故不参会将会影响您下一次的参会报名。快来参加吧:我要报名》》》快来提问吧:我要提问》》》
炮制辅料是指具有辅助作用的附加物料,它对主药起到增强疗效或降低毒性,或影响主药理化性质等作用。常用的辅料分为两大类:液体辅料和固体辅料。液体辅料主要包括酒、醋、盐水、生姜汁、蜂蜜、甘草汁、黑豆汁、米泔水等。固体辅料主要包括稻米、麦麸、白矾、豆腐、土、蛤粉、河砂、滑石粉等。首先要熟悉该辅料对药物有无药性影响,在哪些炮制方法中使用,使用中有何特点,目的是什么。另外最好结合加辅料炒法和炙法等具体内容来综合记忆。 (一)液体辅料 该类辅料须渗入药物组织内部,多以其自身的性质对药物药性产生影响。 1.酒有黄酒、白酒之分。酒性大热、味甘、辛,能活血通络,祛风散寒,行药势,矫味矫臭。所含主要成分乙醇是良好的溶酶,药物经酒制后,有助于有效成分的溶出,而增加疗效。炙药多用黄酒,浸药多用白酒。性味苦寒的药物酒炙可缓和药性,引药上行,如大黄、黄芩、黄柏等;活血化瘀、祛风通络的药物酒炙可协同增效,如当归、川芎。有不良嗅味的药物酒炙可矫嗅去腥,如乌梢蛇、紫河车。酒蒸主要增强药物的补益作用,如女贞子、肉苁蓉等。 2.醋古时称酢、醯、苦酒,常用米醋。醋性味酸、苦温。具有引药入肝、理气、止血、行水、消肿、解毒、散瘀止痛、矫味矫臭作用。同时醋具酸性,能使药物中所含有的游离生物碱等成分结合成盐,增强溶解度而易煎出有效成分,提高疗效,如醋制延胡索等。药物经醋炙,可引药入肝经,增强疗效,如乳香、三棱醋炙增强活血散瘀止痛作用;柴胡、香附醋炙增强疏肝止痛作用。峻下逐水药醋炙降低毒性,缓和泻下作用,如甘遂、商陆等。树脂类、动物粪便类药物醋炙可矫嗅矫味,如五灵脂、乳香、没药。五味子醋蒸可协同增强酸涩收敛之性。
简单介绍一下关于药物高通量筛选技术的知识一.概念高通量筛选(High throughput screening,HTS)技术是指以分子水平和细胞水平的实验方法为基础,以微板形式作为实验工具载体,以自动化操作系统执行试验过程,以灵敏快速的检测仪器采集实验结果数据,以计算机对实验数据进行分析处理,同一时间对数以千万样品检测,并以相应的数据库支持整个体系运转的技术体系。二. 高通量筛选技术体系的组成1. 化合物样品库化合物样品主要有人工合成和从天然产物中分离纯化两个来源。其中,人工合成又可分为常规化学合成和组合化学合成两种方法。2.自动化的操作系统自动化操作系统利用计算机通过操作软件控制整个实验过程。操作软件采用实物图像代表实验用具,简洁明了的图示代表机器的动作。自动化操作系统的工作能力取决于系统的组分,根据需要可配置加样、冲洗、温解、离心等设备以进行相应的工作。3.高灵敏度的检测系统检测系统一般采用液闪计数器、化学发光检测计数器、宽谱带分光光度仪、荧光光度仪等。4.数据库管理系统数据库管理系统承担4个方面的功能: 样品库的管理功能;生物活性信息的管理功能; 对高通量药物筛选的服务功能; 药物设计与药物发现功能。三. 高通量筛选模型常用的筛选模型都在分子水平和细胞水平,观察的是药物与分子靶点的相互作用,能够直接认识药物的基本作用机制。1. 分子水平的药物筛选模型:受体筛选模型;酶筛选模型;离子通道筛选模型1.1受体筛选模型:指受体与放射性配体结合模型。以受体为作用靶的筛选方法,包括检测功能反应、第二信使生成和标记配体与受体相互作用等不同类型。1.2酶筛选模型:观察药物对酶活性的影响。根据酶的特点,酶的反应底物,产物都可以作为检测指标,并由此确定反应速度。典型的酶筛选包括1) 适当缓冲液中孵化;(2)控制反应速度,如:温度,缓冲液的pH值和酶的浓度等;(3)单时间点数器, 需测量产物的增加和底物的减少。1.3离子通道筛选模型: (1)贝类动物毒素的高通量筛选,其作用靶为Na+通道上的蛤蚌毒素结合位点,用放射性配体进行竞争性结合试验考察受试样品。(2)用酵母双杂交的方法高通量筛选干扰N型钙通道β3亚单位与α1β亚单位相互作用的小分子,寻找新型钙通道拮抗剂。2.细胞水平药物筛选模型观察被筛样品对细胞的作用,但不能反映药物作用的具体途径和靶标,仅反映药物对细胞生长等过程的综合作用。包括: 内皮细胞激活; 细胞凋亡; 抗肿瘤活性; 转录调控检测; 信号转导通路; 细菌蛋白分泌; 细菌生长。四.问题及展望高通量筛选技术与传统的药物筛选方法相比有以下几个优点:反应体积小;自动化;灵敏快速检测;高度特异性。但是,高通量筛选作为药物筛选的一种方法,并不是一种万能的手段,特别是在中药研究方面,其局限性也是十分明显的。首先,高通量筛选所采用的主要是分子、细胞水平的体外实验模型,因此任何模型都不可能充分反映药物的全面药理作用;其次,用于高通量筛选的模型是有限的和不断发展的,要建立反映机体全部生理机能或药物对整个机体作用的理想模型,也是不现实的。但我们应该相信,随着对高通量筛选研究的不断深入,随着对筛选模型的评价标准、新的药物作用靶点的发现以及筛选模型的新颖性和实用性的统一,高通量筛选技术必将在未来的药物研究中发挥越来越重要的作用。
炮制辅料是指具有辅助作用的附加物料,它对主药起到增强疗效或降低毒性,或影响主药理化性质等作用。常用的辅料分为两大类:液体辅料和固体辅料。液体辅料主要包括酒、醋、盐水、生姜汁、蜂蜜、甘草汁、黑豆汁、米泔水等。固体辅料主要包括稻米、麦麸、白矾、豆腐、土、蛤粉、河砂、滑石粉等。首先要熟悉该辅料对药物有无药性影响,在哪些炮制方法中使用,使用中有何特点,目的是什么。另外最好结合加辅料炒法和炙法等具体内容来综合记忆。 (一)液体辅料 该类辅料须渗入药物组织内部,多以其自身的性质对药物药性产生影响。 1.酒 有黄酒、白酒之分。酒性大热、味甘、辛,能活血通络,祛风散寒,行药势,矫味矫臭。所含主要成分乙醇是良好的溶酶,药物经酒制后,有助于有效成分的溶出,而增加疗效。炙药多用黄酒,浸药多用白酒。性味苦寒的药物酒炙可缓和药性,引药上行,如大黄、黄芩、黄柏等;活血化瘀、祛风通络的药物酒炙可协同增效,如当归、川芎。有不良嗅味的药物酒炙可矫嗅去腥,如乌梢蛇、紫河车。酒蒸主要增强药物的补益作用,如女贞子、肉苁蓉等。 2.醋 古时称酢、醯、苦酒,常用米醋。醋性味酸、苦温。具有引药入肝、理气、止血、行水、消肿、解毒、散瘀止痛、矫味矫臭作用。同时醋具酸性,能使药物中所含有的游离生物碱等成分结合成盐,增强溶解度而易煎出有效成分,提高疗效,如醋制延胡索等。药物经醋炙,可引药入肝经,增强疗效,如乳香、三棱醋炙增强活血散瘀止痛作用;柴胡、香附醋炙增强疏肝止痛作用。峻下逐水药醋炙降低毒性,缓和泻下作用,如甘遂、商陆等。树脂类、动物粪便类药物醋炙可矫嗅矫味,如五灵脂、乳香、没药。五味子醋蒸可协同增强酸涩收敛之性。 3.蜂蜜 蜂蜜生则性凉,熟则性温,故能补中。中药炮制常用的是炼蜜,能和药物起协同作用,增强药物疗效,或具解毒、缓和药性、矫味矫臭等作用。如止咳平喘的药物蜜炙增强润肺止咳的作用,如百部、款冬花;补气药甘草、黄芪蜜炙增强补脾益气作用;麻黄蜜炙缓和辛散之性,马兜铃蜜炙缓和苦寒之性,还能矫味免吐等。注意,炮制目的不是单一的,如麻黄、马兜铃蜜炙还可增强润肺止咳的作用。 4.食盐水 食盐性味咸寒,能强筋骨,软坚散结,清热凉血,解毒,防腐,并能矫味。多制成食盐水溶液盐炙使用,可引药入肾经,增强疗效。如杜仲、巴戟天增强补肝肾作用;小茴香、橘核、荔枝核增强理气疗疝作用;知母、黄柏增强滋阴降火作用;益智仁增强缩小便和固精的作用。 5.生姜汁 生姜性味辛、温,升腾发散而走表,能发表散寒,温中止呕,开痰,解毒。药物经姜汁制后能抑制其寒性,增强疗效,降低毒性。厚朴姜炙可缓和副作用,增强宽中和胃的功效;黄连、竹茹姜炙可增强止呕作用,黄连还可缓和苦寒之性。半夏、南星、白附子常用生姜、白矾复制以降低毒性,增强化痰作用。 6.甘草汁 甘草性味甘、平,具补脾益气,清热解毒,祛痰止咳,缓急止痛的作用。药物经甘草汁制后能缓和药性,降低毒性。如甘草汁煮远志、吴茱萸。 7.黑豆汁 黑豆性味甘、平,能活血利水,祛风,解毒,滋补肝肾。药物经黑豆汁制后能增强药物的疗效,降低药物毒性或副作用,如何首乌等。 8.米泔水 又称“米二泔”。能益气除烦,止渴,解毒。对油脂有吸附作用。常用来浸泡含油质较多的药物,如米泔水漂苍术、白术等,可除去部分油质,降低药物辛燥之性,增强补脾和中的作用。 (二)固体辅料 在加辅料炒中,河砂、滑石粉均有中间传热体作用,土、蛤粉既有中间传热体作用,又可协同增效。中间传热体主要是利用辅料的温度使药物受热均匀,质地酥脆,易于粉碎,利于成分煎出。协同增效主要是利用辅料的药性影响药物的作用,如苍术、枳壳麸炒可协同增强健脾燥湿作用。 1.稻米 稻米性味甘、平,能补中益气,健脾和胃,除烦止渴,止泻痢。米炒党参可增强健脾止泻作用;斑蝥、红娘子米炒可降低毒性、矫嗅矫味。 2.麦麸 麦麸性味甘、淡,能和中益脾。与药物共制能缓和药物的燥性,增强疗效。麦麸还能吸附油质,可用来麸炒或麸煨。 3.白矾 白矾性味酸、寒,能解毒,祛痰杀虫,收敛燥湿,防腐。与药物共制,可防止腐烂,降低毒性,增强疗效,如白矾制半夏、天南星等。 4.豆腐 豆腐具有较强的沉淀与吸附作用,与药物共制后可降低其毒性,去除污物,如豆腐煮藤黄、硫黄降低毒性;豆腐煮珍珠洁净药物。 5.土 中药炮制常用的是灶心土、黄土、红土、赤石脂等。灶心土味辛温。能温中和胃,止血,涩肠止泻等。土炒白术、山药、白芍、当归等均可协同增强补脾止泻作用。 6.蛤粉 蛤粉性味咸寒,能清热,利湿化痰,软坚。蛤粉炒阿胶可降低滋腻之性,矫味,增强清热化痰作用。 7.河砂 中药炮制用河砂作中间传热体拌炒药物,主要取其温度高、传热快、受热均匀,可使坚硬的药物经砂炒后质地松脆,以便粉碎和利于煎出有效成分,提高疗效。医学,教育网http://www.med66.com 8.滑石粉 中药炮制用滑石粉炒药物和煨药,如滑石粉炒刺猬皮,滑石粉煨肉豆蔻等。炒制主要是使韧性大的动物药质地变得酥脆,利于粉碎;煨制主要是除去过量的油脂,以消除刺激性,增强止泻作用。
[size=3][font=宋体][/font][/size][size=2][color=#d40a00]维权声明:本文为[font=Times New Roman]hehu2010[/font][font=宋体]原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。[/font][/color][/size] [size=4][b]中药分散片及其辅料的研究进展[/b][/size] 分散片 (dispersible tablets)又称水分散片 (water dispersible tablets),是指遇水可迅速崩解形成均匀黏性混悬液的片剂[l]。随着医药工业的发展 ,西药分散片已经载入各国药典,《英国药典》1980年开始收载阿司匹林等3种分散片。《中国人民共和国药典》2000年版开始收载分散片,但中药分散片在各国药典中并不多见。目前,已有文献报道的中药分散片有绞股蓝总苷分散片[2]黄心分散片[3]、黄芩清肺分散片[4]、葛根黄豆苷元分散片[5] 感冒灵分散片[6]及麝香保心分散片[7]等。2005版《中国人民共和国药典》规定,分散片要求在(20±1) 的 100 ml水中,振摇 3 min,应全部崩解并通过二号筛[8],相对与普通剂型来讲,这样大大提高了药物的生物利用度,并提高老、幼和吞服困难的患者的顺应性。它结合了片剂和液体制剂的优点,并克服两者的不足,这种新剂型不仅服用方便,而且吸收快、生物利用度高、不良反应小,主要要适用于难溶 药物和生物利用度有问题的药物,不适合毒副作用较大、安全系数较低和易溶水的药物。分散片的生产工艺与设备无特殊要求,是一种具有开发前景的新型片剂,近几年已得到迅速发展。现就中药分散片制备过程中遇到的问题作一综述。 1.分散片的处方。 分散片的处方主要组分为药物、一种或多种崩解剂、填充剂、遇水即形成高黏度的溶胀辅料、助流剂、润湿剂等。 1.1药物。由于中药活性成分复杂,且容易吸潮,使药物成团,难以成型,严重影响到片剂的崩解和生物利用度,因此将中药制成分散片,具有较大的技术难度。如果将中药提取分离出有效部位,并进行适当的精制处理,尽可能地减少制剂用量,再通过实验设计筛选出合适 的分散片处方和制备工艺,完全可以制备出美观、符合质量要求的中药分散片。 1.2崩解剂。崩解剂的种类、型号、加入方法 、是否联用等因素均会影响分散片的崩解时限。其中选用优质的崩解剂是最重要的因素之一 。雷同康[9]认为,优质的崩解剂是指吸水溶胀 度大于5mL/g的崩解剂。孔隙率和强溶胀性是这类崩解剂最重要的速崩机理 ,尤其是溶胀性。 当崩懈剂含量约为7 6%时 ,将获得最短的崩解时间 ,此时 ,片剂孔径分布是最合理的细孔结 构 .这种细孔结构的总孔隙溶剂达到饱和,它所产生的压力能导致有效的崩解 溶胀过程成为主要的崩解机理 。但当崩解剂含量超过8%时 ,片剂内部毛细管变粗 ,水的快速渗透反而隔离了周围的细孔结构区 ,使其中的空气不能及时逸出 ,阻止水分进入细 孔区[10]。分散片处方中常用的崩解剂有: 交联羧甲基纤维素钠 (cCMC—Na):cCMC—Na溶胀性强,但不溶于水 ,具有优良的崩解作用[11]。Fererro[12]用水不溶性药物鞣酸蛋白作模型药,系统地研究了cCMC—Na在直接压片中的崩解效率。实验结果表明 ,当其含量为5% ~ 10%,压片压力为 250—280MPa时 ,崩解时问最短 ,仅为十几秒钟。 若处方中没有它,则 30min内部都不会崩解。 羧甲淀粉钠 (CMS-Na):CMS-Na是淀粉经化学修饰的产品,它是淀粉的低取代衍生物,颗粒吸水后能迅速溶胀,但不碎裂,可缩短大多数片剂的崩解时限,其溶胀度为 14.8mL/g,尤其适用于不溶性药物[13,14], 刚臧志等[15]用正交试验筛选了西咪替丁分散片的处方,结果以20%联羧甲淀粉钠、25%改性淀粉、10%微晶纤维素配合使用,崩解效果最佳,为 (70.2±5.16)秒,分散均匀性、混悬性均合格。由此提 ,几种不同的崩解剂联用,将有可能取得优于单种崩解剂更好的崩解效果,所以在方筛选中要注意考虑到这一点。 低取代羟丙纤维素 (LS- HPC):有较强的吸湿性,遇水溶胀而小溶解 ,且具有毛糙的表面结构,可增强药粉和颗粒问的镶嵌作用,提高片剂黏度和光洁度,所以选用LS- HPC为辅 料,能起崩解和黏结双重作用,用量一般为2% ~5%[16,17]。 交联聚乙烯吡咯烷酮 (PPVP):聚乙烯吡咯烷酮 (PVP) 溶于水,吸湿性强 ,溶胀性较弱 ,而 PPVP崩解效果好。外加PPVPxl。具有很高的毛细管活性及水合能力,迅速将水吸入片 中,然后膨胀崩解 ,内加的PPVPxl10吸水使固体颗粒崩解为更细小的粉末从而增加主药 的溶出。 微晶纤维素(MCC):是目前应用最广的一种辅料,它具有海绵状的多孔管状结构。受压时,MCC的多孔结构由杂乱无事而成为线性排列 ,再加之塑性变形,使MCC遇水后,水分子 进入片剂内部,破坏微品之间的氧键,促使片剂速崩。 MCC可压性好,适合于直按压片法。 由于它溶胀性很弱,一般不单独用作崩解剂,往往和其他溶胀性能强的辅料如LS- HPC联合 使 用[18]。 1.3填充剂。 乳糖:是一种优 良的填充剂 ,在压片过程即使压力稍有变化,也不至于影响片剂的硬度,片重差异变化小,较少出现黏冲、脱片等现象。成品光洁美观,有良好的药物溶出速率。中药分散片中如果原料药黏性较差,可考虑使用乳糖作填充剂。但黏性较强的原料药不宜使用乳糖[19],因其有可能影响崩解度。 硫酸钙(二水物):不溶于水,无引湿性,对油类有极强的吸附能力,可广泛用作对水敏感的药物填充剂,中药分散片中如原料药的黏性较强,可考虑使用硫酸钙作填充剂[19]。其他如山梨醇、微晶纤维索、甘露醇,麦芽糊精等均可考虑使用。 1.4溶胀性辅料 溶胀性辅料对分散片这一剂型间接地起到促进崩解的作用。常用以下品种:预凝胶淀粉。预 凝胶淀粉是将普通淀粉在高于糊化温度 (45℃)下处理 ,使淀粉吸水膨胀,破坏分子之间氧 键甚至破坏淀粉颗粒,然后升温,待糊化完伞后,经于燥压制成薄膜, 粉碎而得。其具有良好的流动性、可压性、崩解性和自我润滑性[20]。 海藻酸钠:海藻酸钠溶于水而形成粘稠的胶体溶液,其黏度随聚合度、浓度及pH值而异,pH5~10时黏度最大[21]。另外,还可采用瓜耳胶、苍耳胶、葡聚糖、多糖类、亲水性纤维素衍生物 (如羧甲基纤维素钙、羟丙 基纤维素或羟丙基甲基纤维素等)。 1.5 其它辅料 其它辅料包括表面活性剂、助流剂、亲水性润滑剂等 ,它们的加入将有助于提高分散片的质量 。较常用的表面活性剂 是十二烷基硫酸钠 (SLS)[16,22],溶于黏合剂中使用 ,效果最好,可显著促进片剂崩解和药物溶解 。此外,也有用磺基丁二酸二辛酯钠的[23]。 分散片中广泛采用微粉硅胶[24]为助流剂 ,无论在制粒压片或粉末直接压片中都有利于改善颗 粒或粉末的流动性 。 同时 ,由于它的强极性和亲水性 ,有利于水分透入片剂 ,加速片剂的崩解,同时硅醇基吸附药物后能显著提高难溶性药物的溶出速率[25]。 由于崩解剂为不溶性物质.崩解后口感似沙砾,为克服这一缺点。常用甘露醇为填充剂,可以改善口感。
DNA编码化合物库(DNA Encoded compound Library,简称DEL)合成与筛选的概念是美国Scripps 研究院的Sydney Brenner(2002年诺贝尔生理学及医学奖获得者)和 Richard Lerner(时任 Scripps 研究所所长)于1992年提出并申请了发明专利。具体地,组合化学的优势是可以快速地产生巨大数量的化合物汇合体,但在筛选过程中无法得知起作用的化合物信息。如果将一个具体的化合物与一段独特序列的DNA在分子水平连接(即对小分子化合物进行DNA编码),在筛选完成后,通过高通量DNA测序仪对筛选出小分子独特的DNA序列进行识别,从而解决由组合化学产生的巨型化合物库无法用于筛选的问题。中文名 DAN编码分子库药物筛选技术背景:药物筛选包括传统高通量药物筛选和DNA编码分子库药物筛选等,分子库是药物靶点筛选的起点和支撑。DNA编码分子库药物筛选技术在近5-7年内逐渐发展起来,已经成为创新药研发中的一种较为成熟的新兴前沿技术,并走出大学实验室,得到各大药物公司的广泛接受,在实际创新药研发中起着越来越重要的作用。已经在香港大学化学系李笑宇教授课题组完成了深入的研究工作,并取得了良好的成果。该技术的基本路线、参数已经成熟,不再需要进行验证研究,可以直接用于实际的药物筛选。李笑宇课题组曾经和拜耳、默克等世界知名药企进行过合作,并将该DNA编码分子库方法应用于实际的药物研发中,针对一些重要的恶性肿瘤的药物靶点,成功地筛选出了一系列高活性的药物候选化合物。这些实际应用充分验证了该技术的可行性、适用性和成熟性。取得发明专利。技术优势:(在李笑宇教授与拜耳的合作中已得到验证):1、大幅提高成功概率 2、大幅降低研发成本 3、大幅缩短研发周期主要工艺范畴为这些领域所包含的化学合成工艺、蛋白质表达与表征、DNA的固相自动合成与纯化、细胞间操作工艺,以及一些DNA测序的样品处理工艺等。本项目的各个技术环节均已经较为成熟,在多年中和各个大型制药企业的合作中已经得到了充分的验证。下一步将在实践中,进一步将技术细节、工艺流程等方面标准化、自动化,以提高分子库合成与筛选的效率。技术对比:传统高通量药物筛选:分子库数量有限,主要筛选中心:5-6 百万化合物 二十年以上的积累 价格非常昂贵,分子库的维护极为复杂。筛选周期长 (6-12个月/靶点); 高通量筛选在新药研发中需求巨大,但是在实际应用中却存在巨大的壁垒。DAN编码分子库药物筛选:超高通量 (千万~千亿级),分子库可以随时构建:百万级/月; 价格适中,分子库的维护极为简单:一个 -80°C 冰箱; 筛选周期短:1 天/靶点; 低门槛:无需任何特殊仪器设备。市场概括:DNA编码分子库的报道:国际DNA-encoded化学库研讨会每两年在瑞士举行一次 。第四届在2014年召开时,仅有英国葛兰素史克、瑞士罗氏、丹麦vipergen、丹麦Nuevolution、美国百时美施贵宝、瑞士Philochem、美国辉瑞、美国X-CHEM等大公司参加 。第五届将于2016年8月26日召开,国际知名公司:强生、辉瑞制药、诺华、赛诺菲、罗氏、默沙东、葛兰素史克、拜耳、 安进、阿斯利康、礼来、雅培、艾伯维、美敦力、百时美施贵宝、梯瓦、利洁时、武田、百特、吉利德、默克雪兰诺、赛默飞世尔科技、诺和诺德、柯惠医疗等均已报名参加同类公司对比:1.葛兰素史克 (GSK) :GSK在约10年前收购美国波士顿的Praecis公司的DNA编码分子库技术平台之后,一直致力于将本技术在药物研发中的应用。GSK在本领域的的技术为传统的组合化学的split-mix-split方法与酶连标记相结合。他们的分子库的特点为数目极大,为几十亿量级。分子库所筛选的靶点也种类繁多,涵盖了基本上所有的疾病类型。然而,GSK多年以来分子库虽然化合物数目巨大,但是化学结构上只有一种类型:三嗪类杂环化合物。因此较大的限制了GSK分子库的应用。2.Ensemble Therapeutics: 该公司与2002年开始运行,在美国波士顿,由哈佛大学的David Liu教授所创立。Ensemble使用DNA模板控制技术来合成分子库,主要集中在大环多肽分子库,数目并不大,每一个库大约5万个化合物,至今构建了大约几十万个大环多肽。Ensemble和罗氏、辉瑞、GSK、施贵宝都有过或是正在有药物研发合作。但是Ensemble公开的信息不多,所进行的药物筛选基本集中在癌症靶点。3.X-Chem: 同样位于美国波士顿。X-hem的分子库合成技术与GSK类似,但采取化学连接而不是酶连来进行分子库中的编码。X-Chem的分子库的数目更大,据报道已经达到了上万亿个化合物的级别。然而,从公开的数据来看,X-Chem分子库的化合物仍然集中在易合成的肽类、杂环,或是两者结合的结构类型。X-Chem和多个大型药企都有筛选的合作。4.DiCE Molecule: 位于美国加州,由斯坦福大型的Pehr Harbury教授刚刚创立。DiCE的技术主要在于将DNA编码分子库和微流控、自动化结合起来。由于该公司刚刚成立,信息非常少。从Harbury教授发表的论文来看,分子库基本上都是多肽,化合物数量在几十万左右。5.Vipergen:位于丹麦哥本哈根。该公司利用DNA分子自组装来合成分子库的技术。虽然该公司成立了近10年,但是公开信息也较少。大部分分子库也是多肽类化合物,并和若干大药企建立了筛选合作。6.NuEvolution:同样位于丹麦哥本哈根,发展历史和Vipergen非常类似。即基于一种专利技术,进行分子库的合成,同大药企进行合作。NuEvolution也是做大型分子库的公司,分子库数量在几十亿量级。7.Philochem:位于瑞士苏黎世,为瑞士联邦理工学院Dario Neri教授创立。Philochem在本领域中比较特殊,他们用DNA编码分子库做fragment-based drug discovery,即基于碎片的药物发现。Philochem公开的信息也较少,从文献和专利来看,他们研究的方向非常的集中,主要在1-2个癌症靶点上,并且很少和大药企进行合作。2015年药物筛选市场份额 国内:70~105亿人民币 国际:80~120亿美元基于DNA编码分子库的药物筛选占有药物筛选市场的10%左右,预计保持100%的平均年复合增长率。
[b] 2017年中国药科大学药用辅料及仿创药物研发评价中心招聘启事[/b] 中国药科大学位于江苏省南京市,为教育部直属、国家“211工程”重点建设高校,是一所历史悠久、特色鲜明、在药学界享有盛誉的全国重点大学。为提升我国制药行业整体水平,保障药品安全性和有效性,加快科研成果向企业转化速度,中国药科大学于2016年9月成立中国药科大学药用辅料及仿创药物研发评价中心,主要致力于药用辅料、创新型药物、高端制剂的研究开发和药品一致性评价研究,因中心发展需要,现公开招聘[b]药分项目负责人[/b]、[b]研发QA[/b]各一人。一、岗位性质 非事业编制人事代理二、工作地点 中国药科大学玄武校区三、岗位要求 从事药物分析相关工作三年以上四、简历投递 请将应聘材料发送至邮箱yleicpu@126.com

[font=Times New Roman][size=4][b]药物筛选[/b]是现代[color=#ba0000]药物开发[/color]流程中检验和获取具有特定生理活性化合物的一个步骤,系指通过规范化的实验手段从大量化合物或者新化合物中选择对某一特定作用靶点具有较高活性的化合物的过程。药物筛选的过程从本质上讲就是对化合物进行[color=#ba0000]药理活性[/color][color=#002bb8]实验[/color]的过程,随着药物开发技术的发展,对新化合物的生理活性实验从早期的验证性实验,逐渐转变为筛选性实验,即所谓的药物筛选。作为筛选,需要对不同化合物的生理活性做横向比较,因此药物筛选的实验方案需具有标准化和定量化的特点。随着[color=#002bb8]组合化学[/color]和[color=#002bb8]计算化学[/color]的发展,人们开始有能力在短时间内大规模合成和分离多种化合物,因而在现代新药开发流程中药物筛选逐渐成为发现先导化合物的主要途径之一。[/size][/font][align=center][img]http://ng1.17img.cn/bbsfiles/images/2010/06/201006171011_225210_1623423_3.jpg[/img][/align]
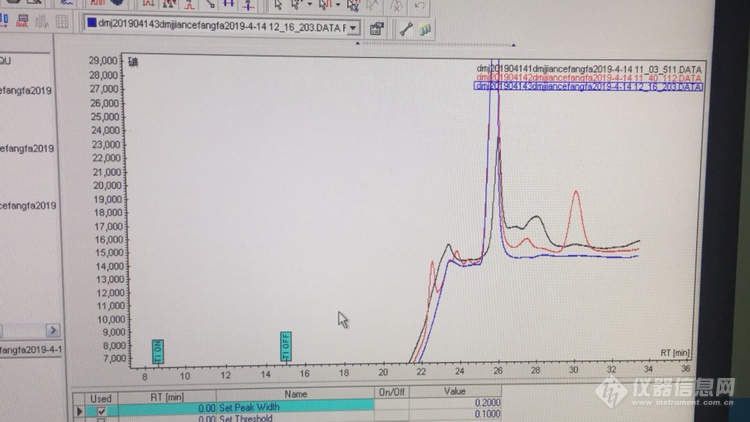
希望各位大神多多指教!我检测的物质是二十八烷醇但是,我的辅料跟它同时出峰,我用的0.53的柱子,柱流速为1ml/min,色谱柱条件为180摄氏度保持3min,8摄氏度/min,升至230,保持10min;10摄氏度/min升至270,保持10min。三个色谱图分别是阴性溶液、片剂、对照。[img=,690,388]https://ng1.17img.cn/bbsfiles/images/2019/05/201905060949146802_2632_1823055_3.png!w690x388.jpg[/img][img=,690,388]https://ng1.17img.cn/bbsfiles/images/2019/05/201905060949146802_2632_1823055_3.png!w690x388.jpg[/img]
最近做一种胶囊的药物分析,测定药效成分含量,我老师让我检测之前先把胶囊里的辅料去除掉,他怕辅料对药效成分检测产生干扰,并对除辅料的条件进行单因素优化。我想问的是,有必要去除辅料吗?辅料去除过程中,药效成分肯定也有损失,这样检测出来的结果就不是此药物实际的结果,也就没有意义。我这样想对吗?
药品中大多数都是辅料,各个辅料在药品中充当着不同的角色,最常用的辅料有哪些呢?其在成药中扮演着什么角色呢?欢迎讨论!回帖格式如下:=============================药品名1:剂型:辅料:各辅料性质及作用:是否可被其他辅料替换:=============================药品名2:剂型:辅料:各辅料性质及作用:是否可被其他辅料替换:=============================药品名3:剂型:辅料:各辅料性质及作用:是否可被其他辅料替换:...=============================
来源:医药经济报 药用辅料界的全球变革进程越来越快。在前不久国际药用辅料协会(IPEC)召开的2007年研讨会上,除了一如既往地强调辅料的重要作用之外,“监管”、“规范”以更高的频率被提及。 研讨会的中心议题是“药用辅料供应商与大型制药公司之间必须更加紧密地合作来共同降低药品生产成本、推动制药技术创新,同时要尽快融入新的辅料监管环境”。围绕这一中心议题,研讨会重点探讨了药用辅料安全性、辅料新规定的影响以及当前主要市场辅料监管状况。而围绕这三项内容进行的变革,将影响到2007年全球辅料行业的发展进程。 加强生产过程的安全性 近年来,制药公司一直在锲而不舍地寻找药物的新剂型及规格,以确保这些新剂型的临床治疗作用不会打折扣。同时,随着市场需求不断增加、生命健康产业规模的壮大,制药行业自身也存在往更深层次、更大范围发展的要求,因此,开发新辅料、规范辅料行业变得越来越迫切。国际药用辅料协会一直在呼吁全球主要的辅料生产地区加强监管,前不久还来到中国敦促成立相关工作机构以加强对中国辅料行业的监督。 如今,欧洲已经开始实施药用辅料的GMP生产质量管理规范,要求辅料生产商必须按照GMP规范来生产。欧洲业内人士认为,之所以实行药用辅料GMP规范,是为了用更高的安全标准来提高药物使用的安全性,除此之外,进行适当的监管不仅可以提高欧洲厂家的竞争力,对世界各地的药用辅料生产商来说也可以起到带动作用。 欧洲业内人士还指出,生产商乃至整个欧洲药用辅料领域需要一段时间来适应GMP规范,当下要做的应该是想办法避免新规定的出台给辅料供应商们增加不必要的负担。实际上,国际药用辅料协会已经提供了专门针对药用辅料的GMP指南,这份可操作的权威性文件不仅能帮助辅料生产商达到日益严格的要求,而且为制药公司与辅料生产商之间的合作提供了法规上的约束和帮助,以确保所使用辅料的安全性。 考验制药公司的杂质问题 对药用辅料生产商来说,除了要对GMP有所心理准备之外,还将面临涉及生产过程中的一项新规定:药品中基因毒性杂质的含量应控制在可接受的限值水平之内。根据新规定,当人们每天摄入的基因毒性杂质的TTC值(即毒性物质限量)低于1.5微克时,这种基因毒性杂质的水平可以被接受;在某些情况下(比如短期接触时),较高的TTC值也许仍然可以被接受。 有业内人士认为,这对药用辅料生产商来说绝对是一大挑战,说不定还将成为行业优胜劣汰的重要参数之一。 《基因毒性杂质限制指南》已于今年1月1日起开始实施。虽然它并非专门针对药用辅料,但监管部门在审批新药上市之前,将会将根据这条新规定来对药用辅料中的基因毒性杂质进行毒理学评价。 由于辅料的常规合成过程只有在使用反应材料的提前下才能得以实施,而这些反应材料具有潜在的基因毒性,在某些情况下,辅料中存在基因毒性杂质也就不可避免。《基因毒性杂质限制指南》的主要起草人在这次IPEC研讨会上表示:“在制药行业,有相当比例的合成产品可能含有基因毒性杂质,这自然成为一个较大的监管问题,同时也是关系到人体健康的一个问题。要对这种基因毒性杂质的危害进行定量的分析难度很大,《指南》可以为评价基因毒性杂质提供较清楚明了的参考。” 而如果制药公司从一开始就意识到了基因毒性杂质的重要性,它们也就会相应地提高处理这一问题的技术水平。至于新规定是否将给制药公司增加负担,《基因毒性杂质限制指南》主要起草人的态度是乐观的,“不认为这一新的指南将会对制药公司的经营业绩产生负面的影响”。 积极作用慢慢显现 有一种观点认为,在新法规出台后,不可避免地将减少当前使用的辅料的种类。不过,也有另一种持反对态度的观点认为,药用辅料的质量、规格等将由此得到更大程度的提高以及扩展,已经有许多制药公司正在研究《指南》,并与辅料生产商展开了比从前更深层次、更大范围的合作与交流。 业内人士认为,这种制药公司和辅料生产商合作新貌的出现具有积极的意义,一个显而易见的结果就是可以改变药品生产中的大量资源浪费的诟病。一直以来,制药行业的生产要素并没有得到持续改进和优化,久而久之导致在生产某些产品时的浪费现象高达50%,设备利用率甚至低到了15%;然而,大多数制药公司消耗在生产上的费用占到了全部费用的25%,几乎与研发费用的投入持平。可以说,虽然制药公司生产出了合格的高质量产品,但却是付出了高昂的代价取得的。制药行业的创新成果正在减少,运行成本却在不断上升,因此,大量资源浪费与这种背景所形成的矛盾将日渐深刻。《指南》一旦能够在制药企业和辅料生产商之间成功地发挥出作用,必将有助于更合理配置制药资源,优化行业结构。 业内人士还对前景进行了展望:“随着对剂型、关键性产品、生产要素和质量特性的理解加深,贯彻好Q8(制剂开发)、Q9(风险管理)和Q10(质量体系指南)等文件,与此同时生产出新型药用辅料,从而取得更好的生产结果,为病人提供更加有效的药品。” 欧洲需要向日美看齐 到目前为止,欧洲虽然规定制药公司必须提交制剂、原料药的主文件,但对药用辅料却没有作出这样的硬性规定。国际药用辅料协会欧洲监管事务委员会主席Carl Mroz提到了日本的作法。日本近来修改了1948年制定的药事法,要求制药公司必须向监管部门提交药物的辅料主文件(EMF)。 Carl Mroz认为欧洲也应该推行这种做法,因为欧洲一向缺乏辅料主文件的管理漏洞已经引起了行业的热论。Carl Mroz在研讨会上声讨了这种弊端:“我们希望建立一种机制,让新型辅料以更快的速度进入欧洲市场。不推出新的辅料,制药公司的创新激情就会泯灭。试问,如果制药公司打算开发含有新型辅料的新给药系统,却由于缺乏这种新辅料的相关数据的支持和参考,相信有再伟大的设想也不敢贸然着手开发的。在一定程度上,这已经阻碍了欧洲开发新辅料、新药物的进程。” Carl Mroz称,日本和美国已经推行了EMF模式,欧洲为了保持其制药的综合实力,未来能在向中国、俄罗斯这样的新兴药物市场占据一席之地,应该尽快地推行辅料EMF模式。 可以明显感觉到,近几年全球辅料行业有一股以监管为主要变革力量的潜流在涌动着。一方面,全球新药研发后继乏力使得一部分研发注意力转向发掘药用辅料;另一方面,制药领域内生性发展要求使得对药用辅料行业的监管日渐严格。在今后的若干年里,“迎头赶上”将是药用辅料行业发展的精神状态。
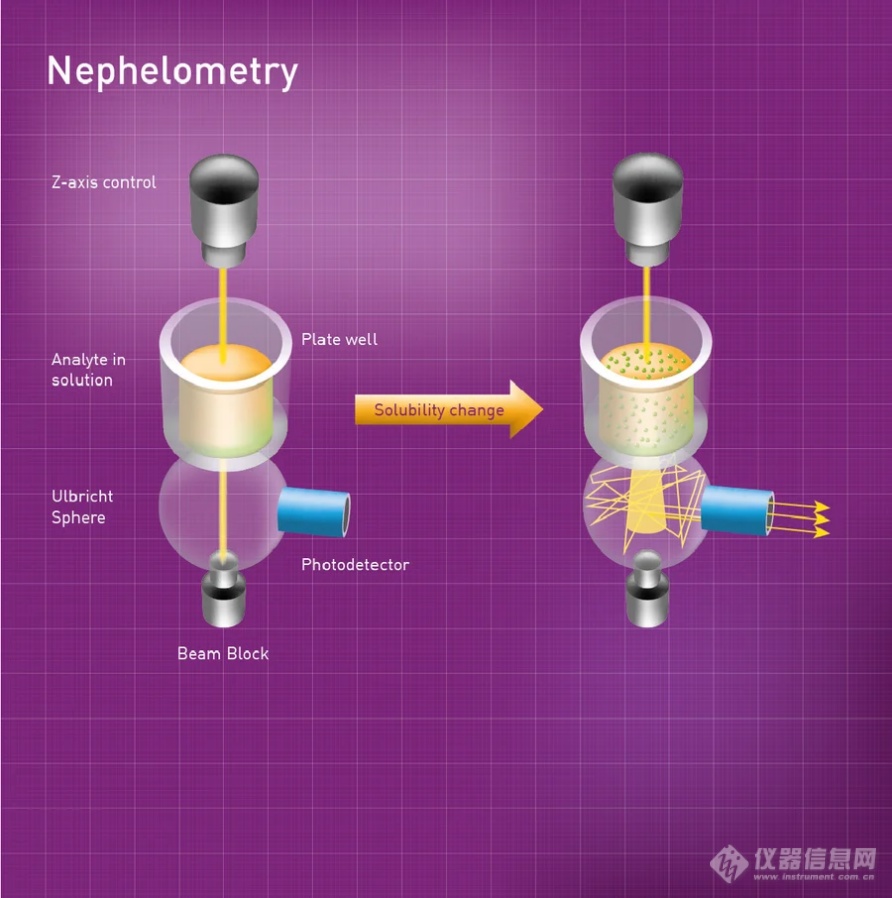
在药物开发过程早期进行ADMET(吸收、分布、代谢、排泄和毒性)评估的能力在当今的药物发现环境中是至关重要的。这意味着需要进行高通量分析,以尽早发现潜在的ADMET问题,从而减少损耗。溶解度是药物的关键特性之一,对分析方法开发、药物生物利用度、吸收和毒性研究,以及药物剂量和药物配方都有重要影响。低溶解度化合物的开发难度更大,获得可再现的ADMET筛选数据也更费时费力。因此,在药物开发的后期阶段进行成本更高的检测之前,研究人员需要一种快速、经济高效的解决方案来确定溶解度。[align=left][b]药物溶解度研究[/b][/align]药物溶解度研究旨在评估药物在不同条件下,在各种溶剂或缓冲液中的溶解度。通常需要测量药物在特定温度或pH值下可溶解的量。溶解度通常表示为药物在溶剂中的最大溶解浓度,也称为饱和浓度。药物溶解度测定在药物发现过程中的不同阶段都至关重要。在早期化学筛选的所有标准中,不理想的溶解度是最不利的性质之一,溶解度低的分子具有很高的失败风险。因此,在药物发现过程中要尽早进行溶解度测定。低溶解度不仅会阻碍新药活性的测试,还可能引发其他不良后果,包括影响其他检测、隐藏其他不良特性,以及对药物动力学和动态性质的潜在影响。总之,这可能会导致药物开发时间大大延迟,或者在尝试改良之前就出现失败。常见的平衡溶解度测定的方法是在恒温条件下将药物和靶标一起振荡至少24小时并测量溶液中的药物浓度(摇瓶法;图 2)。最终浓度通常通过高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法测定,整个过程耗时较长,且通量较低。[b]散射比浊法节省时间并提高通量[/b]散射比浊法是一种快速、可扩展、灵敏且精确的颗粒物质浓度测定方法,有利于药物溶解度研究。另外,这还是一种无损技术,可用于动力学分析,只需制备很少的样品,且可以适应高通量微孔板格式。[url=https://www.bmglabtech.cn/]BMG LABTECH[/url]的NEPHELOstar [i]Plus[/i]是一种专用的微孔板散射浊度仪,可通过测量前向散射光来检测液体样品中的不溶性颗粒。这种方法基于对样品中不溶性颗粒散射光强度的检测。NEPHELOstar [i]Plus[/i]的高强度光源是波长为635 nm的激光。激光穿过样品孔,进入Ulbricht球散射光检测器。如果光线没有被颗粒偏转,会直接穿过球体,不会产生信号。如果样品中存在不溶颗粒,散射光会在球体内部反射,被光电二极管检测到。Ulbricht球可收集散射角度高达 80 度的光线。[align=left][b]结论[/b]散射比浊法是一种快速、可靠、低成本的溶解度筛选方法,可利用384孔板进行高通量筛选。使用NEPHELOstar [i]Plus[/i] 在384孔板中进行全自动动力学溶解度筛选,可在75分钟内分析24种化合物,批间差异率为5%。在提交的化合物中,其中约有90%的化合物,其动力学溶解度可通过此方法得出并排序。[/align]
药物活性筛选仪的房间设计方案?谁有理想的药物活性筛选仪房间设计方案?
通量药物筛选技术都有哪些呢?
药物活性筛选仪的房间设计方案?谁有理想的药物活性筛选仪房间设计方案?
药物活性筛选仪的房间设计方案?谁有理想的药物活性筛选仪房间设计方案?
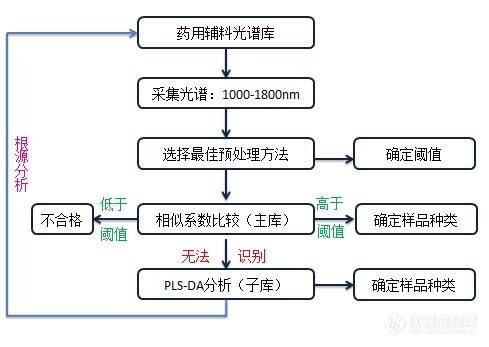
[align=center][b]sup-NIR分析仪在药用辅料快速识别体系建立中的应用研究[/b][/align][align=center]研究生:孙巧凤[/align][align=center]导师:臧恒昌教授[/align][b]摘要目的:[/b]药用原辅料是药品生产过程中的基础物质,也是药品质量的关键影响因素。我国药品生产质量管理规范要求采取核对或检验等适当的措施,确认每一包装内的原辅料正确无误,给制药企业带来了巨大的挑战。近几年国家提出了实行药品与药用原辅料和包装材料关联审批,在政策放宽的情况下,如何低成本、准确而快速的监管原辅料是一个十分关键的问题。欧盟的近红外草案规定当近红外方法应用于原辅料的放行时,可以被称为主要方法,这说明[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]分析技术对于原辅料质量快速评价具有强有力的优势。通过对药用原辅料建立[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]快速分析体系,将有效的推动国产[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱仪[/color][/url]服务于药品生产行业,为广大人民群众的用药安全提供保障。[b]方法:[/b]本实验采用sup-NIR1520对17种不同的药用辅料进行光谱采集,并利用化学计量学方法建立了辅料的快速识别体系,药用辅料数据库建立的方法主要利用光谱间的相关系数值以及偏最小二乘判别分析定性分析方法,数据库的验证结果证明了sup-NIR分析仪在药用辅料定性方面应用的可行性。在建立的PLS-DA模型中发现此仪器不仅可以用于不同种药用辅料之间的快速识别,还可以应用于同种辅料不同型号的样品快速识别。[b]关键词:[/b][url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]分析技术;sup-NIR分析仪;药用原辅料[align=center]Research on the establishment of rapid identification systemof pharmaceutical excipients with sup-NIR analyzer[/align][align=center]Graduatestudent: Qiaofeng Sun[/align][align=center] Supervisor: Hengchang Zang[/align][align=left][b]Abstract Objective[/b]: Pharmaceutical excipients and raw materials arethe basic substances in the production of drugs, and they are the keyinfluencing factors of quality of medicine. GMP requires that appropriatemeasures should be taken to confirm that the materials in each package arecorrect, which has brought great challenges to the pharmaceutical companies. Inrecent years, The State has proposed the associated examination and approval ofdrugs and pharmaceutical excipients and raw materials and packaging materials.Under such circumstances, how to supervise raw and excipients materialsaccurately, quickly is a key technical issue. How to supervise the rawmaterials and excipients with low cost, accurate and fast is a key issue. TheEU's near-infrared draft stipulates that when near-infrared methods are appliedto the release of raw materials and excipients, it can be called the mainmethod, which indicates that NIRS has strong advantages for the qualityevaluation of raw materials and excipients. The establishment of a rapidanalysis system for near-infrared spectroscopy of pharmaceutical raw materialsand excipients will effectively promote domestic portable near-infraredspectrometers to serve the pharmaceutical industry and provide security for thepeople's drug safety. [b]Methods:[/b]In this experiment, 17 kinds of different pharmaceuticalexcipients were collected by sup-NIR1520, and rapid identification database forexcipients was established by chemometrics methods. The method of building thedatabase mainly used the correlation coefficient values and the PLS-DAqualitative analysis method, and the validation results of the database provedthe feasibility of the sup-NIR analyzer in the qualitative application ofpharmaceutical excipients. From the PLS-DA models, it was found that thisinstrument can be used not only for fast identification among differentpharmaceutical excipients, but also for the same kind of excipients ofdifferent types.[/align][align=left][b]Key words:[/b] Near infraredspectroscopy sup-NIR analyzer pharmaceutical excipients and raw materials[/align][b]1 材料1.1 仪器与软件[/b]Sup- NIR1520型[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]分析仪(聚光科技有限公司)工作温度是5-35 ℃,工作湿度是(5-85)%,工作压力为(86-116)kPa;采用带TEC温控系统的InGaAs检测器;光纤漫反射探头;参比盒;RIMP光谱采集及处理软件;MATLAB 2015a数据处理软件。[b]1.2 样品[/b]17种药用辅料均为药厂生产中使用的辅料,质量均符合药典规定标准。17种药用辅料,每种10个批次,共170批样品。[b]2 方法2.1[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]的采集[/b]样品不经预处理,室温条件为20-25 ℃,采用光纤漫反射探头直接采集样品光谱,不同位置重复采集3次光谱,取平均;波长范围为1000-1800nm;扫描次数30次;分辨率为11 nm;以白板作为参比。[b]2.2 辅料识别体系的建立[/b]利用每种辅料7张光谱的内部相关系数确定每种辅料的阈值,以此相关系数阈值为辅料一级识别体系的判断依据,对验证集进行预测,依据相关系数的阈值判断样品的归属,归属多个种类的利用PLS-DA继续分析。建立辅料识别体系的主要策略如图2-1:[align=center][img=,489,347]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251725504841_7871_3389662_3.png!w489x347.jpg[/img][/align][align=center]图2-1 辅料识别体系技术路线图[/align][align=center]2.3样品集的划分[/align]采用Kennard-Stone method(KS法)分别将17种辅料划分为校正集和验证集,其中每种辅料取7个批次作为校正集,3个批次作为辅料识别体系的验证样品,即119个样品为校正集,51个样品作为验证集;其中校正集中,每类辅料的7个光谱取平均作为辅料识别体系的标准图谱。2.4 一级识别体系的建立[b][/b]2.4.1预处理方法的选择本研究考察了标准归一化法、多元散射校正、一阶导数、二阶导数,并根据识别体系的识别率和拒绝率确定最佳预处理方法。[b][/b]2.4.2阈值的确立根据每种辅料的内部相关系数值大小确定此种辅料的阈值,主要规则如下:若同类别的相关系数均大于0.97,为了增大识别体系的准确率,以不同种类间的一般阈值0.97为此类辅料的阈值;若辅料内部出现小于0.97的相关系数值,则以最小值作为此类辅料的判别阈值。[b][/b]2.4.3 结果分析一级识别体系主要是以相关系数值作为判断标准,将17张标准图谱作为一级识别体系的基础,以每种辅料的阈值作为体系的判断种类归属的依据。验证样品首先与标准图谱计算相关系数进行初步判断。[b][/b]2.5二级识别体系的建立某些辅料因结构相似等因素干扰导致无法直接用一级识别体系直接正确判断,存在一个以上大于阈值的相关系数值,则将所有大于阈值的辅料的7张原始光谱导出与内部的3个验证样品进行PLS-DA定性分析并最终归类。并将其建立成PLS-DA判别分析的二级识别体系。[b][/b]2.6识别体系的外部验证按照建立识别体系时相同的方法采集得到外部验证样品光谱,利用外部验证集对辅料识别体系的准确性进行验证,观察该数据库对于外来样品的识别和拒绝情况。[b][/b]3实验结果3.1 样品的原始光谱采用sup-NIR1520光谱仪采集的170批药用辅料的原始光谱图如图2-2所示. 由原始光谱图可以看出不同的辅料光谱之间是存在差异的但同时也存在光谱的重叠。所以需要借助化学计量学方法对其进行光谱矩阵进行数据运算。[align=center][img=,491,240]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251736087373_5680_3389662_3.png!w491x240.jpg[/img][/align][align=center]图2-2 辅料样品的原始光谱图[/align][b]3.2 样品集的划分结果[/b]将样品划分为119个校正集和51个验证集,划分结果见表2-1。校正集119个样品中包括17种样品,每种样品7张光谱,其原始光谱如图2-3-a所示。同样验证集样品包括17种辅料,每种3张验证光谱,其原始光谱如图2-3-b。将119张光谱每7张取平均,每种样品保留一张平均后的光谱作为一级识别体系的标准谱图。标准谱图如图2-4所示。[align=center][img=,575,542]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251736463497_6475_3389662_3.png!w575x542.jpg[/img][/align][align=center][img=,517,297]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251737193350_8509_3389662_3.png!w517x297.jpg[/img][/align]3.3 一级识别体系的建立[b][/b]3.3.1 预处理方法的选择结果样品辅料均为固体粉末,其颗粒大小的不规则性可能会因为影响光程而引入噪音,除此之外,还包括仪器、人为等因素带来的干扰,会使[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]包含一些非样品自身性质的无关信息,为了减少或消除其他因素带来的干扰,采用化学计量学方法对光谱数据进行预处理。首先考察了SNV与MSC预处理方法对光谱矩阵相关系数的影响,具体结果如表2-2所示,由表中数据可知,随机挑出三种辅料的光谱经过SNV和MSC预处理后,三种辅料内部的相关系数以及与验证集的相关系数均不变,通过计算得知这两种预处理方法对于相关系数的影响不大,因此其他辅料没有进行SNV和MSC预处理的考察。导数预处理可以去除基线漂移和背景的干扰,放大光谱间的差异,本研究考察了FD、SD以及不同的平滑窗口宽度对于识别体系识别率与拒绝率的影响,选出最佳的预处理方法以及最佳平滑窗口宽度。识别体系对于自身样品的识别率均为100 %,而拒绝率经过不同的预处理后结果不同,整体考虑FD预处理后的拒绝率最高,因此选择FD作为光谱的最佳预处理方法。由于导数运算的同时会增大噪声的影响,因此应同时进行平滑处理,而不同的窗口宽度产生的平滑效果不同,本研究同时考察了不同窗口宽度的平滑效果,以17种辅料综合考虑来看,当平滑窗口宽度为13时,数据库的识别率和拒绝率最大,因此选FD+SG 13点平滑为最佳预处理方法。[b][/b]3.3.2 阈值的确立本研究是以光谱矩阵中的相关系数值为判断指标,因此每种辅料内部的相关系数阈值的确定十分重要,为了确保阈值的准确可靠,我们用以下两种规则确定阈值:若同类别的相关系数均大于0.97,为了增加识别体系的准确率,以不同种类间的一般阈值0.97为此类辅料的阈值,以甘露醇类辅料为例,如表2-2所示,甘露醇类内的相关系数值均大于0.98,为保证识别体系的验证准确率,以0.97为此类辅料的阈值,相同情况的其他种类的辅料均以0.97为阈值;若辅料内部出现小于0.97的相关系数值,则以最小值作为此类辅料的判别阈值。以十二烷基硫酸钠为例,如表2-3所示为十二烷基硫酸钠相关系数结果,此时阈值选为0.96。相同情况的其他辅料均以最小值为阈值。根据以上两种原则计算出的所有辅料的阈值见表2-4。[align=center][img=,608,428]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251738094300_1550_3389662_3.png!w608x428.jpg[/img][/align][align=center][img=,582,264]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251738082012_8458_3389662_3.png!w582x264.jpg[/img][/align]3.3.3 结果分析将辅料的标准谱图以及验证集样品光谱图经FD+SG 13点平滑预处理,根据2.4中的阈值进行一级识别体系的判别,经过预处理后的谱图见图2-5,计算预处理后的验证集样品与17种辅料的标准谱图之间的相关系数,根据阈值进行辅料种类的归属,此时的验证属于库内验证。一级识别体系的验证存在两种情况,一种是仅有一个相关系数值大于阈值此时可以正确归属该辅料,如图2-6所示为第4个验证样品与17种辅料的相关系数值,横坐标为辅料的编号,纵坐标为相关系数值。从图中看出此验证样品仅与第四个辅料之间的相关系数大于阈值,因此可将其正确的归类为第四种辅料甘露醇。另一种情况是同时出现多个两个或以上的数值大于阈值,此时会出现辅料归属的不确定性。如图2-7所示,第25个验证样品同时与硬脂酸镁和十二烷基硫酸钠相匹配,一级识别体系无法正确判断,应进一步分析。其他验证样品利用相同的原理进行验证。最终的验证结果显示,微晶纤维素类样品PH101、PH102,淀粉类样品糊精、CMS、预胶化淀粉及玉米淀粉,硬脂酸镁及十二烷基硫酸钠三大类样品间因其结构相似无法正确判断,而除此之外的其他样品均能成功识别和拒绝。因此需根据上述三类样品建立PLS-DA定性分析模型,作为识别体系的子库。[align=center][img=,538,603]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251739356596_6435_3389662_3.png!w538x603.jpg[/img][/align][align=center][img=,501,294]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251739346185_9267_3389662_3.png!w501x294.jpg[/img][/align][b]3.4二级识别体系的建立[/b]二级子库的建立是为了将一级识别体系识别中不确定种类的的样品进行进一步的定性分析,子库的建立采用的是PLS-DA定性分析方法。由一级识别体系的验证结果可知共有三大类的样品由于结构相似相关系数值无法正确区分,现根据上述情况建立了三个独立的PLS-DA模型作为一级识别体系的补充。[b]3.4.1淀粉类样品PLS-DA模型的建立[/b]首先将一级识别体系中的玉米淀粉、糊精、预胶化淀粉、CMS的28张原始光谱调出作为定性模型的校正集,将一级识别体系验证集中易混淆的12个样品挑出作为模型的验证集。用上述40个批次的样品建立模型。利用原始光谱建立的PLS-DA模型如图2-8所示,图中后半部分为验证样品,校正集和验证集的识别率拒绝率均为100%,说明利用此方法能将四类辅料完全分开。[align=center][img=,502,266]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251740551806_2263_3389662_3.png!w502x266.jpg[/img][/align][b]3.4.2PH101和PH102辅料PLS-DA模型的建立[/b]PH101和PH102是不同型号的同一种辅料,都属于微晶纤维素,因此结构十分相似,难以区分。利用PLS-DA模型不经预处理即可将两种样品分开,模型的校正集是两种辅料的14张校正光谱图,验证集6个样品。如图2-9所示,图中的红色虚线为PLS-DA生成的判别线,线上方为一类,线下方为另一类。模型校正集和验证集的识别率以及拒绝率均为100%。[align=center][img=,485,281]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251742494590_6583_3389662_3.png!w485x281.jpg[/img][/align][b]3.4.3硬脂酸镁和十二烷基硫酸钠PLS-DA模型的建立[/b]硬脂酸镁与十二烷基硫酸钠在相关系数法判别时也无法正确分开,两种辅料可能是由于结构或者包装等其他因素导致一些相似的特征出现,同样利用PLS-DA模型判别两种辅料,在导入原始光谱时即可完全分开,模型的校正集是两种辅料的14张校正光谱图,验证集6个样品,模型结果见图2-10,模型校正集和验证集的识别率拒绝率均为100%[align=center][img=,509,271]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251744222873_6541_3389662_3.png!w509x271.jpg[/img][/align][b]3.4.4 二级识别体系结果分析[/b]由以上三个定性模型可知,在一级识别体系中无法正确判断的样品均能在不经预处理的条件下利用PLS-DA方法正确区分,识别率和拒绝率均为100 %,说明将相关系数法和PLS-DA法相结合判断药用辅料的种类是可行的,模型结果见表2-5。另一方面说明了sup-NIR1520分析仪可以用来区分这些辅料,实现定性判别的作用。[align=center][img=,528,168]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251745073638_3095_3389662_3.png!w528x168.jpg[/img][/align][b]3.5辅料识别体系的外部验证[/b]由上述结果可知,建立的识别体系在快速识别药用辅料方面是可行的,为了进一步证明此识别体系的准确性和可靠性,设计外部验证集考察模型对于外来辅料的识别能力。[b]3.5.1外部验证光谱图[/b]在相同条件下采集了60个不同种类和批次的样品光谱作为识别体系的外部验证集,样品的原始光谱及预处理后的光谱见图2-11。样品集的验证流程与识别体系内部验证相同,先利用预处理后的相关系数值进行初步判断,如果相关系数值很高的样品再利用PLS-DA模型验证。根据验证结果分为三类具体描述。[align=center][img=,505,260]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251742510972_5235_3389662_3.png!w505x260.jpg[/img][/align][b]3.5.2相关系数直接判别[/b]由一级识别体系直接判断出的验证样品共17个,即与17种辅料的相关系数值中仅有一个值大于阈值,表2-6种列举了其中8个样品的相关系数结果,其中表头中的数字表示验证样品的编号。[align=center][img=,562,543]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251746036984_3446_3389662_3.png!w562x543.jpg[/img][/align][b]3.5.3PLS-DA判别[/b]共有19个验证样品的相关系数值与两种及以上的辅料相似,因此需利用建立的二级识别体系进行进一步的验证,PLS-DA结果显示19个样品均能正确归属种类。表2-7为其中8个验证样品的相关系数结果。其中第10个、16个、25个外部验证样品的PLS-DA分析结果见图2-12、图2-13、图2-14,图中的灰色圆圈代表验证样品,由结果可知利用PLS-DA均能正确识别。[align=center][img=,566,561]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251746386429_3985_3389662_3.png!w566x561.jpg[/img][/align][align=center][img=,490,747]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251742232524_3277_3389662_3.png!w490x747.jpg[/img][/align][b]3.5.4不属于识别体系内的样品[/b]由于外部验证集的范围并不完全在识别体系范围内,所以会出现相关系数值均低于所有阈值的现象,此种情况说明该验证样品不属于识别体系内的任何一种辅料。由检测数据可以看出,24个验证样品均能被识别体系正确拒绝,拒绝率达到100%。由以上三种情况可知,外部验证集的60个样品均能被此识别体系正确的识别和拒绝,再次证明了识别体系的准确性和可靠性,既说明了此方法可以准确的应用到辅料的快速识别,又说明了sup-NIR1520分析仪在辅料定性识别应用中的可行性。[b]4讨论和结论[/b]本实验采用sup-NIR1520分析仪对17种不同的药用辅料进行光谱采集,并利用化学计量学方法建立了17种辅料的快速识别库,证明了sup-NIR1520分析仪在药用辅料定性方面应用的可行性。此自主研发的仪器不仅可以用于不同种药用辅料之间的快速识别,还可以应用于同种辅料不同型号的样品快速识别如PH101和PH102,识别率和拒绝率均达到100%。[align=center][b]参考文献[/b][/align] 王动民, 纪俊敏, 高洪智. 多元散射校正预处理波段对[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]定标模型的影响. 光谱学与光谱分析, 2014, 34(9):2387-2390. BrownC D, Vegamontoto L, Wentzell P D. Derivative Preprocessing and OptimalCorrections for Baseline Drift in Multivariate Calibration. AppliedSpectroscopy, 2000, 54(7):1055-1068.
热分析技术在药物分析中的应用进展热分析技术是研究物质在加热或冷却过程中产生某些物理变化和化学变化的技术。自1887年Lechatelier提出差热分析至今已发展成为一门专门的热分析技术。因其具有方法灵敏、快速、准确等优点,该技术及其分析仪器也得到快速发展。不久Sadtler的DTA标准图谱集,热分析专著《Thermal analysis》也相继面世。热分析技术在药物分析领域也广泛应用,如化学药品的鉴别、理化常数测定、纯度考查、稳定性考察以及近年来对中药活性成分的研究、中药材真伪品的鉴别、中药制剂质量分析等。目前,一些发达国家已把热分析方法作为控制药品质量的主要方法之一,美国药典23版与英国药典1993年版均已收载了热分析方法。1 热分析技术的方法分类1.1 差热分析(differential thermal analysis,DTA) DTA是最先发展起来的热分析技术。当给予被测物和参比物同等热量时,因二者对热的性质不同,其升温情况必然不同,通过测定二者的温度差达到分析目的。以参比物与样品间温度差为纵座标,以温度为横座标所得的曲线,称为DTA曲线。1.2 差示扫描量热法(differential scanning calorimentry, DSC) DSC是在DTA基础上发展起来的一种热分析方法。由于被测物与参比物对热的性质不同,要维持二者相同的升温,必然要给予不同的热量,通过测定被测物吸收(吸热峰)或放出(放热峰)热量的变化,达到分析目的。以每秒钟的热量变化为纵座标,温度为横座标所得的曲线,称为DSC曲线,与DTA曲线形状相似,但峰向相反。1.3 热重分析(thermogravimetry,TGA) TGA是一种通过测量被分析样品在加热过程中重量变化而达到分析目的的方法。即将样品置于具有一定加热程序的称量体系中,测定记录样品随温度变化而发生的重量变化。以被分析物重量(%)为纵座标,温度为横座标的所得的曲线即TGA曲线。其它尚有导数热重量分析、热机械分析(TMA)、质谱差示分析等。2 热分析技术在药物分析中的应用 热分析技术常用于新药研究中。药物分析中应用最多的是将TGA与DSC联合使用。热分析技术可用于判断药物的熔点,确定药物的结晶水,测定药物的纯度,处方及辅料筛选等。2.1 药品熔点的判断 熔点是衡量药物质量的重要指标之一。确定药物的熔点需确定这个药物是熔融同时分解还是熔点,再确定其熔融同时分解或熔点的具体温度。如果采用历版中国药典收载的毛细管测定法,很难作到准确判断。如采用DSC与TGA相结合进行测定,则可对其作出准确的判断。80年代初重庆市药品检验所曾用DSC和TGA确定磷酸氯喹的熔点,1986年杨腊虎又用DSC测定九种熔点标准品物质的熔点。2.2 药品的纯度测定 利用热分析技术测定药品纯度的理论依据是范德霍夫方程,即药品熔点的下降与杂质存在的克分子分数成正比。采用逐步加热程序技术(step heating programming technique)可扩大测定范围简化测定过程并缩短测定时间。但此方程的适用条件为被测药物不能熔融同时分解,并药物与共存杂质之间不得形成固溶剂。当不需要得到药物的准确纯度时,可采用与对照品同时测定DSC或TGA曲线,通过分析热分析曲线来确定药物的纯度。文献报道了用热分析技术测定药物的纯度和用DSC测定硝苯地平的纯度。2.3 药物的多晶型分析 不同晶型的药物具有不同的生物利用度,因而具不同疗效。区别药物的晶型,过去通常采用红外分光光度法和X-射线衍射法。后来常用DSC或DTA分析法。用热分析技术不仅可区别同一药物的不同晶型,而且还可提供其热力学变化过程,为选择转晶条件提供依据。如对甲苯咪唑、多沙唑喹、法莫替丁、头孢新酯等的多晶型研究。徐坚等还用热分析技术研究了甲氧氯普胺两种晶型的互变条件及各自的溶解热。2.4 差向异构体的分析 不少的药物存在差向异构体,同一药物不同的差向异构体之间,其生物利用度不同。侯美琴等报导了用DTA和DSC分析双炔失碳的差向异构体,测定出其中α体的纯度,并为其制剂的剂量调整提供依据。2.5 药物中结晶水与吸附水的确定 确定药物分子中有无结晶水和结晶水的个数,过去常用卡氏水份测定法或在一定条件下测定干燥失重来决定。这些方法很难区分是分子中的结晶水还是吸附水。采用DSC-TG技术则可解决此问题。2.6 药物制剂中活性成份分析 热分析技术可用于药物制剂中活性成分的定性分析、定量分析和药物与辅料间的相互作用以及处方的设计。1980年有人报道不经分离直接用DSC技术测定磺胺类药物、硝基呋喃类药物以及解热镇痛类药物的胶囊剂和片剂。近年有文献报道用DSC考察了制剂中,活性成份间及活性成份与辅料间是否发生反应,即通过观察各活性成份、辅料以及制剂的DSC曲线的差异,发现是否出现新峰,以达到考察它们间是否相容,可否进行配伍的目的。2.8 药物的稳定性研究 汤启昭利用热分析技术研究了葡萄糖酸亚铁固体的稳定性,并与气相色谱分析结合,提高了热分析的研究水平;武凤兰用热分析技术研究了固体药物对乙酰氨基酚的分解动力学。

Accuman制药原辅料快检系统助力药厂新GMP实施最新的便携式拉曼光谱仪Accuman,让制药企业能够以较低成本进行简单、快速、准确的原辅料药品来料检测,从而使生产符合《药品生产质量管理规范(2010年修订)》(简称新GMP)所提出的要求。Accuman内置有目前海洋光学性能最好的光谱仪,具有检测速度快、测量结果准确、性价比高三大特点。http://ng1.17img.cn/bbsfiles/images/2012/12/201212191308_413837_2432394_3.jpg与市面同类产品相比,Accuman具有更高的灵敏度。对于不同包装的样品,Accuman都可以进行准确快速的测量,即使是棕色玻璃瓶装样品,检测时间一般也不到15秒,极大地减少药厂来料检测所需要花费的时间,满足新GMP中对原辅料药品逐一检测的要求。同时,Accuman集成有性能优秀的激光器以及先进的TE制冷功能,仪器具有良好的信噪比,对微弱的拉曼信号也有很好的采集效果。因此Accuman能够轻松区分结构相似的物质,例如相似的水合物或同分异构体。软件方面,Accuman所配有的软件符合美国的21CFR PART11标准,并具有中文操作界面,界面简洁明了,能够实现一键识别功能,使操作人员能够迅速掌握仪器使用,减少对实验人员的培训时间;软件能够实现自建数据库,使仪器能够符合厂家的个性化要求,并且还可根据客户需求选配常用原辅料的数据库。中国国家食品药品监督管理局于2011年发布关于贯彻实施《药品生产质量管理规范(2010年修订)》(2010新GMP)的文件,要求各新建药品生产企业、药品生产企业新建(改、扩建)车间均应符合2010新GMP的要求。Accuman拉曼光谱测量系统便是在这个背景下应运而生。该系统由海洋光学亚洲分公司技术团队设计研发而成,在拉曼光谱仪的本地技术支持方面具有很强的优势,可以完全满足国内生产用户的需求。
Accuman制药原辅料快检系统,据宣传,特别的好使。“便携式拉曼光谱仪Accuman,让制药企业能够以较低成本进行简单、快速、准确的原辅料药品来料检测,从而使生产符合《药品生产质量管理规范(2010年修订)》(简称新GMP)所提出的要求。”“即便是棕色玻璃瓶装样品,检测时间一般也不到15秒,极大地减少药厂来料检测所需要花费的时间,满足新GMP中对原辅料药品逐一检测的要求。”这样的表述让人很是神往啊!!!我们是制药企业,所以,我很关注。这个系统在内地有用户了吗?效果如何呢?如果有的话,出来现身说法一下吧。
老板要建一个药物筛选实验室
现在做的辅料含量测定时用的气相色谱,方法是将药品经过一个前处理化学反应过程即将其中的待测辅料转化成一个气相可测定的物质,以此物质来定药品中辅料含量。现在通过单一的此辅料成分,已经将前处理的化学反应条件基本摸清,而且GC测定方法也确定了。可现在的问题是在确定化学反应条件时,反应原料(除了此辅料成分外)的用量,都是按照与辅料的物质的量比来确定的,那么现在我要用此样品处理方法对药品进行处理时,这个上述的化学反应条件应该怎么做呢?还是按照单一辅料时确定的各化学反应参数(溶剂量,催化剂量等。。。。),如果是直接将药品替换原来的单一辅料,其他化学反应参数各用量一样,但由于药品中此辅料的量不确定,这实际上还是会导致化学反应条件中个反应物物质的量比的变化啊?我的问题是在做上述涉及到化学反应,同时化学反应条件会影响到最后GC测定时,具体应该如何去选择样品处理的方法?谢谢大家,欢迎交流~~~
海洋光学(www.OceanOpticsChina.cn)近期推出最新的便携式拉曼光谱仪Accuman,让制药企业能够以较低成本进行简单、快速、准确的原辅料药品来料检测,从而使生产符合《药品生产质量管理规范(2010年修订)》(简称新GMP)所提出的要求。Accuman内置有目前海洋光学性能最好的光谱仪,具有检测速度快、测量结果准确、性价比高三大特点。http://www.oceanopticschina.cn/images/accuman/accuman.jpg与市面同类产品相比,Accuman具有更高的灵敏度。对于不同包装的样品,Accuman都可以进行准确快速的测量,即使是棕色玻璃瓶装样品,检测时间一般也不到15秒,极大地减少药厂来料检测所需要花费的时间,满足新GMP中对原辅料药品逐一检测的要求。同时,Accuman集成有性能优秀的激光器以及先进的TE制冷功能,仪器具有良好的信噪比,对微弱的拉曼信号也有很好的采集效果。因此Accuman能够轻松区分结构相似的物质,例如相似的水合物或同分异构体。软件方面,Accuman所配有的软件符合美国的21CFR PART11标准,并具有中文操作界面,界面简洁明了,能够实现一键识别功能,使操作人员能够迅速掌握仪器使用,减少对实验人员的培训时间;软件能够实现自建数据库,使仪器能够符合厂家的个性化要求,并且还可根据客户需求选配常用原辅料的数据库。中国国家食品药品监督管理局于2011年发布关于贯彻实施《药品生产质量管理规范(2010年修订)》(2010新GMP)的文件,要求各新建药品生产企业、药品生产企业新建(改、扩建)车间均应符合2010新GMP的要求。Accuman拉曼光谱测量系统便是在这个背景下应运而生。该系统由海洋光学亚洲分公司技术团队设计研发而成,在拉曼光谱仪的本地技术支持方面具有很强的优势,可以完全满足国内生产用户的需求。
[em0801]讲义主要内容:一、辅料概述二、药用辅料基本技术要求三、制剂中对药用辅料的要求四、改剂型过程中药用辅料使用需要注意的问题五、处方中辅料变更的基本原则六、小结[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=108450]药用辅料在技术审评中的评价要点[/url]
我已经上传到资料中心,认证会员免积分下载,非认证会员下载需1分。该书是由英国药学出版社和美国药学会共同编辑出版的《药用辅料手册》是一本影响全球制剂工业的权威之作。该书拥有国际上辅料业著名专家20人组成的学术指导委员会,各国的执笔人员达到100人之多。该书涵盖辅料的基本工艺性质、物理化学性质、稳定性、配伍相容性、生物学特性以及相关的安全性和法规许可的咨询信息,甚至详细的参考文献等,其对我国药学、食品、化妆品领域的研究人员来说是一本极具参考价值的实用参考书。 该书共83MB,为PDF格式。由于文件较大为方便下载共12个压缩分卷。药用辅料手册(第4版)[1]part1 http://www.instrument.com.cn/download/shtml/036350.shtml药用辅料手册(第4版)[1]part2 http://www.instrument.com.cn/download/shtml/036363.shtml药用辅料手册(第4版)[1]part3 http://www.instrument.com.cn/download/shtml/036365.shtml药用辅料手册(第4版)[1]part4 http://www.instrument.com.cn/download/shtml/036366.shtml药用辅料手册(第4版)[1]part5 http://www.instrument.com.cn/download/shtml/036370.shtml药用辅料手册(第4版)[1]part6 http://www.instrument.com.cn/download/shtml/036371.shtml药用辅料手册(第4版)[1]part7 http://www.instrument.com.cn/download/shtml/036372.shtml药用辅料手册(第4版)[1]part8 http://www.instrument.com.cn/download/shtml/036373.shtml药用辅料手册(第4版)[1]part9http://www.instrument.com.cn/download/shtml/036375.shtml药用辅料手册(第4版)[1]part10 http://www.instrument.com.cn/download/shtml/036377.shtml药用辅料手册(第4版)[1]part11http://www.instrument.com.cn/download/shtml/036378.shtml药用辅料手册(第4版)[1]part12 http://www.instrument.com.cn/download/shtml/036379.shtml
药用辅料目录[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=57365]药用辅料目录[/url]