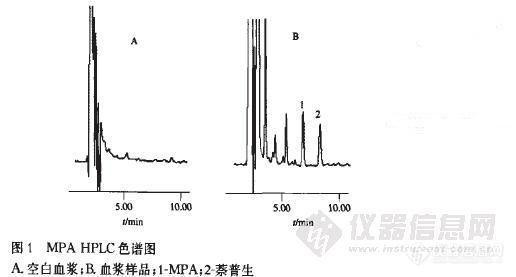
【作者】 任斌; 李敏薇; 唐蕾; 王长希; 李瑞明; 容颖慈; 陈坚平; 黎曙霞;【机构】 中山大学附属第一医院; 中山大学附属第一医院 广东广州510080; 广东广州510080;【摘要】 目的:建立高效液相色谱法快速测定人血浆中霉酚酸药物浓度。方法:色谱柱为Diamonsil C18(4.6mm×250mm,5μm);流动相为乙腈-10mmol.L-1磷酸二氢钾溶液(pH=3.0)(50∶50);柱温25℃;流速1.5mL.min-1;检测波长254nm。结果:本测定方法的线性范围为0.1~50mg.L-1,r=0.999 8。平均回收率为(97.5±5.4)%,日内RSD不大于5.8%,日间RSD不大于7.2%。MPA的最低检测浓度为0.1mg.L-1。结论:本方法简单、快速、灵敏、重复性好,适用于MPA临床血药浓度监测及人体药动学研究。 http://ng1.17img.cn/bbsfiles/images/2012/08/201208141952_383837_1609970_3.jpg
各位是如何理解药物的转运机制这个词的?
请教一下各位:药物中杂质的来源主要有哪些?什么是一般杂质?什么是特殊杂质?
了解不同时间药物在血浆或血清中的浓度,对于计算一种药物的代谢动力学很有必要;反之,药物动力学也是药物吸收、分布、代谢和排泄过程的一部分。准确了解药物在体内吸收、分布、代谢和排泄的规律,便于精确地计算所需药物剂量,既能保持有效的药物浓度,同时避免用药过量致毒。预先对多屏深孔Solvinert(MultiScreen Deep Well Solvinert )和多屏Solvinert滤板进行了验证,进行血浆或血清中蛋白质的板内沉淀,以便展开总药物分析。在滤板上可以快速、细致并完整地转移滤液,这样就可以在进行总药物分析之前为样品制备提供一个自动化兼容的平台。Solvinert滤板过滤的滤液中不含蛋白质,这与质谱分析法和紫外线分析法的结果一致。使用多屏深孔和多屏Solvinert滤板可产生有复验性的结果,它是一个稳定且可靠的平台。血清中的蛋白质被这些滤板过滤并沉淀之后,得到的样本中基本上不含蛋白质,回收率很高,便于萃取。药物动力学特性可以让新药开发商更了解药物的有效性和安全性,而这在新药的注册审批中是必要的。为了更好地了解候选药物的代谢动力,金斯瑞( GenScript)建议用动物来做药物分布及其代谢的研究,分析在不同时间段、不同组织或血清中,药物及其代谢物的情况。金斯瑞进行精确的药物和药物代谢动力学研究,涉及两个主要方面:药物分布及其代谢动力研究和抗体药物的代谢动力研究。群体药代动力学研究的是个体之间药物浓度变异来源及其相关性,这些个体是指按临床上相关剂量接受候选药物的目标患者人群。患者的某些人口统计学特征、病理生理特征以及治疗方面的特征,比如体重、排泄和代谢功能、以及接受其他治疗,都能够有规律地改变药物剂量-浓度关系。例如,主要由肾脏排除的药物,在接受同样剂量的情况下,在肾功能衰竭患者体内的稳态浓度,通常高于肾功能正常的患者体内的稳态浓度。群体药代动力学的研究目的就是找出那些使剂量-浓度关系发生变化的、可测定的病理生理因素,确定剂量-浓度关系变化的程度,当这些变化与临床上有意义的治疗指数改变相关的情况下,能够恰当地调整剂量。在药品开发中使用群体PK方法,使获得完整的药代动力学资料有了可能,不但能从来自研究受试者的相对稀疏的数据中获取资料,而且还能从相对密集的数据或从稀疏数据和密集数据的组合中获取资料。群体PK方法能够分析来自各种不均衡设计的数据,也能分析因为不能按常用的药代动力学分析方式分析而通常被排除的研究数据,比如从儿科患者和老年患者获取的浓度数据,或在评价剂量或浓度与疗效或安全性之间的关系时所获取的数据。传统药代动力学研究的受试者通常是健康的志愿者或特别挑选的患者,一组成员的平均情况(即平均血浆浓度-时间曲线)一直是关注的主要焦点。许多研究将个体之间药代动力学的变异作为一个需要降到最低的因素进行观察,通常是通过复杂的研究设计和对照方案,或通过有严格限制的入选标准/排除标准,将其降到最低。事实上,这些资料对在临床应用期间可能会出现的变异至关重要,但是却被这些限制所掩盖。而且,传统药代动力学研究只关注单个变量(例如肾功能)的作法,还使其难以研究变量之间的交互作用。
[center]跨国药企上书 外资药企争议基本药物制度[/center]虽然新医改方案征求意见的截止日期已过,但来自各方的建议仍源源不断汇入相关部门。3日,记者获得中国外商投资企业协会药品研制和开发行业委员会(以下简称RDPAC)对于医改征求意见稿的一份建议书,RDPAC的执行总裁萧滋杰也接受了本报记者的专访,详述对于新医改方案的认同和不认同,特别对于基本药物制度的执行,提出一些不同的看法。 外资药企,是中国医药市场上的一股重要力量,占据了处方药市场30%的市场份额。这个群体对于新医改的影响力不容忽视。而RDPAC,正是跨国药企在华的代言人。争议基本药物社区全覆盖在新医改方案中,建立国家基本药物制度是一项重要内容。所谓基本药物,是国家按照“防治必需、安全有效、价格合理、使用方便、中西药并重”的原则,结合我国用药特点并参照国际经验,确定的药物通用名目录。事实上,基本药物目录在我国一直存在,但一直以来形同虚设,未起到实际作用。为此,新医改旨在通过建立一系列制度保障基本药物目录的运行。 征求意见稿对基本药物制度做出如下阐述:中央政府统一制定和发布国家基本药物目录。基本药物由国家实行招标定点生产或集中采购,直接配送,在合理确定生产环节利润水平的基础上统一制定零售价。这也正是被外界诟病的“统购统销”。——此前,代表民族药企的中国医药企业管理协会已经上书发改委等相关部门,对此似乎违背市场经济运行的做法表示了不同的意见。“在这一点上,我们也是同样的看法。”萧滋杰说,按照招标定点生产,有悖国家反垄断的原则,会让少数垄断企业获益,但危及大部分企业的生存。他认为,对基本药物的生产和流通企业不宜作单一的定点或招标限定,可以在政府的有效监管下鼓励企业合理竞争,通过竞争性议价或团购方式来遴选药品供销企业。 而基层医疗卫生机构全部使用基本药物的新政,更让跨国药企坐立不安。征求意见稿明确指出,城市社区卫生服务中心(站)、乡镇卫生院、村卫生室等基层医疗卫生机构,应全部使用基本药物,其他各类医疗机构也要将基本药物作为首选药物并确定使用比例。这让一直试图拓展基层医疗市场的跨国药企发现,自己生产的中高价药物可能无法拿到进入这一市场的敲门砖。值得一提的是,新医改下,社区医疗等基层医疗市场未来增长潜力巨大,这一背景下,众多跨国药企一改往日只重视三甲医院的营销,转而向社区拓展,但如果社区只准使用基本药物,大部分跨国药企可能都将和这一未来扩容最大的市场无缘。对此,萧滋杰表示,此种做法并不合理。对社区医院用药的限制与拓展社区医疗的初衷背道而驰。“国家拓展社区医疗,是为了从大医院分流病患。但如果患者和医生在社区医院没有了用药的选择权,很多患者可能会再次回流到三级医院。
急!急!急!新手请教各位大侠,LC/MS/MS能进行药物杂质限度检查吗?如何确定一药物中某杂质是否超出限度?
对药物的制剂的定量方法有何要求?
当葛兰素史克公司今年初设立了一个专利池以刺激对被忽视疾病的研究的时候,它们把利润极为丰厚的艾滋病药物专利排除在外,这并不令人惊讶。 但是现在有一个把艾滋病药物放入专利池的强有力的人道主义理由——如今国际药品采购机制(UNITAID)这个卫生组织正在推广这一理由。英国国会关于艾滋病的小组估计,到2030年,5000万人将需要艾滋病药物。已经有超过600万人因为无法获得救命药物而死于艾滋病。 UNITAID提议的专利池可能完全改变这种情况。它的运行方式可以是收集企业、大学或研究所持有的专利,让发展中国家以低廉的授权费用获得这些专利用于药品生产或研究。 这有别于药物专利通常的运作方式。当一家公司研发出一种新药的时候,专利保护持续大约20年。它禁止其他公司制造和销售该药,或者把它用于研究。有时候,专利持有人可能会让其他组织获取它的受保护的知识,但是通常只能获取极为有限的能力和付出高昂的费用——这让中低收入国家无望参与进来。 专利确保了最大的利润并让公司弥补它们把一种药物推向市场所花费的无数金钱。但是这也意味着那些只能买得起廉价“仿制药”的人们必须等待数年。而且如果其中一种药物有专利,科学家就无法开发新的联合疗法——世界卫生组织把联合疗法推荐为减少耐药性风险的最佳方法。 UNITAID的艾滋病专利池意味着可以立刻生产仿制药,而且可以开始进行新药联用以及对儿童友好的配方的研究。 正确的主意,合适的时间? 专利池并不是确保发展中国家获得药物的唯一方式。一些国家,例如巴西,印度和泰国,已经发出了强制许可证,让制药商可以制造专利药的仿制版本。这些国家在保护它们制造廉价救命药物的权利方面的态度与制药公司保护它们的股价方面的态度一样积极。 但是强制许可是一条艰难的道路,充满了包括来自制药公司的法律行动在内的复杂因素。而且尽管它降低了现存药物的价格,它没能刺激研究。UNITAID的专利池可能让创新恢复活力,挽救发展中国家的生命。 而且有很好的理由认为该组织可以让一个专利池运作起来。UNITAID在通过批量采购协议从而降低艾滋病药物方面拥有良好的记录。它还拥有“获取药物”运动的一个关键的前成员Ellen t'Hoen的专家知识。无国界医生组织利用该运动改善了穷人对抗逆转录病毒药物的获取。 一些制药公司至少在原则上也开始接受这个主意。强生公司、Gilead以及印度的仿制药制造商Cipla已经公开表示支持,据报道诺华和默克也正在与UNITAID协商。即便是葛兰素史克也在最近致英国卫报的一封信中说,它们并没有排除加入专利池的选项。 付款和奖金 但是UNITAID仍然需要提出一个让各个公司加入的激励措施——仅凭企业的良好意愿,它们不太可能加入进来。 目前的提案把重点放在了自愿捐助专利的特许使用金上。t'Hoen告诉本网站说,这些特许使用金“不会很少”。但是考虑到艾滋病药物能够带来巨大的利润——发达国家每年每位患者使用替诺福韦德的费用是3500英镑(5500美元)——这些公司不太可能仅仅满足于特许使用金。 由知识生态学国际组织提出的一个替代方案是建立一个数百万美元的奖金基金,从而诱惑各个公司加入这个专利池。那些加入专利池的公司有资格获得奖金,例如,可以为对于公共卫生有最大影响的公司发奖。 这个主意正在获得来自几个权威学术人士的支持,诸如澳大利亚乔治研究所药物研发项目的负责人Mary Moran,以及克林顿艾滋病项目等捐助者。 一些发展中国家也支持这个主意。孟加拉国、巴巴多斯、玻利维亚和苏里南都写信给世界卫生组织(它负责组织和管理UNITAID),要求它考虑这个奖金基金/专利池的模式。它们提出,捐助者药物采购预算的10%可以投入这个基金,这就可能积累到数百万美元。无疑,捐助者和非政府组织将就具体的百分比进行争论,或者甚至就资助该基金的方式进行争论,但是它们和各国政府需要在这个动力消失之前提出一个可行的方案。 UNITAID提出专利池的方案正值世界知识产权组织(WIPO)在新领导人的带领下重整旗鼓。该组织的新领导人Francis Gurry正在设法恢复该组织的发展议程,t'Hoen 说WIPO已经向UNITAID提供了技术支持。 UNITAID如今需要确保它们成功地促成一项对于发展中国家极为重要的协定。
大家好,本人刚工作不久,在一家制药公司,以后主要做关于药物杂质方面的研究,仪器也正在采购,是安捷伦的q-tof,刚开始接触这一行不是很懂,想请教各位大神分享一下经验,感激不尽。
http://img.dxycdn.com/cms/upload/userfiles/image/2013/02/08/424366159_small.jpg欧洲制药团体正在加快发动药物研发的引擎。这个包含有30个合作伙伴的团体,正采用众包、开放式创新模式,发起一次新的活动以推动新的治疗药物的开发,该团体包括了拜耳、强生旗下杨森和5个其它制药巨头。7家合作伙伴计划献出至少30万个化合物,研究机构及其它合作方也计划开发大约20多万个化合物,目的是对该团体中的参与者共同分享药物研发成果,研发战略,这与以往制药集团传统的、秘密进行的药物研发方式形成了鲜明对比。“对制药公司来说,这是一个很大的改变,因为他们的化合物数据库通常被秘密保存,”荷兰非营利组织TI制药公司科学主管Ton Rijnders说。“他们这样做是因为这种方式与以往建立自己更大的化合物数据库相比成本更低,而且参与该团体的学术机构把他们的创新理念也输送了进来。”事实上,制药集团已经变得更加开放,正在与外部组织一起来扭转消极的药物研发趋势。由欧盟10亿欧元支持的创新药物计划(IMI)也对这个新的药物研发团体进行了支持,并取得了较大进步,引入了大型制药公司参与到这个行列。例如,创新药物计划支持了2012年10月份宣布的、由罗氏领头10家主要制药公司参与的一项活动,该活动目的是借助干细胞开发出人类疾病模型,帮助神经疾病和糖尿病药物的开发。这次最新的1.96亿欧元的药物研发活动,有8000万欧元来自欧洲委员会第七框架研究计划,剩余预算由制药企业、大学及其它合作方完成。TI制药对该药物研发活动正在进行组织协调。7个主要制药企业包括阿司利康、拜耳、丹麦灵北、杨森、默沙东、赛诺菲及比利时优时比公司。
1.前言 致癌试验的目的是考察药物在动物体内的潜在致癌作用,从而评价和预测其可能对人体造成的危害。任何体外实验、动物毒性试验和人体应用中出现的潜在致癌性因素均可提示是否需要进行致癌试验。国际上,对于预期长期使用的药物已经要求进行啮齿类动物致癌试验。在研究药物的潜在致癌作用中,致癌试验比现有遗传毒性试验和系统暴露评价技术更有意义。这些试验也可帮助理解无遗传毒性药物的潜在致癌作用。目前常规用于临床前安全性评价的遗传毒性试验、毒代动力学试验和毒性机理研究的数据,不仅有助于判断是否需要进行致癌试验,而且对于解释研究结果与人体安全性的相关性也是十分重要的。由于致癌试验耗费大量时间和动物资源,只有当确实需要通过动物长期给药研究评价人体中药物暴露所致的潜在致癌性时,才应进行致癌试验。 2.历史背景 在日本,根据1990年“药物毒性研究指导原则手册”,如果临床预期连续用药6个月或更长时间,则需要进行致癌试验。尽管连续用药少于6个月,如果存在潜在致癌性因素,也可能需要进行致癌试验。在美国,大多数药物在广泛应用于人体之前,已进行了动物致癌试验。根据美国药品食品监督管理局(FDA)要求,一般药物使用3个月或更长时间,需要进行致癌试验。在欧洲,“欧共体药品管理条例”规定了需要进行致癌试验的情况,包括长期应用的药物,即至少6个月的连续用药,或频繁的间歇性用药以致总的暴露量与前者相似的药物。 自2005以来,我国《药品注册管理办法》附件中规定预期临床连续用药6个月以上或需经常间歇使用的药物应进行致癌试验,并指出了进行致癌试验的多个考虑因素。2007年1月国家食品药品监督管理局药品审评中心发布的《治疗用生物制品非临床安全性技术审评一般原则》中阐述了相关产品致癌试验的要求。 2009年10月药品审评中心组织毒理专家、企业和研究单位代表召开了制定“药物致癌试验必要性技术指导原则”专题讨论会,会上基本认同了ICH S1A中内容的适用性,并结合国内情况进行了一些调整。
创新药物的研制很难跟上疾病的发展变化啊,怎么才能在最短的时间内研制出最具效果的药物呢?
[B][center]药物中杂质的来源及杂质限量检查[/center] [/B]药物只有合格品与不合格品;一般化学试剂分为4个等级(基准试剂、优级纯、分析纯、化学纯) [B]药物中一般杂质检查 [/B][B]氯化物为一指示性杂质。[/B] 通过对氯化物的控制,可同时控制与氯化物结合的一些阳离子以及某些同时生成的副产物。可从氯化物检查结果显示药物的纯度,间接考核生产、贮藏过程是否正常。 1. 原理 药物中微量的氯化物在硝酸酸性条件下与硝酸银反应,生成氯化银的胶体微粒而显白色浑浊,与一定量的标准氯化钠溶液在相同条件下产生的氯化银浑浊程度比较,判定供试品中氯化物是否符合限量规定。 Ag+ + Cl- → AgCl ↓ [B]硫酸盐检查法 [/B] 1. 原理 药物中微量的硫酸盐在稀盐酸酸性条件下与氯化钡反应,生成硫酸钡的微粒而显白色浑浊,与一定量的标准硫酸钾溶液在相同条件下产生的硫酸钡浑浊程度比较,判定供试品中硫酸盐是否符合限量规定。 [B]铁盐检查法 [/B]硫氰酸盐法 巯基醋酸法 砷盐检查法 1. 古蔡氏法 1. 原理 金属锌与酸作用产生新生态的氢,与药物中微量砷盐反应生成具挥发性的砷化氢,遇溴化汞试纸产生黄色至棕色的砷斑,与同条件下一定量标准砷溶液所生成的砷比较斑,判断砷盐的含量。 [B]硒、氟及硫化物检查法 [/B]1. 氧瓶燃烧法 适用于以共价键结合的卤素、硫、硒的有机药物。 本法系将有机药物防入充满氧气的密闭燃烧瓶中进行燃烧,将燃烧所产生的欲测组分吸收于适当的吸收液中,然后根据欲测组分的性质,选用合适的分析方法进行鉴别、检查或含量测定。 [B]注意事项及讨论 [/B]1. 根据被燃烧分解的样品量选用适宜大小的燃烧瓶。 2. 测定氟化物时应改用石英燃烧瓶。 1. 硒检查法 (1). 操作方法 样品与对照品液,调节Ph2.0±0.2,加盐酸羟胺,二氨基萘,比色。 [B]硫化物检查法 [/B] 方法同砷盐检查第一法,不装醋酸铅棉花,以醋酸铅试纸代替溴化汞试纸。 标准液取1ml 5/ml [B]澄清度检查法 [/B]将一定浓度的供试品溶液与浊度标准液分别置于配对的比浊用玻璃管,同置黑色背景上,在漫射光下观察。浊度标准液 硫酸肼与乌洛托品溶液混合分五个等级,未超过0.5等级即为澄清。BP98规定未超过1等级即为澄清。 [B]溶液颜色检查法 [/B]CHP2000 [B]1. 比色法[/B] 色调标准贮备液 黄色液 重铬酸钾液(BP98用氯化铁) 红色液 氯化钴液 蓝色液 硫酸铜液 配成各种色调色号标准比色液共50种。 [B]2. 分光光度法 [/B] [B]易碳化物检查法 [/B]检查药物中含有的遇硫酸易碳化或易氧化而呈色的有机杂质。 对照品液 样品液 加硫酸5后,加供试品。 [B]炽灼残渣检查法[/B] 取供试品1.0~2.0g或个药品项下规定的重量,置已炽灼至恒重的坩埚中,精密称定,缓缓炽灼至完全碳化,放冷至室温;除另有规定外,加硫酸使湿润,低温加热至硫酸蒸气除尽后,在700~800炽灼使完全灰化,移至干燥器内,放冷至室温,精密称定,再在700~800炽灼至恒重,即得。残渣限量一般为0.1~0.2% 一般应使炽灼残渣量为1~2mg 若需将炽灼残渣留作重金属检查时,炽灼温度必须控制在500~600。 [B]干燥失重测定 [/B]1. 常压恒温干燥法 2. 干燥剂干燥法 3. 减压干燥法 [B]水分测定法 [/B][B]费休氏法 [/B] 本法是根据碘和二氧化硫在吡啶和甲醇溶液中能与水起定量反应的原理以测定水分。 [B]甲苯法[/B] 在加热状态下,甲苯夹带着水分蒸出,收集蒸出的水分测定。 [B]药物中特殊杂质检查 [/B] [B]一、物理法 [/B] [B]二、化学反应法 [/B](一)容量分析法 (二)重量分析法 (三)比色法和比浊法 [B]三、色谱法 [/B]1.纸色谱法 薄层色谱法 TLC是药典中最常用的特殊杂质限量检查方法。 1.在一定供试品及检查条件下,不允许有杂质斑点存在 2.以待测杂质对照品检测 3.将供试品稀释到适当浓度作为杂质对照品溶液 4.选用质量符合规定的与供试品相同的药物作为杂质对照品 [B]高效液相色谱法 [/B] [B][url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法 [/B] 1.面积归一化法 2.主成分自身对照法 3.内标法测定 4.内标法加校正因子法 5.外标法 有机溶剂残留量测定法 [B]分光光度法 紫外分光光度法 比色法 [url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]分光光度法[/B]
中药别名 中药名称有其正名。由于历代文献记载的不同和地区差异等原因,一味药在处方中常出现多种名称。目前对处方中的药名,以《中国药典》收载的药品名称为正名;如果药典未收载的药品则以《部颁药品标准》收载的药品名称为正名;如果以上两级标准中均未收载的药品,则以地区医药部门的有关规定和《中药大辞典》的药品名称为正名。其他的中药名均为别名。调剂人员在掌握药物正名的同时,也应熟悉本地区常用的药物别名,以保证正确配付药物。 有些处方药名的前头配有说明语,以表示对药物的要求,有以药物产地者(如云茯苓、川黄连);有以加工炮制规格者(如制首乌、焦山楂);有以采收季节者(如春柴胡、冬桑叶);有以新陈者(如鲜荷叶、陈棕榈);有以颜色者(如白檀香、红栀子)和以药用部位者(如全瓜蒌、全紫苏)等。 并开药物 并开药物系指处方中将2~3种药物合并开在一起。主要是医师处方求其简略。并开其意图大致有二:一是疗效基本相同的药物,如二冬即指天冬和麦冬,都具有养阴、益胃、清心肺作用;二活即指羌活和独活,都具有祛风胜湿、止痛作用;焦三仙即指焦神曲、焦山楂、焦麦芽三药,均有消食健胃作用,所以常并开同用。二是配伍时使其产生协同作用,如知柏即指知母和黄柏,其配伍能增强滋阴降火作用。 必须注意处方中并开药不得含糊和引起误解为准。另外,尚须注意各地区并开用药习惯不同,处方应付有差异。 调剂人员应了解常见并开药应付,保证配方迅速正确。
晶云药物科技有限公司(简称晶云)已与华嘉(香港)有限公司—隶属大昌华嘉 (简称华嘉)签订合作协议,将会为华嘉在中国的广大制药界客户,提供药物固态表征领域的一系列高端讲座和培训,以共同推进中国制药界对固态表征仪器在制药界应用和其在药物研发过程中的重要性的了解。 华嘉公司仪器部专业提供分析仪器及设备,独家代理众多欧美先进仪器,产品范围包括:颗粒,物理,化学,生化,通用实验室的各类分析仪器以及流程仪表设备,在中国的石化,化工,制药,食品,饮料,农业科技等诸多领域拥有大量用户,具有良好的市场声誉。其中固态表征领域的产品就包括粒度仪,密度计,旋光计,接触角测量仪,BET比表面积测量仪等各种高端进口仪器。 “中国政府正在大力增加制药行业的投资力度,以提高中国在药物研发领域的能力和国际竞争力”,晶云首席执行官陈敏华博士说,“在药物的高级研发方面,中国制药业尚处于起步阶段。导致这个现象的部分原因是国内制药行业在对原料药和制剂的研发认知上,与美国和欧洲的制药行业尚有不小差距。虽然不少中国制药公司有能力购买昂贵的固态表征和其它分析仪器,但他们并不一定懂得如何正确的使用这些仪器,合理的阐释实验数据,并深刻理解其所提供的信息和对药物研发的作用。” 苏州晶云药物科技有限公司是中国首家并且也是目前唯一一家专注于药物晶型研究和提供药物固态信息领域研发方案的技术服务公司。晶云的科研人员拥有丰富的原料药和制剂的研发经验。无论是以研发创新药物为主的全球各大制药公司,还是以生产仿制药(包括原料药和制剂)为主的国内各制药公司,晶云都可以成为其在药物固态研发领域的紧密合作伙伴,为其提供药物固态研发领域的各种解决方案,其中包括药物晶型研究,盐型/多晶型/共晶型筛选,单晶的生长和结构鉴定,结晶工艺的优化,手性药物的结晶提纯,临床前制剂的研发,无定形药物制剂的研发等各个方向。晶云不局限于简单的为客户操作实验和提供实验结果,更重要的是给客户提供一个适合其需求并完全满意的全套研发方案。 晶云技术团队在药物晶型研究和药物固态表征领域拥有数十年的丰富经验,曾被邀请为许多全球和国内的制药公司提供该领域的专业技术咨询和培训。晶云即将为华嘉客户提供的讲座和培训不仅包含了药物固态表征技术的基本理论,还将集中讨论如何利用这些仪器解决药物研发生产中碰到的实际问题,并辅以大量的制药行业中的案例分析。晶云和华嘉的一个共同使命就是帮助广大中国制药公司在新药研发领域迅速赶上欧美制药公司水平。相信由两家公司联合举办的讲座和培训将为成为实现这一使命的重要平台。 晶云药物科技有限公司 晶云药物科技有限公司(Crystal Pharmatech)总部设立在苏州工业园区内的生物纳米科技园,在美国新泽西州建有分部。核心团队由中美科学家及管理人员共同组成,拥有在全球前三大制药公司数十年的丰富研发和生产经验。团队利用掌握的核心技术开发出中国在药物晶型研究及提供药物固态信息研发方案的首个高新技术平台,并通过该平台为全球制药公司提供该领域的高级技术研发服务。公司拥有的享有自主知识产权的高新技术和高新仪器,结合团队目前已经完全掌握的该专业领域的核心技术,将保证技术平台不仅可以填补国内在该领域的空白,而且使技术平台处于国际领先地位。公司的业务集中在以药物的固态信息为中心的专业领域,主要包括原料药及其中间体的成盐,共晶和多晶的筛选,原料药和制剂的表征和评估,晶型药物结晶工艺流程的优化和放大,临床前药物制剂的研发,以及上述相关领域内自主知识产权技术和产品的开发,高级技术咨询及其培训等。 想了解更多信息,敬请登陆: http://www.crystalpharmatech.com/华嘉(香港)有限公司——隶属大昌华嘉 大昌华嘉是一家著名的国际贸易集团,总部位于瑞士的苏黎世。华嘉公司自1900年以来便与中国进行友好贸易往来,业务范围涉及机器、仪器、消费品、纺织品、化工原料等诸多领域。"科技的市场智慧”是对华嘉公司形象的准确概括。高品质的产品,专业的应用及完善的售后服务,对各种客户文化背景的深刻理解以及娴熟的市场贸易技巧使得客户获得的不仅是经济上的利益,而且是技术上的进步。华嘉公司仪器部专业提供分析仪器及设备,独家代理众多欧美先进仪器,产品范围包括:颗粒,物理,化学,生化,通用实验室的各类分析仪器以及流程仪表设备,在中国的石化,化工,制药,食品,饮料,农业科技等诸多领域拥有大量用户,具有良好的市场声誉。我们的业务逐年增加,市场不断扩大。华嘉公司在中国设有多个销售,服务网点,旨在为客户提供全方位的产品和服务。 想了解更多信息,敬请登陆:http://www.dksh-instrument.cn/
制药企业药物合成研发人员,与CRO(医药研发外包)合成人员的不同:CRO合成人员一般是medichem和process。medichem合成人员认为最自豪,最自鸣得意的就是, 就是我一年做了多少化学反应,做了多少新的物质。而往往很多反应,只要反应,有他要的东西,不考虑如何优化,如何提纯处理,就直接送制备色谱了,得到他要的产物,鉴定合成,工作就完成了。process合成人员的工作应该是药物发现过程中的化学研究阶段,将工艺放大生产出1kg级别,10kg级别规模的目标化合物,用于满足临床前研究、剂型、初步临床的需求。一个合格的制药企业药物合成研发人员的工作主要是药物仿制或者药物发现过程中的化学研究的第三个阶段:合成路线的确定、优化、验证,含量测定以及质量标准的制定等,相比较CRO合成人员的合成工作来说要相对复杂繁琐。这就要求合成研发工作者在必须掌握药物合成发面的专业知识外,还要熟知药物分析专业知识和注册申报药政法规知识。再者合成研发工作者的合成研发工作一切都是以药物申报规范为准绳:1:在考虑工业化生产的条件下,打通工艺。工业化生产,这个条件就限制了很多实验室的技术。例如:要得到比较纯的物质,在这个条件下,就必须放弃柱层析,制备液相制备等等。只能从工艺上,后处理来想办法。2:在打通工艺的基础上,完成工艺参数的优化。这部分研究包括:(1)在不产生杂质的条件下尽量合并反应步骤。(2)在不影响收率和质量的条件下尽量减少溶媒和其他辅助原料。(3)尽量避免采用无水、无氧、易爆炸、易中毒工艺。(4)尽量避免采用价格昂贵的原辅料,避免高污染的工艺。(5)尽量对原辅料回收套用。(6)对温度、压力、反应时间及其他参数优化。3:杂质研究。在药物合成工作中,杂质研究是重中之重,也是最难的。因为人用药物的安全性和杂质的种类和限度是有很大的关联性的。杂质研究一般包括以下方面:(1)杂质的鉴定、分离和制备。(2)杂质的关联性研究(原料带入、副产物、中间体等等)。(3)杂质的消除和避免(4)杂质限度的确定4:晶型研究。对于晶型研究也是一个难点。从事药物研发的人都知道,不同的晶型API药物的释放度和吸收都是都很大差别的。原研厂家往往都是在工艺专利快到期的情况下,推出晶型专利,晶型专利相当于化合物专利。对于工艺专利来说还比较好绕开,最难的就是如何避开原研厂家的晶型专利。
制剂过程中药物晶型可能会发生变化,但是有辅料干扰,请问有些什么方法可以确定制剂中药物晶型的?
[center]跨国药企移情致命病药物[/center] 过去10年来,一些重点治疗领域给跨国制药行业的巨头们带来了丰厚的利润。但是,十年河东十年河西,随着经营环境的变化,它们正在放弃这些领域里的研发活动,转向那些更加有利可图的疾病,如抗癌和抗老年痴呆症治疗药物等。这同时又可以顺应风险规避意识越来越强的监管部门。 最近一段时间,礼来、雅培、惠氏和辉瑞等公司纷纷宣布削减对“初级保健药物”的研发投入,这些药物主要是被用来治疗从咳嗽感冒到心脏病和高胆固醇之类的疾病。相反,它们开始钟情于更加致命的疾病的药物,这样更容易获得监管部门的批准,并且治疗手段更加专业。 “摇钱树”风险增加 市场调研机构Morningstar公司的资深分析师Damien Conover表示,这些制药巨头们希望挖掘那些竞争度相对较低的市场的潜力(比如与胆固醇治疗相比),尤其是抗癌和抗老年痴呆症治疗市场。以往,制药公司总是认为,开发抗癌和抗老年痴呆症药物的成本过于昂贵,因为使用这些药物的患者相对较少。但是,随着全球人口的老龄化,遭受这些疾病侵害的病人很可能明显增加。 促使大型制药公司向新的治疗领域转移的另外一个因素是,在诸如心脏病等以前作为“摇钱树”的治疗领域里,研发出来的新药获批上市的难度日益加大,因为FDA对这类新药可能存在的风险保持了越来越高的警惕性。 FDA之所以对新药审批越发谨慎,是因为近年来制药行业相继发生了一些药物毒副作用事件。在这些事件中,药物的副作用远远超过了它们给病人带来的治疗好处。以关节炎止痛药万络为例,在研究显示该药可能会引起心脏病发作之后,默沙东公司将该药从市场上召回。同样,葛兰素史克公司给它生产的糖尿病治疗药物文迪雅添加了警告标志,因为研究显示:该药会增加病人心脏病发作的几率。 正是这些事件让FDA开始多了一份谨慎,并且对它们来说,在目前情况下也没有多大必要批准另外一只降胆固醇药物,因为现有的药物立普妥已经被证实用来治疗高胆固醇疗效显著,并且相对比较安全。 多重作用推动研发 事实上,根据美国企业公共政策研究所(AEI)研究员Scott Gottlieb发表的一份报告,FDA变得如此小心翼翼,以至于该机构内部负责审批心脏病药物的部门,过去4年来还没有一次性地通过一只心脏病新药上市申请。在FDA药物审查小组中,负责心脏病药物审查的小组所面临的任务最为艰巨。 但是,在对待抗癌药物和抗老年痴呆症药物的审批上,FDA似乎更愿意采取折衷的做法,因为目前市场上并没有多少用于治疗这些疾病的药物,并且这些疾病更为致命。 Gottlieb表示,当一只抗癌药物引起一些罕见但却是破坏性的副作用时,人们往往不会给予过多关注;但是如果一种感冒药(或是常规止痛药)出现了问题,情况完全相反。 对制药公司来说,进军这些新的治疗领域还有另外一个优点:由于癌症和老年痴呆症的致命性,它们可以给治疗药物设定更高的售价。因此,虽然使用的病人相对较少,但它们仍然可以从中收获一只“重磅炸弹”药物。 伊利诺伊州小型生物科技企业Advanced Life Sciences公司董事及总裁John Flavin表示,抗癌和抗老年痴呆症药物往往也是患者余下的生命里每天都要使用的药物,这一特点将使它们变得更加有利可图。 Edward Jones & Co公司分析师Linda Bannister表示,大型制药公司还将从转向专业药物中得益,因为向数量相对较少的肿瘤医生和老年痴呆症治疗专家推销一只药物的成本要小得多。相反,由于初级保健医生数量庞大,推销初级保健药物时必须接触的对象也就很多。 医药市场研究机构IMS Health公司认为,制药公司肯定将从这种战略中获取丰厚的利润。根据该公司提供的数据,从现在起到2012年,全球抗癌药的销售额将以年均复合增长率12%~15%的增长,这几乎高于整个医药市场增长率的近一倍。今年,全球抗癌市场的规模预计超过480亿美元,因此,根据上述预测,到了2012年,这一市场规模将跃升到750亿~800亿美元。 初级保健受影响 不过,大型制药公司在转向开发用来治疗这些致命疾病的药物的过程中也会带来一些社会风险:虽然受到这些致命疾病打击的小部分病人将得到帮助,但随着制药公司放弃对初级保健药物的研发,社会一般人群的健康也许将由此受到影响。 Gottlieb表示,即使疗效稍好一点的初级保健药物(比如用于治疗疼痛或高血压的新一代药物)只带来轻微的改进,但它们在庞大人群中产生的累积效果是相当巨大的。如果大型制药公司放弃对这些药物的研发,那么,病人将会失去解决生活中遇到的日常医疗问题的机会。 但是,制药公司却提供了另外一种可能性,它们表示,虽然大型制药公司也许将它们的研发重点从初级保健药物转向了专业药物,但初级保健药物的研发不会处于停滞状态,市场的空缺将由小型生物科技企业承担。 这种情况正好在雅培和Advanced Life Sciences公司之间得到印证。雅培将一只很有希望的抗生素新药Cethromycin的开发权出售给了Advanced Life Sciences公司,从而能使自己放手在新的治疗领域里寻找药物。经过多年的开发,Advanced Life Sciences公司向FDA提交了新药审批申请,并且有希望在2009年晚些时候开始销售用于治疗肺炎的Cethromycin。 对此,Edward Jones & Co公司分析师Linda Bannister表示,随着大型制药公司放弃对某些治疗领域(甚至像心脏病这些有潜在致命性的疾病)的研发,病人和广大股东最终都有可能从中得益。 她说,制药公司已经在心血管治疗领域里取得了很大的成绩,然而用于治疗癌症的药物仍然相对偏少,研发重点的转移对病人和制药公司来说都是一种好的结局,可以实现双赢。 但是,Gottlieb却有不同的看法:大型制药公司投入巨资对普通疾病进行研究的日子正在结束,这是因为我们也许想当然地认为广大公众已经在这些治疗领域里获得了公共健康的好处。 信息来源:医药经济报
新浪科技讯 北京时间5月15日消息,目前在哥伦比亚,经常有人在大街小巷兜售一种危险药物,它不仅控制人的自由意志,还能清除受害者的记忆。这位药物名为莨菪碱,它还有个俗称叫“魔鬼呼吸”,源自一种非常特殊、常见于南美洲的树。 有关这种药物的故事是城市传闻的素材。在有人讲述的恐怖故事中,服用魔鬼呼吸的受害者遭到强奸,同意别人把自己在银行里存的钱取走,甚至同意“捐”出自己的器官。《恶习》(Vice)杂志的赖安-达菲去哥伦比亚旅行时发现了许多这种强效药。通过采访受害人和出售这种药物的当事人,他揭露了哥伦比亚药物世界鲜为人知的惊人文化。 哥伦比亚首都波哥大毒品走私犯迪蒙西亚-布兰克表示,这是一种十分可怕的药物,因为它使用起来非常简单,让人防不胜防。他对《恶习》杂志说:“把莨菪碱吹到街上行人的脸上,几分钟内药性发作,就能将人控制。莨菪碱无色无味,难以发现。只要人受到这种药物的影响,你就可以带他们去任何地方。他们会像孩子一样听话。1克莨菪碱类似于1克可卡因,但后期它比炭疽病还严重。高剂量的莨菪碱能致命。”布兰克指出,这种药物使人完全变成行尸走肉,阻止受害人产生记忆。所以药效消失后,受害人根本记不起发生了什么。 一位受害人对《恶习》说,在街上一名男子走过来向她问路,由于那个地方并不远,她就带他来到询问地点,后来他们一起喝了点果汁。接下来,她带这名陌生男子来到她家,帮他把所有财产收集起来,其中包括存款和男友的相机等。这名女子说:“丢了钱令人痛苦,但我觉得自己非常幸运,没有失去更重要的东西。” 《英国临床药理学杂志》报道,这种又叫天仙子碱的药物产生的失忆功效和安定药一样。在古代,已死哥伦比亚领导人的情人被服用这种药物,然后有人让她们进入主人坟墓,将其活埋。以前,美国中央情报局把这种药物用作“冷战”审讯的工具,它的用途类似于使人吐露实情的麻醉药。 由于含有的特殊化学成分,这种药物还能使人产生强烈幻觉。在哥伦比亚常见的Borrachero是莨菪碱的来源,可粗略地译为“使你醉倒”的树。它那绿色树冠和很大的黄花以及白花看起来非常迷人,但哥伦比亚的母亲都警告她们的孩子不要睡在这种树的下面。专家对哥伦比亚充斥和莨菪碱有关的犯罪活动的原因感到困惑,却断言这和这个国家以前混乱的药物文化以及正在发生的内战有关。
求助:我现在正在做大环内酯类的药物检测,可是提取的回收率太低,用的是乙腈提取,请问是怎么回事?
聚乙二醇在药物制剂中的应用摘自《中国药剂学杂志》 作者:张 伟 聚乙二醇(polyethylene glycol,PEG)别名聚氧乙烯醇或聚氧乙烯二醇,系环氧乙烷与单乙二醇(或双乙二醇)在碱性催化剂催化之下聚合而成,分子质量因聚合度不同而异,通常在200~35 000之间,其化学通式为HOCH2(CH2 OCH2)n CH2OH。PEG 的性质随分子质量而变化,目前常见的PEG种类有PEG200、PEG300、PEG400、PEG600、PEG2 000、PEG4 000、PEG6 000、PEG8 000 等。[color=#DC143C]1 药物溶剂[/color]PEG200、PEG300、PEG400、PEG600 系无色、略有微臭的粘性液体,化学性质稳定,安全低毒,故常作为药物的溶剂。另外,为了增加难溶性药物的溶解度,常使用潜溶剂即乙醇、甘油、丙二醇、苯甲醇、聚乙二醇等与水组成的混合溶剂。[color=#00008B]1.1 用于软胶囊剂[/color]软胶囊剂的囊材多以一定比例的明胶、增塑剂和水等组成,因此对蛋白质性质无影响的药物和附加剂均可填充。如各种油类、液态药物、药物溶液、药物混悬液和固体药物等。由于低分子质量PEG 能与水混溶,故是水溶性药物和某些有机药物很好的溶剂,如硝苯地平软胶囊。目前,软胶囊剂多为固体药物粉末混悬在油性或非油性(PEG400 等)分散介质中包制而成。另有报道,水合氯醛应用聚乙二醇作为溶剂可大大降低它对明胶蛋白的分解作用[1]。[color=#DC143C]1.2 用于注射剂[/color]由于PEG200~PEG600 可提高难溶性药物的溶解度且对水不稳定药物有稳定作用,故可作为注射用溶剂。单一以PEG 作为注射用溶剂的注射剂并不多见,如噻替哌注射液以PEG400 或PEG600作为溶剂,可避免噻替哌在水中的聚结沉降作用;盐酸苄去氢骆驼莲碱注射液以PEG200 作为溶剂,安全稳定,贮放2 a保持不变。但一般多用混合溶剂(潜溶剂),如以V(PEG300):V(苯甲醇):V(丙二醇) = 80:5:15 时可作为质量分数为5 %黄体酮或睾丸酮注射液的混合溶剂,此2 种注射液经肌肉注射后,与体液接触即在局部析出药物沉淀,形成药物仓库,逐渐从组织中释放,具有长效作用[2]。市售商品有病毒灵注射液、安乃近注射液、痢菌净注射液、穿心莲注射液、菌毒杀星注射液等。[color=#00008B]1.3 用于滴眼剂[/color]研究表明,以PEG400 为溶剂,可制成吲哚美辛滴眼剂。对此滴眼剂进行的稳定性研究结果表明,PEG400 处方优于Span80 处方[3]。另外,PEG 可作为滴眼剂中的增稠剂,增加粘度,使药物在眼内停留时间延长,从而增加药效,减少刺激作用。[color=#DC143C]2 润滑剂与粘合剂[/color]PEG4 000、PEG6 000 是片剂中水溶性润滑剂的典型代表,在片剂处方中可直接加入适量聚乙二醇进行整粒,也可将其先配成醇溶液、混悬液或乳液进行制粒,润滑效果不变。利用聚乙二醇制得片剂的崩解和溶出不受影响,可提高主药在胃内的溶解性,最终有助于增加生物利用度。近年来,聚乙二醇在片剂中的使用越来越广泛,它们不仅可用作润滑剂,还可作为粘合剂,以PEG4 000 最为常用。如以PEG4 000 为粘合剂(熔点较低,在高速搅拌下呈熔融态),α-乳糖为填充剂,交联聚乙烯吡咯烷酮为崩解剂,硬脂酸镁为润滑剂,采用熔融制粒法可制备卡马西平速释片[4]。另外对于热不稳定药物,若采用PEG4 000 为粘合剂,可在干燥状态下进行粉末直接压片,效果较为理想。市售商品主要有痢菌净片、多钙片、钙中钙片、痢特灵片等。
近几年频频出现药物制剂中检出基因毒性杂质残留而被召回的事件。何为基因毒性杂质呢?“基因毒性杂质”(又称遗传毒性杂质Genotoxic Impurity ,GTI),是指本身直接或间接损伤细胞DNA,产生基因突变或体内诱变,具有致癌可能或者倾向的化合物。其主要来源为原料药合成过程中的起始物料、中间体、试剂和反应副产物,此外,药物在合成、储存或者制剂过程中也可能因为降解而产生基因毒性杂质,因其特点为毒性极强,在很低浓度时即可造成人体遗传物质的损伤,进而导致基因突变并可能促使肿瘤的发生,对用药的安全性产生了强烈的威胁。化学药品中的典型基因毒性杂质包括亚硝胺类杂质和磺酸酯类杂质,它们经过代谢激活后基因毒性非常强,是药物研发过程当中最易产生且需严格把控的基因毒性杂质。因此,各国的法规机构如ICH、FDA、EMA等都对基因毒性杂质提出了明确的要求,越来越多的药企在创新药和仿制药研发过程中也更加关注基因毒性杂质的控制和检测。2020 版《中国药典》四部通则中新增了《遗传毒性杂质控制指导原则》,本指导原则对基因毒性杂质的监管策略与ICH M7指导原则几乎保持一致。2020年5月国家药监局药审中心网站发布了《化学药物中亚硝胺类杂质研究技术指导原则》,该原则为注册申请上市以及已上市化学药品中亚硝胺类杂质的研究和控制提供了指导。在理论上,大部分药物都存在残留基因毒性杂质或被基因毒性杂质污染的风险,因此建立便捷、高效的分析方法是非常有必要的。
[center]2009年我国将制订并颁布国家基本药物目录[/center]卫生部部长陈竺8日在2009年全国卫生工作会上表示,我国将制订并颁布国家基本药物目录(2009版)。 他指出,卫生部将会同有关部门制订国家基本药物目录管理办法和生产供应招投标管理办法,完善基本药物价格形成机制、使用报销政策和国家储备制度。 “建立国家基本药物制度,对于保障人民群众用药的公平可及和安全有效,降低群众用药负担具有重要意义。”陈竺说。 陈竺指出,加快建设国家基本药物制度,还要建立健全药物政策和基本药物制度管理机构,组建国家基本药物委员会,建立健全国家基本药物目录遴选并定期调整机制和部门协同工作机制。要制订医疗机构的基本药物优先选择和合理使用政策及措施,明确规定不同规模、不同层级医疗卫生机构的基本药物配备率和使用率;政府举办的基层医疗卫生机构原则上全部配备使用基本药物;加强基本药物生产和配送合同管理。要开展合理用药舆论宣传与教育引导工作,提高公众对基本药物制度的认知度和对基本药物的信赖度。 他表示,将选择部分地区开展基本药物制度试点,总结经验,不断完善,逐步推广。 信息来源:新华网
求助 :最新化学药物稳定性技术指导原则与药物质量试验控制分析验测实务全书,电子版,谢谢
[size=4](一)药物代谢的遗传多态性[/size][size=4]由于肝脏药酶系特别是P450的遗传多态性,以致造成药物代谢的个体差异,这影响了药物的药理作用、不良反应和致癌的易感性等。对某些药代谢的缺陷者称为:弱代谢者(poor metabolizer)或PM-表型1,而强代谢者(extensive metabolizer)称为EM-表型。在第一相中的药物代谢多态性以异喹胍和乙妥英为例,分别为P450UD6和P4502C的变异。对异喹胍的羟化作用有遗传性缺陷的个体,在应用β-受体拮抗剂、三环类抗郁剂、某些膜抑制抗心律紊乱药、抗高血压药和钙离子拮抗剂等,由于药物代谢的异常,使药效增强、时间延长,容易发生不良反应。在第二相反应的药物代谢多态性,以异烟肼和磺胺二甲嘧啶为例,可区分为乙酰化快型和慢型两种,慢型乙酰化个体长期服用肼苯达嗪和普鲁卡因酰胺后可产生红斑狼疮综合征,服异烟肼后易发生周围神经病变(表2-4)。P4501A1,P4501A2是芳香碳氢化合物羟化酶,激活某些致癌原,其遗传变异与某些癌的易患性有关。[/size][align=center][size=4]表2-4 遗传多态性与药物代谢[/size][/align][table][tr][td=1,1,126][size=4]代谢途径[/size][/td][td=1,1,158][size=4]药物举例[/size][/td][td=1,1,142][size=4]人群中的频率(%)[/size][/td][td=1,1,142][size=4]酶[/size][/td][/tr][tr][td=1,1,126][size=4]C-氧化[/size][/td][td=1,1,158][size=4]异喹胍,金雀花碱,右旋甲吗喃,阿片类[/size][/td][td=1,1,142][size=4]白种人5-10[/size][/td][td=1,1,142][size=4]CYP4502D6[/size][/td][/tr][tr][td=1,1,126][size=4]C-氧化[/size][/td][td=1,1,158][size=4]β-肾上腺受体拮抗剂,乙妥英,甲苯巴比士[/size][/td][td=1,1,142][size=4]白种人4[/size][/td][td=1,1,142][size=4]CYP4502C[/size][/td][/tr][tr][td=1,1,126][size=4]乙酰化[/size][/td][td=1,1,158][size=4]环已巴比土,异烟肼,磺胺二甲嘧啶,咖啡因[/size][/td][td=1,1,142][size=4]日本人10[/size][/td][td=1,1,142][size=4]N-乙酰基转移酶白种人30-70[/size][/td][/tr][/table]
简单介绍一下关于药物高通量筛选技术的知识一.概念高通量筛选(High throughput screening,HTS)技术是指以分子水平和细胞水平的实验方法为基础,以微板形式作为实验工具载体,以自动化操作系统执行试验过程,以灵敏快速的检测仪器采集实验结果数据,以计算机对实验数据进行分析处理,同一时间对数以千万样品检测,并以相应的数据库支持整个体系运转的技术体系。二. 高通量筛选技术体系的组成1. 化合物样品库化合物样品主要有人工合成和从天然产物中分离纯化两个来源。其中,人工合成又可分为常规化学合成和组合化学合成两种方法。2.自动化的操作系统自动化操作系统利用计算机通过操作软件控制整个实验过程。操作软件采用实物图像代表实验用具,简洁明了的图示代表机器的动作。自动化操作系统的工作能力取决于系统的组分,根据需要可配置加样、冲洗、温解、离心等设备以进行相应的工作。3.高灵敏度的检测系统检测系统一般采用液闪计数器、化学发光检测计数器、宽谱带分光光度仪、荧光光度仪等。4.数据库管理系统数据库管理系统承担4个方面的功能: 样品库的管理功能;生物活性信息的管理功能; 对高通量药物筛选的服务功能; 药物设计与药物发现功能。三. 高通量筛选模型常用的筛选模型都在分子水平和细胞水平,观察的是药物与分子靶点的相互作用,能够直接认识药物的基本作用机制。1. 分子水平的药物筛选模型:受体筛选模型;酶筛选模型;离子通道筛选模型1.1受体筛选模型:指受体与放射性配体结合模型。以受体为作用靶的筛选方法,包括检测功能反应、第二信使生成和标记配体与受体相互作用等不同类型。1.2酶筛选模型:观察药物对酶活性的影响。根据酶的特点,酶的反应底物,产物都可以作为检测指标,并由此确定反应速度。典型的酶筛选包括1) 适当缓冲液中孵化;(2)控制反应速度,如:温度,缓冲液的pH值和酶的浓度等;(3)单时间点数器, 需测量产物的增加和底物的减少。1.3离子通道筛选模型: (1)贝类动物毒素的高通量筛选,其作用靶为Na+通道上的蛤蚌毒素结合位点,用放射性配体进行竞争性结合试验考察受试样品。(2)用酵母双杂交的方法高通量筛选干扰N型钙通道β3亚单位与α1β亚单位相互作用的小分子,寻找新型钙通道拮抗剂。2.细胞水平药物筛选模型观察被筛样品对细胞的作用,但不能反映药物作用的具体途径和靶标,仅反映药物对细胞生长等过程的综合作用。包括: 内皮细胞激活; 细胞凋亡; 抗肿瘤活性; 转录调控检测; 信号转导通路; 细菌蛋白分泌; 细菌生长。四.问题及展望高通量筛选技术与传统的药物筛选方法相比有以下几个优点:反应体积小;自动化;灵敏快速检测;高度特异性。但是,高通量筛选作为药物筛选的一种方法,并不是一种万能的手段,特别是在中药研究方面,其局限性也是十分明显的。首先,高通量筛选所采用的主要是分子、细胞水平的体外实验模型,因此任何模型都不可能充分反映药物的全面药理作用;其次,用于高通量筛选的模型是有限的和不断发展的,要建立反映机体全部生理机能或药物对整个机体作用的理想模型,也是不现实的。但我们应该相信,随着对高通量筛选研究的不断深入,随着对筛选模型的评价标准、新的药物作用靶点的发现以及筛选模型的新颖性和实用性的统一,高通量筛选技术必将在未来的药物研究中发挥越来越重要的作用。
各位老师: 请问:家禽养殖过程中要使用若干药物,能否用液相或气相检测这些药物中是否含有呋喃类、喹诺酮类、磺胺类?谢谢。
皮肤给药。 (2)药物的理化性质。 药物的吸收不决定于其在胃肠道的总浓度,而是取决于可吸收的,即非解离的药物浓度,也就是取决于药物的pka值与吸收部位的ph值。同时,药物脂溶性愈大 则愈易吸收;溶解速率愈大愈吸收得快。对难溶性固体药物而言,其粉末愈细,粒径愈小,比表面积愈大,溶解速度愈快,药物吸收速度也愈快,吸收量愈多,药效 就愈好。 (3)赋形剂。制备药剂时,往往要用某些赋形剂,他们不仅影响到生产工艺及制剂的外观性质,如:硬度、粘度、光 泽、颜色、味道等方面,而且会改变制剂的溶出速率、生物利用度,从而影响制剂的疗效。例如:乳糖是一种比较理想的常用赋形剂,用于睾丸酮片,有加速吸收的 作用;而用于异烟肼片,其疗效完全被乳糖阻碍 药物相互作用对疗效的影响 药物的相 互作用系指一种药物的作用,被同时应用的另一种药物所改变。近年来,临床上联合应用多种药物治疗某患者的一种疾病的现象日益增多。这些药物同时服用后,由 于药物间相互作用,有的产生协同作用,增强疗效;但也有的产生拮抗作用,使疗效降低,甚至会产生毒性,带来毒副反应。例如:咖啡因与麦角胺合用时,溶解度 加大,吸收增加,疗效提高。又如,洋地黄与氯噻嗪、氯噻酮、喹噻酮、利尿酸、速尿等高效利尿药合用治疗心脏性水肿时,往往造成血钾过低,增加心脏对洋地黄 的敏感性,引起中毒反应。
化学药物主要包括化学合成的原料药物(即药物化合物)及其制剂。化学药物发明专利申请就包括原料药物及其制剂本身的发明。也包括这些化合物及其制剂的制备方法和用途的发明。一、化学药物发明专利申请的概况 1、申请的数量 2001年涉及药物的总申请量(包括药物化合物、西药、中药、生化药物)为5155件,其中国内为3776件,国外1379件;我们西药处2001年申请总量1733件,PCT申请985件,占56.84%,国内申请612件,占35.31%。 2、国内外比例 对于制剂而言,94年之前,国内外申请比例约为1:l;94年之后,我国加入国际合作条约之后,PCT申请进入我国的申请量剧增,占据制剂申请总量的60%,再加上非PCT的国外申请,国外申请占申请总数的70%以上;国内申请只占30%以下。而对于原料药物的专利申请来说,国外申请所占比例更大。加入WTO后,更多国外企业将来我国需求市场,这样必定有更多的专利申请进入我国。
求助!!!不溶于水的脂溶性药物,查到它的pka是8.13呈现碱性,用MCX小柱过柱,5%氨化甲醇洗脱,备用液为了提高极性是80%甲醇水复溶(每100毫升含有50微升甲酸),结果柱回收率只有70左右,要怎么提高啊?或者有没有简便的看甲醇水里面的甲酸含量能不能使药物完全离子化的方法啊?