要做个吗啡的定量检测,我用安捷伦6890N ,我内标用的是SKF,也知道了吗啡的峰,请问我需要怎么才能定量,以前只会做定性,谁叫我下啊?我已经配了吗啡1mg/ml和SFK 1mg/ml的液体,怎么用?
视频参赛,吗啡可待因快检!
可待因 蒂巴因 吗啡下游产品有哪些?医药或其他
中国科技网讯 据物理学家组织网8月15日(北京时间)报道,一个国际研究小组获得了重大突破,他们发现了人体免疫系统放大对阿片类药物依赖性的关键机制,并证实可通过药物来阻断吗啡和海洛因成瘾,同时帮助缓解疼痛。临床试验预计将在未来18个月内进行。 澳大利亚阿德莱德大学和美国科罗拉多大学博尔德分校的科学家通过实验室研究发现,一种名为纳洛酮的药物可以选择性地阻断免疫成瘾反应。这项发表于《神经科学杂志》的新成果有望带来“二合一”型药物,既可缓解病人的剧烈疼痛症状,又能帮助海洛因成瘾者戒除药物依赖。 “我们的研究确凿地表明,我们可以通过大脑的免疫系统来阻止成瘾,而不针对大脑的神经系统。”研究论文的主要作者、阿德莱德大学医学院的马克·哈钦森说,“在成瘾过程中,中枢神经系统和免疫系统都发挥着重要作用,但我们的研究显示,只需阻止大脑中的免疫反应,就能阻断对阿片类药物的渴望。” 该团队将研究重点放在名为TLR4的免疫受体上。“阿片类药物,比如吗啡和海洛因,绑定TLR4受体的方式与免疫系统对细菌的正常反应相同,但问题是,TLR4随即变成了药物依赖性的放大器。”哈钦森说。 哈钦森表示,纳洛酮能够自动关闭对药物的依赖,它减少了对阿片类药物的需要以及与成瘾相关的行为,同时,大脑中的神经化学也在发生变化——大脑不再生产多巴胺了,这种重要的化学物质能够向大脑传递服用药物后的兴奋感。 研究论文的另一作者、科罗拉多大学博尔德分校神经科学中心教授琳达·沃特金斯说:“这项工作从根本上改变了我们对阿片类药物、奖励和上瘾机制的了解,多年来我们一直在怀疑TLR4可能是阻断阿片类药物成瘾的关键,现在我们掌握了证据。” 沃特金斯表示,用来阻止成瘾的药物纳洛酮是上世纪70年代发明的一种非阿片类镜像药物,他们相信可以将它与吗啡合用,进而开发出帮助患者缓解剧烈疼痛的同时又不至于让人上瘾的新止疼药物。(记者 陈丹) 总编辑圈点 药物成瘾是一个引人入胜的科学课题,因为对它的研究可以揭示出大脑运作是多么复杂。如哈钦森团队揭示的,药物依赖的形成不光涉及中枢神经,其关键一环是免疫受体发挥作用。相关实验不光证明,纳洛酮与吗啡共用可避免成瘾,还为今后研制戒毒新药提供了思路。或许有一天,在药物成瘾与戒断机理完全揭示之后,人类将告别毒品引发的生理痛苦。 《科技日报》(2012-08-16 一版)
做一个毒物混标,混标里面有吗啡。毛发基质中吗啡定量离子对出峰前面还有一个峰,乙腈溶解的混标就没有。吗啡毛发基质混标分别走了乙酸胺和甲酸乙酸胺两个流动相两张图都附上了,这是基质杂质影响吗[img]https://ng1.17img.cn/bbsfiles/images/2020/07/202007031811420709_1257_3381572_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2020/07/202007031811430201_7336_3381572_3.png[/img]
[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相[/color][/url]检测残留溶剂时,其中吗啡林不出峰,会是什么原因呢?请大神提出意见吧!
自制火锅底料中的罂粟碱、吗啡、那可丁、可待因和蒂巴因检测中吗啡标准品从哪里买啊?只是检测罂粟壳带入的成分吗?
罂粟蒴果中可待因、吗啡、罂粟碱的GC-MS检验罂粟含有丰富的吗啡等吗啡型生物碱,为一年生草本,有乳状液体,茎自基部分枝,高60-120cm ,有白霜,无毛,下部叶有叶柄,上部叶抱茎,心脏形,有不对称粗齿,蒴果球形,直径2.5-5cm ,花期4-5月,果期6-8月。随着我国禁毒工作的不断深入,在铲除非法种植dupin原植物的同时,在法庭科学上,须对这类植物进行相关生物碱的检验。本文介绍了利用GC-MS对罂粟蒴果中可待因、吗啡、罂粟碱进行检测,方法简单。1 实验部分1.1仪器与试剂Varin3900 /2100GC-MS. 甲醇,丙酮,无水硫酸钠,均为分析纯。三种标准品均从公安部物证鉴定中心购得。1.2实验条件气相色谱条件:DB-5 30m X0.25mmX0.32 um 弹性石英毛细管柱;柱温:80℃(1min)20℃/min280℃(19min);进样口温度:250℃;分流比40:1;载气:高纯氦;进样量1ul.质谱条件:传输线温度240℃,离子阱温度150℃,EI源(70eV),扫描范围40-550amu.1.3检材的提取与净化取检材2-5克,加10克无水硫酸钠研磨,以丙酮提取,过滤,水浴或微波挥干,1ml甲醇溶解待检。2 结果与讨论该法中,罂粟蒴果中可待因、吗啡、罂粟碱的保留时间分别为12.33min、12.70min、16.26min,离子碎片峰依次为:可待因m/z299、162、124;吗啡285、162、215、124;罂粟碱339、324、308、292、266等。
求助仪器信息网的诸位大神:检测水中的吗啡用哪个SPE柱最合适,有没有做过这种实验的大拿,帮忙解释一下具体情况,感谢!!!
我现在在做中药,其中要检测吗啡和罂粟碱的含量,问题是流动相一直没有找到好的组合,另外对照品只有盐酸罂粟碱,不知道盐酸罂粟碱和罂粟碱的出峰时间差多大,希望各位高手i能帮忙给个好建议

10,抽取5个版友);中奖名单:zgx3025(注册ID:v2844608)吕梁山(注册ID:shih20j07)大川之子,纵横四海(注册ID:chuangu120)dahua1981(注册ID:dahua1981)捌道巴拉巴巴巴(注册ID:v3082413)http://ng1.17img.cn/bbsfiles/images/2016/12/201612071513_01_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/12/201612071513_02_1610895_3.jpg【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================复方甘草片中的吗啡含量测定方法:SPE基质:药品应用编号:101793化合物:吗啡固定相:ProElut C18-U色谱柱/前处理小柱:ProElut C18-U 1000mg/6ml 30/pkg样品前处理:样品制备:取固相萃取柱(ProElut C18-U 1 g/6 mL Cat#:63506) 一支,依次用甲醇-水(3:1)15 ml及水5 ml冲洗,再用pH值约为9的氨水溶液(取水适量滴加氨试液至pH值约为9)冲洗至流出液pH值约为9(约10 mL),待用。取本品20片,精密称定,研细,精密称取约10片量,置磨口锥形瓶中,精密加水90ml,超声处理5分钟,精密加稀盐酸(6→10)10ml,摇匀,超声处理20分钟,使吗啡溶解,取出,放至室温,滤过,精密量取续滤液1.0ml,置上述固相柱上,滴加氨试液(300 μL)适量使柱内溶液的pH值约为9(上样前应取同体积续滤液预先调试,以确定滴加氨试液的量),摇匀,待溶剂滴尽后,用水约20ml冲洗,用含2%甲醇的5%醋酸溶液洗脱,用5ml量瓶收集洗脱液至刻度,摇匀,即得。对照品配制:另取吗啡对照品适量,精密称定,用含2%甲醇的5%醋酸溶液溶解并定量稀释制成每1ml中约含吗啡0.01mg的溶液,同法测定。色谱条件:分析条件 色谱柱:Inspire C8,250×4.6 mm,5 μm (Cat#:81106) 流动相:0.05mol/L KH2PO4:0.0025庚烷磺酸钠水溶液:乙腈=5:5:2 流 速:1.0 mL/min 柱 温:30 ℃ 检测器:UV 220 nm 进样量:10 μL文章出处:天津迪马实验室关键字:复方甘草片中,吗啡,2010药典,Inspire C8,81106,ProElut C18-U,63506摘要:复方甘草片中的吗啡含量测定谱图:http://www.dikma.com.cn/Public/Uploads/images/mafei(1).PNG图例:吗啡
本人现在急需MSTFA和0-6吗啡衍生化反应的产物质朴图,高抬贵手,,,谢谢
盐酸吗啡是否可以不用衍生化,用OV-17柱子直接进样检测?
要做复方甘草片吗啡的含量测定了,不知道买什么品牌什么规格的c18固相萃取柱好?请大家赐教!
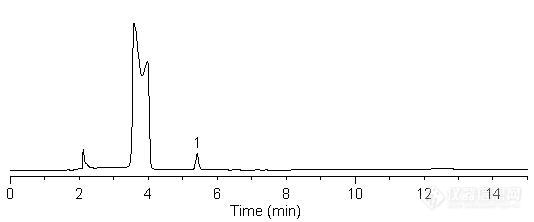
复方甘草片中的吗啡含量测定DM-93样品制备 制备方法: 吗啡含量测定:样品制备:取固相萃取柱(ProElut C18-U 1 g/6 mL) 一支,依次用甲醇-水(3:1)15 ml及水5 ml冲洗,再用pH值约为9的氨水溶液(取水适量滴加氨试液至pH值约为9)冲洗至流出液pH值约为9(约10 mL),待用。取本品20片,精密称定,研细,精密称取约10片量,置磨口锥形瓶中,精密加水90ml,超声处理5分钟,精密加稀盐酸(6→10)10ml,摇匀,超声处理20分钟,使吗啡溶解,取出,放至室温,滤过,精密量取续滤液1.0ml,置上述固相柱上,滴加氨试液(300 μL)适量使柱内溶液的pH值约为9(上样前应取同体积续滤液预先调试,以确定滴加氨试液的量),摇匀,待溶剂滴尽后,用水约20ml冲洗,用含2%甲醇的5%醋酸溶液洗脱,用5ml量瓶收集洗脱液至刻度,摇匀,即得。对照品配制:另取吗啡对照品适量,精密称定,用含2%甲醇的5%醋酸溶液溶解并定量稀释制成每1ml中约含吗啡0.01mg的溶液,同法测定。 分析条件 色谱柱:Inspire C8,250×4.6 mm,5 μm (Cat#:81106)流动相: 0.05mol/L KH2PO4:0.0025庚烷磺酸钠水溶液:乙腈=5:5:2 流速: 1.0 mL/min 柱温: 30 ℃ 检测器: UV 220 nm 进样量: 10 μL 吗啡对照: http://ng1.17img.cn/bbsfiles/images/2012/06/201206151459_372651_2370618_3.jpg1-吗啡 峰号 保留时间 min 峰面积μV*s 峰高mV 理论塔板数N USP拖尾因子 分离度 1 5.349 581405 94977 14928.574 1.141 复方甘草片样品: http://ng1.17img.cn/bbsfiles/images/2012/06/201206151459_372652_2370618_3.jpg1-吗啡 &#
《国食药监食 3 号/附件 3:火锅食品中罂粟碱、吗啡、那可丁、可待因和蒂巴因的测定》有谁能提供一下这个方法的文本?谢谢
复方对乙酰氨基酚片含测中咖啡因的含量,滴定时,老是偏高,怎么回事哦
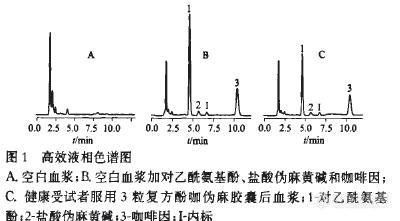
【作者】 胡晓; 张丽芳; 温金华; 蔡军;【机构】 南昌大学医学院临床药理研究所;【摘要】 目的:建立一种同时测定人血浆中对乙酰氨基酚、伪麻黄碱和咖啡因的高效液相色谱(HPLC)法,并用于含上述组分的复方制剂的人体药动学研究。方法:以茶碱为内标,血样经醋酸乙酯提取后,采用高效液相色谱紫外(HPLC-UV)法进行测定。色谱柱为Diamonsil C18柱(4.6mm×150mm,5μm);流动相为甲醇-0.05mol.L-1磷酸二氢钾(23∶77,pH2.4);流速1mL.min-1。检测波长210nm。结果:人血浆中对乙酰氨基酚、盐酸伪麻黄碱和咖啡因质量浓度测定的线性范围分别为0.12~11.52mg.L-1,0.008~0.432mg.L-1和0.03~2.16mg.L-1;最低可定量质量浓度分别为0.12,0.008,0.03mg.L-1;各组分日内、日间RSD均小于15%,方法回收率均大于88%。结论:该方法能快速可靠地同时测定人血浆中对乙酰氨基酚、伪麻黄碱和咖啡因的浓度,可用于含上述组分的复方制剂的人体药动学或生物等效性研究。【关键词】 http://ng1.17img.cn/bbsfiles/images/2012/08/201208142012_383851_1609970_3.jpg
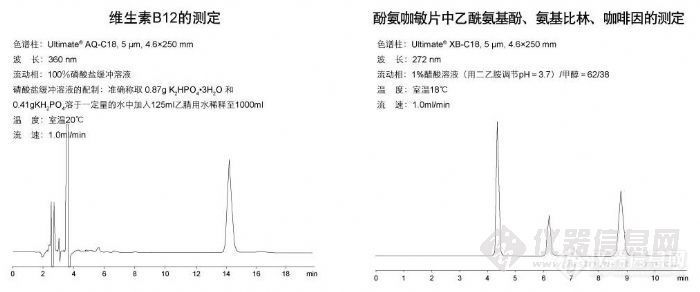
维生素B12的测定和酚氨咖敏片中乙酰氨基酚、氨基比林、咖啡因的测定http://ng1.17img.cn/bbsfiles/images/2009/11/200911021850_180185_1896702_3.jpg
我们公司做毒死蜱,合成工艺第一步是三氯乙酰氯和丙烯腈加成氯苯为溶剂,要根据标样的归一情况来确定投料量。标样里面丙烯腈大约10%三氯乙酰氯3.5%氯苯85%左右,之前一直是这个数据,今天突然三氯乙酰氯就变成2.8左右了。色谱条件是,进样口260,柱温90,检测器260。载气氮气,氢火焰检测器,柱子是SE—30非极性柱,用的空气发生器。仪器是国产的福利GC9790②。还有个问题就是氯苯有时候会出平顶峰,进样量0.2微升不到都平顶。以上两个问题还请各位大侠指导一下。
有没有人用DB 31/2010-2012这个标准[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]法测火锅底料中的罂粟碱、吗啡、可待因、那可丁、蒂巴因的,回收率能做到多少?我们用的净化包做的前处理,其中罂粟碱,那可丁,蒂巴因这三种没有内标物用的外标,回收率比较低,想请教一下是什么原因导致的回收率低?
问题:DB31/ 2010-2012 食品安全地方标准 火锅食品中罂粟碱、吗啡、那可丁、可待因和蒂巴因的测定液相色谱-串联质谱法。 这个标准可以测卤牛肉中的罂粟吗?我的意思是 会不会超范围 检测。标准上 适用于火锅食品 回复1: 明显就不归火锅食品那类呀。回复2: 我们做过,可以的回复3: 这个很简单!要做方法偏离! 偏标是肯定了!要做验证!
邻氯乙酰乙酰苯胺的国标或行标
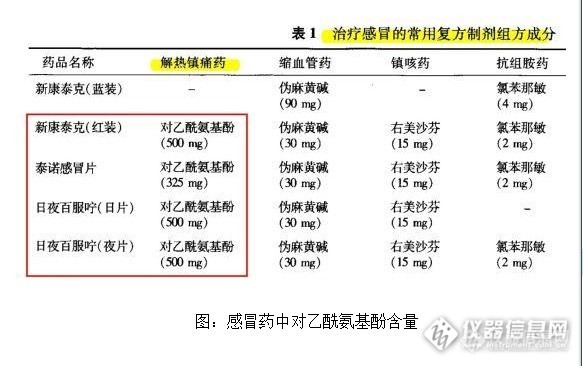
点击查看FDA声明原文 FDA警告,过量服用对乙酰氨基酚药物将会导致肝功能衰竭甚至死亡,高危人群包括在24小时内服用超过处方规定剂量药物的患者,同时服用超过一种含对乙酰氨基酚成分药物的患者,以及在服用含对乙酰氨基酚成分药物时饮用含酒精饮料的患者。 FDA自2011年起开始要求制药企业将对乙酰氨基酚的含量控制在每单位325毫克以内,但截止至2014年1月14日,市场上仍有部分单位对乙酰氨基酚含量超过325毫克的药物正在流通销售。 FDA表示,将在近期启动相关法律程序,禁止开具每单位对乙酰氨基酚含量超过325毫克的药物处方。 国内康泰克、百服宁等超标近54% 调查发现,国内多家知名品牌感冒药的对乙酰氨基酚含量高于每单位325毫克,包括新康泰克、百服宁等。 中美史克生产的新康泰克美扑伪麻片(红装),其每片对乙酰氨基酚含量同样是500毫克。 上海施贵宝制药有限公司生产的日夜百服咛、加合百服宁的每单位对乙酰氨基酚含量为500毫克,超出美国FDA规定含量上限54%。 此外,有多个品牌感冒药的单位对乙酰氨基酚含量达到美FDA规定的上限325毫克,它们分别是:白加黑、泰诺、银得菲。 其他品牌如快克、感康、康必得等单位对乙酰氨基酚含量在250毫克以内。 走访沪上多家药房后发现,最为常见的白加黑、新康泰克等感冒药均为处方药,需要处方及身份证才能购买。 大量非处方药含对乙酰氨基酚 不过,一药房工作人员提醒道,前述感冒药被转为处方药管理,并非缘于对乙酰氨基酚的过量,而是系其含有伪麻黄碱的缘故。 事实上,由于良好的镇痛祛热疗效,对乙酰氨基酚药物使用普及度很高,国内亦将其列为非处方药(OTC),即不需要持有医生处方即能买到,同时也能通过网络合法销售。 搜索淘宝等线上商城后发现,在网上不仅可以随意买到各种各样品牌的对乙酰氨基酚药品,而且购买数量亦完全没有限制。 沪上一医药销售人员表示,由于在各种药物中使用广泛,以及非处方药可以任意购买的缘故,患者容易同时购买多种含有对乙酰氨基酚的药物,导致患者在不知情的情况下过量服用。 根据FDA统计,在1998年至2003年间,对乙酰氨基酚过量服用是导致病人肝衰竭的主要原因。美国疾病控制中心在2007年也曾经发布报告称,全美每年有1600起急性肝功能衰竭,其中对乙酰氨基酚过量服用是最大缘由。 该销售人员解释道,美FDA长期以来都对药物中对乙酰氨基酚的含量作出规定,但因为非处方药的关系,仍有大量患者过量服用,所以FDA将对乙酰氨基酚的含量限制在325毫克以内,也是为了在不影响疗效的情况下尽可能的让患者减少服用,降低副作用。 FDA在此次声明中亦表示,将采取新的行动针对对乙酰氨基酚类的非处方药进行监管。 小知识:对乙酰氨基酚(扑热息痛) 对乙酰氨基酚是乙酰苯胺类解热镇痛药,别名有乙酰氨基酚、扑热息痛、醋氨酚、退热净等。该药具有解热镇痛作用,主要用于缓解轻、中度的疼痛,如关节痛、头痛、神经痛、牙痛及痛经等。 作为非处方药,虽然有质量稳定,疗效确切的优点,但该药的滥用,使用不当也会产生不良反应或严重的肝毒性和肾毒性。 此药对肝损害是最主要的不良反应,其次是引起肾衰,此外也可能导致血小板减少、哮喘发作等症状。 在无其他药物或无酒精干扰情况下,对乙酰氨基酚的安全剂量为:成人口服每次300-600毫克,最大日剂量不超过4000毫克,退热疗程不宜超过3天,镇痛疗程不宜超过5天。儿童12岁以下按体重每次10-15mg/kg,疗程不宜超过3天。 若患者饮酒或空腹或与其他药物有相互作用的药物合用时,应调低剂量或禁用。
[align=center]超高效液相色谱-串联质谱法测定[/align][align=center]火锅底料中罂粟碱、吗啡、那可丁、可待因和蒂巴因的回收率问题研究[/align]摘要:本研究利用Quenchers法对火锅底料样品进行样品前处理,超高效液相色谱-串联质谱法检测,其中罂粟碱、那可丁、蒂巴因采用外标定量法,吗啡和可待因采用内标法定量。实验结果显示在1.0-50.0ng/mL范围内,罂粟碱、那可丁、蒂巴因线性良好,在5.0-250ng/mL范围内,吗啡和可待因线性良好,以阴性样品基质溶液配制的标准溶液进行定量分析,样品回收率在70%~100%之间。关键词:Quenchers 线性范围 回收率[color=#333333]Abstract: the Quenchers method was used in this study to pre-treat the base material samples of hot pot, and to detect by UP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS. Among them, Papaverine, [/color]Noscapine[color=#333333] and Thebaine were quantified by external standard method, while Morphine and Codeine were quantified by internal standard method[color=windowtext].The[/color][/color] experimental results showed that in the range of 1.00-50.0 ng/mL, the linearity of Papaverine, Noscapine and Thebaine was good, and in the range of 5.0-25.0ng/mL, the linearity of Morphine and Codeine was good. Quantified by standard solution of prepared from the negative sample matrix solution , the recovery rate was between 70% to 100%.Key words: Quenchers linear range recovery1. 试剂与材料1.1乙腈:色谱纯1.2甲酸:质谱纯1.3 标准品:罂粟碱、吗啡、那可丁、可待因、蒂巴因混合标准溶液,其中罂粟碱、那可丁、蒂巴因浓度为10 mg/L,吗啡、可待因浓度为50 mg/L。1.4内标物质:吗啡-D3、可待因-D3混合内标溶液20mg/L。1.5 Quenchers净化包:Agela1.6 有机滤膜:0.22 μm2. 仪器设备液相色谱-串联质谱仪 Agilent 6470:带电喷雾离子源(ESI); 分析天平:感量0.001g;离心机:≥10 000 转/分钟;涡旋混合器。3. 试验方法3.1标准溶液的配制:3.1.1 准确吸取罂粟碱、吗啡、那可丁、可待因、蒂巴因混合标准溶液1.00mL至10mL容量瓶中,用甲醇稀释并定容至刻度,得到罂粟碱、那可丁、蒂巴因浓度为1.0μg/mL,吗啡、可待因浓度为5μg/mL的标准混合储备液。再分别准确吸取吗啡-D3、可待因-D3混合内标溶液1.00mL,用甲醇稀释并定容至刻度,得到浓度为2.0μg/mL的内标混合储备液。3.1.2分别精密吸取上述混合标准储备溶液和同位素内标混合储备液(3.1.1)适量,用乙腈(1.1)稀释成罂粟碱、那可丁、蒂巴因浓度为 1.0 ng/mL、2.0 ng/mL、5.0 ng/mL、10.0 ng/mL、20.0 ng/mL、50.0 ng/mL,吗啡、可待因浓度为 5.0 ng/mL、10.0 ng/mL、25.0 ng/mL、50.0 ng/mL、100 ng/mL、250 ng/mL 的系列标准工作溶液,内标溶液浓度均为 50.0 ng/mL。临用新配3.2 提取称取 2 g 火锅底料试样(精确至 0.001 g)于 50 mL 离心管中,加入375 μL[color=red] [/color]同位素内标溶液(3.1.1),再加入 5 mL 水,振摇使分散均匀,加入 15 mL 乙腈,涡旋振荡 5 min,加入Quenchers提取管中提取,涡旋震荡1min,以 4000 转/分钟离心 5 min,取上清液待净化。3.3 净化移取 1.5 mL 上清液至2ml的Quenchers净化管中,涡旋混合 1 min,以 10 000 转/分钟离心 5 min,移取上清液,0.22 μm 有机滤膜过滤,取滤液待测。4. 测定4.1色谱条件1) 色谱柱:UHP HILIC(粒径1.9μm,2.1×100mm)2) 进样量:5 μL;3) 柱 温:40 ℃;4) 流 速:0.3 mL/min;5)流动相:A 相:乙腈,B 相:含 0.1 %甲酸的 10 mmol/L 甲酸铵溶液,按表 1 进行梯度洗脱[align=center]表1梯度洗脱程序[/align][table=568][tr][td][align=center]时间/min[/align][/td][td][align=center]A相[/align][/td][td][align=center]B相[/align][/td][/tr][tr][td][align=center]0[/align][/td][td][align=center]90[/align][/td][td][align=center]10[/align][/td][/tr][tr][td][align=center]0.5[/align][/td][td][align=center]80[/align][/td][td][align=center]20[/align][/td][/tr][tr][td][align=center]2.0[/align][/td][td][align=center]80[/align][/td][td][align=center]20[/align][/td][/tr][tr][td][align=center]2.5[/align][/td][td][align=center]90[/align][/td][td][align=center]10[/align][/td][/tr][tr][td][align=center]4.5[/align][/td][td][align=center]90[/align][/td][td][align=center]10[/align][/td][/tr][/table]4.2 质谱条件1)电离方式:ESI+2)检测方式:多反应监测(MRM)3)雾化气、鞘气:氮气4)干燥气流速:7L/min5)喷雾电压:500V6)干燥器温度:300℃7)鞘气流速:11L/min8)鞘气温度:300℃9)毛细管电压:3500V(+)3000V(-)10)定性离子对、定量离子对、Fregmentor电压及碰撞能量见表2表2定性离子对、定量离子对、Fregmentor电压及碰撞能量[table=577][tr][td][align=center]目标物质[/align][/td][td][align=center]定性离子对(m/z)[/align][/td][td][align=center]定量离子对(m/z)[/align][/td][td][align=center]Fregmentor电压(V)[/align][/td][td][align=center]碰撞能量[/align][align=center](eV)[/align][/td][/tr][tr][td=1,2][align=center]那可丁[/align][/td][td][align=center]414.0/220.0(ESI+)[/align][/td][td=1,2][align=center]414.0/220.0(ESI+)[/align][/td][td][align=center]165[/align][/td][td][align=center]21[/align][/td][/tr][tr][td][align=center]414.0/353.0(ESI+)[/align][/td][td][align=center]165[/align][/td][td][align=center]25[/align][/td][/tr][tr][td=1,2][align=center]罂粟碱[/align][/td][td][align=center]340.4/201.9(ESI+)[/align][/td][td=1,2][align=center]340.4/201.9(ESI+)[/align][/td][td][align=center]160[/align][/td][td][align=center]32[/align][/td][/tr][tr][td][align=center]340.4/171.0(ESI+)[/align][/td][td][align=center]160[/align][/td][td][align=center]36[/align][/td][/tr][tr][td=1,2][align=center]蒂巴因[/align][/td][td][align=center]312.3/58.2(ESI+)[/align][/td][td=1,2][align=center]312.3/58.2(ESI+)[/align][/td][td][align=center]102[/align][/td][td][align=center]11[/align][/td][/tr][tr][td][align=center]312.3/249.0(ESI+)[/align][/td][td][align=center]102[/align][/td][td][align=center]15[/align][/td][/tr][tr][td=1,2][align=center]可待因[/align][/td][td][align=center]300.4/165.0(ESI+)[/align][/td][td=1,2][align=center]300.4/165.0(ESI+)[/align][/td][td][align=center]165[/align][/td][td][align=center]40[/align][/td][/tr][tr][td][align=center]300.4/215.0(ESI+)[/align][/td][td][align=center]165[/align][/td][td][align=center]36[/align][/td][/tr][tr][td=1,2][align=center]吗啡[/align][/td][td][align=center]286.0/164.9(ESI+)[/align][/td][td=1,2][align=center]286.0/164.9(ESI+)[/align][/td][td][align=center]160[/align][/td][td][align=center]41[/align][/td][/tr][tr][td][align=center]286.0/181.0(ESI+)[/align][/td][td][align=center]160[/align][/td][td][align=center]41[/align][/td][/tr][tr][td=1,2][align=center]可待因-D3[/align][/td][td][align=center]303.5/165.0(ESI+)[/align][/td][td=1,2][align=center]303.5/165.0(ESI+)[/align][/td][td][align=center]160[/align][/td][td][align=center]40[/align][/td][/tr][tr][td][align=center]303.5/215.0(ESI+)[/align][/td][td][align=center]160[/align][/td][td][align=center]36[/align][/td][/tr][tr][td=1,2][align=center]吗啡-D3[/align][/td][td][align=center]289.1/165.0(ESI+)[/align][/td][td=1,2][align=center]289.1/165.0(ESI+)[/align][/td][td][align=center]165[/align][/td][td][align=center]40[/align][/td][/tr][tr][td][align=center]289.1/185.0(ESI+)[/align][/td][td][align=center]165[/align][/td][td][align=center]36[/align][/td][/tr][/table]5.线性关系5.1.1 在4.1、4.2的色谱和质谱条件下上机测定甲醇为溶剂配制的标准溶液并建立标准曲线,得到罂粟碱、吗啡、那可丁、可待因、蒂巴因的线性关系R[sup]2[/sup]分别为0.9968、0.9992、0.9958、0.9987、09993,均满足实验要求。5.1.2 在4.1、4.2的色谱和质谱条件下上机测定,以净化包处理过的阴性样品基质溶液为溶剂配制的标准溶液并建立标准曲线,得到罂粟碱、吗啡、那可丁、可待因、蒂巴因的线性关系R[sup]2[/sup]分别为0.9971、0.9998、0.9956、0.9991、09989,均满足实验要求。6.加标回收试验6.1空白加标试验分别向6个50mL空白离心管中加入150μL罂粟碱、那可丁、蒂巴因浓度为1.0μg/mL,吗啡、可待因浓度为5.0μg/mL的标准混合储备液,后按照3.2、3.3的步骤进行处理后上机,以甲醇为溶剂配制的标准溶液进行定量,得到的平均空白回收率如表3:表3:甲醇为溶剂配制的标准溶液测定的空白加标回收率[table][tr][td][align=center]目标物质[/align][/td][td][align=center]添加量(ng/mL)[/align][/td][td][align=center]实测值(ng/mL)[/align][/td][td][align=center]回收率(%)[/align][/td][/tr][tr][td][align=center]那可丁[/align][/td][td][align=center]10[/align][/td][td][align=center]3.86[/align][/td][td][align=center]38.6[/align][/td][/tr][tr][td][align=center]罂粟碱[/align][/td][td][align=center]10[/align][/td][td][align=center]3.97[/align][/td][td][align=center]39.7[/align][/td][/tr][tr][td][align=center]蒂巴因[/align][/td][td][align=center]10[/align][/td][td][align=center]1.96[/align][/td][td][align=center]19.6[/align][/td][/tr][tr][td][align=center]可待因[/align][/td][td][align=center]50[/align][/td][td][align=center]49.32[/align][/td][td][align=center]98.6[/align][/td][/tr][tr][td][align=center]吗啡[/align][/td][td][align=center]50[/align][/td][td][align=center]48.56[/align][/td][td][align=center]97.1[/align][/td][/tr][/table]由表3可得,以甲醇为溶剂配制的标准溶液测定的空白加标回收率中,以内标法定量的吗啡、可待因回收率良好,以外标法定量的罂粟碱、那可丁、蒂巴因回收率太低,达不到标准要求,可见在没有样品基质的条件下净化包中成分对目标物质会有吸附,因此该方法不适合做空白回收试验。6.2阴性样品加标回收试验1分别称取 2 g 火锅底料阴性样品(精确至 0.001 g)于6个不同的 50 mL 离心管中,再分别加入150μL罂粟碱、那可丁、蒂巴因浓度为1.0μg/mL,吗啡、可待因浓度为5.0μg/mL的标准混合储备液,后按照3.2、3.3的步骤进行处理后上机,以甲醇为溶剂配制的标准溶液进行定量,得到阴性样品平均加标回收率如表4:表4:甲醇为溶剂配制的标准溶液测定的阴性样品加标回收率[table][tr][td][align=center]目标物质[/align][/td][td][align=center]添加量(ng/mL)[/align][/td][td][align=center]实测值(ng/mL)[/align][/td][td][align=center]回收率(%)[/align][/td][/tr][tr][td][align=center]那可丁[/align][/td][td][align=center]10[/align][/td][td][align=center]4.62[/align][/td][td][align=center]46.2[/align][/td][/tr][tr][td][align=center]罂粟碱[/align][/td][td][align=center]10[/align][/td][td][align=center]4.35[/align][/td][td][align=center]43.5[/align][/td][/tr][tr][td][align=center]蒂巴因[/align][/td][td][align=center]10[/align][/td][td][align=center]2.63[/align][/td][td][align=center]26.3[/align][/td][/tr][tr][td][align=center]可待因[/align][/td][td][align=center]50[/align][/td][td][align=center]48.62[/align][/td][td][align=center]97.2[/align][/td][/tr][tr][td][align=center]吗啡[/align][/td][td][align=center]50[/align][/td][td][align=center]49.37[/align][/td][td][align=center]98.7[/align][/td][/tr][/table]由表4可得,以甲醇为溶剂配制的标准溶液测定的空白加标回收率中,以内标法定量的吗啡、可待因回收率良好,以外标法定量的罂粟碱、那可丁、蒂巴因回收率太低,达不到标准要求。6.3阴性样品加标回收试验2分别称取 2 g 火锅底料阴性样品(精确至 0.001 g)于6个不同的 50 mL 离心管中,再分别加入150μL罂粟碱、那可丁、蒂巴因浓度为1.0μg/mL,吗啡、可待因浓度为5.0μg/mL的标准混合储备液,后按照3.2、3.3的步骤进行处理后上机,以净化包处理过的阴性样品基质溶液为溶剂配制的标准溶液进行定量,得到阴性样品加标回收率如表5:表6:阴性样品基质为溶剂配制的标准溶液测定的阴性样品加标回收率[table][tr][td][align=center]目标物质[/align][/td][td][align=center]添加量(ng/mL)[/align][/td][td][align=center]实测值(ng/mL)[/align][/td][td][align=center]回收率(%)[/align][/td][/tr][tr][td][align=center]那可丁[/align][/td][td][align=center]10[/align][/td][td][align=center]8.54[/align][/td][td][align=center]85.4[/align][/td][/tr][tr][td][align=center]罂粟碱[/align][/td][td][align=center]10[/align][/td][td][align=center]8.65[/align][/td][td][align=center]86.5[/align][/td][/tr][tr][td][align=center]蒂巴因[/align][/td][td][align=center]10[/align][/td][td][align=center]7.53[/align][/td][td][align=center]75.3[/align][/td][/tr][tr][td][align=center]可待因[/align][/td][td][align=center]50[/align][/td][td][align=center]46.92[/align][/td][td][align=center]92.4[/align][/td][/tr][tr][td][align=center]吗啡[/align][/td][td][align=center]50[/align][/td][td][align=center]48.33[/align][/td][td][align=center]96.7[/align][/td][/tr][/table]由表5可得,以阴性样品基质为溶剂配制的标准溶液测定的阴性样品加标回收率中,吗啡、可待因、罂粟碱、那可丁、蒂巴因回收率均符合标准要求,且以内标定量的回收率优于以外标定量的回收率。7.结论Quenchers法进行样品前处理,超高效液相色谱-串联质谱法检测火锅底料中罂粟碱、吗啡、那可丁、可待因和蒂巴因的实验结果显示在1.0-50.0ng/mL范围内,罂粟碱、那可丁、蒂巴因线性良好,在5.0-250ng/mL范围内,吗啡和可待因线性良好。在没有样品基质的条件下,Quenchers试剂包中的成分对目标物质会有吸附严重降低空白的回收率,因此该方法不适合做空白回收率试验。同时样品基质会严重降低样品加标回收率,当用阴性样品基质溶液配制的标准溶液定量分析时,样品加标回收率才能满足实验要求,且以内标法定量的样品回收率优于外标法。
关于乙酰氯的国家标准在网上找了很久,找到了份氯乙酰氯的然后发现了乙酰氯GOST 5829-1971乙酰氯 技术条件 (俄罗斯标准)GJB 702-1989 氯乙酰氯 (中国国家军用标准)哪位老师有做过,或者了解乙酰氯国家标准的可否帮下忙,传一份给我,急用,先谢谢大家了
各位老师,乙酰乙酸乙酯说有烯醇类和酮类平衡的混合物。那是不是就是说,我进一针乙酰乙酸乙酯的分析纯,应该出两个峰,一个乙酰乙酸乙酯(烯醇类),一个是乙酯乙酯乙酯(酮类)。
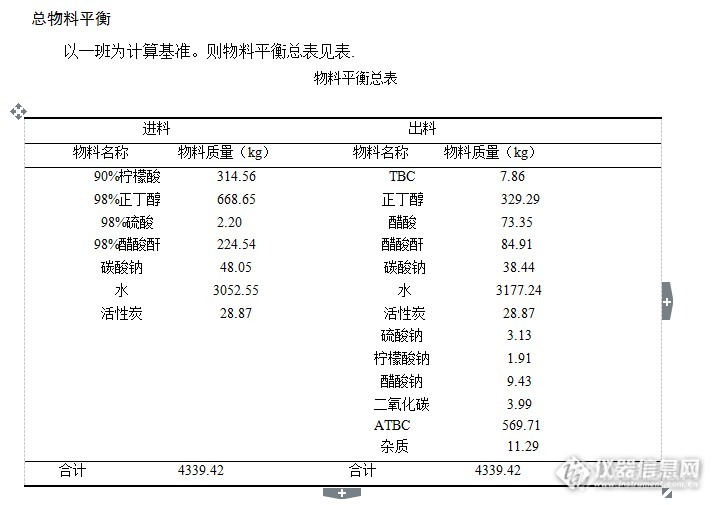
1.产品情况介绍 乙酸柠檬酸三丁酯,学名2-乙酰基-1,2,3丙烷三正丁酯,英文名称,Actyl Tri-n-ButylCitrate,简称ATBC,分子式C20H34O8,分子量402.472,为无色或微黄色油状液体,.相对密度1.046(25℃),粘度0.0427Pa·s(25℃),凝固点-80℃1沸173℃(133.3Pa),343℃(101324.72Pa),闪点(开杯法)20℃,折射率1.4408(25.5℃),挥发速度0.000009g/(cm·h)(105℃),水解速度=5%的溶液中和残余的酸性物质,并将中和后的物料送至静置釜内以除去大量的水及生成的盐(ATBC在水中溶解度极小)。为尽可能除去中和生成的盐,将中和后的物料送入水洗釜,用物料量1.2倍的水分三次洗涤,水洗后的物料送入水洗静置釜,分离出废水和盐分后,再次进入水洗釜水洗,反复三次,随后将ATBC送入干燥塔脱去残余的微量水分,干燥后的产品经脱色釜用活性炭脱去其中大部分杂质后,经过滤机除去活性炭,即可得成品ATBC. 合成乙酯柠檬酸三丁酯的工艺流程框图如图2-1所示。http://ng1.17img.cn/bbsfiles/images/2016/09/201609051953_608497_3005330_3.pnghttp://ng1.17img.cn/bbsfiles/images/2016/09/201609051955_608503_3005330_3.png3 可行性分析3工艺可行性分析 通过对乙酰柠檬酸三丁酯性质、用途及应用前景的分析,看到了无毒增塑剂乙酰柠檬酸三丁酯的发展前景。综合比较目前国内外研究乙酰柠檬酸三丁酯的各种方法,在考虑了工艺成熟程度、产品收率、环境保护与安全生产等因素的基础上,确定了以浓硫酸为酯化和乙酰化催化剂的工艺设计。在考虑设计方案时,考虑到中小企业的需要,确定了年产500吨的设计规模,具有投资少、见效快的优点。而且在设计酯化与乙酰化工序中,兼顾未来改用固体酸催化剂时,留有一定改造余地。 通过物料衡算,确定了各操作单元的进出物料量及原料消耗定额,其中主要原料消耗定额(每吨乙酰柠檬酸三丁lb)如下:无水柠檬酸510kg,正丁醇617kg,酯酸-f248.2kg,硫酸4kg,碳酸钠86.5kg,活性炭50.9kg。同时也确定了工艺用水量和废水排放量。 通过热量衡算解决了加热蒸气消耗量及最大消耗量,冷却水、冷冻水用量及最大用量,并确定了各换热器的换热面积。 在物料衡算和热量衡算的基础上选择了主要设备,结合所输送介质的特性确定了各设备的材质,根据各设备所储存或处理物料量,确定了各设备的型号,规格。 结合各设备所控制的温度和压力,为使操作控制方便,在考虑经济、实用的基础上对所用仪表进行了选型。 通过工艺流程图设计,解决了各个设备的前后顺序,各设备的相对位置,各个管路上阀门的控制方式,各操作参数的控制方式等问题,并在设计中考虑了各工艺管道的规格、材质。 结合带控制点工艺流程工艺流程和设备布置,对第三层的管道也进行了布置设计。 考虑到安全生产和环境保护,对危险性较大的场所按要求采取相应防护措施,减少对人的伤害和财产损失,对于排放的废物,在经过处理后尽可能达到国家排放标准。 本设计工艺与传统生产方法相比,具有下列优点:①乙酰柠檬酸三丁酯的传统生产工艺是将精制的柠檬酸三丁酯作为乙酰化的原料经乙酰化反应而制得,该工艺路线与传统工艺路线相比缩短了工艺路线,省去了脱醇前的碱洗、水洗等工序,减少了设备投资和加工费用。②该工艺与传统工艺相比,采用非精制的柠檬酸三丁酯作为乙酰化的原料,同时乙酰化过程不需再添加催化剂,即可生产出合格产品,降低了生产成本。③该工艺省去了碱洗、水洗等工序,减少的柠檬酸三丁酯的损失,提高了乙酰柠檬酸三丁酯的收率,降低了原料的消耗,并减少了废水的排放,降低了废水处理的难度。
[b]《空气和废气监测分析方法》(第四版增补版) 环氧氯丙烷 乙酰丙酮分光光度法 [b]环氧氯丙烷的标准曲线哪个大神有?[/b]扩项急用,万分感谢[/b]
想请教一下大家,对乙酰氨基酚的紫外吸收波长是多少呀,我查了文献有个说在205nm到230nm之间,但也有用270nm的,我看药典上“有关物质”的测定下用的是254nm,“含量测定”项下用的是257nm,但我在做实验时在254nm波长处检测不到对乙酰氨基酚,不知道是怎么回事,郁闷中……说明:我做的是制备液相,走空白能检测到信号,加对乙酰氨基酚样品后没什么反应,看是以为是浓度不够,后来加大浓度还是检测不到,又以为是254nm波长处没有吸收,但药典也是254nm呀,检查了可能出现的问题,也没找到为什么, 为什么空白都能检测到信号,进样后检测不到呢???很郁闷 请大家指教!!