
泽泻高效液相色谱法检测 药材泽泻为泽泻科植物泽泻的干燥块茎。与其它药材不同的是它是冬季茎叶开始枯萎时采挖,然后洗净,干燥,除去须根和粗皮,长的非常像土豆,这就是泽泻药材。http://ng1.17img.cn/bbsfiles/images/2015/08/201508281929_563417_2536753_3.png http://ng1.17img.cn/bbsfiles/images/2015/08/201508281929_563418_2536753_3.png 该植物早期有人把它叫做泽芝、水泻、鹄泻、及泻等,多生长在沼泽边缘,故而得名。因它花较大,白色艳丽,花期较长,有人常在家中或庭院中作为花卉养殖观赏。 全株有毒,地下块茎毒性较大。性寒,味微苦,可入药,具有利水、渗湿、泄热、化浊降脂、降低血清总胆固醇、减缓动脉粥样硬化形成等功效。主治肾炎水肿、肠炎泻痢、痰饮眩晕、遗精尿血、小便不利、高脂血症、脂肪肝及糖尿病等病症。 下面我们用高效液相色谱法检测泽泻中主要药物成分23-乙酰泽泻醇B含量。【实验部分】【原理】 精密称取适量泽泻样品经乙腈溶解,超声提取后注入高效液相色谱系统,C18色谱柱分离,紫外检测器检测,外标法(保留时间定性,峰面积定量)计算,得出泽泻中23-乙酰泽泻醇B含量。【仪器及试剂】 仪器:高效液相色谱仪(紫外检测器+高压泵+柱温箱等),超声波清洗仪,溶剂过滤器,电子天平(0.001),五号筛(药典筛)等。 试剂:乙腈(色谱纯),超纯水等。【样品溶液制备】 对照品溶液制备:精密称取23-乙酰泽泻醇B对照品1mg于50ml容量瓶中,加乙腈溶解定容,制成20μg/ml 23-乙酰泽泻醇B对照品溶液,备用。 供试品溶液制备:取样品泽泻适量,充分粉碎后过药典筛五号筛,精密称取过筛粉末0.5g置于具塞锥形瓶中,精密加入乙腈25ml,密塞,称定重量,超声处理30分钟后,放冷,再次称定重量,用乙腈补足减少的重量,摇匀,0.45μm有机相微膜滤过,待测。【色谱条件】检测器:紫外检测器检测波长:208nm色谱柱:Promosil C18 ( 250 mm X 4.6mm,5μm )流动相:乙腈:水=73:27(V:V)流速:1.0ml/min柱温:30℃进样量:10μl【色谱图】对照品溶液色谱图: http://ng1.17img.cn/bbsfiles/images/2015/08/201508281929_563419_2536753_3.png供试品溶液色谱图:http://ng1.17img.cn/bbsfiles/images/2015/08/201508281929_563420_2536753_3.png【计算】样品中被测物含量计算公式:http://ng1.17img.cn/bbsfiles/images/2015/08/201508281929_563421_2536753_3.pngD----供试品中被测物百分含量,以(%)表示V----供试品稀释的总体积,单位(mL)P3----供试品中被测物峰面积值P4-----对照品中被测物峰面积值ρ2----对照品被测物浓度。单位为mg/mlM2----样品质量,单位(mg)http://ng1.17img.cn/bbsfiles/images/2015/08/201508281929_563422_2536753_3.png【结果】 通过以上公式计算,泽泻中23-乙酰泽泻醇B的含量近似为0.058%,高于药典要求的不小于0.05%,该泽泻中23-乙酰泽泻醇B含量符合药典要求,该检测项目合格。【结论】 以上方法检测泽泻中23-乙酰泽泻醇B含量,虽然样品中干扰物较多,一定程度上影响了供试品色谱图的效果,对实验结果有微弱的影响(可能和实验室温度、风度等因素有关,由于实验室条件有限,没做该方面验证),但总体来说该方法较方便、快捷,结果准确、可靠,操作简单、易行,该方法适合该类样品检测。
[font=宋体]动脉粥样硬化([/font]atherosclerosis[font=宋体],[/font]AS[font=宋体])引发的动脉血管狭窄以及斑块的破裂可造成心肌梗死、冠心病、脑卒中等严重心脑血管疾病的发生。据全球数据显示,全球每年约有[/font]2 000[font=宋体]万人死于[/font]AS[font=宋体],且患病个体日趋年轻化,对人类健康和生命构成极大威胁[/font][sup][1][/sup][font=宋体]。[/font][font=宋体]随着现代生活方式的改变,高龄、肥胖、糖尿病、非酒精性脂肪肝病([/font]nonalcoholic fatty liver disease[font=宋体],[/font]NAFLD[font=宋体])、高血压、高血脂等成为[/font]AS[font=宋体]的传统危险因素。[/font]AS[font=宋体]是一种累及大、中动脉的慢性血管炎性疾病,其特征为脂质蓄积、炎症、氧化应激、血管内皮细胞([/font]endothelial cells[font=宋体],[/font]ECs[font=宋体])活化、巨噬细胞活化和泡沫细胞形成、血管平滑肌细胞([/font]vascular smooth muscle cells[font=宋体],[/font]VSMCs[font=宋体])增殖[/font][sup][2][/sup][font=宋体]。[/font]AS[font=宋体]的发病机制首先是各种危险因素下引起的内皮功能障碍,单核细胞分化为巨噬细胞,巨噬细胞通过吞噬氧化或其他化学修饰的低密度脂蛋白([/font]low density lipoprotein[font=宋体],[/font]LDL[font=宋体])形成泡沫细胞,脂质沉积进而[/font]VSMCs[font=宋体]增殖和迁移,最终导致内膜不断增生和动脉粥样斑块的形成[/font][sup][3][/sup][font=宋体]。目前,针对[/font]AS[font=宋体],临床药物治疗主要集中在调脂和抗炎[/font]2[font=宋体]个方面,调脂药物主要靶向降低低密度脂蛋白胆固醇([/font]low-density lipoproteincholesterol[font=宋体],[/font]LDL-C[font=宋体])或三酰甘油([/font]transglutaminase[font=宋体],[/font]TG[font=宋体]),抗炎药物治疗靶点主要为炎症因子白细胞介素[/font]-6[font=宋体]([/font]interleukin-6[font=宋体],[/font]IL-6[font=宋体])和[/font]IL-1β[sup][4][/sup][font=宋体]。[/font] [font=宋体]中医理论认为[/font]AS[font=宋体]其可归属于“脉痹”“胸痹”等范畴。现代人过食肥甘厚味,饮食不节,或长期偏嗜饮酒导致脾胃虚损,或者素体脾虚,脾主运化功能减弱,升清降浊功能失调,津液运行不利,湿聚为痰。痰浊黏滞内停于脉道之内,滞涩气血运行,凝聚成核块,形成瘀血,致痰瘀互结,阻塞脉道,影响脉行血气化功能,损伤脉络结构。脾运失健、痰浊阻滞是[/font]AS[font=宋体]发病机制的关键。健脾化浊法为[/font]AS[font=宋体]的治本之法。泽泻利水渗湿,泄热化浊,白术健脾益气,助脾运化水湿,泽泻[/font]-[font=宋体]白术药对为健脾祛湿之经典药对。薛伯寿教授治疗[/font]AS[font=宋体]使用频率较高的药对中包括泽泻[/font]-[font=宋体]白术药对[/font][sup][5][/sup][font=宋体]。董波教授善用泽泻[/font]-[font=宋体]白术药对治疗冠心病伴高血压[/font][sup][6][/sup][font=宋体]。黄永生教授治疗[/font]AS[font=宋体]使用频次超过[/font]30[font=宋体]次的有[/font]35[font=宋体]味中药中,泽泻和白术位列其中[/font][sup][7][/sup][font=宋体]。泽泻为泽泻科植物泽泻[/font][i]Alisma orientale [/i](Samuel) Juz.[font=宋体]的干燥块茎,白术是菊科植物白术[/font][i]Atractylodes macrocephala [i]Koidz[/i].[/i][font=宋体]的干燥根茎,被称为“补气健脾第一要药”。根据国家卫健委颁布的可用于保健食品的物品名单,泽泻和白术位列其中,均具有良好的食用和药用价值[/font][sup][8][/sup][font=宋体]。众多研究发现,泽泻[/font]-[font=宋体]白术药对及其有效成分可通过多靶点、多途径防治[/font]AS[font=宋体],本文通过梳理泽泻[/font]-[font=宋体]白术药对现有文献,分析并总结泽泻[/font]-[font=宋体]白术药对及活性成分在防治[/font]AS[font=宋体]中的作用机制,以期为泽泻[/font]-[font=宋体]白术药对后续的深入实验研究和临床应用及保健食品开发提供参考。[/font] [b]1 [font=黑体]泽泻[/font]-[font=黑体]白术药对物质基础[/font][/b] [font=宋体]现代研究表明泽泻中主要化学成分为三萜、倍半萜,此外还包括二萜类、挥发油、含氮化合物、苯丙素及其他类[/font][sup][9][/sup][font=宋体]。药理研究结果表明,泽泻醇[/font]A[font=宋体]([/font]alisol A[font=宋体])、[/font]24-[font=宋体]乙酰泽泻醇[/font]A[font=宋体]([/font]alisol A 24-ace[font=宋体],[/font]AA-24-a[font=宋体])、泽泻醇[/font]B[font=宋体]([/font]alisol B[font=宋体])、[/font]23-[font=宋体]乙酰泽泻醇[/font]B[font=宋体]([/font]alisol B 23-acetate[font=宋体],[/font]AB23A[font=宋体])等三萜类成分为泽泻中发挥调血脂、降血压、利尿、抗炎作用的主要有效成分[/font][sup][10][/sup][font=宋体]。[/font][font=宋体]白术化学成分中倍半萜类、聚乙炔类、多糖类为主要成分,此外还有三萜、聚乙炔、香豆素、苯丙素、黄酮、黄酮苷、甾体等类化合物。白术内酯[/font]I[font=宋体]([/font]atractylenolide-Ⅰ[font=宋体],[/font]AT-Ⅰ[font=宋体])、白术内酯[/font]Ⅱ[font=宋体]([/font]atractylenolide-Ⅱ[font=宋体],[/font]AT-Ⅱ[font=宋体])、白术内酯[/font]Ⅲ[font=宋体]([/font]atractylenolide-Ⅲ[font=宋体],[/font]AT-Ⅲ[font=宋体])是发挥抗炎、抗菌、健脾功效的倍半萜白术内酯类成分,是白术的主要有效成分及白术质量控制的关键指标[/font][sup][11][/sup][font=宋体]。多糖指白术多糖,在白术总成分中含量较高,主要有抗肿瘤活性、降糖、调节脂质代谢、抗炎、神经保护作用、肝脏保护作用以及生长促进等作用[/font][sup][12][/sup][font=宋体]。吴嘉朔[/font][sup][13][/sup][font=宋体]通过[/font]UHPLC-QE-Orbitrap-MS[font=宋体]方法研究发现泽泻醇[/font]A[font=宋体]、[/font]24-[font=宋体]乙酰泽泻醇[/font]A[font=宋体]、泽泻醇[/font]B[font=宋体]、[/font]23-[font=宋体]乙酰泽泻醇[/font]B[font=宋体]、[/font]AT-I[font=宋体]、[/font]AT-Ⅱ[font=宋体]、[/font]AT-Ⅲ[font=宋体]均为泽泻汤入血成分。[/font] [b]2 [font=黑体]泽泻[/font]-[font=黑体]白术药对配伍后对其有效成分含量与功效的影响[/font][/b] [font=宋体]中药发挥药效的物质基础为其活性成分,药对配伍后成分发生变化是研究中药配伍机制的关键。朱玉岚等[/font][sup][14][/sup][font=宋体]通过高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法研究发现泽泻白术共煎时[/font]23-[font=宋体]乙酰泽泻醇[/font]B[font=宋体]、[/font]24-[font=宋体]乙酰泽泻醇[/font]A[font=宋体]的提取率都较泽泻单煎时的提取率高。唐文强等[/font][sup][15][/sup][font=宋体]通过建立泽泻汤的[/font]UPLC[font=宋体]指纹图谱,发现[/font]15[font=宋体]批泽泻汤中[/font]AT-Ⅰ[font=宋体]、[/font]AT-Ⅱ[font=宋体]、[/font]AT-Ⅲ[font=宋体]、泽泻醇[/font]A[font=宋体]、泽泻醇[/font]B[font=宋体]和[/font]23-[font=宋体]乙酰泽泻醇[/font]B[font=宋体]的含量平均值分别为[/font]0.031 2[font=宋体]、[/font]0.0326[font=宋体]、[/font]0.017 2[font=宋体]、[/font]0.121 3[font=宋体]、[/font]0.581 0[font=宋体]、[/font]0.577 8 mg/mL[font=宋体]。[/font] [font=宋体]药对配伍后的药效学评价是判断药物配伍合理性的重要考察标准。鞠爱霞等[/font][sup][16][/sup][font=宋体]通过建立高脂血症模型,发现泽泻汤全方及其拆方逆转了高脂血症对[/font]CYP3A4 mRNA[font=宋体]表达水平的抑制作用,对酶活性的影响具有一致性,且单味泽泻组与全方组治疗效果优于白术组。彭敏[/font][sup][17][/sup][font=宋体]通过建立高脂血症模型,发现与单味泽泻相比,泽泻白术复方在血清和肝脏的总胆固醇([/font]total cholesterol[font=宋体],[/font]TC[font=宋体])和[/font]TG[font=宋体]浓度,以及脏器指数方面,都具有护肝方面的优势。泽泻组和复方组均激活了小鼠肝中对胆固醇代谢有关的基因的表达,而白术组对相关基因表达影响不大。以上研究表明泽泻白术配伍合理,相较于单方使用,泽泻和白术联合使用在调血脂方面更具优势,且泽泻较白术具有较强的调血脂作用。[/font]

[b]摘要:目的:[/b][color=#000000]探索提取温度、液固比和提取时间对泽泻多糖产率的影响,得到提取泽泻[/color][color=#000000]多糖最优工艺条件。[/color][b]方法:[/b][color=#000000]用均匀设计实验优化泽泻[/color][color=#000000]多糖的提取工艺,用苯酚硫酸法测出每次实验所得多糖的纯度,再求得每次实验纯多糖的得率,然后应用回归分析的方法分析实验得出的数据,以纯多糖的得率为指标,对提取温度、液固比、提取次数和提取时间3个因素进行分析,得出最佳工艺条件,并进行验证。[/color][b]结果:[/b][color=#000000]实验得出茵陈多糖的最佳提取条件是:提取温度100℃、提取时间135 min、提取液固比40:1。[/color][b]结论:[/b][color=#000000]验证实[/color][color=#000000]验平均得率为8.83%,预测值是8.28%,二者很接近,说明我们得到的最佳工艺条件是可靠的。[/color]1前言[color=#000000]泽泻为泽泻科植物泽泻[i]Alsima orientalis(sam.)Juzep.[/i]的干燥块茎,分布在中国、韩国和日本等国。性味甘、淡、寒,归肾、膀胱经[sup][/sup]。作为常用中药,是六味地黄丸、龙胆泻肝丸、五苓散等临床常用重要方剂的主要组成[sup][/sup]。具有利水渗湿,泄热,化浊降脂等功效,用于治疗小便不利,水肿胀满,泄泻尿少,痰饮眩晕,热淋涩痛,高脂血症等症[sup][/sup]。1.1泽泻的化学成分泽泻中的三萜类化合物主要有:泽泻醇A、泽泻醇A-24-乙酸酯、泽泻醇B-23-乙酸酯、表泽泻醇A、11-去氧泽泻醇A、泽泻醇C、泽泻醇C-23-乙酸酯、16,23-氧化泽泻醇E、泽泻醇F、阿里泽泻醇A和阿里泽泻醇B等原萜烷型四环三萜[sup][/sup]。从生物途径归纳,三萜类都是由 23- 泽泻醇 B 衍生而来[sup][/sup]。中药泽泻中获得的倍半萜类化合物多数为愈创木烷型。现分离到的倍半萜化合物主要有:泽泻醇,环氧泽泻烯,Orientalol A,B,C,Sulfooriental A,B,C,D[sup][/sup]。Yamaguchi等首次从泽泻鲜品中分离出一个贝壳杉烷型四环二萜类化合物,并最终确定了绝对构型为(-)-16R-ent-kauranre-2,12-doine[sup][/sup]。彭国平等从泽泻中分离出两个新的贝壳杉烷型四环二萜类化合物:泽泻二萜醇(Oriediterpenol)及泽泻二萜醇苷 (Oriediter-penoside)[sup] [/sup]。泽泻除了萜类成分外,此外,泽泻还含挥发油、多糖、蒽醌、磷脂、蛋白质及淀粉等成分[sup][/sup]。如胡萝卜素-6-硬酸脂、β-谷甾醇、三十烷、正二十烷、卫矛醇、挥发油(内含糖醛)、少量生物碱、天门冬素、脂肪酸、树脂、植物凝集素、大黄素、酸性多糖,胆碱,以及大量淀粉、蛋白质、氨基酸和钾、钙、镁等金属元素[sup][/sup]。1.2 泽泻的药理作用现代研究表明,泽泻有明显的利尿,抑制肾结石形成,降血压,降血脂及抗动脉粥样硬化,抗脂肪肝,抗肾炎活性和调节免疫等作用[sup][/sup]。1.3立题依据多糖具有多种生物活性, 具有提高免疫, 降血糖,抗肿瘤, 抗病毒等功能, 被认为是构成生命的四大基本物质之一。由于其独特功能和较低的毒性, 多糖类化合物在抗衰老、 抗病毒和肿瘤治疗、 糖尿病治疗等方面有良好的应用前景。另外,多糖可以改善食品的食用品质、加工特性和外观特性, 可用于抑制脂质氧化, 稳定酸性饮料, 也可作为乳化剂等, 在食品中的用途十分广泛[sup][/sup]。目前已发现的天然多糖有几百种,其中植物多糖对肿瘤治疗及调节机体免疫力效果显著,同时还有治疗肝炎、抗衰老等药理作用,且毒副作用很小[sup][/sup]。由于泽泻的药理作用显著,而关于泽泻多糖研究的文献很少,因此对于泽泻多糖的研究也具有很大的意义。开发泽泻多糖产品,首先需要把多糖从泽泻中提取出来。笔者决定对泽泻多糖的提取工艺进行研究,对其提取条件进行优化,从而为泽泻多糖的深入开发利用提供实验依据。本课题我们就重点探讨泽泻多糖的最佳提取条件,通过对泽泻多糖提取过程中影响泽泻多糖产率、纯度的因素进行单因素实验,然后进行均匀设计实验,用线性回归的分析方法分析实验得出的数据,寻找泽泻多糖的最优化工艺条件。1.4提取方法的确定提取植物多糖的方法有多种,一般是采用水提醇沉法,采用水提醇沉法提取,可防止引起糖苷键的断裂[sup][/sup]。李小凤等[sup][/sup]通过单纯的水提醇沉法对泽泻多糖进行了提取和含量测定。此外,很多研究对多糖的水提醇沉工艺做了优化,如朱秀灵等[sup][/sup]采用超声波辅助提取银杏叶多糖;缪建等[sup][/sup]采用酶法结合水提醇沉法提取银杏叶多糖;金汝城等[sup][/sup]采用均匀设计优化超声波法提取黄芪多糖。由于实验设备有限,本实验采用水提醇沉法对泽泻多糖进行提取。[/color][color=#000000]2 实验材料2.1实验仪器FA2104N型电子分析天平(上海民桥精密科学仪器有限公司)HH-1数显恒温水浴锅(金坛市晶玻实验仪器厂)80-2离心机(上海荣泰生化工程有限公司)RE-52A旋转蒸发仪(上海亚荣生化仪器厂)GZX-9070电热恒温鼓风干燥箱(上海博讯实业有限公司医疗设备厂)DZF-6050真空干燥箱(巩义市予华仪器责任有限责任公司)SHD-Ⅲ型循环水式多用真空泵(保定市新区阳光科教仪器厂)BCD-223MT冰箱(河南新飞电器有限公司)722可见分光光度计(上海菁华科技仪器有限公司)24目,100目标准筛(浙江上虞市华丰五金仪器有限公司)2.2实验材料和试剂泽泻(河北省安国药材市场)无水乙醇(分析纯,天津市美琳工贸有限公司)蒸馏水(实验室自制)葡萄糖(分析纯,天津市科密欧化学试剂有限公司)苯酚(分析纯,天津市福晨化学试剂厂)浓硫酸(分析纯,北京化工厂)[/color][color=#000000]3实验方法3.1泽泻粗多糖的提取流程将预备好的泽泻放入70℃真空烘箱中干燥2h,粉碎取过24目筛,不可过100目筛的粉末,装在密封袋中置于干燥器中备用。泽泻多糖提取的实验流程如下:精密称定已制备的泽泻粉末5.000g于500mL圆底烧瓶中,加入规定液固比的蒸馏水,用恒温水浴锅T℃水浴加热不同时间,先用脱脂棉过滤得粗滤液,然后用布氏漏斗抽滤粗滤液,通过旋蒸仪旋转蒸发将所得滤液浓缩至约10mL,加95%乙醇30mL,置具塞锥形瓶中,冰箱4℃放置约18h,然后用10mL试管离心(3000rpm,10min),弃去上清液,得沉淀,于50℃、0.099MPa真空干燥箱中放置3.5h后,关闭电源,真空放置过夜。然后,将所得沉淀与离心管一起称重,通过差量法计算多糖产率。其中,液固比、水浴温度T、提取时间t及提取次数根据实验过程中考察因素的改变,作相应更改。粗多糖产率=粗多糖质量/泽泻样品质量×100%3.2 泽泻纯多糖含量的测定本课题中,泽泻提取工艺最佳条件分析中所用的是纯多糖含量,粗多糖的数值只是作为参考数值。本实验中是通过苯酚-浓硫酸反应使多糖显色,在紫外可见分光光度计490nm处测得吸光度,然后通过将数据代入当天测得的标准曲线中,计算出相应多糖浓度,从而计算出不同提取条件下泽泻中纯多糖的含量。3.2.1 标准曲线的绘制标准液的配制:称取葡萄糖0.1259g于100mL容量瓶中,加蒸馏水至刻度,摇匀得1.259g/L的储备液,分别精密量取储备液1.0mL、0.8mL、0.6mL、0.4mL、0.2mL,置于25mL的容量瓶中,加水至刻度,摇匀。则得五个不同浓度的标准液。配制5%苯酚溶液:称取苯酚1.2508g于烧杯中,用加热至约50℃的蒸馏水溶解,转移至25mL的容量瓶中,加水至刻度,摇匀,避光保存以备用。标准曲线的绘制:取2mL移液管,分别取2mL蒸馏水和五个标准溶液于六根具塞试管中,再用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url][/color][/url]移取1mL5%的苯酚溶液,快速加入上述具塞试管中,充分混匀,用5mL移液管取5mL浓硫酸快速加入上述试管中,盖好试管塞,充分摇匀。从放入沸水浴中计时,沸水浴15min,冷水浴10min,室温放置5min(六个溶液之间间隔3min加硫酸)。将上述反应30min后的溶液分别在490nm处测定吸光度,以吸光度A为纵坐标,以葡萄糖标准溶液C(Co=50.36)为横坐标,绘制标准曲线。(见图1-1)标准曲线的线性范围为:0.10072×10[sup]-4[/sup]g/mL ~0.50360×10[sup]-4[/sup]g/mL曲线方程:A=0.0165C-0.0216,相关系数:r=0.9998[/color][align=center][img=,619,343]https://ng1.17img.cn/bbsfiles/images/2019/08/201908261725042952_9256_3237657_3.png!w619x343.jpg[/img][/align][align=center]图1-1 标准曲线[/align][align=center] [/align]3.2.2 苯酚-浓硫酸法测多糖含量分别取不同提取条件下所得粗多糖0.040g于小烧杯中,加少量温水搅拌使其溶解,转移至250mL容量瓶中,加蒸馏水至刻度,摇匀。使用前用布氏漏斗抽滤,滤去不溶物,得澄清滤液。然后用2mL移液管分别移取2mL上述滤液于具塞试管中,再用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url][/color][/url]移取1mL 5%的苯酚溶液,快速加入上述具塞试管中,充分混匀,用5mL移液管取5mL浓硫酸快速加入上述试管中,充分摇匀,盖好试管塞。沸水浴15min,冷水浴10min,室温放置5min,反应完全后在490nm处测定其吸光度,每次需配制空白对照用来校正可见分光光度计。将测得的吸光度带入标准曲线方程中计算出所配溶液的多糖浓度,进而可计算出纯多糖的产率。3.2.3 纯多糖产率的计算纯多糖产率=(纯多糖浓度×体积×粗多糖质量)/(粗多糖测样量×泽泻质量)×100%3.3 单因素实验3.3.1 液固比对泽泻多糖提取率的影响考察液固比,是为了能够在使用较少溶剂的情况下提取出最多的多糖,这不光能够减少工业生产中单位产量水的使用量,同样也为多糖提取液后期处理减少了时间和成本,具有重要的经济和生态效益。在结合前人相关中药材多糖提取实验的基础上,确定考察液固比为10:1、20:1、30:1、40:1、50:1。纯多糖产率见表3-1。[align=center] 表3-1 液固比对多糖提取率的影响 [/align] [table=582][tr][td]提取温度[/td][td] [align=center]80℃[/align] [/td][td=2,1] 提取时间[/td][td] [align=center]2.5h[/align] [/td][td=2,1] [align=center]提取次数[/align] [/td][td]1[/td][/tr][tr][td] [align=center]液固比(mL/g)[/align] [/td][td=2,1] 10:1[/td][td=2,1] 20:1[/td][td]30:1[/td][td]40:1[/td][td] [align=center]50:1[/align] [/td][/tr][tr][td]多糖产率(%)[/td][td=2,1] 3.38[/td][td=2,1] 3.46[/td][td]5.43[/td][td]7.87[/td][td]6.81[/td][/tr][/table]3.3.2 提取温度对泽泻多糖提取率的影响中药材提取过程中,温度是极其重要的条件。通过查阅文献及综合各方面考虑,确定提取温度为60℃、70℃、80℃、90℃、100℃。多糖产率见表3-2。[align=center]表3-2 提取温度对多糖提取率影响[/align] [table=640][tr][td]液固比[/td][td] [align=center]20:1[/align] [/td][td=2,1] [align=center]提取时间[/align] [/td][td] [align=center]2.5h[/align] [/td][td=2,1] [align=center]提取次数[/align] [/td][td=2,1] [align=center]1次[/align] [/td][/tr][tr][td]提取温度[/td][td=2,1] [align=center]60℃[/align] [/td][td=2,1] [align=center]70℃[/align] [/td][td] [align=center]80℃[/align] [/td][td=2,1] [align=center]90℃[/align] [/td][td] [align=center]100℃[/align] [/td][/tr][tr][td]多糖产率(%)[/td][td=2,1] [align=center]1.81[/align] [/td][td=2,1] [align=center]2.87[/align] [/td][td] [align=center]4.55[/align] [/td][td=2,1] [align=center]5.75[/align] [/td][td] [align=center]9.57[/align] [/td][/tr][/table][color=fuchsia] [/color]3.3.3 提取时间对泽泻多糖提取率的影响通过查阅文献,本实验确定考察时间为0.5h、1h、1.5h、2h、2.5h、3h、3.5h。多糖产率见表3-3。[align=center]表3-3 提取时间对多糖提取率的影响[/align] [table=653][tr][td]液固比[/td][td] [align=center]20:1[/align] [/td][td=2,1] [align=center]提取温度[/align] [/td][td] [align=center]80℃[/align] [/td][td=3,1] [align=center]提取次数[/align] [/td][td=2,1] [align=center]1次[/align] [/td][/tr][tr][td] [align=center]提取时间(h)[/align] [/td][td=2,1] 0.5[/td][td=2,1] 1[/td][td] [align=center]1.5[/align] [/td][td]2[/td][td] [align=center]2.5[/align] [/td][td]3[/td][td] [align=center]3.5[/align] [/td][/tr][tr][td] [align=center]多糖产率(%)[/align] [/td][td=2,1] [align=center]3.57[/align] [/td][td=2,1] 3.38[/td][td] [align=center]4.75[/align] [/td][td] [align=center]5.04[/align] [/td][td] [align=center]5.00[/align] [/td][td] [align=center]4.55[/align] [/td][td] [align=center]5.15[/align] [/td][/tr][/table]3.3.4 提取次数对泽泻多糖提取率的影响众所周知,在最合适的料液比、提取温度、提取时间条件下,提取次数越多,药物的有效成分在中药材中溶出的就会越多,提取率相应就会越高,但提取次数决定操作成本,提取次数越多,成本越高,且工艺用水量大。所以根据前人提取数据,将提取次数定为1次、2次、3次。多糖产率见表3-4。[align=center]表3-4 提取次数对多糖提取率的影响[/align] [table=582][tr][td]提取温度[/td][td] [align=center]80℃[/align] [/td][td=2,1] [align=center]提取时间[/align] [/td][td] [align=center]2.5h[/align] [/td][td] [align=center]液固比[/align] [/td][td] [align=center]20:1[/align] [/td][/tr][tr][td]提取次数[/td][td=2,1] [align=center]1[/align] [/td][td=2,1] [align=center]2[/align] [/td][td=2,1] [align=center]3[/align] [/td][/tr][tr][td]多糖产率(%)[/td][td=2,1] [align=center]3.46[/align] [/td][td=2,1] [align=center]5.71[/align] [/td][td=2,1] [align=center]8.68[/align] [/td][/tr][/table]3.4 均匀设计实验3.4.1 均匀设计实验方案在泽泻(均为5g干粉)多糖提取工艺中,我们要考察的主要因素有:提取温度、料液比及提取时间三个因素。根据单因素实验结果确定各因素的取值范围:提取温度X[sub]1[/sub] :55℃~100℃;料液比X[sub]2[/sub]:1:15~1:60:提取时间X[sub]3[/sub]:1.5h~3.75h。再根据各种因素的取值范围、试验精度要求,按提取温度间隔5℃,液料比间隔5,提取时间间隔0.25h,设计出一个3因素10水平的均匀设计表。根据均匀设计表中所列的提取条件,按照泽泻粗多糖的提取流程,对泽泻粗多糖进行提取,并计算其产率。(见表4-1)提取得到粗多糖并测定多糖纯度,进而求得纯多糖产率。[align=center]表4-1 均匀设计实验数据[/align] [table=638][tr][td] [table][tr][td] [table=100%][tr][td] 条件 编号[/td][/tr][/table] [/td][/tr][/table][img=,98,65]https://bbs.instrument.com.cn/xheditor/xheditor_skin/blank.gif[/img][img=,84,52]https://bbs.instrument.com.cn/xheditor/xheditor_skin/blank.gif[/img][/td][td] [align=center]温度(℃)[/align] [/td][td] [align=center]料液比[/align] [align=center](g/mL)[/align] [/td][td] [align=center]时间(min)[/align] [/td][td] [align=center]粗多糖产率(%)[/align] [/td][td] [align=center]纯多糖产率(%)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]55[/align] [/td][td] [align=center]1:35[/align] [/td][td] [align=center]180[/align] [/td][td] [align=center]14.24[/align] [/td][td] [align=center]1.22[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]60[/align] [/td][td] [align=center]1:60[/align] [/td][td] [align=center]120[/align] [/td][td] [align=center]15.44[/align] [/td][td] [align=center]1.67[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]65[/align] [/td][td] [align=center]1:30[/align] [/td][td] [align=center]225[/align] [/td][td] [align=center]12.72[/align] [/td][td] [align=center]1.27[/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]70[/align] [/td][td] [align=center]1:55[/align] [/td][td] [align=center]165[/align] [/td][td] [align=center]14.94[/align] [/td][td] [align=center]2.50[/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]75[/align] [/td][td] [align=center]1:25[/align] [/td][td] [align=center]105[/align] [/td][td] [align=center]13.62[/align] [/td][td] [align=center]3.74[/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]80[/align] [/td][td] [align=center]1:50[/align] [/td][td] [align=center]210[/align] [/td][td] [align=center]23.82[/align] [/td][td] [align=center]6.55[/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]85[/align] [/td][td] [align=center]1:20[/align] [/td][td] [align=center]150[/align] [/td][td] [align=center]23.19[/align] [/td][td] [align=center]5.98[/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]90[/align] [/td][td] [align=center]1:45[/align] [/td][td] [align=center]90[/align] [/td][td] [align=center]23.05[/align] [/td][td] [align=center]5.71[/align] [/td][/tr][tr][td] [align=center]9[/align] [/td][td] [align=center]95[/align] [/td][td] [align=center]1:15[/align] [/td][td] [align=center]195[/align] [/td][td] [align=center]16.52[/align] [/td][td] [align=center]4.92[/align] [/td][/tr][tr][td] [align=center]10[/align] [/td][td] [align=center]100[/align] [/td][td] [align=center]1:40[/align] [/td][td] [align=center]135[/align] [/td][td] [align=center]39.93[/align] [/td][td] [align=center]8.74[/align] [/td][/tr][/table]3.4.2 最优提取条件的选择用SPSS 19.0统计软件,以纯多糖得率为评价指标对各因素进行线性回归分析,模型的优度通过复相关系数和方差分析来判定。结果如表4-2。[align=center]表4-2 回归方程[/align] [table=638][tr][td] [align=center] [/align] [/td][td] [align=center]回归方程式[/align] [/td][td] [align=center]R[/align] [/td][td] [align=center]P[/align] [/td][/tr][tr][td] [align=center]回归方程1[/align] [align=center]回归方程2[/align] [align=center]回归方程3[/align] [/td][td] [align=center]Y=-9.850+0.164X[sub]1[/sub]+0.033X[sub]2[/sub]+0.001X[sub]3[/sub][/align] [align=center]Y=-7.595+0.153X[sub]1[/sub][/align] [align=center]Y=3.780-0.002X[sub]2[/sub] X[sub]3[/sub]+3.004E-5 X[sub]1[/sub]X[sub]2[/sub] X[sub]3[/sub] [/align] [/td][td] [align=center]0.919[/align] [align=center]0.902[/align] [align=center]0.960[/align] [/td][td] [align=center]0.008[/align] [align=center]0.000[/align] [align=center]0.000[/align] [/td][/tr][/table]表4-2中,Y为纯多糖得率,X1为提取温度,X2为液固比,X3为提取时间。方程1,R[sup]2[/sup]= 0.844,P值为0.008,回归非常显著,常数项和X1项P值分别0.041和0.002小于0.05 ,回归显著,有统计意义,而X2,X3均回归不显著,方程1多糖产率预测值为7.98%;方程2为将各项及其交叉乘积项全部纳入进行逐步回归的结果,我们发现,最后的方程中只保留了X1项,方程2的 R[sup]2[/sup]= 0.813,常数项和X1项P值分别为0.006和0.000,均小于0.01,回归亦非常显著有效,其预测值为7.66%。方程3为全体向后回归分析结果,R[sup]2[/sup]= 0.922,P值为0.000,常数项乘积项P值分别为0.001,0.000和0.000,均小于0.01 。故回归非常显著,其预测值为8.28%。3.4.3 最优提取条件的验证综合上述三方程的回归结果,及均匀设计和单项实验的结果,我们采取提取温度100℃、提取时间为135 min、提取料液比为40,即第10组的条件为最佳条件,并重复3次进行实验验证。结果见表4-3。[align=center]表4-3 最优提取条件测得的多糖含量[/align] [table][tr][td] [align=center]实验编号[/align] [/td][td] [align=center]提取条件[/align] [/td][td] [align=center]粗多糖得率(%)[/align] [/td][td] [align=center]纯多糖得率(%)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td=1,4] [align=center]提取温度:100℃[/align] [align=center]料液比:1:40[/align] [align=center]提取时间:135 min[/align] [/td][td] [align=center]32.24[/align] [/td][td] [align=center]8.57[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]28.64[/align] [/td][td] [align=center]8.99[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]28.99[/align] [/td][td] [align=center]8.92[/align] [/td][/tr][tr][td] [align=center]平均值[/align] [/td][td] [align=center]29.96[/align] [/td][td] [align=center]8.83[/align] [/td][/tr][/table]4 实验结果4.1 单因素实验结果4.1.1 液固比采用提取温度80 ℃,加热2.5h,提取1次,考察了液固比对提取收率的影响。图4-1表明,固液比从10:1增到20:1多糖产率并无太大变化,液固比从20:1增到30:1纯多糖产率提高了56.94 %,同样,从30:1到40:1纯多糖产率又提高了44.94%。而在40:1到50:1之间,反而下降。主要是由于开始增加提取液体积有利于细胞内容物的溶出,而液固比到达40:1之后,多糖成分已基本溶出,故多糖产率并没有提高,反倒降低。考虑到工业生产中水的用量和多糖产率的综合因素,可以得出40:1应为最佳提取液固比。[align=center][img=,542,271]https://ng1.17img.cn/bbsfiles/images/2019/08/201908261726359481_8405_3237657_3.png!w542x271.jpg[/img][/align][align=center]图4-1 液固比对泽泻粗多糖得率的影响[/align][align=center] [/align]4.1.2 提取温度采用液固比为20:1,提取时间2.5h,提取1次,考察了提取温度对多糖产率的影响,结果见图4-2。由图中可以看出,当温度从60 ℃上升到70 ℃时,粗多糖得率共提高了58.56%,从70℃到80℃,提高了58.54%,80℃到90℃,提高了26.37%,从90℃到100℃,提高了66.43%。随着温度的上升,多糖产率一直在增加,说明温度的提高对多糖的溶出有显著影响。显然,从60℃到90℃,多糖产率几乎呈线性上升,从90℃到100℃,较60℃到90℃上升更快,且产率最高。过低的温度会造成提取物溶出少甚至不溶出,而较高温度会显著提高多糖产率。所以,即使较高的温度会略微增加能源上的成本,但是却使多糖产率增加数倍,提高药材利用率,大大降低总生产成本。综合以上各方面因素考虑,得出多糖的最佳提取温度为100 ℃。[align=center][img=,556,281]https://ng1.17img.cn/bbsfiles/images/2019/08/201908261727189034_3165_3237657_3.png!w556x281.jpg[/img][/align][align=center]图4-2 提取温度对泽泻多糖得率的影响[/align][align=center] [/align]4.1.3 提取时间中药材有效药物成分溶出需要一定的时间,较短会造成药物有效成分无法最大限度地溶出,过长的提取时间则会导致有效成分分解。采用提取温度80 ℃,液固比20:1,提取1次,考察了提取时间对多糖得率的影响,结果见图4-3。可以看出,提取时间超过2h后多糖得率并未继续增加,反而下降;而2h之前,多糖得率增加显著,从1h到2h增加了49.11%。虽然在3.5h处总产率较2h增加了0.11%,但是提取时间却较2h多出将近一倍,大大增加了生产成本,故2h为最佳提取时间。[align=center][img=,560,260]https://ng1.17img.cn/bbsfiles/images/2019/08/201908261727397775_5830_3237657_3.png!w560x260.jpg[/img][/align][align=center]图4-3 提取时间对泽泻多糖得率的影响[/align]4.1.4 提取次数采用提取温度80 ℃,提取时间2.5h,液固比20:1,考察了提取次数对多糖得率的影响,结果见图4-4。结果发现:提取3次时多糖得率最高,比1次提取提高了1.5倍,差别显著。而提取两次较提取一次,也提高了65.03%,提高显著。提取三次的多糖产率是提取一次的2.5倍。因此,从约成本,提高药材利用率的角度考虑,确定最佳提取次数为3次。[align=center][img=,548,269]https://ng1.17img.cn/bbsfiles/images/2019/08/201908261727581933_5743_3237657_3.png!w548x269.jpg[/img][/align][align=center]图4-4 提取次数对泽泻多糖得率的影响[/align][align=center] [/align]4 . 2 均匀设计实验结果本实验采用水提醇沉法提取泽泻多糖,通过对料液比、提取时间、提取温度等三个可控条件进行均匀设计实验,结合实验及生产实际,确定了泽泻多糖提取的最优条件,并利用该最优条件测定了泽泻多糖的含量,计算出了纯多糖的得率。结果见表4-4。[align=center]表4-4 泽泻多糖提取最优条件及多糖含量[/align] [table][tr][td=4,1] [align=center]最优提取条件[/align] [/td][td=1,2] [align=center]粗多糖得率[/align] [align=center](%)[/align] [/td][td=1,2] [align=center]纯多糖得率[/align] [align=center](%)[/align] [/td][/tr][tr][td] [align=center]提取温度[/align] [/td][td] [align=center]提取料液比[/align] [/td][td] [align=center]提取时间[/align] [/td][td] [align=center]提取次数[/align] [/td][/tr][tr][td] [align=center]100℃[/align] [/td][td] [align=center]1:40[/align] [/td][td] [align=center]135 min[/align] [/td][td] [align=center]1次[/align] [/td][td] [align=center]29.96[/align] [/td][td] [align=center]8.83[/align] [/td][/tr][/table]所得纯多糖实际产率8.83%与理论得率8.28%十分接近。[color=#000000]5 讨论5 . 1多糖提取与含量测定过程(1)在多糖提取过程中,除待测因素温度、料液比、提取时间按要求改变外,其他条件均应保持一致,以减少系统误差,增加数据的准确性。(2)在转移多糖溶液的过程中要尽可能的减少损失及其操作的一致,如粗过滤完抽滤时滤渣滤棉中残余多糖成分的转移,旋蒸浓缩提取液后的转移和离心过程中多糖的转移应最大程度减少多糖损失量,并保持操作的一致性。(3)在绘制标准曲线及用苯酚-硫酸法测多糖含量时,加入苯酚后一定要混匀,以防止硫酸直接氧化苯酚,导致糖类反应不完全。此外,苯酚须现用现配,避光保存。(4)在硫酸与糖反应时,一般方法是加入苯酚和硫酸后摇匀,直接室温放置30min后测其吸光度,为了保证反应完全,本实验在加入硫酸并摇匀后,先沸水浴15min,再冷水浴10min,再室温放置5min后测量吸光度。并在测量时保证每组的反应时间一致。(5)纯多糖含量的测定过程,为了保证数据的准确性,单因素实验中同一组的最好同时测,均匀设计实验的十组最好同一天测完。(6)由于实验时间有限,对于泽泻多糖测定时,采用的是以往经验的可见光范围490nm进行测定,这是实验中不完善的地方,准确的操作应通过实验找到多糖吸光度最大的波长进行测定。5 . 2 单因素实验由于单因素只是考虑单个提取条件对产率的影响,不能考虑到多种因素共同的影响,所以只是作为参考结果,对于单因素对多糖提取的影响具有参考价值,但是从总的生产上来说,均匀设计具有更加实用的价值。本实验中,单因素最优条件为:液固比40:1,提取温度100℃,提取时间2h,提取次数3次。单因素中提取次数的结果中提取两次较提取一次产率的增长值,还没有提取三次较提取两次的增长值大。可能是因为提取温度不够高,多糖溶出较慢所致。单从单因素的角度来看提取三次为最佳条件。但是从生产过程考虑,提取次数的增加会增加很大工作量,一般会选择一次就能提取完全的条件。而均匀设计实验中也证明,在100℃,40:1,135min条件下多糖的产率就可以达到8.74%,比单因素实验中提取三次的量还要高,故选择一次为最佳提取次数。5 . 3 均匀设计实验均匀设计实验结果8.83%同实验分析的理论结果8.28%较为接近,这也证明了实验数据的准确性,并通过回归分析确定了实验的最佳提取条件。均匀设计是在单因素的基础上进行的,综合两个实验的数据结果,不难发现提取的最佳条件为:提取温度100℃、提取时间为135 min、提取料液比为40、提取一次。5 . 4 整体结果讨论单因素实验中,我们可以得到以下关于单因素对多糖提取率的影响。提取次数与多糖产率呈正相关,提取时间也是呈正相关。提取时间与多糖产率的关系是到一定时间就达到稳定,即超过这个时间显著性不过。液固比与多糖产率的关系是存在一个峰值,低于此值,产率随液固比增加而增加,超过此值则随液固比增加而产率降低。这也给我们一些启发,对于这些植物药中似多糖类水溶性物质的提取条件也应存在此种规律,可作为以后研究的参考。均匀设计实验是在单因素的基础上,综合考虑了提取时间、温度和液固比对多糖产率的影响,是较符合实际生产条件的一项实验,具有较高的应用参考价值。当然,除了本课题中考虑到的因素,可能还有其他未被考虑到的一些因素。均匀设计只是以线性回归的方式对实验数据进行分析,而现在有更为先进的如响应面分析法等。这都说明多糖的提取工艺有很大的提升空间。参考文献 中药大辞典.上海:上海科学技术出版社,2006:2067Xie Min.Phmaracology of traditional Chinese medical formulas.Beijing:The People’s Public Health Publish House,2007 国家药典委员会编.中国药典(一部).中国医药出版社,2010:213 黄珍,刘咏松.泽泻降血脂药理作用及物质基础研究进展.山西中医学院学报,2008,9(5):55~56 陈曦.泽泻的研究现状与进展.中国民族民间医药,2011,20(9):50~51,53 臧萍.泽泻的研究现状及展望.中国中医药现代远程教育,2009,07(6):180~182Yamaguchi K.Akauurane derivative isolated from Alisma orientale Acta Crystallogr SectC Cryst. Struct .医药导报,2003,22(5):295Peng GP,LouFC.Isolation and indentification of diterpenoids fromAlisma orientalis .Actapharmaceutica sinica,2002,37:950~954 丁霞,吴水生.泽泻的研究进展.中医药信息,2008,25(5):19~21 王建平,傅旭春,泽泻的药理作用和临床研究进展.2011年浙江省医学会临床药学分会学术年会论文汇编,2011 冯欣煜,姚志凌.泽泻药理研究与临床新用.中国医药指南,2007,S1:37~38 尹艳,高文宏,于淑娟,等.多糖提取技术的研究进展.食品工业科技,2007,28(2):248~250 吴华振.植物多糖的药理作用及应用进展.实用医技杂志,2005,12(7):1803~1804 杨艳,徐应淑.川、黔地区金钗石斛多糖的含量测定.中国药房,2010,21(27):2552~2554 李小凤,韦庆宁,史柳芝,等.泽泻多糖的提取及含量测定.山东化工,2012,41(7):26~28 朱秀灵,戴清源,冯宏波.超声波辅助提取银杏叶多糖工艺研究. 安徽工程科技学院学报,2010,25(3):6~8 缪建,杨文革,周彬.银杏叶多糖提取工艺的优化. 中国食品添加剂,2007,12(2):153~156 金汝城,周术涛,张东博,等.均匀设计优化超声波法提取黄芪多糖的研究. 安徽农业科学,2009,37(12):5498~5499[/color][align=center] [/align]
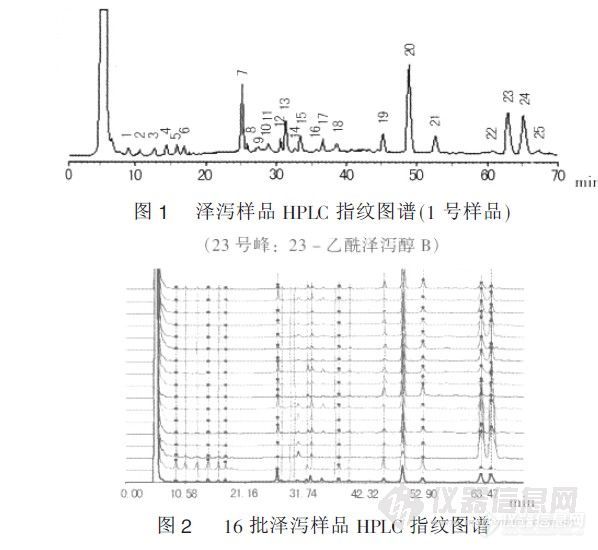
作者:巩丽萍 王少云 张克 【摘要】:目的建立泽泻饮片甲醇提取液的高效液相指纹图谱(HPLC-FP),为其鉴别提供依据。方法在Dia-monsil TM C18柱(250mm×4.6mm,5μm)上以甲醇-水为流动相进行梯度洗脱,流速:0.5mL·min-1;记录时间70min;蒸发光散射检测器(ELSD)检测;检测条件:漂移管温度82.5℃,雾化气体流速1.9L·min-1;实验数据用聚类分析和相似度软件处理。结果得到15个共有峰,聚类分析和相似度分析结果显示16批泽泻饮片的指纹图谱存在差异。结论结果重现性好,为控制泽泻饮片的质量提供了可靠的分析方法。【作者单位】: 山东省药品检验所 山东大学药学院 山东恒信检测技术开发中心 【关键词】: 泽泻 指纹图谱 高效液相色谱 蒸发光散射检测器 http://ng1.17img.cn/bbsfiles/images/2012/07/201207310810_380720_2352694_3.jpg
维权声明:本文为03yx2原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。 中文摘要 目的:建立泽泻药材中药效成分含量测定方法。方法:采用高效液相色谱法测定泽泻药材中泽泻醇B-23-乙酸脂的含量。结果:泽泻醇B-23-乙酸脂的平均回收率为99.47%,符合要求。泽泻中泽泻醇B-23-乙酸脂的含量不低于0.050%为宜。结论:本方法可作为泽泻定量控制的方法。关键词:泽泻;泽泻醇B-23-乙酸脂;高效液相色谱法;含量测定Abstract Purpose: To establish the efficacy of herbal medicine ingredients Zexie determination. Method: Determination of Zexie ingredients in Zexie stupid B-23-acid lipid content. Results: Zexie alcohol B-23-acid lipid, the average recovery rate was 99.47 percent, to meet the requirements. Zexie Zexie alcohol in the B-23-acid fat content of not less than 0.050 percent suitable. Conclusion: This method can be used as Zexie quantitative control methods. keywords:Rhizoma Alismatis Orientalitis;23 acetyl alisol B;HPLC;Determination.
https://wenku.so.com/d/ce6e8a062d3722ed156fbca7b6a263c3 [font=arial][size=22px][color=#333333]泽泻梗的功效与作用及禁忌 word版本[/color][/size][/font]
六味地黄丸主要成分:熟地黄、山药、山茱萸、泽泻、丹皮、茯苓,每种药的作用都是什么?哪个是君药呢?

[color=#444444]用的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url],乙醇和乙酰丙酸反应生成乙酰丙酸。乙醇和乙酰丙酸乙酯的峰分不开。柱前压0.15mpa.柱温200检测260注样260应该怎么调才能把峰分开?乙酰丙酸沸点245,乙酰丙酸乙酯沸点203[/color][color=#444444][img=,600,800]https://ng1.17img.cn/bbsfiles/images/2019/07/201907100951384017_3086_1843534_3.jpg!w600x800.jpg[/img][/color]
国内最大最专业的国家标准物质服务平台坛墨质检-国家标准物质中心(北京坛墨质检科技有限公司),是国家质检总局指定的国家标准物质研制单位,是国内最大最专业的食品、环境、职业卫生标准物质生产商和服务商。BW6129 罗汉果苷III,对照品,有证书 HPLC≥98% BW6130 拟人参皂苷Rh2,对照品,有证书 HPLC≥98% BW6131 (S型)原人参三醇,对照品,有报告 HPLC≥98% BW6132 (R型)人参皂苷Rh1 HPLC≥98% BW6133 (R型)人参皂苷Rh2,对照品,有报告 HPLC≥96% BW6134 人参皂苷Rh4,对照品,有报告 HPLC≥98% BW6135 人参皂苷Rh7,对照品,有证书 HPLC≥98% BW6136 (R型)人参皂苷Rg2,对照品,有证书 HPLC≥98% BW6137 (R型)人参皂苷Rg3 HPLC≥98% BW6138 人参皂苷F5 HPLC≥98% BW6139 人参皂苷Rg5 HPLC≥98% BW6140 人参皂苷Rk1 HPLC≥98% BW6141 人参皂苷Rk2 HPLC≥98% BW6142 人参皂苷Rk3 HPLC≥98% BW6143 三七皂苷Fe HPLC≥98% BW6144 越南参皂苷R3 HPLC≥94% BW6145 越南参皂苷R4 HPLC≥98% BW6146 越南参皂苷R8 HPLC≥98% BW6147 人参皂苷Ra1 HPLC≥98% BW6148 泽泻醇A HPLC≥98% BW6149 泽泻醇B HPLC≥98% BW6150 泽泻醇A-24-醋酸酯; HPLC≥98% BW6151 25-甲氧基泽泻醇A HPLC≥98% BW6152 23-乙酰泽泻醇C HPLC≥98% BW6153 泽泻醇F HPLC≥98% BW6154 25-脱水泽泻醇A HPLC≥98% BW6155 24-乙酰泽泻醇F,对照品,有证书 HPLC≥97% 坛墨质检现有员工79人,办公室面积450平米,实验室1650平米;销售、客服、财务及行政人员35人,实验室工作人员21人,库房14人,市场部8人。实验仪器设备:气相色谱、液相色谱、气质联用、液质联用、离子色谱、紫外分光光度计,原子吸收、ICP-OES和ICP-MS;库房面积450平米,库房工作人员12人,现货产品5万个,坛墨质检自主研发的产品近3000个,已申报国标345项,填补国内空白的产品达到65项。坛墨质检是国内唯一提供标准溶液定制服务的标准物质研制单位,定制范围:特殊浓度定制、特殊溶剂定制、混标定制。
国内最大最专业的国家标准物质服务平台坛墨质检-国家标准物质中心(北京坛墨质检科技有限公司),是国家质检总局指定的国家标准物质研制单位,是国内最大最专业的食品、环境、职业卫生标准物质生产商和服务商。 BW6142人参皂苷Rk3HPLC≥98%BW6143三七皂苷FeHPLC≥98%BW6144越南参皂苷R3HPLC≥94%BW6145越南参皂苷R4HPLC≥98%BW6146越南参皂苷R8HPLC≥98%BW6147人参皂苷Ra1HPLC≥98%BW6148泽泻醇AHPLC≥98%BW6149泽泻醇BHPLC≥98%BW6150泽泻醇A-24-醋酸酯;HPLC≥98%BW615125-甲氧基泽泻醇AHPLC≥98%BW615223-乙酰泽泻醇CHPLC≥98%BW6153泽泻醇FHPLC≥98%BW615425-脱水泽泻醇AHPLC≥98%BW615524-乙酰泽泻醇F,对照品,有证书HPLC≥97%BW6156α-常春藤皂苷HPLC≥98%BW6157白头翁皂苷A3HPLC≥98%BW6160白头翁皂苷D,对照品,有报告HPLC≥98%BW6161白头翁皂苷E2HPLC≥98%BW6162白头翁皂苷E3HPLC≥98%BW6163白头翁皂苷E4HPLC≥98%BW6164常春藤苷HHPLC≥98%BW6165灰毡毛忍冬次皂苷甲HPLC≥98%BW6166灰毡毛忍冬次皂苷甲对照品HPLC≥98%BW6168齐墩果酸-3-O-β-D葡萄糖( 1→3)-α-L-鼠李糖(1→2)-α-L-阿拉伯糖苷HPLC≥98%BW6169Lup-20(29)-en-28-oic acid, 3-oxHPLC≥98% 坛墨质检现有员工79人,办公室面积450平米,实验室1650平米;销售、客服、财务及行政人员35人,实验室工作人员21人,库房14人,市场部8人。实验仪器设备:气相色谱、液相色谱、气质联用、液质联用、离子色谱、紫外分光光度计,原子吸收、ICP-OES和ICP-MS;库房面积450平米,库房工作人员12人,现货产品5万个,坛墨质检自主研发的产品近3000个,已申报国标345项,填补国内空白的产品达到65项。坛墨质检是国内唯一提供标准溶液定制服务的标准物质研制单位,定制范围:特殊浓度定制、特殊溶剂定制、混标定制。
国内最大最专业的国家标准物质服务平台坛墨质检-国家标准物质中心(北京坛墨质检科技有限公司),是国家质检总局指定的国家标准物质研制单位,是国内最大最专业的食品、环境、职业卫生标准物质生产商和服务商。 产品编号 产品名称 标准值 BW68908-甲基大黄酚HPLC≥98%BW6136(R型)人参皂苷Rg2,对照品,有证书HPLC≥98%BW6137(R型)人参皂苷Rg3HPLC≥98%BW6139人参皂苷Rg5HPLC≥98%BW6140人参皂苷Rk1HPLC≥98%BW6141人参皂苷Rk2HPLC≥98%BW6142人参皂苷Rk3HPLC≥98%BW6143三七皂苷FeHPLC≥98%BW6144越南参皂苷R3HPLC≥94%BW6145越南参皂苷R4HPLC≥98%BW6146越南参皂苷R8HPLC≥98%BW6147人参皂苷Ra1HPLC≥98%BW6148泽泻醇AHPLC≥98%BW6149泽泻醇BHPLC≥98%BW6150泽泻醇A-24-醋酸酯;HPLC≥98%BW615125-甲氧基泽泻醇AHPLC≥98%BW615223-乙酰泽泻醇CHPLC≥98%BW6153泽泻醇FHPLC≥98%BW615425-脱水泽泻醇AHPLC≥98%BW615524-乙酰泽泻醇F,对照品,有证书HPLC≥97%BW6156α-常春藤皂苷HPLC≥98%BW6157白头翁皂苷A3HPLC≥98%BW6160白头翁皂苷D,对照品,有报告HPLC≥98%BW6161白头翁皂苷E2HPLC≥98%BW6162白头翁皂苷E3HPLC≥98%BW6163白头翁皂苷E4HPLC≥98% 坛墨质检现有员工79人,办公室面积450平米,实验室1650平米;销售、客服、财务及行政人员35人,实验室工作人员21人,库房14人,市场部8人。实验仪器设备:气相色谱、液相色谱、气质联用、液质联用、离子色谱、紫外分光光度计,原子吸收、ICP-OES和ICP-MS;库房面积450平米,库房工作人员12人,现货产品5万个,坛墨质检自主研发的产品近3000个,已申报国标345项,填补国内空白的产品达到65项。坛墨质检是国内唯一提供标准溶液定制服务的标准物质研制单位,定制范围:特殊浓度定制、特殊溶剂定制、混标定制。
[size=3][size=4]我需要做乙酰丙酸的标准曲线,看别的文章后,按他写的方法试过,完全不是他说的结果,请问哪位做过乙酰丙酸的标准曲线,用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url],可否将方法相告!不胜感激![/size][/size]
急求标准对二氯苯、五氯化磷、乙酰氯、对甲苯磺酰胺、乙二醇甲醚、马来酸国标、化工标准、地方标准都行谢谢!![em0808]
乙酰丙酮烯醇式羟基氢的吸收峰为何不是尖峰,而是宽峰?
各位老师,乙酰乙酸乙酯说有烯醇类和酮类平衡的混合物。那是不是就是说,我进一针乙酰乙酸乙酯的分析纯,应该出两个峰,一个乙酰乙酸乙酯(烯醇类),一个是乙酯乙酯乙酯(酮类)。
朋友们谁有苯甲酸甲酯、对甲苯磺酸、TEBAC、甲醇钠、4-二甲胺基吡啶、苯甲酰氯、乙硫醇、巴豆醛、乙酰乙酸甲酯、丙酰氯、DCP的国标、行标或企业标准啊?帮忙找一下啊,谢谢!

NMR测定乙酰丙酮稀醇化焓(enthalpy)http://www.colby.edu/chemistry/PChem/lab/enthalpyenolnmr.pdf[img]http://ng1.17img.cn/bbsfiles/images/2007/11/200711230907_70737_1604620_3.jpg[/img]
带乙酰基的东西能走液相吗,用甲醇和水走出的谱图每次都不一样
问:请问乙酰氯的GC分析方法极其标准?我们是是化工企业,生产高纯乙酰氯,分析量很大,我们目前用GC-FID毛细管柱子,没有标准品,含量大约99。5%,请问这样分析的缺陷,用HPLC行不行?假如有其他微量杂质,是否还要用质谱仪?
[font='微软雅黑','sans-serif'][size=12pt]空[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]量甲醛的测定乙酰丙酮分光光度法[/size][/font][font='Times New Roman','serif'][size=12pt]GB/T15516[/size][/font][font='微软雅黑','sans-serif'][size=12pt]中乙酰丙酮溶液的配制,新蒸馏的[/size][/font][font='Times New Roman','serif'][size=12pt]0.25ml[/size][/font][font='微软雅黑','sans-serif'][size=12pt]乙酰丙酮该怎么蒸馏可不可以不蒸馏直接用?[/size][/font][font='微软雅黑','sans-serif'][size=12pt][color=#ff0000]注:问题来自水质分析交流群。[/color][/size][/font]
最近做乙酰甲胺磷发现一个奇特的现象。方法如下,乙腈提取提取,浓缩后过某大品牌氨基柱,乙腈甲苯3:1淋洗,浓缩后甲醇水定容,上LCMSMS,定量用基质标。基质为普通白菜。上机试液理论值100ppb,结果乙酰甲胺磷没有出来,开始以为氨基柱的问题,后来一个突发想法,把试样稀释了十倍,再上机分析,乙酰甲胺磷回来了,而且值为6~8ppb,符合回收率。LCMSMS为watersuplc,TQD,C18液相柱。请问各位同行,有用液质做乙酰甲胺磷的大侠吗?基质效应那么大?
乙酰甲胺磷经过S、A、W等品牌的SPE柱子净化后,回收率能有多少?A、W的NH2柱乙腈甲苯(3+1),回收率为0;W的工程师在W实验室得到同样的结果,用乙腈甲醇(3+1),回收率为0;乙腈水(3+1)回收率为114%您,怎么看?
1、1瓶新购的分析纯试剂AR乙酰丙酮,1瓶3年前购买的AR 乙酰丙酮,和标准浓度甲醛显色读取吸光度值,做曲线。 显色后颜色看起来差不多,但吸光度值相差不小,曲线斜率也不一样,AR 乙酰丙酮的有效期多长,对结果有何影响?2、分光光度计的检定:一般实验室是怎么检定的?是用那个标准片,还是用标准试剂核查不同波长的吸光度值?3、大家用的分光光度计都是什么型号的(我们用的是723PC)?哪种比较好用?
[color=#444444]在检测乙酰乙酸乙酯的纯度,但乙酰乙酸乙酯在[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]中的峰形总有前沿,是色谱柱的问题还是其他方面?望指教一二[/color]
乙酰基六肽-8英文名:Acetyl Hexapeptide-8CAS:616204-22-9【详情请咨询国肽生物】化学式:C34H60N14O12S分子量:888.91序 列:Ac-Glu-Glu-Met-Gln-Arg-Arg-NH2结构式产品特性:1. 能局部阻断神经传递收缩信息,影响皮囊神经传导,使脸部肌肉放松 ,达到平抚动态纹,静态纹和细纹。2. 功效可以与A型肉毒素媲美 ,但是又避开了肉毒素又必须注射和使用成本高昂的缺点,具有与肉毒杆菌素注射相同的除皱效果质量标准:外观:白色粉末分子量:888.9+水分:8%肽含量:80%纯度:95%氨基酸组份:应用:抗皱,保湿提高皮肤弹性和色泽产品推荐用量:0.01%-0.05%包装:10g,50g,100g/塑料瓶储存:阴凉,干燥避光处保存,在冰箱中2-8度保存保质期:以上储存条件下2年机理:乙酰基六肽-8参与竞争 SNAP - 25 在融泡复合体的位点, 从而影响复合体的形成。当融泡复合体稍有不稳定, 囊泡不能有效释放神经递质, 从而致使肌肉收缩减弱,防止皱纹的形成。国肽生物主要提供:多肽合成、多肽定制、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、美容肽、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。详情请咨询国肽生物
[size=4]如题,谁用过乙酰丙酮法测气体中的甲醛,有什么经验?过程中应主要哪些问题?热烈欢迎大家积极发言。[/size]
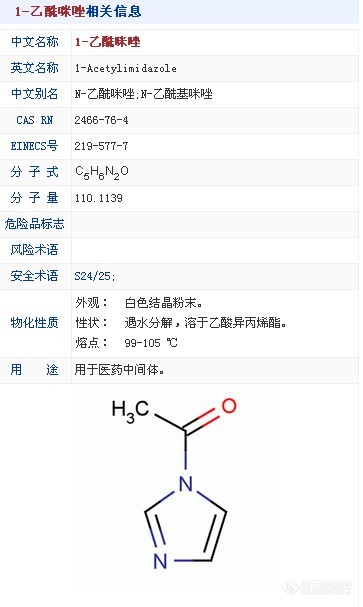
1-乙酰咪唑相关信息如图所示。水解产物是否为咪唑和乙酸?产品的体系为乙醇,水和多肽。乙酰咪唑是用来合成多肽时封闭和试剂,要求检测残留量,如果水解产物是咪唑的话,很想知道咪唑的检测方法(残留量),当然是越快速的越好。定性检测。谢谢各位!http://ng1.17img.cn/bbsfiles/images/2011/08/201108291337_312722_1665695_3.jpg
乙酰二茂铁的合成目的原理实验目的 1 通过乙酰二茂铁的制备,了解用Friendel-Crafts酰基化反应制备非苯芳酮的原理和方法。2 学习柱色谱分离提纯产品和薄层色谱跟踪反应进程的原理和操作方法。实验原理 二茂铁又名双环戊二烯基铁,是由2个环戊二烯负离子和一个二价铁离子键合而成。一般认为,以乙酸酐为酰化剂,三氟化硼,氢氟酸,磷酸为催化剂,主要生成一元取代物;如用无水三氯化铝为催化剂,酰氯或酸酐为酰化剂,当酰化剂与二茂铁的摩尔比为2∶1时,反应产物以1,1′-二元取代物为主。二茂铁及其衍生物的分离最好是用层析法。本实验用柱色谱分离提纯产品,可用薄层色谱法跟踪反应进程,柱色谱和薄层色谱均属于吸附色谱,柱色谱分离提纯是根据二茂铁,乙酰二茂铁和1,1′-二乙酰基二茂铁对活性氧化铝吸附能力的差异而进行分离提纯。用薄层色谱跟踪反应进程,根据二茂铁和乙酰二茂铁的斑点大小可以了解乙酰化反应的进程。仪器药品 5ml圆底烧瓶,克莱森接头,干燥管,电磁加热搅拌器,30cm色谱柱(自制),30×100mm载玻片,离心试管50ml烧杯,玻璃钉漏斗,吸滤瓶,锥形瓶,氮气袋,250ml烧杯二茂铁,乙酸酐,85%H3PO4,25%NaOH,二氯甲烷,棉花,洗净的砂,Ⅲ级活性氧化铝,己烷,醇,硅胶,0.5%羚甲基纤维素,干燥氮气。过程步骤 一、乙酰二茂铁的制备称取100mg(0.54mmol)二茂铁,放入5ml圆底烧瓶中,加入2.0ml醋酸酐。装上带有干燥管的克莱森接头。水浴温热并搅拌使二茂铁溶解。移去水浴,打开塞子迅速加入3ml 85% H3PO4,使反应液变成深红色,室温下搅拌1.5h,在反应期间定期用毛细管在液面上吸取2滴左右反应液放入具塞小试管中,假如10滴二氯甲烷,所得溶液用薄层色谱法展开,以了解反应进程。当二茂铁的斑点很浅时,表示反应基本完成。将反应液滴入盛有1g碎冰5ml烧杯中,滴加25%NaOH中和恰至碱性,得到大量桔黄色沉淀。充分冷却后抽滤,1ml冷水分几次洗涤沉淀,抽干,干燥后称重约110~120mg。二、乙酰基二茂铁的柱色谱法分离(1)干法装柱将粗产品溶于0.5ml二氯甲烷加入300mgⅢ级活性氧化铝,振荡均匀得浆状物。在通风橱中,在干燥氮气下除去溶剂至恒重,得到松散的颗粒状物,精确称取1/2用作柱色谱分离。将自制的1.5×30cm色谱柱洗净,干燥,柱底铺一层玻璃棉或脱脂棉,再铺一层约5~8mm厚的砂,填平。称取5gⅢ级活性的中性氧化铝(60~80目),通过漏斗将氧化铝装入柱管内,轻敲柱管,使之填均匀。将精确称得含有1/2产品重的氧化铝装入柱内,顶部盖一层约5mm厚的砂子,使氧化铝顶端和砂子上层保持水平。(2)洗脱用己烷作洗脱剂从柱顶加入,缓慢滴入己烷逐渐展开得到黄色、橙色分离的色谱带。黄色的二茂铁带首先从柱下流出,用己称重的锥形瓶收集洗脱溶液。当黄色谱带完全洗脱下来时,改用体积比为1∶1的二氯甲烷己烷混合物洗脱,同时橙色带往下移动,逐渐改变溶剂的比例到体积比9∶1二氯甲烷己烷混合溶剂时,则将橙色色谱带完全洗脱下来,用另一只已称重的锥形瓶收集洗脱液。最后改用体积比为9∶1二氯甲烷甲醇洗脱时,可以看到很淡的,很少量的,棕色色带向下移动,将该洗脱液另行收集。(3)收集产品在通风橱内,各组分洗脱液分别在水浴上蒸馏,回收溶剂。浓缩后的溶液放置冷却析出结晶,将产品放在盛有石蜡片的干燥器内至恒重。可回收到未反应的二茂铁20~22mg;得到乙酰二茂铁80~90mg 1,1′-二乙酰基二茂铁少于2mg。分别测定熔点。注意事项1.二茂铁需经升华或用石油醚(30~60℃)重结晶纯化。2.仪器应是充分干燥的。3.乙酸酐是临用前经重新蒸馏的。4.吸附剂的活性与其含水量的关,含水量越低,活性越高。氧化铝放入高温炉中(300~400℃)烘3h得无水物即Ⅰ级氧化铝。Ⅲ级氧化铝可用Ⅰ级活性氧化铝加入重量的6%的水而得到。如所用氧化铝活性过强会使产品不易洗脱,浪费较多的溶剂。5.这里是考虑到柱色谱的容器。一般粗产品重75mg以上都仅取1/2作柱色谱分离。6.二茂铁易升华,故测熔点时要封管。熔点的文献值:二茂铁为173℃,乙酰二茂铁为85℃,1,1ˊ-乙酰基二茂铁为130℃。分析思考1. 二茂铁乙酰化反应的机理怎样?2. 怎样利用薄层层析判断乙酰化反应的进程?3. 乙酰二茂铁在石油醚和乙醚中溶解度哪个更大?为什么?4. 柱层析分离二茂铁衍生物时,如何选择展开的溶剂? [img]http://ng1.17img.cn/bbsfiles/images/2007/05/200705162025_52002_1632583_3.gif[/img][img]http://ng1.17img.cn/bbsfiles/images/2007/05/200705162025_52003_1632583_3.gif[/img]
GB/T15516-1995 乙酰丙酮分光光度法测环境空气中甲醛。标准采样体积的计算:[font='Times New Roman'] [/font][size=3]Vnd=V[font=宋体]m[/font][font=宋体]×2.694×273/(273+Tm)×Pm/P0[/font][/size][font='Times New Roman'][/font]请问一下,式中2.694是啥意思啊?
[font=&][size=18px]N,N-二甲基乙酰胺又称乙酰基二甲胺、乙酰二甲胺,简称DMAC,是一种非质子高极性溶剂,有微氨气味,溶解力很强,可溶解的物质范围很广,能与水、芳香族化合物、酯、酮、醇、醚、苯和三氯甲烷等任意混溶,且能使化合物分子活化,因此广泛用作溶剂及催化剂。在溶剂方面作为高沸点、高闪点、热稳定性高、化学性稳定的溶剂,可用于聚丙烯腈的抽丝溶剂、合成树脂及天然树脂、甲酸乙烯酯、乙烯基吡啶等共聚物及芳烃羧酸的溶剂;在催化剂方面可用于尿素加热制氰尿酸、卤代烷与金属氰化物反应制腈、乙炔钠与卤代烷反应制烷基炔、有机卤化物与氰酸盐反应制异氰酸酯等过程。N,N-二甲基乙酰胺还可用作电解溶剂及摄影用成色剂的溶剂、脱油漆剂、有机合成原料、农药及医药原料。从C8馏分中分离苯乙烯的萃取蒸馏溶剂等。[/size][/font]