2012年06月22日 来源: 科学与发展网络 作者: 李娇 经过中国国家食品药品监督管理局(SFDA)一年多的监督和检查,中国科学家研制的戊型肝炎疫苗应该在今年底之前就能用了。 科学家在厦门大学的国家传染病诊断试剂与疫苗工程技术研究中心(NIDVD)研制出这种疫苗。 该疫苗获得SFDA的批准前在医学杂志《柳叶刀》发表三期临床试验,试验显示在防止感染方面疫苗是100%有效的。 厦门万泰沧海生物技术公司(简称INNOVAX)是厦门大学的研发伙伴,据INNOVAX总经理高永忠称,该公司目前正在准备将疫苗引入市场。 预计中国的疫苗将成为世界上第一个投产的戊肝疫苗。 2007年,葛兰素史克(GSK)与美国军方合作开发了一种单独的疫苗。该疫苗在尼泊尔进行的二期试验发现其在防止感染方面具备超过95%的有效性。 据GSK公司的一名发言人Eleanor Bunch称,该公司没有将这种疫苗推向投产,对进一步试验资助以及通过合作伙伴商业化的努力是不成功的。但她表示,GSK仍然“愿意与第三方共同运作来分享所取得的成果和专业知识”。 戊型肝炎病毒导致每年大约2000万人感染。由此而导致每年大约300万人患急性病症,而7万人死亡。这对孕妇来说是特别危险的,因为20%的病例会发展成为这种病的急性形式,这将是致命的。 牛津大学临床研究尼泊尔小组的Buddha Basnyat对疫苗的前景表示欢迎,该小组是由位于加德满都的Patan医院主办的。“这一重要的疫苗终于可以用了,这是件伟大的事,”他告诉科学与发展网络。 世界卫生组织传播干事Tarik Jasarevic告诉科学与发展网络,“中国应该因发展中国家的首个得到许可的HEV(戊型肝炎病毒)疫苗而受到赞扬。” 厦门大学和INNOVAX公司现在计划申请将这种疫苗注册到世界卫生组织的资格预审项目,该项目可以让药品能被联合国儿童基金会(儿童基金会)和联合国HIV/AIDS联合项目(UNAIDS)等机构使用。 位于新德里的国际遗传工程和生物技术中心印度分部的病毒学研究组组长Shahid Jameel表示,中国的新疫苗对于那些去疾病流行国家(比如印度、中国)旅行的人以及疾病流行地区的孕妇来说是特别有用的。 “在后者的人群里,我相信它能拯救很多生命,所以这是一个重大的进展,”Jameel 告诉科学与发展网络道。 美国疾病控制和预防中心(CDC)病毒性肝炎部门流行病学和监测分部主任Scott Holmberg表示,“鉴于非洲撒哈拉以南地区的戊型肝炎的大爆发,很多孕妇和两岁以下的婴儿在爆发中(死亡了),美国CDC调查员渴望找到一种能在爆发情况下有效的疫苗。”(李娇)
[b][font=inherit]项目概况[/font][/b]乙型肝炎病毒表面抗原等项目诊断试剂盒、校准品及相关耗材招标项目的潜在投标人应在全国公共资源交易平台(陕西省西安市)网站〖首页〉电子交易平台〉陕西政府采购交易系统〉企业端获取招标文件,并于 2023年02月24日 09时30分 (北京时间)前递交投标文件。[b][font=inherit]一、项目基本情况[/font][/b]项目编号:DXSY2022-066项目名称:乙型肝炎病毒表面抗原等项目诊断试剂盒、校准品及相关耗材采购方式:公开招标预算金额:2,000,000.00元采购需求:合同包1(乙型肝炎病毒表面抗原等项目诊断试剂盒、校准品及相关耗材):合同包预算金额:2,000,000.00元合同包最高限价:2,000,000.00元[table=100%][tr][td]品目号[/td][td]品目名称[/td][td]采购标的[/td][td]数量(单位)[/td][td]技术规格、参数及要求[/td][td]品目预算(元)[/td][td]最高限价(元)[/td][/tr][tr][td]1-1[/td][td]诊断用生物试剂盒[/td][td]乙型肝炎病毒表面抗原等项目诊断试剂盒、校准品及相关耗材[/td][td]1(批)[/td][td]详见采购文件[/td][td]2,000,000.00[/td][td]2,000,000.00[/td][/tr][/table]本合同包不接受联合体投标合同履行期限:2023-04-01 00:00:00 至2024-03-31 00:00:00(具体服务起止日期可随合同签订时间相应顺延)
[table][tr][td]项目概况河南省红十字血液中心乙型肝炎病毒、丙型肝炎病毒、人类免疫缺陷病毒(1+2型)核酸检测试剂盒([url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]-荧光法)采购项目招标项目的潜在投标人应在登录“河南省公共资源交易中心 (http://www.hnggzy.net/) ”,凭 CA 数字证书获取招标文件,并于2023年09月06日09时00分(北京时间)前递交投标文件。[/td][/tr][tr][td]一、项目基本情况[/td][/tr][tr][td]1、项目编号:豫财招标采购-2023-783[/td][/tr][tr][td]2、项目名称:河南省红十字血液中心乙型肝炎病毒、丙型肝炎病毒、人类免疫缺陷病毒(1+2型)核酸检测试剂盒([url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]-荧光法)采购项目[/td][/tr][tr][td]3、采购方式:公开招标[/td][/tr][tr][td]4、预算金额:5,492,500.00元[/td][/tr][tr][td]最高限价:5492500元[/td][/tr][tr][td=2,1][table][tr][td]序号[/td][td]包号[/td][td]包名称[/td][td]包预算(元)[/td][td]包最高限价(元)[/td][/tr][tr][td]1[/td][td]豫政采(2)20231230-1[/td][td]河南省红十字血液中心乙型肝炎病毒、丙型肝炎病毒、人类免疫缺陷病毒(1+2型)核酸检测试剂盒([url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]-荧光法)采购项目[/td][td]5492500[/td][td]5492500[/td][/tr][/table][/td][/tr][tr][td]5、采购需求(包括但不限于标的的名称、数量、简要技术需求或服务要求等)[/td][/tr][tr][td]5.1 采购货物名称及数量:乙型肝炎病毒、丙型肝炎病毒、人类免疫缺陷病毒(1+2型)核酸检测试剂盒([url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]-荧光法) 650盒(384人份/盒)。5.2 标包划分:1 个标包5.3 采购货物技术性能指标:具体参数详见招标文件第五章“采购需求”5.4 采购范围:试剂的供货、运输、保险、装卸、验收交付、培训、技术支持、质保及相关伴随服务等5.5 资金来源:财政资金,已落实5.6 交货期:合同签订后7日内按要求分批次交货5.7 交货地点:采购人指定地点[/td][/tr][tr][td]6、合同履行期限:按合同执行[/td][/tr][tr][td]7、本项目是否接受联合体投标:否[/td][/tr][tr][td]8、是否接受进口产品:否[/td][/tr][tr][td]9、是否专门面向中小企业:否[/td][/tr][tr][td]二、申请人资格要求:[/td][/tr][tr][td]1、满足《中华人民共和国政府采购法》第二十二条规定;[/td][/tr][tr][td]2、落实政府采购政策满足的资格要求:[/td][/tr][tr][td]节约能源、保护环境、扶持不发达地区和少数民族地区、促进中小微企业、监狱企业及残疾人福利性单位发展等政府采购政策。[/td][/tr][tr][td]3、本项目的特定资格要求[/td][/tr][tr][td]3.1根据《财政部关于在政府采购活动中查询及使用信用记录有关问题的通知》(财库〔2016〕125 号)和《河南省财政厅关于转发财政部关于在政府采购活动中 查询及使用信用记录有关问题的通知》(财库〔2016〕15 号)被列入中国政府采购网( www.ccgp.gov.cn)“政府采购严重违法失信行为记录名单”的(指政府采购行政处罚有效期内);被列入“中国执行信息公开网”(http://zxgk.court.gov.cn/shixin)失信被执行人的;被列入“信用中国”网站(www.creditchina.gov.cn)“重大税收违法失信主体”的投标人将被拒绝参加投标。注:(采购人、代理机构在开标后对所有投标供应商信用记录进行查询,并将查询结果网页打印存档,投标供应商不良信用记录以代理机构开标后查询结果为准。 )3.2单位负责人为同一人或者存在直接控股、管理关系的不同供应商,不得参加同一合同项下的投标。[/td][/tr][tr][td]三、获取招标文件[/td][/tr][tr][td]1.时间:2023年08月16日 至 2023年08月22日,每天上午00:00至12:00,下午12:00至23:59(北京时间,法定节假日除外。)[/td][/tr][tr][td]2.地点:登录“河南省公共资源交易中心 (http://www.hnggzy.net/) ”,凭 CA 数字证书[/td][/tr][tr][td]3.方式:《河南省公共资源交易中心-市场主体系统》中下载投标项目所含全部资料[/td][/tr][tr][td]4.售价:0元[/td][/tr][tr][td]四、投标截止时间及地点[/td][/tr][tr][td]1.时间:2023年09月06日09时00分(北京时间)[/td][/tr][tr][td]2.地点:河南省公共资源交易中心远程开标室(一)-2[/td][/tr][tr][td]五、开标时间及地点[/td][/tr][tr][td]1.时间:2023年09月06日09时00分(北京时间)[/td][/tr][tr][td]2.地点:河南省公共资源交易中心远程开标室(一)-2(郑州市经二路12号(经二路与纬四路向南50米路西))[/td][/tr][tr][td]六、发布公告的媒介及招标公告期限[/td][/tr][tr][td]本次招标公告在《河南省政府采购网》、《河南省公共资源交易中心网》上发布, 招标公告期限为五个工作日。[/td][/tr][tr][td]七、其他补充事宜[/td][/tr][tr][td]1、本项目采用“远程不见面”开标方式,供应商无需到河南省公共资源交易中心现场参加开标会议及递交纸质标书,无需到达现场提交原件资料。2、不见面服务的具体事宜请查阅河南省公共资源交易中心网站“办事指南”专区的《新交易平台使用手册(培训资料)》中《河南省公共资源“智慧交易”平台-不见面开标大厅投标人操作手册》。3、逾期上传/送达的或者未上传/未送达指定地点的响应文件,采购人不予受理[/td][/tr][tr][td]八、凡对本次招标提出询问,请按照以下方式联系[/td][/tr][tr][td]1. 采购人信息[/td][/tr][tr][td]名称:河南省红十字血液中心[/td][/tr][tr][td]地址:郑州市金水区同乐路9号[/td][/tr][tr][td]联系人:司丽萍[/td][/tr][tr][td]联系方式:0371-63831305[/td][/tr][tr][td]2.采购代理机构信息(如有)[/td][/tr][tr][td]名称:中韵天隆工程集团有限公司[/td][/tr][tr][td]地址:郑州市金水区青年路145号升龙环球大厦C座26楼2608室[/td][/tr][tr][td]联系人:王京拴 王自红[/td][/tr][tr][td]联系方式:0371-88881296[/td][/tr][tr][td]3.项目联系方式[/td][/tr][tr][td]项目联系人:王京拴 王自红[/td][/tr][tr][td]联系方式:0371-88881296[/td][/tr][/table]
替比夫定协助根治-慢性乙型肝炎来自第60届美国肝病研究学会(AASLD)年会最新研究结果HBV共价闭合环状DNA(ccc DNA)的存在是慢性乙肝(CHB)患者停药后复发的原因,由于ccc-DNA存在于肝细胞核内,故常规检查无法动态监测其肝内水平。研究显示,HBsAg水平与肝组织中HBV ccc DNA水平呈正相关。因此,用HBsAg水平预测停药后持久应答对于停药标准的确定、实现CHB的有限疗程策略具有重要意义。 今年在波士顿举行的第60届美国肝病研究学会(AASLD)年会报告了两项有关替比夫定治疗期间HBsAg动力学变化与停药后持久应答相关性的研究,使替比夫定在慢乙肝治疗中的地位再次备受关注。众所周知,替比夫定具有强效病毒抑制及高HBeAg血清学转换率的双重优势和停药后持久应答率高的特点,这为患者通过有限疗程的治疗实现病毒的长期抑制提供了可能。本届年会报告的替比夫定研究为如何通过HBsAg水平的变化,预测替比夫定停药后的持久应答提供了重要的临床依据。http://oneyao.net/uploadfile/article/uploadfile/201001/20100121090143399.jpghttp://oneyao.net/uploadfile/article/uploadfile/201001/20100121090806846.jpghttp://oneyao.net/uploadfile/article/uploadfile/201001/20100121090853922.jpghttp://oneyao.net/uploadfile/article/uploadfile/201001/20100121090935172.jpg 替比夫定治疗期间 HBsAg水平可预测停药后持久完全应答 来自中国上海瑞金医院的谢青教授观察了替比夫定治疗CHB患者2年间HBsAg水平与停药后2年持久应答的相关性。研究方法是:22例CHB患者应用替比夫定600 mg/d持续治疗104周,完成104周治疗后,达到停药标准的患者予以停药,停药后继续观察104周(共随访208周)以了解持久应答情况。停药标准定义为HBeAg阳性患者达到HBeAg血清学转换、HBV DNA检测不到(0.8 log IU/ml、52周及以后血清HBsAg水平较基线下降值 >1 log IU/ml以及104周时血清HBsAg定量<2 logIU/ml,可预测停药能获得持久完全应答。24周时血清HBsAg水平较基线下降值3log IU/ml,并在随后的治疗过程中下降值维持3log IU/ml,提示治疗104周停药后,不仅可获得持久完全应答,甚至可在停药期间获得HBsAg血清学转换。由此可见,治疗期间HBsAg水平显著下降可预测替比夫定治疗2年后停药2年获得持久完全应答(图2)。 该项研究提示,可通过治疗期间HBsAg水平来预测替比夫定疗效及停药后持久完全应答情况,这对于更准确地把握替比夫定停药时机、实现有限疗程治疗CHB具有重要参考意义。 治疗中HBsAg迅速下降可预测替比夫定治疗3年后实现HBsAg清除 依据2009欧洲肝脏研究学会(EASL)指南,HBsAg转阴伴(或不伴)血清学转换是CHB的理想治疗终点。治疗中HBsAg水平是否有助于预测HBsAg转阴是目前研究的热点,德国汉诺威医学院沃思特恩(Wursthorn)对替比夫定治疗CHB患者3年血清HBsAg下降动力学进行了研究。 研究对象是GLOBE研究中替比夫定组治疗2年获得HBV DNA检测不到后进入2303延长研究至少52周的患者,其中162例HBeAg阳性,143例HBeAg阴性。 结果显示,替比夫定治疗3年,HBeAg阳性患者的HBeAg转阴率为71%,HBeAg血清学转换率为57%,9例(6%)患者获得HBsAg转阴,5例(3%)获得HBsAg血清学转换;HBeAg阴性患者中 2例(1%)获得HBsAg转阴,1例(1%)获得HBsAg血清学转换;基线血清HBsAg水平与HBV DNA水平显著相关,替比夫定治疗3年两组患者HBsAg水平均较基线下降。HBeAg阳性患者的HBsAg水平下降主要呈现在治疗的第1年,而阴性患者的HBsAg水平下降主要在治疗的第2、3年时才观察到。 根据替比夫定治疗24周HBsAg下降幅度,可将患者HBsAg下降分为3种模式:① HBsAg迅速下降,24周下降幅度≥ 0.5logIU/ml,此组患者在第3年出现HBsAg转阴几率最大;② HBsAg缓慢下降,24周下降幅度≤0.5 logIU/ml,此组患者至第3年出现HBsAg转阴的几率远低于上组患者;③ 在24周内呈现HBsAg波动,此组中无患者出现HBsAg转阴。 根据替比夫定治疗1年HBsAg 下降幅度,同样可分为3种模式:①HBsAg迅速下降,1年下降≥ 1logIU/ ml,此组患者在第3年出现HBsAg转阴几率最高达25%;② HBsAg缓慢平稳下降,但第一年下降≤1 logIU/ml,此组患者至第3年出现HBsAg转阴的几率远低于上组患者,仅1.4%;③ 在第一年呈现HBsAg波动,此组中无患者出现HBsAg转阴。 大部分HBsAg转阴患者24周及1年时HBsAg呈迅速下降。在HBeAg阳性患者和HBeAg阴性患者中,24周及1年HBsAg迅速下降与高HBsAg清除率相关。1年时血清HBsAg水平较基线下降值≥ 1logIU/ ml的患者,3年时HBsAg转阴率为25%(图3)。 由此得出结论,HBeAg阳性患者与阴性患者基线血清学HBsAg水平与HBV DNA水平相关。替比夫定治疗可降低CHB患者血清学HBsAg水平。治疗时HBsAg迅速下降 (24周下降≥0.5logIU/ml,1年下降≥ 1logIU/ ml)是未来实现HBsAg清除的强有力预测指标。 小 结 ● 替比夫定治疗CHB期间,HBsAg水平可预测停药后持久完全应答情况,有助于选择停药时机,实现有限疗程策略; ● 替比夫定治疗可降低患者血清HBsAg水平,治疗时HBsAg迅速下降 (24周下降≥0.5 logIU/ml,1年下降≥ 1logIU/ml)是HBsAg清除的有力预测指标。
http://share.vrs.sohu.com/549029/v.swf视频:重庆啤酒豪赌乙肝疫苗十三年 股价如自由落体坠落 本报记者 刘国锋 重庆啤酒(600132)10日披露了“治疗用(合成肽)乙型肝炎疫苗”研究进度。包括券商医药行业研究员、私募投资者、疫苗研发专家在内多位业内人士对中国证券报记者表示,若不考虑安慰剂组应答率过高,可认为重庆啤酒治疗用乙型肝炎疫苗研发“失败” 相关公司股票走势http://d1.biz.itc.cn/q/cn/132/600132/tline2.png?1326168727331 重庆啤酒25.61-2.84-9.98%。公告称,重庆啤酒股票将于10日复牌。 疗效指标很不乐观 重庆啤酒10日公告显示,在主要疗效指标中,无论是“意向性治疗人群”还是“符合方案人群”,其安慰剂组与εPA-44 600μg组及εPA-44 900μg组相比,HBeAg/抗HBe血清转换在统计意义上均无差异。 在次要疗效指标中,第76周的血清学应答、病毒学应答及生化学应答情况,其试验的安慰剂组与εPA-44 600μg组及εPA-44 900μg组相比,在统计意义上均无差异。 在临床安全性指标中,εPA-44 600μg组和εPA-44 900μg组发生不良事件的比例分别为54.2%和51.7%,均高于安慰剂组45.8%的比例;εPA-44 600μg组和εPA-44 900μg发生严重不良事件的比例均为0.8%,均低于安慰剂组3.3%的水平。 对市场曾广泛质疑的主要疗效指标中安慰剂组应答率过高的问题,重庆啤酒未作回应,试验终稿对该数据维持不变。长期对重庆啤酒治疗性乙肝疫苗临床试验做草根调查的深圳私募投资者王先生对中国证券报记者表示,在1月4日的临床专家讨论会议上,曾有专家对安慰剂组的疗效提出强烈质疑。 两位券商医药行业研究员对中国证券报记者表示,从临床数据终稿看,次要疗效指标未打破原有悲观预期,重庆啤酒治疗用乙型肝炎疫苗基本可宣告无效。现在唯一的疑问仍是为何安慰剂组应答率如此高。 大连汉信生物的一位资深疫苗研发人员认为,从数据看,重庆啤酒治疗性乙肝疫苗没有什么疗效。 总结报告仍是看点 中国证券报记者致电武汉生物制品研究所病毒疫苗研究室主任李萍萍时了解到,疫苗研发的Ⅰ期临床试验主要考察药品安全性,Ⅱ期临床试验主要考察治疗有效性,如果Ⅱ期临床有效性看不出明显差异,想进入Ⅲ期临床就非常困难。 上述券商医药行业研究员显然更为激进,认为临床上主要看重统计学指标意义,目前重庆啤酒治疗用乙肝疫苗的主要和次要治疗指标在统计学意义上均没有差异,也就无法继续进行试验。 上海奉贤生物医药技术转移中心一位疫苗专家对中国证券报记者表示,现在从表面看,重庆啤酒治疗用乙肝疫苗确实无效,但必须看到设计方案,才能知道能否还有希望。治疗性疫苗与预防性疫苗在试验预期上有较大不同,美国已出现的治疗性肿瘤疫苗,主要效果并不是把肿瘤治好,而是将肿瘤患者的生存时间延长4个月,最后被批准上市。目前可把治疗性疫苗理解为一种提高免疫力的药物。从这个角度讲,重庆啤酒于4月6日出具的临床研究总结报告终稿仍是一大看点。
[b][font=inherit]项目概况[/font][/b]乙型肝炎病毒表面抗原等项目诊断试剂盒、校准品及相关耗材(二次)招标项目的潜在投标人应在全国公共资源交易平台(陕西省西安市)网站〖首页〉电子交易平台〉陕西政府采购交易系统〉企业端〗获取招标文件,并于 2023年03月28日 09时30分 (北京时间)前递交投标文件。[b][font=inherit]一、项目基本情况[/font][/b]项目编号:DXSY2022-066.1B1项目名称:乙型肝炎病毒表面抗原等项目诊断试剂盒、校准品及相关耗材(二次)采购方式:公开招标预算金额:2,000,000.00元采购需求:合同包1(乙型肝炎病毒表面抗原等项目诊断试剂盒、校准品及相关耗材):合同包预算金额:2,000,000.00元合同包最高限价:2,000,000.00元[table=100%][tr][td]品目号[/td][td]品目名称[/td][td]采购标的[/td][td]数量(单位)[/td][td]技术规格、参数及要求[/td][td]品目预算(元)[/td][td]最高限价(元)[/td][/tr][tr][td]1-1[/td][td]诊断用生物试剂盒[/td][td]乙型肝炎病毒表面抗原等项目诊断试剂盒、校准品及相关耗材[/td][td]1(批)[/td][td]详见采购文件[/td][td]2,000,000.00[/td][td]2,000,000.00[/td][/tr][/table]本合同包不接受联合体投标合同履行期限:2023-04-01 00:00:00 至2024-03-31 00:00:00(具体服务起止日期可随合同签订时间相应顺延)[b][font=inherit]二、申请人的资格要求:[/font][/b]1.满足《中华人民共和国政府采购法》第二十二条规定 2.落实政府采购政策需满足的资格要求:合同包1(乙型肝炎病毒表面抗原等项目诊断试剂盒、校准品及相关耗材)落实政府采购政策需满足的资格要求如下:2.1?《节能产品政府采购实施意见》(财库[2004]185号);2.2?《环境标志产品政府采购实施的意见》(财库[2006]90号);2.3?《国务院办公厅关于建立政府强制采购节能产品制度的通知》(国办发〔2007〕51号);2.4?《财政部?司法部关于政府采购支持监狱企业发展有关问题的通知》(财库〔2014〕68号);2.5?《财政部、民政部、中国残疾人联合会关于促进残疾人就业政府采购政策的通知》财库〔2017〕141号;2.6?陕西省财政厅关于印发《陕西省中小企业政府采购信用融资办法》(陕财办采〔2018〕23号);2.7?《财政部?发展改革委?生态环境部?市场监管总局关于调整优化节能产品、环境标志产品政府采购执行机制的通知》(财库〔2019〕9号);2.8?财政部、工业和信息化部关于印发《政府采购促进中小企业发展管理办法》的通知(财库〔2020〕46号);2.9?《关于运用政府采购政策支持乡村产业振兴的通知》(财库〔2021〕19号);2.10?《关于进一步加大政府采购支持中小企业力度的通知》(财库〔2022〕19号);2.11?本项目为非专门面向中小企业的采购;2.12?其他需要落实的政府采购政策。3.本项目的特定资格要求:合同包1(乙型肝炎病毒表面抗原等项目诊断试剂盒、校准品及相关耗材)特定资格要求如下:3.1具有独立承担民事责任能力的法人、其他组织或自然人,提供合法有效的统一社会信用代码营业执照(事业单位提供事业单位法人证书,自然人应提供身份证明);3.2法定代表人直接参加投标的,须提供法定代表人身份证明(附法人身份证复印件,法人身份证原件备查);法定代表人授权代表参加投标的,须提供法定代表人授权委托书(附法人及被授权人身份证复印件,被授权人身份证原件备查) 3.3社会保障资金缴纳证明:提供2022年1月1日以来至开标前任意一个月的社会保障资金缴存单据或社保机构开具的社会保险参保缴费情况证明。依法不需要缴纳社会保障资金的供应商应提供相关文件证明;3.4税收缴纳证明:提供2022年1月1日以来至开标前任意一个月的纳税证明或完税证明(提供增值税、企业所得税至少一种),纳税证明或完税证明上应有代收机构或税务机关的公章或业务专用章。依法免税的供应商应提供相关文件证明;3.5财务状况证明:提供2022年1月1日以来至开标前任意一个月的财务报表(至少包括资产负债表、现金流量表和利润表)或具有财务审计资质的单位出具的2020年度或2021年度财务审计报告或开标日前三个月内基本存款账户银行出具的资信证明(附基本存款账户开户许可证或加盖银行章的基本存款账户信息));2022年以后新成立企业提供成立之日至开标前任意一个月的财务报表(至少包括资产负债表、现金流量表和利润表)或开标日前三个月内基本存款账户银行出具的资信证明(附基本存款账户开户许可证或加盖银行章的基本存款账户信息);??3.6提供履行合同所必需的设备和专业技术能力的书面声明;3.7?提供参加政府采购活动前三年内在经营活动中没有重大违法记录的书面声明。(提供书面声明,加盖供应商公章);3.8国产货物:供应商为制造厂家须提供营业执照、医疗器械生产企业许可证、医疗器械注册证及附件;供应商为经销商的须提供营业执照、医疗器械经营许可证,制造厂家营业执照、医疗器械生产许可证、医疗器械注册证及附件(试剂类可提供有医疗器械注册证,耗材类可提供注册证或备案证明);3.9进口货物:供应商为制造厂家须提供医疗器械注册证(“进”字号注册证)及附件(附页)并能证明其为货物生产厂家的资料(包含但不限于:产品宣传册、技术白皮书、检验报告等)其余特定资格要求的资料均不做要求;供应商为经销商的须提供营业执照、医疗器械经营许可证、所投产品医疗器械注册证(“进”字号注册证)及附件(附页),并提供能证明货物完整授权链条的资料(包括但不限于:厂家产品授权委托书、中国或陕西总代提供的授权委托书等);3.10供应商未被列入“信用中国”网站(www.creditchina.gov.cn)以下情形之一:①记录失信被执行人;②重大税收违法案件当事人名单。同时,在中国政府采购网(www.ccgp.gov.cn)“政府采购严重违法失信行为信息记录”中查询没有处于禁止参加政府采购活动的记录名单;3.11单位负责人为同一人或者存在直接控股、管理关系的不同供应商,不得参加同一合同项下的政府采购活动;3.12本项目不接受联合体投标。[b][font=inherit]三、获取招标文件[/font][/b]时间: 2023年03月07日 至 2023年03月13日 ,每天上午 00:00:00 至 12:00:00 ,下午 12:00:00 至 23:59:59 (北京时间)途径:全国公共资源交易平台(陕西省西安市)网站〖首页〉电子交易平台〉陕西政府采购交易系统〉企业端〗方式:在线获取售价: 0元[b][font=inherit]四、提交投标文件截止时间、开标时间和地点[/font][/b]时间: 2023年03月28日 09时30分00秒 (北京时间)提交投标文件地点:【全国公共资源交易平台(陕西省西安市)】网站〖首页〉电子交易平台〉陕西政府采购交易系统〉企业端〗在线提交开标地点:【全国公共资源交易平台(陕西省西安市)】网站〖首页〉不见面开标〗[b][font=inherit]五、公告期限[/font][/b]自本公告发布之日起5个工作日。[b][font=inherit]六、其他补充事宜[/font][/b][font=inherit][color=#000000][font=inherit]1、获取方式:打开【全国公共资源交易平台(陕西省[/font][/color][color=#000000][font=inherit][/font][font=inherit]西安市)】网站(简称西安市公共资源交易平台,官网地址:[/font][font=inherit]http://sxggzyjy.xa.gov.cn/[/font][font=inherit]),从〖首页[/font][font=inherit][/font][font=inherit]〉电子交易平台[/font][font=inherit][/font][font=inherit]〉陕西政府采购交易系统[/font][font=inherit][/font][font=inherit]〉企业端〗登录后,首先在〖招 标公告[/font][font=inherit]/[/font][font=inherit]出让公告〗模块中预览全部可供参与的项目,然后选择有意向的项目点击〖我要投 标〗,成功后切换到〖我的项目〗模块,依次点选〖项目流程[/font][font=inherit][/font][font=inherit]〉项目管理[/font][font=inherit][/font][font=inherit]〉交易文件下载〗免费获取本项目电子招标文件([/font][font=inherit]*.SXSZF[/font][font=inherit])。[/font][font=inherit][/font][/color][/font][font=inherit][color=#000000][font=inherit]2、供应商初次使用电子交易平台时[/font][/color][color=#000000][font=inherit],[/font][font=inherit]请先阅读【全国公共资源交易平台[/font][font=inherit]([/font][font=inherit]陕西省[/font][font=inherit][/font][font=inherit]西安市[/font][font=inherit])[/font][font=inherit]】 [/font][font=inherit](http://sxggzyjy.xa.gov. cn/)[/font][font=inherit]网站〖首页〉服务指南〉下载专区〗中的《西安市市级单位电子化政府采购项 目投标指南》[/font][font=inherit],[/font][font=inherit]并按要求完成诚信入库登记 、[/font][font=inherit]CA[/font][font=inherit]认证及企业信息绑定 。[/font][font=inherit][/font][/color][/font][font=inherit][color=#000000][font=inherit]3、办理 [/font][/color][color=#000000][font=inherit]CA[/font][font=inherit]认证[/font][font=inherit]:[/font][font=inherit]电子交易平台现已接入陕西 [/font][font=inherit]CA[/font][font=inherit]、深圳 [/font][font=inherit]CA[/font][font=inherit]、西部 [/font][font=inherit]CA[/font][font=inherit]、北京 [/font][font=inherit]CA[/font][font=inherit]四家数字证书公司[/font][font=inherit],[/font][font=inherit]各供应商在交易过程中登录系统、加密[/font][font=inherit]/[/font][font=inherit]解密投标文件、文件签章等均可使用上述四家[/font][font=inherit]CA[/font][font=inherit]公司签发的数字证书。办理须知及所需资料详见[/font][font=inherit]:http://www.sxggzyjy.cn/fwzn/004003/20220701/6972feo2-f996-4928-951e-545dab02e53c.htm1[/font] [font=inherit][/font][/color][/font][font=inherit][color=#000000][font=inherit]4、供应商于文件发售时间内登录全国公共资源交易平台(陕西省[/font][/color][color=#000000][font=inherit][/font][font=inherit]西安市)系统([/font][font=inherit]http://sxggzyjy.xa.gov.cn/[/font][font=inherit]),选择本项目点击[/font][font=inherit]“[/font][font=inherit]我要投标[/font][font=inherit]”[/font][font=inherit],参与投标活动;网上报名成功后,下载电子招标文件:投标人应登录西安市公共资源交易平台〖首页〉电子交易平台〉陕西政府采购交易系统〉企业端〗,在〖招标公告[/font][font=inherit]/[/font][font=inherit]出让公告〗模块中预览全部可供参与的项目,然后选择有意向的项目点击〖我要投标〗,成功后切换到〖我的项目〗模块,依次点选〖项目流程〉项目管理〉交易文件下载〗免费获取本项目电子招标文件([/font][font=inherit]SXSZF[/font][font=inherit])。请务必在采购文件获取期限内及时下载电子招标文件并做好备份,逾期下载通道将关闭,未及时下载招标文件将会影响后续开评标活动。[/font][font=inherit][/font][/color][/font][font=inherit][color=#000000][font=inherit]5、制作电子投标文件([/font][/color][color=#000000][font=inherit]*.SXSTF[/font][font=inherit])需要使用专用制作工具。软件下载及操作说明详见西安市公共资源交易平台〖首页[/font][font=inherit][/font][font=inherit]〉服务指南[/font][font=inherit][/font][font=inherit]〉下载专区〗中的《政府采购项目投 标文件制作软件及操作手册》。[/font][font=inherit][/font][/color][/font][font=inherit][color=#000000][font=inherit]6、提交投标文件截止时间前,供应商应随时留意【陕西省政府采购网】、【全国公共资源交易平台(陕西省[/font][/color][color=#000000][font=inherit][/font][font=inherit]西安市)】上可能发布的变更公告。若变更公告中明确注明本项目提供有变更文件的,供应商应登录企业端后,从〖项目流程[/font][font=inherit][/font][font=inherit]〉项目管理[/font][font=inherit][/font][font=inherit]〉答疑文件下载〗获取更新后的电子招标文件([/font][font=inherit]*.SXSCF[/font][font=inherit]),使用旧版电子招标文件制作的电子投标文件([/font][font=inherit]*.SXSTF[/font][font=inherit]),系统将拒绝接收。[/font][font=inherit][/font][/color][/font][font=inherit][color=#000000][font=inherit]7、本项目采用[/font][/color][color=#000000][font=inherit]“[/font][font=inherit]不见面开标[/font][font=inherit]”[/font][font=inherit]形式,供应商可登录全国公共资源交易平台[/font][font=inherit]([/font][font=inherit]陕西省[/font][font=inherit][/font][font=inherit]西安市[/font][font=inherit])[/font][font=inherit]网站〖首页〉不见面开标〗系统,在线参加开标过程。操作手册详见 〖首页〉服务指 南〉下载专区〗中的 《西安公共资源交易不见面开标大厅供应 商操作手册》。[/font][font=inherit][/font][/color][/font][font=inherit][color=#000000][font=inherit]8、按照陕西省财政厅 《关于政府采购供应商注册登记有关事项的通知》中的要求,供应商应通过陕西省政府采购网 [/font][/color][color=#000000][font=inherit](http://www.ccgp-shaanxi.gov.cn/)[/font][font=inherit]注册登记,加入陕西省政府采购供应商库 。[/font][font=inherit][/font][/color][/font][font=inherit][color=#000000][font=inherit]9、其他事项见本项目招标文件。[/font][/color][color=#000000][font=inherit][/font][/color][/font][b][font=inherit]七、对本次招标提出询问,请按以下方式联系。[/font]1.采购人信息[/b]名称:西安市第五医院地址:西安市莲湖区西关正街112号联系方式:029-88621331[b]2.采购代理机构信息[/b]名称:陕西东欣世源招标咨询有限公司地址:陕西省西安市市辖区陕西省西安市高新区丈八街办科技三路57号融城云谷5栋1单元803号联系方式:余工、张工13609197871[b]3.项目联系方式[/b]项目联系人:余工、张工电话:13609197871

最近“问题疫苗”闹的大家人心惶惶, 据说乡镇就乱点,在城市里正规医院里打的都是正规的。娃娃6岁之前都打的一类的疫苗,不必过分恐慌,除非你掏钱打过二类疫苗。关于这次“问题疫苗”,二类疫苗本身没问题,就是经销商中间储存环节没有冷链运输和保存设施,出不出问题就难说了~ 其实有12中疫苗没有第一类疫苗,全部为第二类疫苗:冻干人用狂犬病疫苗(Vero细胞)、重组乙型肝炎疫苗(CHO细胞、汉逊酵母)等。 但是恐慌是一回事,事情的解决是另一回事啊! 目前各地的回复是这样的: 广东卫计委:未向任何无资质的企业或个人采购任何疫苗,至今采购的每一支疫苗都有批签发合格证; 上海卫计委:此案中的非法疫苗没有涉及到上海; 江苏省疾控中心:山东问题疫苗暂未涉及江苏; 云南疾控中心:自2010年至今,未采购山东问题疫苗; 吉林省卫计委:未发现问题疫苗,疫苗均严格冷藏使用; 北京市卫计委:纳入免疫规划用一类、二类疫苗均来自有资质疫苗生产(经营)企业; 四川省疾控中心:未采购无资质疫苗; 浙江省疾控中心:还未发现本案中的非法疫苗; 湖南省疾控中心:省内由疾控系统主渠道供应的二类疫苗占80%左右,剩下20%由社会销售;主渠道供应的疫苗可以保证质量和效果; 贵州省卫计委:未向任何无资质的企业或个人采购任何疫苗; 既然这么多省都没有问题,那“问题疫苗”如何销往20几个省市?
新华社东京3月21日电 (记者蓝建中)日本神户大学日前发表公报称,该校研究人员成功开发出一种新型口服丙肝疫苗。这种口服疫苗价格低廉,还可常温保存,与传统疗法配合使用,有望提高丙肝治愈率。 早前疫苗只发挥预防疾病作用,但随着免疫学研究的发展,人们发现了疫苗还有治疗作用,一些疫苗也被称为治疗性疫苗。 神户大学教授堀田博领导的研究小组针对丙肝病毒中特有的NS3蛋白质,利用酸奶中常见的双歧杆菌进行基因重组,开发出了新型口服丙肝疫苗,在动物实验中成功激活了针对丙肝病毒的细胞免疫性。 研究人员让实验鼠每隔一天服用一次这种疫苗,持续4周后,实验鼠肠道就开始产生具有免疫作用的淋巴细胞,它能与丙肝病毒中的NS3蛋白质发生反应,从而提高对丙肝病毒的免疫力。 慢性丙型肝炎患者中,有30%即使接受标准疗法治疗仍不理想。此前研究人员在开发治疗药物时主要以遏制病毒增殖为目标,新研究的思路则是通过提高患者自身的免疫力来提高治愈率。 研究小组将继续完善动物实验和临床研究,希望7年后能投入临床使用。相关研究成果将于近期刊登在荷兰《疫苗》杂志网络版上。
由礼来公司(Eli Lilly)牵头组建的独立的、非赢利性团体组织——亚洲癌症研究组(ACRG)和默克(Merck)公司(众所周知的美国和加拿大以外的MSD)以及辉瑞制药有限公司(Pfizer Inc.)联合全世界最大的基因组研究机构BGI共同宣布发表于《自然-遗传学》(Nature Genetics)杂志的研究结果:有关复发性乙型肝炎病毒(HBV)在肝细胞癌(HCC)中整合的一项全基因组研究。该项研究为同类当中的首次研究,从这项研究得出的结果或许对帮助提高肝细胞癌(HCC,全球范围内最常见的肝癌类型)诊断和治疗可以提供重要见解和看法。论文第一作者、新加坡国立大学和香港大学(HKU)名誉副教授Ken Sung博士说:“这项研究为乙型肝炎病毒(HBV)整合机制提出了新的见解和看法,这将推动肝癌和临床预后结局的影响。我们也期望可以通过进一步深入的研究调查来提高肝细胞癌(HCC)的诊断和治疗。”乙型肝炎病毒(HBV)整合被认为是肝细胞癌(HCC)发病的主要原因之一,研究人员已经证实乙型肝炎病毒(HBV)的DNA可以整合到宿主基因组中去,这样就会诱导宿主的染色体不稳定(绝大多数人类癌症的典型特征之一)或者改变内源性基因的表达及其功能的正常发挥。之前也曾有乙型肝炎病毒整合到HCC基因组的相关研究,但由于技术障碍以及样本量相对较小而使研究一直受到限制。在该项研究当中,ACRG,BGI和其他合作者对一个大样本队列的患有HCC的中国患者进行了全基因组测序,以期能通过此来描述全基因组整合模式,并确定乙型肝炎病毒整合的发生率。通过测序和分析,研究人员发现乙型肝炎病毒(HBV)整合是肝肿瘤事件中一个很普遍的现象,并且这种整合现象较邻近的正常肝组织(30.7%)来看,在肿瘤中的整合更常见(86.4%)。除外之前已经报道的TERT和MLL4基因,研究人员还发现另外三个新的基因(CCNE1,SENP5和ROCK1)与再发的乙型肝炎病毒的整合有关,而在这五个基因当中,每一个均在癌症形成以及进展过程中起很重要的作用。BGI负责该项目的主要研究者Hancheng Zheng表示:“对于(全球范围内)致力于更好地理解HCC中乙型肝炎病毒整合研究的科研人员/科研机构来讲,这项研究激起了他们的极大兴趣。也正是基于这些研究成果,我们可以更好地探讨乙型肝炎病毒整合的详细分子机制,以及整合带来的临床预后影响,这也必将推动发现并形成未来更好的肝癌治疗方法。”研究人员还注意到乙型肝炎病毒整合事件(复发)的数量与肿瘤大小、以及血清HBsAg和α-甲胎蛋白水平呈正相关。与那些肿瘤中较高数量的乙型肝炎病毒整合(n3)相比,肿瘤中没有检测到或低数量(n3)检测到乙型肝炎病毒整合的患者生存时间更长,这也表明乙型肝炎病毒整合事件是HCC患者的一个不良的预后指标。香港大学名誉教授、NUS和IMCB头颈肿瘤以及上海罗氏公司兼职教授John Luk说:“深入理解HCC中的再发性乙型肝炎病毒插入机制,有助于科学研究团体/机构明确肝癌的新的分子靶点,而这也正是有效治疗肝癌的瓶颈所在。”研究人员表示HBV整合所表现出的一些特点可能有助于病毒控制宿主肿瘤的某些特定基因。他们发现,HBV整合位点通常接近或插入整合的基因内,这可能正是HBV控制某些癌基因或肿瘤抑制基因表达的分子机制。研究观察到超过40%的整合在1,800[/col
长期以来,科学家们一直认为,通过加速人体免疫系统的运作,机体自身天然防线能够获得额外的力量来攻击肿瘤及其它疾病。但是,几十年过去了,很多颇具前景的潜在“免疫调节剂”、“免疫刺激剂”以及“治疗性疫苗”的临床试验均以失败告终。现在,有证据表明,治疗性疫苗实际上是有疗效的。传统疫苗是提供持久的保护以防止感染疾病,而治疗性医疗是用来对抗现有的疾病的。2010年4月,美国食品与药品管理局(FDA)批准了首个治疗性疫苗——Dendreon的Provenge。Provenge(sipuleucel-T)在临床试验中显示,对于某种特定类型的转移性前列腺癌男性患者,可以延长大约4个月的生命。这种疫苗可以激发免疫应答,对抗存在于大多数前列腺癌细胞中的一个特定的抗原或识别分子。Provenge所激发的不仅仅是患者的免疫系统,还有投资者、临床医生还有被免疫加强治疗相对较少的副作用和较高的收益所鼓励的大大小小的公司。Provenge一个疗程的费用为93000万美元。对分子生物学和免疫学的不断深入的认识也激发了新的希望,一些机制不明、甚至在十来年前无法获得的候选疫苗纷纷出现。现在,FierceVaccines选取了正在临床研究阶段的颇受关注的10个治疗性疫苗。通常,治疗癌症的疫苗会得到最多的关注,这部分是因为治疗性疫苗的耐受性很好,与传统化疗药物的毒副作用形成了鲜明的对比。而免疫刺激这一想法最后被证明在肿瘤学上是有限的,这也刺激了研究人员将治疗性疫苗的适应症从原来的传染性疾病如艾滋病和肝炎扩展到癌症。开发治疗性疫苗的关键问题之一是训练免疫系统如何识别和摧毁“坏”细胞,这样疫苗就可以帮助机体对抗一种类型的肿瘤或者可以个性化治疗的疾病。因此,我们的名单中包括了一些针对癌症以外疾病的前沿治疗性疫苗。IICT- 107 - 胶质母细胞瘤VGX- 3100 - 宫颈癌MAGE - A3 - 皮肤癌,肺癌NeuVax - 乳腺癌AE37 - 乳腺癌NexVax2 - 乳糜泻ADXS- HPV - 宫颈癌,头颈癌CRS- 207 - 胰腺癌PEV7 - 复发性外阴阴道念珠菌病GI- 4000 - 胰腺癌疫苗名称:ICT-107开发公司:ImmunoCellular Therapeutics治疗疾病:胶质母细胞瘤http://www.bioon.com/z/UploadFiles_1874/201111/2011112813093132.gif就像很多在开发阶段的治疗性疫苗一样,ICT-107利用了树突细胞在免疫应答中的作用。这种类型的细胞显示或者“呈现”免疫系统的另一种行为:抗原识别出外来的入侵者,比如细菌和病毒,或者人体自身产生的麻烦比如肿瘤。它们标记出这些必须被摧毁的东西。ICT-107带有多个与胶质母细胞瘤相关的抗原,胶质母细胞瘤是一种快速转移和致命的脑癌。早期的临床试验有16名新诊断为胶质母细胞瘤的患者参加,结果显示,3年总体生存率为55%,而标准治疗方法(SOC)的3年总体生存率是16%。最近,ImmunoCellular Therapeutics开始了这个候选疫苗的临床II期研究。在I期临床试验中,患者在标准的手术、放疗和化疗外,接受了3剂ICT-107.数据显示,接受了该候选疫苗的初诊患者有38% 3年后肿瘤没有复发。在这些患者中,有19%超过4年没有复发。之前,公司报告,研究结果显示,患者使用该疫苗后的2年生存率为80.2%,这一数据明显优于仅使用标准治疗方法的患者,后者的2年生存率的中位值仅为26.5%。没有严重的不良反应报告,轻微的副作用限于疲劳、皮疹和瘙痒感。树突细胞已经是最近的新闻了:2011年诺贝尔生理学和医学奖授予了Ralph M. Steinman,因为他发现了树突细胞在适应性免疫系统中的关键作用。虽然树突细胞早在19世纪就被提到,但是直到1973年才被研究人员命名。Steinman是命名树突细胞的研究人员之一。对树突细胞理解的不断深入是推动治疗性疫苗从概念到实践的重要因素。
短短一个月之内,乙肝疫苗事件不断发酵,将生产公司和监管部门推向风口浪尖。被列入国家计划免疫超过20年的乙肝疫苗产业直面调整重构。从1989年引入全球制药巨头默沙东乙肝疫苗技术,再将销售渠道铺遍国内31个省区,深圳康泰生物用了24年;然而,从12月初爆发乙肝疫苗“致死门”事件,再到全国27个省区全面叫停康泰生物乙肝疫苗,前后不过20天。此后,原本与康泰生物呈鼎立之势的大连汉信(曾为已退市公司S*ST云大的控股子公司)及国药集团旗下的天坛生物也先后卷入乙肝疫苗事件,累计4名婴幼儿在接种上述两公司乙肝疫苗后死亡。至此,全国范围内的乙肝疫苗巨头悉数“落马”,被列入国家计划免疫超过20年,早已踏入“红海”市场的乙肝疫苗产业完全失控。失控的不仅仅是康泰生物及乙肝疫苗,还有年均1600万名新生儿及3200万父母。在此背景下,国产乙肝疫苗产业似有重蹈三鹿事件覆辙的迹象,整个行业遭受了前所未有的信任危机。乙肝疫苗致死门的真相到底是什么?谁才是惨剧的真正凶手?证券时报记者日前探访位于风暴中心的康泰生物。平静深圳南山科技园科发路6号,这是康泰生物的总部驻地。在康泰生物周围,云集着长城电脑(000066,股吧)、深桑达A、爱默森等多家知名上市公司或外资公司,相比之下,康泰生物看似不起眼。然而就在十几天前,这家公司还控制着国内近三成的乙肝疫苗供应量。一组数据显示,去年国内共签发6800万瓶各种规格的乙肝疫苗产品,其中康泰生物产品近2500万瓶,约占四成比例。其余市场则被大连汉信、天坛生物、华北制药(600812,股吧)等公司瓜分。今年前10个月,康泰生物市场份额下滑至26%,但仍然不容小觑。与国内品牌相比,葛兰素史克“安在时”等外资乙肝疫苗在中国市场份额并不大。包括康泰生物在内的中国企业,均拒绝承认乙肝疫苗存在质量问题、因而导致全国多名婴儿在接种后离奇死亡。不过,康泰生物、天坛生物等公司的澄清并未消除公众疑虑,国家食药总局直接下令在全国范围内停用康泰生物乙肝疫苗,这等于在需求端彻底堵死了康泰生物。作为乙肝疫苗事件的主角,康泰生物近期如坐针毡,据康泰生物一位内部人士向记者透露,公司已下达封口令,在死亡婴幼儿尸检报告及食药总局的权威报告发布之前,严禁任何人公开接受媒体采访。记者日前赴康泰生物总部探访,正值午饭时间,多名佩戴康泰生物工牌的人士进进出出。当记者试图混入员工队伍中进入康泰生物时,却被多名门卫拦下。门卫告诉记者,近期常有各色人等在康泰生物门前转悠,但根据公司要求,不允许任何未经预约的陌生人进入厂区。记者随后致电康泰生物要求预约采访,公司方面则回应称,康泰生物正在进行自查,暂不接受采访,也不方便透露相关信息。据记者观察,康泰生物厂区内部并无明显异常,尽管门卫人数较多,但并未达到如重庆啤酒(600132,股吧)2011年乙肝疫苗揭盲后股价暴跌期间,整个公司严阵以待的状态。至少从表面上看,康泰生物并不像是正在遭受全国公众的拷问,显得较为平静。然而,一旦食药总局认定乙肝疫苗与死亡婴幼儿存在直接关联,则康泰生物及其竞争对手或有倾覆之灾。神秘在康泰生物身上,一直贴着类似于“国退民进”的标签,而康泰生物的现任掌门人杜伟民,在医药圈内形象甚为低调,甚至可以说是神秘。由于中国是全球知名的乙肝大国,乙肝携带者接近1亿人,加上乙肝病人及乙肝携带者在升学、就业、婚恋方面曾经遭受的种种歧视,中国内地人对乙肝有着天然的恐惧,这与欧美以及香港社会有明显区别。另外,目前医学上尚无法根治乙肝且其传染性较大,因此国内早在1992年就将乙肝疫苗列入国家计划免疫,即新生婴幼儿可免费接种乙肝疫苗,这就是所谓的一类疫苗。按照一般的操作标准,新生儿在出生后24个小时之内及1个月、6个月之后分别接种1支乙肝疫苗。在医药央企“5进3”之前,国内乙肝疫苗主导权掌握在中国生物技术集团旗下六大生物制品研究所及天坛生物手中。2009年,国务院启动医药央企“5进3”计划,中国生物技术集团及上海医工院陆续被并入国药集团,中国生物技术集团旗下的研究所也进行了公司改制。此后,上述改制成国企的研究所未能守住领地,乙肝疫苗份额日趋下降。深圳民企康泰生物却一路崛起,高峰时期蚕食了国内乙肝疫苗市场半壁江山。据了解,在很多县级公立医院,只供应康泰生物乙肝疫苗,其他公司的产品无法进入。事实上,在医药央企“5进3”之前,康泰生物已经开始高速增长,2008年时营收直逼亿元大关。资料显示,康泰生物1992年成立后便致力于资本运作,2005年向证监会申请上市且通过审查,不过公司上市之行莫名中止。此后上实医药、交大昂立(600530,股吧)等医药资本先后退出,康泰生物也不再启动上市计划。2009年,康泰生物实施重组,杜伟民通过深圳市瑞源达投资有限公司正式进入康泰生物。深圳市场监督管理局网站资料显示,目前康泰生物最大股东系新疆瑞源达股权投资有限公司,持股64.3%,股东多达37位,其中包括7家机构股东。杜伟民身兼康泰生物董事长及总经理,尽管他控制着国内最大的乙肝疫苗生产基地,且准备在深圳投资8.5亿元建立亚洲最大的疫苗生产单体建筑,但在业内并不属于巨鳄型人物,公开资料极少。记者从华北一家生产乙肝疫苗的公司了解到,该公司平素与杜伟民并无过多的来往,对他不甚了解。近期不少人怒斥杜伟民是“惯犯”,指出其曾控制的江苏延申一款狂犬病疫苗涉嫌造假,被当时的药监局勒令停业整顿。当然,在食药总局最终尸检报告出来之前,无法证实康泰生物及其他公司乙肝疫苗与婴幼儿死亡存在直接关联。而一个不容忽视的细节是,即便目前全民质疑并攻讦康泰生物及杜伟民,但杜伟民始终尚未出面澄清,这与农夫山泉掌门人钟睒睒、恒大地产董事局主席许家印等人在公司面对质疑时的强硬回击对比鲜明。凶手食药总局相关资料显示,针对于康泰生物乙肝疫苗事件的尸检已于本月下旬开始。按照正常流程,食药总局首先必须查清婴幼儿的真实死因,然后再确定死因是否与康泰生物疫苗有关,整个过程可能需要30个工作日。理论上,只要严格遵循尸检流程,在现代医学条件下,不难查清背后的真实原因。进行尸检的同时,卫计委及食药总局也联合召开了发布会,旨在消减公众有关乙肝疫苗涉嫌致死的诸多质疑。该发布会披露了一项数据,即从2000年至今年12月份,国内共上报了188例接种乙肝疫苗后死亡病例。中国疾控中心指出,这188例死亡案例中,乙肝疫苗及接种过程均无问题,其中有18例属于疫苗异常反应,但未超出世卫组织的规定范围。参照上述比例,此次涉事的康泰生物、大连汉信等公司乙肝疫苗可能也不存在质量问题。但只要有一例病例证明婴幼儿死亡确系乙肝疫苗所致,接下来的行业风暴显然可以预计。“如果最终确定乙肝疫苗便是罪魁祸首,康泰生物等公司固然要付出沉重代价,但相关的机构及制度也难辞其咎。”深圳一位医药行业研究员对记者表示,乙肝疫苗本质上也是药物,而药物必然会有正常的不良反应,但不至于因不良反应而直接致死,除非质量确实有问题。上述研究员表示,不管结果如何,乙肝疫苗整条产业链都应该反思。据了解,康泰生物乙肝疫苗在某些省区近乎垄断,天坛生物、华北制药的乙肝疫苗无法分羹,客观上造成了单一来源采购。而在华东某些省区,大连汉信则成为了单一来源采购。所谓单一来源采购,是指向特定一个供应商采购的政府采购方式。但在乙肝疫苗领域,国内并存酵母乙肝疫苗、重组(汉逊酵母)乙肝疫苗及基因工程(CHO)疫苗,三者互为补充,至少有10家公司具备疫苗生产能力,在细分领域还形成重叠。换言之,省级单位在统一采购乙肝疫苗时,运用单一来源采购方式的合理性值得商榷。目前业内对这种采购方式疑虑重重,特别是康泰生物及杜伟民一贯被视为“能量很大”,单一来源采购难以自证清白。除了采购制度外,医疗机构在为婴幼儿及成年人接种乙肝疫苗时,往往并未提供备选方案,或未征询监护人及当事人的意见。如北京大学深圳医院妇产科工作人员告诉记者,目前该医院乙肝疫苗全部换成了进口疫苗,但当记者问及可否挑选乙肝疫苗时,该工作人员却并未给出明确答复,深圳另外几家三甲医院也存在类似的情况。事实上,囿于专业知识所限及一类疫苗的免费属性,大多数人通常不会在意接种疫苗的品种及生产方,医患之间客观上缺乏必要的沟通。重构康凯生物乙肝疫苗事件爆发后,天坛生物与华北制药乙肝疫苗一度被相关省区作为替代品,资本市场也闻风而动,认为瓜分康泰生物市场份额的机会已来临。不过,天坛生物、大连汉信等随即卷入乙肝疫苗事件,令各路资本叫苦不迭。那么,乙肝疫苗究竟有多大市场呢?记者了解到,乙肝疫苗主要市场来自于新生儿,且发改委对疫苗产品一贯实施控价策略,目前的一类乙肝疫苗的出厂价约为5元/支。在经过省级采购及逐级分配之后,每支乙肝疫苗在医疗终端的售价可能会翻倍。以全国年均出生1600万新生儿,每个新生儿接种3支乙肝疫苗计算,乙肝疫苗年容量约为5亿元,再加上二类疫苗及进口疫苗的销售规模,整个乙肝疫苗的规模约为7~8亿元,仅相当于天坛生物去年预防制品营收规模。对于大多数人而言,乙肝疫苗属于一次性用药。由此可见,乙肝疫苗市场规模相对有限,很多乙肝疫苗企业唯有依靠抢占市场取得规模效应,规模越大、边际效应反而越高。当然,此处的乙肝疫苗仅指预防性乙肝疫苗,与治疗性乙肝疫苗的规模不能同日而语。在大连汉信、天坛生物卷入乙肝疫苗事件之前,即便康
乙肝疫苗暴露出来的问题,引发了全民对疫苗的大震动、大恐慌。会否是疫苗行业的一场灾难性的大地震?
天然疫苗和人工疫苗 本综述概述了细胞和抗体介导的免疫保护及免疫记忆的基本机制,以此为基础,用抗原在免疫保护中的作用来评估疫苗研究的成功和困难,人类在出生后12~48个月期间,来自母乳和血清的获得性抗体可避免儿童期常见病和其它感染性疾病.基于此事实,形成了这样一种概念:获得性抗体骤减了婴幼儿的各种感染,所以使它们变成了有效的疫苗.如果没有这种被动保护条件下的"天然疫苗",除非婴幼儿在早期有效接种了各种疫苗且免疫系统发育成熟,否则会感染很严重的急性儿科疾病。尽管接种疫苗有可能在预防常见儿科急症上有效,但对于一些看来轻症的儿科感染象胃肠道感染和呼吸道感染,接种的疫苗好像无效,这种看似轻症的感染最终可能激发免疫病理性疾病,哺乳习惯的改变可导致机体和感染之间稳态的破坏,而且从保健水平看,可导致疾病模式的改变,包括不断频发的某种自身免疫病和恶性病. 介绍: 在过去的100年间,对免疫记忆的特性已进行广泛研究,不仅有免疫学家还有临床大夫及大众健康视角。免疫记忆的功能是研究保护性疫苗的基础,有些疫苗对抵御儿童疾病和天花已证明很成功,世界范围内接种了预防天花的病毒疫苗,使天花已经绝迹,然而,仍无有效的疫苗来防御结核、麻疹和寄生虫病(如疟疾、利什曼病和血吸虫病),而且还无疫苗可预防人类免疫缺陷病毒(HIV),登革病毒,呼吸道合胞病毒,EB病毒,巨细胞病毒、轮状病毒、单纯疱疹病毒和乳头状瘤病毒等的感染及御防各种肿瘤。另外,一些抗病毒疫苗,象抗麻疹病毒和腮腺炎病毒的疫苗,一旦病毒入侵,远不能提供完全的保护,这些成功和失败证明我们对免疫记忆的本质还没完全理解,这篇综述提出了以下问题:人工疫苗是通过天然疫苗预测的吗?疫苗的生理平衡是什么?对于免疫性和疫苗的哪些方面是我们未知的? 免疫保护的机制 抗感染的主要机制是非特异性机制(干扰素、补体、天然抗体、自然杀伤细胞、活化的吞噬细胞),还有一些其它的机制,这些非特异防御机制在宿主防御中起重要作用(95%),例如,干扰素受体缺失会使小鼠对病毒感染的敏感性提高好几倍,特异性免疫从系统发生上看是一个相当新的防御系统,是宿主和感染源共同进化的结果。 `抗体和细胞是免疫系统的两部分,它们担负着以下重要任务,B细胞表面的免疫球蛋白受体和分泌的抗体直接识别复合折叠蛋白或糖抗原,保护性抗体通过与毒素结合或促进病原体的溶解使之失去活性,IgM和IgG对血液和淋巴系统中的抗原感染有免疫保护作用,IgA在粘膜防御中起保护作用,IgE激活皮肤和粘膜表面的肥大细胞和嗜碱性粒细胞。而T细胞识别的是由MHC分子递呈在细胞表面的小肽,细胞毒性CD8+T细胞特异性识别细胞自身合成的和MHCⅠ类分子递呈的抗原肽,此路经不仅包括自身肽,还有病毒、胞内寄生菌和肿瘤抗原。吞噬性抗原是在吞噬溶酶体中加工处理后由MHCⅡ类分子递呈,滤泡树突状细胞(DC)将抗原(自身感染的或含有感染的外源抗原或衰变的自身抗原)运送到器官的淋巴组织,因而DC通常在诱导T细胞介导的细胞免疫应答中直接发挥作用。T细胞主动迁移至外周固有组织,T细胞可通过直接接触或通过特异性免疫介质(如干扰素或肿瘤坏死因子)的释放来发挥作用,也可通过募集和活化巨噬细胞非特异性发挥作用。导致急性致死性感染的细胞毒性病毒或细菌一般可由可溶性扩散因子包括T细胞依赖性细胞因子(如γ干扰素和肿瘤坏死因子)和特异性中和抗体,使其得到有效的控制,非细胞毒性病原体通常不直接引起细胞或组织的损害。因而即使它们持续存在,也不会致病,,这种情况下免疫防御是由引起炎症和组织损伤的穿孔素、细胞毒素和释放细胞因子的T细胞介导的。既然免疫系统不能尽早地区分感染是否致细胞病变,那也不能从真正意义上预见它对宿主有益的最终结果,它只是对抗原产生的应答反应。 因而,免疫保护是适度防止各种致细胞损伤的感染和避免过度免疫应答导致组织损伤之间的一个平衡状态。在抗无或弱细胞病变的感染时免疫失衡,出现病理损伤而致疾病的临床例子有:TB,HBV,HCV,或HIV导致的AIDS。以下几项说明T,B淋巴细胞反应是先天的,即:抗原结构,抗原定位,抗原剂量和抗原有效期(其作用在表1中已简略归纳)。1、 通常T,B淋巴细胞应答仅在次级淋巴器官被诱导(如淋巴结,peyer's 片,脾脏) 2、 T细胞对有效剂量,并维持至少3~5天的定居在次级淋巴器官的细胞相关抗原发生应答,停留在次级淋巴器官外的抗原常被免疫忽略,另外,那些定居在初级或次级淋巴器官的抗原(如血清蛋白)可使所有有潜在激活活性的T细胞诱导调亡,这一过程称为阴性选择
乙肝疫苗出事了后,引起了行业的震动。虽说最后查明不是疫苗本身的质量问题,但是,好像有数据表明疫苗的接种率明显的下降了 。你还打疫苗吗?
[color=#DC143C]11未应助[/color]可以的話拜託幫忙了感謝1.抗HIV和HBV病毒药物L-Fd4C及相关核苷类似物 [科学通报 Chinese Science Bulletin] 胡清萍 , 赵康 , 陈曙辉 2.L-核苷类抗HIV、HBV活性化合物研究进展 Advances in L-Nucleosides as Anti-HIV and Anti-HBV Agents [化学进展 Progress in Chemistry] 董春红 , 常俊标 , Dong Chunhong , Chang Junbiao 3.抗乙型肝炎病毒β-L-(-)型核苷类似物的研究 [医学新知杂志 Journal of New Medicine] 吴金明 , 韩清锡 , 林菊生 4.核苷类似物耐药对我国抗乙肝病毒治疗的影响 Influence of nucleoside analogues resistance on anti-HBV treatment [中华医学杂志 National Medical Journal of China] 侯金林 , 孙剑 , HOU Jin-lin , SUN Jian 5.核苷类似物抗乙肝病毒治疗后耐药新认识 [中华传染病杂志 Chinese Journal of Infectious Diseases] 侯金林 , 孙剑 6.核苷5'-硫代磷酰氨基酸酯电喷雾质谱研究 Electrospray Ionization Mass Spectra of Nucleoside 5'- Thiophosphoramidates [分析测试学报 Journal of Instrumental Analysis] 苗志伟 , 付华 , 陈益 , 赵玉芬 7.抗乙型肝炎病毒核苷类似物耐药机制的研究进展 [国外医学(药学分册) Foreign Medical Sciences(Section of Pharmacy)] 滕光菊 , 李保森 8.β-L-核苷类化合物:抗病毒药物研究与开发的新热点 [中南药学 Central South Pharmacy] 汤军 , 杨静华 , 吴国生 , 项光亚 9.抗乙型肝炎病毒药物研究进展 Advances of anti-HBV Drugs [天津药学 Tianjin Pharmacy] 吴剑涓 10.与核苷类似物治疗有关的HBV聚合酶基因变异 [国际流行病学传染病学杂志 International Journal of Epidemiology and Infectious Disease] 申凤俊 , 贾继东 , 王宝恩 , 阴赪宏 11.核苷(酸)类似物长期治疗的常见耐药位点及发生率 Mutation incidence of and resistant sites in HBV after longterm nucleoside analogs therapy [中华肝脏病杂志 Chinese Journal of Hepatology] 梁雪松 , 万谟彬 12.重视抗乙型肝炎病毒药物耐药的研究 [实用肝脏病杂志 Journal of Clinical Hepatology] 成军 13. 抗乙肝新药阿德福韦的研究进展 Research advance in a new anti-HBV agent-adefovir [中国新药与临床杂志 Chinese Journal of New Drugs and Clinical Remedies] 蒋晔 , 徐智儒 , 张晓青 14.抗乙肝病毒新药--阿德福韦酯 [中国药学杂志 Chinese Pharmaceutical Journal] 蒋晔 , 徐智儒 , 张晓青 15.抗乙肝新药阿德福韦酯的研究现状及展望 Review on the Study of New Drug Adefovir Dipivoxil for the Treatment of Hepatitis B [中国药事 Chinese Pharmaceutical Affairs] 孙德清 , 郭瑞臣 , Sun Deqing 16.核苷类抗病毒药物进展 Review of anti-virus agent of nucleosides [抗感染药学 Anti-Infection Pharmacy] 张文婷 , 倪孟祥 , 张绍谭 , ZHANG Wen-ting , NI Meng-xiang , ZHANG Shao-tan 17.阿德福韦酯的合成 Synthesis of Adefovir Dipivoxil [中国医药工业杂志 Chinese Journal of Pharmaceuticals] 蒋晔 , 徐智儒 , 张丽芳 , 张晓青 18.阿德福韦酯药动学研究进展 Progress of pharmacokinetic characteristics of adefovir dipivoxil [中国药学杂志 Chinese Pharmaceutical Journal] 蒋晔 , 徐智儒 , 张晓青 19.抗病毒新药阿地福韦 [华西医学 West China Medical Journal] 胡国平 , 赵连三 20.抗乙肝病毒新药恩替卡韦的研究进展 The research progress of entecavir-a new anti-HBV medicine [继续医学教育 Continuing Medical Education] 李颖 21.抗乙型肝炎新药阿德福韦 [肝脏 Chinese Hepatology] 杨敏燕 , 姚光弼 22.反相高效液相色谱法测定阿德福韦酯及其降解产物 Determination of Adefovir Dipivoxil and Its Degradation Products by Reversed-Phase High Performance Liquid Chromatography [色谱 Chinese Journal of Chromatography] 蒋晔 , 徐智儒 , 张晓青 23.抗乙型病毒性肝炎新药--阿德福韦酯 Adefovir dipivoxil-A new drug for hepatitis B [中华肝脏病杂志 Chinese Journal of Hepatology] 曾民德 , 茅益民 24.阿德福韦酯与拉米夫定抗乙肝病毒疗效对比 The comparison Between Lamivudine and Adefovir Dipivoxil for Anti-virus Therapeutic Efficacies in Chronic Hepatitis B [江西医学院学报 Acta Academiae Medicinae Jiangxi] 李琴英 , 黄镇 , 范敏 , 金志文 , 王莉萍 , 王海辉 , 杨红梅 引用的文献 25.Antiviral L-nucleosides specific for hepatitis B virus infection 《Antimicrobial Agents and Chemotherapy》 Bryant M L Placidi L Placidi L 2001 / 45 / P 229-235
看到一则消息,说2014年有好几种治疗丙肝的药物即将上市。如吉利德公司丙肝治疗药物Sovaldi(sofosbuvir),雅培的新型丙型肝炎三联组合药物(ABT-450/利托那韦+ABT-267+ABT-333),强生的丙型肝炎药物Olysio(simeprevir)等。这么多公司投入这么大的力量研发丙肝治疗新药,难道说丙肝是所有肝炎中危害最大的?
十五岁以下人群补种乙肝疫苗 为促进基本公共卫生服务逐步均等化,提高卫生服务效率,促进医改重点工作整体推进,中国将免费向城乡居民提供六项重大公共卫生服务。 在卫生部举行的重大公共卫生服务项目启动电视电话会议上 ,卫生部党组书记、副部长张茅透露:中央财政已下达第一批六项重大公共卫生服务项目资金,标志其正式启动。这六项重大公共卫生服务项目是: 为十五岁以下人群补种乙肝疫苗项目。 百度 仪器仪表交易网压力变送器计划用三年时间,在全国范围内对一九九四年至二00一年出生的未免疫人群实施乙肝疫苗接种,进一步降低该人群乙肝病毒感染率和乙肝表面抗原携带率。今年全国需接种二千三百三十万人,占应接种人群的百分之三十一。 农村妇女乳腺癌、宫颈癌检查项目。从今年到二0一一年为一千万农村妇女进行宫颈癌检查,对其中一百二十万人进行乳腺癌检查,提高农村妇女“两癌”早诊早治率,降低死亡率。 增补叶酸预防神经管缺陷项目。百万贫困白内障患者复明工程。消除燃煤型氟中毒危害项目。农村改水改厕项目。
[font=inherit]一、项目基本情况[/font] 项目编号:JLZT20240626/JM-2024-06-00645 项目名称:长春市中心血站耗材(丙肝检测试剂等) 预算金额:300.000000 万元(人民币) 最高限价(如有):0.279500 万元(人民币) 采购需求: 本项目采购乙型肝炎病毒表面抗原诊断试剂盒(酶联免疫法)、人类免疫缺陷病毒抗原抗体诊断试剂盒(酶联免疫法)、丙型肝炎病毒抗体诊断试剂盒(酶联免疫法)、梅毒螺旋体抗体诊断试剂盒(酶联免疫法)、人类T淋巴细胞白血病病毒抗体检测试剂盒(双抗原夹心酶联免疫法)、核酸血筛检测系列标准物质、血筛四项混合标准物质、HBsAg质控品、HCVAb标准物质、HTLV抗体质控品、乙型肝炎病毒表面抗原检测试纸条、乙型肝炎病毒表面抗体诊断试剂盒(酶联免疫法)、乙型肝炎病毒e抗原检测试剂盒(酶联免疫法)、乙型肝炎病毒e抗体检测试剂盒(酶联免疫法)、乙型肝炎病毒核心抗体检测试剂盒(酶联免疫法)等,具体内容详见《招标文件(采购要求)》 合同履行期限:签订合同后一年 本项目( 不接受 )联合体投标。 [font=inherit]二、申请人的资格要求:[/font] 1.满足《中华人民共和国政府采购法》第二十二条规定; 2.落实政府采购政策需满足的资格要求: 本项目非专门面向中小企业采购的项目; 2.1《政府采购促进中小企业发展管理办法》(财库〔2020〕46号); 2.2《财政部、司法部关于政府采购支持监狱企业发展有关问题的通知》(财库[2014]68号); 2.3《关于促进残疾人就业政府采购政策的通知》(财库〔2017〕141号); 2.4《关于环境标志产品政府采购实施的意见》(财库〔2006〕90号) 2.5《国务院办公厅关于建立政府强制采购节能产品制度的通知》(财库〔2007〕51)等国家最新政策。 3.本项目的特定资格要求:3.1(1)供应商人须在中华人民共和国境内注册,能够独立承担民事责任的法人、其他组织或者自然人,具备所提供产品生产或经营能力,能够提供采购内容及其相应的服务的能力;(2)供应商如为制造商须具备《医疗器械生产许可证》或《医疗器械生产备案凭证》;(3)供应商如为代理商须具备《医疗器械经营许可证》或《医疗器械经营备案凭证》;(4)产品具备有效的《中华人民共和国医疗器械注册证》或《医疗器械备案凭证》(适用于按医疗器械管理的设备);3.2财务要求:财务状况良好,具有会计师事务所或审计机构出具的审计报告或银行出具的资信证明;3.3依法缴纳税收和社会保障资金的良好记录证明材料;3.4信誉要求:(1)供应商须符合财政部(财库【2016】125号)要求,供应商需提供通过信用中国(www.creditchina.gov.cn)和中国政府采购网(www.ccgp.gov.cn)的信用信息查询记录,对列入信用中国失信被执行人、重大税收违法案件当事人名单(重大税收违法失信主体)、政府采购不良行为记录和中国政府采购网政府采购严重违法失信行为记录名单的供应商,拒绝其参与采购活动;(2)供应商近三年内在经营活动中没有重大违法记录;(3)供应商未被工商行政管理机关在全国企业信用信息公示系统(www.gsxt.gov.cn)中列入严重违法失信企业名单;(4)供应商近三年(2021年1月1日至2024年06月30日)内在中国裁判文书网(wenshu.court.gov.cn)无行贿犯罪记录;3.5单位负责人为同一人或者存在直接控股、管理关系的不同供应商,不得参加同一合同项下的政府采购活动。除单一来源采购项目外,为采购项目提供整体设计、规范编制或者项目管理、监理、检测等服务的供应商,不得再参加该采购项目的其他采购活动; [font=inherit]三、获取招标文件[/font] 时间:2024年08月08日 至 2024年08月15日,每天上午8:30至11:30,下午13:30至16:30。(北京时间,法定节假日除外) 地点:政采云平台https://www.zcygov.cn/ 方式:供应商登录政采云平台https://www.zcygov.cn/在线申请获取采购文件(进入“项目采购”应用,在获取采购文件菜单中选择项目,申请获取采购文件),其他途径获取的招标文件开标时一律按无效投标处理)。 售价:¥0.0 元,本公告包含的招标文件售价总和 [font=inherit]四、提交投标文件截止时间、开标时间和地点[/font] 提交投标文件截止时间:2024年08月29日 09点30分(北京时间) 开标时间:2024年08月29日 09点30分(北京时间) 地点:政采云平台https://www.zcygov.cn/ [font=inherit]五、公告期限[/font] 自本公告发布之日起5个工作日。 [font=inherit]六、其他补充事宜[/font] 本次招标公告同时在《中国政府采购网》、《长春市公共资源交易网》上发布。 [font=inherit]七、对本次招标提出询问,请按以下方式联系。[/font] 1.采购人信息 名 称:长春市中心血站 地址:长春市经济技术开发区自由大路5916号 联系方式:王春阳0431-85839117 2.采购代理机构信息 名 称:吉林省中通招投标有限公司 地 址:吉林省长春市人民大街7088号伟峰国际2202室 联系方式:籍婷婷0431-89611388 3.项目联系方式 项目联系人:籍婷婷 电 话: 0431-89611388
为进一步提高Hib疫苗的国产化程度,延长疫苗有效期,2007年,甘肃省科技厅以重大科技专项形式支持兰州生物制品研究所开展“冻干Hib结合疫苗研制”。到目前为止,甘肃省冻干Hib结合疫苗已完成了临床前研究,研究进展良好,达到了预期的技术指标。甘肃省科技厅介绍,冻干Hib结合疫苗的研制,是对Hib疫苗剂型的创新开发,该疫苗的研制成功,将会对相关病症的防控发挥重要作用。据了解,Hib是b型流感嗜血杆菌的简称,主要通过空气飞沫传染,5岁以下儿童、尤其是2个月—2岁的婴幼儿很容易被传染,是引起婴幼儿下呼吸道感染、脑膜炎的致病菌,也是我国儿童呼吸道疫病的首位致病菌,且Hib对多种抗生素很容易产生耐药性,所以感染后较难诊治。接种Hib疫苗能对Hib引起的疾病进行有效预防。但因现有Hib疫苗是液体剂型,有效期短、不易储存和运输,且价格昂贵,所以我国目前仅在部分发达地区使用Hib疫苗。
1【题目】HBV前S基因变异及其临床意义 【作者】吴炜 李兰娟 2【题目】HBcAg与前S1抗原部分基因的融合表达及其抗原性分析 【作者】周伯平 陈心春 等 3【题目】乙型肝炎病毒不同株的混杂感染可能是慢性重型肝炎的一个特点 【作者】张瑞 王海涛 4【题目】乙型肝炎病毒多表位嵌合蛋白的表达, 纯化和鉴定 【作者】甘慧, 王海平
新华社华盛顿5月9日电(记者林小春)美国研究人员9日在学术期刊《科学》上报告说,他们开发出一种新计算方法,可以更快地发现抵御艾滋病病毒的强力抗体,这一成果有望加快艾滋病疫苗研发。 开发艾滋病疫苗是全球面临的重要任务和挑战。尽管艾滋病病毒已发现30多年,但由于其多变和多样性,迄今还没有一种针对该病的疫苗能离开实验室并大量应用。不过近年来,科研人员在艾滋病病毒“中和抗体”研究方面已取得重要进展。 “中和抗体”是免疫细胞分泌的一类蛋白,能在某些病毒侵入细胞之前与该病毒结合,阻止其黏附、感染细胞,相当于把病毒“中和”掉。 美国国家卫生研究院疫苗研究中心的科研人员,将已知“中和抗体”的相关数据与生物信息学分析结合起来,开发出一种相对简单快速的计算方法,能通过分析血样对毒株的反应,准确判断某人的血液中有哪几类抗体能够抵御艾滋病病毒。 这份报告的共同第一作者周同庆对新华社记者说,长期以来人们一直在研究那些具有强力中和活性的艾滋病病毒感染者的血液,因为了解这些人如何产生攻击艾滋病病毒的强力“中和抗体”,可为设计疫苗提供线索。但血液中有多种抗体,常规分析方法不易确定哪种抗体能更有效地抵御艾滋病病毒,即便能确定相关抗体的中和原理,一般也需要多年艰苦研究,同时涉及复杂技术且需要大量血样。 周同庆及其同事开发出的新算法,则依据已知的艾滋病病毒抗体的中和反应数据,组建数据库,通过比对血样成分对抗艾滋病病毒时留下的“中和指纹”与数据库中的相关抗体数据,可快速准确地确定血中“有用”抗体的类型和比例。对一些艾滋病病毒感染者的血样测试表明,该算法准确有效。 周同庆说,这一方法在未来艾滋病疫苗研发过程中,可用来快速评估接种人群的免疫反应,有重要应用前景。此外,他们还着手将这一技术扩展应用到丙型肝炎、流感等其他传染病疫苗研究中。 《科学》期刊配发的一篇评论文章指出,疫苗开发正从基于病毒灭活的经验科学,向基于核酸和蛋白质等相关研究的理性设计过程转型,包括新算法在内的一些艾滋病研究新进展表明,“对于新艾滋病疫苗的设计和测试前景,我们应该持乐观态度”。
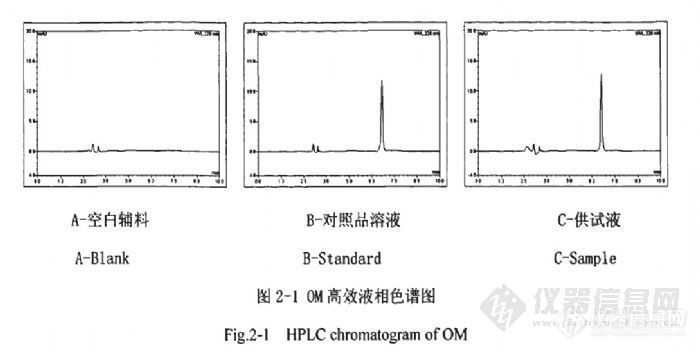
作者:李宗伟; (南方医科大学;)摘要:背景 全世界约有20亿人感染了乙肝病毒,约有3.5亿人患有慢性感染。估计每年有60万人死于急性或慢性乙型肝炎。在儿童时期获得慢性感染的成人中,约25%会因慢性感染死于肝癌或肝硬化。乙型肝炎病毒的传染性比艾滋病毒强50至100倍。乙型肝炎是一个重要的全球卫生问题,也是最严重类型的病毒性肝炎。它可造成慢性肝病,患者死于肝硬化和肝癌的风险极高,乙型肝炎病毒是影响卫生工作者的一个重要的职业危害。 乙型肝炎在中国和亚洲其他地区流行。这些地区大多数人在儿童时期即已感染乙型肝炎病毒,8-10%的成年人会转为慢性感染。乙型肝炎病毒造成的肝癌是导致男子因癌症死亡的三大因为之一,也是导致妇女因癌症死亡的一个主要因为。亚马逊和中东欧南部地区亦为慢性感染高发区。在中东和印度次大陆,估计有2-5%的人口为慢性感染状态。西欧和北美有不到1%的人口为慢性感染状态。 苦参素(Matrine)是从天然植物苦豆子(Sophora Alopecuroides L.)和苦参(Sophora Flavescerls Ait)根中科学提取的生物碱,经氧化合成、纯化、提取而得到的有效单体,是苦参碱的N-氧化物,氧化苦参碱因具有特殊的氧结构从而使分子极性大增,较苦参碱具有独特的作用机理和疗效。 苦参素以氧化苦参碱(Oxymatrine,OM)为主及少量的氧化槐果碱(Oxysophoepine)的混合碱,按干燥品计算,含氧化苦参碱(C15H24N2O2)不得少于98.0%。氧化苦参碱,分子式:C15H24N2O2·H2O,分子量:282.38。苦参素为白色或类白色的结晶性粉末;无臭,昧苦;在水、乙醇、氯仿中易溶,在丙酮中溶解,在乙醚中微溶。 基础药理与临床研究表明有抗癌、抗病毒、抗寄生虫、抗炎、抗心律失常及明显升高白细胞作用,具有广阔的开发前景。近年研究发现,苦参素具有消除或抑制病毒的复制,能调节机体的免疫力,增强肝脏的解毒能力。稳定肝细胞,促进肝细胞再生,提高肝细胞活力,保护肝内酶系统,改善肝功能。用它治疗慢性肝炎,可有效降低ALT,改善临床症状。意义及目的 苦参素还存在着由于脂溶性差,口服生物利用度低,这在一定程度上限制了其临床疗效的发挥。制备成微球或是微丸、纳米制剂则成本较高且难于实现工业化。而药剂学研究中的凝胶骨架缓释片技术能提高其体内吸收,显著地改善其生物有效性,且工艺简单、成本较低。本课题结合临床实际,选择治疗病毒性肝炎具有良好作用的苦参素作为模型药物,在中医药理论及现代实验设计思想的指导下,进行了抗肝炎苦参素凝胶缓释片的制备工艺、理化性质、质量标准、稳定性以及药物代谢动力学方面的研究,为解决苦参素的吸收提供了新的思路。 方法 1.本文以制备12h控制释放的苦参素凝胶骨架缓释片为目的,在以此为基础上,对处方前的各项指标进行考察。建立苦参素的体外的分析方法,并通过详细的方法学确证了体外分析方法的可靠性。建立高效液相色谱法用于氧化苦参碱基本理化性质、片剂的释放度和含量的测定。并对苦参素在各种促渗剂饱和液中
[em43] 请问从事动物疫苗(活疫苗)检验有没有危险性?会不会被传染?
中国网10月10日讯 今天上午,卫生部举行例行新闻发布会,卫生部新闻办主任邓海华主持发布会并回答了记者提问。 有记者提问到,最近纷纷报道乙肝病毒携带者办理健康证,食品加工行业的要求,请问卫生部对此的态度是什么? 对此邓海华表示,根据《食品安全法》第四章第三十四条和《食品安全法实施条例》第四章第二十三条的规定,从事接触直接入口食品工作的人员患有痢疾、伤寒、甲型病毒性肝炎、戊型病毒性肝炎等消化道传染病,以及患有活动性肺结核、化脓性或者渗出性皮肤病等有碍食品安全的疾病的、食品生产经营者应当将其调整到其他不影响食品安全的工作岗位。其中,有碍食品安全的疾病不包括乙型病毒性肝炎,也就是说,法律法规没有禁止乙肝病毒携带者从事接触直接入口食品的工作。因此,在食品从业人员专项健康体检中,不宜再设定乙型病毒性肝炎有关体检项目。 邓海华说,对于乙肝和乙肝病毒携带者的问题,我想强调的是,党和政府对乙肝防治工作高度重视,不断加强对乙肝防治工作的领导,制定防治规划,采取综合措施,控制乙肝的流行与传播。特别是自上世纪90年代起,大力推行儿童乙肝疫苗接种策略,1992年将乙肝疫苗接种纳入计划免疫管理。2002年,经国务院批准,将乙肝疫苗纳入儿童计划免疫。从今年起,按照《医药卫生体制改革近期重点实施方案(2009-2011年)》确定的重点工作,三年内在全国范围内对1994年至2001年出生的15岁以下的未免疫人群实施乙肝疫苗接种,这将对进一步防止青少年感染乙肝病毒提供有效的保障。 据介绍,近年来,在加强乙肝防治工作和知识宣传的同时,卫生部加大和其他部门的合作,在相关法律法规制定中不断完善对乙肝病毒携带者合法权益保护的条款。2004年修订的《传染病防治法》、2005年开始实施的《公务员录用体检通用标准(试行)》、2007年我部会同劳动和社会保障部联合下发的《关于维护乙肝表面抗原携带者就业权利的意见》,以及刚才介绍的食品安全法及其实施条例的相关规定,这些对形成一个全社会关心乙肝防治工作、关心乙肝患者和乙肝表面抗原携带者的良好氛围提供了有力的支持。 邓海华表示,最近,针对媒体和社会普遍关注的体检中乙肝两对半检测问题,卫生部会同有关部门组织国内权威专家,就规范入学、就业健康体检中乙肝检查项目进行了广泛深入的研究讨论,形成了共识。当前社会上对乙肝病毒携带者的误解主要是由于人们对乙肝知识缺乏了解。乙肝是血源性传播性疾病,不会通过呼吸道和消化道传染,日常生活和工作接触不会传播乙肝病毒,乙肝病毒携带者不是乙肝病人,身体没有临床症状,肝功能正常,不会因一般的生活接触、共同学习、工作等对周围人群构成威胁。专家认为,取消入学、就业体检中的乙肝血清学检测项目(乙肝五项检测,俗称“两对半”)不会影响他人健康,也不会造成乙肝的传播 从及早发现乙肝病人、及早治疗、对患者健康负责的角度出发,在入学、就业体检中保留丙氨酸氨基转移酶(ALT,简称转氨酶)检查项目以及评价肝脏功能,比检测乙肝五项对诊断乙肝更具有临床参考意义。目前,按照相关工作程序,卫生部有关司局正在依据上述共识制订指导性意见。待意见出台时,卫生部将召开新闻发布会,请权威专家进行详细解读。
国家卫计委疾控局免疫处处长李全乐称,乙肝疫苗事件后,10省(自治区、直辖市)的调查显示,中国儿童乙肝疫苗的报告接种率骤降30%。时隔4个月,乙肝疫苗的接种率有所回升,但回升速度缓慢,过程艰难。药物出事故,查明原因就好了。现在原因已经明了,我们还需要如此“谨慎”吗?
传统疫苗的研究是把原有的野生的病毒或细菌在实验室培养制备后,通过物理、化学的方式将其灭活,即为原始疫苗的主要成分,加上佐剂再通过注射或口服进行免疫,但这种方式也会带来比较大的毒副反应。因此,目前又进入到第三代亚单位或基因工程/多肽疫苗的研发。根据疫苗研发技术的发展,当前疫苗的种类可以分为亚单位疫苗、基因重组疫苗、合成多肽疫苗和免疫球蛋白载体疫苗。其中基因重组疫苗又分为重组DNA疫苗、重组活疫苗、杂交株活疫苗、基因缺失活疫苗,免疫球蛋白载体疫苗又可分为抗毒特性抗体疫苗、表位嵌合免疫球蛋白等。国内外疫苗研究在研发人士的努力之下取得了不少新进展。1、HPV基因工程疫苗人乳头瘤病毒(HPV)疫苗是预防宫颈癌的第一支防癌疫苗,目前研制成功的HPV疫苗是预防性疫苗,HPV治疗性疫苗还在研制中。它是由默克公司和葛兰素史克公司两家分别独立研制成功的,一个是四价,一个是两价,目前在数十个国家和地区广泛使用。在美国使用的价格大约是每人份360美元,这一价格在我国是很难被大多数人接受的,因此我国亟待研制自己的HPV疫苗。据悉,目前国内有两家HPV疫苗研究单位申报了临床试验,已有一家拿到了临床批件。2、基因工程幽门螺杆菌疫苗研究证实,幽门螺杆菌(Hp)是胃病发生的元凶。目前临床上主要是采用抑制胃酸分泌的药物联合多种抗生素治疗Hp引起的相关胃病,单一抗生素的根治率不超过30%,由于Hp一般隐藏于pH值很低的胃黏膜处,药物难以达到作用部位,耐药严重。第三军医大学国家免疫生物制品工程技术中心从1995年就开始了Hp疫苗的研制:(1)首先,创立了“Hp分子内佐剂黏膜疫苗”学说,并得到了实践的验证。(2)首次建立了高效筛选Hp疫苗组分的体系,成功构建了可用于生产的Hp疫苗工程菌株。研究建立了国内外第一份《Hp疫苗制造与检定质量标准》。(3)建立了Hp疫苗Ⅰ、Ⅱ、Ⅲ期人体临床试验所需的30多种技术规范、标准及实验检测技术。通过这些关键技术的发明与创立,按照国际标准完成临床试验,结果表明Hp胃病疫苗安全性良好,保护率为72.10%,达到口服类疫苗国际先进水平。该项目申请了15项专利,获得了8项授权。该疫苗目前已经成功进入产业化发展阶段。目前国际上也有很多机构也在对Hp疫苗进行研究,如诺华等一些公司,他们的疫苗目前还处在临床Ⅰ、Ⅱ期试验当中。3、人用禽流感疫苗和甲型H1N1流感疫苗我国在禽流感和甲流的控制、疫苗的研发方面走在了世界的前面。2008年4月2日,国家食品药品监管局(SFDA)正式批准了北京科兴生物制品有限公司生产的大流行流感疫苗,标志着我国成为继美国之后第二个具备人用禽流感疫苗制备技术和生产能力的国家,说明我国从疫情监测、病人发现、病毒分离鉴定、病毒培养改造、临床试验到工业化生产整个技术链条是完整的,实质性地完成了疫苗的技术储备,也具备了实物的储备条件。2009年9月3日,北京科兴生物制品公司研制的甲型H1N1流感疫苗获得SFDA药品生产注册。这是全球首个获得政府药品批准文号的甲型流感疫苗,命名为“盼尔来福.1”。整个疫苗研制周期仅用了87天。该疫苗一剂免疫后21天,儿童、少年和成人三个年龄组保护率均在81.4%~98.0%范围内,达到了国际公认的评价标准(保护率70%以上)。可用于3岁~60岁人群。4、“中国号”艾滋病疫苗我国目前研发了多个艾滋病疫苗,分别处于Ⅰ、Ⅱ期临床试验阶段。由中国疾病预防控制中心与北京生物制品所研制的“DNA――天坛疫苗复合型艾滋病疫苗”于2007年12月1日起进行Ⅰ期临床试验,现已经结束,开始进入Ⅱ期临床试验。另一个是由吉林大学孔维教授等人研制的艾滋病疫苗,目前正在进行临床试验。5、新型结核疫苗尽管结核病疫苗应用已经很长时间了,但是近年来结核病有增无减,控制情况不理想,主要原因还是与结核杆菌变异有很大关系。墨西哥研制出了可预防最常见的肺结核病的新疫苗。这种疫苗比目前使用的疫苗更有效,因为传统疫苗只针对高危性结核,但高危性结核仅占10%。据悉,新型疫苗还可以预防近几年出现的新型结核病。该疫苗已在动物实验上取得了理想效果,预计不久将进行人体试验。6、联合疫苗从现实使用需求来看,一剂多防的疫苗是未来的研究方向,由于存在免疫干扰现象,这一研究也是非常困难的,尽管难度很大,新型联合疫苗也在不断的研制中。新型联合疫苗的开发包括以DPT为基础的联合疫苗、以活疫苗为载体的联合疫苗和口服联合疫苗。为进一步减少免疫接种次数,国内外开展了几种联合疫苗同时接种的观察。目前现有的联合疫苗都是以DPT为核心,加上其他疫苗而组成的,例如DPT/Hib、DPT/IPV等。现有联合疫苗分为两大类:一是多疾病联合疫苗,它通常包含多种单个疫苗来预防多种病,组成这种联合疫苗的单个疫苗通常是分别开发在先,联合在后(无细胞百日咳除外);二是多价联合疫苗,包含了同一种细菌或病毒的不同亚型或血清型,这些在疫苗开发时就联合在一起,未曾分开。现有已经上市的联合疫苗有DTwcp/IPV、DTwcp/Hib、DTwcp/HB等,正在开发中的联合疫苗包括破伤风/狂犬病、黄热病/伤寒Vi疫苗等。另外,疫苗在接种手段上也在进行改进,目前绝大多数疫苗是采用注射方式接种,依存性相对较差,突发事件中大规模预防接种等情况,都希望采用非注射的方式进行接种,如黏膜接种或纳米透皮技术等。部分新近上市或进入临床试验的黏膜接种疫苗如Ty21a伤寒活疫苗,CVD103-HgR霍乱活疫苗,霍乱O1/O139/rCTB联合菌苗,四价恒河猴轮状病毒活疫苗,鼻内接种的三价冷适应流感活疫苗,减毒伤寒杆菌活载体疟疾黏膜疫苗(Ⅱ期临床)。7、治疗性疫苗传统观念认为,疫苗的作用是对疾病的预防,但近年来疫苗也正在慢慢改变着它的内涵和功能。治疗性疫苗的研究结果对传统发出了挑战:疫苗不仅能防病,还能通过加强或调整患者免疫功能而达到治病作用。例如幽门螺杆菌是一种慢性感染性疾病,由于免疫产生耐受,因此可以通过免疫手段强化细胞免疫功能或者是特殊的抗体功能达到一定的治疗效果,这一结果已经在动物实验和人体试验上得到了证实。目前国内有3个乙肝治疗性疫苗正在进行临床试验,如闻玉梅院士与天坛生物等首次研制开发的抗原-抗体复合物乙肝治疗性疫苗,已获得SFDA批准进入Ⅲ期临床试验。8、另类疫苗(非感染性疾病疫苗)非感染性疾病也可以通过疫苗进行预防或治疗。癌症疫苗已经不再是梦想。东京大学研制的几种癌症疫苗在日本10多个临床试验中取得了较好的疗效。在其他治疗手段已经不起作用的802名患者身上试验表明,有60%显现出癌症部位缩小或者在一定时期内病情不再恶化等良好疗效。他们从癌细胞中找到了可以引起强烈免疫反应的17种癌相关抗原,从而制成了这几种癌症疫苗。这几种癌症疫苗的对象包括食道癌、胰腺癌、大肠癌、膀胱癌等10多种癌症。高血压疫苗也取得了新进展。这种抗高血压疫苗能够产生一种能对血管紧张素Ⅱ产生作用的抗体。血管紧张素Ⅱ是一种机体产生的荷尔蒙,能够调节机体液体的压力,这种抗体能够关闭血管紧张素Ⅱ的接收器,从而防治高血压的产生。美国食品药品管理局(FDA)已批准一种糖尿病疫苗进入临床试验。Ⅰ型糖尿病的发病机理是来自免疫系统的T细胞移动到胰腺处,摧毁能制造胰岛素的β细胞。故可使用树突状细胞糖尿病疫苗保护胰岛细胞。老年性痴呆疫苗也取得了新进展。曼彻斯特大学用小白鼠免疫实验表明:该疫苗不仅能防止β淀粉样蛋白的积累,而且使脑中淀粉样变减少,认知能力提高,并没有脑水肿的迹象。专家认为,新研制的疫苗有望防止老年痴呆症。关节炎疫苗有望在5年内问世。英国纽卡斯尔大学研究的关节炎疫苗已在8名风湿性关节炎的志愿者身上进行了使用,并取得了良好的效果。该疫苗有望在5年内问世。乙肝纳米疫苗取得新进展。美国密歇根大学的科学家宣布,他们成功研制了鼻内喷雾使用的乙肝疫苗纳米乳,通过缓释和更加靶向的方式,有望成为现有乙肝疫苗的替代品。此新型疫苗无需冷藏,且不需要像目前的疫苗要在6个月内注射三次。此外,尼古丁/可卡因防成瘾疫苗、避孕疫苗也已处于研发之中。疫苗的研究作为生物制药领域的热点,一直是方兴未艾。如HIV疫苗、广谱流感疫苗、结核杆菌新疫苗、治疗性疫苗、生物反恐疫苗等,新型疫苗的蓬勃发展和传统疫苗的发扬光大,正是当今疫苗发展的时代写照与特征。(中国医药报)
[center]中药治疗乙肝表面抗原转阴获得效果 优势独特[/center]中医药在治疗乙肝方面具有独特的优势。记者从正在深圳召开的中药• 乙肝战略发展研讨会上获悉,由于着眼于恢复人体免疫系统、阻断病毒持续复制,中药在治疗乙肝表面抗原转阴方面获得了比较好的效果。 广东省肝脏病学会会长李福山教授说,中医和西医治疗乙肝各有优势与不足。乙肝病毒感染是全身性疾病,是自身免疫功能发生了问题。中国传统医学理论认为,正气内存,邪不可干。在同一环境中,有的人感染乙肝病毒,有的人却安然无恙,有的人可能自身产生保护性抗体,这说明感染病毒后患病与否与个体差异有关。 李福山说,乙型肝炎病毒携带者,之所以长期携带,是自身的免疫系统处于“疲惫”状态,对乙肝病毒“置若罔闻”,病情相对稳定,抗体长期与病毒共存。这一状态,在传统医学看来,是正(肌体)邪(病毒)相持时期,如果正气强盛,乙肝病毒就可能被清除;假若乙肝病毒强盛,正气虚弱就可能导致肝炎,不再是乙肝病毒携带者,而是地地道道的乙型病毒肝炎。此时是西医抗病毒治疗的最佳时机,如果配合具有疏肝健脾、滋养肾水的中药,则能全面提高自身的抗病毒能力,取得事半功倍的临床效果。 广东岭南肝病研究所所长杨炯说,作为国家食品药品监督管理局批准的新药,乙肝灵胶囊上市两年来获得了较好效果。据广东岭南肝病研究所进行的临床跟踪观察结果显示,3156例乙肝病毒携带者服用一年后,乙肝表面抗原转阴为605例,转阴率为19.2%。信息来源:中国医药123网
酒精性肝炎:长期饮酒? ? ? 喝进去的酒是靠肝来代谢的,在代谢过程中产生的乙醛会损伤肝细胞,长期饮酒,乙醛累积,容易造成酒精肝。刚开始会食欲不振、上腹胀痛,慢慢发展成酒精性肝炎,酒精性肝硬化,甚至会患上肝癌。
[font=黑体][size=4]中国生物技术集团公司简介:[/size][/font] 中国生物技术集团公司(原中国生物制品总公司,2003年8月6日经国家工商行政管理总局核准更名,下称中生集团)为国务院国有资产监督管理委员会管理的国有重要骨干企业,[color=#DC143C]现下辖中国科学器材进出口总公司、中国医疗卫生器材进出口公司及北京生物制品研究所、长春生物制品研究所、成都生物制品研究所、兰州生物制品研究所、上海生物制品研究所、武汉生物制品研究所六个生物制品研究所,并有一家上市公司即北京天坛生物制品股份有限公司[/color]。在近万名职工中,科技人员达到4000多名,是集科研开发、生产、经营为一体的全国最大的生物技术企业集团。 新中国成立以来,中生集团所属各生物制品研究所向市场提供了包括计划免疫所需的各类疫苗和治疗用品,使我国彻底消灭了天花和基本消灭了脊髓灰质炎等困扰人类几个世纪的恶性传染病。据国家卫生部统计,自1978年国家实施计划免疫以来,中生集团生产的各类预防制品在我国共减少麻疹、白喉、百日咳、脊髓灰质炎、结核、破伤风等6种疾病的发病3亿多人次,减少死亡400多万人,减少住院费用400多亿元人民币。1985年中生集团在国内最先研制成功乙型肝炎疫苗,经十余年的推广使用,使乙肝传播得到有效控制,特别是新生儿乙肝感染率已由10%下降到1%。近年来,中生集团又在世界上首先研究出痢疾疫苗、轮状病毒疫苗等。1998年我国发生特大洪涝灾害,中生集团及时组织调拨了钩端螺旋体和伤寒等大批疫苗,为实现党中央提出的“大灾之后无大疫”目标做出了特殊贡献。
重庆啤酒“1号机密”:乙肝疫苗项目到底是什么?◇→ 重啤乙肝疫苗设计流程:1998年10月,重庆啤酒收购佳辰生物,乙肝疫苗故事从此开始;2003年6月,乙肝疫苗I期临床实验开始,紧接着在2004年11月,乙肝疫苗的I期临床结果出炉;2006年4月启动II期A阶段,于2007年12月出具II期A阶段总结报告;2009年8月前后,II期B阶段北方组的临床实验开始,2010年6月,II期B阶段南方组的实验开始。◇→ 重啤乙肝疫苗具有三大特点I期主要验证疫苗的安全性,II期主要是验证疫苗的有效性以及探索最佳的剂量,当然,II期B阶段扩大了样本数量。无论是私募还是公募,通过对II期A阶段长达五年的观察,得出了乙肝疫苗具有三大特点:“时间越长,效果越好;剂量越大,效果越好;停药后无反弹”。 ◇→ 重啤乙肝疫苗后续实验进度根据实验流程安排,II期B阶段北方组在76周后将进入开放式平台,在这一阶段,注射的乙肝疫苗剂量将大大增加,即自愿者将接受900微克×15针的乙肝疫苗,整个实验周期为144周。与此同时,II期B阶段南方组的临床实验也在如火如荼地进行当中。2012年1月6日,按照计划,RPS医药科技(北京)公司将在该日出具乙肝疫苗II期统计分析结果终稿。◇→ 重啤乙肝疫苗潜在的竞争对手在攻克乙肝疫苗的道路上,重庆啤酒面临着来自国内外的竞争。中国工程院院士闻玉梅,被众多重庆啤酒投资者视为吴玉章教授最大的竞争对手。公开资料显示,闻玉梅院士在过去20年一直积极从事乙肝疫苗“乙克”的研究,而且该疫苗的临床实验已经进入了III期冲刺阶段。与国内的潜在竞争者相比,国际医药巨头更是来势凶猛。例如葛兰素史克公司推出的替诺福韦,该药不仅是世界卫生组织(WHO)推荐的艾滋病持续治疗一线药物,也是欧美权威指南推荐的慢性乙肝首选的抗病毒药物,据悉,替诺福韦正在中国进行III期临床实验,预计将在2013年前后在中国市场上市。