【指南与共识】流式细胞术在CAR-T细胞免疫治疗相关检验中的应用专家共识
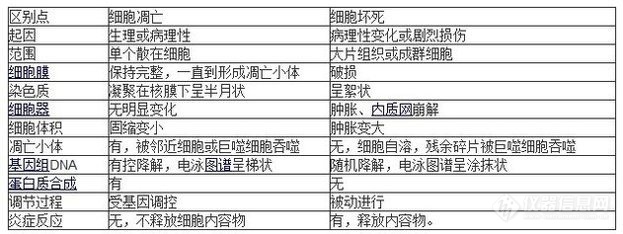
文章来源:中华检验医学杂志, 2022,45(8) : 790-801作者:中国中西医结合学会检验医学专业委员会摘要嵌合抗原受体(CAR)-T细胞免疫治疗是近年来肿瘤治疗领域一个举世瞩目的重大成果。流式细胞术(FCM)在CAR-T细胞免疫治疗相关检验的每一个步骤中都起到非常重要的作用,包括靶点筛查、CAR-T细胞产品成分鉴定、毒性预估、微小残留病(MRD)检测、免疫功能评价、免疫微环境研究等。为了深刻认识FCM在CAR-T细胞免疫治疗这一新兴领域的作用,规范每一项应用中的操作,进一步促进其在CAR-T细胞免疫治疗中的应用,中国中西医结合学会检验医学专业委员会制定了此专家共识。嵌合抗原受体(chimeric antigen receptor,CAR)-T细胞免疫治疗是近年来肿瘤治疗领域一个举世瞩目的重大成果[1, 2, 3, 4, 5, 6, 7],尤其是CD19-CAR-T细胞免疫治疗难治复发B细胞急性淋巴细胞白血病(acute lymphoblastic leukemia,ALL)获得了90%左右的缓解率[1, 2, 3],单独使用或者桥接异基因造血干细胞移植均极大程度地提高了患者的完全缓解率和生存率;CAR-T细胞免疫治疗其他类型白血病、淋巴瘤、骨髓瘤以及实体瘤也在不断探索并取得巨大进步[4, 5, 6, 7]。流式细胞术(flow cytometry,FCM)在CAR-T细胞免疫治疗相关检验的每个步骤中都起到非常重要的作用 [1, 2, 3, 4, 5, 6, 7]。作为一项免疫治疗,CAR-T细胞免疫治疗相关检验中涉及的FCM与临床常规不同,体现在靶点评估需要精确设门并且同时关注正常细胞的表达,CAR-T细胞免疫治疗后微小残留病(minimal/measurable residual disease,MRD)需要考虑靶点丢失以及输入的CAR-T细胞影响,而CAR表达细胞比例和数量的检测以及免疫相关检测均缺乏规范化,给临床工作带来不确定性等。为了能使更多相关领域的科研、临床和实验室检测人员认识FCM在CAR-T细胞免疫治疗中的作用和注意事项,规范在每项检验中的实验方案和技术操作,进一步促进其在CAR-T细胞免疫治疗中的应用,中国中西医结合学会检验医学专业委员会组织专家结合文献学习和多家医疗机构的临床工作实践制定了本专家共识。适用范围、术语和定义一、适用范围各类医疗机构临床实验室、商业化实验室和科研单位在使用FCM进行CAR-T细胞免疫治疗相关临床检验时,均可采用或参照使用本专家共识。鉴于CAR-T细胞生产过程中的创新性和复杂性,并且该步骤极少在临床诊断实验室中进行,本共识不涉及此研发过程。二、术语和定义1.多参数流式细胞术(multiparametric flow cytometry,MFC):虽然MFC的术语出现于20世纪80年代,当初指代两色以上FCM,后期对此也没有明确定义,但是现在普遍建议采用三激光八色或者以上机型。2.CAR-T细胞免疫治疗:人体免疫细胞(来自自体或异体均可),在体外经过基因修饰后具备了特异性识别和杀伤表达特定抗原的肿瘤细胞的能力,输入患者体内以实现清除肿瘤细胞或者其他病态细胞的免疫治疗方法[1, 2, 3, 4, 5, 6, 7]。CAR-T细胞免疫治疗技术包括几个步骤:(1)从患者或者供者血液中分离出自体或者异体T淋巴细胞;(2)用CAR编码的病毒载体进行体外修饰、培养;(3)最后输入患者体内。近年来为了增强治疗效果降低副作用,已发展到第4代CAR-T细胞免疫治疗技术。3.细胞因子:细胞因子是由多种免疫细胞分泌的一类小分子蛋白质,具有介导和调节免疫过程等作用。目前已经发现的人类细胞因子有200多种。根据结构和功能一般可分为白细胞介素(interleukin,IL)、干扰素(interferon,IFN)、肿瘤坏死因子(tumor necrosis factor,TNF)、集落刺激因子、趋化因子和生长因子等。4.细胞因子释放综合征:细胞因子释放综合征(cytokine release syndrome,CRS)是一种发生在任何免疫治疗后,由于内源性或者输注的T细胞和/或其他免疫效应细胞活化或者聚集导致的超生理反应。症状多样,但是必须包括初发时发热,可能伴有低血压、毛细管渗漏(低氧)和终末器官衰竭。尽管没有将细胞因子检测纳入定义,而CRS分级也主要是根据临床表现,但是鼓励进行C反应蛋白、细胞因子、铁蛋白等相关检测,便于为将来的研究提供依据[8]。5.趋化因子及其配体:趋化因子是能使细胞发生趋化运动的小分子细胞因子,其配体很多是免疫功能检测中区分淋巴细胞亚群的重要标志物,例如半胱氨酸-半胱氨酸基序趋化因子受体(cysteine-cysteine motif chemokine receptor,CCR)系列,半胱氨酸-氨基酸-半胱氨酸基序趋化因子受体(cysteine-X-cysteine motif chemokine receptor,CXCR)系列[9]。6.抗原表达率:精确设门后,特定细胞上抗原表达的百分比。临床工作中由于受到抗体和荧光素选择、抗原抗体结合过程、温度光照和放置时间导致荧光信号改变、仪器设置、设门精确度、个体差异、细胞异质性、对照细胞群、检测目的等多种因素影响,以诊断为目标的临床实验室,一般由流式操作人员排除各种影响因素后,按照表达、部分表达、不表达进行定性描述[10],以方便临床和实验室对目的细胞群进行简单直观的性质判断。7.抗原表达强度:与某种抗原分子在细胞上表达量的多少有关,FCM的直观体现为荧光强度。根据抗原表达强度将阳性细胞表达分为强表达(bright,bri)、中等强度表达、弱表达(dim)和异质性表达[10],可能会随着治疗和疾病或者活化状态发生改变。8.单链可变区片段(single-chain variable fragment,scFv):构建CAR-T细胞需要将CAR基因通过病毒载体或非病毒系统转染并整合到T细胞基因组上。CAR基因正常表达时,形成跨膜的CAR结构,细胞外域的重链可变区和轻链可变区通过15~20个氨基酸短肽连接而成的部分即为scFv。编码的scFv元件既是CAR-T细胞识别肿瘤抗原的重要成分,也可作为FCM评价CAR表达情况的检测靶点之一。9.同型阴性对照:用于检测抗体与细胞表面可结晶段受体非特异性结合导致背景信号的阴性对照。应该用与检测抗体相同标记、同种属来源、相同亚型、相同浓度的免疫球蛋白进行染色,如果是间接标记抗体,还需要做二抗的荧光素背景对照,其作用是设置仪器条件,消除背景染色。对于正常标本中不存在的未知标志或者与阴性细胞界限不清的标志,或者标本中比例极低需要精确检测的标志,同型阴性对照是普遍采用的对照。CAR-T细胞免疫治疗相关检验中的FCM项目CAR-T细胞的生产研发、临床治疗每个环节都与FCM检测密不可分,包括靶点筛查、患者选择、CAR-T细胞成分鉴定、毒性预估、MRD检测、回输物和患者标本免疫功能评价、免疫微环境和复发机制研究等。鉴于CAR-T细胞治疗这一全新领域集合了肿瘤细胞和正常细胞免疫表型、肿瘤干细胞免疫表型、免疫细胞亚群、细胞因子检测、CAR-T细胞检测、因部分病例靶点丢失甚至系别转变导致需要调整方案的FCM MRD检测、肿瘤异质性和免疫微环境检测等(表1),以及CAR-T细胞治疗设计的多样性和复杂性、临床工作中使用不同靶点或者联合靶点CAR-T细胞治疗、使用其他细胞因子或者信号分子靶向药物控制副作用等,这些都对FCM检测提出更高的要求。因此深入了解每个环节需要使用的标本类型、检测方案以及最低检测要求,将有助于进一步规范检测流程,提高检测水平,保证检测质量。FCM在CAR-T细胞免疫治疗靶点筛查中的应用随着CAR-T细胞治疗技术的不断完善,CAR-T细胞的功能和治疗的安全性都有了很大提升,并有CAR-自然杀伤(natural killer,NK)细胞、双特异性靶点CAR-T细胞等类似靶向细胞免疫治疗产品出现。但是作为特异性免疫治疗,胞外抗原识别区的设计,尤其是有效靶点的选择始终是每一种CAR-T细胞治疗相关产品的关键环节。理想的靶点应该满足下述要求:高覆盖率(某种疾病的群体中,肿瘤细胞表达该抗原的患者比例高)、高表达率(阳性个体中几乎所有肿瘤细胞都表达)、高表达强度(在肿瘤细胞表面抗原分子数量多,表现为同一种荧光标记时,荧光强度高)、高特异性(在正常细胞中不表达或者少表达,对患者不会造成严重影响)[11]。FCM作为一项快速、简便、直观、定性定量的技术,是目前实现这一目的的重要检测手段,而CAR-T细胞治疗靶点的选择虽然都是在免疫分型或者MRD的基础上进行,但是比常规临床诊断有更严格的特殊注意事项[12, 13]。共识2:为了尽可能给CAR-T细胞免疫治疗提供客观评价,建议一项研究或治疗过程中尽量采用相同的方案,至少是关键抗体和组合相似的方案。同一患者的随访监测尽量在同一台仪器上进行,且尽量仪器条件(包括补偿)相同,或者进行仪器间条件比对。推荐强度:建议执行。)专家组成员(按姓名字母顺序排列