[b]Q:[b][b][b][/b][/b]吡罗昔康注射液的检测,应用编号是?[/b]A:103260===============================================================【活动内容】1、每个工作日上午10:00左右发布一个关于应用数据库的应用问答题,版友根据题目给出自己理解的答案。2、每个工作日下午15:10公布参考答案。【活动奖励】幸运奖:抽奖软件,当天随机抽取3个或5个回答正确的版友ID号(最后一个ID号,截止至下午15:00),每人奖励[color=#ff0000]2钻石币[/color](抽奖人数≤10,抽取3个版友;抽奖人数>10,抽取5个版友);中奖名单:zimeng3211(注册ID:zimeng3211)初心(注册ID:m3170710)yifan1117(注册ID:yifan1117)yy_0324(注册ID:yy_0324)zengzhengce163(注册ID:zengzhengce163)[img=,690,388]https://ng1.17img.cn/bbsfiles/images/2018/11/201811201514021392_9421_1610895_3.png!w690x388.jpg[/img][img=,690,388]https://ng1.17img.cn/bbsfiles/images/2018/11/201811201514045012_1219_1610895_3.png!w690x388.jpg[/img]积分奖励:所有回答正确的版友奖励[color=#ff0000]10个积分[/color](幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次[/b][align=left][color=#ff0000][b]PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。[/b][/color][/align][align=left][color=#ff0000][b] 下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。[/b][/color][/align][align=center]=======================================================================[/align]方法:HPLC基质:标准溶液应用编号:103260化合物:吡罗昔康色谱柱:[url=http://www.dikma.com.cn/product/details-817.html]Leapsil C18 2.7μm 100 x 4.6mm[/url]样品前处理:对照品溶液:取吡罗昔康对照品适量,精密称定,加流动相溶解并定量稀释制成每1ml中约含40μg的溶液。色谱条件:色谱柱:Leapsil C18 100*4.6 mm,2.7 μm (Cat#:86002)流动相:乙腈:0.05 mol/L磷酸二氢钾溶液(磷酸调pH=3.0)=35:65流速: 1 mL/min柱温: 30 ℃检测器: UV 246 nm (含量测定) 230 nm (有关物质)进样量: 20 μL文章出处:天津应用实验室关键字:吡罗昔康注射液、吡罗昔康、2015药典、Leapsil C18、HPLC摘要:Leapsil C18检测吡罗昔康。图谱:[img]http://www.dikma.com.cn/u/image/2014/09/16/1410847870119331.png[/img][img]http://www.dikma.com.cn/u/image/2014/09/16/1410847874126173.png[/img]

问题:迪马科技 2015中国药典吡罗昔康检测的USP拖尾因子是?答案:0.994获奖名单:999youran(ID:999youran)zengzhengce163(ID:zengzhengce163)sixingxing(ID:v2889187)http://ng1.17img.cn/bbsfiles/images/2015/12/201512081526_576855_1987954_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/12/201512081526_576856_1987954_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/12/201512081526_576857_1987954_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/12/201512081526_576858_1987954_3.jpg【活动奖励】幸运奖(2钻石币):抽奖软件,当天随机抽取3个回答正确的版友ID号(最后一个ID号,截止至下午3:00),每人奖励2个钻石币积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================吡罗昔康样品制备制备方法对照品:取吡罗昔康对照品适量,精密称定,加流动相溶解并定量稀释制成每1 mL中约含40 μg的溶液分析条件色谱柱Platisil ODS 250 x 4.6 mm,5 μm (Cat#:99503)流动相乙腈:0.05 mol/L磷酸二氢钾溶液(磷酸调pH=3.0)=35:65流速1 mL/min柱温30 ℃检测器UV 230 nm进样量20 μL色谱图对照品http://ng1.17img.cn/bbsfiles/images/2015/12/201512080958_576701_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 18.814 1591013 79104 19837.438 0.994 -- *药典要求理论板数按吡罗昔康峰计算不低于5000本品种同时使用了SpursilC18、LeapsilC18两款色谱柱,在药典规定条件下进行吡罗昔康的检测,均满足药典要求。

问题:吡罗昔康注射液检测药典要求理论板数按吡罗昔康峰计算不低于?答案:药典要求理论板数按吡罗昔康峰计算不低于5000【活动奖励】幸运奖(2钻石币):抽奖软件,当天随机抽取3个回答正确的版友ID号(最后一个ID号,截止至下午3:00),每人奖励2个钻石币中奖名单:捌道巴拉巴巴巴(注册ID:v3082413)m3071659(注册ID:m3071659)999youran(注册ID:999youran)http://ng1.17img.cn/bbsfiles/images/2016/03/201603301614_588622_1610895_3.pnghttp://ng1.17img.cn/bbsfiles/images/2016/03/201603301614_588623_1610895_3.png 积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================吡罗昔康注射液样品制备制备方法对照品:取吡罗昔康对照品适量,精密称定,加流动相溶解并定量稀释制成每1 mL中约含40 μg的溶液分析条件色谱柱Platisil ODS 250 x 4.6 mm,5 μm (Cat#:99503)流动相乙腈:0.05 mol/L磷酸二氢钾溶液(磷酸调pH=3.0)=35:65流速1 mL/min柱温30 ℃检测器UV 246 nm (含量测定) 230 nm (有关物质)进样量20 μL色谱图对照品246 nmhttp://ng1.17img.cn/bbsfiles/images/2017/01/201701191700_667678_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 18.814 1825409 90792 19841.081 0.994 -- *药典要求理论板数按吡罗昔康峰计算不低于5000230 nmhttp://ng1.17img.cn/bbsfiles/images/2017/10/2016033009593245_01_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 18.814 1591013 79104 19837.438 0.994 -- *药典要求理论板数按吡罗昔康峰计算不低于5000本品种同时使用了Spursil C18、Leapsil C18两款色谱柱,在药典规定条件下进行吡罗昔康的检测,均满足药典要求。

2010 版中国药典 VIII R 规定TOC分析仪是要定期进行系统适用性测试,GE为客户提供即开即用的液体系统适用性标准品,省心省力。8月15日-9月15日,GE携全国代理商惠馈客户,优惠活动如下:如果了解更多有关TOC的系统适用性测试知识,可以点击此处http://ng1.17img.cn/bbsfiles/images/2012/08/201208221014_385307_2359237_3.jpg
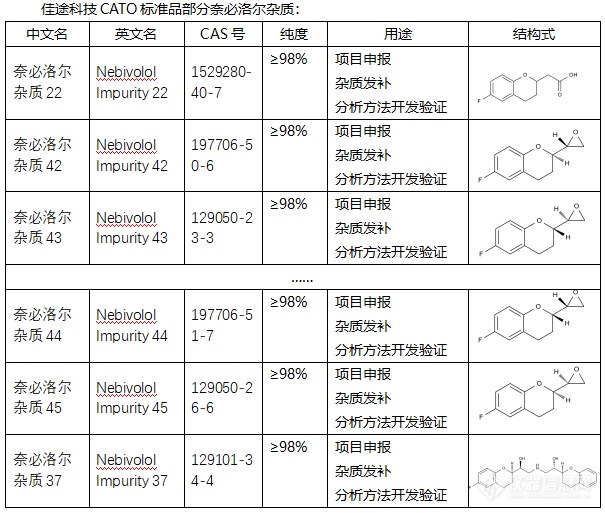
[font=宋体]◇[/font][b][font=宋体]奈必洛尔[/font][/b][font=宋体]杂质[/font][font=宋体][font=宋体] 奈必洛尔杂质是指在奈必洛尔([/font][font=Calibri]Nebivolol[/font][font=宋体])的生产或保存过程中产生的非目标化合物。奈必洛尔杂质有多种,包括但不限于以下几种:奈比洛尔杂质([/font][font=Calibri]L-[/font][font=宋体]奈必洛尔),英文名称为[/font][font=Calibri](-)-Nebivolol[/font][font=宋体],[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]118457-16-2[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=Calibri]9[/font][font=宋体],[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]920275-23-6[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=Calibri]C[/font][font=宋体](非对映体混合物),英文名为[/font][font=Calibri]Nebivolol Impurity C (Mixture of Diastereomers)[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=Calibri]B[/font][font=宋体],英文名为[/font][font=Calibri]Nebivolol impurity B[/font][font=宋体],[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]119365-25-2[/font][/font][font=宋体];[/font][font=宋体][font=宋体]去氟奈必洛尔,英文名为[/font][font=Calibri]Desfluoro Nebivolol[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=宋体]Ⅰ和奈必洛尔杂质Ⅱ等。[/font][/font][font=宋体][font=Calibri] CATO[/font][font=宋体]标准品提供的[/font][/font][b][font=宋体]奈必洛尔[/font][/b][font=宋体]全套的杂质[/font][font=宋体],[/font][font=宋体]这些杂质对于药物的纯度和稳定性研究至关重要,也是药物研发过程中不可或缺的一部分[/font][font=宋体]。[/font][img=,605,513]https://ng1.17img.cn/bbsfiles/images/2024/02/202402182153192686_9605_6381607_3.png!w605x513.jpg[/img][font=宋体][color=#05073b][back=#fdfdfe] 广州[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]佳途科技[/back][/color][/font][font=宋体][color=#05073b][back=#fdfdfe]股份有限公司[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]深知药物研发与质量控制的重要性[/back][/color][/font][font=宋体][font=宋体],[/font][font=Calibri]CATO[/font][font=宋体]标准品厂家,提供[/font][/font][b][font=宋体]奈必洛尔[/font][/b][font=宋体]全套[/font][font=宋体]的[/font][font=宋体]杂质,为客户提供更加精准、可靠的分析标准品,助力药物研发事业的快速发展[/font][font=宋体],[/font][font=宋体]以满足客户在药物研发和质量控制方面的需求。[/font]
1 整体框架结构GB2760-1996以及随后每年的增补品种仍然沿用1981年标准的格式,正文包括“范围”、“引用标准”、“食品添加剂品种、使用范围、最大使用量”三部分。由于对标准使用所做的解释和说明不够,往往使得食品和食品添加剂生产企业,甚至监督管理机构不能够完全正确地理解、执行。例如,某监督机构在对牛肉干制品抽检中检出微量苯甲酸就判定其产品违反GB2760规定,给予处罚,而没有充分考虑该添加剂的可能来源,如配料中使用了含苯甲酸的酱油,即没有考虑到“残留”原则而造成了错误判断。虽然这可能是由于标准的宣传贯彻不够,但客观上也说明了标准本身确实存在着缺陷,不能让标准执行者和监督管理者理解实施。CAC的GSFA则在前言中对术语定义、质量规格要求、残留原则、食品分类系统作了系统地解释、说明和要求。例如,在“进入食品中的食品添加剂残留物”章节,明确规定了食品添加剂可以因在食品配料中的残留而进入食品中的三种允许情况,很好地避免了上述问题。在列表格式方面,GB2760按照食品添加剂的功能分类排序,规定了每一种食品添加剂的使用范围和最大使用量。这种格式在七、八十年代,食品工业还不太发达,批准使用的食品添加剂范围相对狭窄的情况下是可以满足工作需要的,但是随着科学技术和食品工业的不断飞速发展,以及我国加入WTO和市场经济全球一体化进程的加速,食品添加剂使用标准的内容越来越庞杂。现有的格式在实际使用过程中存在着一些不便,例如:如果一种添加剂具有两种以上功能,就会在标准的不同段落出现,很容易查找不全 如果想查找某种食品中允许使用的食品添加剂情况,更是难上加难。GSFA的列表格式则有很多优点,表1按照食品添加剂的第一个英文字母排序,限定了每一种或一组食品添加剂允许使用的食品以及允许的最大用量,并在每种添加剂的名称后标注国际代码编号(1NS编号)和功能类别。表2与表l的资料内容相同,只不过是按照食品类别排序,便于查找。表3列出了“未规定ADI”的添加剂,当这些添加剂按照该标准前言中的良好生产规范(GMP)适量使用时,原则上可以允许在所有食品中使用。表3的附录列出了表3所不能适用的食品类别或个别食品,这些食品类别的添加剂的使用应遵循表1和表2的规定。2 食品添加剂功能类别GB2760中食品添加剂主要分为酸度调节剂、抗结剂、消泡剂、抗氧化剂、漂白剂、膨松剂、胶姆糖基础剂、着色剂、护色剂、乳化剂、酶制剂、增味剂、面粉处理剂、被膜剂、水分保持剂、营养强化剂、防腐剂、稳定和凝固剂、甜味剂、增稠剂、其他、香料共22类。GSFA将食品添加剂的功用分为酸、酸度调节剂、抗结剂、消泡剂、抗氧化剂、膨胀剂、着色剂、护色剂、乳化剂、乳化用盐、固化剂、增香剂、面粉处理剂、发泡剂、胶凝剂、被膜剂、保湿剂、防腐剂、推进剂、膨松剂、稳定剂、甜味剂、增稠剂共23类。两者的重要区别是GSFA明确指出为了保持或提高营养质量而添加的物质不包括在内,而GB2760中营养素强化剂属于其中非常重要的一大类。鉴于对营养强化剂所进行的危险性评估和标准化管理与一般的食品添加剂有所不同,建议在标准修订时,将营养强化剂的部分仍纳入GB14880之内单独修订。另外,我国与CAC对于酶制剂的管理方式也不尽相同,按照GB2760酶制剂均属食品添加剂,而GSFA是按照酶制剂的作用特点分成食品添加剂和加工助剂分别对待,这是我国应该借鉴的。3 食品添加剂品种截至2003年底,我国批准允许使用的食品添加剂近460种,其中包括120种营养素强化剂,不包括香料。目前,列入GSFA的添加剂约有370种。两者在数目上虽然相近,但在具体品种上有相当部分的差异。例如,我国允许使用的相当部分食品添加剂品种属于天然的动植物提取物,虽然有相当长时间的使用历史,但是质量规格资料较为贫乏,纯度不高或者质量不够稳定,安全性毒理学评价不够系统规范,很难为联合国粮农组织/世界卫生组织食品添加剂联合专家委员会(JECFA)所认可,自然也未被纳入GSFA。尽管经过多方努力,曾经有两种天然色素(红曲红、栀子黄)列入JECFA评价的优先名单,但是一直未能提交相关资料。甜菊糖苷也有类似问题,由于不能提供必要的质量规格资料,再次评估的时机被搁浅。JECFA的评价影响了世界上一部分国家和地区对食品添加剂的管理决策,这无形中给我国的食品添加剂工业造成了负面影响。另外,还有一部分添加剂品种的差异属于在国外或国际上已经使用多年,也在GSFA之列,但由于我国目前没有生产、使用商提出申请,也未进行暴露量评估而未纳入GB2760。对于这部分添加剂建议采取审慎态度,不宜急于采纳照搬。4 食品添加剂使用范围一食品分类GB2760没有明确的食品分类系统,对食品涵盖范围的限定不够清晰,没有给予必要的解释说明,给标准的实施执行带来一些困惑,尤其是当有些条款的规定与我国食品工业的产品分类不一致时更是如此。其次,使用范围过细和过粗的现象都有存在,例如“炸鸡调料”、“香橙果珍干粉”过细,“软饮料”过粗。另外,食品名称不规范、前后不一致的现象较多出现,如“生湿及干面条”和“生切面”的表述同时存在等等。此外,由于缺乏对食品类别的标准化编码,很难查找某种食品中食品添加剂的允许使用情况,这往往是添加剂使用和监督中最常遇到的困难。GSFA在食品分类方面提供了一个很好的模板,标准中的食品分类系统是食品添加剂使用时的定位工具。它是在欧共体食品饮料工业联盟制定的食品分类系统上修订而成的,适用于所有食品,包括那些不允许使用添加剂的食品。分为乳制品、脂肪,油和脂肪乳剂、可食冰、水果和蔬菜、糖果、谷物和谷物制品、焙烤制品、肉和肉制品、鱼和鱼制品、蛋和蛋制品、甜料、盐,调味料,汤,调味汁,沙拉,蛋白制品、特殊营养用食品、饮料、即食小食品以及复合食品品种共16大类,大类下又分若干小类,如04.1为水果,04.1.2为加工水果。需要说明的是如果允许一食品添加剂应用于一食品总类时,就理所当然地允许其应用于总类下面的所有亚类,除非另有规定。同样,如允许一添加剂应用于一亚类,也就允许其应用于该亚类下的所有次类的食品以及在此次类下所涉及的若干或个别食品。该食品分类系统简化和规范了对食品添加剂的使用规定,建议在GB2760修订时,参照GSFA食品分类系统的基本原则,分析目前GB2760涉及的食品类别品种,结合我国食品行业的有关分类,制定明确的食品分类系统框架和主要内容。5 使用规定GB2760和GSFA在使用限量规定上的差异主要表现在以下几个方面。首先,早年间GB2760的使用规定主要根据申报者提出的申请,采用危险性评估的程度不够,因此有些限量指标显得不够严谨、科学,例如规定碳酸氢钾在矿物质饮料中最大使用量为0.033g/L等。GSFA是将法典各产品标准中涉及添加剂的条款进行汇总,按照新的格式要求列入进来。同时,起草国还搜集了世界各国的几十万份数据,按照“一种添加剂如经过JECFA评价,且分别在两个国家或地区同时允许使用,便可将该产品收录”的原则,补充了新的内容,因此,它是一个相当庞杂的标准,相当部分内容不适用于我国的情况。建议在标准修订时采用危险性评估方法,结合我国消费人群的膳食暴露量以及食品中添加剂的监测数据,参考GSFA的相关内容做出规定。其次,GB2760规定某些添加剂品种可以“按生产需要适量使用”于“各类食品”,但忽略了对“各类食品”的限制,例如对于婴幼儿食品、牛乳、面粉等食品的必要限制,造成了管理上的漏洞。GSFA则将这类添加剂统一列表,规定可以按照生产需要适量使用,同时又以附件的形式列出了应该除外的食品类别和品种,从而很好地解决了这个问题。另外,对于结构、功能、安全性相同或类似的添加剂做出规定时,GB2760有时将其视为同一组添加剂统一规定,有时又分具体品种单独规定,显得凌乱。而GSFA通常将其作为一个品种规定其使用范围和最大限量,例如,GSFA在规定叶绿素铜盐类的使用时,将叶绿素铜钠盐和叶绿素铜钾盐作为一个品种规定,这样得以简化了制表的繁杂,便于使用。结语中国已经加入WTO,CAC标准对我国的食品工业发展和国际贸易将产生巨大的影响,它是目前和将来我国食品卫生国家标准制定、修订过程中的重要参考依据。因此,分析比较GB2760和GSFA的主要差异具有重要的意义。据悉,GB2760的修订工作已于今年年初启动,有关部门表示整个标准修订过程将本着科学、公开、透明的原则进行,广泛征求相关部门、行业、企业意见和建议,力争制定出既保护消费者健康又符合我国经济技术发展状况以及WTO相关要求的添加剂卫生标准。
氯吡格雷杂质是一种化学物质,它是氯吡格雷的同分异构体或相关化合物。氯吡格雷是一种血小板聚集抑制剂,用于预防和治疗动脉粥样硬化血栓形成事件。COTO标准品是一种高纯度的标准物质,用于测定氯吡格雷及其杂质的纯度、含量和化学性质。通过与COTO标准品进行对比和分析,可以确定氯吡格雷及其杂质的结构、组成和含量,从而保证氯吡格雷的质量和安全性。在药物研发和生产过程中,COTO标准品的使用非常重要。它可以提供可靠的参照物,用于质量控制、药物分析和化学计量学研究。通过使用COTO标准品,可以确保氯吡格雷及其杂质的准确性和可靠性,为药物的安全性和有效性提供保障。总的来说,COTO标准品在氯吡格雷杂质的研究和控制中具有重要作用。通过使用COTO标准品,可以更好地了解氯吡格雷及其杂质的性质和含量,从而确保药物的安全和有效性。同时,也需要加强生产过程中的管理和监督,加强质量标准和监管措施的执行力度,确保药物质量和安全。
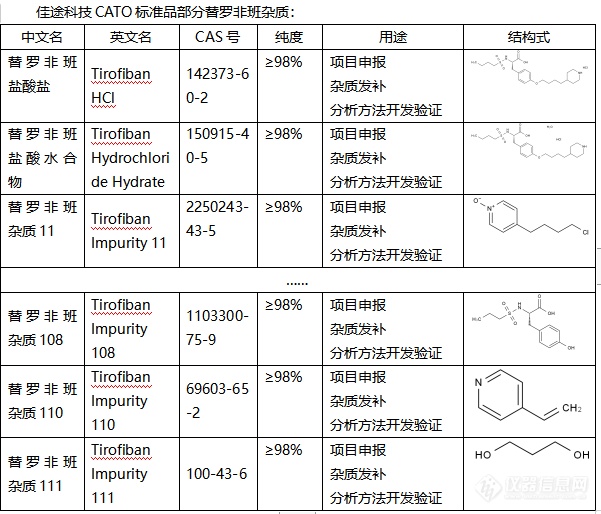
在当今的医疗领域,药物的质量控制至关重要,直接关系到患者的生命健康。替罗非班是一种广泛应用于心血管疾病治疗的药品,其质量控制尤为重要。而杂质分析作为药物质量控制的关键环节,能够准确评估药物的安全性和有效性。本文将重点探讨替罗非班杂质分析与CATO标准品应用研究的重要性。首先,杂质分析是确保药物质量的重要手段。在替罗非班的制备过程中,可能会产生一系列杂质,这些杂质的存在可能对药物的疗效和安全性产生不良影响。CATO标准品作为一种有效的分析工具,能够准确鉴定和量化替罗非班中的杂质,为药物的质量控制提供科学依据。其次,CATO标准品的应用有助于深入了解杂质的来源和性质。通过与标准品的比对分析,研究人员可以追溯杂质的产生途径,从而优化生产工艺,降低杂质的产生。此外,CATO标准品还可以用于评估杂质的毒性和风险,为药物的安全性评价提供有力支持。此外,CATO标准品在指导药物生产和改进方面也具有重要意义。通过对替罗非班中杂质的准确分析,生产商可以针对性地优化生产工艺、加强质量控制,从而提高药物的纯度和安全性。这不仅有助于保障患者的用药安全,还有助于提升企业的生产效益和市场竞争力。综上所述,替罗非班杂质分析与CATO标准品应用研究在药物质量控制中发挥着关键作用。通过深入研究替罗非班中的杂质,并借助CATO标准品这一强大工具,我们能够更好地了解杂质的来源、性质和影响,从而优化药物的生产工艺、提升药物的安全性和有效性。[img=,601,514]https://ng1.17img.cn/bbsfiles/images/2024/02/202402021849065001_3752_6381568_3.png!w601x514.jpg[/img]欢迎有需要的各位联系
卫生部在2011年第12号卫生部公告中发布了4项食品安全国家标准,其中之一即为《GB 2760-2011 食品安全国家标准 食品添加剂使用标准》(以下简称新标准),该新标准将于2011年6月20日起正式实施,新标准的前言中明确指出对2007版的《GB 2760-2007 食品添加剂使用卫生标准》(以下简称旧标准)部分食品分类系统进行了调整,为使广大网友对该新旧标准的食品分类系统的调整有更具体的了解,食品伙伴网对食品论坛中网友发布的相关讨论帖进行了整理,仅供行业人士参考,对比分析具体结果: 1、对比过程中发现如下问题: 和旧标准相比新标准的食品分类系统中删除了01.01.02.01调味乳,但搜索发现表A1里有涉及到该分类号。 2、新增了如下食品分类: 01.01.02 灭菌乳,同时将旧标准中的01.01.02 调制乳调整为01.01.03 调制乳。 01.02 发酵乳和风味发酵乳,同时将旧标准中的01.02 发酵乳调整为01.02.01. 01.02.02 风味发酵乳。同时删除了旧标准中的01.02.01、01.02.02. 04.04.03 其他豆制品。 06.05.02.04 粉圆。 13.02.01 婴幼儿谷类辅助食品、13.02.02 婴幼儿罐装辅助食品。 14.03.01.01 发酵型含乳饮料、14.03.01.02 配制型含乳饮料、14.03.01.03 乳酸菌饮料(旧标准中的分类号为14.07)、14.03.03 复合蛋白饮料。 3、调整了如下食品分类: 将旧标准中03.02雪糕类删除,在新标准中将其合并到03.01冰淇淋类。 将旧标准中如下分类删除05.02.03、05.02.04、05.02.05、05.02.06、05.02.07、05.02.08、05.02.08.01、05.02.08.02、05.02.09,合并到05.02.02. 旧标准中14.07乳酸菌饮料调整为新标准的14.03.01.03 乳酸菌饮料。 乳品的分类调整比较复杂,在其他几点中都有所涉及。 4、删除了如下食品分类: 04.02.02.03.01 酱渍的蔬菜、04.02.02.03.02 盐渍的蔬菜、04.02.02.03.03 糖醋渍的蔬菜、04.02.02.03.04 其他腌渍的蔬菜。 04.03.02.03.01酱渍的食用菌和藻类、04.03.02.03.02盐渍的食用菌和藻类、04.03.02.03.03糖醋渍的食用菌和藻类、04.03.02.03.04其他腌渍的食用菌和藻类。 06.03.01.03 蛋糕预拌粉、06.03.01.04 其他专用粉。 08.03.05.01 高温蒸煮肠、08.03.05.02 低温蒸煮肠、08.03.05.03 其他肉肠。 14.01.02 自然来源饮用水、14.01.04 饮用矿物质水。 16.05 油炸食品、16.05.01 油炸小食品、16.05.02 其他油炸食品。 01.02.01 原味发酵乳(全脂、部分脱脂、脱脂)、01.02.02 调味和果料发酵乳。 13.05.01 孕产妇(乳母)配方食品、13.05.02 运动营养食品(运动饮料除外)。
核心提示:GB2760-2011与GB2760-2007标准对比分析之四——可在各类食品中按生产需要适量使用的食品添加剂卫生部在2011年第12号卫生部公告中发布了4项食品安全国家标准,其中之一即为《GB 2760-2011 食品安全国家标准 食品添加剂使用标准》(以下简称新标准),该新标准将于2011年6月20日起正式实施,新标准的前言中明确指出对2007版的《GB 2760-2007 食品添加剂使用卫生标准》(以下简称旧标准)部分内容进行了调整,食品伙伴网已经对食品分类系统、食品工业用加工助剂和食品工业用酶制剂的调整分别进行了详细的对比,详细内容见GB2760-2011与GB2760-2007标准对比分析之一——食品分类系统、GB2760-2011与GB2760-2007标准对比分析之二——食品工业用加工助剂、GB2760-2011与GB2760-2007标准对比分析之三——食品用酶制剂,本次继续对可在各类食品中按生产需要适量使用的食品添加剂进行详细的对比分析,希望通过这样的系列对比分析,食品行业人士能够对新标准的使用有更深入的了解。 本次对比分析的总体情况:旧标准中列举可在各类食品中按生产需要适量使用的食品添加剂共71种,而新标准中列举了77种,经过对比发现旧标准中有两种可在各类食品中按生产需要适量使用的食品添加剂没有在新标准中收录。新标准中新增了8种。具体结果如下: 新标准中增加的可在各类食品中按生产需要适量使用的食品添加剂名单,共8种,分别是:冰乙酸(低压羰基化法)、赤藓糖醇、甲基纤维素、抗坏血酸钠、酶解大豆磷脂、羟丙基淀粉、碳酸钠、天然胡萝卜素。 新标准中删除的可在各类食品中按生产需要适量使用的食品添加剂名单,共2种,分别是:磷酸二氢钠、磷酸氢二钠。 除了新增和删除的情况之外,分析过程中还发现名称修改及功能新增的情况,列表如下: 添加剂名称修改的情况:
核心提示:GB2760-2011与GB2760-2007标准对比分析之一——食品分类系统卫生部在2011年第12号卫生部公告中发布了4项食品安全国家标准,其中之一即为《GB 2760-2011 食品安全国家标准 食品添加剂使用标准》(以下简称新标准),该新标准将于2011年6月20日起正式实施,新标准的前言中明确指出对2007版的《GB 2760-2007 食品添加剂使用卫生标准》(以下简称旧标准)部分食品分类系统进行了调整,为使广大网友对该新旧标准的食品分类系统的调整有更具体的了解,食品伙伴网对食品论坛中网友发布的相关讨论帖进行了整理,仅供行业人士参考,对比分析具体结果: 1、对比过程中发现如下问题:和旧标准相比新标准的食品分类系统中删除了01.01.02.01调味乳,但搜索发现表A1里有涉及到该分类号。 2、新增了如下食品分类:01.01.02 灭菌乳,同时将旧标准中的01.01.02 调制乳调整为01.01.03 调制乳。01.02 发酵乳和风味发酵乳,同时将旧标准中的01.02 发酵乳调整为01.02.01。01.02.02 风味发酵乳。同时删除了旧标准中的01.02.01、01.02.02。04.04.03 其他豆制品。06.05.02.04 粉圆。13.02.01 婴幼儿谷类辅助食品、13.02.02 婴幼儿罐装辅助食品。14.03.01.01 发酵型含乳饮料、14.03.01.02 配制型含乳饮料、14.03.01.03 乳酸菌饮料(旧标准中的分类号为14.07)、14.03.03 复合蛋白饮料。 3、调整了如下食品分类:将旧标准中03.02雪糕类删除,在新标准中将其合并到03.01冰淇淋类。将旧标准中如下分类删除05.02.03、05.02.04、05.02.05、05.02.06、05.02.07、05.02.08、05.02.08.01、05.02.08.02、05.02.09,合并到05.02.02。旧标准中14.07乳酸菌饮料调整为新标准的14.03.01.03 乳酸菌饮料。乳品的分类调整比较复杂,在其他几点中都有所涉及。 4、删除了如下食品分类:04.02.02.03.01 酱渍的蔬菜、04.02.02.03.02 盐渍的蔬菜、04.02.02.03.03 糖醋渍的蔬菜、04.02.02.03.04 其他腌渍的蔬菜。04.03.02.03.01酱渍的食用菌和藻类、04.03.02.03.02盐渍的食用菌和藻类、04.03.02.03.03糖醋渍的食用菌和藻类、04.03.02.03.04其他腌渍的食用菌和藻类。06.03.01.03 蛋糕预拌粉、06.03.01.04 其他专用粉。08.03.05.01 高温蒸煮肠、08.03.05.02 低温蒸煮肠、08.03.05.03 其他肉肠。14.01.02 自然来源饮用水、14.01.04 饮用矿物质水。16.05 油炸食品、16.05.01 油炸小食品、16.05.02 其他油炸食品。01.02.01 原味发酵乳(全脂、部分脱脂、脱脂)、01.02.02 调味和果料发酵乳。13.05.01 孕产妇(乳母)配方食品、13.05.02 运动营养食品(运动饮料除外)。 5、修改了如下食品分类名称:01.0 乳及乳制品(13.0 特殊营养用食品涉及品种除外)修改为乳及乳制品(13.0 特殊膳食用食品涉及品种除外)。01.01 乳及调制乳修改为巴氏杀菌乳、灭菌乳和调制乳。01.01.01 纯乳(全脂、部分脱脂、脱脂),包括复原乳修改为巴氏杀菌乳。01.03.01 乳粉(全脂奶粉、脱脂奶粉和部分脱脂奶粉)和奶油粉修改为乳粉和奶油粉04.04.01.01 豆腐类(北豆腐、南豆腐、内酯豆腐、冻豆腐)修改为豆腐类。04.05.02.01 烘焙/炒制坚果与籽类修改为熟制坚果与籽类。04.05.02.01.01带壳烘焙/炒制坚果与籽类修改为带壳熟制坚果与籽类。04.05.02.01.02脱壳烘焙/炒制坚果与籽类修改为脱壳熟制坚果与籽类。04.05.02.05 其他方法(如腌渍的果仁)修改为其他加工的坚果与籽类(如腌渍的果仁)。
2010年11月15日泰国发布通报,泰国食品药品管理局办公室公布拟制定作为食品成分的益生菌的使用标准。 本法规草案提议制定作为食品成分的益生菌的使用标准如下: –No. 1:益生菌不包括在公共卫生部通告附件1中公布的食品中禁止的微生物、细菌和酵母菌列表中; –No. 2:“益生菌”意指当以足够的数量控制时,将对宿主生物体具有有益作用的活的微生物,豁免的生物治疗剂、不在食品和转基因微生物中使用的有益微生物 “健康声明”意指涉及食品、食品成分或营养的,与健康直接和间接相关的声明或其它信息; –No. 3:益生菌作为食品成分应用应当经过泰国食品药品管理局的许可: 3.1除了应当论证安全使用的证据和遵循由泰国食品药品管理局发布的标准之外,益生菌作为食品成分应当按照附件II中所列; 3.2 含有益生菌的食品在储存和使用期间应当保持每克食物活力益生菌不少于1,000,000菌落; –No. 4:益生菌健康声明应当按照泰国食品药品管理局发布的标准; –No. 5:含有益生菌的食品应当依照下列各项标示: (1) 公共卫生部关于标签的通告 (2) 公共卫生部关于此类食品的通告 无论在什么情况下涉及健康声明,应当标示下列详细资料: –添加的益生菌的属、种类和菌株; –按照声明对消费者有益的数量和推荐的持续时间; –健康声明的综述; –使用和储存条件的说明; –提供给消费者的联系地址、电话号码或网址; –No. 6:含有益生菌的食品的包装应当按照公共卫生部关于包装的通告; –No.7:本通告应当在政府官方公报上公布日期后实施。
连日来,反式脂肪酸都处于舆论的风头浪尖。继央视报道市面上许多用到植物奶油的食品都含有对人体有一系列副作用的反式脂肪酸之后,卫生部开始针对反式脂肪酸展开风险监测评估。这一现象再次引发了消费者对食品安全的担忧。请关注—— 前不久,关于反式脂肪酸对健康有害的报道引起了社会的广泛关注,有媒体将它与杀虫剂DDT相媲美,并声称其为“食品史上的又一灾难”。反式脂肪酸连日来受到了社会各界的口诛笔伐,食品安全问题也再次引发了人们的担忧。 反式脂肪酸存在健康风险 不久前,央视报道市面上所销售的很多用到植物奶油(又称氢化油)的食品都含有反式脂肪酸,而反式脂肪酸对人体有一系列副作用,极有可能导致冠心病、糖尿病、肥胖等疾病高发的危害。 笔者走访北京许多超市发现,在饼干、蛋黄派、巧克力、沙拉酱等商品的成分表中,随处可见“氢化植物油”、“植物奶油”等字样,也就是说,这些食品中都含有反式脂肪酸。除此之外,各种美味的生日蛋糕、冰激凌等也都含有反式脂肪酸。 那么,反式脂肪酸到底有哪些危害呢? 据了解,反式脂肪酸其实是一种具有反式结构的不饱和脂肪酸,它是在液态植物油氢化过程中产生的。上世纪80年代,由于担心存在于荤油中的饱和脂肪酸可能会对心脏带来威胁,植物油又有高温不稳定及无法长时间储存等问题,科学家就利用氢化的过程,将液态植物油改变成固态,反式脂肪酸由此开始被人们广泛使用。 中国农业大学食品营养与工程学院教授李里特介绍说:“当时的植物油由于成本低及胆固醇含量少,故而很受欢迎。然而,近年来,随着科学家们的深入研究,发现这种反式脂肪酸的摄入竟然比胆固醇对人体的危害还大,从而引起了广泛关注。” “研究表明反式脂肪酸摄入量多时可升高低密度脂蛋白(坏胆固醇),降低高密度脂蛋白(好胆固醇),增加患动脉硬化和冠心病的危险,还会影响儿童生长发育和神经系统健康以及可能使患肥胖病,糖尿病等慢性病的几率增加。”中国营养学会主任医师高慧英指出。 我国缺乏食用标准 自反式脂肪酸被曝可能存在健康风险后,关于该不该使用含有大量反式脂肪酸的植物奶油成为社会热议的焦点。食物中含多少反式脂肪酸才在安全范围以内?每人每天摄入反式脂肪酸的量需要控制在多少范围内? 李里特表示:“目前国家还没有权威的文件出台,也没有设定相关标准。它对于人体的危害不是一蹴而就的,而是慢慢发展的,就好比香烟对于人体的危害一样,虽然没有人试验过摄入多少反式脂肪酸才
[font=SimSun, STSong, &]2024年3月12日,国家卫生健康委员会发布了《食品安全国家标准 食品添加剂使用标准》(GB 2760-2024),并将于2025年2月8日实施。食品伙伴网将2024版GB 2760与2014版及其纳入新版标准中的增补公告进行了比对分析,以下概述了2024版GB 2760较2014版的整体变化及各个附表的主要变化,供相关食品企业参考。[/font][font=SimSun, STSong, &]一、纳入了增补公告批准使用的添加剂[/font][font=SimSun, STSong, &]为了方便标准使用者查询,GB 2760-2024纳入了GB 2760-2014实施以来国家卫生健康委以公告形式批准使用的食品添加剂品种和使用规定,截至国家卫生健康委2023年第5号公告。[/font][font=SimSun, STSong, &]二、正文的修订情况[/font][font=SimSun, STSong, &](1)修订食品添加剂定义,在定义中增加了营养强化剂的内容,并明确营养强化剂的使用应符合《食品安全国家标准 食品营养强化剂使用标准》(GB14880)和相关规定。[/font][font=SimSun, STSong, &](2)修订INS和CNS定义,并明确说明当CAC的INS号发生变化时以CAC的INS号为准。[/font][font=SimSun, STSong, &](3)“4食品分类系统”的修改:删除“如允许某一食品添加剂应用于某一食品类别时,则允许其应用于该类别下的所有类别食品,另有规定的除外”内容,将其体现在附录A的A.3中。[/font][font=SimSun, STSong, &](4)增加了“8食品添加剂的功能类别”“9附录A中食品添加剂使用规定索引”“10营养强化剂”“11胶基糖果中基础剂物质”内容。[/font][font=SimSun, STSong, &]三、附录A的修订情况[/font][font=SimSun, STSong, &](1)修改附录A中食品添加剂使用规定的查询方式。将2014版标准中表A.3的内容体现到表A.1和表A.2中,原表A.2合并入表A.1。2024版标准中表A.2规定了表A.1中例外食品编号对应的食品类别。[/font][font=SimSun, STSong, &](2)修订食品添加剂的使用规定。进一步明确继承原则和完善相同色泽着色剂、防腐剂、抗氧化剂总和不超过1原则的描述,实质性要求未变化。[/font][font=SimSun, STSong, &]2024版标准规定“表A.1列出的食品添加剂按照规定的使用范围和最大使用量使用。如允许某一食品添加剂应用于某一食品类别时,则允许其应用于该类别下的所有类别食品,另有规定的除外。下级食品类别中与上级食品类别中对于同一食品添加剂的最大使用量规定不一致的,应遵守下级食品类别的规定”。[/font][font=SimSun, STSong, &]1、表A.1的修订情况[/font][font=SimSun, STSong, &](1)修订部分食品添加剂品种和/或使用规定。删除了落葵红、密蒙黄、酸枣色、2,4-二氯苯氧乙酸、海萝胶、偶氮甲酰胺;删除了罐头类食品中防腐剂的使用规定,涉及ε-聚赖氨酸盐酸盐、乳酸链球菌素、山梨酸及其钾盐、稳定态二氧化氯;删除食醋中冰乙酸、果蔬汁浆中纳他霉素、蒸馏酒中β-胡萝卜素和双乙酰酒石酸单双甘油酯、凉果类和话梅类中滑石粉、“16.07其他(发酵工艺)”中聚氧乙烯木糖醇酐单硬脂酸酯等的使用规定;[/font][font=SimSun, STSong, &](2)修改了部分食品添加剂的使用要求。增加了阿斯巴甜、安赛蜜与天门冬酰苯丙氨酸甲酯乙酰磺胺酸等在相同食品类别中共同使用时的总量要求;完善了饮料类别中液体饮料与相应的固体饮料食品添加剂使用的对应关系,修改备注为“以即饮状态计,相应的固体饮料按稀释倍数增加使用量”。修订了二氧化硫、脱氢乙酸及其钠盐等在部分食品类别中的使用规定;将原标准中归类为“其他类”的部分食品类别重新进行了归类,并调整了相应的食品添加剂使用规定等;[/font][font=SimSun, STSong, &](3)修改了部分食品添加剂的基本信息。例如修改了苯甲酸及其钠盐等食品添加剂的中文名称、中国编码(CNS号);爱德万甜等食品添加剂的英文名称和国际编码(INS号)等。[/font][font=SimSun, STSong, &]2、表A.2的修订情况[/font][font=SimSun, STSong, &]2024版表A.2为表A.1中例外食品编号对应的食品类别,相对于2014版GB2760的表A.3,其主要变化如下:[/font][font=SimSun, STSong, &](1)修订食品类别名称:如将“灭菌乳”修订为“灭菌乳和高温杀菌乳”,在该分类下增加了“高温杀菌乳”;将“白糖及白糖制品(如白砂糖、绵白糖、冰糖、方糖等)”修订为“白砂糖及白砂糖制品、绵白糖、红糖、冰片糖”,将原11.01.02 的红糖、冰片糖整合至11.01.01。删除了“等”字,说明除已在11.01.01名称中列明的,其他的全部转入11.01.02类别中的“其他糖”。[/font][font=SimSun, STSong, &](2)细分部分食品分类:如2014版“02.01(基本不含水的脂肪和油)”大类修改为02.01的细分类“02.01.01.01(植物油)、02.01.01.02(氢化植物油)、02.01.02(动物油脂(包括猪油、牛油.鱼油和其他动物脂肪等))、02.01.03(无水黄油、无水乳脂)”。[/font][font=SimSun, STSong, &]四、附录B的修订情况[/font][font=SimSun, STSong, &](1)修订食品用香料、香精使用原则。进一步明确具有其他食品添加剂功能或其他食品用途的食品用香料的使用要求,应配制成食品用香精用于食品加香。如:苯甲酸、肉桂醛、瓜拉纳提取物、双乙酸钠(又名二醋酸钠)、琥珀酸二钠、磷酸三钙、氨基酸类等。[/font][font=SimSun, STSong, &]1、表B.1的修订情况[/font][font=SimSun, STSong, &]2024版表B.1为不得添加食品用香料、香精的食品名单,相对于2014版GB 2760,其主要变化如下:[/font][font=SimSun, STSong, &](1)修订食品类别名称:将“灭菌乳”修订为“灭菌乳和高温杀菌乳”,在该分类下增加了“高温杀菌乳”;[/font][font=SimSun, STSong, &](2)新增食品分类:增加“13.02 婴幼儿辅助食品”类别,通过新增食品类别从而进一步明确禁止“婴幼儿辅助食品”使用香精香料。[/font][font=SimSun, STSong, &]2、表B.2、B.3的变化[/font][font=SimSun, STSong, &]修改完善了部分食品用香料品种。梳理了表B.2和表B.3的食品用香料名单,进行以下调整:[/font][font=SimSun, STSong, &](1)删除了多个香料品种。删除了枯茗油、葫芦巴、玫瑰茄、石榴果汁浓缩物、玉米穗丝、3-乙酰基-2,5-二甲基噻吩、氨基乙酸(羟基乙腈法)。其中,枯茗油、葫芦巴已为香辛料,玫瑰茄、石榴果汁浓缩物、玉米穗丝已为普通食品,3-乙酰基-2,5-二甲基噻吩行业已不再使用。[/font][font=SimSun, STSong, &](2)非洲竹芋提取物由合成香料调整为天然香料。[/font][font=SimSun, STSong, &](3)大茴香脑、根皮素由天然香料调整为合成香料。[/font][font=SimSun, STSong, &](4)多项香料修改或增加的中英文名称、FEMA编号、编码。例如:葡萄糖基甜菊糖苷、非洲竹芋提取物、6-甲基辛醛、香兰醇、4-癸烯酸等。[/font][font=SimSun, STSong, &]五、附录C的修订情况[/font][font=SimSun, STSong, &]1、表C.1、C2的修订情况[/font][font=SimSun, STSong, &]2024版表C.1为可在各类食品加工过程中使用,残留量不需限定的加工助剂名单(不含酶制剂),表C.2为需要规定功能和使用范围的加工助剂名单(不含酶制剂),相对于2014版GB 2760,其主要变化如下:[/font][font=SimSun, STSong, &](1)明确过氧化氢的使用范围。将过氧化氢从表C.1中删除,列入表 C.2,并规定其功能为“脱硫剂、脱色剂、去碘剂”,使用范围为“淀粉糖和淀粉加工工艺、油脂加工工艺、海藻加工工艺、胶原蛋白肠衣加工工艺、乳清粉和乳清蛋白粉的加工工艺”。[/font][font=SimSun, STSong, &](2)删除了1,2-二氯乙烷、矿物油、磷酸铵、抗坏血酸、抗坏血酸钠5个加工助剂品种。根据JECFA最新评估结果,同时参考美国、欧盟的规定,删除了1,2-二氯乙烷品种和使用规定。将矿物油使用规定与白油(液体石蜡)的使用规定进行整合。将磷酸铵使用规定与磷酸氢二铵和磷酸二氢铵进行整合。将抗坏血酸和抗坏血酸钠纳入附录A进行规定。[/font][font=SimSun, STSong, &](3)修订部分加工助剂的功能和使用范围。例如,删除了β-环状糊精用于巴氏杀菌乳、灭菌乳的规定;增加离子交换树脂用于糖处理工艺的规定;删除了白油(液体石蜡)功能中的“被膜剂”功能,增加了“防黏剂”功能。[/font][font=SimSun, STSong, &](4)统一规范了消泡剂的使用规定。删除了表A.1中丙二醇和吐温类中的消泡剂功能,在表 C.2 丙二醇的功能中增加消泡剂,删除了表A.1中吐温类用于豆类制品的使用规定,在表 C.2 中吐温类的使用范围中增加“豆类制品(最大使用量为0.05g/kg,最大使用量以每千克黄豆的使用量计)”。[/font][font=SimSun, STSong, &](5)修订部分加工助剂的中英文名称表述。例如,氮气修改为“氮气(液氮)”,6号轻汽油(植物油抽提溶剂)修改为“植物油抽提溶剂”,植物活性炭(稻壳活性炭)修改为“植物活性炭(稻壳来源)”。[/font][font=SimSun, STSong, &]2、表C.3的修订情况[/font][font=SimSun, STSong, &]2024版表C.3为食品用酶制剂及其来源名单,相对于2014版GB 2760,其主要变化如下:[/font][font=SimSun, STSong, &](1)新增1中酶制剂。新增“普鲁兰酶(Pullulanase),来源为李氏木霉Trichodermareesei,供体为Aspergillusnishimurae”。[/font][font=SimSun, STSong, &](2)删除1种酶制剂。删除了“溶血磷脂酶(磷脂酶B)Lysophospholipase (lecithinase B),来源为李氏木霉Trichoderma reesei,共体为Aspergillus nishimurae”。[/font][font=SimSun, STSong, &](3)修订部分酶制剂的中英文名称。例如,果糖基转移酶(又名β-果糖基转移酶)修改为“蔗糖1-果糖转移酶(又名果糖基转移酶 )”,纤维二糖酶修改为“β-葡萄糖苷酶(又名纤维二糖酶)”,果胶酯酶修改为“果胶酯酶(果胶甲基酯酶)”,葡糖异构酶修改为“葡糖异构酶(木糖异构酶)”。[/font][font=SimSun, STSong, &](4)修订部分酶制剂来源或供体名称、供体的描述。[/font][font=SimSun, STSong, &]六、附录D的修订情况[/font][font=SimSun, STSong, &](1)附录D中增加了营养强化剂的编号D.16,并根据GB 14880的规定增加了营养强化剂的定义。[/font][font=SimSun, STSong, &](2)根据GB 30616-2020中关于食品用香料的定义,将D.21食品用香料定义修改为“添加到食品产品中以产生香味、修饰香味或提高香味的物质”。[/font][font=SimSun, STSong, &]七、附录E的修订情况[/font][font=SimSun, STSong, &]为了使食品分类描述更加科学合理,进一步规范了部分食品类别的描述,表E.1的主要变化如下:[/font][font=SimSun, STSong, &]2024版表E.1为食品分类系统,相对于2014版GB 2760,其主要变化如下:[/font][font=SimSun, STSong, &](1)新增7个食品类别。在相关食品类别中增加兜底的其他类别,如06.03.02.06其他小麦粉制品(如面筋等)、06.05.02.05其他淀粉制品(如凉粉等)、06.12其他粮食制品、08.02.03肉丸类、08.02.04其他预制肉制品、12.10.03.05其他液体复合调味料;增加了16.05食品加工用菌种制剂(16.04除外)。[/font][font=SimSun, STSong, &](2)为与相关食品产品的食品安全国家标准保持协调一致,修改了部分食品类别。删除12.03.01酿造食醋、12.03.02配制食醋、12.04.01酿造酱油、12.04.02配制酱油、12.05.01酿造酱,将配制酱油和配制食醋归入12.10.03液体复合调味料;删除12.05.02配制酱,将其归入12.10.02 半固体复合调味料,并将大类12.05食品类别名称修改为“酿造酱”。并对相应的食品添加剂使用规定进行修改。[/font][font=SimSun, STSong, &](3)调整部分食品类别。例如:1.01分类中增加了“高温杀菌乳”;修改了蜜饯凉果的食品分类;调整食糖、调味酱的分类;删除半起泡葡萄酒食品分类;将原08.03.07.03 肉脯类调整至08.03.02“熏、烧、烤肉类(熏肉、叉烧肉、烤鸭、肉脯等);将09.02.03分类的名称由“冷冻鱼糜制品(包括鱼丸等)修改为“冷冻水产糜及其制品(包括冷冻丸类产品等)”;[/font][font=SimSun, STSong, &](4)修订部分食品分类号。将“面糊(如用于鱼和禽肉的拖面糊)、裹粉、煎炸粉”的食品分类号由“06.03.02.04”调整为“06.11”。[/font]
http://www.greenherbs.com.cn/bbs/dispbbs.asp?boardid=2&Id=7651724918 唑吡坦杂质A CIV Zolpidem Related Compound A CIV 对照品/标准品1724907 酒石酸唑吡坦 CIV Zolpidem Tartrate CIV 对照品/标准品1724893 唑吡坦 CIV Zolpidem CIV 对照品/标准品1724805 盐酸唑拉西泮 Zolazepam Hydrochloride 对照品/标准品1724769 硫酸锌 Zinc Sulfate 对照品/标准品1724747 氧化锌 Zinc Oxide 对照品/标准品1724689 齐留通杂质C Zileuton Related Compound C 对照品/标准品1724678 齐留通杂质B Zileuton Related Compound B 对照品/标准品1724667 齐留通杂质 A Zileuton Related Compound A 对照品/标准品1724656 齐留通 Zileuton 对照品/标准品1724532 齐多夫定杂质C(胸腺嘧啶) Zidovudine Related Compound C (thymine) 对照品/标准品1724521 齐多夫定杂质B Zidovudine Related Compound B 对照品/标准品1724500 齐多夫定 Zidovudine 对照品/标准品1724317 扎西他滨杂质A Zalcitabine Related Compound A 对照品/标准品1724306 扎西他滨 Zalcitabine 对照品/标准品1724000 盐酸育亨宾 Yohimbine Hydrochloride 对照品/标准品1722005 木糖 Xylose 对照品/标准品1721002 盐酸赛洛唑啉 Xylometazoline Hydrochloride 对照品/标准品1720600 木糖醇 Xylitol 对照品/标准品1720429 盐酸赛拉嗪 Xylazine Hydrochloride 对照品/标准品1720407 赛拉嗪 Xylazine 对照品/标准品1720203 呫吨酮 Xanthone 对照品/标准品1720000 呫吨酸 Xanthanoic Acid 对照品/标准品1719102 华法林杂质 A Warfarin Related Compound A 对照品/标准品1719000 华法林 Warfarin 对照品/标准品1717708 牡荆素(牡荆甙) Vitexin 对照品/标准品1717504 含量测定系统适用性用维生素D Vitamin D Assay System Suitability 对照品/标准品1716002 维生素A Vitamin A 对照品/标准品1715000 硫酸紫霉素 Viomycin Sulfate 对照品/标准品1714528 长春瑞滨杂质A Vinorelbine Related Compound A 对照品/标准品1714506 酒石酸长春瑞滨 Vinorelbine Tartrate 对照品/标准品1714007 硫酸长春新碱 Vincristine Sulfate 对照品/标准品1713004 硫酸长春碱 Vinblastine Sulfate 对照品/标准品1711508 阿糖腺苷 Vidarabine 对照品/标准品1711472 维替泊芬杂质A Verteporfin Related Compound A 对照品/标准品1711461 维替泊芬 Verteporfin 对照品/标准品1711440 维拉帕米杂质F Verapamil Related Compound F 对照品/标准品1711439 维拉帕米杂质E Verapamil Related Compound E 对照品/标准品1711428 维拉帕米杂质D Verapamil Related Compound D 对照品/标准品1711406 维拉帕米杂质B Verapamil Related Compound B 对照品/标准品1711304 维拉帕米杂质A Verapamil Related Compound A 对照品/标准品1711224 维库溴铵杂质F Vecuronium Bromide Related Compound F 对照品/标准品1711202 盐酸维拉帕米 Verapamil Hydrochloride 对照品/标准品1711188 维库溴铵杂质C Vecuronium Bromide Related Compound C 对照品/标准品1711177 维库溴铵杂质B Vecuronium Bromide Related Compound B 对照品/标准品1711166 维库溴铵杂质A Vecuronium Bromide Related Compound A 对照品/标准品1711155 维库溴铵 Vecuronium Bromide 对照品/标准品1711133 赖氨加压素 Lypressin 对照品/标准品1711100 加压素 Vasopressin 对照品/标准品1711009 香草醛熔点标准品 Vanillin Melting Point Standard 对照品/标准品1710006 香草醛 Vanillin 对照品/标准品1709018 Vancomycin B with Monodechlorovancomycin 对照品/标准品1709007 盐酸万古霉素 Vancomycin Hydrochloride 对照品/标准品1708795 缬沙坦杂质 C Valsartan Related Compound C 对照品/标准品1708784 缬沙坦杂质 B Valsartan Related Compound B 对照品/标准品1708773 缬沙坦杂质 A Valsartan Related Compound A 对照品/标准品1708762 缬沙坦 Valsartan 对照品/标准品1708751 戊柔比星分离度用混合物 Valrubicin Resolution Mixture 对照品/标准品1708730 戊柔比星 Valrubicin 对照品/标准品1708729 丙戊酸杂质A Valproic Acid Related Compound A 对照品/标准品1708718 丙戊酸杂质 B Valproic Acid Related Compound B 对照品/标准品1708707 丙戊酸 Valproic Acid 对照品/标准品1708503 L- 缬氨酸 L-Valine 对照品/标准品1708015 D-缬更昔洛韦 D-Valganciclovir 对照品/标准品1708004 缬更昔洛韦盐酸盐 Valganciclovir Hydrochloride 对照品/标准品1707908 缬草烯酸 Valerenic Acid 对照品/标准品1707894 万乃洛韦杂质G Valacyclovir Related Compound G 对照品/标准品1707883 万乃洛韦杂质F Valacyclovir Related Compound F 对照品/标准品1707872 万乃洛韦杂质E Valacyclovir Related Compound E 对照品/标准品1707861 万乃洛韦杂质D Valacyclovir Related Compound D 对照品/标准品1707855 万乃洛韦杂质C Valacyclovir Related Compound C 对照品/标准品1707839 盐酸万乃洛韦 Valacyclovir Hydrochloride 对照品/标准品1707806 熊去氧胆酸 Ursodiol 对照品/标准品1706701 C13尿素 Urea C 13 对照品/标准品1706698 尿素 Urea 对照品/标准品1706009 乌拉莫司汀 Uracil Mustard 对照品/标准品1705800 阿糖尿苷 Uracil Arabinoside 对照品/标准品1705505 十一烯酸 Undecylenic Acid 对照品/标准品1705323 泛癸利酮杂质A Ubidecarenone Related Compound A 对照品/标准品1705312 系统适用性试验用泛癸利酮 Ubidecarenone for System Suitability 对照品/标准品1705301 泛癸利酮 Ubidecarenone 对照品/标准品1705006 L- 酪氨酸 L-Tyrosine 对照品/标准品1704003 泰洛沙泊 Tyloxapol 对照品/标准品1703850 酒石酸泰洛星 Tylosin Tartrate 对照品/标准品1703805 泰洛星 Tylosin 对照品/标准品1702008 氯筒箭毒碱 Tuboc
食品微生物检测,菌落总数限量标准规定样品中蛋白质含量大于40%时,菌落总数限量为40000,如果是氨基酸含量大于40%是否适用于这一限量标准呢?(正常情况下的限量标准是1000)
[b]中华人民共和国农业行业标准-绿色食品兽药使用准则[/b]1、 范围 本标准规定了生产绿色食品允许使用的兽药种类、剂型、使用对象以及停药期以及禁止使用的兽药种类。 本标准适用于A级绿色食品的生产、管理和认定。 2、规范性引用文件 下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注明日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注明日期的引用文件,其最新版本适用于标准。 NY/T391绿色食品产地环境技术条件 中华人民共和国兽药典中国兽药典委员会 兽药质量标准中华人民共和国农业部 进口兽药质量标准中华人民共和国农业部 兽用生物制品质量标准中华人民共和国农业部 中华人民共和国动物防疫法中华人民共和国主席令 动物性食品中兽药最高残留限量中华人民共和国农业部 3、术语和定义 下列术语和定义适用于本标准。 3、1绿色食品 遵循可持续发展原则,按照特定生产方式生产,经专门机构认定,许可使用绿色食品标志的无污染的安全、优质、营养类食品。 3、2A级绿色食品 生产地的环境质量符合NY/T391的要求,生产过程中严格按照绿色食品生产资料使用准则和生产规程要求,限量使用限定的化学合成生产资料,产品质量符合绿色食品产品标准,经专门机构认定,许可使用A级绿色食品标志的产品。 3、3兽药 用于预防、治疗和诊断畜禽等动物疾病,有目的地调节其生理机能并规定作用、用途和用量的物质。包括:血清、菌(疫)苗、诊断液等生物物品;兽用的中药材、中成药、化学原料及其制剂;抗生素、生化药品、放射性药品。 3、3、1抗寄生虫药 能够杀灭或驱除体内、体外寄生虫的兽药,其中包括中药材、中药材、中成药、化学药品、抗生素及其制剂。 3、3、2抗菌药 能够抑制或杀死病原菌的兽药,其中包括中药材、中成药、化学药品、抗生素及其制剂。 3、3、3消毒防腐剂 用于抑制或杀灭环境中的有害微生物、防止疾病发生和传染的兽药。 3、3、4疫苗 由特定细菌、病毒、立克次体、螺旋体、支原体等微生物以及寄生虫制成的主动免疫制品。凡将特定细菌、病毒等微生物及寄生虫毒力致弱或采用异源毒制成的疫苗称活疫苗,用物理或化学方法将其灭活制成的疫苗称灭活疫苗。 3、4绿色食品生产资料 经专门机构认定,符合绿色食品生产要求,并正式推荐用于绿色食品生产的生产资料。 4、使用准则 绿色食品生产者应供给动物充足的营养,提供良好的饲养环境,加强饲养管理,采取各种措施以减少应激,增强支物自身的抗病力。应严格按《中华人民共和国动物防疫法》的规定防止畜禽发病和死亡,力争不用或少用药物。畜禽疾病以预防为主,建立严格的生物安全体系。必要时,进行预防、治疗和诊断疾病所用的兽药必须符合《中华人民共和国兽药典》、《兽药质量标准》、《兽用生物制品质量标准》和《进口兽药质量标准》有关规定。所用兽药必须来自具有生产许可证的生产企业,并且具有企业、行业或国家标准,产品批准文号;或者具有《进口兽药登记许可证》。所用兽药的标签必须遵守兽药标签和使用说明书管理规定。使用兽药时还应遵循以下原则: 4、1优先使用绿色食品生产资料的兽药产品。 4、2允许使用消毒防腐剂对饲养环境、厩舍和器具进行消毒,但不准对动物直接施用。不能使用酚类消毒剂。 4、3允许使用疫苗预防动物疾病。但是活疫苗应无外源病原污染,灭活疫苗的佐剂未被动物完全吸收前,该动物产品不能作为绿色食品。 4、4允许使用钙、磷、硒、钾等补充药,酸碱平衡药,体液补充药,电解质补充药,营养药,血容量补充药,抗贫血药,维生素类药,吸附药,泻药,润滑剂,酸化剂,局部止血药,收敛药和助消化药。 4、5允许使用附录A中的抗寄生虫药和抗菌药,使用中应注意以下几点: 4、5、1严格遵守规定的作用与用途、使用对象、使用途径、使用剂量、疗程和注意事项。 4、5、2停药期必须遵守附录A中规定的时间。 4、5、3产品中的兽药残留量应符合《动物性食品中兽药最高残留限量》规定。认证标准并抽检产品中的兽药残留量。 4、6建立并保持患病动物的治疗记录,包括患病家畜的畜号或其他标志、发病时间及症状、治疗用药的经过、治疗时间、疗程、所用药物的商品名称及主要成分。 4、7禁止使用有致畸、致癌、致突变作用的兽药。 4、8禁止在饲料中添加兽药。 4、9禁止使用激素类药品。 4、10禁止使用安眠镇静药,中枢兴奋药,镇痛药,解热镇痛药,麻酸药,肌肉松驰药,化学保定药,麻醉药,肌肉松驰药,化学保定药,巴比妥类药等用于调节神节神经系统机能的兽药。 4、11禁止使用基因工程兽药。
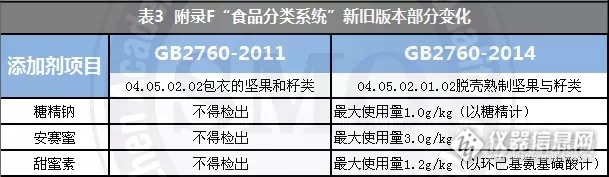
【标准解读】GB2760-2014《食品安全国家标准 食品添加剂使用标准》2014年12月31日国家卫计委发布了GB 2760-2014《食品安全国家标准 食品添加剂使用标准》,该标准将替代2011年版本并于2015年5月24日起实施。修订概况◆ 相比2011版,新版食品添加剂标准增补了原卫生部2010年16号公告至国家卫计委2014年17号公告的食品添加剂规定;◆ 将食品营养强化剂和胶基糖果中基础剂物质及其配料名单调整由其他相关标准进行规定;◆ 修改了3.4带入原则,增加了3.4.2条款;◆ 修改了附录A、B、C、D、F中的部分内容;◆ 增加“附录A中食品添加剂使用规定索引”。修订特点● 增强科学性:依据JECFA风险评估报告科学调整使用范围及用量;● 跟进行业发展:明确“预混料”这一添加剂发展新方向的使用;● 结合实际:对部分缺乏工艺必要性的食品添加剂使用规定进行修订,完善食品类别。部分主要修订内容1. 含铝食品添加剂使用规定调整2011年我国居民铝膳食暴露评估结果显示:面食含铝量最高,且面粉、馒头、油条对铝暴露量的贡献率最高,结合国际上含铝食品添加剂的使用规定和卫生部关于含铝食品添加剂征求意见的结果,对硫酸铝钾和硫酸铝铵的使用范围进行了调整;同时为减少膨化食品带来的儿童含铝食品添加剂的摄入量,删除7种合成着色剂铝色淀在膨化食品中的使用规定。(见下表1)http://ng1.17img.cn/bbsfiles/images/2015/02/201502101706_535191_1536848_3.jpg2. 梳理无工艺必要性的食品添加剂在新版标准修订过程中,根据行业调查发现2011版标准中有28种食品添加剂的34条规定没有工艺必要性,因此删除了这些规定。部分被删除的食品添加剂见表2。http://ng1.17img.cn/bbsfiles/images/2015/02/201502101707_535192_1536848_3.jpg3. “带入原则”中明确“预混料”中食品添加剂的使用新版标准3.4.2条指出:“当某食品配料作为特定终产品的原料时,批准用于上述特定终产品的添加剂允许添加到这些食品配料中,同时该添加剂在终产品中的量应符合本标准要求。在所述特定食品配料标签上映明确标示该食品配料用于上述特定食品的生产。”这类常见配料如:用于肉制品加工的复合调味料和裹粉、煎炸粉;用于糕点加工的蛋糕预拌粉。同是规定食品添加剂由食品原料带入食品终产品的情况,3.4.2与3.4.1条(即旧版3.4条)的区别是: ——3.4.1规定的是添加剂在食品原料中发挥工艺作用,随原料不可避免被带入终产品,在终产品不发挥工艺作用; ——3.4.2规定的是添加剂在食品原料中不发挥工艺作用,以食品原料为载体被加入终产品,在终产品中发挥工艺作用。举例:某植物油产品是某种蛋糕的配料,为方便蛋糕(终产品)生产,该植物油中添加了在蛋糕生产过程中起着色作用的β-胡萝卜素(脂溶性色素,在植物油中分散均匀,便于在蛋糕中使用)。根据GB2760-2014的规定,β-胡萝卜素不能在植物油中使用,但可作为着色剂在焙烤食品中食用,蛋糕属于焙烤食品,因此β-胡萝卜素可在蛋糕中使用,最大使用量为1.0g/kg。由此可判断,在该植物油中可添加β-胡萝卜素且在植物油中的添加量换算到蛋糕中时不超过1.0g/kg,该情况符合带入原则3.4.2.。同时,该植物油标签上应明确标示用于蛋糕生产。4. 表B.1“不得添加食品用香料、香精的食品名单”增加了食品类别“16.02.01茶叶、咖啡”。5. 表B.2“允许使用的食品用天然香料名单” ——八角茴香、牛至、甘草根、中国肉桂、丁香、众香子、莳萝籽已列入食品香辛料名单,属食品调味料,不宜作为香料品种,故在表中删除上述品种; ——规范部分香料名称,有的进行必要说明和完善,如“杭白菊油”修改为“杭白菊花油”;“茶树油”修改为“茶树油(又名互叶白千层油)”。6. 表C.1“可在各类食品加工过程中使用,残留量不需要限定的加工助剂名单(不含酶制剂)”增加了过氧化氢品种。7. 修订了附录F“食品分类系统”修订了46个食品类别,修订内容包括分类、分类依据、分类的具体描述等。其中值得一提的是,2011版中的“04.05.02.02包衣的坚果和籽类”(如鱼皮花生)在新版分类中被取消,将其涵盖在已有食品类别中,其可以使用的食品添加剂也相应发生改变(见表3)。http://ng1.17img.cn/bbsfiles/images/2015/02/201502101708_535193_1536848_3.jpg
食品中香料的使用将进一步得到规范。国际食品法典委员会近日通过的食品香料指南,通过了15种食品添加剂的近300条使用规定。该指南正式实施后,将指导和规范香料的使用。 食品香料使用指南对食品用香料物质、卫生要求、标签、香料质量规格标准等均做出了进一步规定。指南规定,香料的使用不应对消费者的健康带来危害。例如,供食品使用的香料应该达到一定的纯度规格。香料或香料中某些成分可能引起健康问题时,必须在危险性评估的基础上采取相应的危险性管理措施,如建立最大限量等。 香料虽只是名目繁多的食品添加剂里一种,但由于任何一种食品在生产中都要用到大量的食品香料以增加食品风味,有些单一产品使用香料的数量甚至多达千种,因此,从一定程度上讲,香料的安全使用是食品顺畅出口的有效“助推器”。各国纷纷收集香料的法规制定,使得其安全性日益凸显,其中欧盟、美国、日本等制定的有关香熏香料、天然香料的使用规定尤其受到关注。 食品香料指南的指导性意义在于使市场上香料的使用不再含混不清和随心所欲,在有法可依的前提下现实执行中仍将面临多重困难。自我国实施食品添加剂管理办法以来,对食品香料的管理均采取了与国际接轨的办法,但缺乏可操作性强和合理性的香精良好生产规范以及香料标签标准;且由于涉及配方保密和知识产权问题,现实中,食品标签上通常未标注有关信息或只注明“加有香料香精”这一空泛术语,致使企业在添加香料的过程中随意性过大,目前发现仍有部分出口企业还存在使用违禁香料的现象。 相关食品行业和生产出口企业应密切跟踪关注和研究香料国际标准的有关规定,有技术力量的企业还可积极参与国际标准的制定,以促进质量安全管理水平和国际标准的接轨。而对于香料的添加和使用,检验检疫部门提醒出口企业注意如下:从原料、生产环境、操作人员、设备等方面对香料的使用进行全程式监控。对于较常用的香兰素、麦芽酚以及简单的醇类、醛类、酸类和酯类等物质的使用上,要遵循适量。同时,对违禁香料的使用切忌掉以轻心,亟待改掉某些危害人体健康的香料使用上的随意性,在保证独具的产品风味的同时避免由于香料物质的滥用而给消费者健康带来危害。
食品安全无小事,人民健康是大事。食品安全治理是一项全国范围的规模工程,需要有一套总的安全标准体系从宏观上对食品安全行为作硬性的规定,以便对食品安全的标准、监管、惩处等各项要求有一个统一的参照。不过就如矛盾的普遍性寄存于特殊性一样,国家安全标准也需要通过地方安全标准去体现。 国家食品安全标准是食品安全工作的基础,不过由于全国各地的民俗风情、饮食习俗等地域差异,使得统一的安全标准将不可避免的因为差异而导致在某些特定领域产生标准的滞后性和监管空白区,安全标准的涉及范围和执行力度在某些特定领域或将减弱,标准、监管等要求很难做到位。 而地方根据自身情况制定相对应的安全标准则能有效地弥补此缺陷。地方对自身所在区域的情况了解充分,包括经济、文化、习俗、历史等各种因素。在国家标准安全体系内,因地制宜地量身制定标准,可以最大化做到“有的放矢”。 构建良性的食品安全标准体系尚任重道远,且在诸如监管、标准、信息追朔等方面也有待完善,但国家与地方双向同步安全标准体系建设却是基本框架。国家标准作总的纲领,地方标准作重要补充;国家标准普遍适用,地方标准则具体运用,且具强制执行唯一性。两者互相配合,彼此互补,可以使国家标准在执行的过程中通过地方有针对性的标准而得到有效实施,和严格具体的落实。
在做药品检测中,检验依据容易出现疑问。同一种药品,同一处方,出现两个或者两个以上的药品检验标准,我们使用那一个,请各位老师说出自己的高见,谢谢!!!例如:脑心舒口服液,一个标准是:卫生部颁药品标准(中药成方制剂第二十册);一个标准是:国家药品监督局颁布的,国家中成药标准汇编(经络肢体 脑系分册)。
标准品使用与管理注意事项(1) 新开瓶标准品药在瓶上注明开瓶日期,应根据瓶号依次来使用(整瓶使用或者送样情况除外),同一批号的标准品或工作对照品必须使用完一瓶后再开启另一瓶,标准品使用过程中,已取出的标准品严禁再放回原瓶中。(2) 标准品使用前从储藏室取出放入干燥器中平衡至室温,放置一定时间(视具体情况而定)后称量,是为了避免由于温度差导致的标准品吸潮,称量完成后立即用塑胶盖盖好后用封口膜封好,按瓶标签上的储存条件放置。(3) 同一瓶工作标准品的开启使用次数视具体情况而定,使用次数很少或具有吸湿性的工作对照品分装时应考虑一次性使用分装量。
对照品:用于鉴别、检查、含量测定和校正检定仪器性能的标准物质;对照品由国家药品检定机构审查认可,其标准应不低于制品的质量标准。 标准品:用于生物检定、抗生素或生物药品中含量或效价测定的标准物质,以效价单位(U)表示。 对照品与标准品概念不清?对照品与标准品是2个不同的概念,中国药典凡例中已有明确的定义:对照品系指用于鉴别、检查、含量测定和校正检定仪器性能的标准物质。标准品:用于生物检定、抗生素或生物药品中含量或效价测定的标准物质,以效价单位(U)表示。文献中常将2种概念混淆,认为对照品就是标准品,是1种物质2种提法而已,造成错误的原因,可能是有的药品既有对照品,又有标准品。 例如:当用微生物法测定头孢克罗效价时,用头孢克罗标准品,用HPLC或UV法测定时,则用对照品;非那西丁当用作熔点校准物质时,用熔点标准品,测定含量时,用对照品。即使是同一种物质的标准品和对照品,它们的规格、标定方法以及用途都可能是不同的。
在抗生素类的标准物质使用时,经常会遇到标准品和对照品的概念。关于这二者的区别,现在比较流行的说法是在做HPLC时使用的标准物质应为对照品。摘录典型观点如下:[B]“标准品都是按效价单位(或μg)计,以国际标准品进行标定。标准品的标示量是按生物活性来计算的,不是按纯度来标示,此种标示法对单组分或多组分物质均适用,尤适用于多组分物质,如乙酰螺旋霉素标准品,是由4种有效成分组成,若欲于一个纯度来标示其含量是不可能的,但用效价(即生物活性)来标示是可行的;对照品的标示量则必定是某单一组分的纯度指标。所以日常工作中,标准品和对照品在定量时是不可相互替代的。以罗红霉素为例,现今是国家标准品与对照品并存,以抗生素微生物检定法测其含量时,必须使用罗红霉素标准品;但以HPLC法测定其含量时,又必须使用罗红霉素对照品,不可混淆。”[/B]但是我见过一些行业标准,比方说HPLC测土霉素残留中,在说到标准液的配制时,写得就是“土霉素标准品”。难道这里面的“标准品”是“对照品”的错误用法?[em0716] 请大家发表一下看法
请问糠氨酸标准品哪里有卖?麻烦告知糠氨酸的中英文化学名以及结构式。谢谢!
标准品小常识之一 保存和运输1. 标准品常见的保存方法?(1)常温保存:通常用于化学性质比较稳定的标准品,建议保存于干燥阴凉的地方,必要时要避光保存。(2)+4℃冷藏:用于常温下不是很稳定的物质,保存于冰箱冷藏室。(3)-20℃冷冻:用于化学性质不稳定,常温下容易分解的物质,保存于-20 ℃冷冻室。(4)-80℃保存:一些具有生物活性的物质,需要保存于特定的-80℃的冰箱。2. 对于配制成溶液的标准品的保存?大部分的溶液标准物质都是冷藏避光贮存的,使用前于(20 ± 3℃)平衡,并摇动均匀。安瓿瓶一经打开,应立即使用,不可再次熔封后作为标准物质使用,也可选择一次性制备成中间标准储备溶液保存、使用。对于一些溶质溶解度低,溶液性质稳定的标准溶液,为防止低温下溶质析出,可放置于阴凉干燥的地方室温保存。3. 标准品的运输条件?相对于长期保存的条件,运输过程由于时间比较短,所以运输条件相对来说要求没有保存条件那么严格。合格的标准品都是经过短期稳定性检验的,短期稳定性检验的条件要比一般的运输条件苛刻。长期保存条件为常温和+4 ℃的标准品都可以在常温条件下运输,-20 ℃保存的标准品在运输时可以放入冰袋来降低温度,而-80 ℃保存的物质则需要在运输时加入干冰。但是干冰的有效时间只能维持1 天左右,所以这类型的物质不适合于长途运输。
[color=#333333]对照品与标准品概念[/color][color=#333333]对照品与标准品是2个不同的概念,中国药典凡例中已有明确的定义:对照品系指用于鉴别、检查、含量测定和校正检定仪器性能的标准物质,而标准品系指用于生物检定、抗生素或生物药品中含量或效价测定的标准物质,以效价单位(U)表示.文献中常将2种概念混淆,认为对照品就是标准品,是1种物质2种提法而已[1,2],造成错误的原因,可能是有的药品既有对照品,又有标准品.例如,当用微生物法测定头孢克罗效价时,用头孢克罗标准品,用HPLC或UV法测定时,则用对照品;非那西丁当用作熔点校准物质时,用熔点标准品,测定含量时,用对照品.即使是同一种物质的标准品和对照品,它们的规格、标定方法以及用途都可能是不同的.[/color]
近日,日本发布最新食品添加剂使用标准(2011年9月1日起生效)和指定食品添加剂名单(2011年9月5日起生效)。最新标准原文链接:Standards for Use -2011.9.1 食品添加剂使用标准List of Designated Additives-2011.9.5 指定的食品添加剂背景资料:日本的食品添加剂可分为“指定的食品添加剂”,“现存的食品添加剂”,“天然调味剂原料”和“通常作为食品也可作为食品添加剂的物质”。1)指定的食品添加剂。1947年,日本食品卫生法对添加剂实施主动列表制度,即只允许在食品中使用日本厚生省指定的认为安全的食品添加剂。在1995年之前,主动列表系统仅适用于化学合成的添加剂。在1995年,日本对食品卫生法进行修订,使该系统涵盖除个别豁免外的所有合成及非合成添加剂。指定的食品添加剂可分为有使用标准的食品添加剂及无使用标准的食品添加剂两类。不受主动列表系统约束的食品添加剂包括以下几类:2)现存的食品添加剂。1995年法规修订之前,已经在市场上销售或使用的不受主动列表系统约束的食品添加剂,均为非化学合成添加剂。1996年4月16日,日本后生省公布了现存食品添加剂清单。3)天然调味剂原料,不受主动列表系统约束;4)通常作为食品也可作为食品添加剂的物质。
光催化抗菌材料及制品抗菌性能的评价Photo-catalytic antimicrobial materials and products-Assessment for antimicrobial activity and efficacy 我现在只有国标,我需要一份其他相关的权威标准(美国等国家的标准)[em09501][em09501][em09511]非常感谢!!!yanxiali2009@yahoo.com.cn
综述了目前应用于纺织品抗菌测试的菌种种类及其性质,并介绍了目前常用的抗菌测试标准的要点、应用范围及其优缺点。抗菌纺织品的最重要的性能指标是抗菌性。测试抗菌性时,要求培养基浓度、温湿度、pH值及试验时间与穿衣条件相一致,实验仪器应为微生物实验常用仪器,且对任何形状的纺织材料都能测试。抗菌性的测试方法中,发展较早的是日本和美国,最有代表性且应用较广的是美国的AATCC试验法100和日本的工业标准。国内使用较多的评价方法一般都是参照AATCC(American Association of Textile Chemists andColorists,美国纺织染色家和化学家协会)标准和日本JAFET(日本纤维制品新功能协议会)批准的"SEK"标志认证标准的方法。我国于1992年颁布了纺织行业标准FZ/T01021-1992《织物抗菌性能试验方法》,1996年颁布了国家标准GB15979-2002《一次性使用卫生用品卫生标准》。但是抗菌性能评价的方法和标准还远末作到系统、统一、规范,尤其是抗菌纺织品的性能评价和产品规范在我国还有许多问题不明确,只能做到简单的定性检测。鉴于当前我国对抗菌纺织品的全面评价还不能适应国内生产和对外贸易的需要,本文对目前世界上使用较多的抗菌测试方法及标准进行了对比,