
如下图,这是磺胺类同分异构体的两个项目,母离子均为281,现在出现下面两个相连的两个峰,不知道这算是拖尾峰还是同分异构体的峰型?http://ng1.17img.cn/bbsfiles/images/2015/03/201503101707_537837_2452889_3.jpg
邻甲苯胺及其同分异构体的分离The Separation of O-Toluidine and Its isomers摘要:为了实现邻甲苯胺及其同分异构体的完全分离,首先,作者将邻甲苯胺及其同分异构体乙酰化,然后采用气相色谱-质谱联用方法,通过改进色谱条件,使其取得了完全分离。试验表明采用气-质联用方法可以实现邻甲苯胺及其同分异构体的完全分离。关键词:邻甲苯胺;分离;异构体;乙酰化Abstract: In order to achieve the complete separation of o-toluidine and its isomers, firstly, o-toluidine and its isomers were acetylation, and then the authors used gas chromatography-mass spectrometry methods, by improving the chromatographic conditions, so as to achieve their completely separation. The results showed that the gas-chromatography-mass spectrometry method can achieve the completely separation of o-toluidine and its isomers.Keywords: o-toluidine; separation; isomers; acetylation1 前言在禁用偶氮染料检测过程中,邻甲苯胺是经常被检出者之一。邻甲苯胺有两个同分异构体,分别是间甲苯胺和对甲苯胺。其中,邻甲苯胺属于禁用芳香胺,而间甲苯胺和对甲苯胺则不属于禁用芳香胺。三个化合物的沸点非常接近,分别为:邻甲苯胺(200±2℃)、间甲苯胺(203±3℃)、对甲苯胺(201±1℃)。而且三者的质谱图很相似,只是分子极性上略有差别,故造成在用气相色谱-质谱联用方法检测到邻甲苯胺时经常出现假阳性结果。如不采用薄层色谱、液相色谱等其它分析手段共同鉴别,是无法判断是否假阳性结果的。但是要排除假阳性结果,就需要重新寻找条件,而且更换仪器费时费力,且多数实验室不一定同时具备这些设备,这就给我们的日常检测工作带来了很多的麻烦和不便。本文作者结合自身知识和经验,对常见的邻甲苯胺及其异构体分离问题进行了研究。通过查阅相关资料,作者发现邻甲基乙酰苯胺(296℃)、间甲基乙酰苯胺(303℃)和对甲基乙酰苯胺(307℃)三者的沸点相差较大,所以作者首先通过试验将邻甲苯胺及其异构体分别乙酰化,然后通过改进色谱条件,使以上化合物达到了完全分离,提高了检测效率,减少了检测过程中的假阳性检出。 2 试验2.1 仪器与试剂气相色谱-质谱联用仪(GC-MS):Agilent 7890A/5975C,美国Agilent公司毛细管柱:DB-17MS柱(30m×0.25mm×0.25μm)叔丁基甲醚、乙酸酐、无水碳酸钠和无水碳酸钾均为分析纯 旋转蒸发仪 上海亚荣生化仪器厂邻甲苯胺及其同分异构体均为德国Dr.Ehrenstorfer公司。2.2 试剂配制标准品溶液:用叔丁基甲醚为溶剂,分别称取适量邻甲苯胺、间甲苯胺和对甲苯胺标准品配成合适浓度的单标溶液及混合溶液。碳酸钾溶液:0.1mol.L-1水溶液,取13.8g[font
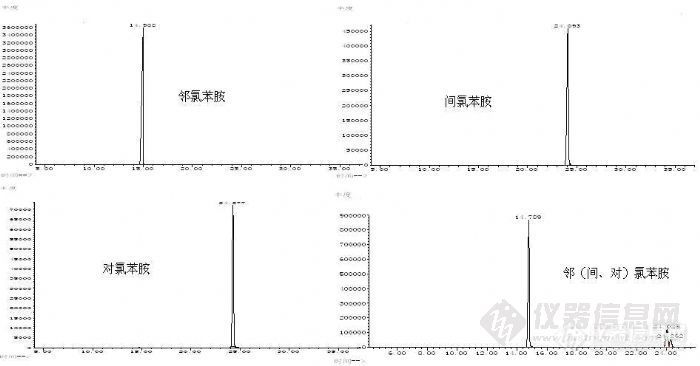
对氯苯胺及其同分异构体的分离对氯苯胺(106-47-8)为禁用芳香胺,而它的两种同分异构体间氯苯胺(108-42-9)、邻氯苯胺(91-51-2)则不是禁用芳香胺。如果仅仅靠GC-MSD无法确认该样品是否使用禁用偶氮染料,遇到这种情况时GB/T17592-2006推荐使用其他色谱手段对样品进行定性分析。如薄层色谱、液相色谱等,但这需要重新寻找条件,而且更换仪器费时费力,且多数实验室不一定同时具备这些设备。作者利用气相色谱-质谱联用方法(GC-MSD)对常见的对氯苯胺及其异构体分离进行了研究,通过改进色谱条件,使以上化合物达到很好的分离,减少了检测过程中的假阳性检出。1 实验部分4.3.1.1 仪器与试剂气相色谱-质谱联用仪(GC-MS):Agilent 7890A/5975C,美国Agilent公司毛细管柱:DB-17MS柱(30m×0.25mm×0.25μm)甲醇 色谱纯 美国Fisher公司旋转蒸发仪 上海亚荣生化仪器厂对氯苯胺及其同分异构体均为德国Dr.Ehrenstorfer公司。4.3.1.2 试剂配制用色谱纯级甲醇为溶剂,分别称取适量对氯苯胺、邻氯苯胺和间氯苯胺标准品配成合适浓度的混合溶液。4.3.1.3 仪器操作条件色谱柱:DB-17MS 30m×0.25mm×0.25μm;温度:进样口220℃ ;辅助器280℃;离子源230℃ ;四极杆温度:150℃;柱温:40℃保持2分钟,以20℃/分钟升温至100℃ ,保持25分钟,再以40℃/分钟升至280℃,保持0分钟;载气:He;流速:1.0mL/分钟;离子化方式:EI;质量扫描范围:35-350amu;进样方式:不分流进样;进样0.2μL。2 结果与讨论2.1 试验结果http://ng1.17img.cn/bbsfiles/images/2011/10/201110011241_320594_1606903_3.jpg虽然对氯苯胺及其异构体质谱图非常相似,但是由图4.3可以看出,在本实验条件下,对氯苯胺及其异构体无论是单标还是混标都实现了很好的分离。单标保留时间分别为:邻氯苯胺(14.988min);间氯苯胺(24.097min);对氯苯胺(24.277min)。混标保留时间分别为:邻氯苯胺(14.789min);间氯苯胺(24.029min);对氯苯胺(24.262min)。在混标样品中间氯苯胺和对氯苯胺虽然有部分峰是重叠的,未实现两者的基线分离,但是两者保留时间相差0.233min,基本上达到了有效分离,可以满足检测的要求。此外,如果样品遇到间氯苯胺和对氯苯胺异构体无法确认的时候,可以利用本文试验条件,通过向样品中加入一定量的间氯苯胺或对氯苯胺,观察样品加标前后哪个峰的面积显著增大,从而进一步确定该样品是否
禁用偶氮染料可分解致癌芳香胺同分异构体解析 摘要:国标GB 17592-2006 规定了24种禁止检出的致癌及可疑致癌芳香胺,这些芳香胺大多有同分异构体,某些同分异构体容易导致误判,本文较全面地解析这些同分异构体,为分析判断提供依据。关键词:致癌芳香胺,同分异构体,解析一:前言 某些使用或间接使用含致癌及可疑致癌芳香胺的有机染颜料的产品中,经还原分裂有部分会释放出这些有毒芳香胺,给人民身体健康带来危害,国外也已禁止此类产品的输入,这些有毒芳香胺及其同分异构体可能是生产这些染颜料的原料中带入的;也可能是从反应过程中发生的副反应带入;也可能在偶氮染料检测时产生。作为替代使用的途径之一,某些染颜料生产企业也可能使用这些致癌及可疑致癌芳香胺的同分异构体作重氮组分,生产出性能近似但不含此类芳香胺的合格产品。因此,对这些芳香胺的同分异构体作全面的解析以防误判就很必要。 在这些芳香胺的同分异构体中,化学性质近似,而物理性质有些相差较大,用保留时间与标样的对照即可分辨是否为可疑芳香胺,有些物理性质相似,保留时间接近,这就需要使用质谱提供的二维信息进行解析,质谱匹配差距大,就可判定不是标的物,质谱匹配度相近(≤3),由于存在干扰因素,匹配度最高的不一定是标的物,这就需要从其质谱特征离子峰的丰度甚至比例关系进行解析,判断某峰是否是可疑芳香胺及其同分异构体或是混合物,有时还要适当改变分析条件如衍生化等以使其分离,为进一步定性定量提供可能。二,致癌及可疑致癌芳香胺及其同分异构体解析 以下逐个对这些存在同分异构体的芳香胺进行解析。1:邻甲苯胺,分子式:C7H9N,分子量:107.07名称CAS#熔点℃沸点℃匹配度【1】邻甲苯胺000095-53-4α:-21β:-5.5199.797间甲苯胺000108-44-1-43.6203.394对甲苯胺000106-49-043-45200.594 邻甲苯胺与间甲苯胺及对甲苯胺间沸点差距较小,匹配度相近(≤3),因此从保留时间及匹配度上难以判断是何物。可用乙酰化方法分离,可使邻甲苯胺与对甲苯胺及间甲苯胺分离,邻甲基乙酰苯胺出峰时间早于对甲基乙酰苯胺或间甲基乙酰苯胺。2: 2,4-二甲基苯胺,2,6-二甲基苯胺,分子式:C8H11N,分子量:121.09名称CAS#熔点℃沸点[fon
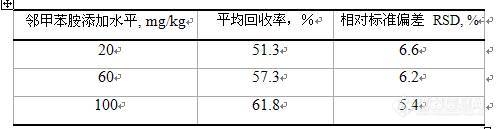
看见同行(看着这话题,绝对是同行,多交流)发着文章http://bbs.instrument.com.cn/shtml/20101012/2857370/,我这把手上的东西整整,算是补充吧。大家多多提意见吧!摘要 针对纺织品偶氮染料检验中常检出的禁用邻甲苯胺及其异构体,结合气相色谱-质谱和高效液相色谱-二极管阵列检测器(HPLC/DAD),摸索了以气相色谱-质谱进行初期定性筛选、以高效液相色谱进行确证和定量的芳香胺异构体检测方法,避免了检验中其异构体造成的假阳性检出。本方法在2 μg/mL~100 μg/mL浓度范围内线性关系良好,线性相关系数可达到0.9999;回收率为51%~62%。关键词 纺织品;检测;禁用邻甲苯胺;异构体1 前言采用气相色谱-质谱联用方法检测染料产品中24种有害芳香胺含量,按照现行国家标准中提供的气相色谱条件,会有多种异构体保留时间相同或非常接近,而且这些异构体的质谱图又非常相似,从而造成无法使用特征离子对其进行定性和定量,往往会形成假阳性结果的产生。当前针对有害芳香胺的气相色谱/质谱检测方法,大都采用非极性或极性较弱的色谱柱,如HP-5MS、DB-5MS、DB-35MS,这些色谱柱普遍存在的缺点是对常见的异构体不能很好的分离。有文献报道采用中等极性色谱柱DB - 17MS(固定相等同于50%苯甲基聚硅氧烷),对芳香胺异构体有一定的分离能力,但没能实现禁用芳香胺的基线分离,造成定量上的偏差。高效液相色谱法(HPLC)可同时测定多种芳香胺,在分离异构体上是强有力的确证方法,准确定性和定量,分析方法易于推广。本方法采用气相色谱-质谱联用对异构体进行初期定性筛选、以高效液相色谱进行确证并外标定量,对常检出的的禁用邻甲苯胺及其异构体检测进行了研究。本方法通过进一步摸索优化高效液相色谱条件,使邻甲苯胺及其异构体达到基线分离,有效避免了检测过程中的假阳性检出。2 实验材料与方法2.1 仪器和设备气相色谱/质谱联用仪:美国Agilent 公司7890A /5975 C,带自动进样器,四极杆质谱检测器;气相色谱柱:HP-5MS 5% Phenyl Methyl Silox,325 °C:30 m x 250 μ[size=
我检测的药物用HPLC检测的过程中出现两个峰,α异构体和β异构体,这个药物随着时间的变化α异构体和β异构体间发生转化,在做标准曲线的时候遇到了问题:怎样以两个峰面积和为纵坐标,浓度为横坐标做标准曲线呢?望高手不吝赐教,感谢!
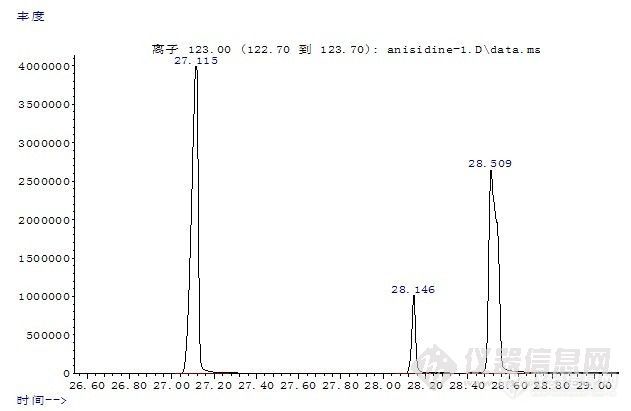
邻氨基苯甲醚同分异构体的分离摘要:为了实现邻氨基苯甲醚同分异构体的完全分离,作者采用气相色谱-质谱联用方法,通过改进色谱条件,使其取得了完全分离。试验表明采用气-质联用方法可以实现邻氨基苯甲醚同分异构体的完全分离。关键词:邻氨基苯甲醚;分离;异构体The Separation of O-Anisidine and Its isomersAbstract: In order to achieve the complete separation of o-anisidine and its isomers, the authors used gas chromatography - mass spectrometry methods, by improving the chromatographic conditions, so as to achieve their complete separation. The results showed that the gas-chromatography-mass spectrometry method can achieve the complete separationof o-anisidine and its isomers. Keywords: o-Anisidine; separation; isomers 1 前言采用气相色谱-质谱联用方法检测染料产品中23种有害芳香胺含量,按照现行国家标准GB/T17592-2006《纺织品禁用偶氮染料的测定》中提供的色谱条件,不但检测时间很长,而且大多数同分异构体保留时间相同或非常接近,同时这些异构体的质谱图又非常相似,从而造成无法使用特征离子对其进行定性和定量。如采用其它分析手段共同鉴别,如薄层色谱、液相色谱等,需要重新寻找条件,而且更换仪器费时费力,且多数实验室不一定同时具备这些设备。作者对芳香胺邻氨基苯甲醚及其异构体分离的问题进行了研究,其中,邻氨基苯甲醚属于有害芳香胺,而其同分异构体不属于有害芳香胺。作者通过改进色谱条件,使以上化合物达到很好的分离,提高了检测效率,减少了检测过程中的假阳性检出。2 试验2.1 仪器与试剂气相色谱-质谱联用仪(GC-MS):Agilent 7890A/5975C,美国Agilent公司毛细管柱:DB-17MS柱(30m×0.25mm×0.25μm)乙醚、硫酸亚铁等以上试剂均为分析纯;甲醇 色谱纯 美国Fisher公司旋转蒸发仪 上海亚荣生化仪器厂邻氨基苯甲醚及其同分异构体均为德国Dr.Ehrenstorfer公司。2.2 仪器操作条件色谱柱:DB一17MS 30m×0.25mm×0.25μm;温度:进样口220℃ ;辅助器280℃;离子源230℃ ;四极杆温度:150℃;柱温:40℃保持2分钟,以15℃/分钟升温至85℃ ,保持20分钟,再以30℃/分钟升至280℃,保持0分钟;载气:He;流速:1.0ml/分钟;离子化方式:EI;质量扫描范围:35—350;进样方式:不分流进样;进样0.2μL。2.3 执行标准试样处理按国标GB/T17592-2006执行。3 结果与讨论http://ng1.17img.cn/bbsfiles/images/2010/11/201011021932_256750_1604317_3.jpg图1 邻(间、对)氨基苯甲醚总离子流图由图1可以看出,邻氨基苯甲醚及其异构体在本实验条件下,可以得到很好的基线分离。保留时间分别为:邻氨基苯甲醚(27.115分钟);间氨基苯甲醚(28.509分钟);对氨基苯甲醚(28.146分钟)。在对染料产品中23种有害芳香胺含量的测定过程中,由于异构体的存在,并且多数异构体的质谱图很相似,如果保留时间相同,往往会形成假阳性结果的产生。当前针对有害芳香胺的气相色谱/质谱检测方法,大多采用非极性或极性较弱的色谱柱,如HP-5MS,DB-5MS,DB-35MS,这些色谱柱普遍存在的缺点是对常见的芳香胺异构体不能很好的分离。本方法通过使用中等极性色谱柱DB-17MS(固定相等同于50%苯甲基聚硅氧烷),同时使用三阶程序升温,很好的解决了这个问题。通过上面的数据与国标GB/T17592-

纺织品禁用偶氮染料测试--色谱柱条件优化区分同分异构体 摘要:本文介绍了纺织品禁用偶氮染料的测定经常遇到的同分异构体而导致的假阳性问题,重点介绍了邻甲苯胺和对氯苯胺2种,采用气质联用仪,对色谱柱条件优化来实现分离的方法,以及在试验过程中的一些经验、体会。关键词:偶氮染料;同分异构体;假阳性;色谱柱;检测一、前言偶氮染料是指染料分子结构中含有偶氮基( —N =N—) 的染料。这类染料具有色谱齐全、颜色鲜艳、色牢度较高、成本低等优点。目前全球有三分之二左右的合成染料属于偶氮染料, 估计约2000 个品种,年产量近60万吨。我国实施的国家强制性标准GB 18401—2010《国家纺织产品基本安全技术规范》中也将可分解芳香胺染料的检测作为其中重要的检测项目。GB/T 17952-2011中规定了纺织品中24种禁用偶氮染料。欧洲REACH法规No 1907/2006附件17中也列举了22种禁用芳香胺。而大多使用气质联用仪来检测。由于气相色谱- 质谱法(GC-MSD 法)是将色谱保留时间和质谱信息相结合进行定性, 因此对具有相同出峰时间和质谱图的同分异构体的鉴别存在一定局限性。本文重点列举了邻甲苯胺和对氯苯胺2种禁用芳香胺及其异构体的优化分离。二、试验部分2.1原理纺织样品在柠檬酸盐缓冲溶液介质中用连二亚硫酸钠还原分解以产生可能存在的禁用芳香胺,用适当的液-液分配柱提取溶液中的芳香胺,浓缩后,用合适的有机溶剂定容,用配有质量选择检测器的气相色谱仪(GC/MSD)进行测定。 必要时,选用另外一种或多种方法对异构体进行确认。用高效液相色谱-二极管阵列检测器(HPLC/DAD)或气象色谱-质谱仪进行定量。2.2 主要试剂及设备甲醇(色谱纯,定容或涤纶产品萃取后溶解转移)叔丁基甲醚(色谱纯,内标稀释液,过柱子提取液)无水乙醚(分析纯,过柱子提取液)氯苯(分析纯,涤纶产品抽提)柠檬酸盐缓冲液(分析纯)连二亚硫酸钠(分析纯)24种偶氮染料混标,300ppm(做定性定量标准曲线)三种内标标准品:萘-D8, 2,4,5-三氯苯胺,蒽-D10单标标准品:邻甲苯胺,间甲苯胺,对甲苯胺,对氯苯胺,邻氯苯胺,间氯苯胺。反应器,恒温水浴锅,硅藻土柱子,旋转蒸发器,气质联用仪http://ng1.17img.cn/bbsfiles/images/2015/07/201507091000_554536_2974654_3.pnghttp://ng1.17img.cn/bbsfiles/images/2015/07/201507091000_554537_2974654_3.pnghttp://ng1.17img.cn/bbsfiles/images/2015/07/201507091000_554538_2974654_3.pnghttp://ng1.17img.cn/bbsfiles/images/2015/07/201507091000_554539_2974654_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/07/201507091000_554540_2974654_3.pnghttp://ng1.17img.cn/bbsfiles/images/2015/07/201507091000_554535_2974654_3.png2.4 分析步骤2.3.1 取有代表性试样,剪成5mm×5mm的小片,混合。从混合样中称取1.0g,精确0.01g,置于反应器中,加入16mL预热到(70±2)℃的柠檬酸盐缓冲液,将反应器密闭,用力振荡,使所有试样浸于液体中,置于水浴中,并在(70±2)℃保温30min,使所有的织物充分润湿。然后,打开反应器,加入3.0mL连二亚硫酸钠溶液,并立即密闭振摇,使反应器再于(70±2)℃中保温30min,取出后2min内冷却到室温。2.3.2用玻璃棒挤压反应器中试样,将反应液全部倒入提取住内,任其吸附15min,用4×20mL乙醚分四次洗提反应器中的试样,每次需混合乙醚和试样,然后将乙醚洗液滗入提取住中,控制流速,收集乙醚提取液于圆底烧瓶中。2.3.3 将上述收集的盛有乙醚提取液的圆底烧瓶置于真空旋转蒸发器上,于35℃左右的低真空下浓缩至近1mL,再用缓氮气流驱除乙醚溶液,使其浓缩至近干。用1ml三内标液定容后转移至进样瓶中,上机测试。2.5 标准曲线2.5.1 GB/T 17592-2011的限量值为20 mg/kg,EN 14362.1-2012中的限量值为30mg/kg,故配制的标准品浓度应适宜。为了分析方便,将三种内标放在一起(简称三内标),内标物浓度也需合适。2.5.2 三内标浓度:10mg/l。300mg/L混标稀释梯度为3mg/l、6mg/l、15mg/l、30mg/l。标准曲线的建立是本试验的重要环节,从配制到建立做了完整的谱图。配制表见表1,上机曲线见图1-图5。 表1 禁用芳香胺标准曲线配制表nameCAS No.浓度/ppm 浓度/ppm浓度/ppm浓度/ppm浓度/ppmtoluidine95-53-4303.330.3315.1656.0663.0334-dimethylaniline95-68-1299.729.9714.9855.9942.9976-dimethylaniline87-62-7303.930.3915.1956.0783.039anisidine90-04-0300.230.0215.0106.0043.002chloroaniline106-47-8305.430.5415.2706.1083.054methoxy-5-methylaniline120-71-8301.230.1215.0606.0243.0124,5-trimethylaniline137-17-7299.729.9714.9855.9942.997chloro-2-methylaniline95-69-2300.530.0515.0256.0103.0054-diaminotoluene95-80-7300.730.0715.0356.014
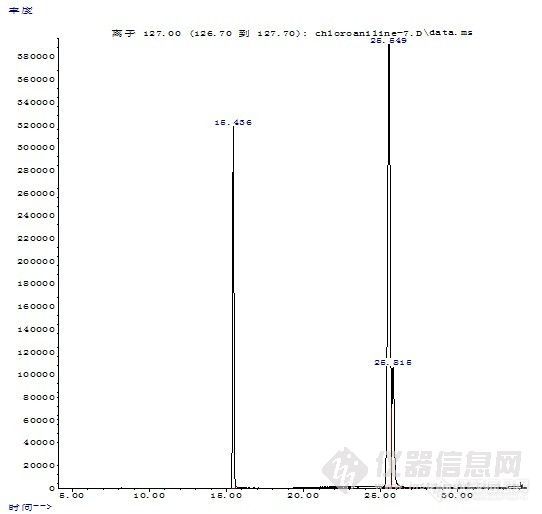
[font=宋体][size=2][size=2][1007][/size] [color=#f10b00]维权声明:本文为[/color][/size][url=http://bbs.instrument.com.cn/user.asp?username=dahua1981][color=#444444][size=2]dahua1981[/size][/color][/url][color=#fe2419][size=2]原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现的,均属侵权违法行为,我们将追究法律责任。[/size][/color][/font][size=3][font=宋体][b]对氯苯胺及其同分异构体的分离[/b][/font][/size][b][size=3][font=Times New Roman]The Separation of p-Chloroaniline and Its isomers[/font][/size][/b][size=3][font=Times New Roman][/font][/size][size=3][font=宋体]摘要:为了实现对氯苯胺同分异构体的完全分离,作者采用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url][/font][font=Times New Roman]-[/font][font=宋体]质谱联用方法,通过改进色谱条件,使其取得了较好分离。试验表明采用气[/font][font=Times New Roman]-[/font][font=宋体]质联用仪可以实现对氯苯胺同分异构体的较好分离。[/font][/size][size=3][font=宋体]关键词:氯苯胺;分离;异构体[/font][/size][font=Times New Roman][size=3][b]Abstract:[/b] [/size][back=white][size=2]In order to achieve the complete separation of [/size][/back][size=3]p-chloroaniline[/size][back=white][size=2] and its isomers, the authors used gas chromatography-mass spectrometry methods, by improving the chromatographic conditions, so as to achieve their better separation. The results showed that the gas-chromatography-mass spectrometry can achieve the better separation of [/size][/back][size=3]p-chloroaniline[/size][back=white] and its isomers.[/back][/back][/back][/back][/back][/back][/back][/back][/back][/back][/back][/back][/back][/back][/back][/font][size=3][font=Times New Roman][b]Keywords:[/b] p-chloroaniline separation isomers[/font][/size][size=3][font=Times New Roman][/font][/size][size=3][b][font=Times New Roman]1 [/font][font=宋体]前言[/font][/b][/size][size=3][font=宋体]目前,检测纺织品[/font][font=Times New Roman]24[/font][font=宋体]种禁用芳香胺一般采用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url][/font][font=Times New Roman]-[/font][font=宋体]质谱联用仪[/font][font=Times New Roman](GC-MSD)[/font][font=宋体],通过比较样品和标准品的出峰时间和质谱图,确认样品中是否含有禁用芳香胺,这种方法对于具有同分异构体的芳香胺具有一定的难度,原因在于有一部分禁用芳香胺的同分异构体在[/font][font=Times New Roman]GC-MSD[/font][font=宋体]上具有和禁用芳香胺同样的出峰时间和质谱图,而且这些芳香没有被列入禁用行列。比如,对氯苯胺[/font][font=Times New Roman](106-47-8)[/font][font=宋体]为禁用芳香胺,而它的两种同分异构体间氯苯胺[/font][font=Times New Roman](108-42-9)[/font][font=宋体]、邻氯苯胺[/font][font=Times New Roman](91-51-2)[/font][font=宋体]则不是禁用芳香胺。如果仅仅靠[/font][font=Times New Roman]GC-MSD[/font][font=宋体]无法确认该样品是否使用禁用偶氮染料,遇到这种情况时[/font][font=Times New Roman]GB/T17592-2006[/font][font=宋体]推荐使用其他色谱手段对样品进行定性分析。如薄层色谱、液相色谱等,但这需要重新寻找条件,而且更换仪器费时费力,且多数实验室不一定同时具备这些设备。作者利用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url][/font][font=Times New Roman]-[/font][font=宋体]质谱联用方法[/font][font=Times New Roman](GC-MSD)[/font][font=宋体]对常见的对氯苯胺及其异构体分离进行了研究,通过改进色谱条件,使以上化合物达到很好的分离,减少了检测过程中的假阳性检出。[/font][/size][size=3][b][font=Times New Roman]2 [/font][font=宋体]实验部分[/font][/b][/size][size=3][b][font=Times New Roman]2.1 [/font][font=宋体]仪器与试剂[/font][/b][/size][size=3][font=宋体][url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url][/font][font=Times New Roman]-[/font][font=宋体]质谱联用仪([/font][font=Times New Roman]GC-MS[/font][font=宋体]):[/font][font=Times New Roman]Agilent 7890A/5975C[/font][font=宋体],美国[/font][font=Times New Roman]Agilent[/font][font=宋体]公司[/font][/size][size=3][font=宋体]毛细管柱:[/font][font=Times New Roman]DB-17MS[/font][font=宋体]柱([/font][font=Times New Roman]30m×0.25mm×0.25μm[/font][font=宋体])[/font][/size][size=3][font=宋体]甲醇[/font][font=Times New Roman] [/font][font=宋体]色谱纯[/font][font=Times New Roman] [/font][font=宋体]美国[/font][font=Times New Roman]Fisher[/font][font=宋体]公司[/font][/size][size=3][font=宋体]旋转蒸发仪[/font][font=Times New Roman] [/font][font=宋体]上海亚荣生化仪器厂[/font][/size][size=3][font=宋体]对氯苯胺及其同分异构体均为德国[/font][font=Times New Roman]Dr.Ehrenstorfer[/font][font=宋体]公司。[/font][/size][size=3][b][font=Times New Roman]2.2 [/font][font=宋体]试剂配制[/font][/b][/size][size=3][font=Times New Roman] [/font][font=宋体]用色谱纯级甲醇为溶剂,分别称取适量[/font][font=宋体]对氯苯胺、邻氯苯胺[/font][font=宋体]和[/font][font=宋体]间氯苯胺[/font][font=宋体]标准品配成合适浓度的混合溶液。[/font][/size][size=3][b][font=Times New Roman]2.3 [/font][font=宋体]仪器操作条件[/font][/b][/size][size=3][font=宋体]色谱柱:[/font][font=Times New Roman]DB[/font][font=宋体]一[/font][font=Times New Roman]17MS 30m×0.25mm×0.25μm[/font][font=宋体];温度:进样口[/font][font=Times New Roman]220[/font][font=宋体]℃[/font][font=Times New Roman] [/font][font=宋体];辅助器[/font][font=Times New Roman]280[/font][font=宋体]℃[/font][font=宋体];离子源[/font][font=Times New Roman]230[/font][font=宋体]℃[/font][font=Times New Roman] [/font][font=宋体];四极杆温度:[/font][font=Times New Roman]150[/font][font=宋体]℃[/font][font=宋体];柱温:[/font][font=Times New Roman]40[/font][font=宋体]℃[/font][font=宋体]保持[/font][font=Times New Roman]2[/font][font=宋体]分钟,以[/font][font=Times New Roman]20[/font][font=宋体]℃[/font][font=宋体]/分钟升温至[/font][font=Times New Roman]100[/font][font=宋体]℃[/font][font=Times New Roman] [/font][font=宋体],保持[/font][font=Times New Roman]25[/font][font=宋体]分钟,再以[/font][font=Times New Roman]40[/font][font=宋体]℃[/font][font=宋体]/分钟升至[/font][font=Times New Roman]280[/font][font=宋体]℃[/font][font=宋体],保持[/font][font=Times New Roman]0[/font][font=宋体]分钟;载气:[/font][font=Times New Roman]He[/font][font=宋体];流速:[/font][font=Times New Roman]1.0ml/[/font][font=宋体]分钟;离子化方式:[/font][font=Times New Roman]EI[/font][font=宋体];质量扫描范围:[/font][font=Times New Roman]35-350[/font][font=宋体];进样方式:不分流进样;进样[/font][font=Times New Roman]0.2μ L[/font][font=宋体]。[/font][/size][size=3][b][font=Times New Roman]3 [/font][font=宋体]结果与讨论[/font][/b][/size][size=3][b][font=Times New Roman]3.1 [/font][font=宋体]试验结果[/font][/b][/size][size=3][b][font=宋体]([/font][font=Times New Roman]1[/font][font=宋体])[/font][font=宋体]邻[/font][font=Times New Roman]([/font][font=宋体]间、对[/font][font=Times New Roman])[/font][font=宋体]氯苯胺总离子流图[/font][/b][/size][align=center][img]http://ng1.17img.cn/bbsfiles/images/2010/10/201010131431_251266_1604317_3.jpg[/img][/align][align=center][size=3][/size][/align][align=center][size=3][font=宋体]图[/font][font=Times New Roman]1 [/font][font=宋体]邻[/font][font=Times New Roman]([/font][font=宋体]间、对[/font][font=Times New Roman])[/font][font=宋体]氯苯胺总离子流图[/font][/size][/align][size=3][font=宋体]虽然对氯苯胺及其异构体质谱图非常相似,但是由图[/font][font=Times New Roman]1[/font][font=宋体]可以看出,在本实验条件下,对氯苯胺及其异构体实现了很好的分离。保留时间分别为:对氯苯胺[/font][font=Times New Roman](25.815min)[/font][font=宋体];间氯苯胺[/font][font=Times New Roman](25.549min)[/font][font=宋体];邻氯苯胺[/font][font=Times New Roman](15.436min)[/font][font=宋体]。间氯苯胺和对氯苯胺虽然有部分峰是重叠的,未实现两者的基线分离,但是两者保留时间相差[/font][font=Times New Roman]0.266min[/font][font=宋体],基本上达到了有效分离,可以满足检测的要求。此外,如果样品遇到间氯苯胺和对氯苯胺异构体无法确认的时候,可以利用本文试验条件,通过向样品中加入一定量的间氯苯胺或对氯苯胺,观察样品加标前后哪个峰的面积显著增大,从而进一步确定该样品是否是假阳性检出。[/font][/size][size=3][b][font=宋体]([/font][font=Times New Roman]2[/font][font=宋体])[/font][font=宋体]邻氯苯胺的峰纯度[/font][/b][/size][align=center][img]http://ng1.17img.cn/bbsfiles/images/2010/10/201010131432_251267_1604317_3.jpg[/img][/align][align=center][size=3][/size][/align][align=center][size=3][font=宋体]图[/font][font=Times New Roman]2 [/font][font=宋体]邻氯苯胺的峰纯度及其标准质谱图[/font][/size][/align][size=3][font=宋体]由图[/font][font=Times New Roman]2[/font][font=宋体]可知,在该实验条件下,[/font][font=宋体]邻氯苯胺[/font][font=宋体]的保留时间为[/font][font=Times New Roman]15.436min[/font][font=宋体],[/font][font=宋体]峰对称性很好,且该峰处共有四个离子,与邻氯苯胺的标准质谱图一致。其中,离子[/font][font=Times New Roman]127[/font][font=宋体]和[/font][font=Times New Roman]129[/font][font=宋体]为邻氯苯胺的分子离子及其同位素离子,离子[/font][font=Times New Roman]92[/font][font=宋体]为邻氯苯胺失掉一个氯原子后生成的,而离子[/font][font=Times New Roman]65[/font][font=宋体]为苯环裂解为五圆环后生成的。这说明在该实验条件下,邻氯苯胺峰没有干扰离子。[/font][/size][size=3][b][font=宋体]([/font][font=Times New Roman]3[/font][font=宋体])[/font][font=Times New Roman] [/font][font=宋体]间氯苯胺的峰纯度[/font][/b][/size][align=center][img]http://ng1.17img.cn/bbsfiles/images/2010/10/201010131432_251268_1604317_3.jpg[/img][/align][align=center][size=3][/size][/align][align=center][size=3][font=宋体]图[/font][font=Times New Roman]3 [/font][font=宋体]间氯苯胺的峰纯度及其标准质谱图[/font][/size][/align][size=3][font=宋体]由图[/font][font=Times New Roman]3[/font][font=宋体]可知,在该实验条件下,[/font][font=宋体]间氯苯胺[/font][font=宋体]的保留时间为[/font][font=Times New Roman]25.549min[/font][font=宋体],[/font][font=宋体]峰对称性很好,且该峰处也有[/font][font=Times New Roman]129[/font][font=宋体]、[/font][font=Times New Roman]127[/font][font=宋体]、[/font][font=Times New Roman]92[/font][font=宋体]、[/font][font=Times New Roman]65[/font][font=宋体]四个离子,与间氯苯胺的标准质谱图一致。这说明在该实验条件下,间氯苯胺峰没有其它干扰离子。[/font][/size][size=3][b][font=宋体]([/font][font=Times New Roman]4[/font][font=宋体])[/font][font=Times New Roman] [/font][font=宋体]对氯苯胺的峰纯度[/font][/b][/size][align=center][img]http://ng1.17img.cn/bbsfiles/images/2010/10/201010131433_251269_1604317_3.jpg[/img][/align][align=center][size=3][/size][/align][align=center][size=3][font=宋体]图[/font][font=Times New Roman]4 [/font][font=宋体]对氯苯胺的峰纯度及其标准质谱图[/font][/size][/align][size=3][font=宋体]由图[/font][font=Times New Roman]4[/font][font=宋体]可知,在该实验条件下,[/font][font=宋体]对氯苯胺[/font][font=宋体]的保留时间为[/font][font=Times New Roman]25.815min[/font][font=宋体],峰对称性很好,且该峰处也只有[/font][font=Times New Roman]129[/font][font=宋体]、[/font][font=Times New Roman]127[/font][font=宋体]、[/font][font=Times New Roman]92[/font][font=宋体]、[/font][font=Times New Roman]65[/font][font=宋体]四个离子,与对氯苯胺的标准质谱图一致。虽然对氯苯胺峰与间氯苯胺峰没有实现基线完全的分离,但是可以通过向样品萃取液中添加单标的方法来进一步排除异构体,从而减少假阳性结果的产生。[/font][/size][size=3][font=宋体]总之,通过对上面图[/font][font=Times New Roman]2[/font][font=宋体]、图[/font][font=Times New Roman]3[/font][font=宋体]和图[/font][font=Times New Roman]4[/font][font=宋体]的分析,可以看出三个化合物的峰纯度都很高,可以满足检测要求。[/font][/size][size=3][b][font=Times New Roman]3.2 [/font][font=宋体]讨论[/font][/b][/size][size=3][font=宋体]在国家强制标准[/font][font=Times New Roman]GB18401-2003[/font][font=宋体]附录[/font][font=Times New Roman]C[/font][font=宋体]所列的还原条件下染料中不允许分解出的[/font][font=Times New Roman]24[/font][font=宋体]种芳香胺中,有些芳香胺存在异构体,且多数异构体的质谱图很相似,只是离子丰度比有所差异。如果检测过程中,色谱条件选择不合适的话,它们保留时间也会相同,进而出现异构体共流出的情况,这时往往会导致假阳性结果的产生。当前针对有害芳香胺的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url][/font][font=Times New Roman]/[/font][font=宋体]质谱检测方法,大多采用非极性或极性较弱的色谱柱[/font][sup][font=Times New Roman][1-4][/font][/sup][font=宋体],如[/font][font=Times New Roman]HP-5MS[/font][font=宋体]、[/font][font=Times New Roman]DB-5MS[/font][font=宋体],这些色谱柱普遍存在的缺点是对常见的芳香胺异构体不能很好的分离。针对这个问题,本文使用中等极性色谱柱[/font][font=Times New Roman]DB-17MS([/font][font=宋体]固定相等同于[/font][font=Times New Roman]50[/font][font=宋体]%苯甲基聚硅氧烷[/font][font=Times New Roman])[/font][font=宋体],通过对柱温等条件的优化以使异构体得到有效分离。[/font][/size][size=3][font=宋体]在色谱分析中,柱温是一个重要的操作变数,直接影响分离效能和分析速度。柱温对组分分离的影响较大,提高柱温使各组分的挥发靠拢,不利于分离,所以,从分离的角度考虑,宜采用较低的柱温。但柱温太低,被测组分在两相中的扩散速率大为减小,分配不能迅速达到平衡,峰形变宽,柱效下降,并延长了分析时间。选择的原则是:在使最难分离的组分能尽可能好的分离的前提下,尽可能采取较低的柱温,但以保留时间适宜,峰形不拖尾为度。具体操作条件的选择应根据不同的实际情况而定。[/font][/size][size=3][font=宋体]目前,用于极性相近化和物的分析通常采用程序升温,即柱温按预定的加热速度,随时间作线性或非线性的增加。升温的速度一般常是呈线性的,即单位时间内温度上升的速度是恒定的,例如每分钟[/font][font=Times New Roman]2[/font][font=宋体]℃[/font][font=宋体]、[/font][font=Times New Roman]4[/font][font=宋体]℃[/font][font=宋体]、[/font][font=Times New Roman]6[/font][font=宋体]℃[/font][font=宋体]等等。[/font][font=宋体]在较低初始温度,沸点较低的组分,即最早流出的峰可以得到良好的分离。随柱温增加,较高沸点的组分也能较快的流出,并和低沸点组分一样也能得到分离良好的尖峰。[/font][font=Arial][/font][/size][size=3][font=宋体]通过前面的试验结果可以看出,本方法通过使用中等极性色谱柱[/font][font=Times New Roman]DB-17MS[/font][font=宋体],同时使用三阶程序升温,很好的解决了对氯苯胺异构体的分离问题。该方法只需要使用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url][/font][font=Times New Roman]-[/font][font=宋体]质谱联用仪[/font][font=Times New Roman](GC-MSD)[/font][font=宋体],结合程序升温,而不必再通过其它仪器或手段来作异构体确认,缩短了检测时间,提高了检测的效率。作者通过大量的试验证明,该方法快速、精确、重现性和稳定性好,具有很高的可行性和可靠性。[/font][font=Arial][/font][/size][size=3][b][font=Times New Roman]4 [/font][font=宋体]结论[/font][/b][/size][size=3][b][font=Times New Roman] [/font][/b][font=宋体]由前文分析可以得出如下结论:[/font][/size][size=3][font=Times New Roman]a) [/font][font=宋体]该方法实现了对氯苯胺异构体的分离,因此可以不必再用其它手段或方法做异构体的确认,也在一定程度上提高了检测效率,节约了检测成本。[/font][/size][size=3][font=Times New Roman]b)[/font][font=宋体]该方法快速、精确、重现性和稳定性好,具有很高的可行性和可靠性。[/font][/size][size=3][font=宋体]但是该方法还不能使对氯苯胺和间氯苯胺实现完全的基线分离,需要今后做进一步的研究。总之,该方法具有很好的推广和应用价值。[/font][/size][size=3][font=Times New Roman][/font][/size][size=3][font=宋体]参考文献[/font][/size][size=3][font=Times New Roman][1] GB19601-2004,[/font][font=宋体]《染料产品中[/font][font=Times New Roman]23[/font][font=宋体]中有害芳香胺的限量及测定》[/font][font=Times New Roman][s].[/s][/font][/size][size=3][font=Times New Roman][2] [/font][font=宋体]杨继生,徐逸云,蒋华[/font][font=Times New Roman].[/font][font=宋体]对纺织品禁用偶氮染料检测方法的探讨[/font][font=Times New Roman][J].[/font][font=宋体]印染[/font][font=Times New Roman].2005,06:37-39.[/font][/size][size=3][font=Times New Roman][3] [/font][font=宋体]康云[/font][font=Times New Roman]. [/font][font=宋体]禁用偶氮染料检测中的若干问题[/font][font=Times New Roman][J].[/font][font=宋体]中国纤检[/font][font=Times New Roman].2005,8:24-25.[/font][/size][size=3][font=Times New Roman][4] [/font][font=宋体]胡小钟,余建新等[/font][font=Times New Roman].[/font][font=宋体]禁用偶氮染料检测中假阳性结果的鉴别方法[/font][font=Times New Roman][J].[/font][font=宋体]分析化学研究报告[/font][font=Times New Roman].2000[/font][font=宋体],[/font][font=Times New Roman]28(4):411-416.[/font][/size]
求购头孢地尼E-异构体对照品头孢地尼做分析方法验证,其中有关物质头孢地尼E-异构体标准品买不到。很多销售公司都有但是资质不全我不能买他们的。请教各位大侠们,帮个忙吧。急用!!谢谢!!!!
质谱中同分异构体(分子式相同)如何定性?二级还是标准品
环氧七氯包含两种同分异构体,分别为内环氧七氯(trans-, isomer A,28044-83-9)和外环氧七氯(cis-, isomer B,1024-57-3)而国标“GBT 5009.19-2008 食品中有机氯农药多组分残留量的测定”中只提及环氧七氯,请问各位专家我在选择标准品时应该选择同分异构体混合物还是其中一种?
最近做二异丙基萘含量测定,由于购买的只是一种混合物(含7种异构体),但是只有一个cas登记号,按照标准方法(内标法),确实发现并确定了7种组分流出顺序,根据标准方法只是计算二异丙基萘的总量。但是突然想计算不同异构体的具体含量,这又该如何计算呢?由于异构体中有几种是很难找到(买到)单标的,此时可用面积归一化法计算可以吗?是否需要通过面积归一化法来单独建立不同异构体的标准曲线?这样算出来的结果具有说服力吗?如何不行,该如何计算呢?望老师赐教,谢谢!
大家有没有用过中检所的抗生素标准品的?如头孢氨苄、阿莫西林等,我正在用,结果用液质联用检测出两个色谱峰,质谱结果显示,这两个峰都是同一种物质,猜测标准品不纯,是同分异构体的混合物,大家有没有类似的遭遇?
一、案例磺胺类药物是一类应用最早的人工合成抗菌药物,能抑制革兰阳性菌及一些阴性菌,可以治疗多种细菌感染,具有抗菌谱广、疗效强等优点。磺胺类药物特别是磺胺嘧啶、磺胺甲基嘧啶、磺胺二甲氧嘧啶、磺胺甲基异嗯唑等作为饲料添加剂或动物疫病治疗药物被广泛应用。然而磺胺类药物在体内作用时间和代谢时间较长,过量使用必会导致磺胺类药物在食用动物产品中的蓄积。食品磺胺类药物残留,可引起过敏、中毒和导致耐药性菌的产生,它还能引起造血系统障碍,发生急性溶血性贫血、粒细胞缺乏症、再生障碍性贫血等。二、选用的标准农业部1025号公告-7—2008动物性食品中磺胺类药物残留检测——酶联免疫吸附法。三、测定方法1.样品的制备与保存取新鲜或解冻的空白或供试动物组织,剪碎,置于组织匀浆机中高速匀浆。取鸡蛋去除壳后用均质器500r/min匀浆20s,使蛋清和蛋黄充分混合。将已制备的样品在-20℃冰箱中储存备用。2.提取称取样品(2.00±0.02)g于50ml离心管中,加乙腈8mL,振荡20min,4000r/min离心5min:分取上清液2.5ml。于10mL离心管中,于50℃水浴下用氮气吹干;加正己烷1mL,涡动20s溶解残留物,再加缓冲液工作液1mL,涡动1min,4000r/min离心10min,取下层水相20μL分析。3.测定①使用前将试剂盒于室温(19~25℃)下放置1~2h。②每个标准溶液和试样溶液按两个或两个以上平行计算,将所需数目的酶标板条插入板架。③加系列标准溶液或试样液20μL于对应的微孔中,随即加酶标记物工作液50μL/孔,再加磺胺类药物抗体工作液80μL/孔,轻轻振荡混匀,用盖板膜盖板,置25℃避光反应60min。④倒出微孔中的液体,将酶标板倒置在吸水纸上拍打,以保证完全除去孔中的液体。再加洗涤工作液250μL/孔,重复操作两遍以上(或用洗板机洗涤)。⑤加底物液A液和B液各50μl/孔,轻轻振荡混匀,用盖板膜盖板,室温下避光反应30min。⑥加终止液50μL/孔,轻轻振荡混匀,置酶标仪于450nm波长处测量吸光度值。4.结果判定和表述用所获得的标准溶液和试样溶液吸光度值的比值进行计算。相对吸光度值(%)=B/B0×100%式中 B一一标准(试样)溶液的吸光度值;B0——空白(浓度为0的标准溶液)的吸光度值。将计算的相对吸光度值(%)对应磺胺类药物标准品浓度(μg/L)的自然对数作半对数坐标系统曲线图,对应的试样浓度可从校正曲线算出。方法筛选结果为阳性的样品,需要用确证的方法进行确证。5.竞争物的交叉反应率见表1。表1竞争物的交叉反应率竞争物交叉反应率/%竞争物交叉反应率,%磺胺二甲嘧啶磺胺二甲氧嘧啶磺胺二甲基嘧啶磺胺嘧啶磺胺甲基异毂唑10023121%1%磺胺噻唑磺胺吡啶磺胺喹彀啉磺胺问甲氧嘧啶1%1%1%6.试剂①乙腈②正已烷③十二水合磷酸氢二钠。④二水合磷酸氢二氢钾。⑤氯化钠。⑥氯化钾⑦磺胺类药物快速检测试剂盒:2~8℃保存。a.系列标准工作溶液:O、1μg/L、3μg/L、9μg/L、27μg/L、81μg/L。b.包被有磺胺类药物偶联抗原的96孔板,12×8孔。c.磺胺类药物抗体工作液。d.酶标记物工作液。e.底物液A液。f.底物液B液。g.终止液。h.20倍浓缩洗涤液。i.20倍浓缩缓冲液。⑧洗涤工作液:用水将20倍浓缩液按1:19的体积比进行稀释(1份20倍浓缩洗涤液+19份水),用于酶标板的洗涤。2~8℃保存,有效期1个月。⑨缓冲工作液:用水将20倍浓缩缓冲液按1:19的体积比进行稀释(1份20倍浓缩洗涤液+19份水),用于酶标板的洗涤。2~8℃保存,有效期1个月。7.仪器①酶标仪(配备有450nm滤光片)。②氮气吹干装置。③均质器。④振荡器。⑤离心机。⑥天平(感量0.01g)。⑦微量移液器(单道20~200/μl、100~1000μL;多道250μL)。
各位版友老师好: 如题,求助关于农药标准品中同分异构体的问题。我们用气质做氯氰菊酯,一般都是4个峰,皮下倒是从来没有详细区分这四个究竟是什么同分异构体,而标准物质证书上也没有写明。但是,今天皮下上司给了一份农药名录,需要核查是否能够检测,其中就有lambda-cypermethrin,beta-cypermethrin,alpha-...... 所以特上来求助,万分感激!~
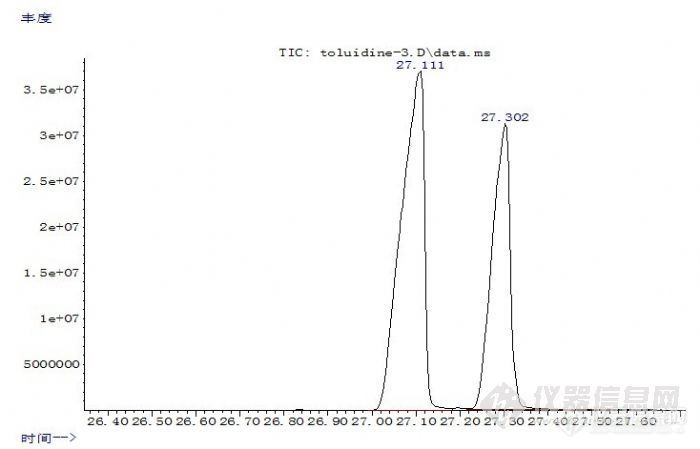
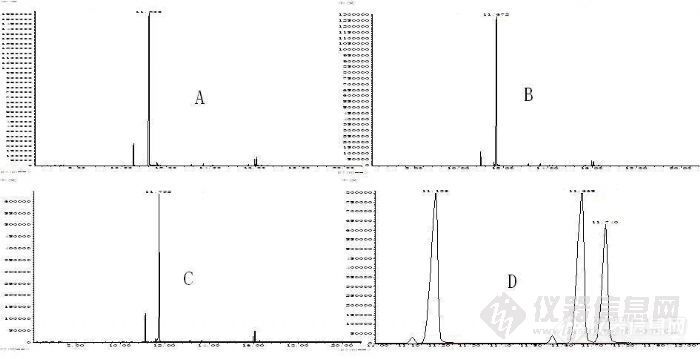
[align=left][font=宋体][color=#fe2419][color=#000000][1006] [/color]维权声明:本文为[/color][url=http://bbs.instrument.com.cn/user.asp?username=dahua1981][color=#444444][size=2]dahua1981[/size][/color][/url][size=2][color=#fe2419]原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现的,均属侵权违法行为,我们将追究法律责任。[/color][/size][/font][/align][align=center][size=3][font=宋体][b]邻甲苯胺及其同分异构体的分离[/b][/font][/size][b][size=3][font=Times New Roman]The Separation of O-Toluidine and Its isomers[/font][/size][/b][/align][align=left][size=3][font=宋体]摘要:为了实现邻甲苯胺同分异构体的完全分离,作者采用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url][/font][font=Times New Roman]-[/font][font=宋体]质谱联用方法,通过改进色谱条件,使其取得了较好分离。试验表明采用气[/font][font=Times New Roman]-[/font][font=宋体]质联用方法可以实现邻甲苯胺同分异构体的较好分离。[/font][/size][size=3][font=宋体]关键词:邻甲苯胺;分离;异构体[/font][/size][font=Times New Roman][size=3][b]Abstract:[/b] [/size][back=white][size=2]In order to achieve the complete separation of [/size][/back][size=3]o-toluidine[/size][back=white][size=2] and its isomers, the authors used gas chromatography-mass spectrometry methods, by improving the chromatographic conditions, so as to achieve their better separation. The results showed that the gas-chromatography-mass spectrometry method can achieve the better separation of [/size][/back][size=3]o-toluidine[/size][back=white] and its isomers.[/back][/back][/back][/back][/back][/back][/back][/back][/back][/back][/back][/back][/back][/font][size=3][font=Times New Roman][b]Keywords:[/b] o-toluidine separation isomers[/font][/size][size=3][font=Times New Roman][/font][/size][size=3][b][font=Times New Roman]1 [/font][font=宋体]前言[/font][/b][/size][size=3][font=宋体]在禁用偶氮染料检测过程中,邻甲苯胺是经常被检出者之一。邻甲苯胺有两个同分异构体,分别是间甲苯胺和对甲苯胺。其中,邻甲苯胺属于禁用芳香胺,而间甲苯胺和对甲苯胺则不属于禁用芳香胺。三个化合物的沸点非常接近,分别为:邻甲苯胺([/font][font=Times New Roman]200±[/font][font=Times New Roman]2[/font][font=宋体]℃[/font][font=宋体])、间甲苯胺([/font][font=Times New Roman]203±[/font][font=Times New Roman]3[/font][font=宋体]℃[/font][font=宋体])、对甲苯胺([/font][font=Times New Roman]201±[/font][font=Times New Roman]1[/font][font=宋体]℃[/font][font=宋体])。而且三者的质谱图很相似,只是分子极性上略有差别,故造成在用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url][/font][font=Times New Roman]-[/font][font=宋体]质谱联用方法检测到邻甲苯胺时经常出现假阳性结果。[/font][/size][size=3][font=宋体]如不采用薄层色谱、液相色谱等其它分析手段共同鉴别,是无法判断是否假阳性结果的。但是要排除假阳性结果,就需要重新寻找条件,而且更换仪器费时费力,且多数实验室不一定同时具备这些设备,这就给我们的日常检测工作带来了很多的麻烦和不便。本文作者结合自身知识和经验,对常见的邻甲苯胺及其异构体分离问题进行了研究。作者通过改进色谱条件,使以上化合物达到很好的分离,提高了检测效率,减少了检测过程中的假阳性检出。[/font][font=Times New Roman] [/font][/size][size=3][b][font=Times New Roman]2 [/font][font=宋体]试验[/font][/b][/size][size=3][b][font=Times New Roman]2.1 [/font][font=宋体]仪器与试剂[/font][/b][/size][size=3][font=宋体][url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url][/font][font=Times New Roman]-[/font][font=宋体]质谱联用仪([/font][font=Times New Roman]GC-MS[/font][font=宋体]):[/font][font=Times New Roman]Agilent 7890A/5975C[/font][font=宋体],美国[/font][font=Times New Roman]Agilent[/font][font=宋体]公司[/font][/size][size=3][font=宋体]毛细管柱:[/font][font=Times New Roman]DB-17MS[/font][font=宋体]柱([/font][font=Times New Roman]30m×0.25mm×0.25μm[/font][font=宋体])[/font][/size][size=3][font=宋体]甲醇[/font][font=Times New Roman] [/font][font=宋体]色谱纯[/font][font=Times New Roman] [/font][font=宋体]美国[/font][font=Times New Roman]Fisher[/font][font=宋体]公司[/font][/size][size=3][font=宋体]旋转蒸发仪[/font][font=Times New Roman] [/font][font=宋体]上海亚荣生化仪器厂[/font][/size][size=3][font=宋体]邻甲苯胺及其同分异构体均为德国[/font][font=Times New Roman]Dr.Ehrenstorfer[/font][font=宋体]公司。[/font][/size][size=3][b][font=Times New Roman]2.2 [/font][font=宋体]试剂配制[/font][/b][/size][size=3][font=Times New Roman] [/font][font=宋体]用色谱纯级甲醇为溶剂,分别称取适量邻甲苯胺、间甲苯胺和对甲苯胺标准品配成合适浓度的混合溶液。[/font][/size][size=3][b][font=Times New Roman]2.3 [/font][font=宋体]仪器操作条件[/font][/b][/size][size=3][font=宋体]色谱柱:[/font][font=Times New Roman]DB[/font][font=宋体]一[/font][font=Times New Roman]17MS 30m×0.25mm×0.25μm[/font][font=宋体];温度:进样口[/font][font=Times New Roman]220[/font][font=宋体]℃[/font][font=Times New Roman] [/font][font=宋体];辅助器[/font][font=Times New Roman]280[/font][font=宋体]℃[/font][font=宋体];离子源[/font][font=Times New Roman]230[/font][font=宋体]℃[/font][font=Times New Roman] [/font][font=宋体];四极杆温度:[/font][font=Times New Roman]150[/font][font=宋体]℃[/font][font=宋体];柱温:[/font][font=Times New Roman]40[/font][font=宋体]℃[/font][font=宋体]保持[/font][font=Times New Roman]2[/font][font=宋体]分钟,以[/font][font=Times New Roman]10[/font][font=宋体]℃[/font][font=宋体]/分钟升温至[/font][font=Times New Roman]70[/font][font=宋体]℃[/font][font=Times New Roman] [/font][font=宋体],保持[/font][font=Times New Roman]20[/font][font=宋体]分钟,再以[/font][font=Times New Roman]30[/font][font=宋体]℃[/font][font=宋体]/分钟升至[/font][font=Times New Roman]280[/font][font=宋体]℃[/font][font=宋体],保持[/font][font=Times New Roman]0[/font][font=宋体]分钟;载气:[/font][font=Times New Roman]He[/font][font=宋体];流速:[/font][font=Times New Roman]1.0ml/[/font][font=宋体]分钟;离子化方式:[/font][font=Times New Roman]EI[/font][font=宋体];质量扫描范围:[/font][font=Times New Roman]35amu-350amu[/font][font=宋体];进样方式:不分流进样;进样[/font][font=Times New Roman]0.2μ L[/font][font=宋体]。[/font][/size][size=3][b][font=Times New Roman]3 [/font][font=宋体]结果与讨论[/font][/b][/size][size=3][b][font=Times New Roman]3.1 [/font][font=宋体]试验结果[/font][/b][/size][size=3][b][font=宋体]([/font][font=Times New Roman]1[/font][font=宋体])邻[/font][font=Times New Roman]([/font][font=宋体]间、对[/font][font=Times New Roman])[/font][font=宋体]甲苯胺总离子流图[/font][/b][/size][/align][align=center][img]http://ng1.17img.cn/bbsfiles/images/2010/10/201010131355_251259_1604317_3.jpg[/img][/align][align=center][size=3][/size][/align][align=center][size=3][font=宋体]图[/font][font=Times New Roman]1 [/font][font=宋体]邻[/font][font=Times New Roman]([/font][font=宋体]间、对[/font][font=Times New Roman])[/font][font=宋体]甲苯胺总离子流图[/font][/size][/align][size=3][font=宋体]由图[/font][font=Times New Roman]1[/font][font=宋体]可以看出,邻甲基苯胺及其异构体在本实验条件下,可以得到较好的分离。保留时间分别为:邻甲基苯胺[/font][font=Times New Roman](27.111[/font][font=宋体]分钟[/font][font=Times New Roman])[/font][font=宋体];间甲基苯胺和对甲基苯胺[/font][font=Times New Roman](27.302[/font][font=宋体]分钟[/font][font=Times New Roman])[/font][font=宋体]。间甲基苯胺和对甲基苯胺保留时间很接近而无法有效分离,但是两者都是非禁用芳香胺,该实验条件是可以满足检测要求的。[/font][/size][size=3][b][font=宋体]([/font][font=Times New Roman]2[/font][font=宋体])[/font][font=Times New Roman] [/font][font=宋体]邻甲苯胺峰纯度[/font][/b][/size][align=center][img]http://ng1.17img.cn/bbsfiles/images/2010/10/201010131357_251261_1604317_3.jpg[/img][/align][align=center][size=3][/size][/align][align=center][size=3][font=宋体]图[/font][font=Times New Roman]2 [/font][font=宋体]邻甲基苯胺峰纯度及其标准质谱图[/font][/size][/align][size=3][font=宋体]由图[/font][font=Times New Roman]2[/font][font=宋体]可知,在该实验条件下,邻甲苯胺的峰对称性很好,且该峰处只有[/font][font=Times New Roman]106[/font][font=宋体]、[/font][font=Times New Roman]107[/font][font=宋体]、[/font][font=Times New Roman]77[/font][font=宋体]和[/font][font=Times New Roman]79[/font][font=宋体]四个离子,与邻甲苯胺的标准质谱图一致。其中,离子[/font][font=Times New Roman]107[/font][font=宋体]为邻甲苯胺的分子离子,[/font][font=Times New Roman]106[/font][font=宋体]为邻甲苯胺分子的同位素离子;[/font][font=Times New Roman]77[/font][font=宋体]和[/font][font=Times New Roman]79[/font][font=宋体]则来自于邻甲苯胺失去甲基和氨基后的苯环离子。这说明在该实验条件下,邻甲苯胺峰没有其它干扰离子。[/font][/size][size=3][b][font=宋体]([/font][font=Times New Roman]3[/font][font=宋体])[/font][font=宋体]间甲苯胺和对甲苯胺峰纯度[/font][/b][/size][align=center][img]http://ng1.17img.cn/bbsfiles/images/2010/10/201010131358_251262_1604317_3.jpg[/img][/align][align=center][size=3][/size][/align][align=center][size=3][font=宋体]图[/font][font=Times New Roman]3 [/font][font=宋体]间甲基苯胺和对甲基苯胺峰纯度及其标准质谱图[/font][/size][/align][size=3][font=宋体]由图[/font][font=Times New Roman]3[/font][font=宋体]可以看出,[/font][font=宋体]在该试验条件下,[/font][font=宋体]间甲基苯胺和对甲基苯胺虽没完全分离,但它们的峰对称性都很好,该峰处的四个离子与间甲苯胺和对甲苯胺标准质谱图也一致。[/font][/size][size=3][font=宋体]由图[/font][font=Times New Roman]2[/font][font=宋体]和图[/font][font=Times New Roman]3[/font][font=宋体]可以得出,该方法用来鉴别邻甲基苯胺同分异构体是可行的。[/font][/size][size=3][b][font=Times New Roman]3.2[/font][font=宋体]讨论[/font][/b][/size][size=3][font=宋体]在对染料产品中[/font][font=Times New Roman]23[/font][font=宋体]种有害芳香胺含量的测定过程中,由于异构体的存在,并且多数异构体的质谱图很相似,如果保留时间再相同,往往会形成假阳性结果的产生。当前针对有害芳香胺的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url][/font][font=Times New Roman]/[/font][font=宋体]质谱检测方法,大多采用非极性或极性较弱的色谱柱[/font][sup][font=Times New Roman][1-4][/font][/sup][font=宋体],如[/font][font=Times New Roman]HP-5MS[/font][font=宋体],[/font][font=Times New Roman]DB-5MS[/font][font=宋体],[/font][font=Times New Roman]DB-35MS[/font][font=宋体],这些色谱柱普遍存在的缺点是对常见的芳香胺异构体不能很好的分离。本方法通过使用中等极性色谱柱[/font][font=Times New Roman]DB-17MS([/font][font=宋体]固定相等同于[/font][font=Times New Roman]50[/font][font=宋体]%苯甲基聚硅氧烷[/font][font=Times New Roman])[/font][font=宋体],同时使用三阶程序升温,比较好的解决了这个问题。[/font][/size][size=3][font=宋体]在色谱分析中,柱温是一个重要的操作变数,直接影响分离效能和分析速度。柱温对组分分离的影响较大,提高柱温使各组分的挥发靠拢,不利于分离,所以,从分离的角度考虑,宜采用较低的柱温。但柱温太低,被测组分在两相中的扩散速率大为减小,分配不能迅速达到平衡,峰形变宽,柱效下降,并延长了分析时间。选择的原则是:在使最难分离的组分能尽可能好的分离的前提下,尽可能采取较低的柱温,但以保留时间适宜,峰形不拖尾为度。具体操作条件的选择应根据不同的实际情况而定。[/font][/size][size=3][font=宋体]目前,用于极性相近化和物的分析通常采用程序升温,即柱温按预定的加热速度,随时间作线性或非线性的增加。升温的速度一般常是呈线性的,即单位时间内温度上升的速度是恒定的,例如每分钟[/font][font=Times New Roman]2[/font][font=宋体]℃[/font][font=宋体]、[/font][font=Times New Roman]4[/font][font=宋体]℃[/font][font=宋体]、[/font][font=Times New Roman]6[/font][font=宋体]℃[/font][font=宋体]等等。[/font][font=宋体]在较低初始温度,沸点较低的组分,即最早流出的峰可以得到良好的分离。随柱温增加,较高沸点的组分也能较快的流出,并和低沸点组分一样也能得到分离良好的尖峰。[/font][font=Arial][/font][/size][size=3][font=宋体]通过上面的数据可以看出,该方法实现了邻甲基苯胺与间(对)甲苯胺的基线分离,虽然无法实现间甲苯胺和对甲苯胺的完全分离,但是对于邻甲苯胺假阳性结果的排除来说已经足够了。作者通过大量的试验证明,该方法快速、精确、重现性和稳定性好,具有很高的可行性和可靠性。[/font][/size][size=3][b][font=Times New Roman]4 [/font][font=宋体]结论[/font][/b][/size][size=3][font=Times New Roman] [/font][font=宋体]由前文分析可以得出如下结论:[/font][/size][size=3][font=Times New Roman]a) [/font][font=宋体]该方法实现了邻甲基苯胺异构体的较好分离,因此可以不必再用其它手段或方法做异构体的确认,也在一定程度上提高了检测效率,节约了检测成本。[/font][/size][size=3][font=Times New Roman]b)[/font][font=宋体]该方法快速、精确、重现性和稳定性好,具有很高的可行性和可靠性。[/font][/size][size=3][font=宋体]该方法无法实现间甲基苯胺和对甲基苯胺的分离,但是,因为二者皆为非禁用芳香胺,所以该方法仍然具有很好的推广和应用价值。[/font][/size][size=3][font=宋体]参考文献[/font][/size][size=3][font=Times New Roman][1] GB19601-2004,[/font][font=宋体]《染料产品中[/font][font=Times New Roman]23[/font][font=宋体]中有害芳香胺的限量及测定》[/font][font=Times New Roman][s].[/s][/font][/size][size=3][font=Times New Roman][2] [/font][font=宋体]杨继生,徐逸云,蒋华[/font][font=Times New Roman].[/font][font=宋体]对纺织品禁用偶氮染料检测方法的探讨[/font][font=Times New Roman][J].[/font][font=宋体]印染[/font][font=Times New Roman].2005,06:37-39.[/font][/size][size=3][font=Times New Roman][3] [/font][font=宋体]康云[/font][font=Times New Roman]. [/font][font=宋体]禁用偶氮染料检测中的若干问题[/font][font=Times New Roman][J].[/font][font=宋体]中国纤检[/font][font=Times New Roman].2005,8:24-25.[/font][/size][size=3][font=Times New Roman][4] [/font][font=宋体]胡小钟,余建新等[/font][font=Times New Roman].[/font][font=宋体]禁用偶氮染料检测中假阳性结果的鉴别方法[/font][font=Times New Roman][J].[/font][font=宋体]分析化学研究报告[/font][font=Times New Roman].2000[/font][font=宋体],[/font][font=Times New Roman]28(4):411-416.[/font][/size]
比如666的同分异构体,常见的有四种,α-666 β-666 γ-666 δ-666. 有些地方可能也叫做BHC,其中α-666就是最标准的六氯环己烷 C6H6Cl6 γ-666则是农药中常见的林丹。 目前国内好像仍然有生产和使用?或者叫甲乙丙丁四种六六六(老的国内叫法,还是蛮有中文特色的)======================================================DDT化学名为双对氯苯基三氯乙烷(Dichlorodiphenyltrichloroethane),化学式(ClC₆H₄)₂CH(CCl₃它的异构体比较奇葩,四种异构体叫做P,P'-DDE、O,P'-DDT P,P'-DDD P,P'-DDT。真够复杂的。不过看名字似乎就是两种前缀(P,P'和O,P')和三个后缀(DDE DDT DDD),他们分别有啥区别??另外,有要求测666和DDT的其他几种异构体的么?
欧盟限量基准中规定了氰戊菊酯:RR+SS 异构体 RS+SR异构体的限量。两个异构体在不同的物体中限量是不一样的,请问一下,我现在没有他们单独的标准品,怎么通过峰来判断,在保留时间上氰戊菊酯有两个峰,这四种同分异构体是怎么出峰的,出峰顺序是怎么样的。[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用仪[/color][/url],DB-5柱,非常感谢!
脂肪酸同分异构体的鉴定,买了C16:1的标准品,出了一个峰是C16:1 7c,但是实验目的是想要C16:1 5c,是要重新买标准品吗?
[color=#444444]如题所示,本人正在做玩具中壬基酚,辛基酚的检测,用的是液相色谱串联质谱法,分别购买了三种壬基酚的同分异构体104-40-5、25154-52-3、84852-15-3,三种辛基酚的同分异构体140-66-9、1806-26-4、27193-28-8,现在的问题是这六种物质只出了四个峰,通过单标比较发现,其中25154-52-3和84852-15-3分不开,同一时间出峰,140-66-9和27193-28-8也分不开,为一个峰。试过许多根柱子了,流动相也改变过了,还是分不开,现在用的流动相是甲醇-0.1%氨水溶液。大家懂行的帮帮忙吧,提点建议,另外,如果实在分不开,能把他们当成一种物质处理吗?还是要舍弃一种?这对定量限,检测线等都有影响吧,该怎么处置呢?我们是想做成标准的。跪求了。[/color]

看到一论文 说二甲基甲酰胺(DMF)有顺反异构体,这还真的第一次听说!http://ng1.17img.cn/bbsfiles/images/2014/12/201412262213_529354_2103464_3.png
我们实验室使用23200.113检测果蔬样品已经两年了,但是一直有几个疑问没能解决,与其他人咨询过,但是各家说法有些不一致,所以想向各位大神咨询一下答案。像氟虫腈,甲拌磷,倍硫磷这类化合物,在限值标准2763中写的是:以氟虫腈/甲拌磷/倍硫磷表示,但是结果要包含2个以上同分异构体的含量,这样就涉及到不同化合物结果加和,关于加和方法我有以下3个疑问(以氟虫腈为例):1:氟虫腈检出限为0.005mg/kg,如果各同分异构体单独含量都不达检出限,但是加和后能达到检出限以上,这种情况是加和报检出 还是 不加和报未检出?2:若某个样品,氟虫腈的有部分同分异构体含量不达检出限,但是加上它们后,检出值超过了这个样品的国标限值,这个样品应该算超标还是算未超标?3:同分异构体检出后,以检出浓度计算得出了各个异构体的含量,做加和计算时,需不需要考虑它们之间的质量换算系数?比如氟虫腈亚砜换算成氟虫腈,氟虫腈相对分子质量437.15,氟虫腈亚砜相对分子质量421.15。以上问题期待收到各位专家的答复,感谢!?
多溴那么多异构体!标准品也不可能都买。现在就买了些常规的,大概二十几个。做的时候先SCAN一下,在已有标准品的出峰位置看一下,然后定性定量。但是其他的怎么弄呢,而且异构体的出峰时间相差也比较大?
[color=#444444]请问大家有没有遇到反应生成顺反异构体的问题,在色谱中显示相邻很近的两个峰(可以分开),用内标法该如何进行定量(不知道为具体为哪个顺反异构体且标准物无商售,我的产物为2-甲氧基环己醇)。诸如此类的异构体在色谱中该如何定量分析?[/color]
SVHC第八批物质种有一组甲基六氢邻苯二甲酸酐,是由4个同分异构体组成,CAS号分别为:25550-51-0 19438-60-9 48122-14-1 57110-29-9但是就其分子式来看应该只有三种同分异构体,为什么会有4个CAS号呢,或者是船式和椅式的构象不同造成的4种同分异构体?
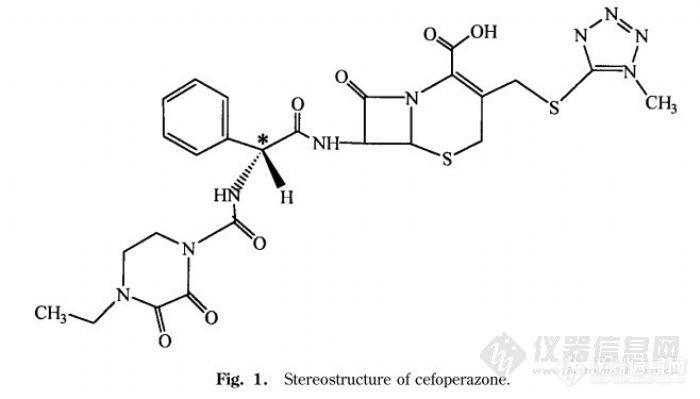
哪位老师知道头孢哌酮的s异构体是哪个C原子的手型导致的啊?就是药典中所述头孢哌酮s异构体是指哪个C原子? 另外有文献指出如下:“头孢哌酮钠在C3位可形成同分异构体,即日抗基所称副产物II,质量标准中控制限度1.5%。需要注意的是,头孢哌酮常有一未知杂质容易被误为认为是S-异构体,但是其UV吸收与S-异构体不同,可采用二极管阵列检测器进行鉴别或者控制。”这里所说的一未知杂质具体是哪个有老师知道吗?另外一篇文献显示头孢哌酮手性碳如图,该碳引起的异构体是否是药典中的S异构体呢?file:///C:/Users/ADMINI~1/AppData/Local/Temp/PQL651~GYQV‚3)CJ$JHK2.jpghttp://ng1.17img.cn/bbsfiles/images/2011/01/201101102123_273270_1352078_3.jpg这EP中有关物质F的手性碳不同。有没有可能该图即为上一文献中的未知杂质呢???谢谢指导。。
最近在合成一个药物的异构体,用的是D-谷氨酸。没有药效,目的是做个标样。有药效的构形是L构形的。这两个化合物只是原料用谷氨酸的构形补一样,合成的结果测旋光业是对的即D构型旋光是正,L构型旋光是-补知道为什么用蛋白柱却分不开呢(我用的柱子,流动相都没问题,按照标准来的)D构型与L构型的出峰位置一样,百思不得其解阿发信或打电话都可以阿感谢!!!

这几天看到两个帖子,将一个标准品中的几个峰的问题,在我平时的工作中也遇到一些,抛砖引玉菊酯类,这个不用讲了,多数都有异构体,以第一张图来看,自左至右分别是氯菊酯(两个峰)、氯氰菊酯(三个峰)、氰戊菊酯(两个峰)、溴氰菊酯(一小一大两个峰),我用的0.32的柱子,具体的出峰情况还要视柱子和分析条件来定。其他的比如氯氟氰菊酯、胺菊酯一小一大两个峰;氟氰戊菊酯和氟氯氰菊酯类似于氯氰菊酯的样子,一堆峰。菊酯类的标样都是以总含量计算的,如果没有特殊说明,处理的时候需要把几个峰面积加起来计算。六六六和滴滴涕,太经典了,没有什么可讲的。氯丹的n个峰看都看不清楚的……有机磷,毒虫畏(是它哦?貌似)、磷胺两个峰丙环唑、苯醚甲环唑两个峰阿维菌素有两个,不过残留好象只算一个吧??其他比如硫丹的标样可能有杂质峰,七氯中有环氧七氯的峰,这个都是要提高警惕的。其他的请大家补充[img]http://ng1.17img.cn/bbsfiles/images/2009/04/200904231648_146262_1788829_3.jpg[/img]
[img=分离二甲苯异构体,344,298]https://ng1.17img.cn/bbsfiles/images/2024/04/202404201205312124_3575_3161146_3.png!w344x298.jpg[/img]我们5米的柱子(具有特殊选择性的固定相)能快速分离二甲苯异构体,以及二溴苯、二氯苯、氯甲苯、溴硝基苯、二甲苯酚、甲苯胺、二甲苯胺、卤代苯胺等芳香异构体,希望能拓展应用与合作交流,帮助有需要的企业解决[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]分析领域一些有挑战性的分离难题。