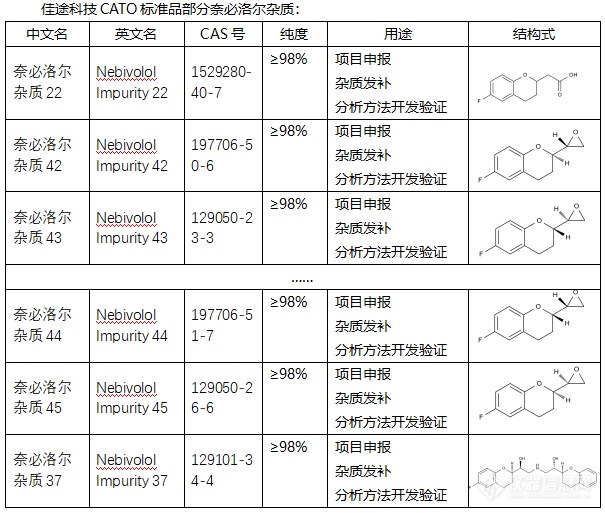
[font=宋体]◇[/font][b][font=宋体]奈必洛尔[/font][/b][font=宋体]杂质[/font][font=宋体][font=宋体] 奈必洛尔杂质是指在奈必洛尔([/font][font=Calibri]Nebivolol[/font][font=宋体])的生产或保存过程中产生的非目标化合物。奈必洛尔杂质有多种,包括但不限于以下几种:奈比洛尔杂质([/font][font=Calibri]L-[/font][font=宋体]奈必洛尔),英文名称为[/font][font=Calibri](-)-Nebivolol[/font][font=宋体],[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]118457-16-2[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=Calibri]9[/font][font=宋体],[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]920275-23-6[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=Calibri]C[/font][font=宋体](非对映体混合物),英文名为[/font][font=Calibri]Nebivolol Impurity C (Mixture of Diastereomers)[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=Calibri]B[/font][font=宋体],英文名为[/font][font=Calibri]Nebivolol impurity B[/font][font=宋体],[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]119365-25-2[/font][/font][font=宋体];[/font][font=宋体][font=宋体]去氟奈必洛尔,英文名为[/font][font=Calibri]Desfluoro Nebivolol[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=宋体]Ⅰ和奈必洛尔杂质Ⅱ等。[/font][/font][font=宋体][font=Calibri] CATO[/font][font=宋体]标准品提供的[/font][/font][b][font=宋体]奈必洛尔[/font][/b][font=宋体]全套的杂质[/font][font=宋体],[/font][font=宋体]这些杂质对于药物的纯度和稳定性研究至关重要,也是药物研发过程中不可或缺的一部分[/font][font=宋体]。[/font][img=,605,513]https://ng1.17img.cn/bbsfiles/images/2024/02/202402182153192686_9605_6381607_3.png!w605x513.jpg[/img][font=宋体][color=#05073b][back=#fdfdfe] 广州[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]佳途科技[/back][/color][/font][font=宋体][color=#05073b][back=#fdfdfe]股份有限公司[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]深知药物研发与质量控制的重要性[/back][/color][/font][font=宋体][font=宋体],[/font][font=Calibri]CATO[/font][font=宋体]标准品厂家,提供[/font][/font][b][font=宋体]奈必洛尔[/font][/b][font=宋体]全套[/font][font=宋体]的[/font][font=宋体]杂质,为客户提供更加精准、可靠的分析标准品,助力药物研发事业的快速发展[/font][font=宋体],[/font][font=宋体]以满足客户在药物研发和质量控制方面的需求。[/font]
请高手指点一下,我做系统适应性试验过程如下,时隔1小时进标准品1次,标准品在20分钟左右出峰完全,连续5次,在chemstation报告中设定“编辑噪音范围”,然后不知所措[em09501],请教如何出系统适应性报告
高效液相色谱试验的问题:05版药典中多数系统适应性试验都没写用标准品还是供试品来做,所以多数我们都用对照品来做了。而2010版药典中很多改为用供试品或供试品经过处理来做系统适应性试验,以便于更好的分离要检成分与杂质。但当供试品中不含有规定的成分时,就不出峰等,就体现不出系统适应性试验的作用了。这样的情况下该怎么做?改用对照品吗,还是改用其他方法?但改了之后又与药典不一致怎么办?
http://simg.instrument.com.cn/bbs/images/brow/emyc1010.gif如题 ,这东西貌似挺火的 请大家注意是要标准品鉴于玛卡酰胺和玛卡烯目前没有标准品出售,本帖更改为征集二者的化学结构图,最好是立体的哦!
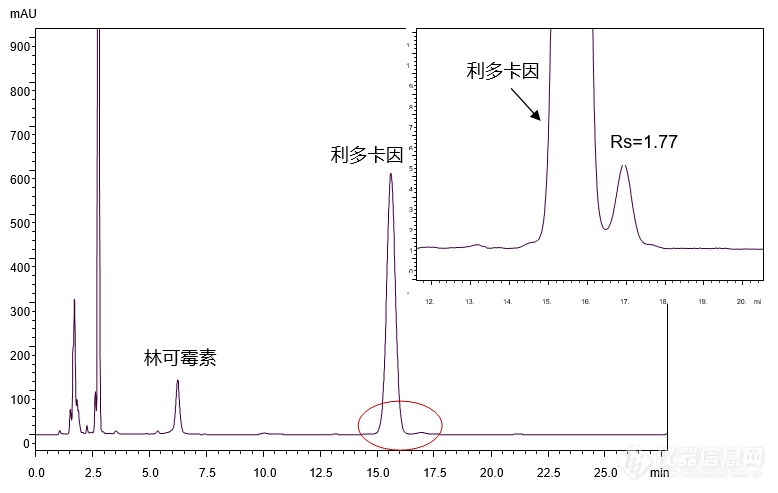
[align=center][b]【国家药品标准】林可霉素利多卡因凝胶的分析[/b][/align][align=center][b][/b][/align][align=right][b]——依据国家药品标准WS-10001-(HD-0140)-2002方法[/b][/align][b]林可霉素利多卡因凝胶[/b]为复方制剂,每克含林可霉素5毫克,利多卡因4毫克。适应症为用于轻度烧伤、创伤及蚊虫叮咬引起的各种皮肤感染。 [img=,193,127]http://ng1.17img.cn/bbsfiles/images/2018/07/201807260834522166_2994_2222981_3.gif!w193x127.jpg[/img] [img=,140,64]http://ng1.17img.cn/bbsfiles/images/2018/07/201807260834520028_3541_2222981_3.gif!w140x64.jpg[/img] 林可霉素 利多卡因 Lincomycin Lidocaine M.W.: 406.54 M.W.: 234.34客户提供林可霉素利多卡因凝胶样品,希望本实验室帮忙通过筛选色谱柱及调节分析条件,依据[color=#ff0000][b]国家药品标准WS-10001-(HD-0140)-2002[/b][/color]方法,实现林可霉素利多卡因凝胶样品的良好分析。首先,使用能在纯水条件下稳定使用的高极性色谱柱[color=#ff0000][b]CAPCELL PAK C[sub]18[/sub] AQ S5 4.6 mm i.d. × 150 mm[/b][/color],对林可霉素利多卡因凝胶样品进行分析,结果如图1所示,[color=#330099]利多卡因与其峰后杂质之间分离度为1.77[/color]。[align=center][img=,690,437]http://ng1.17img.cn/bbsfiles/images/2018/07/201807260858200006_8607_2222981_3.png!w690x437.jpg[/img][/align][align=center]图1 CAPCELL PAK C[sub]18 [/sub]AQ分析所得色谱图[/align]注:峰上标数字为分离度。[img=,528,205]http://ng1.17img.cn/bbsfiles/images/2018/07/201807260858202566_2695_2222981_3.png!w528x205.jpg[/img]为进一步提高利多卡因与其峰后杂质之间的分离度,在原条件基础上将柱温由30℃降低至25℃,并分别使用 CAPCELL PAK C[sub]18[/sub] AQ、CAPCELL PAK C[sub]18[/sub] MG及高含碳量ODS色谱柱SUPERIOREX ODS进行分析,结果如图2所示。[align=center][img=,690,490]http://ng1.17img.cn/bbsfiles/images/2018/07/201807260859201516_7229_2222981_3.png!w690x490.jpg[/img][/align][align=center]图2 25℃条件下不同色谱柱分析结果对比[/align]注:峰上标数字为分离度。[img=,637,223]http://ng1.17img.cn/bbsfiles/images/2018/07/201807260859204236_7198_2222981_3.png!w637x223.jpg[/img]如图2所示,在柱温25℃条件下使用三款色谱柱进行分析,其中,[color=#ff0000][b]CAPCELL PAK C[sub]18[/sub] AQ色谱柱分析结果最好,利多卡因与其峰后杂质分离得到最佳分离,分离度为4.23[/b][/color];[color=#330099][b]使用CAPCELL PAK C[sub]18[/sub] MG色谱柱进行分析时,利多卡因与其峰后杂质分离度为3.27[/b][/color];而使用SUPERIOREX ODS色谱柱分析时,利多卡因与其峰后杂质未得到有效分离。综上,在国家药品标准WS-10001-(HD-0140)-2002方法基础上,将色谱柱柱温由30℃降低至25℃,使用高极性色谱柱CAPCELL PAK C[sub]18[/sub] AQ及中等极性色谱柱CAPCELL PAK C[sub]18[/sub] MG进行分析,均可在25 min内完成林可霉素利多卡因凝胶样品的分析,并得到利多卡因与其峰后杂质之间的良好分离结果。[align=right][/align][align=right][/align][align=right] [/align][align=right]三耀精细化工品销售(中国)有限公司[/align][align=right]技术开发部[/align][align=right]地址:北京经济技术开发区宏达南路5号[/align][align=right]宏达利德工业园1栋418室[/align][align=right]邮编:100176[/align]
请问色谱系统适应性试验怎么做,具体方法是什么?样品分析方法是用的面积百分比法,系统适应性方法是不是要和样品一致呢?还有就是如果买不到对照品怎么做系统适应性试验?可以用样品代替吗?刚开始接触这些,不太了解,哪位老师可以指点下,谢谢
[font=宋体]中国食品药品检定研究院(以下简称“中检院”)对卡铂、来那度胺和硫普罗宁杂质Ⅱ标准物质原料采购项目进行公告,现诚邀符合项目要求的供应商报名参加。[/font][font=宋体]一、项目基本情况[/font][font=宋体]项目名称:中检院卡铂、来那度胺和硫普罗宁杂质Ⅱ标准物质原料采购项目[/font][font=宋体]项目编号:ZFCG202300002[/font][font=宋体]项目需求:[/font][table][tr][td=1,1,52][font=宋体]序号[/font][/td][td=1,1,124][font=宋体]品种名字[/font][/td][td=1,1,150][font=宋体]预算金额(万元)[/font][/td][td=1,1,94][font=宋体]采购数量[/font][/td][td=1,1,98][font=宋体]货期要求[/font][/td][/tr][tr][td=1,1,52][font=宋体]1[/font][/td][td=1,1,124][font=宋体]卡铂[/font][/td][td=1,1,150][font=宋体]5.1[/font][/td][td=1,1,94][font=宋体]300g[/font][/td][td=1,1,98][font=宋体]一个月[/font][/td][/tr][tr][td=1,1,52][font=宋体]2[/font][/td][td=1,1,124][font=宋体]来那度胺[/font][/td][td=1,1,150][font=宋体]6[/font][/td][td=1,1,94][font=宋体]300g[/font][/td][td=1,1,98][font=宋体]二个月[/font][/td][/tr][tr][td=1,1,52][font=宋体]3[/font][/td][td=1,1,124][font=宋体]硫普罗宁杂质Ⅱ[/font][/td][td=1,1,150][font=宋体]10[/font][/td][td=1,1,94][font=宋体]200g[/font][/td][td=1,1,98][font=宋体]三个月[/font][/td][/tr][/table][font=宋体] [/font][font=宋体]技术要求:[/font][font=宋体]1.[/font][font=宋体]卡铂:同一批号、均匀且纯度≥99.5%,符合现行国家药品标准规定,提供检验报告书;资质要求:具有该品种原料生产许可证或持有该品种制剂批准文号的生产企业。[/font][font=宋体]2.[/font][font=宋体]来那度胺:同一批号、均匀且纯度≥99.5%,符合现行国家药品标准规定,提供检验报告书;资质要求:具有该品种原料生产许可证或持有该品种制剂批准文号的生产企业。[/font][font=宋体]3.[/font][font=宋体]硫普罗宁杂质Ⅱ:同一批号、均匀且纯度≥99%,符合现行国家药品标准规定。提供检验报告书,并附结构确证、纯度分析、稳定性资料及相关图谱。[/font][font=宋体]4.[/font][font=宋体]原料质保期要求:在标化合格后一年内。[/font][font=宋体]二、供应商资格要求[/font][font=宋体]1.[/font][font=宋体]具有独立承担民事责任的能力;[/font][font=宋体]2.[/font][font=宋体]具有良好的商业信誉和健全的财务会计制度;[/font][font=宋体]3.[/font][font=宋体]具有履行合同所必需的专业技术能力;[/font][font=宋体]4.[/font][font=宋体]有依法缴纳税收和社会保障资金的良好记录;[/font][font=宋体]5.[/font][font=宋体]参加政府采购活动前三年内,在经营活动中没有重大违法记录;[/font][font=宋体]6.[/font][font=宋体]资格审查时,通过“信用中国”网站、中国政府采购网、国家企业信用信息公示系统、天眼查、企查查网站等渠道查询供应商信用记录,经查询列入失信被执行人、重大税收违法案件当事人名单、政府采购严重违法失信行为记录名单、经营异常名录信息、严重违法失信企业名单(黑名单)信息的,经查询在经营活动中有重大违法记录的,截至本项目采购活动开始前三年内因违法经营受到刑事处罚或者责令停产停业、吊销许可证或者执照、较大数额罚款等行政处罚的,不得参加本项目;[/font][font=宋体]7.[/font][font=宋体]单位负责人为同一人或者存在控股、管理关系的不同单位,不得参加同一项目响应;[/font][font=宋体]8.[/font][font=宋体]本项目不接受联合体参加,禁止转包或分包;[/font][font=宋体]9.[/font][font=宋体]法律、行政法规规定的其他条件。[/font][font=宋体]三、报名方式[/font][font=宋体]1.[/font][font=宋体]本项目采取网上报名的方式,不设现场报名及其他形式的报名。符合项目要求的潜在供应商需填写完整报名表(附件1)发送至邮箱hqzc@nifdc.org.cn。(邮件命名:项目名称+报名单位名称)[/font][font=宋体]2.[/font][font=宋体]报名供应商需提交真实有效的响应文件(附件2)并加盖公章,密封邮寄至中检院联系人处。[/font][font=宋体]3.[/font][font=宋体]报名和文件邮寄送达时间截止至2023年1月19日(北京时间),逾期送达不予接收。[/font][font=宋体]四、供应商确定原则[/font][font=宋体]请报名供应商以单品种总价进行报价,本项目根据质量和服务均能满足实质性响应且报价最低原则确定供应商。[/font][font=宋体]五、联系方式[/font][font=宋体]采购单位:中国食品药品检定研究院[/font][font=宋体]地址:北京市大兴区生物医药产业基地华佗路31号院后勤政采部[/font][font=宋体]联系人: 袁玉萍[/font][font=宋体]联系电话:010-53852873[/font][font=宋体]电子邮箱:hqzc@nifdc.org.cn [/font][font=宋体]附件:[/font][font=宋体]1.[/font][font=宋体]报名表[/font][font=宋体]2.[/font][font=宋体]供应商响应文件[/font][align=right][font=宋体]中检院[/font][/align][align=right][font=宋体]2023[/font][font=宋体]年1月11日[/font][/align]【附件】[list][*][img]https://www.nifdc.org.cn/directory/web/fileTypeImages/icon_xls.gif[/img] [url=https://www.nifdc.org.cn/directory/web/nifdc/infoAttach/161b0e45-7a85-425c-ba18-db5c6983f1db.xlsx]附件1:报名表.xlsx[/url][*][img]https://www.nifdc.org.cn/directory/web/fileTypeImages/icon_xls.gif[/img] [url=https://www.nifdc.org.cn/directory/web/nifdc/infoAttach/7df1e302-bf54-4d16-8982-4be1494103e4.xlsx]附件2:供应商响应文件.xlsx[/url][/list]
http://www.greenherbs.com.cn/bbs/dispbbs.asp?boardid=2&Id=7681612594 七氟醚杂质C Sevoflurane Related Compound C 对照品/标准品1612572 七氟醚杂质 B Sevoflurane Related Compound B 对照品/标准品1612550 七氟醚杂质 A Sevoflurane Related Compound A 对照品/标准品1612540 七氟醚 Sevoflurane 对照品/标准品1612539 盐酸舍曲林 Sertraline Hydrochloride 对照品/标准品1612528 盐酸舍曲林杂质A Sertraline Hydrochloride Related Compound A 对照品/标准品1612517 盐酸舍曲林消旋体混合物 Sertraline Hydrochloride Racemic Mixture 对照品/标准品1612506 L-丝氨酸 L-Serine 对照品/标准品1612426 芝麻油杂质B Sesame Oil Related Compound B 对照品/标准品1612415 芝麻油杂质A Sesame Oil Related Compound A 对照品/标准品1612404 芝麻油 Sesame Oil 对照品/标准品1612029 番泻苷 B Sennoside B 对照品/标准品1612018 番泻苷 A Sennoside A 对照品/标准品1612007 番泻苷 Sennosides 对照品/标准品1611955 硒 蛋氨酸 Selenomethionine 对照品/标准品1611900 盐酸司来吉兰 Selegiline Hydrochloride 对照品/标准品1611004 司可巴比妥 CII Secobarbital CII 对照品/标准品1610090 东莨菪亭 Scopoletin 对照品/标准品1610001 氢溴酸东莨菪碱 Scopolamine Hydrobromide 对照品/标准品1609831 沙奎那韦杂质A Saquinavir Related Compound A 对照品/标准品1609829 甲磺酸沙奎那韦 Saquinavir Mesylate 对照品/标准品1609807 双水杨酯 Salsalate 对照品/标准品1609625 沙美特罗杂质B Salmeterol Related Compound B 对照品/标准品1609614 沙美特罗杂质A Salmeterol Related Compound A 对照品/标准品1609603 昔美酸沙美特罗 Salmeterol Xinafoate 对照品/标准品1609501 水杨酸片 Salicylic Acid Tablets 对照品/标准品1609024 水杨酸杂质B Salicylic Acid Related Compound B 对照品/标准品1609013 水杨酸杂质A Salicylic Acid Related Compound A 对照品/标准品1609002 水杨酸 Salicylic Acid 对照品/标准品1608000 水杨酰胺 Salicylamide 对照品/标准品1607506 连翘粉状贯叶提取物 Powdered St. John's Wort Extract 对照品/标准品1607040 糖精钠 Saccharin Sodium 对照品/标准品1607029 糖精钙 Saccharin Calcium 对照品/标准品1607007 糖精 Saccharin 对照品/标准品1606503 芦丁 Rutin 对照品/标准品1606208 硝酚胂酸 Roxarsone 对照品/标准品1605523 罗哌卡因杂质B Ropivacaine Related Compound B 对照品/标准品1605512 罗哌卡因杂质A Ropivacaine Related Compound A 对照品/标准品1605500 盐酸罗哌卡因 Ropivacaine Hydrochloride 对照品/标准品1604916 罗库溴铵合剂峰的识别 Rocuronium Peak Identification Mixture 对照品/标准品1604905 罗库溴铵 Rocuronium Bromide 对照品/标准品1604870 利凡斯的明杂质B Rivastigmine Related Compound B 对照品/标准品1604869 利凡斯的明杂质A Rivastigmine Related Compound A 对照品/标准品1604814 利托那韦杂质混合物 Ritonavir Related Compounds Mixture 对照品/标准品1604803 利托那韦 Ritonavir 对照品/标准品1604701 盐酸利托君 Ritodrine Hydrochloride 对照品/标准品1604665 利培酮系统适用性试验用混合物 Risperidone System Suitability Mixture 对照品/标准品1604654 利培酮 Risperidone 对照品/标准品1604643 利塞膦酸杂质C Risedronate Related Compound C 对照品/标准品1604632 利塞膦酸杂质B Risedronate Related Compound B 对照品/标准品1604621 利塞膦酸杂质A Risedronate Related Compound A 对照品/标准品1604610 利塞膦酸钠 Risedronate Sodium 对照品/标准品1604600 利美索龙 Rimexolone 对照品/标准品1604508 盐酸金刚乙胺 Rimantadine Hydrochloride 对照品/标准品1604348 利鲁唑杂质A Riluzole Related Compound A 对照品/标准品1604337 利鲁唑 Riluzole 对照品/标准品1604202 醌式利福平 Rifampin Quinone 对照品/标准品1604009 利福平 Rifampin 对照品/标准品1603800 利福布丁 Rifabutin 对照品/标准品1603108 核糖 Ribose 对照品/标准品1603006 维生素B2 Riboflavin (Vitamin B2) 对照品/标准品1602706 利巴韦林 Ribavirin 对照品/标准品1602003 间苯二酚 Resorcinol 对照品/标准品1601849 二类残留溶剂-二甲苯 Residual Solvent Class 2 - Xylenes 对照品/标准品1601827 二类残留溶剂-三氯乙烯 Residual Solvent Class 2 - Trichloroethylene 对照品/标准品1601805 二类残留溶剂-甲苯 Residual Solvent Class 2 - Toluene 对照品/标准品1601780 二类残留溶剂-四氢萘 Residual Solvent Class 2 - Tetralin 对照品/标准品1601770 二类残留溶剂-四氢呋喃 Residual Solvent Class 2 - Tetrahydrofuran 对照品/标准品1601769 二类残留溶剂-二氧噻吩烷 Residual Solvent Class 2 - Sulfolane 对照品/标准品1601747 二类残留溶剂-吡啶 Residual Solvent Class 2 - Pyridine 对照品/标准品1601725 二类残留溶剂-硝基甲烷 Residual Solvent Class 2 - Nitromethane 对照品/标准品1601703 二类残留溶剂-N-甲基吡咯烷酮 Residual Solvent Class 2 - N-Methylpyrrolidone 对照品/标准品1601689 二类残留溶剂-甲基环己烷 Residual Solvent Class 2 - Methylcyclohexane 对照品/标准品1601667 二类残留溶剂-甲基丁基酮 Residual Solvent Class 2 - Methylbutylketone 对照品/标准品1601645 二类残留溶剂- 2-甲氧基乙醇 Residual Solvent Class 2 - 2-Methoxyethanol 对照品/标准品1601623 二类残留溶剂-甲醇 Residual Solvent Class 2 - Methanol 对照品/标准品1601601 二类残留溶剂-己烷 Residual Solvent Class 2 - Hexane 对照品/标准品1601587 二类残留溶剂-甲酰胺 Residual Solvent Class 2 - Formam
海洛因、咖啡因的FTIR检验及谱图解释 摘要: 目的提高用红外光谱法鉴定海洛因、咖啡因纯品、混合物伪品的水平。方法用红外光谱法有针对性地选择特征峰,探明海洛因、咖啡因红外光谱与结构的关系。结果获得海洛因、咖啡因的特征峰。结论该方法克服了鉴定中的盲目性。 关键词:海洛因;咖啡因;红外光谱 Analysis of heroin and caffeine by FTIR and interpretations of the IR spectra FENGji-min ,LIU Shi-hai ABSTRACT: Objective To enhanced the capability to identify and differentiate the pure/mixture as well as some fakes heroin and caffeine.Method Explain away relationship between the spectra with structure characteristics of heroin and caffeine.Result Characteristic peaks.for beroin and caffeine were selected、Conclusion Pure/mixture as well as some fakes heroin and caffeine can be identified accurately with FTIR. KEY WORDS: heroin;caffeine;infrared spectroscopy 红外光谱法是国际上常用的毒品检验方法。红外光谱分析毒品主要有以下几个特点:所需检材量小,一般只需微克级;不破坏检材,样品仍可进行其它分析;操作简便,不需要特殊的前处理,10分钟可以完成一个样品分析;不需要其它试剂,不污染环境,有益于操作人员健康;重现性好,特异性强;适应性广,受杂质种类限制少。 目前有关红外光谱检验毒品的文献,大都只介绍了各种毒品纯品的红外光谱,很少对其吸收带做必要的解释。而不了解各吸收带与结构的对应关系做毒品鉴定,带有极大的盲目性,特别是分析混有杂质的毒品,无论是计算机检索,还是人工识图,都十分困难。鉴于目前这种情况,笔者在大量实验的基础上对海洛因盐酸盐和咖啡因的红外光谱解释做了初步尝试,以期与国内同行进行交流。 1 海洛因纯品的红外光谱及其解释 海洛因(heroin),是吗啡的衍生物,其盐酸盐的化学结构式见图。 海洛因盐酸盐的红外光谱中3439/cm为N-H的伸缩振动吸收,2957/cm为3个CH3中C-H反对称伸缩振动的偶合,2632、2524、2083/cm 是海洛因盐酸盐中叔胺盐离子的N+-H对称和反对称伸缩振动吸收。1762/cm为与苯环相连的乙酰氧基的羰基的伸缩振动,1738/cm为与6元环相连的乙酰氧基的羰基的伸缩振动吸收。二个羰基的伸缩振动之所以峰位有差别,是因为苯环的电负性比6元环的吸电性强,屏蔽作用大。吸电子的诱导效应使成键的电子密度向键的几何中心接近,降低了羰基C=0的极性,增加了双键性,伸缩振动力常数增加。吸电子基团的诱导效应和苯环上大的取代基的屏蔽作用导致羰基伸缩振动更多的向高频位移。1242和1037/cm两条谱带分别归属于=C-O-C=0中O-C=0和-O-C=的反对称和对称伸缩振动,是乙酰氧基光谱中两条最特征的谱带。两者和1761、1737/cm谱带结合起来指示酯类的存在。1630/cm为六元环上C=C的伸缩振动,乙酰氧基的强吸电性使其强度增大。1492、1445/cm是苯环的骨架振动。1445/cm也包含=N-CH3中C-H的变形振动吸收。 1469、1369/cm谱带分别为甲基的反对称变角振动和对称变角振动。它们的强度明显增强,是由于甲基直接和羰基相连所引起的,是乙酰结构的明显特征。1180、1157、1131为C-O的反对称伸缩振动和对称伸缩振动。1106/cm为同时与苯环和6元环相连的C-O-C键的伸缩振动。911/cm属于六元环上-CH=CH-中反式CH面外弯曲振动。764、696/cm为苯环上2个相邻氢原子的面外变角振动吸收。 2 咖啡因纯品的红外光谱及其解释咖啡因(caffeine)又称咖啡碱。由茶叶或咖啡中提得的一种生物碱。也可人工合成。呈白色晶体或粉末。密度1.23。熔点234-237℃。小剂量作用于大脑皮层高位部分,促使精神兴奋,较大剂量可直接兴奋呼吸中枢和血管运动中枢。1996年1月国家卫生部将其列入第一类精神药品。 1695/cm是2位碳原子上羰基C=O的伸缩振动,由于受邻位N原子诱导效应的影响所以出现在较高的波数。1659/cm是6位碳原子上C=O的伸缩振动,它既受邻位N原子诱导效应的影响,也与邻位4、5原子间的双键形成共轭。共轭使C=O双键特性减弱,力常数降低,伸缩振动向低频位移,同时强度增加。3114/cm是芳香环C-H的伸缩振动,其变角振动出现在745/cm。4、5原子C=C伸缩振动和8、9原子C=N伸缩振动的叠加出现在1600/cm和1551/cm。N-CH3的C-H伸缩振动出现在2959/cm,CH3不仅受N原子的影响,而且N原子也受邻近原子的影响。3个N-CH3的N原子与不同的原子相连,C-H变角振动出现在多个位置,它们分别是1485、1456、1426、1404/cmo O=C-N 中C-N的伸缩振动分别出现在1551和1360/cm。N3-C4的伸缩振动出现在1026/cm。1074/cm为C5-C6的伸缩振动。 3 海洛因和咖啡因混合物的检验 从毒贩手中缴获的海洛因等毒品中经常掺杂有咖啡因。例如从云南发生的一起贩毒大案中缴获的毒品(公安部物证鉴定中心编为滇111号),经红外光谱检验,其红外光谱如图。把它与前面两图相比较可以发现:3116、2957、1705、1660、1549、1284、1241、974、761、745、611、480、447、426/cm为咖啡因的红外吸收;3437、2957、2634、2088、1762、1737、1489、1445 1366 1241 1182 1156 1132、1109 1033、974、912、873、837、798、761、698、644、522/cm为海洛因盐酸盐的红外吸收。经进一步检验得知,该样品中海洛因盐酸盐与咖啡因的质量比为1:0.8。 样品2则是上海一起贩毒大案中缴获的毒品(公安部物证鉴定中心编为沪85号),经红外光谱检验,其红外光谱图与前两图相比较可以发现 3113、2955、1696、1658、1549、1449、1287、1241975、748、446、423/cm为咖啡因的红外吸收。3446、2955 2634 2086 1763 1735 1487、1241 1106、1037、975、910、873、798、696、571、472/cm为海洛因盐酸盐的红外吸收。
菌落总数是食品中重要的安全卫生指标,表示食品受细菌污染的程度。但很多人确不知道食品落菌总数的标准,上海尼那环保科技有限公司企业管理部摘录下,仅供参考。1、膨化食品的落菌总数标准依据国家强制性标准GB17401-2003《膨化食品卫生标准》规定,膨化食品的菌落总数应为≤10000cfu/g、大肠菌群应为≤90MPN/100g,超过国家标准规定可判断为不合格膨化食品。2、固体饮料的落菌总数标准依据国家强制性标准GB7101-2003《固体饮料卫生标准》规定,固体饮料产品的菌落总数应≤1000cfu/g;大肠菌群应≤90MPN/100g;霉菌应≤50cfu/g,超过国家标准规定可判断为不合格固体饮料。3、糕点、面包、月饼的落菌总数标准依据国家强制性标准GB 7099-2003《糕点、面包卫生标准》规定,月饼产品中菌落总数不得超过1500cfu/g,大肠菌群不得超过30MPN/100g,霉菌计数不得超过100cfu/g;蛋糕生产的标准要求:菌落总数≤10000cfu/g,大肠菌群≤300MPN/100g,霉菌≤150cfu/g,超过国家标准规定可判断为不合格糕点类产品。4、食醋的落菌总数标准依据国家强制性标准GB2719-2003《食醋卫生标准》规定,食醋中菌落总数不得超过10000cfu/mL ,超过国家标准规定可判断为不合格食醋。5、冷冻饮品的落菌总数标准依据国家强制性标准GB2759.1-2003《冷冻饮品卫生标准》规定,含淀粉或果类的冷冻饮品菌落总数应≤3000cfu/g,大肠菌群应≤100MPN/100g;含乳蛋的冷冻饮品的菌落总数应≤25000cfu/g,大肠菌群应≤450MPN/100g,超过国家标准规定可判断为不合格雪糕或冷饮。6、饼干的落菌总数标准依据国家强制性标准GB7100-2003《饼干卫生标准》规定,非夹心饼干的菌落总数不得超过750cfu/g,夹心饼干菌落总数不得超过2000cfu/g;饼干产品的霉菌计数不得超过50cfu/g,超过国家标准规定可判断为不合格饼干。7、巴氏杀菌、灭菌乳的落菌总数标准依据国家强制性标准GB19645 -2005《巴氏杀菌、灭菌乳卫生标准》规定,灭菌乳菌落总数不得超过10cfu/g,大肠菌群不得超过3MPN/100g,超过国家标准规定可判断为不合格乳制品。8、蜜饯的落菌总数标准依据国家强制性标准GB14884-2003《蜜饯卫生标准》规定,蜜饯食品中菌落总数不得超过1000cfu/g;霉菌不得超过50cfu/g,超过国家标准规定可判断为不合格乳蜜饯产品。9、调味品的落菌总数标准 依据SB/T10371-2003《鸡精调味料》标准规定,鸡精调味料中大肠菌群不得超过90MPN/100g,超过国家标准规定可判断为不合格鸡精产品。10、瓶装水的落菌总数标准依据国家强制性标准GB17324-2003《瓶装饮用纯净水卫生标准》规定,饮用纯净水的菌落总数应≤20cfu/ml,大肠菌群≤3MPN/100ml;强制性国家标准GB19298-2003《瓶(桶)装饮用水卫生标准》规定,饮用水的菌落总数应≤50 cfu/ml,大肠菌群应≤3MPN/100ml;强制性国家标准GB8537-1995《饮用天然矿泉水》规定,天然矿泉水的菌落总数为50cfu/ml,大肠菌群为0。若超过国家标准规定可判断为不合格纯净水或矿泉水。11、酱腌菜的落菌总数标准依据国家强制性标准GB2714-2003《酱腌菜卫生标准》规定,酱腌菜产品的大肠菌群不得超过30MPN/100g,若超过国家标准规定可判断为不合格酱腌菜。12、食糖的落菌总数标准依据国家强制性标准GB13104-2005《食糖卫生标准》规定,白砂糖、绵白糖的菌落总数不得超过100cfu/g,超过国家标准规定可判断为不合格糖制品。13、肉干、肉铺的落菌总数标准依据强制性国家标准GB2726-2005《熟肉制品卫生标准》规定,肉制品中大肠菌群不得超过30MPN/100g,超过国家标准规定可判断为不合格肉制品。14、油炸小食品的落菌总数标准依据国家强制性标准GB16565-2003 《油炸小食品卫生标准》规定,油炸类炒货大肠菌群为≤30MPN/100g,超过国家标准规定可判断为不合格炒货制品。15、果、蔬汁饮料的落菌总数标准依据国家强制性标准GB19297-2003《果、蔬汁饮料卫生标准》规定,果(蔬)汁及果(蔬)汁饮料产品的菌落总数不得超过100cfu/mL,酵母不得超过20cfu/mL,超过国家标准规定可判断为不合格果、蔬汁饮料。16、果冻的落菌总数标准依据国家强制性标准GB19299-2003《果冻卫生标准》规定,果冻中菌落总数≤100cfu/g、大肠菌群≤30MPN/100g,超过国家标准规定可判断为不合格果冻产品。17、黄酒的菌落总数标准依据国家强制性标准GB2758-2005《发酵酒卫生标准》规定,黄酒产品的菌落总数应≤50cfu/ml,超过国家标准规定可判断为不合格黄酒。18、芝麻酱的菌落总数标准依据国家标准规定芝麻酱产品的大肠菌群应≤90个/100g,超过国家标准规定可判断为不合格芝麻酱。19、碳酸饮料的菌落总数标准依据国家强制性标准GB2759.2-2003《碳酸饮料卫生标准》规定,碳酸饮料产品的酵母应≤10cfu/mL,菌落总数应≤100cfu/mL,大肠菌群应≤6MPN/100mL;超过国家标准规定可判断为不合格碳酸饮料。20、熟肉制品的菌落总数标准强制性国家标准GB2726-2005《熟肉制品卫生标准》规定,菌落总数标准限量值为≤30000cfu/g,超过国家标准规定可判断为不合格熟肉制品。21、豆制品及面筋的菌落总数标准依据国家强制性标准GB2711-2003《非发酵性豆制品及面筋卫生标准》规定,定型包装非发酵豆制品的菌落总数为≤750 cfu/g;依据国家强制性标准GB2712-2003《发酵性豆制品卫生标准》规定,定型包装发酵性豆制品的大肠菌群为≤30MPN/100g。若超过国家标准规定可判断为不合格豆制品或面筋。22、方便面的菌落总数标准依据国家强制性标准GB17400-2003《方便面卫生标准》规定,方便面的面块+调料菌落总数为≤50000cfu/g,大肠菌群为≤150 MPN/100g,超过国家标准规定可判断为不合格方便面。
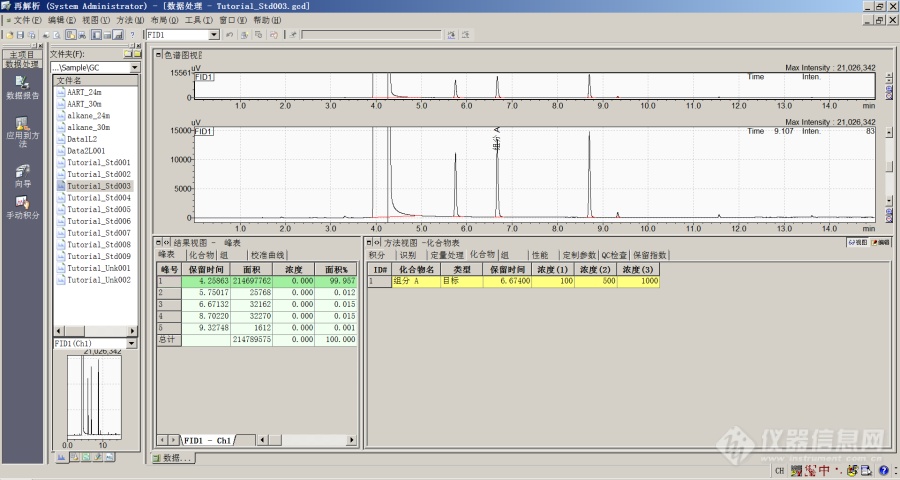
[color=black]Labsolution色谱数据工作站的系统适应性评价功能的使用方法[/color][align=center][color=black]概述[/color][/align][color=black]Labsolution色谱数据工作站系统适应性功能的使用方法[/color][align=center][color=black]背景介绍[/color][/align][color=black]色谱工作者在进行样品检测之前,通常需要确定色谱系统是有效和适用的,通常会使用分离度、柱效、拖尾因子和重复性来进行确认,对于医药行业的色谱工作者而言,这项要求尤其重要。[/color][color=black]目前实验室常见的色谱数据工作站均可以在色谱数据结果中出具分离度、理论塔板数、拖尾因子和重复性的数值,色谱工作者可以根据色谱数据工作站给出结果判定色谱系统适用性是否满足分析方法要求。[/color][color=black]使用Labsolution 系列色谱数据工作站的用户,可以利用工作站进行结果的评价。[/color][align=center][color=black]操作方法[/color][/align][color=black]例如某次实验分析获得三个标准数据文件——Std-001、Std-002、Std-003,分析方法对色谱数据中某组分的分离度要求大于1.5、拖尾因子要求小于1.6、理论塔板数要求大于2000。那么可以按照如下的顺序对数据文件进行处理:[/color][color=black]1 编制化合物表[/color][color=black]运行Labsolution的再解析模块,然后点击“数据处理”,打开任意一个标准数据文件,然后点击助手栏的“向导”图标,输入基本定量信息并编辑化合物表,如图1所示:[/color][img]https://ng1.17img.cn/bbsfiles/images/2021/09/202109212302334935_8950_1604036_3.png[/img][align=center]图1 化合物表视图[/align]2 编辑系统适应性计算信息[color=black]点击Labsolution色谱数据工作站菜单栏“方法”——“系统适应性设置”按钮,以理论塔板数为例,参照图2进行设置并保存成为方法文件(注意保存时一定需要选中“系统适应性设置”)。[/color][img]https://ng1.17img.cn/bbsfiles/images/2021/09/202109212302340002_7710_1604036_3.png[/img][align=center]图2 系统适应性设置[/align][color=black]3 编辑批处理表[/color][color=black]点击Labsolution色谱数据工作站的“批处理再解析”图标,编辑批处理表格,将需要进行计算的方法文件和数据文件添加到表格中,此外需要在批处理表格中添加系统适应性项目,并指定开始和结束行。[/color][img]https://ng1.17img.cn/bbsfiles/images/2021/09/202109212302342639_4066_1604036_3.png[/img][color=black]然后运行批处理表,即可得到系统适应性的评价报告。[/color][img]https://ng1.17img.cn/bbsfiles/images/2021/09/202109212302344036_2347_1604036_3.png[/img]
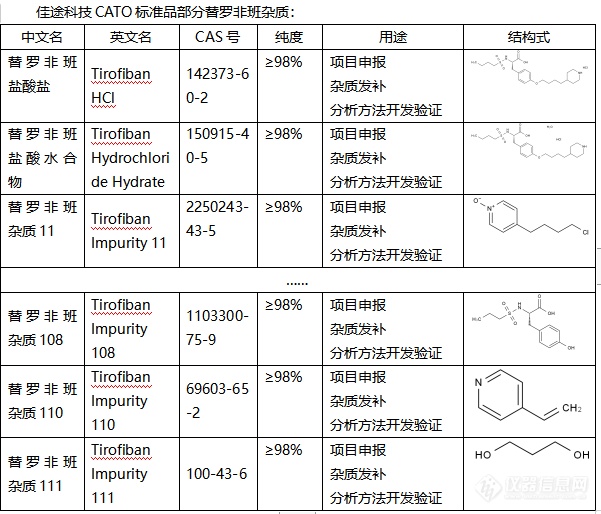
在当今的医疗领域,药物的质量控制至关重要,直接关系到患者的生命健康。替罗非班是一种广泛应用于心血管疾病治疗的药品,其质量控制尤为重要。而杂质分析作为药物质量控制的关键环节,能够准确评估药物的安全性和有效性。本文将重点探讨替罗非班杂质分析与CATO标准品应用研究的重要性。首先,杂质分析是确保药物质量的重要手段。在替罗非班的制备过程中,可能会产生一系列杂质,这些杂质的存在可能对药物的疗效和安全性产生不良影响。CATO标准品作为一种有效的分析工具,能够准确鉴定和量化替罗非班中的杂质,为药物的质量控制提供科学依据。其次,CATO标准品的应用有助于深入了解杂质的来源和性质。通过与标准品的比对分析,研究人员可以追溯杂质的产生途径,从而优化生产工艺,降低杂质的产生。此外,CATO标准品还可以用于评估杂质的毒性和风险,为药物的安全性评价提供有力支持。此外,CATO标准品在指导药物生产和改进方面也具有重要意义。通过对替罗非班中杂质的准确分析,生产商可以针对性地优化生产工艺、加强质量控制,从而提高药物的纯度和安全性。这不仅有助于保障患者的用药安全,还有助于提升企业的生产效益和市场竞争力。综上所述,替罗非班杂质分析与CATO标准品应用研究在药物质量控制中发挥着关键作用。通过深入研究替罗非班中的杂质,并借助CATO标准品这一强大工具,我们能够更好地了解杂质的来源、性质和影响,从而优化药物的生产工艺、提升药物的安全性和有效性。[img=,601,514]https://ng1.17img.cn/bbsfiles/images/2024/02/202402021849065001_3752_6381568_3.png!w601x514.jpg[/img]欢迎有需要的各位联系
有没有人做咖啡因的啊?现在我们公司想买咖啡因标准品,但是问了好几个地方,都说管制的,没法买。想问问大家哪里买的
12月1日起,多项与食品质量直接相关的国家标准将正式实施,其中既有《运动饮料》等涉及具体食品的产品标准,也有《婴幼儿配方粉企业良好生产规范》等涉及企业质量安全管理的生产标准,更有《保健食品中大豆异黄酮的测定方法 高效液相色谱法》等与食品安全相关的检测标准,还有《食品用塑料自粘保鲜膜》这样的包装标准和《塑料一次性餐饮具通用技术要求》这样的通用标准,它们将一起进入我国食品安全规范的大家庭,为食品安全保驾护航。 标准对兴奋剂等方面要求更严,运动饮料严禁添加世界反兴奋剂机构最新版规定的禁用物质。更新后的《运动饮料》将运动饮料定义为:“营养素及其含量能适应运动或体力活动人群的生理特点,能为机体补充水分、电解质和能量,可被迅速吸收的饮料”,首次强调运动饮料被机体迅速吸收的特点。 同时,新国标还取消了产品分类、对净含量的要求和“国际奥委会禁用物质”的附录。在理化指标上,放宽了钠和钾含量的范围,删除了抗坏血酸、硫胺素及其衍生物、核黄素及其衍生物、钙、镁等指标。同时,细化了卫生指标,要求铅含量≤0.3毫克/升;砷≤0.2毫克/升;每毫升样品中含有的菌落总数≤30000;不得检出致病菌。此前,我国尚未有一次性塑料餐具的国家标准,而是由每个企业制定企业标准,一次性塑料饭盒等不可降解餐具长期无标准可依,虽未明文禁止,却始终没有合法身份。12月1日起施行的国标《塑料一次性餐饮具通用技术要求》将彻底结束这一现状,长期不被认可的一次性塑料饭盒等不可降解餐具将有合法地位。 除此之外,标准还对一次性餐饮具的范围进行了明确的界定:是指预期用餐或类似用途的器具,包括一次性使用的餐盒、盘、碟、刀、叉、勺、筷子、碗、杯、罐、壶、吸管等,但不包括无预期用餐目的或类似用途的食品包装物,如生鲜食品托盘、酸奶杯、果冻杯等。同时,对餐饮具的耐热水性能、耐热油性能、漏水性能、负重性能以及微波炉耐温性能等,都作了具体的规定。 从12月1日起正式实施的国标《食品用塑料自粘保鲜膜》增加了对原料的技术要求,对于使用的树脂要求必须为“食品级”原料。而且,可用于包装食品的保鲜膜将标示“食品用”字样,并将标示出“不能接触带油脂食品”、“不得微波炉加热”、“不得高温使用”等警示性语言。 对于我国的广大婴幼儿配方企业来说,从12月1日起开始实施的国家标准《婴幼儿配方粉企业良好生产规范》,为其如何生产质量安全可靠的婴幼儿配方奶粉设定了“规矩”。该标准规定了婴幼儿配方生产企业在原材料采购、产品加工、包装及贮运等过程中,有关人员、建筑、设施、设备的设置,以及卫生、生产过程、产品品质等管理应达到的条件和要求,以确保提供安全、可靠、健康的产品。 以原材料为例,标准从原材料的采购与处理、原材料的卫生与质量管理等方面都进行了严格的规定,如标准规定,原料购进后对来源、规格、包装情况进行初步检查,按验收制度的规定填写入库账、卡,入库后应向质检部门申请取样检验。外包装有破损的原料应单独存放并有标示,在检验合格后方可使用。
[size=4] 近日,卫生部在其官方网站就乳品安全标准向社会公开征求意见,其中专门提出了婴儿[/size][color=#ff0033][size=4]配方[/size][/color][color=#ff0033][size=4]食品[/size][/color][size=4]安全标准,表明官方力图避免因监管手段缺失发生新的婴幼儿食品安全隐患的姿态。“在现阶段,中国乳品消费者希望获得的最大尊重是关于乳品是否安全优质的知情权和保障权。 早在去年底,卫生部就组织质检总局等十个有关部门,成立了乳品安全标准工作[/size][color=#ff0033][size=4]协调[/size][/color][size=4]小组和乳品安全标准工作专家组开展标准修订工作。经过[/size][color=#ff0033][size=4]系统[/size][/color][size=4]梳理,清理后的标准共三大类75项,意见稿同时还对乳清蛋白与酪蛋白比例、DHA和ARA的添加以及亚油酸、亚麻酸等做出相关规定。有分析人士认为,从相关标准的规范化建议来看,新标准在一定程度上参考了国内[/size][color=#ff0033][size=4]企业[/size][/color][size=4]的相应标准。以三元“爱力优”为例,在其科学设计的ilactou营养系统中,特别添加的FOS+GOS+Polyfructose益生元组合及多种有效成分,这在意见稿中均有不同程度的体现。专家表示,目前国内奶粉厂家基本都有一套自己的标准体系,新标准将在一定程度上推进中国奶粉产业的规范化进程。 [b]过硬的品质成就行业典范[/b] 三元不仅是在三聚氰胺事件中独善其身的企业,而且一直以苛刻的检验标准、严格的生产流程、不断加强质量安全[/size][color=#ff0033][size=4]管理[/size][/color][size=4],本着对消费者负责的态度去生产每一件产品。 三元的好奶源保证好品质。奶源的健康,是产品质量安全的源头。三元绿荷牧场的牛从选种、饲养到挤奶、检疫的全过程都要经过严格的生产认证。原奶进厂后,要经过20多项微生物快速检测机,检测合格的才能作为奶源。对奶源的层层把关,使三元60年无一重大意外出现,60年始终如一的做安全奶,做放心奶。 全面完善的质量监管体系。河北三元引进国内外先进的乳品生产设备,在乳品的生产、存储及配送过程中实行全程监测,严格按照国家标准及国家实施的食品质量安全市场准入制度组织生产,生产厂的全部设备都已实现自动化,这也是三元未来的发展目标。 责任书写大爱。河北三元对每一位员工强化企业的品牌意识、质量意识,真正将“质量是企业的生命”的观念灌输到每一位三元人心里。 三元是一家符合奥运标准和国庆标准、先后为北京奥运会和建国60年特供乳制品的企业,代表着中国企业的形象;作为行业领导者,三元肩负着引领中国乳业健康发展的重任;作为一个乳品企业,则需要通过持续不断地发展,为数以亿计的消费者提供安全放心的好牛奶。 [/size] [size=4][b]行业典范助力国家乳品质量标准[/b] 2010年,河北三元的质量检验与品质标准更是达到了中国乳业的领先水平,并在未来三年内还将继续推进企业自建牧场、托管牧场、大型的牧场园区、良种繁育中心、奶牛养殖大户等基地建设模式,打造世界一流的奶源基地,生产安全、优质的原奶,领衔行业质量安全管理,助力国家乳品质量标准的出台,树立行业典范。通过三元世界一流的加工技术为消费者提供一流品质的乳制品, 对此,有资深业内人士表示,如果说质量管理活动本身将再造河北三元的核心竞争力,那么河北三元开展的产业链控制将不可避免地成为其他乳企效仿的质量评估新标准,一场追求精确、追求适应本土的“标准化运动”将由此蔚然成风。 我们完全有理由相信,在新的乳品安全标准即将颁布的背景下,一个更规范、更持续的乳品行业即将来临。[/size]
来源:医药报讯 继欧盟和美国食品药品管理局(FDA)批准赛诺菲-安万特公司生产的血管紧张素Ⅱ受体拮抗剂厄尔沙坦作为第一个用于治疗合并高血压的2型糖尿病肾病的药物后,近日,国家食品药品监督管理局(SFDA)也批准将此类疾病作为厄尔沙坦的新适应证。这是迄今为止我国惟一获得SFDA批准的用于治疗2型糖尿病肾病合并高血压的药物。 糖尿病合并高血压是引起终末期肾病的最主要原因。将厄尔沙坦用于治疗2型糖尿病肾病合并高血压基于一个大规模的临床研究。该研究对590例2型糖尿病合并高血压并伴持续性微量白蛋白尿患者,进行了平均两年的随机分组研究。结果发现,厄尔沙坦300毫克组两年后发生糖尿病肾病的相对风险下降了70%,且患者肾病进展或死亡的危险性明显降低。 美国芝加哥医学院的Edmundlewis博士认为,厄尔沙坦被批准用于治疗2型糖尿病肾病合并高血压,意味着现在有了新的治疗措施来延缓肾脏疾病的进展,从而可使患者延缓或避免接受透析疗法或肾脏移植,标志着此类疾病在药物治疗上有了重大进步。
你购买过液相色谱系统适应性专用对照品吗,还是直接以含量用对照品来做,如阿莫西林?
维权声明:本文为luxw原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。 浅析EP(欧洲药典)、USP(美国药典)和CP(中国药典)的质量标准区别名词解读:EP: European Pharmacopeia欧洲药典,缩写为EP。为欧洲药品质量检测的指导文献。所有药品或原料的生产厂家在欧洲范围内销售和使用的过程中,必须遵循《欧洲药典》的质量标准。USP:U.S. Pharmacopeia 美国药典,缩写为USP。为美国药品质量检查的指导文献。出版时为U.S. Pharmacopeia / National Formulary《美国药典/国家处方集》(简称USP/NF)。CP:The People's Republic of China Pharmacopoeia中华人民共和国药典,缩写CP。为中国制药行业中药、西药、生物制品等质量检查的指导文献,分一部:中药、二部:西药、三部:生物制品。2010版将于10月1日起执行。 正文:由于其质量标准中药品的检测项目繁多,我就不一一来比较,只拿出相对较为复杂的“液相法含量测定”来进行简单的比较。知识水平有限、时间也不是很多,因此他们之间的许多不同可能没有发掘出来,还请大家和我一道,继续发掘、一起分析!EP和USP在一定程度是相通的,也就是说他们对于同一个药品的质量标准是相同的,但也不能排除有不同的情况,比如在流动相比例、检测波长上就有的品种不同。而他们对于CP来说,区别就很多了,我要描述的也主要是这个方面:色谱柱:CP一般的规定是填料,而对柱长、粒径等不做规定。那么,对我们而言,色谱柱的选择就成了一个问题,我们需要花时间去找柱子。而EP、USP,基本上就把柱子的长度、直径、粒径都规定好了。洗脱方法:EP、USP多采用梯度洗脱,配制起来比较复杂,稍微的ph值不适当或比例问题就会影响实验结果,且在标准中大多规定了主峰或相关杂质峰的保留时间,因此难度较大。而CP多采用等度洗脱,操作、试验都相对较容易。无论是梯度还是等度,只要把相关的物质分离出来就可以了。梯度洗脱费时、费力,但能把一般等度无法洗脱的有关物质分离出来,为保证科学的分析样品,此方法值得CP借鉴。样品溶解:EP、USP多流动相溶解样品的方式,CP多采用水溶解。用流动相溶解有利也有弊,利的是能够保证样品分析的准确性,弊的是流动相中有机试剂对人员的伤害很大,防护措施一定要做好。系统适应性:随着2010版药典的施行,CP的一些品种也增加了系统适应性的检测,尤其是有关物质的检查,但还是没有完全普及开来。而对于EP、USP来说,每个药品的标准都是含有系统适应性检测的,目的很简单:只有系统是合格的,才能保证接下来的实验是有效的。而对于系统适用性的样品,除了破坏得到外,还需要杂质对照品,因此在花费上比起CP来说,会高出许多。总结:以上几点就是我浅显的分析,稍微总结一下,如下:1. CP的方法更简单,对人员伤害小,但样品分析结果的说服力稍差;2. EP、USP对样品分析精确,尤其是在杂质分析方面:比如有的品种[fo
请问怎样用紫外可见分光光度计测乌洛托品的含量,标准曲线的溶液如何配制?
核心提示:GB2760-2011与GB2760-2007标准对比分析之一——食品分类系统卫生部在2011年第12号卫生部公告中发布了4项食品安全国家标准,其中之一即为《GB 2760-2011 食品安全国家标准 食品添加剂使用标准》(以下简称新标准),该新标准将于2011年6月20日起正式实施,新标准的前言中明确指出对2007版的《GB 2760-2007 食品添加剂使用卫生标准》(以下简称旧标准)部分食品分类系统进行了调整,为使广大网友对该新旧标准的食品分类系统的调整有更具体的了解,食品伙伴网对食品论坛中网友发布的相关讨论帖进行了整理,仅供行业人士参考,对比分析具体结果: 1、对比过程中发现如下问题:和旧标准相比新标准的食品分类系统中删除了01.01.02.01调味乳,但搜索发现表A1里有涉及到该分类号。 2、新增了如下食品分类:01.01.02 灭菌乳,同时将旧标准中的01.01.02 调制乳调整为01.01.03 调制乳。01.02 发酵乳和风味发酵乳,同时将旧标准中的01.02 发酵乳调整为01.02.01。01.02.02 风味发酵乳。同时删除了旧标准中的01.02.01、01.02.02。04.04.03 其他豆制品。06.05.02.04 粉圆。13.02.01 婴幼儿谷类辅助食品、13.02.02 婴幼儿罐装辅助食品。14.03.01.01 发酵型含乳饮料、14.03.01.02 配制型含乳饮料、14.03.01.03 乳酸菌饮料(旧标准中的分类号为14.07)、14.03.03 复合蛋白饮料。 3、调整了如下食品分类:将旧标准中03.02雪糕类删除,在新标准中将其合并到03.01冰淇淋类。将旧标准中如下分类删除05.02.03、05.02.04、05.02.05、05.02.06、05.02.07、05.02.08、05.02.08.01、05.02.08.02、05.02.09,合并到05.02.02。旧标准中14.07乳酸菌饮料调整为新标准的14.03.01.03 乳酸菌饮料。乳品的分类调整比较复杂,在其他几点中都有所涉及。 4、删除了如下食品分类:04.02.02.03.01 酱渍的蔬菜、04.02.02.03.02 盐渍的蔬菜、04.02.02.03.03 糖醋渍的蔬菜、04.02.02.03.04 其他腌渍的蔬菜。04.03.02.03.01酱渍的食用菌和藻类、04.03.02.03.02盐渍的食用菌和藻类、04.03.02.03.03糖醋渍的食用菌和藻类、04.03.02.03.04其他腌渍的食用菌和藻类。06.03.01.03 蛋糕预拌粉、06.03.01.04 其他专用粉。08.03.05.01 高温蒸煮肠、08.03.05.02 低温蒸煮肠、08.03.05.03 其他肉肠。14.01.02 自然来源饮用水、14.01.04 饮用矿物质水。16.05 油炸食品、16.05.01 油炸小食品、16.05.02 其他油炸食品。01.02.01 原味发酵乳(全脂、部分脱脂、脱脂)、01.02.02 调味和果料发酵乳。13.05.01 孕产妇(乳母)配方食品、13.05.02 运动营养食品(运动饮料除外)。 5、修改了如下食品分类名称:01.0 乳及乳制品(13.0 特殊营养用食品涉及品种除外)修改为乳及乳制品(13.0 特殊膳食用食品涉及品种除外)。01.01 乳及调制乳修改为巴氏杀菌乳、灭菌乳和调制乳。01.01.01 纯乳(全脂、部分脱脂、脱脂),包括复原乳修改为巴氏杀菌乳。01.03.01 乳粉(全脂奶粉、脱脂奶粉和部分脱脂奶粉)和奶油粉修改为乳粉和奶油粉04.04.01.01 豆腐类(北豆腐、南豆腐、内酯豆腐、冻豆腐)修改为豆腐类。04.05.02.01 烘焙/炒制坚果与籽类修改为熟制坚果与籽类。04.05.02.01.01带壳烘焙/炒制坚果与籽类修改为带壳熟制坚果与籽类。04.05.02.01.02脱壳烘焙/炒制坚果与籽类修改为脱壳熟制坚果与籽类。04.05.02.05 其他方法(如腌渍的果仁)修改为其他加工的坚果与籽类(如腌渍的果仁)。
http://www.greenherbs.com.cn/bbs/dispbbs.asp?boardid=2&Id=7651724918 唑吡坦杂质A CIV Zolpidem Related Compound A CIV 对照品/标准品1724907 酒石酸唑吡坦 CIV Zolpidem Tartrate CIV 对照品/标准品1724893 唑吡坦 CIV Zolpidem CIV 对照品/标准品1724805 盐酸唑拉西泮 Zolazepam Hydrochloride 对照品/标准品1724769 硫酸锌 Zinc Sulfate 对照品/标准品1724747 氧化锌 Zinc Oxide 对照品/标准品1724689 齐留通杂质C Zileuton Related Compound C 对照品/标准品1724678 齐留通杂质B Zileuton Related Compound B 对照品/标准品1724667 齐留通杂质 A Zileuton Related Compound A 对照品/标准品1724656 齐留通 Zileuton 对照品/标准品1724532 齐多夫定杂质C(胸腺嘧啶) Zidovudine Related Compound C (thymine) 对照品/标准品1724521 齐多夫定杂质B Zidovudine Related Compound B 对照品/标准品1724500 齐多夫定 Zidovudine 对照品/标准品1724317 扎西他滨杂质A Zalcitabine Related Compound A 对照品/标准品1724306 扎西他滨 Zalcitabine 对照品/标准品1724000 盐酸育亨宾 Yohimbine Hydrochloride 对照品/标准品1722005 木糖 Xylose 对照品/标准品1721002 盐酸赛洛唑啉 Xylometazoline Hydrochloride 对照品/标准品1720600 木糖醇 Xylitol 对照品/标准品1720429 盐酸赛拉嗪 Xylazine Hydrochloride 对照品/标准品1720407 赛拉嗪 Xylazine 对照品/标准品1720203 呫吨酮 Xanthone 对照品/标准品1720000 呫吨酸 Xanthanoic Acid 对照品/标准品1719102 华法林杂质 A Warfarin Related Compound A 对照品/标准品1719000 华法林 Warfarin 对照品/标准品1717708 牡荆素(牡荆甙) Vitexin 对照品/标准品1717504 含量测定系统适用性用维生素D Vitamin D Assay System Suitability 对照品/标准品1716002 维生素A Vitamin A 对照品/标准品1715000 硫酸紫霉素 Viomycin Sulfate 对照品/标准品1714528 长春瑞滨杂质A Vinorelbine Related Compound A 对照品/标准品1714506 酒石酸长春瑞滨 Vinorelbine Tartrate 对照品/标准品1714007 硫酸长春新碱 Vincristine Sulfate 对照品/标准品1713004 硫酸长春碱 Vinblastine Sulfate 对照品/标准品1711508 阿糖腺苷 Vidarabine 对照品/标准品1711472 维替泊芬杂质A Verteporfin Related Compound A 对照品/标准品1711461 维替泊芬 Verteporfin 对照品/标准品1711440 维拉帕米杂质F Verapamil Related Compound F 对照品/标准品1711439 维拉帕米杂质E Verapamil Related Compound E 对照品/标准品1711428 维拉帕米杂质D Verapamil Related Compound D 对照品/标准品1711406 维拉帕米杂质B Verapamil Related Compound B 对照品/标准品1711304 维拉帕米杂质A Verapamil Related Compound A 对照品/标准品1711224 维库溴铵杂质F Vecuronium Bromide Related Compound F 对照品/标准品1711202 盐酸维拉帕米 Verapamil Hydrochloride 对照品/标准品1711188 维库溴铵杂质C Vecuronium Bromide Related Compound C 对照品/标准品1711177 维库溴铵杂质B Vecuronium Bromide Related Compound B 对照品/标准品1711166 维库溴铵杂质A Vecuronium Bromide Related Compound A 对照品/标准品1711155 维库溴铵 Vecuronium Bromide 对照品/标准品1711133 赖氨加压素 Lypressin 对照品/标准品1711100 加压素 Vasopressin 对照品/标准品1711009 香草醛熔点标准品 Vanillin Melting Point Standard 对照品/标准品1710006 香草醛 Vanillin 对照品/标准品1709018 Vancomycin B with Monodechlorovancomycin 对照品/标准品1709007 盐酸万古霉素 Vancomycin Hydrochloride 对照品/标准品1708795 缬沙坦杂质 C Valsartan Related Compound C 对照品/标准品1708784 缬沙坦杂质 B Valsartan Related Compound B 对照品/标准品1708773 缬沙坦杂质 A Valsartan Related Compound A 对照品/标准品1708762 缬沙坦 Valsartan 对照品/标准品1708751 戊柔比星分离度用混合物 Valrubicin Resolution Mixture 对照品/标准品1708730 戊柔比星 Valrubicin 对照品/标准品1708729 丙戊酸杂质A Valproic Acid Related Compound A 对照品/标准品1708718 丙戊酸杂质 B Valproic Acid Related Compound B 对照品/标准品1708707 丙戊酸 Valproic Acid 对照品/标准品1708503 L- 缬氨酸 L-Valine 对照品/标准品1708015 D-缬更昔洛韦 D-Valganciclovir 对照品/标准品1708004 缬更昔洛韦盐酸盐 Valganciclovir Hydrochloride 对照品/标准品1707908 缬草烯酸 Valerenic Acid 对照品/标准品1707894 万乃洛韦杂质G Valacyclovir Related Compound G 对照品/标准品1707883 万乃洛韦杂质F Valacyclovir Related Compound F 对照品/标准品1707872 万乃洛韦杂质E Valacyclovir Related Compound E 对照品/标准品1707861 万乃洛韦杂质D Valacyclovir Related Compound D 对照品/标准品1707855 万乃洛韦杂质C Valacyclovir Related Compound C 对照品/标准品1707839 盐酸万乃洛韦 Valacyclovir Hydrochloride 对照品/标准品1707806 熊去氧胆酸 Ursodiol 对照品/标准品1706701 C13尿素 Urea C 13 对照品/标准品1706698 尿素 Urea 对照品/标准品1706009 乌拉莫司汀 Uracil Mustard 对照品/标准品1705800 阿糖尿苷 Uracil Arabinoside 对照品/标准品1705505 十一烯酸 Undecylenic Acid 对照品/标准品1705323 泛癸利酮杂质A Ubidecarenone Related Compound A 对照品/标准品1705312 系统适用性试验用泛癸利酮 Ubidecarenone for System Suitability 对照品/标准品1705301 泛癸利酮 Ubidecarenone 对照品/标准品1705006 L- 酪氨酸 L-Tyrosine 对照品/标准品1704003 泰洛沙泊 Tyloxapol 对照品/标准品1703850 酒石酸泰洛星 Tylosin Tartrate 对照品/标准品1703805 泰洛星 Tylosin 对照品/标准品1702008 氯筒箭毒碱 Tuboc

2010 版中国药典 VIII R 规定TOC分析仪是要定期进行系统适用性测试,GE为客户提供即开即用的液体系统适用性标准品,省心省力。8月15日-9月15日,GE携全国代理商惠馈客户,优惠活动如下:如果了解更多有关TOC的系统适用性测试知识,可以点击此处http://ng1.17img.cn/bbsfiles/images/2012/08/201208221014_385307_2359237_3.jpg
大家好,哪位身边有waters Empower系统适应性软件包,我们用的是waters2695,Empower2软件。我们老板出的价格不高,就当做助人为乐吧,最好是上海地区的,我邮箱 wfq342601@163.com
工作标准品质量标准的建立 要首先建立工作标准品的质量标准,总的原则是在原法定标准的基础上建立,该标准要严于药典标准。 法定标准品及标定检验方法:法定标准品是指USP、EP、CP等标准品的现行批号。要选择药典的检验方法。不同的标准采用不同的药典检验方法。 工作标准品质量标准的建立 要首先建立工作标准品的质量标准,总的原则是在原法定标准的基础上建立,该标准要严于药典标准。要将主成份含量提高,有关物质的限度降低,其它项目可不变。 一、工作标准品的标定 1、要按照工作标准品的质量标准进行标定检验。标定时要全检,复标时只测定含量。标定或复标合格后,经批准后,可用作工作标准品。如果选用了近期生产的质量较好的放行原料药作为工作标准品,标定时可以只测定含量。 2、如果标定的是USP工作标准品,那么标定时要使用USP现行批号的法定标准品,其它类推。 3、工作标准品的标定过程 A 若需要,应对标准品进行预处理(如干燥);B 选用两个熟练的人员进行标定;C 各称取一份法定标准品,三份样品;D 系统适应性试验应合格; E 同一化验员含量结果的RSD应不大于0.5%,不同化验员含量结果平均值的相对偏差应不大于0.3%; F 平均后作为标定结果 。 4、当无标准品时,自制工作标准品需按以下方法的进行标化:同一批号分别称取5份样品,每份样品进样两次,含量结果的RSD应不大于1.0%,经计算后的结果作为此自制标准品的纯度值。 5、此方法的每个平行样结果都必须符合己确立的指标时方可使用。此时,总平均值可用作自制标准品的纯度值。但此结果要考虑到水、残留溶剂或残渣的含量对结果的影响,要进行适当调整。 二、工作标准品的有效期及复标日期 1、工作标准品的有效期为两年(从标定之日起算,短于原料药的有效期)。 2、工作标准品含量每半年复标一次。 3、工作标准品的批号在原料药的批号后加-RS,作为工作对照品的批号。如:110727-RS。
有没有参加中检院保健食品中阿替洛尔能力验证,交流下
求二氧化锡XRD标准卡,谢谢啦
【网络讲堂】:安捷伦科技GPC/SEC柱和标准品及其应用介绍【讲座时间】:2015年01月20日 10:00【主讲人】:雷启福 (苏州大学药理学博士。先后在睿智化学、默克化工等企业进行药物分析以及色谱分离技术研究。加入安捷伦科技以后,专注于色谱分离技术的应用和技术支持,在制药、化工等领域积攒了丰富的经验。)【会议简介】Polymer Lab是一家专注于聚合物分析的专业化公司,不仅在GPC分析仪器,及其GPC柱和标准样品领域一直占据第一的位置。在2010年安捷伦将其纳入麾下后,大大补充了GPC和SEC的生产线。这次的在线讲堂将会给大家带来的内容是GPC方法优化、GPC和SEC柱及标准品,和其在化工、食品、制药等领域的应用。-------------------------------------------------------------------------------1、报名条件:只要您是仪器网注册用户均可报名参加。2、报名并参会用户有机会获得100元手机充值卡一张哦~3、报名截止时间:2015年01月20日 09:304、报名参会: http://www.instrument.com.cn/webinar/meeting/meetingInsidePage/13095、报名及参会咨询:QQ群—231246773
2014年12月24日,国家卫生计生委发布《食品安全国家标准 食品添加剂使用标准》(GB 2760-2014)(2014年第21号公告),该标准将于2015年5月24日实施并替代2011年版。 与2011年版相比,新版GB 2760涉及食品用香料香精部分的主要变化有以下几点: 第一,允许使用食品用香料品种数量发生变化,删除了八角茴香、牛至、甘草根、中国肉桂、丁香、众香子、莳萝籽等天然香料品种;增加了异戊酸异丙酯等24种合成香料。 第二,不得添加食品用香料、香精的食品名单发生变化,增加“16.02.01茶叶、咖啡”。 第三,部分香料名称发生变化。如:“杭白菊油”修改为“杭白菊花油”。 第四,引用标准发生变化。如食品用香精标签应符合相关标准规定。
中新网10月21日电 卫生部日前在其官方网站就乳品安全标准公开征求意见。征求意见稿中专门提出了婴儿配方食品安全标准。卫生部指出,要力图避免因监管手段缺失发生新的婴幼儿食品安全隐患。尽管国际食品法典委员会允许使用水解蛋白质或单体氨基酸防止过敏体质的婴儿对蛋白质过敏,但考虑到配套食品安全监管手段等现实问题,此次标准修订中持谨慎态度,力图避免因监管手段缺失发生新的婴幼儿食品安全隐患。乳清蛋白与酪蛋白比例规定可以在一定程度上保证产品的乳的来源,征求意见稿对此进行了规定。国际食品法典委员会(CAC)和多数国家将DHA和ARA作为可选择添加成分,设置了最高添加量。目前尚没有充分的科学依据来确定DHA和ARA的最低限量,欧盟0.2%最低限量也是标签声称的要求,中国现有标签标准已明确DHA和ARA的标示规定。征求意见稿同时规定了供人体内合成DHA和ARA的前体物质亚油酸、亚麻酸等脂肪酸规定。对于生产过程的环境控制问题,考虑到沙门氏菌、阪崎肠杆菌作为常见的致病菌对婴幼儿,尤其是6月龄以下婴儿条件致病性,标准征求意见稿做出相应规定。对于工艺参数及指标问题,考虑到不同的乳制品产品的生产工艺、生产设备等方面差别很大,标准征求意见稿对与安全密切相关的关键控制点设置了具体的参数要求。从2008年12月开始,卫生部牵头,会同十部门开展乳品安全标准制修订工作。经过系统梳理,目前中国各种乳品质量安全相关的标准共160余项(含已发布和正在制订过程中)。通过分析标准存在的问题,开展与国际标准的对比研究,并结合中国生产和消费的国情,提出了新的乳品质量安全标准框架和目录。清理后的标准共三大类75项,分为产品标准17项、生产规范2项、检验方法标准56项。
[b][font=宋体]问题描述:系统适应性试验是怎样做的?每做一批样都需要进[/font]5[font=宋体]针对照吗?[/font][font=宋体]解答:[/font][/b][font=宋体]([/font]1[font=宋体])《中国药典》规定高效液相色谱法色谱系统适应性试验应包括:色谱柱的理论塔板数、分离度、重复性和拖尾因子。[/font][font=宋体]([/font]2[font=宋体])理论塔板数通常反映色谱柱的分离效率(简称柱效),《中国药典》中不同物质的最低理论塔板要求不一样。理论塔板数取决于固定相的种类、性质(粒度、粒径分布等)、填充状况、柱长、流动相的种类和流速及测定柱效所用物质的性质。[/font][font=宋体]([/font]3[font=宋体])分离度是判断两物质在一个方法中分离的程度,虽然与柱效相关,但在衡量系统适用性时,首先强调的应该是分离度,只有当色谱图中仅有一个色谱峰或测定微量成分时,规定柱效才有其特殊重要性。[/font][font=宋体]([/font]4[font=宋体])重现性保证了方法的可重复性,拖尾因子对柱效提出了要求,柱子老化、塌陷,拖尾因子则难以达到要求。[/font][font=宋体]([/font]5[font=宋体])在进行高效液相色谱系统适应性试验时,除了重复性要求测定五次外其余参数没有要求进样次数。[/font][font=宋体]([/font]6[font=宋体])除非另有规定,系统适应性参数由待测组分的数据计算,目前大部分工作站都能直接获得理论塔板数、分离度、拖尾因子等系统适应性数据。配置系统适应性试验待测溶液时,溶液中包含一定量的待测组分和一些其它物质(如药品辅料或杂质)。当色谱系统有显著变化或者要用特殊试剂时,则要重新做系统适应性实验。只有系统适应性试验符合规定的要求,才能将液相色谱方法用于检测。[/font][font='微软雅黑','sans-serif'][color=black][back=white]领取更多《实战宝典》请进:[url]http://instrument-vip.mikecrm.com/2bbmrpI[/url][/back][/color][/font][font='微软雅黑','sans-serif'][color=black][back=white] [/back][/color][/font]