[color=#444444]有网友问,最近我需要检测大量样品中的紫檀芪含量。常规的检测方法是用高效液相色谱分析,但由于此次检测规模大,因此需要找一种更加简便的方法。于是我们老师让我看看紫檀芪这种物质是否有荧光现象,如果有的话就可以通过测荧光强弱来判断样品中的紫檀芪浓度大小。我在网上找了很多资料,没有有关紫檀芪荧光效应的介绍,请问谁做过这方面检测或荧光判断浓度大小的。[/color]
检测黄芪药材中的黄芪甲苷,用elsd检测器,c18柱,雾化管30 漂移管70 药典方法乙腈比水32比68 对照品塔板数11000,但是样品塔板数才2800,含量合格,要求塔板数是4000这是怎么回事,重做了好多次塔板数就是上不去
国内最大最专业的国家标准物质服务平台坛墨质检-国家标准物质中心(北京坛墨质检科技有限公司),是国家质检总局指定的国家标准物质研制单位,是国内最大最专业的食品、环境、职业卫生标准物质生产商和服务商。BW6104 6-羟基芹菜素-6-O-葡萄糖-7-O-葡萄糖醛酸苷,对照品,有报告 HPLC≥98% BW6105 6-羟基山奈酚-3,6,7-三-O-葡萄糖苷,对照品,有报告 HPLC≥98% BW6106 6-羟基山奈酚-3-O-芸香糖-6-O-葡萄糖苷,对照品,有报告 HPLC≥98% BW6107 多根乌头碱,对照品,有报告 HPLC≥98% BW6108 塔拉萨敏/塔拉乌头胺,对照品,有报告 HPLC≥98% BW6109 德尔塔林,对照品,有报告 HPLC≥98% BW6110 硬飞燕草碱,对照品,有报告 HPLC≥98% BW6111 尼奥林/雪上一支蒿乙素,对照品,有报告 HPLC≥98% BW6112 10-羟基乌头碱,对照品,有报告 HPLC≥96% BW6113 13-去羟基印乌碱,对照品,有报告 HPLC≥98% BW6114 黄芪甲苷/黄芪皂苷IV,对照品,有报告 HPLC≥98% BW6115 异黄芪皂苷I,对照品,有报告 HPLC≥98% BW6116 异黄芪皂苷II,对照品,有报告 HPLC≥98% BW6117 (3β,6α,16β,20R,24S)-3-O--20, 24-环氧-16,25-二羟基-9,19-环羊毛甾烷-6-O-葡萄糖苷,对照品,有报告 HPLC≥97% BW6118 Cyclocephaloside II HPLC≥98% BW6119 罗汉果皂苷IVa,对照品,有证书 HPLC≥98% BW6120 异-罗汉果皂苷V,对照品,有报告 HPLC≥98% BW6121 罗汉果皂苷IIIA1,对照品,有报告 HPLC≥98% BW6122 罗汉果皂苷IIA2 HPLC≥98% BW6123 罗汉果皂苷IIIe HPLC≥98% BW6124 罗汉果黄素,对照品,有报告 HPLC≥98% BW6125 11-0-罗汉果苷V HPLC≥98% BW6126 罗汉果苷IV/罗汉果皂苷IVe,对照品,有报告 HPLC≥98% BW6127 赛门苷I,对照品,有报告 HPLC≥98% BW6128 罗汉果苷VI HPLC≥90% 坛墨质检现有员工79人,办公室面积450平米,实验室1650平米;销售、客服、财务及行政人员35人,实验室工作人员21人,库房14人,市场部8人。实验仪器设备:气相色谱、液相色谱、气质联用、液质联用、离子色谱、紫外分光光度计,原子吸收、ICP-OES和ICP-MS;库房面积450平米,库房工作人员12人,现货产品5万个,坛墨质检自主研发的产品近3000个,已申报国标345项,填补国内空白的产品达到65项。坛墨质检是国内唯一提供标准溶液定制服务的标准物质研制单位,定制范围:特殊浓度定制、特殊溶剂定制、混标定制。
黄芪静脉输液中黄芪甲苷和黄芪多糖的含量测定摘要:建立黄芪静脉输液中黄芪甲苷和黄芪多糖的含量测定方法。方法:用高效液相色谱法测定黄芪甲苷的含量,用碘量法测定黄芪多糖的含量。结果:黄芪甲苷和黄芪多糖的平均回收率分别为9751%、9918%,相对标准差分别为248%、191%。结论:本文建立的方法准确可靠、灵敏度高、重现性好,可作为黄芪静脉输[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]量控制的有效方法。关键词:黄芪甲苷;黄芪多糖;高效液相色谱法;碘量法; 英文摘要:ToestablishthemethodfordeterminationofastragalosideIVandastragaluspolysaccharidesinRadixAstragaliinjectionMETHODS:AstragalosidewasdeterminedbyHPLCandastragaluspolysaccharidesbyiodometryRESULTS:Therecoveriesofastragalosideandastragaluspolysaccharideswere9751%RSD=248%and9918%(RSD=191%)respectivelyCONCLUSION:Thismethodisaccurate,sensitiveandrepeatable,andcanbeusedforqualitycontrolofthepreparation英文关键词:astragaloside;astragaluspolysaccharide;HPLC;iodometry;contentdetermination黄芪为补气药,性甘温,归肺、脾经,具有补气固表、利尿托毒、排脓、敛疮生肌之功效。医疗实践证明,黄芪注射液对心气虚损、血脉瘀阻、病毒性心肌炎、心功能不全、脾虚困湿之肝炎有较好的疗效,也是肿瘤、免疫功能低下等较理想的辅助治疗药物。目前临床所使用的黄芪注射液为小容量针剂,需稀释后滴注,且不含黄芪多糖,所以疗效不够理想。为此,武警四川总队乐山医院和四川省乐山市三民药物研究所共同研制了含黄芪多糖、黄酮、苷类等有效成分的黄芪静脉输液。黄芪注射液的含量检测尽管WS3-β-3335-98执行标准仅要求采用薄层色谱法,但因高效液相色谱法操作更简便,精密度更高,故笔者参照文献以蒸发光散色高效液相色谱法[1]测定黄芪静脉输液中的黄芪甲苷含量;至于黄芪多糖含量的检测则选择采用碘量法。1仪器与试药11仪器美国奥泰公司高效液相色谱仪,包括蒸发光散射(ELSD)500检测器、Alltech426主机泵;电动离心机(江苏金坛公司);TP-150超声波清洗机(北京天鹏公司)。12试药黄芪甲苷对照品(中国药品生物制品检定所,批号:0781-9908);甲醇、乙醇、正丁醇、氢氧化钠、硫酸、葡萄糖均为分析纯;乙腈为色谱纯;水为重蒸馏水。2方法和结果21黄芪甲苷含量的测定211色谱条件:色谱柱为ODS柱(250mm×40mm),柱温为40℃,流动相为乙腈-水(36∶64),流速为06ml/min,进样量为20μl。212漂移管温度选择:根据ELDS检测使用手册推荐,设置气体流速为300slpm,漂移管温度为75℃,观察流动相(不进样)进入检测器的基线噪音,不断改变漂移管温度(步长为5℃),根据基线随温度的变化情况,选择95℃为试验最优温度。213载气流速选择:设定漂移管温度为95℃,取黄芪甲苷对照液恒量,得相应峰面积,不断改变气体流速(步长为025slpm)观察峰面积和基线的变化情况,最终选择270slpm为试验最优载气流速。214最低检测限试验:精密称取黄芪甲苷对照品适量,加甲醇溶解并稀释成浓度为1mg/ml的溶液作为贮备液,精密量取适量,逐步稀释测定,直到黄芪甲苷主峰信号为检测器噪声水平的3倍为止。得黄芪甲苷最低检测限为153ng。215线性试验:取“214”项黄芪甲苷对照品贮备液适量,精密量取10、20、30、40、50、60分别置于10ml容量瓶中,加甲醇稀释至刻度(约相当于黄芪甲苷01、02、03、04、05、06mg)。以对照品峰面积的常用对数值为横坐标(X),以进样量的常用对数值(Y)为纵坐标进行线性回归,得回归方程为Y=06001X—34896(r=09991),黄芪甲苷进样量在20μg~120μg范围内线性关系良好。216精密度试验:精密称取黄芪甲苷对照品适量,加甲醇溶解并稀释至浓度为025mg/ml的溶液作为对照溶液,注入液相色谱仪,连续重复进样6次,测得黄芪甲苷的相对标准差为179%,精密度符合规定。217重现性试验:精密量取黄芪注射液适量(相当于黄芪甲苷约20mg)5份,按“2110”项下方法制备,测定黄芪甲苷含量。结果黄芪注射液中黄芪甲苷为2390mg,RSD=201%,表明方法重现性良好。218稳定性试验:取“217”项下样品溶液,分别于0、1、2、3、5、8h取样测定峰面积,结果RSD=107%,表明黄芪甲苷溶液在8h内基本稳定。219回收率试验:分别精密量取黄芪注射液适量(约相当于黄芪甲苷10、12、14mg)共3份,每份各精密加入对照溶液(0404mg/ml)25、30、35ml,按“2110”项下方法制备,测定黄芪甲苷含量,结果详见表1。由表1可见,平均回收率为9751%,RSD=248%,符合规定,说明方法具有可行性。2110样品中黄芪甲苷的含量测定:精密量取黄芪注射液100ml,置于烧杯中浓缩至10ml,加无水乙醇40ml沉淀,放置20min,离心,沉淀用80%的乙醇溶液洗涤2次,每次10ml,合并离心液与洗涤液,置水浴上蒸干。残渣加1%NaOH溶液10ml溶解,用饱和的正丁醇水溶液提取3次,每次20ml,合并正丁醇的水溶液,蒸干,残渣再加1%NaOH溶液5ml溶解,通过已处理的D101大孔吸附树脂柱(Φ15×20cm,内装树脂高约10cm)吸附,以1%NaOH溶液50ml洗脱,弃去,用蒸馏水洗至中性,再用30%乙醇溶液50ml洗脱,弃去洗脱液,继续用70%乙醇液50ml洗脱,收集洗脱液并蒸干,残渣加甲醇溶解并定容至10ml,得供试品溶液。精密称取黄芪甲苷对照品适量,加甲醇溶解并稀释成浓度为01、03mg/ml的溶液作为对照溶液。分别精密量取上述溶液各20μl注入液相色谱仪,记录色谱图,并以峰面积和进样量的对数值按二点法计算,详见图1;3批样品按上述方法制备测定,结果详见表2。22黄芪多糖含量的测定[2,3]221线性试验:精密称取105℃干燥至恒重的葡萄糖适量,加水溶解并稀释成浓度为10mg/ml的标准溶液,分别精密量取此标准溶液100、90、80、70、60ml,置于250ml碘量瓶中,分别加水0、10、20、30、40ml,然后精密加入01mol/L碘滴定液25ml,在不断振摇的情况下缓缓滴加01mol/LNaOH40ml,密塞,在暗处放置10min,然后加入05mol/LH2SO4液6ml,摇匀,立即用01mol/LNa2S2O3滴定液滴定,近终点时,加淀粉指示液2ml,继续滴定至蓝色消失,并同时作空白试验校正。以取样量(X)与Na2S2O3的消耗量(Y)进行线性回归,得回归方程为Y=009766X—000244,(r=09999),表明葡萄糖在60mg~100mg的范围内线性关系良好。222重现性试验:精密量取黄芪注射液100ml,按“224”项下方法制备5份,测定黄芪多糖含量,结果为10423mg,RSD=099%,表明方法重现性良好。223回收率试验:分别精密量取黄芪注射液(多糖含量为10423mg/100ml)120、150、180ml,每份各加入葡萄糖标准液(25002mg/ml)50、60、70ml制成80%、100%、120%浓度的溶液。分别浓缩至10ml,加无水乙醇40ml,放置20min,离心。沉淀用80%乙醇洗涤2次,每次10ml,弃去离心液与洗涤液,沉淀加热蒸馏水10ml溶解,并转移至25ml容量瓶中,定容,摇匀。分别精密量取3种不同浓度的溶液80、70、60ml置于250ml碘量瓶中,分别精密加水2、3、4ml,按“224”项方法测定,每个浓度测定3次,共9次,计算得到回收率为9918%,RSD=191%,详见表3。224样品中黄芪多糖的含量测定:精密量取黄芪注射液100ml,浓缩至10ml,加无水乙醇40ml,放置20min,离心。沉淀用80%乙醇洗涤2次,每次10ml,加热蒸馏水3ml使沉淀溶解并定容至10ml,摇匀。移置于250ml碘量瓶中,加入1mol/LH2SO420ml,置于水浴中水解2h,取出,放冷,加入2mol/LNaOH溶液调节pH值=7,冷却至室温。精密加入碘滴定液(01mol/L)25ml,在不断振摇的情况下缓缓滴加01mol/LNaOH40ml,密塞,置暗处放置10min。然后加入05mol/LH2SO46ml,摇匀,立即用Na2S2O3滴定液(01mol/L)滴定,至近终点时,加淀粉指示液2ml,继续滴定至蓝色消失,并同时作空白试验校正,计算即得(每1ml上述碘滴定液相当于9008mg的C6H12O6)。3批黄芪注射液样品,按上述方法测定多糖含量均符合规定,结果详见表4。3讨论测定黄芪甲苷含量时,如将精密量取的黄芪注射液浓缩后仅采用正丁醇的水饱合液提取制得供试品溶液,则所得的样品杂质峰多,基线略有漂移,因此不宜采用。黄芪多糖主要为葡萄糖,因此,可采用以葡萄糖或葡聚糖作对照品的苯酚-浓硫酸法[4]、蒽酮-浓硫酸法[5]或水解后用碘量法等测定其含量,但一般多采用后两种方法。采用蒽酮-浓硫酸法时,由于其线性试验回归方程为C=98481A+08314(r=09663),浓度线性范围为35~165μg/ml,线性关系不好,故不宜采用。
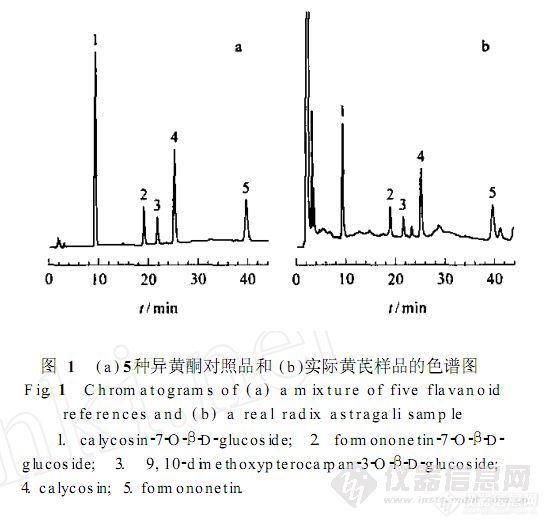
【作者】 王晓辉; 刘涛; 李清; 陈晓辉; 毕开顺;【Author】 WANG Xiaohui,LIU Tao,LI Qing,CHEN Xiaohui,BI Kaishun(School of Pharmacy,Shenyang Pharmaceutical University,Shenyang 110016,China)【机构】 沈阳药科大学药学院; 沈阳药科大学药学院 辽宁沈阳110016; 辽宁沈阳110016;【摘要】 对蒙古黄芪中5种异黄酮类成分的含量进行了反相高效液相色谱法测定。色谱柱为D iam ons il C18柱,流动相为乙腈-水系统,梯度洗脱,检测波长230nm,柱温35℃。毛蕊异黄酮-7-O-β-D-葡萄糖苷在20.12~201.2m g/L、芒丙花素-7-O-β-D-葡萄糖苷在4.62~46.2m g/L、9,10-二甲氧基紫檀烷-3-O-β-D-葡萄糖苷在4.86~48.6m g/L、毛蕊异黄酮在9.24~92.4m g/L、芒丙花素在6.92~69.2m g/L时峰面积与浓度呈良好的线性关系,相关系数分别为0.999 2,0.999 7,0.999 7,0.999 5和0.999 5。5种成分的加样回收率均高于94%,相对标准偏差(RSD)小于3.2%(n=9)。该法简便快速,重复性良好,结果准确可靠,可用于黄芪药材中5种主要异黄酮类成分的含量测定。 http://ng1.17img.cn/bbsfiles/images/2012/07/201207301613_380608_2379123_3.jpg
国内最大最专业的国家标准物质服务平台坛墨质检-国家标准物质中心(北京坛墨质检科技有限公司),是国家质检总局指定的国家标准物质研制单位,是国内最大最专业的食品、环境、职业卫生标准物质生产商和服务商。 产品编号 产品名称 标准值 BW61066-羟基山奈酚-3-O-芸香糖-6-O-葡萄糖苷,对照品,有报告HPLC≥98%BW6108塔拉萨敏/塔拉乌头胺,对照品,有报告HPLC≥98%BW6109德尔塔林,对照品,有报告HPLC≥98%BW6110硬飞燕草碱,对照品,有报告HPLC≥98%BW6111尼奥林/雪上一支蒿乙素,对照品,有报告HPLC≥98%BW611210-羟基乌头碱,对照品,有报告HPLC≥96%BW611313-去羟基印乌碱,对照品,有报告HPLC≥98%BW6114黄芪甲苷/黄芪皂苷IV,对照品,有报告HPLC≥98%BW6115异黄芪皂苷I,对照品,有报告HPLC≥98%BW6116异黄芪皂苷II,对照品,有报告HPLC≥98%BW6117(3β,6α,16β,20R,24S)-3-O--20, 24-环氧-16,25-二羟基-9,19-环羊毛甾烷-6-O-葡萄糖苷,对照品,有报告HPLC≥97%BW6118Cyclocephaloside IIHPLC≥98%BW6119罗汉果皂苷IVa,对照品,有证书HPLC≥98%BW6120异-罗汉果皂苷V,对照品,有报告HPLC≥98%BW6121罗汉果皂苷IIIA1,对照品,有报告HPLC≥98%BW6122罗汉果皂苷IIA2HPLC≥98%BW6123罗汉果皂苷IIIeHPLC≥98%BW6124罗汉果黄素,对照品,有报告HPLC≥98%BW6126罗汉果苷IV/罗汉果皂苷IVe,对照品,有报告HPLC≥98%BW612511-0-罗汉果苷VHPLC≥98%BW6127赛门苷I,对照品,有报告HPLC≥98%BW6128罗汉果苷VIHPLC≥90%BW6129罗汉果苷III,对照品,有证书HPLC≥98%BW6130拟人参皂苷Rh2,对照品,有证书HPLC≥98%BW6131(S型)原人参三醇,对照品,有报告HPLC≥98% 坛墨质检现有员工79人,办公室面积450平米,实验室1650平米;销售、客服、财务及行政人员35人,实验室工作人员21人,库房14人,市场部8人。实验仪器设备:气相色谱、液相色谱、气质联用、液质联用、离子色谱、紫外分光光度计,原子吸收、ICP-OES和ICP-MS;库房面积450平米,库房工作人员12人,现货产品5万个,坛墨质检自主研发的产品近3000个,已申报国标345项,填补国内空白的产品达到65项。坛墨质检是国内唯一提供标准溶液定制服务的标准物质研制单位,定制范围:特殊浓度定制、特殊溶剂定制、混标定制。
国内最大最专业的国家标准物质服务平台坛墨质检-国家标准物质中心(北京坛墨质检科技有限公司),是国家质检总局指定的国家标准物质研制单位,是国内最大最专业的食品、环境、职业卫生标准物质生产商和服务商。 产品编号 产品名称 标准值 BW5171灵芝酸A对照品,有报告HPLC≥98%BW5172隐丹参酮对照品,有报告HPLC≥98%BW5177黄芪总皂苷对照品,有报告UV≥98%BW5178黄芪皂苷I对照品,有报告HPLC≥98%BW5179黄芪皂苷II对照品,有报告HPLC≥98%BW5180黄芪皂苷III对照品,有报告HPLC≥98%BW5183络塞琳对照品,有报告HPLC≥98%BW5184络塞维对照品,有报告HPLC≥98%BW5185络缌对照品,有报告HPLC≥98%BW5186络塞定对照品,有报告HPLC≥98%BW5202盐酸氨基葡萄糖对照品,有报告HPLC≥98%BW5206雷公藤内酯甲;雷公藤酯甲对照品,有报告HPLC≥98%BW5210青蒿素对照品,有报告HPLC≥96%BW5214盐酸育亨宾;17alpha-羟基育亨烷-16alpha-羧酸甲酯盐酸盐对照品,有报告HPLC≥98%BW5216金雀花碱;野靛碱对照品,有报告HPLC≥98%BW5220原薯蓣皂苷;原薯蓣皂甙对照品,有报告HPLC≥98%BW5225芸香柚皮苷对照品,有报告HPLC≥98%BW5242氯化黄连碱;盐酸黄连碱对照品,有报告HPLC≥98%BW5244银杏内酯A对照品,有报告HPLC≥98%BW5245银杏内酯B对照品,有报告HPLC≥98%BW5246银杏内酯C对照品,有报告HPLC≥98%BW5264川芎嗪对照品,有报告HPLC≥98%BW5268羟基积雪草苷对照品,有报告HPLC≥98%BW5269积雪草酸对照品,有报告HPLC≥98%BW5270羟基积雪草酸对照品,有报告HPLC≥98% 坛墨质检现有员工79人,办公室面积450平米,实验室1650平米;销售、客服、财务及行政人员35人,实验室工作人员21人,库房14人,市场部8人。实验仪器设备:气相色谱、液相色谱、气质联用、液质联用、离子色谱、紫外分光光度计,原子吸收、ICP-OES和ICP-MS;库房面积450平米,库房工作人员12人,现货产品5万个,坛墨质检自主研发的产品近3000个,已申报国标345项,填补国内空白的产品达到65项。坛墨质检是国内唯一提供标准溶液定制服务的标准物质研制单位,定制范围:特殊浓度定制、特殊溶剂定制、混标定制。
国内最大最专业的国家标准物质服务平台坛墨质检-国家标准物质中心(北京坛墨质检科技有限公司),是国家质检总局指定的国家标准物质研制单位,是国内最大最专业的食品、环境、职业卫生标准物质生产商和服务商。 BW6109德尔塔林,对照品,有报告HPLC≥98%BW6110硬飞燕草碱,对照品,有报告HPLC≥98%BW6111尼奥林/雪上一支蒿乙素,对照品,有报告HPLC≥98%BW611210-羟基乌头碱,对照品,有报告HPLC≥96%BW611313-去羟基印乌碱,对照品,有报告HPLC≥98%BW6114黄芪甲苷/黄芪皂苷IV,对照品,有报告HPLC≥98%BW6115异黄芪皂苷I,对照品,有报告HPLC≥98%BW6116异黄芪皂苷II,对照品,有报告HPLC≥98%BW6117(3β,6α,16β,20R,24S)-3-O--20, 24-环氧-16,25-二羟基-9,19-环羊毛甾烷-6-O-葡萄糖苷,对照品,有报告HPLC≥97%BW6118Cyclocephaloside IIHPLC≥98%BW6119罗汉果皂苷IVa,对照品,有证书HPLC≥98%BW6120异-罗汉果皂苷V,对照品,有报告HPLC≥98%BW6121罗汉果皂苷IIIA1,对照品,有报告HPLC≥98%BW6122罗汉果皂苷IIA2HPLC≥98%BW6123罗汉果皂苷IIIeHPLC≥98%BW6124罗汉果黄素,对照品,有报告HPLC≥98%BW6126罗汉果苷IV/罗汉果皂苷IVe,对照品,有报告HPLC≥98%BW612511-0-罗汉果苷VHPLC≥98%BW6127赛门苷I,对照品,有报告HPLC≥98%BW6128罗汉果苷VIHPLC≥90%BW6129罗汉果苷III,对照品,有证书HPLC≥98%BW6130拟人参皂苷Rh2,对照品,有证书HPLC≥98%BW6131(S型)原人参三醇,对照品,有报告HPLC≥98%BW6132(R型)人参皂苷Rh1HPLC≥98%BW6133(R型)人参皂苷Rh2,对照品,有报告HPLC≥96% 坛墨质检现有员工79人,办公室面积450平米,实验室1650平米;销售、客服、财务及行政人员35人,实验室工作人员21人,库房14人,市场部8人。实验仪器设备:气相色谱、液相色谱、气质联用、液质联用、离子色谱、紫外分光光度计,原子吸收、ICP-OES和ICP-MS;库房面积450平米,库房工作人员12人,现货产品5万个,坛墨质检自主研发的产品近3000个,已申报国标345项,填补国内空白的产品达到65项。坛墨质检是国内唯一提供标准溶液定制服务的标准物质研制单位,定制范围:特殊浓度定制、特殊溶剂定制、混标定制。
大茴香酸-硫酸荧光体系测定黄芪甲苷刘养清 杜鸣 徐秉玖关键词: 黄芪甲苷; 大茴香酸; 黄芪; 中药复方补阳还五汤; 荧光分光光度法中图分类号: R927.2 R284.1 文献标识码: A 文章编号: 0513-4870(2000)07-0544-03黄芪甲苷(astragaloside)是中药膜荚黄芪Astragalus membranaceus (Fisch.) Bge.和蒙古黄芪Astragalus membranaceus (Fisch.) Bge. var. mongholicus (Bge.) Hsiao的主要活性成分,有抗炎、降压、镇痛、镇静、升高血浆中cAMP水平、促进小鼠再生肝DNA的含量[1,2]以及促进免疫功能等生理活性。黄芪甲苷的测定方法主要有:紫外分光光度法[3,4]、薄层扫描法[5,6]和HPLC法[7,8]。光度法常用香草醛在浓硫酸作用下与甲苷显色反应,空白值较高,干扰严重;薄层扫描法操作繁琐,准确度相对较差。黄芪甲苷仅在200 nm处有末端吸收,对HPLC法不利。黄芪甲苷的荧光分析尚未见报道。本文首次根据在浓硫酸条件下黄芪甲苷与大茴香酸反应产物具有荧光的特性建立了荧光分光光度法测定黄芪甲苷,方法灵敏度高、选择性好、线性范围宽、检出限低、操作简便。可直接用于黄芪生药、中药复方、黄芪制剂以及含药血清等多种样品的测定,无干扰。材料与方法 仪器 日本岛津RF-540型荧光分光光度计。 试剂 黄芪甲苷对照品(中国药品生物制品检定所提供)配成1.0 mg.mL-1的甲醇溶液。2%大茴香酸的无水乙醇溶液,72%硫酸溶液,85%磷酸溶液。所用试剂均为分析纯。 样品及处理 黄芪口服液(上海福达制药有限公司生产,批号980502)。取口服液1.00 mL,加入无水乙醇2.00 mL,离心分离沉淀,上清液蒸干,用甲醇1 mL溶解,备用。补阳还五汤复方汤剂煎煮3次,合并水煎液,分别用石油醚、氯仿、正丁醇萃取4次,每次萃取剂用量为水煎液体积的一半。合并正丁醇相,总体积为800 mL。取正丁醇萃取液2 mL,蒸干,用甲醇2 mL溶解,备用。含药猪血清样品(北京医科大学药学院生药研究室提供):用补阳还五汤复方浸膏连续3 d喂猪,3 d后取血,分离猪血清,取猪血清50 mL,用正丁醇萃取4次,每次萃取剂用量为原血清体积的一半。得含药血清样品100 mL,取正丁醇萃取液4 mL,蒸干,用甲醇2 mL溶解,备用。黄芪生药样品:按文献[3]方法提取分离,甲醇溶样,备用。结果与讨论1 黄芪甲苷反应产物的激发光谱和发射光谱 取1.0 mg.mL-1黄芪甲苷对照品0.1 mL,于5 mL量瓶中,加入2%大茴香酸溶液0.6 mL、72% H2SO4溶液0.8 mL,于60℃水浴中反应20 min,迅速冷却后,用无水乙醇定容至刻度,摇匀,在荧光分光光度计测荧光光谱黄芪甲苷反应产物最大激发波长Ex=320 nm,最大发射波长Em=387 nm。2 大茴香酸用量的影响 取大茴香酸0.1,0.3,0.5,0.6,0.7,0.9 mL按照分析方法操作,选择大茴香酸最佳用量。结果表明大茴香酸用量0.6 mL较合适(图1)。3 稀释液的选择 准确移取1.0 mg.mL-1黄芪甲苷0.1 mL,按照分析方法操作,体积定容时选无水乙醇、甲醇、冰醋酸和水作稀释液,测得其荧光强度(If)分别为77.6,48.4,35.0,1.3。可见无水乙醇对荧光强度影响最小。本文采用无水乙醇作为稀释液。 Fig 1 Effect of amount of anisic acid4 酸的种类和用量的影响 选72% H2SO4, 85% H3PO4及浓HClO4进行实验,结果发现选用72% H2SO4时反应产物的荧光强度最大。对72%硫酸的用量进行选择,结果表明72% H2SO4取0.8 mL为最佳(图2)。 Fig 2 Effect of amount of sulphuric acid5 反应温度的影响 准确移取1.0 mg.mL-1黄芪甲苷对照品0.1 mL,按分析方法内容操作,分别在40,50,60,70,80,90℃和沸水浴中反应20 min,同时做空白。考察荧光强度随温度的变化,结果表明:60℃时反应空白小,荧光强度较高。故实验选择60℃为反应温度较适宜。6 加热时间的影响 将温度控制在60℃,改变加热时间,考察加热时间对反应的影响。结果表明加热时间选20 min为宜。7 反应产物的稳定性 准确移取1.0 mg.mL-1黄芪甲苷对照品0.1 mL,按照分析方法操作,测定荧光强度值,每间隔5 min测定1次,对产物稳定性进行考察。结果表明反应产物在90 min内均稳定。8 工作曲线及检出限 分别准确移取1.0 mg.mL-1黄芪甲苷对照品0.010,0.025,0.050,0.100,0.150和0.200 mL,在最佳实验条件下,测定工作曲线,得回归方程为:Y=-0.4201+1.575X,γ=0.9993。黄芪甲苷浓度在2.0~40 μg.mL-1与荧光强度呈良好的线性关系。检出限为0.02 μg.mL-1。9 干扰考察 为解决基体太浓或基体不一致所造成的影响,在适当稀释溶液后,采用标准加入法测定样品。为考察此反应选择性,利用薄层分离黄芪甲苷[6]后测定样品中其他物质的荧光强度,证明杂质荧光强度与样品总荧光强度的比1.2%。10 样品的测定与回收率实验 取被测样品6份各0.1 mL,依次加入1.0 mg.mL-1黄芪甲苷对照品0.0,0.01,0.02,0.03,0.04和0.05 mL,按照分析方法操作,分别测定了黄芪、复方补阳还五汤、黄芪口服液及猪血清样品中黄芪甲苷的含量,测定结果及回收率实验见表1。SampleContent/%Recovery/%RSD/%HQOL0.210±0.00298.5~101.91.8BYHWT0.280±0.02098.8~102.12.1AMB0.420±0.00498.6~102.02.0PS0.063±0.00198.8~102.41.9黄芪是补阳还五汤的君药,黄芪甲苷定量分析是黄芪中药制剂质量控制的重要指标,本方法灵敏度高,选择性好,操作简便且无干扰,可作为黄芪甲苷的质控方法。基金项目: 九五攀登计划项目杜鸣(北京医科大学药学院分析化学与药物分析研究室,北京 100083 )徐秉玖(北京医科大学药学院分析化学与药物分析研究室,北京 100083 )刘养清(山西师范大学化学系,山西 临汾 041004)收稿日期: 1999-08-03
建立高效液相色谱-蒸发光散射检测器测定黄芪甲苷含量的方法。方法:采用一种新的检测器-蒸发光散射检测器(ELSD)以黄芪甲苷为对照品对黄芪中的黄芪甲苷进行HPLC分析,色谱柱:Phenomenex-ODS;流动相:乙腈-水(37∶63);流速:0.85mL/min;ELSD参数;漂移管温度:100℃;载气流速:2.7L/min。结果:黄芪甲苷在0.396~3.564μg范围内呈线性,回收率为97~94%(RSD=0.68%)。结论:本法具有良好的精密度和重现性,结果准确可靠,可作为原料的质量控制方法。
[color=#444444]黄芪有机氯类农残色谱法测定时最后一个对照品不出峰,ECD检测器,进样口温度230℃,检测器温度300℃,不分流,程序升温,初始温度100℃,10℃/min到220℃,8℃/min到250℃,保持10分钟。为什么最后一个pp'_DDT不出峰呢?请各位高手指教![/color]
想问问各位你们都是用什么测黄芪甲苷的,用什么牌子的仪器,感觉怎么样?国家对测黄芪甲苷的仪器有什么灵敏度或者是其他方面的规定吗?我们公司想买蒸发光散射检测器来测黄芪甲苷,大家觉得哪个好些?老板的心理价位就8-10万吧,谢谢各位[em58]
求助:最近一直咱纳闷,在做黄芪农残有机氯检测,用的是气相ECD检测器,柱子时DB-1701,进样口温度230℃,检测器温度为300℃,不分流进样。程序升温:初始100℃,每分钟10℃升至220℃,每分钟8℃升至250℃,保持10分钟。流速是1s/min,可是做出了九个对照品混合液中只出八个峰,有两个峰即PP'-DDD和PP'-DDT重合分不开,改变流量为2s/min也没见效果,另外进样品中也没见有相应的峰出现,但却在离目标峰不远处有个很大的峰,也是唯一一个峰,请问,大家遇到过此问题是怎么个处理的?
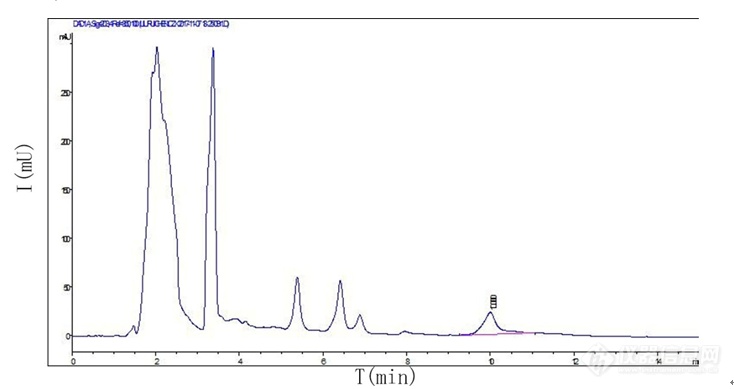
[align=center][b]HP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS法测定黄芪醇提物中的黄芪甲苷的含量[/b][/align][b]黄芪甲苷是黄芪皂苷提取物中的特征性成分,也是具有代表性的主要成分,黄芪甲苷可以促进患者心肌细胞的供氧能力,使冠状动脉供血区供血充足,避免因缺血导致的大范围心肌坏死,继而缓解患者心绞痛症状,平稳心跳速率[sup][/sup]。药典中有关于黄芪药材中黄芪甲苷含量的测定方法,但此方法并不完全适用于黄芪醇提物中的黄芪甲苷的含量测定,而且黄芪水提物与黄芪醇提物中化学成分有差异,预实验中发现测定黄芪水提物中黄芪甲苷含量建立的方法也不适应于黄芪醇提物中中黄芪甲苷含量的测定。本章实验利用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用仪[/color][/url]建立黄芪醇提物中黄芪甲苷含量测定方法,并利用该方法测定其含量,计算出黄芪甲苷的转移率,用于黄芪醇提最佳提取工艺的优选。同时,本章实验系统地验证所建立的方法的可行性,为选择黄芪甲苷的含量测定方法提供参考。[b]1 材料和仪器1.1 样品 [/b] 收集9组黄芪醇提物样品,所有黄芪药材均由济宁华能制药厂提供。[b]1.2 试剂 [/b]黄芪甲苷对照品(成都瑞芬思生物科技有限公司批号H-013-170117);乙腈为色谱纯(赛默飞世尔科技有限公司);D101大孔吸附树脂(廊坊淼阳化工有限公司生产20160310);盐酸溶液(国药集团化学试剂有限公司生产);氢氧化钠溶液(国药集团化学试剂有限公司生产20160824);超纯水。[b]1.3 仪器 [/b]液相色谱仪系统(美国Agligent Technology 公司1260型液相色谱仪,包括G1312B二元泵,G1322A在线脱气机,G1316A柱温箱);NASCA F5100型自动进样器(日本SHISEIDO公司);资生堂CAPCELL PAC CN 色谱柱(2.0*150 mm,5 mm,日本SHISEIDO公司);API 4000型三重四级杆串联离子肼质谱仪(美国Applicated Biosystem Scuex公司)。[b]2 方法学考察2.1 色谱条件[/b]色谱柱为 Synergi C18 80A(250 mm×4.6 mm,4 μm),以十八烷基硅烷键合硅胶为填充剂,以乙腈-水(35 : 65)进行等度洗脱;进样量10 μL;检测波长为203 nm;柱温30 ℃,流速为1 mL/min。黄芪甲苷保留时间约为10 min。黄芪醇提物和黄芪甲苷标准品HPLC色谱图见表5-1,表5-2。[/b][align=center][img=,690,365]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131711071808_2711_3237657_3.png!w690x365.jpg[/img][/align][align=center]图5-1 黄芪醇提物HPLC色谱图[/align][align=center][img=,690,373]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131711240945_4181_3237657_3.png!w690x373.jpg[/img][/align][align=center]图5-2 黄芪甲苷标准品HPLC色谱图[/align][b]2.2 质谱条件 [/b]电喷雾电离,正离子模式(喷雾电压:4.5 kV);鞘气压力:30 arb;辅助气压力:10 arb;离子传输管温度:550 ℃;扫描模式:全扫描;扫描范围:m/z 100-1000。按“2.1.3”项下色谱条件进样,进样量10 μL。为进一步验证10 min出峰的物质是黄芪甲苷,利用LC/MS技术对黄芪皂苷提取物的化学成分进行研究,采用正离子源ESI检测。黄芪甲苷分子量784.97 Da,由于仪器差异,黄芪甲苷出峰时间后移至12.5 min,此峰的鉴定结果质谱图显示含大量黄芪甲苷。图5-3为黄芪皂苷提取物的正离子模式HP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]总离子流图、分离子流图和质谱图。[align=center][img=,690,426]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131711415732_2681_3237657_3.png!w690x426.jpg[/img][/align][align=center]图5-3 黄芪甲苷正离子模式HP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url] 总离子流图、分离子流图和质谱图[/align][b]2.3 供试品溶液的制备[/b]对D101大孔吸附树脂预处理:第一步用乙醇或甲醇清洗吸附柱内壁,向柱内加入称量好的树脂体积0.4-0.5倍的乙醇或甲醇,然后将新的D101大孔吸附树脂投入吸附柱中,使乙醇液面高于D101大孔吸附树脂层0.5 m,浸泡过夜。用2 个柱体积的乙醇或甲醇通过D101大孔吸附树脂层,用乙醇缓慢浸泡D101大孔吸附4-5 h,观察洗脱液加水后不呈白色浑浊为止。再用蒸馏水以2 BV洗柱,洗至洗脱液呈中性。用2 BV的5 %盐酸溶液以4-6 BV/h过柱,浸泡2-4 h。用蒸馏水以2 BV/h洗至洗脱液呈中性。用2 BV的2 %氢氧化钠溶液以4-6 BV/h过柱,浸泡2-4 h。最后用蒸馏水洗D101大孔吸附树脂,洗至洗脱液显中性即可。上样:取黄芪醇提物加水溶解至15 mL得黄芪提取液,以1 mL/min过树脂,先以4 BV蒸馏水洗脱,弃去水液,再用4 BV的70 %乙醇溶液洗脱,用烧杯收集吸附柱内的洗脱液,转入蒸发皿,水浴蒸干后,用甲醇溶解并转移至10 mL容量瓶定容。[b]2.4 对照品溶液的制备[/b]用万分之一天平精密称取10.1 mg黄芪甲苷对照品至10 mL容量瓶,加甲醇定容,得1.01mg/mL的对照品溶液,用0.22μm的微孔滤膜过滤,备用。[b]3 结果3.1 线性关系考察[/b]精密量取黄芪甲苷标准品10.1 mg黄芪甲苷,用甲醇10 mL制备成1.01 mg/mL黄芪甲苷储备液,然后吸取相应体积稀释成浓度梯度为150 μg/mL、250 μg/mL、300 μg/mL、400 μg/mL 、500 μg/mL的对照品溶液,上述对照品溶液按“2.3”项下色谱条件分别进样10 μL,利用自动积分功能测定峰面积积分值,以黄芪皂苷提取物中黄芪甲苷的峰面积积分值对标准品浓度进行线性回归,所得回归方程为y = 2821.6x + 12.438(回归系数[i]R[sup]2[/sup][/i]= 0.9989),证明蒙古黄芪中黄芪甲苷在150~500 μg/mL范围内线性关系良好,黄芪甲苷对照品标准曲线如图5-4所示。[align=center][img=,542,346]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131711574358_4557_3237657_3.png!w542x346.jpg[/img][/align][align=center]图5-4 黄芪甲苷标准曲线[/align][b]3.2 精密度试验[/b]在拟定分析条件下,精密吸取供试品溶液10 μL,连续进样 6 次,记录提取离子流图峰面积,测定黄芪甲苷量,计算得相对标准偏差RSD为1.9% ,提示该方法具有较好的精密度。[b]3.3 重复性实验[/b]取同一黄芪样品 6份,按2. 2 项下方法制备供试品溶液,在拟定分析条件下,准确吸取10 μl 进样分析,测定黄芪甲苷量,计算得 RSD为2.0%,提示该方法重复性良好。[b]3.4 稳定性试验[/b]取黄芪药材供试品溶液,分别在0 h、3 h、6 h、9 h、24 h、48 h后,在拟定分析条件下,准确吸取10 μl 进样分析,测定黄芪甲苷量,计算得RSD为 4.4% ,提示黄芪供试品溶液稳定性较差。[b]3.5 加样回收率试验[/b]精密称取 6 份黄芪甲苷量已知的黄芪水提物样品,每份折合黄芪药材 0. 5 g,分别准确加入浓度为 0. 0 342 mg /ml 黄芪甲苷溶液1 ml,1 ml,2ml,2ml,3ml,3ml,按 2. 2 项下方法制备供试品溶液,准确吸取 1. 0 μl 进样分析,测定黄芪甲苷量,计算回收率,结果见表3-1。由表3-1可见,方法平均回收率为 97.92%,表明该方法具有较好的回收率。[align=center]表5-1 黄芪甲苷加样回收率测定结果[/align] [table][tr][td] [align=center]样号[/align] [/td][td] [align=center]样品中的量/mg[/align] [/td][td] [align=center]加入量/mg[/align] [/td][td] [align=center]测得量/mg[/align] [/td][td] [align=center]回收率/%[/align] [/td][td] [align=center]平均值/%[/align] [/td][td] [align=center]RSD/%[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]1.94 [/align] [/td][td] [align=center]0.96 [/align] [/td][td] [align=center]2.88 [/align] [/td][td] [align=center]97.92 [/align] [/td][td=1,6] [align=center]97.92 [/align] [/td][td=1,6] [align=center]0.7 [/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]1.94 [/align] [/td][td] [align=center]0.96 [/align] [/td][td] [align=center]2.89 [/align] [/td][td] [align=center]98.96 [/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]1.94 [/align] [/td][td] [align=center]1.92 [/align] [/td][td] [align=center]3.83 [/align] [/td][td] [align=center]98.44 [/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]1.94 [/align] [/td][td] [align=center]1.92 [/align] [/td][td] [align=center]3.81 [/align] [/td][td] [align=center]97.40 [/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]1.94 [/align] [/td][td] [align=center]2.88 [/align] [/td][td] [align=center]4.76 [/align] [/td][td] [align=center]97.92 [/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]1.94 [/align] [/td][td] [align=center]2.88 [/align] [/td][td] [align=center]4.73 [/align] [/td][td] [align=center]96.88 [/align] [/td][/tr][/table][b]3.6 黄芪甲苷的含量测定结果[/b]取9组黄芪水提物按照“2.3”项下操作,制备供试品溶液,准确吸取 1 0 μL 进样分析,在拟定的分析条件下,测定黄芪甲苷峰面积积分值,计算相应的黄芪甲苷含量。9组蒙古黄芪中黄芪甲苷含量测定结果如表5-2所示。[align=center]表5-2 9组蒙古黄芪中黄芪甲苷含量测定结果[/align] [table][tr][td] [align=center]试验号[/align] [/td][td] [align=center]峰面积[/align] [/td][td] [align=center]含量(mg/g)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]560.07 [/align] [/td][td] [align=center]0.13 [/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]501.70 [/align] [/td][td] [align=center]0.12 [/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]564.61 [/align] [/td][td] [align=center]0.13 [/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]507.19 [/align] [/td][td] [align=center]0.12 [/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]524.05 [/align] [/td][td] [align=center]0.12 [/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]477.02 [/align] [/td][td] [align=center]0.11 [/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]921.07 [/align] [/td][td] [align=center]0.21 [/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]783.88 [/align] [/td][td] [align=center]0.18 [/align] [/td][/tr][tr][td] [align=center]9[/align] [/td][td] [align=center]924.71 [/align] [/td][td] [align=center]0.22 [/align] [/td][/tr][/table][b]3.7 黄芪甲苷转移率正交试验设计及结果[/b]醇提的黄芪甲苷转移率考察正交试验与醇提的出膏率考察正交试验设计相同,首先以乙醇作为提取溶剂,把影响药材提取效果的提取溶剂乙醇用量(A)、提取次数(B)、提取时间(C)确定为考察因素,以上三个考查因素各分3个水平考察,见表5-3。[align=center]表5-3 实验因素水平表[/align] [table][tr][td=1,2] [align=center]水平[/align] [/td][td=3,1] [align=center]因素[/align] [/td][/tr][tr][td] [align=center]A(乙醇用量/倍)[/align] [/td][td] [align=center]B(提取次数/次)[/align] [/td][td] [align=center]C(提取时间/h)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]4[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]8[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]10[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][/tr][/table]黄芪甲苷转移率=各实验组黄芪提取物中黄芪甲苷含量/原黄芪药材中黄芪甲苷含量×100%。原药材中毛蕊异黄酮苷的含量按照药典的方法测得的结果为0.4042mg/g。跟据实验数据,得到水提实验中设定的不同工艺条件下的毛蕊异黄酮苷的转移率,其中因素D为误差项,作直观分析表和方差分析表,见表5-4,5-5。[align=center]表5-4 黄芪甲苷转移率考察 L[sub]9[/sub](3[sup]4[/sup])正交试验表[/align] [table][tr][td] [align=center]试验号[/align] [/td][td] [align=center]A[/align] [/td][td] [align=center]B[/align] [/td][td] [align=center]C[/align] [/td][td] [align=center]D[/align] [/td][td] [align=center]黄芪甲苷 转移率/%[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]32.01 [/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]28.60 [/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]32.28 [/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]28.92 [/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]29.91 [/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]27.16 [/align] [/td][/tr][tr][td] [align=center]试验号[/align] [/td][td] [align=center]A[/align] [/td][td] [align=center]B[/align] [/td][td] [align=center]C[/align] [/td][td] [align=center]D[/align] [/td][td] [align=center]黄芪甲苷 转移率/%[/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]53.11 [/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]45.09 [/align] [/td][/tr][tr][td] [align=center]9[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]53.33 [/align] [/td][/tr][tr][td] [align=center]K1[/align] [/td][td] [align=center]92.89[/align] [/td][td] [align=center]114.04[/align] [/td][td] [align=center]104.26[/align] [/td][td] [align=center]115.25[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]K2[/align] [/td][td] [align=center]85.99[/align] [/td][td] [align=center]103.60[/align] [/td][td] [align=center]110.85[/align] [/td][td] [align=center]108.87[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]K3[/align] [/td][td] [align=center]151.53[/align] [/td][td] [align=center]112.77[/align] [/td][td] [align=center]115.30[/align] [/td][td] [align=center]106.29[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]优水平[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]R[/align] [/td][td] [align=center]65.54[/align] [/td][td] [align=center]9.17[/align] [/td][td] [align=center]11.04[/align] [/td][td] [align=center]8.96[/align] [/td][td] [align=center] [/align] [/td][/tr][/table][align=center]表5-5 黄芪甲苷转移率考察方差分析结果[/align] [table][tr][td] [align=center]方差来源[/align] [/td][td] [align=center]离差平方和[/align] [/td][td] [align=center]自由度[/align] [/td][td] [align=center]F[/align] [/td][td] [align=center]显著性[/align] [/td][/tr][tr][td] [align=center]A[/align] [/td][td] [align=center]864.64[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]46.01[/align] [/td][td] [align=center]*[/align] [/td][/tr][tr][td] [align=center]B[/align] [/td][td] [align=center]21.63[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]0.07[/align] [/td][td] [align=center]-[/align] [/td][/tr][tr][td] [align=center]C[/align] [/td][td] [align=center]20.57[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]0.07[/align] [/td][td] [align=center]-[/align] [/td][/tr][tr][td] [align=center]D [/align] [/td][td] [align=center]14.18[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]-[/align] [/td][/tr][/table]注:F[sub]0.1[/sub](2,2)=9,F[sub]0.05[/sub](2,2)=19,*为有显著性,-为无显著性。从正交试验结果可知:醇提实验中,各因素对黄芪甲苷转移率的影响大小顺序为:A(乙醇用量)B(提取次数)C(提取时间);每个因素3水平之间的趋势为A[sub]3[/sub]A[sub]1[/sub]A[sub]2[/sub],B[sub]1[/sub]B[sub]3[/sub]B[sub]2[/sub],C[sub]3[/sub]C[sub]2[/sub]C[sub]1[/sub],直观分析得最佳提取工艺为A[sub]3[/sub]B[sub]1[/sub]C[sub]3[/sub],即加醇10倍量,提取1次,每次3h。表5-5的方差分析结果表明: A因素的影响具有统计学差异(PB(提取次数)C(提取时间);每个因素3水平之间的趋势为A[sub]3[/sub]A[sub]1[/sub]A[sub]2[/sub],B[sub]1[/sub]B[sub]3[/sub]B[sub]2[/sub],C[sub]3[/sub]C[sub]2[/sub]C[sub]1[/sub],直观分析得最佳提取工艺为A[sub]3[/sub]B[sub]1[/sub]C[sub]3[/sub],即加醇10倍量,提取1次,每次3h。表5-7的方差分析结果表明: A因素的影响具有统计学差异(P0.05),即乙醇用量对黄芪甲苷转移率具有显著影响。[b]4 讨论[/b]本章实验利用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]技术,测定了黄芪醇提物中黄芪甲苷的含量,并系统地验证所建立的方法的可行性,经过试验条件的摸索,黄芪甲苷的色谱条件为35 %乙腈洗脱,所建立的方法能够较好的将黄芪甲苷与其他成分分开,可用于黄芪皂苷中黄芪甲苷含量测定,黄芪甲苷稳定性试验结果RSD值高于2 %,可能是由于黄芪皂苷Ⅰ或黄芪皂苷Ⅱ在酸性水解的条件下易转化成黄芪皂苷Ⅳ,即黄芪甲苷,使黄芪水提物中黄芪甲苷在48h内的稳定性不好。根据三个因素水平趋势可知,随着乙醇的用量增加,黄芪甲苷的提取效率越来越高,实验设置中每次10倍量是最大乙醇用量,这是从大工业生产和节能降耗等方面考虑的结果。根据煎煮次数水平趋势,提取1次的黄芪甲苷转移率最大,这有可能是因为黄芪皂苷Ⅰ或黄芪皂苷Ⅱ在酸性水解的条件下易转化成黄芪皂苷Ⅳ,即黄芪甲苷,而黄芪皂苷Ⅰ或黄芪皂苷Ⅱ在第一次就较完全的被提取出来,随着时间增加,转换成黄芪皂苷Ⅳ,即黄芪甲苷,第二次时黄芪皂苷Ⅰ或黄芪皂苷Ⅱ的结构可能被破坏,影响其转化成黄芪甲苷。第三次时可能黄芪甲苷被提取的更彻底,转移率又开始小幅增大。在3h内,当提取时间增加,黄芪甲苷会逐渐增大,原因可能是黄芪甲苷的提取更加彻底,黄芪皂苷Ⅰ或黄芪皂苷Ⅱ转化成黄芪甲苷最多。实验设置中每次3h是最大提取时间,这也是从综合成本与效率的角度考虑的结果。因此,综合考虑,将加醇10倍量,提取1次,共3h作为最佳醇提实验工艺。由黄芪甲苷转移率结合出膏率的到的综合评分的结果可以看出,不同提取工艺对黄芪醇提物中黄芪甲苷的含量和出膏率的影响不同,其中7、8、9组评分较高,三个组的黄芪甲苷转移率相较于其他组也是最高,但第8组出膏率却相对较低,另外出膏率高低的顺序也不与黄芪醇提物中黄芪甲苷的转移率高低的顺序项一致,这说明出膏率与黄芪醇提物中黄芪甲苷的转移率并无明显的对应关系。[align=center]参考文献[/align] 朱燕辉, 严奉祥. 黄芪甲苷及其生物学活性.现代生物医学进展,2008, 8 ( 4 ) : 781-783.
活血通络颗粒是由黄芪、丹参、当归、赤芍、地龙、川芎等多味中药组成的复方制剂,具有益气活血、抗凝、降脂等功效。主要用于中风后遗症、脑血栓、脑动脉硬化及高血压、高血脂、心绞痛等心脑血管疾病。黄芪为方中君药,黄芪甲苷为其指标成分,中药复方中黄芪甲苷含量测定已有文献报道。本研究参考文献方法,建立测定活血通络颗粒中黄芪甲苷含量的方法,为控制本品质量打下基础。 1 仪器与试药 薄层扫描仪(日本岛津CS一9000),硅胶G薄层板(青岛海洋化工厂,10cm×10cm),定样毛细管(美国Drumond公司),电子分析天平(梅特勒一托利多仪器上海有限公司),黄芪、丹参、当归等原料药(医药公司),黄芪甲苷对照品(中国药品生物制品检定所),活血通络颗粒剂(本院自制,批号20020326,20020410,20020419)。所用试剂均为分析纯。
国内最大最专业的国家标准物质服务平台坛墨质检-国家标准物质中心(北京坛墨质检科技有限公司),是国家质检总局指定的国家标准物质研制单位,是国内最大最专业的食品、环境、职业卫生标准物质生产商和服务商。 BW6232通关藤苷X对照品,有报告HPLC≥98%BW5024大车前苷对照品,有报告HPLC≥98%BW5475山奈苷对照品,有报告HPLC≥98%BW5133欧前胡素对照品,有报告HPLC≥98%BW5135莱苞迪甙A对照品,有报告HPLC≥98%BW5138秦皮素对照品,有报告HPLC≥98%BW56381-咖啡酰奎宁酸对照品,有报告HPLC≥98%BW51481,3-二咖啡酰奎宁酸对照品,有报告HPLC≥98%BW51491,5-二咖啡酰奎宁酸对照品,有报告HPLC≥98%BW5150盐酸巴马汀(黄藤素,棕榈碱)对照品,有报告HPLC≥98%BW5156异甘草苷对照品,有报告HPLC≥98%BW5162芦荟大黄素对照品,有报告HPLC≥98%BW5166白藜芦醇对照品,有报告HPLC≥98%BW5171灵芝酸A对照品,有报告HPLC≥98%BW5172隐丹参酮对照品,有报告HPLC≥98%BW5177黄芪总皂苷对照品,有报告UV≥98%BW5178黄芪皂苷I对照品,有报告HPLC≥98%BW5179黄芪皂苷II对照品,有报告HPLC≥98%BW5180黄芪皂苷III对照品,有报告HPLC≥98%BW5183络塞琳对照品,有报告HPLC≥98%BW5184络塞维对照品,有报告HPLC≥98%BW5185络缌对照品,有报告HPLC≥98%BW5186络塞定对照品,有报告HPLC≥98%BW5202盐酸氨基葡萄糖对照品,有报告HPLC≥98%BW5206雷公藤内酯甲;雷公藤酯甲对照品,有报告HPLC≥98%BW5210青蒿素对照品,有报告HPLC≥96%BW5214盐酸育亨宾;17alpha-羟基育亨烷-16alpha-羧酸甲酯盐酸盐对照品,有报告HPLC≥98% 坛墨质检现有员工79人,办公室面积450平米,实验室1650平米;销售、客服、财务及行政人员35人,实验室工作人员21人,库房14人,市场部8人。实验仪器设备:气相色谱、液相色谱、气质联用、液质联用、离子色谱、紫外分光光度计,原子吸收、ICP-OES和ICP-MS;库房面积450平米,库房工作人员12人,现货产品5万个,坛墨质检自主研发的产品近3000个,已申报国标345项,填补国内空白的产品达到65项。坛墨质检是国内唯一提供标准溶液定制服务的标准物质研制单位,定制范围:特殊浓度定制、特殊溶剂定制、混标定制。
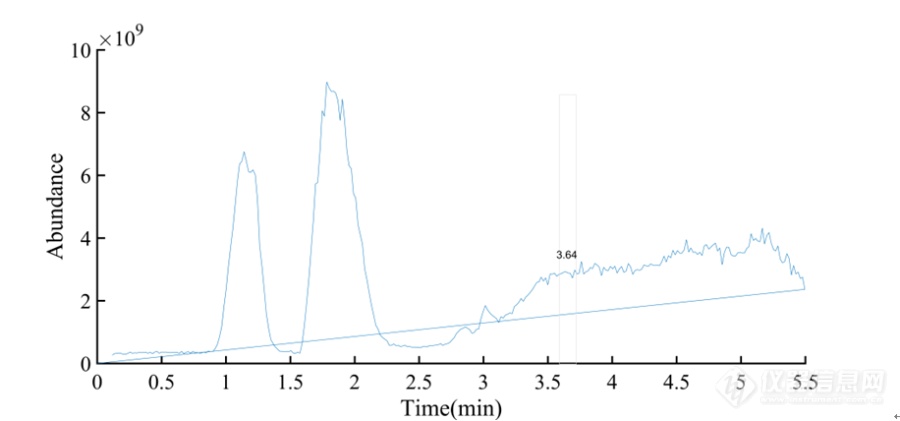
[align=center][b]UP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS法测定黄芪水提物中的黄芪甲苷含量[/b][/align][b] 传统中药的煎煮,大多是用水作为溶剂,因此研究药材的水提物中有效成分的含量对药材的工业生产和实际应用具有不可忽视的指导意义。据文献报道[sup][/sup],黄芪水提物中主要为糖类和皂苷类成分,而水提物药渣中则是提取后剩余的淀粉、纤维素、木质素等原药材的基体成分和一些不易溶于水的酯类、酮类和芳香类成分。黄芪甲苷作为黄芪皂苷中一类重要的物质,已被药典收录为黄芪含量测定的指标成分。为了保证临床应用制剂的质量和进一步开发利用中药黄芪,研究黄芪水提物中黄芪甲苷的含量显得格外重要。在预实验中,笔者发现药典中测定黄芪中黄芪甲苷含量的方法并不完全适用于黄芪水提物中黄芪甲苷含量的测定,预处理时出现乳化现象导致萃取不完全,另外利用药典中规定的蒸发光检测器液相色谱仪测定无法得到理想的线性方程。因此,笔者结合黄芪水提物的性质和仪器灵敏性等特点,利用UP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS法考察黄芪水提物中的黄芪甲苷含量测定的方法学和并利用该方法测定黄芪水提物中黄芪甲苷的含量。[b]1 材料和仪器1.1 样品 [/b] 收集9组黄芪水提取物样品,黄芪饮片为济南济成堂中药饮片有限公司提供(批号18033101)。[b]1.2 试剂 [/b]黄芪甲苷对照品(成都瑞芬思生物科技有限公司批号H-013-170117),乙腈为色谱纯(天津市科密欧化学试剂有限公司);超纯水。[b]1.3 仪器 [/b]Waters XevoTQ-S三重四级杆质谱仪(美国Waters公司)。ACQUITY UPLC H-CLass超高效液相色谱仪(美国Waters公司);超声波清洗机KS-300E(宁波科生仪器厂);电子天平MS205DU(梅特勒/瑞士)。[b]2 方法学考察2.1 色谱与质谱条件[/b]色谱条件:色谱柱为ACQUITY UPLC BEH C18柱(2.1*50 mm,1.7 mm)。流动相为乙腈-水(A∶B)系统。梯度洗脱,A相:0→1 min A保持30%;1→2 min A为30→60%;2→3 min A为60→70%;3→4 min A保持70%;4→4.5 min A为70→30%;A相:4.5→5.5 min A保持30%。流速 0. 2 mL/min,柱温为40 ℃,进样体积 1. 0 μL。质谱条件:电喷雾正离子检测模式,毛细管电压;3.0 kV;脱溶剂气流:N2,流速800 L h[sup]-1[/sup],脱溶剂温度400 ℃;锥孔电压:40 V,锥孔气流:N2,流速150 Lh[sup]-1[/sup];离子源温度: 400 ℃;雾化气压力为7.0 bar碰撞气体: 氩气。采用MRM 定量模式,质量扫描范围为100~1 000 amu。该条件下,获得黄芪甲苷的分子离子峰 m /z 785. 42,子离子峰m /z 143.08。黄芪甲苷提取总离子流图和一级质谱图分别见图3-1和图3-2。[/b][align=center][img=,690,322]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131701299261_9069_3237657_3.png!w690x322.jpg[/img][/align][align=center]图3-1 黄芪甲苷的总离子流图[/align][align=center][img=,690,331]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131701493040_8991_3237657_3.png!w690x331.jpg[/img][/align][align=center]图3-2 黄芪甲苷的一级质谱图[/align][b]2.2 供试品溶液的制备[/b]精密称定1/200重量的黄芪水提物样品(折合黄芪药材0.5g)置于锥形瓶中,精密加入4%氨水溶液100 mL,称定重量,超声30 min,取出放至室温,用4%氨水溶液补足减失的重量,摇匀,过滤,精密吸取续滤液10 mL过Dikma ProElut C18-U-SPE柱(先以甲醇20 mL活化,再以水20 mL平衡),上样后用10 mL水淋洗,弃去,再用适量甲醇洗脱,收集洗脱液,定容至10 mL容量瓶中,摇匀,用0.22 μm的微孔滤膜过滤,即得。[b]2.3 对照品储备溶液的制备[/b]精密称取黄芪甲苷标品1.01mg至10 mL容量瓶中,用甲醇溶解后定容,吸取1 mL至100 mL容量瓶中,用甲醇定容,制成浓度为1.01 μg/mL的对照品储备溶液。[b]3 结果3.1 线性关系考察[/b]精密吸取 2. 3 项下对照品储备溶液 1,3,5 mL,用甲醇稀释并定容到 10mL 容量瓶中,制备0.1,0.3,0.5 mgmL[sup]-1[/sup]质量浓度对照品溶液。另吸取0.1,0.3 mg/mL质量浓度对照品溶液5 mL至10 mL容量瓶,用甲醇定容,得到0.05,0.15 mg/mL质量浓度对照品溶液。在拟定分析条件下,准确吸取 10. 0 μL 进样分析。黄芪甲苷离子选择 m/z 785. 42 为母离子,143.08 为子离子,准确吸取1 0 μL 进样分析。以质量浓度为横坐标,以提取离子流图峰面积为纵坐标进行线性回归,如图3,得回归方程为:Y=46.135X + 1938.8(r[sup]2[/sup]= 0. 9984),提示黄芪甲苷在0. 05~0.5 mg/m L 范围内线性关系良好。黄芪甲苷对照品标准曲线如图3-3所示。[align=center][img=,690,423]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131702057366_9110_3237657_3.png!w690x423.jpg[/img][/align][align=center]图3-3 黄芪甲苷标准曲线[/align][b]3.2 精密度实验[/b]在拟定分析条件下,精密吸取供试品溶液1.0 μL,连续进样 6 次,记录提取离子流图峰面积,测定黄芪甲苷量,计算得相对标准偏差RSD为1.1% ,提示该方法具有较好的精密度。[b]3.3 重复性实验[/b]取同一黄芪样品 6份,按2. 2 项下方法制备供试品溶液,在拟定分析条件下,准确吸取 1. 0 μL 进样分析,测定黄芪甲苷量,计算得 RSD为2.0%,提示该方法重复性良好。[b]3.4 稳定性实验[/b]取黄芪药材供试品溶液,分别在0 h、3 h、6 h、9 h、24 h、48 h后,在拟定分析条件下,准确吸取 1. 0 μL 进样分析,测定黄芪甲苷量,计算得 RSD 为 4.7% ,提示黄芪供试品溶液稳定性较差。[b]3.5 加样回收率实验[/b]精密称取 6 份黄芪甲苷量已知的黄芪水提物样品,每份折合黄芪药材 0. 5 g,分别准确加入浓度为 0. 0 342 mg /mL 黄芪甲苷溶液1 ml,1 ml,2 ml,2 ml,3 ml,3 ml,按 “2. 2 ”项下方法制备供试品溶液,准确吸取 1. 0 μL 进样分析,测定黄芪甲苷量,计算回收率,结果见表3-1。由表3-1可见,方法平均回收率为 102.35% ,表明该方法具有较好的回收率。[align=center] [/align][align=center]表3-1 黄芪甲苷加样回收率测定结果[/align] [table][tr][td] [align=center]样号[/align] [/td][td] [align=center]样品中的量/mg[/align] [/td][td] [align=center]加入量/mg[/align] [/td][td] [align=center]测得量/mg[/align] [/td][td] [align=center]回收率/%[/align] [/td][td] [align=center]平均值/%[/align] [/td][td] [align=center]RSD/%[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]0.069[/align] [/td][td] [align=center]0.034[/align] [/td][td] [align=center]0.1[/align] [/td][td] [align=center]101.68[/align] [/td][td=1,6] [align=center]102.35[/align] [/td][td=1,6] [align=center]2.8[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]0.069[/align] [/td][td] [align=center]0.034[/align] [/td][td] [align=center]0.11[/align] [/td][td] [align=center]104.44[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]0.069[/align] [/td][td] [align=center]0.068[/align] [/td][td] [align=center]0.14[/align] [/td][td] [align=center]104.17[/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]0.069[/align] [/td][td] [align=center]0.068[/align] [/td][td] [align=center]0.13[/align] [/td][td] [align=center]96.42[/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]0.069[/align] [/td][td] [align=center]0.10 [/align] [/td][td] [align=center]0.17[/align] [/td][td] [align=center]102.78[/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]0.069[/align] [/td][td] [align=center]0.10 [/align] [/td][td] [align=center]0.18[/align] [/td][td] [align=center]104.63[/align] [/td][/tr][/table][align=center] [/align][b]3.6 黄芪甲苷的含量测定结果[/b]取9组黄芪水提物按照“2.2”项下操作,制备供试品溶液,准确吸取 1. 0 μL 进样分析,测定黄芪甲苷的含量。黄芪甲苷对照品和黄芪水提物样品的MRM 离子流图见图3-4、图3-5。供试品黄芪甲苷含量测定结果见表3-2。[align=center][img=,690,348]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131702286759_7988_3237657_3.png!w690x348.jpg[/img][/align][align=center]图3-4 黄芪甲苷对照品的 MRM 离子流图[/align][align=center][img=,690,344]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131702391650_7279_3237657_3.png!w690x344.jpg[/img][/align][align=center]图3-5 黄芪水提物样品的 MRM 离子流图[/align][align=center] [/align][align=center]表3-2 9组黄芪水提物中黄芪甲苷含量测定结果[/align] [table][tr][td] [align=center]试验号[/align] [/td][td] [align=center]峰面积[/align] [/td][td] [align=center]含量(mg/g)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]5120.00 [/align] [/td][td] [align=center]0.14 [/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]6744.00 [/align] [/td][td] [align=center]0.21 [/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]10275.67 [/align] [/td][td] [align=center]0.36 [/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]26955.00 [/align] [/td][td] [align=center]1.08 [/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]10599.00 [/align] [/td][td] [align=center]0.38 [/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]7212.33 [/align] [/td][td] [align=center]0.23 [/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]11247.33 [/align] [/td][td] [align=center]0.40 [/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]8008.33 [/align] [/td][td] [align=center]0.26 [/align] [/td][/tr][tr][td] [align=center]9[/align] [/td][td] [align=center]9171.00 [/align] [/td][td] [align=center]0.31 [/align] [/td][/tr][/table][align=center] [/align][b]3.7 正交试验设计及结果[/b]水提的黄芪甲苷转移率考察正交试验与水提的出膏率考察正交试验设计相同,即以水作为提取溶剂,把影响药材提取效果的用水量(A)、提取时间(B)、提取次数(C)确定为考察因素,以上三个考查因素各分3个水平考察,见表3-3。[align=center]表3-3水提实验因素水平表[/align] [table][tr][td=1,2] [align=center]水平[/align] [/td][td=3,1] [align=center]因素[/align] [/td][/tr][tr][td] [align=center]A(用水量/倍)[/align] [/td][td] [align=center]B(提取时间/h)[/align] [/td][td] [align=center]C(提取次数/次)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]4[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]8[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]10[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][/tr][/table][b] [/b]黄芪甲苷转移率=各实验组黄芪提取物中黄芪甲苷含量/原黄芪药材中黄芪甲苷含量×100%。原药材中毛蕊异黄酮苷的含量按照药典的方法测得的结果为0.4042mg/g。跟据实验数据,得到水提实验中设定的不同工艺条件下的毛蕊异黄酮苷的转移率,其中因素D为误差项,作直观分析表和方差分析表,见表3-4,表3-5。[align=center]表3-4 黄芪甲苷转移率考察L[sub]9[/sub](3[sup]4[/sup])正交试验表[/align] [table][tr][td] [align=center]试验号[/align] [/td][td] [align=center]A[/align] [/td][td] [align=center]B[/align] [/td][td] [align=center]C[/align] [/td][td] [align=center]D[/align] [/td][td] [align=center]黄芪甲苷 转移率/%[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]34.12 [/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]51.54 [/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]89.41 [/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]268.30 [/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]92.88 [/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]56.56 [/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]99.83 [/align] [/td][/tr][tr][td] [align=center]试验号[/align] [/td][td] [align=center]A[/align] [/td][td] [align=center]B[/align] [/td][td] [align=center]C[/align] [/td][td] [align=center]D[/align] [/td][td] [align=center]黄芪甲苷 转移率/%[/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]65.10 [/align] [/td][/tr][tr][td] [align=center]9[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]77.56 [/align] [/td][/tr][tr][td] [align=center]K1[/align] [/td][td] [align=center]175.07 [/align] [/td][td] [align=center]402.25 [/align] [/td][td] [align=center]155.78 [/align] [/td][td] [align=center]204.56 [/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]K2[/align] [/td][td] [align=center]417.74 [/align] [/td][td] [align=center]144.42 [/align] [/td][td] [align=center]397.40 [/align] [/td][td] [align=center]207.93 [/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]K3[/align] [/td][td] [align=center]242.49 [/align] [/td][td] [align=center]223.53 [/align] [/td][td] [align=center]282.12 [/align] [/td][td] [align=center]422.81 [/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]优水平[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]R[/align] [/td][td] [align=center]242.67 [/align] [/td][td] [align=center]257.83 [/align] [/td][td] [align=center]241.62 [/align] [/td][td] [align=center]218.25 [/align] [/td][td] [align=center] [/align] [/td][/tr][/table][align=center] [/align][align=center]表3-5 黄芪甲苷转移率考察方差分析结果[/align] [table][tr][td] [align=center]方差来源[/align] [/td][td] [align=center]离差平方和[/align] [/td][td] [align=center]自由度[/align] [/td][td] [align=center]F[/align] [/td][td] [align=center]显著性[/align] [/td][/tr][tr][td] [align=center]A[/align] [/td][td] [align=center]10460.75[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1.13[/align] [/td][td] [align=center]-[/align] [/td][/tr][tr][td] [align=center]B[/align] [/td][td] [align=center]7698.00[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]0.75[/align] [/td][td] [align=center]-[/align] [/td][/tr][tr][td] [align=center]C[/align] [/td][td] [align=center]9736.83[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1.02[/align] [/td][td] [align=center]-[/align] [/td][/tr][tr][td] [align=center]D[/align] [/td][td] [align=center]10424.20[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]-[/align] [/td][/tr][/table]注:F[sub]0.1[/sub](2,2)=9,F[sub]0.05[/sub](2,2)=19,*为有显著性,-为无显著性。从正交试验结果可知,水提实验中,各因素对黄芪甲苷转移率的影响大小顺序为:A(用水量)C(提取次数)B(提取时间);每个因素3水平之间的趋势为A[sub]2[/sub]A[sub]3[/sub]A[sub]1[/sub],B[sub]1[/sub]B[sub]3[/sub]B[sub]2[/sub],C[sub]2[/sub]C[sub]3[/sub]C[sub]1[/sub],直观分析得最佳提取工艺为A[sub]2[/sub]B[sub]1[/sub]C[sub]2[/sub],即加水8倍量,提取2次,每次1h。表3-5的方差分析结果表明: A、B、C三因素对黄芪甲苷转移率的影响都无统计学差异(P0.05)。[b]4 讨论[/b]本章实验利用超高效液相串联三重四级杆质谱仪测定黄芪水提物中黄芪甲苷的含量,相比药典中测定黄芪药材中黄芪甲苷的方法,此方法预处理步骤更少,用时更短,目标峰与其他相邻峰的分离度也更大,适合于黄芪水提物中黄芪甲苷含量的测定。但美中不足的是,供试品的预处理需要过SPE柱,仪器的使用和维护费用更高,实验者在测定样品的含量前需要综合考虑。从测定结果来看,设置的三个因素中,用水量对黄芪甲苷的转移率影响最大,但仍无统计学差异(P0.05),说明用水量、提取次数、提取时间三种工艺的改变对黄芪水提物中黄芪甲苷的含量无显著性影响。第4、5、7组的黄芪甲苷转移率相比其他组的更高,尤其是第4组测得的黄芪甲苷的含量远高于用药典方法测得的药材中黄芪甲苷的含量,正交实验分析结果也说明加水8倍量,提取2次,每次1h是最佳提取工艺。这一结果与水提实验中第3、4、7组测得的出膏率较高有些差异,第4组实验的出膏率也不算低,但不是最高,而出膏率最高的第3组黄芪甲苷的转移率却不高,这说明出膏率与黄芪水提物中黄芪甲苷的转移率并无明显的对应关系。合乎标准要求的有效成分含量是保证药物疗效稳定可靠的硬性指标,实现有效成分提取的最大化是优化工艺条件的重要目标。本章关于不同提取工艺条件下黄芪甲苷转移率的考察研究,对芪龙胶囊和黄芪配方颗粒工艺的优化具有指导性意义。[align=center]参考文献[/align] 黄冬兰,徐永群,陈小康. 黄芪药材及其水提物的红外光谱分析. 光谱实验室,2012,29(5):2823-2826.
有没有哪位大神用紫外或者示差测过黄芪甲苷啊,我们这边没有蒸发光散射,只能用紫外和示差,但是跟着文献上搜出来的资料完全没有走出来的迹象啊。仪器条件如下:1:紫外:流动相30%乙腈水,色谱柱150mm的C18柱子走,检测波长203。2:示差 流动相:67%甲醇水,色谱柱:150mm C18。以上,标都是用甲醇配的,最大浓度是500ppm。
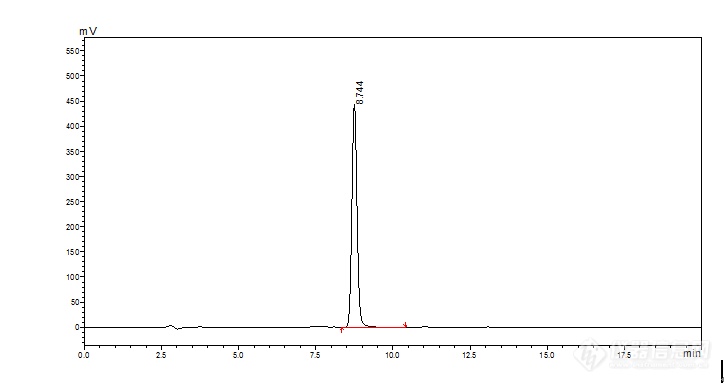
[align=center][b]HPLC法测定黄芪水提物中的毛蕊异黄酮苷含量[/b][/align][b]黄芪中的主要有效成分除皂苷外就是异黄酮类化合物。异黄酮类成分具有调节免疫、抗肿瘤、抗突变、抗氧化、抗炎、抗突变抗辐射、抗心肌缺血、抗心律失常、抗病毒、抗细胞凋亡、保肝、防止动脉粥样硬化等作用[sup][/sup],其代表成分就是毛蕊异黄酮 7-O-β-D 吡喃葡萄糖苷(即毛蕊异黄酮苷)。2010版药典才开始将毛蕊异黄酮苷收录为黄芪中有效成分含量测定项。本章实验借鉴药典中的测定方法,对不同工艺条件下获得的黄芪水提物中的毛蕊异黄酮苷含量进行考察,以期为优化芪龙胶囊和黄芪配方颗粒中黄芪的提取工艺参数提供科学基础和理论依据。[b]1 材料和仪器1.1 样品 [/b] 收集9组黄芪水提取物样品,黄芪饮片为济南济成堂中药饮片有限公司提供(批号18033101)。[b]1.2 试剂 [/b]毛蕊异黄酮苷对照品(成都瑞芬思生物科技有限公司批号M-020-170926),乙腈为色谱纯(天津市科密欧化学试剂有限公司);甲酸(天津市科密欧化学试剂有限公司);超纯水。[b]1.3 仪器 [/b]液相色谱系统,包括日本岛津公司LC-20AT型液相色谱仪,LC-20AT岛津输液泵,CTO-20A柱温箱,SIL-20A自动进样器,SPD-20A紫外-可见光检测器;超声波清洗机KS-300E(宁波科生仪器厂);电子天平MS205DU(梅特勒/瑞士)。[b]2 方法学考察2.1 色谱条件及系统适应性试验[/b]DiamonsiL(钻石)C18柱(250*4.6 mm,5 mm)。以乙腈为流动相A,0.2%甲酸溶液为流动相B,梯度洗脱,A相:0→20 min A为20→40%;20→30 min A保持40%;30→40 min A保持20%。检测波长260 nm;流速为1 mL/min;柱温35 ℃进样量为10 μL。毛蕊异黄酮苷对照品溶液以及黄芪水提物样品色谱图见图4-1与图4-2。[/b][align=center][img=,690,365]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131706005051_4964_3237657_3.png!w690x365.jpg[/img][/align][align=center]图4-1 毛蕊异黄酮苷对照品色谱图[/align][align=center][img=,690,384]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131706118782_6652_3237657_3.png!w690x384.jpg[/img][/align][align=center]图4-2 黄芪水提物样品色谱图[/align][b]2.2 供试品溶液的制备[/b]精密称定1/50重量的黄芪水提物样品(折合黄芪药材2 g)置于锥形瓶中,精密加入50 mL甲醇,超声30 min,过滤,将滤液放至水浴锅上蒸干,残渣用甲醇溶解,并定容至25 mL,用0.22 μm的微孔滤膜过滤,即得。[b]2.3 对照品储备溶液的制备[/b]精密称取黄芪甲苷标品5.10mg至10 mL容量瓶中,用甲醇溶解后定容,摇匀,即得浓度为0.51 mg/mL的对照品储备溶液。[b]3 结果3.1 线性关系考察[/b]精密吸取 2. 3 项下对照品储备溶液 4,2,1,0.5,0.25 mL至10 mL容量瓶中,用甲醇定容,得到浓度为204.00,102.00,51.00,25.50,12.75 μg/mL的对照品溶液。按“2.3”项下色谱条件分别进样10 μL,利用自动积分功能测定峰面积积分值,并以峰面积积分值与浓度进行线性回归。如图3,得回归方程为:Y =25445X + 44225(r[sup]2[/sup]= 0.9994)提示毛蕊异黄酮苷在12.75~204.00 μg/mL范围内线性关系良好。毛蕊异黄酮苷对照品标准曲线如图4-3所示。[align=center][img=,690,406]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131706302801_395_3237657_3.png!w690x406.jpg[/img][/align][align=center]图4-3 毛蕊异黄酮苷标准曲线[/align][b]3.2 精密度实验[/b]按2. 2 项下方法制备供试品溶液,精密吸取供试品溶液10 μL,重复进样 6 次,记录色谱图峰面积,测定毛蕊异黄酮苷含量,计算得相对标准偏差RSD为1.6% ,提示该方法精密度良好。[b]3.3 重复性实验[/b]取同一黄芪样品 6份,按“2. 2”项下方法制备供试品溶液,在拟定分析条件下,精密吸取供试品溶液10 μL,测定毛蕊异黄酮苷含量,计算得RSD为1.1%,提示该方法重复性良好。[b]3.4 稳定性实验 [/b]按2. 2 项下方法制备供试品溶液,分别在0 h、3 h、6 h、9 h、24 h、48 h后,准确吸取 10 μL 进样分析,测定毛蕊异黄酮苷含量,计算得 RSD 为 0.6%,提示黄芪供试品溶液在48h内稳定性良好。[b]3.5 加样回收率实验[/b]精密称取 6 份毛蕊异黄酮苷含量已知的黄芪水提物样品,每份折合黄芪药材 0. 5 g,分别准确加入样品中毛蕊异黄酮苷含量的50%,50%,100%,100%,150%,150%重量的毛蕊异黄酮苷标品,按2. 2 项下方法制备供试品溶液,准确吸取 10 μL 进样分析,测定毛蕊异黄酮苷含量,计算回收率,结果见表4-1。方法平均回收率为108.48%,表明该方法具有较好的回收率。[align=center]表4-1 毛蕊异黄酮苷加样回收率测定结果[/align] [table][tr][td] [align=center]样号[/align] [/td][td] [align=center]样品中的量/mg[/align] [/td][td] [align=center]加入量[/align] [align=center]/mg[/align] [/td][td] [align=center]测得量/mg[/align] [/td][td] [align=center]回收率[/align] [align=center]/%[/align] [/td][td] [align=center]平均值/%[/align] [/td][td] [align=center]RSD[/align] [align=center]/%[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]1.06 [/align] [/td][td] [align=center]0.52 [/align] [/td][td] [align=center]1.64 [/align] [/td][td] [align=center]111.54 [/align] [/td][td=1,6] [align=center]108.85 [/align] [/td][td=1,6] [align=center]2.9 [/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]1.06 [/align] [/td][td] [align=center]0.52 [/align] [/td][td] [align=center]1.64 [/align] [/td][td] [align=center]112.08 [/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]1.06 [/align] [/td][td] [align=center]1.06 [/align] [/td][td] [align=center]2.22 [/align] [/td][td] [align=center]109.20 [/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]1.06 [/align] [/td][td] [align=center]1.06 [/align] [/td][td] [align=center]2.24 [/align] [/td][td] [align=center]111.02 [/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]1.06 [/align] [/td][td] [align=center]1.59 [/align] [/td][td] [align=center]2.72 [/align] [/td][td] [align=center]104.57 [/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]1.06 [/align] [/td][td] [align=center]1.59 [/align] [/td][td] [align=center]2.72 [/align] [/td][td] [align=center]104.67 [/align] [/td][/tr][/table][b]3.6 毛蕊异黄酮苷的含量测定结果[/b]取9组黄芪水提物按照“2.2”项下操作,制备供试品溶液,准确吸取 10 μL 进样分析,测定毛蕊异黄酮苷的含量。结果见表2。[align=center]表4-2 9组黄芪水提物中毛蕊异黄酮苷含量测定结果[/align] [table][tr][td] [align=center]批号[/align] [/td][td] [align=center]峰面积[/align] [/td][td] [align=center]含量(mg/g)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]1123989.50 [/align] [/td][td] [align=center]0.53 [/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]2707047.50 [/align] [/td][td] [align=center]1.31 [/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]1947171.50 [/align] [/td][td] [align=center]0.93 [/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]3573103.75 [/align] [/td][td] [align=center]1.73 [/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]1824562.00 [/align] [/td][td] [align=center]0.87 [/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]2767419.00 [/align] [/td][td] [align=center]1.34 [/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]2077551.50 [/align] [/td][td] [align=center]1.00 [/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]1677225.50 [/align] [/td][td] [align=center]0.80 [/align] [/td][/tr][tr][td] [align=center]9[/align] [/td][td] [align=center]1725416.00 [/align] [/td][td] [align=center]0.83 [/align] [/td][/tr][/table][b]3.7 毛蕊异黄酮苷转移率测定正交试验结果[/b]水提的毛蕊异黄酮苷转移率考察正交试验与水提的出膏率考察正交试验设计相同,即以水作为提取溶剂,把影响药材提取效果的用水量(A)、提取时间(B)、提取次数(C)确定为考察因素,以上三个考查因素各分3个水平考察,见表4-3。[align=center]表4-3水提实验因素水平表[/align] [table][tr][td=1,2] [align=center]水平[/align] [/td][td=3,1] [align=center]因素[/align] [/td][/tr][tr][td] [align=center]A(用水量/倍)[/align] [/td][td] [align=center]B(提取时间/h)[/align] [/td][td] [align=center]C(提取次数/次)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]4[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]8[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]10[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][/tr][/table][b] [/b]毛蕊异黄酮苷转移率=各实验组黄芪提取物中毛蕊异黄酮苷含量/原黄芪药材中毛蕊异黄酮苷含量×100%。原药材中毛蕊异黄酮苷的含量按照药典的方法测得的结果为0.1425mg/g。跟据实验数据,得到水提实验中设定的不同工艺条件下的毛蕊异黄酮苷的转移率,其中因素D为误差项,作直观分析表和方差分析表,见表4-4,4-5。[align=center]表4-4 毛蕊异黄酮苷转移率考察L[sub]9[/sub](3[sup]4[/sup])正交试验表[/align] [table][tr][td] [align=center]批号[/align] [/td][td] [align=center]A[/align] [/td][td] [align=center]B[/align] [/td][td] [align=center]C[/align] [/td][td] [align=center]D[/align] [/td][td] [align=center]毛蕊异黄酮苷[/align] [align=center]转移率/%[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]37.21[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]91.77[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]65.58[/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]121.62[/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]61.36[/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]93.85[/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]70.08[/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]56.28[/align] [/td][/tr][tr][td] [align=center]9[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]57.94[/align] [/td][/tr][tr][td] [align=center]K1[/align] [/td][td] [align=center]194.56[/align] [/td][td] [align=center]228.91[/align] [/td][td] [align=center]187.34[/align] [/td][td] [align=center]156.51[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]K2[/align] [/td][td] [align=center]276.83[/align] [/td][td] [align=center]209.41[/align] [/td][td] [align=center]271.33[/align] [/td][td] [align=center]255.70[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]K3[/align] [/td][td] [align=center]184.30[/align] [/td][td] [align=center]217.37[/align] [/td][td] [align=center]197.02[/align] [/td][td] [align=center]243.48[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]优水平[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]R[/align] [/td][td] [align=center]92.53[/align] [/td][td] [align=center]19.50[/align] [/td][td] [align=center]83.99[/align] [/td][td] [align=center]99.19[/align] [/td][td] [align=center] [/align] [/td][/tr][/table][b] [/b][align=center]表4-5 毛蕊异黄酮苷转移率考察方差分析表[/align] [table][tr][td] [align=center]方差来源[/align] [/td][td] [align=center]离差平方和[/align] [/td][td] [align=center]自由度[/align] [/td][td] [align=center]F[/align] [/td][td] [align=center]显著性[/align] [/td][/tr][tr][td] [align=center]A[/align] [/td][td] [align=center]1715.05[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1.50[/align] [/td][td] [align=center]-[/align] [/td][/tr][tr][td] [align=center]B[/align] [/td][td] [align=center]64.09[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]0.04[/align] [/td][td] [align=center]-[/align] [/td][/tr][tr][td] [align=center]C[/align] [/td][td] [align=center]1407.78[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1.13[/align] [/td][td] [align=center]-[/align] [/td][/tr][tr][td] [align=center]方差来源[/align] [/td][td] [align=center]离差平方和[/align] [/td][td] [align=center]自由度[/align] [/td][td] [align=center]F[/align] [/td][td] [align=center]显著性[/align] [/td][/tr][tr][td] [align=center]D [/align] [/td][td] [align=center]1950.20[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]-[/align] [/td][/tr][/table]注:F[sub]0.1[/sub](2,2)=9,F[sub]0.05[/sub](2,2)=19,*为有显著性,-为无显著性。从正交试验结果可知:水提实验中,各因素对毛蕊异黄酮苷转移率的影响大小顺序为:A(用水量)C(提取次数)B(提取时间);每个因素3水平之间的趋势为A[sub]2[/sub]A[sub]1[/sub]A[sub]3[/sub],B[sub]1[/sub]B[sub]3[/sub]B[sub]2[/sub],C[sub]2[/sub]C[sub]3[/sub]C[sub]1[/sub],直观分析得提取工艺为A[sub]2[/sub]B[sub]1[/sub]C[sub]2[/sub],即加水8倍量,提取2次,每次1h。表4-5的方差分析结果表明: A、B、C三因素的对毛蕊异黄酮的转移率影响都无统计学差异(PC(提取次数)B(提取时间);每个因素3水平之间的趋势为A[sub]2[/sub]A[sub]3[/sub]A[sub]1[/sub],B[sub]1[/sub]B[sub]3[/sub]B[sub]2[/sub],C[sub]2[/sub]C[sub]3[/sub]C[sub]1[/sub],直观分析得提取工艺为A[sub]2[/sub]B[sub]1[/sub]C2,即加水8倍量,提取2次,每次1h。表4-7的方差分析结果表明:A、B、C三因素对综合评分的影响都无统计学差异(P0.05)。[b]4 讨论[/b]本章实验借鉴药典中测定黄芪药材中毛蕊异黄酮苷含量的方法,利用紫外-可见光检测器的高效液相色谱仪测定黄芪水提物中毛蕊异黄酮苷的含量。与药典中方法测得的结果相比,本实验测得的结果除色谱峰分离度稍差外,其他方法学考察指标显示良好。从毛蕊异黄酮苷转移率测定正交试验结果来看,第4组实验毛蕊异黄酮苷转移率最高,这也是正交结果分析中最佳提取工艺,即加水8倍量,提取2次,每次1小时。本结果与上一章实验中第四组黄芪水提物中黄芪甲苷的转移率最高结果一致,但其他组别毛蕊异黄酮苷的转移率高低顺序与上一章黄芪甲苷的转移率高低顺序并不一致,这说明毛蕊异黄酮苷和黄芪甲苷对提取工艺的要求并不完全一致。同一种原药材,加工成不同功效的药物,那么发挥药效的物质也有可能不同,因此相应的提取工艺也是需要根据药效物质适时调整的。另外,用水量在设置的三个因素中对毛蕊异黄酮苷的转移率影响最大,但仍无统计学差异(P0.05),说明用水量、提取次数、提取时间三种工艺的改变对黄芪水提物中毛蕊异黄酮苷的含量无显著性影响。从综合评分计算正交试验结果来看,第4组实验综合评分最高,这也是正交结果分析中最佳提取工艺,即加水8倍量,提取2次,每次1小时。用水量在设置的三个因素中对综合评分影响最大,但仍无统计学差异(P0.05),说明用水量、提取次数、提取时间三种工艺的改变对黄芪水提工艺的综合评分无显著性影响。综合出膏率、黄芪甲苷和毛蕊异黄酮苷的含量得出综合评分来优选黄芪水提的最佳提取工艺,能够从化学成分的角度来客观全面地评价和研究黄芪水提的关键环节,这也为芪龙胶囊和黄芪配方颗粒水提环节工艺的优化提供借鉴和指导。[align=center] [/align][align=center]参考文献[/align] 陈建真,吕圭源, 叶磊, 等.黄芪黄酮的化学成分与药理作用研究进展. 医药导报, 2009, 28(10): 1314-1316. 赵四清,周日宝, 陈胜璜, 等.不同的产地加工方法对中药材金樱子质量的影响. 湖南中医学院学报, 2005, 25(3): 21-22.
黄芪饮片按照中国药典2015年版方法测定黄芪甲苷液相图谱为2个峰,用含黄芪的超微粉制成的颗粒,测定其黄芪甲苷,液相图谱为1个峰,为什么?颗粒不只含有黄芪,含有其他成分,求解答,谢谢
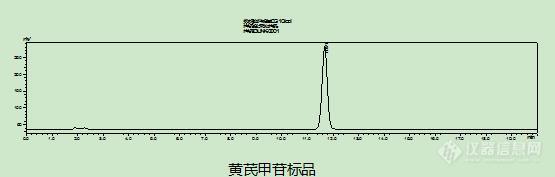
[align=center][color=#333333]黄芪含量测定[/color][/align]1 材料与试剂 乙腈(色谱级)、正丁醇、氨水、甲醇(分析纯)、黄芪甲苷(购自中检院)、血竭样品(送检样品)。2 色谱条件 LC-20AT液相色谱仪(日本岛津),色谱柱:Zorbax SB C18(250mm*4.6μm*5μm)(安捷伦),流动相:以乙腈-水(30:70);蒸发光检测器(奥泰);柱温35℃。3 样品制备(参照2015年版药典) 3.1 标准品溶液的制备 取黄芪甲苷对照品适量,精密称定,加甲醇溶解,即得。[align=center][img=,555,177]https://ng1.17img.cn/bbsfiles/images/2019/09/201909121553061421_926_1858223_3.jpg!w555x177.jpg[/img][/align]3.2 样品溶液的制备 取本品中粉约4g,精密称定,置索氏提取器中,加甲醇40ml,冷浸过夜,再加甲醇适量,加热回流4小时,提取液回收溶剂并浓缩至干,残渣加水10ml,微热使溶解,用水饱和的正丁醇振摇提取4次,每次40ml,合并正丁醇液,用氨试液充分洗涤2次,每次40ml,弃去氨液,正丁醇液蒸干,残渣加水5ml使溶解,放冷,通过D101型大孔吸附树脂柱(内径为1.5cm,柱高为12cm),以水50ml洗脱,弃去水液,再用40%乙醇30ml洗脱,弃去洗脱液,继用70%乙醇80ml洗脱,收集洗脱液,蒸干,残渣加甲醇溶解,转移至5ml量瓶中,加甲醇至刻度,摇匀,即得。[align=center][img=,583,180]https://ng1.17img.cn/bbsfiles/images/2019/09/201909121553295651_9515_1858223_3.jpg!w583x180.jpg[/img][/align]3.3 计算方法 分别精密吸取对照品溶液10μl、20μl,供试品溶液20μl,注入液相色谱仪,测定,用外标两点法对数方程计算,即得。小结:每次接到黄芪样品大家都会来一句怎么又有黄芪,大概黄芪是比较受嫌弃的中药材之一了,药典上的方法过程比较繁琐,一般需要2-3天才能把前处理处理完。检测简述流程:浸泡过夜——索氏提取4h——旋干——萃取 (4次+2次)——蒸干(这个正丁醇不太好旋干比较耗时)——过大孔树脂柱(上样之前要洗至无醇味,然后上样后用3种溶剂洗脱)——旋干——定容待测。为了减少误差及节省时间,我们考察了正丁醇的萃取次数对含量的影响,我们用2次80ml和4次40ml进行对比发现结果相当,实验操作过程中萃取次数越多反而容易引起操作误差,值得大家注意的是大孔树脂上样前要洗至无醇味,这个对结果影响还是有的,保证数据的平行性,用同体积的水进行洗至无醇味。
[color=#fe2419]维权声明:本文为[color=#000000]03yx2[/color]原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。[/color][size=3][font=宋体]醒脑再造丸是由黄芪、淫羊藿、石菖蒲、当归等三十六味中药组成的复方制剂,具有[/font][/size][size=3][font=宋体]化痰醒脑,祛风活络的功效。用于神志不清,语言蹇涩,肾虚痿痹,筋骨酸痛,手足拘挛,半身不遂。[/font][/size][size=3][font=宋体]醒脑再造丸原收载于《中华人民共和国卫生部药品标准中药成方制剂》第四册,为国家药典委员会拟上《中国药典》2010年版一部品种。[color=black]原标准较简单,无含量测定项,不足以控制其质量。根据《中国药典》2010年版一部起草要求[/color][/font][/size][color=black][size=3][font=宋体],建立质控指标[/font][/size][/color][color=black][size=3][font=宋体]。因[/font][/size][/color][color=black][size=3][font=宋体]醒脑再造丸处方中黄芪为君药,[/font][/size][/color][color=black][size=3][font=宋体]黄芪与本品的功能主治有密切关系。[/font][/size][/color][size=3][font=宋体]参照《中国药典》2005年版一部黄芪项下含量测定方法,采用[/font][/size][size=3][font=宋体]HPLC-ELSD[/font][/size][size=3][font=宋体]法[/font][/size][size=3][font=宋体]测定黄芪中黄芪甲苷的含量,控制本制剂的内在质量,具有合理性,且方法[/font][/size][size=3][font=宋体]简便易行[/font][/size][size=3][font=宋体],结果准确,重现性好。[/font][/size][size=3][/size]

【作者】 徐小利; 陈晓虎; 谢静;【Author】 Xu Xiaoli,Chen Xiaohu,Xie Jing(Chongqing Institute for Drug Control,Chongqing,China 401121)【机构】 重庆市药品检验所;【摘要】 目的建立高效液相色谱-蒸发光散射检测(HPLC-ELSD)法测定补中益气丸(浓缩丸)的黄芪甲苷含量。方法色谱柱为Diamonsil(钻石)C18柱(200mm×4.6mm,5μm),柱温为30℃,流动相为乙腈-水(38:62),流速为0.8mL/min,ELSD条件为漂移管温度110℃,气体流速3.0L/min。结果黄芪甲苷进样量在2.494~39.904μg范围内与峰面积线性关系良好,r=0.9999,平均加样回收率为97.26%,RSD=1.94%(n=6)。结论所用方法简便快捷,测定结果可靠,可用于补中益气丸的质量控制。 更多还原【Abstract】 Objective To establish a HPLC-ELSD method to determination of astragaloside Ⅳ in Buzhongyiqi Wan.Methods Diamonsil-C18 column(200 mm× 4.6 mm,5 μ m) was employed,and its temperature was 30 ℃.Axetonitrile-water(38:62) was as the mobile phase at the flow rate of 0.8 mL/min.ELSD inlet heater was set at 110 ℃,and N2 flow rate of 3.0 L/min.Results The calibration curve of astragaloside Ⅳ was linear in the range of 2.494-39.904 μg(r=0.999 9).The average recovery was 97.26%,RSD=1.94%(n=6).Conclusion The... 更多还原【关键词】 高效液相色谱-蒸发光散射法; 补中益气丸; 黄芪甲苷; 含量测定; 【Key words】 HPLC-ELSD; Buzhongyiqi Wan; astragaloside Ⅳ; content determination; http://ng1.17img.cn/bbsfiles/images/2012/08/201208271543_386438_2352694_3.jpg
国内最大最专业的国家标准物质服务平台坛墨质检-国家标准物质中心(北京坛墨质检科技有限公司),是国家质检总局指定的国家标准物质研制单位,是国内最大最专业的食品、环境、职业卫生标准物质生产商和服务商。BW5571 β-桉叶醇对照品,有报告 HPLC≥98% BW5572 环黄芪醇对照品,有报告 HPLC≥98% BW5573 丹参素对照品,有报告 HPLC≥98% BW5574 二氢姜黄素对照品,有报告 HPLC≥98% BW5575 绵马贯众素ABBA; 东北贯众素对照品,有报告 HPLC≥98% BW5576 刺甘草查尔酮对照品,有报告 HPLC≥98% BW5577 大黄素-8-β-D-吡喃葡萄糖苷对照品,有报告 HPLC≥98% BW5578 绵马酸ABA对照品,有报告 HPLC≥98% BW5579 异莲心碱对照品,有报告 HPLC≥98% BW5580 甘草查尔酮A对照品,有报告 HPLC≥98% BW5581 甘草查尔酮B对照品,有报告 HPLC≥98% BW5582 甘草查尔酮C对照品,有报告 HPLC≥98% BW5584 莲心碱对照品,有报告 HPLC≥98% BW5585 芳樟醇对照品,有报告 HPLC≥98% BW5586 木兰花碱 HPLC≥98% BW5587 甲基橙皮苷对照品,有报告 HPLC≥98% BW5588 甲基原薯蓣皂苷对照品,有报告 HPLC≥98% BW5589 丹参酚酸B甲酯对照品,有报告 HPLC≥98% BW5590 桑辛素对照品,有报告 HPLC≥98% BW5591 桑皮苷A对照品,有报告 HPLC≥98% BW5592 桑皮苷C对照品,有报告 HPLC≥98% BW5593 丁烯基苯酞对照品,有报告 HPLC≥98% BW5594 甲基莲心碱对照品,有报告 HPLC≥98% BW5595 新穿心莲内酯对照品,有报告 HPLC≥98% BW5596 氧化芍药苷(羟基芍药苷)对照品,有报告 HPLC≥98% BW5597 茯苓酸对照品,有报告 HPLC≥98% BW5598 伪金丝桃素; 假金丝桃素对照品,有报告 HPLC≥98% 坛墨质检现有员工79人,办公室面积450平米,实验室1650平米;销售、客服、财务及行政人员35人,实验室工作人员21人,库房14人,市场部8人。实验仪器设备:气相色谱、液相色谱、气质联用、液质联用、离子色谱、紫外分光光度计,原子吸收、ICP-OES和ICP-MS;库房面积450平米,库房工作人员12人,现货产品5万个,坛墨质检自主研发的产品近3000个,已申报国标345项,填补国内空白的产品达到65项。坛墨质检是国内唯一提供标准溶液定制服务的标准物质研制单位,定制范围:特殊浓度定制、特殊溶剂定制、混标定制。
国内最大最专业的国家标准物质服务平台坛墨质检-国家标准物质中心(北京坛墨质检科技有限公司),是国家质检总局指定的国家标准物质研制单位,是国内最大最专业的食品、环境、职业卫生标准物质生产商和服务商。BW5152 穿心莲内酯对照品,有报告 HPLC≥98% BW5153 甘草酸对照品,有报告 HPLC≥98% BW5154 甘草次酸对照品,有报告 HPLC≥98% BW5155 甘草苷对照品,有报告 HPLC≥98% BW5156 异甘草苷对照品,有报告 HPLC≥98% BW5157 新橙皮苷对照品,有报告 HPLC≥98% BW5158 大黄酸对照品,有报告 HPLC≥98% BW5160 大黄素甲醚对照品,有报告 HPLC≥98% BW5161 大黄酚对照品,有报告 HPLC≥98% BW5162 芦荟大黄素对照品,有报告 HPLC≥98% BW5164 二氢杨梅素对照品,有报告 HPLC≥98% BW5165 阿魏酸对照品,有报告 HPLC≥98% BW5166 白藜芦醇对照品,有报告 HPLC≥98% BW5167 虎杖苷(白藜芦醇苷)对照品,有报告 HPLC≥98% BW5169 丹皮酚对照品,有报告 HPLC≥98% BW5170 丹酚酸A对照品,有报告 HPLC≥98% BW5171 灵芝酸A对照品,有报告 HPLC≥98% BW5172 隐丹参酮对照品,有报告 HPLC≥98% BW5173 丹参素钠对照品,有报告 HPLC≥98% BW5174 辅酶Q10对照品,有报告 HPLC≥98% BW5175 粉防己碱(汉防己甲素)对照品,有报告 HPLC≥98% BW5176 防己诺林碱(汉防已乙素)对照品,有报告 HPLC≥98% BW5177 黄芪总皂苷对照品,有报告 UV≥98% BW5178 黄芪皂苷I对照品,有报告 HPLC≥98% BW5179 黄芪皂苷II对照品,有报告 HPLC≥98% BW5180 黄芪皂苷III对照品,有报告 HPLC≥98% BW5181 丁香酚对照品,有报告 HPLC≥98% 坛墨质检现有员工79人,办公室面积450平米,实验室1650平米;销售、客服、财务及行政人员35人,实验室工作人员21人,库房14人,市场部8人。实验仪器设备:气相色谱、液相色谱、气质联用、液质联用、离子色谱、紫外分光光度计,原子吸收、ICP-OES和ICP-MS;库房面积450平米,库房工作人员12人,现货产品5万个,坛墨质检自主研发的产品近3000个,已申报国标345项,填补国内空白的产品达到65项。坛墨质检是国内唯一提供标准溶液定制服务的标准物质研制单位,定制范围:特殊浓度定制、特殊溶剂定制、混标定制。
使用蒸发光检测器做黄芪甲苷含量不出峰怎么办?使用的液相是伍丰手动的
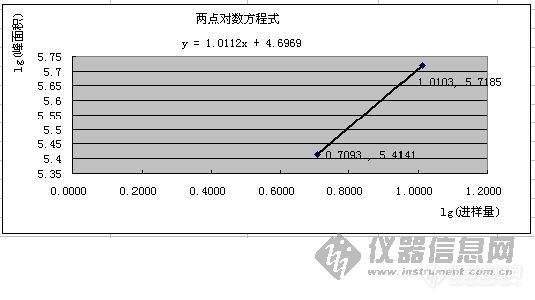
[color=#00008b]前言:本篇是以黄芪含量测定的方法为例来介绍两点对数方程的应用,有关安捷伦1100的操作方法和蒸发光检测器的知识大家可以在本网和回帖中找到,如有疑问我们共同探讨。并在此感谢大家对文章的建议,也使我学到了很多知识,谢谢大家![/color][size=4][b] 解析外标两点对数方程计算黄芪药材含量[/b][/size][b]方 法[/b]: 照高效液相色谱法,ODS柱,以乙腈-水(32:68)为流动相,流速1ml/min,经蒸发光检测器检测,用外标两点对数方程计算黄芪药材中黄芪甲苷的含量。[b]仪 器[/b]: 安捷伦1100型液相色谱仪、蒸发光检测器(ELSD)、ODS柱(4.6um*5mm*200mm)[b]供试品[/b]: 黄芪药材(检测成分:黄芪甲苷)[b]关键词[/b]: 高效液相法、蒸发光检测器、黄芪甲苷、粉碎、提取物、外标两点对数方程[b]正 文[/b]:[color=#dc143c]前处理:[/color]取约20g的黄芪药材放置于小型粉碎机内,粉碎后,盛装在密闭的容器中待用。[color=#dc143c]供试品制备:[/color]取黄芪药材粉末两份,Ⅰ.4.0037g;Ⅱ.4.0022g。分别置索氏提取器中,加甲醇40ml,浸泡过夜(大于8小时)。第二天,加甲醇适量,加热回流4小时,提取液浓缩至干,残渣加水10ml,微热使溶解,用水饱和的正丁醇(制法:把水加入正丁醇中至饱和)振摇提取4次,每次40ml,合并正丁醇液;用氨试液充分洗涤2次,每次40ml,弃去氨液,正丁醇液蒸干,残渣加水5ml使溶解,放冷;通过D101型大孔吸附树脂柱(备注:自己装填),并以水50ml洗脱,弃去水液;再用40%乙醇30ml洗脱,弃去洗脱液;继用70%乙醇80ml洗脱,收集洗脱液,蒸干;用甲醇溶解并转移至5ml量瓶中,加甲醇至刻度,摇匀,即得供试品溶液。简单讲,即把黄芪药材最后提取物(黄芪甲苷)溶解到5ml甲醇中。[color=#dc143c]对照品制备:[/color]称取黄芪甲苷对照品(中检所购入)0.0512g至100ml容量瓶中,用甲醇溶解至刻度,摇匀,即得。[color=#dc143c]测定:[/color]系统平衡后,精密吸取对照品溶液10ul进样,得色谱峰面积Ⅰ.259457 ;进样20ul,得色谱峰面积Ⅱ.523039。供试品溶液进样20ul,两针,色谱峰面积为:Ⅰ.909836,Ⅱ. 902925 。根据对照品峰面积和进样量,以外标两点对数方程计算供试品含量。[color=#dc143c]两点对数方程定义:[/color]是利用两点的对数值呈线性关系求解二元一次方程y=ax+b。本题是利用对照品溶液两针进样量的对数值和所得峰面积的对数值呈线性的关系,把两组数据带入方程y=ax+b中,求得a和b,即求解了该方程式。然后带入供试品峰面积的对数值,求得供试品进样量的对数值,对其求反对数得供试品进样量(黄芪甲苷的量)。方程中x、y值均为进样量和峰面积取对数(lg)后的数值。简单讲,就是通过对照品溶液两针的进样量和峰面积(均取对数lg)求解方程式后,把供试品峰面积(取对数lg)带入方程式求得供试品的进样量。[color=#dc143c]数据处理:[/color]根据外标两点对数方程,应先计算得到方程式中的x、y值,才能求解此方程式。即取对照品进样量的对数值为x,取对照品峰面积对数值为y,计算结果如下:---------对照品-----------Ⅰ--------------------------Ⅱ---------进样量:---0.0512g×10ul(5.12ug)-----0.0512g×20ul(10.24ug)进样量取lg,得x:--------0.7093 --------------------1.0103 -----色谱峰面积:--------259457---------------------523039峰面积取lg,得y:--------5.4141---------------------5.7185 [color=#dc143c]方程式求解:[/color]根据“数据处理”中求得的x、y值,通过Excel图表中的XY散点图,以(0.7093,5.4141)、(1.0103, 5.7185)两点,求得方程如下:[img]http://ng1.17img.cn/bbsfiles/images/2009/09/200909021104_169264_1622024_3.jpg[/img][color=#dc143c]供试品进样量求解:[/color]取供试品色谱峰面积的对数值,得y,带入已求得的方程式y=1.0112x+4.6969,求得x,如下:---------供试品------------Ⅰ----------------------Ⅱ ---------称样量:--------4.0037g -----------------4.0022g -----色谱峰面积:--------909836-------------------902925峰面积取lg,得y:--------5.9590-------------------5.9557 通过方程,求得x:--------1.2481-------------------1.2448根据lg(进样量)=x,求x(1.2481、1.2448)的反对数,得供试品进样量:Ⅰ.17.7052ug 、Ⅱ.17.5711ug(黄芪甲苷)[color=#dc143c]含量计算:[/color]根据供试品称样量、样品的稀释倍数5ml及20ul进样量中黄芪甲苷的量,求得:供试品Ⅰ含量:(17.7052ug×5ml/4.0037g/20ul)×100%=0.1106%供试品Ⅱ含量:(17.5711ug×5ml/4.0022g/20ul)×100%=0.1098%平均值为:(0.1106%+0.1098%)/ 2 = 0.11%[color=#dc143c]结 果:[/color]该批黄芪药材中含黄芪甲苷的量为0.11%。[color=#dc143c]数据处理Excel表:[/color]见附件:[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=169305]黄芪含量测定数据处理全过程[/url][b]参考文献[/b]:1.《中国药典》2005版一部2.《高效液相色谱法及其在药物分析中的应用》(中华康网)3.《你了解蒸发光检测器吗?》(仪器信息网)(全文完,请大家指导!)===============================================================================================蒸发光检测器知识:一.[b]ELSD检测步骤[/b]:1)雾化:在雾化器中,洗脱液通过1个针孔与氮气(也可以用空气)混合,形成均匀的雾状液滴。2)流动相蒸发:液滴通过加热的漂移管时,流动相被蒸发,样品组分形成气溶胶,进人检测室。3)检测:在检测室内,用激光来照射气溶胶,产生散射,测定散射光强,记录散射光强度随时间的变化关系,就得到了色谱图。二.[b]ELSD检测原理[/b]:气溶胶受固定光强的激光照射后,待测组分的质量(m)和散射光强度(I)有以下的关系:I=Kmb lgI=blgm+lgK式中K和b为与蒸发室温度和流动相性质有关的常数。上式说明散射光的对数响应值与组分的质量的对数成线性关系。
国内最大最专业的国家标准物质服务平台坛墨质检-国家标准物质中心(北京坛墨质检科技有限公司),是国家质检总局指定的国家标准物质研制单位,是国内最大最专业的食品、环境、职业卫生标准物质生产商和服务商。BW5152 穿心莲内酯对照品,有报告 HPLC≥98% BW5153 甘草酸对照品,有报告 HPLC≥98% BW5154 甘草次酸对照品,有报告 HPLC≥98% BW5155 甘草苷对照品,有报告 HPLC≥98% BW5156 异甘草苷对照品,有报告 HPLC≥98% BW5157 新橙皮苷对照品,有报告 HPLC≥98% BW5158 大黄酸对照品,有报告 HPLC≥98% BW5160 大黄素甲醚对照品,有报告 HPLC≥98% BW5161 大黄酚对照品,有报告 HPLC≥98% BW5162 芦荟大黄素对照品,有报告 HPLC≥98% BW5164 二氢杨梅素对照品,有报告 HPLC≥98% BW5165 阿魏酸对照品,有报告 HPLC≥98% BW5166 白藜芦醇对照品,有报告 HPLC≥98% BW5167 虎杖苷(白藜芦醇苷)对照品,有报告 HPLC≥98% BW5169 丹皮酚对照品,有报告 HPLC≥98% BW5170 丹酚酸A对照品,有报告 HPLC≥98% BW5171 灵芝酸A对照品,有报告 HPLC≥98% BW5172 隐丹参酮对照品,有报告 HPLC≥98% BW5173 丹参素钠对照品,有报告 HPLC≥98% BW5174 辅酶Q10对照品,有报告 HPLC≥98% BW5175 粉防己碱(汉防己甲素)对照品,有报告 HPLC≥98% BW5176 防己诺林碱(汉防已乙素)对照品,有报告 HPLC≥98% BW5177 黄芪总皂苷对照品,有报告 UV≥98% BW5178 黄芪皂苷I对照品,有报告 HPLC≥98% BW5179 黄芪皂苷II对照品,有报告 HPLC≥98% BW5180 黄芪皂苷III对照品,有报告 HPLC≥98% BW5181 丁香酚对照品,有报告 HPLC≥98% 坛墨质检现有员工79人,办公室面积450平米,实验室1650平米;销售、客服、财务及行政人员35人,实验室工作人员21人,库房14人,市场部8人。实验仪器设备:气相色谱、液相色谱、气质联用、液质联用、离子色谱、紫外分光光度计,原子吸收、ICP-OES和ICP-MS;库房面积450平米,库房工作人员12人,现货产品5万个,坛墨质检自主研发的产品近3000个,已申报国标345项,填补国内空白的产品达到65项。坛墨质检是国内唯一提供标准溶液定制服务的标准物质研制单位,定制范围:特殊浓度定制、特殊溶剂定制、混标定制。
维权声明:本文为yhc2004原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。有机氯农药是一类高效广谱杀虫剂,曾在世界各国广泛使用。我国虽已在1983年停止使用这类农药,但由于它具有化学性质稳定、不易分解,并通过生物链富集在动植物体内,造成了对自然环境的严重污染及对人体健康的极大危害。中药材种植期一般较长,尤其是多年生根类药材,更易受到有机氯农药的污染。我国中药材中的农药残留的污染,是造成中药材质量下降的重要原因,已成为制约我国中药材走向国际市场的主要障碍。因此,中药材中农药残留问题已经引起了国内外的普遍关注,建立和完善中药材中有机氯农药残留量的检测方法十分必要。 黄芪药材为豆科植物蒙古黄芪或膜荚黄芪的干燥根。呈圆柱形,表面淡棕黄色或淡棕褐色,有不整齐的纵皱纹或纵沟。质硬而韧,不易折断,断面纤维性强,并显粉性,皮部黄白色,木部淡黄色,具放射状纹理及裂隙,呈“菊花心状”。气微,味微甜。嚼之有豆腥味。性温,味甘。具有补气固表,利尿,托毒,排脓,敛创生肌之功效。主产于山西、黑龙江、内蒙古等省区。以栽培的蒙古黄芪质量为佳。至今为止,对其中有机氯农药六六六、滴滴涕残留测定的研究未见报道。本文建立了黄芪药材中9种有机氯农药超声提取,毛细管气相色谱检测的方法,为提高传统中药的质量、建立和完善中药产品中有机氯类农药残留量的测定的方法提供依据。 1 仪器与试剂1.1 仪器 THGC-2001气相色谱仪,电子捕获检测器,弹性石英毛细管柱 30m×0.32mm×0.25μm。800型离心机。1.2 试剂 丙酮(分析纯),石油醚(沸程60~90℃,分析纯),二氯甲烷(分析纯)无水硫酸钠(分析纯)硫酸(分析纯)有机氯农药六六六(BHC)(α-BHC,β-BHC,γ-BHC,δ-BHC)、滴滴涕(DDT)(PP΄-DDE, PP΄-DDD ,OP΄ -DDT,PP΄-DDT)及五氯硝基苯(PCNB)标准品(农业部农药检定所)2 方法与结果2.1 对照品的制备2.1.1 对照品储备液的制备精密称取六六六(BHC)(α-BHC,β-BHC,γ-BHC,δ-BHC)、滴滴涕(DDT)(PP΄-DDE, PP΄-DDD ,OP΄ -DDT,PP΄-DDT)及五氯硝基苯(PCNB)农药对照品适量,用石油醚(60~90℃)分别制成每1ml约含4~5µg的溶液,即得2.1.2 混合对照品储备液的制备 精密量取上述各对照品储备液0.5ml,置10ml量瓶中,用石油醚(60~90℃)稀释至刻度,摇匀,即得。2.1.3 混合对照品溶液的制备 精密量取上述混合对照品储备液,用石油醚(60~90℃)制成每1L分别含0µg、1µg、5µg、10µg、50µg、100µg、250µg的溶液,即得。 2.2 色谱条件 弹性石英毛细管柱 30m×0.32mm×0.25μm;进样口温度230℃,检测器温度300℃,不分流进样;流速为28ml/min;程序
国内最大最专业的国家标准物质服务平台坛墨质检-国家标准物质中心(北京坛墨质检科技有限公司),是国家质检总局指定的国家标准物质研制单位,是国内最大最专业的食品、环境、职业卫生标准物质生产商和服务商。 产品编号 产品名称 标准值 BW6053三七总皂苷对照品,有报告HPLC≥98%BW6049氯化木兰花碱对照品,有报告HPLC≥98%BW6050金合欢素;刺槐素对照品,有报告HPLC≥98%BW605910-去乙酰紫杉醇;7-表-去乙酰基紫杉醇对照品,有报告HPLC≥98%BW6060紫檀芪对照品,有报告HPLC≥98%BW6052正丁基苯酞;丁基酞内酯对照品,有报告HPLC≥98%BW6012构树碱A对照品,有报告HPLC≥98%BW6082罗汉果皂苷V对照品,有报告HPLC≥98%BW6019多被银莲花皂苷R8对照品,有报告HPLC≥98%BW6018虎掌草皂甙D对照品,有报告HPLC≥98%BW6010藤黄酸对照品,有报告HPLC≥98%BW6016苍耳亭对照品,有报告HPLC≥98%BW6014麻枫树酚酮B对照品,有报告HPLC≥98%BW6009远志皂苷B对照品,有报告HPLC≥98%BW6017粗茎乌头碱甲对照品,有报告HPLC≥98%BW6011雷酚内酯对照品,有报告HPLC≥98%BW60133β-乙酰氧基-7,25-甘遂二烯-24(R)-醇对照品,有报告HPLC≥98%BW60323,6-二芥子酰基蔗糖对照品,有报告HPLC≥98%BW6039延胡索甲素对照品,有报告HPLC≥98%BW6041野黄芩素(金黄紫碱)对照品,有报告HPLC≥98%BW6040芫花素对照品,有报告HPLC≥98%BW6031华蟾毒精(蟾酥)对照品,有报告HPLC≥98%BW6055澳洲茄胺;澳州茄胺对照品,有报告HPLC≥98%BW6026附子灵对照品,有报告HPLC≥98%BW6028路路通酸(白桦脂酮酸)对照品,有报告HPLC≥98% 坛墨质检现有员工79人,办公室面积450平米,实验室1650平米;销售、客服、财务及行政人员35人,实验室工作人员21人,库房14人,市场部8人。实验仪器设备:气相色谱、液相色谱、气质联用、液质联用、离子色谱、紫外分光光度计,原子吸收、ICP-OES和ICP-MS;库房面积450平米,库房工作人员12人,现货产品5万个,坛墨质检自主研发的产品近3000个,已申报国标345项,填补国内空白的产品达到65项。坛墨质检是国内唯一提供标准溶液定制服务的标准物质研制单位,定制范围:特殊浓度定制、特殊溶剂定制、混标定制。