β-内酰胺类抗生素高分子杂质的检测
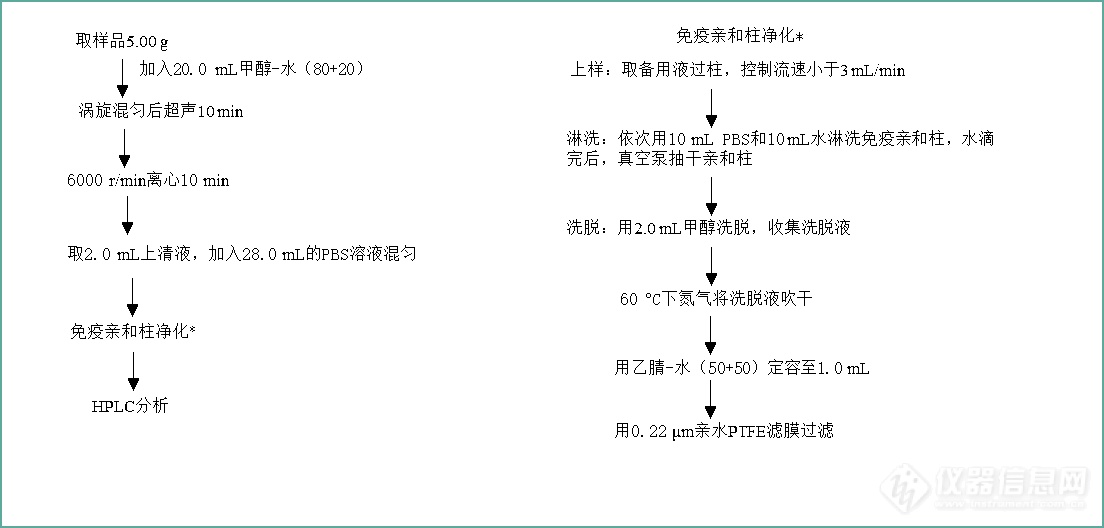
&beta -内酰胺类抗生素中的高分子杂质是引发速发型过敏反应的过敏原,是药物质量控制过程中的重点检测项目。目前药典中关于&beta -内酰胺类抗生素中高分子杂质的测定多采用葡聚糖凝胶Sephadex G-10自填装玻璃管柱,存在柱效低、分离时间长、分离度差、批间重现性差、操作不便等缺点,为了解决这些问题,采用小粒径、高分辨率的体积排阻色谱成品柱已成为&beta -内酰胺类抗生素中高分子杂质检测的必然趋势。 赛分科技体积排阻色谱柱SRT(5 &mu m)、 Zenix&trade (3 &mu m)&mdash &mdash 水溶性体积排阻色谱柱 SRT和Zenix色谱柱固定相采用专利的表面修饰技术(专利US 7,247,387B1和US 7,303,821B1),通过在高纯度具有良好机械稳定性的硅胶基质上,键合一层均匀的纳米厚度中性亲水薄膜而制备得到。 ● 采用可控的化学修饰技术,能确保柱与柱之间有着可靠的重现性;● 精心设计的大孔体积可保证高的分离容量以及优异的分辨率;● 表面亲水涂层覆盖完全,使之具有优异的色谱柱稳定性,延长色谱柱寿命;● 低盐浓度洗脱,适合LC-MS分析;● 专利的表面修饰层,确保对样品的最大回收率;● 广泛适用于生物分子及水溶性聚合物的分离和检测。 SRT和Zenix色谱柱对于水溶性&beta -内酰胺类抗生素中高分子杂质的检测具有良好的效果。Mono GPC &mdash &mdash 油溶性体积排阻色谱柱 Mono GPC以具有极窄粒径和孔径分布的高交联度聚苯乙烯/二乙烯苯(PS/DVB)颗粒为基质,孔径分布均一,使分析中保留时间与分子量具有准确的线性关系。高交联度的多孔颗粒具有优异的化学和物理稳定性,因此在更换有机溶剂时可以使分子量校正曲线的形状及色谱柱的柱效几乎保持不变。Mono GPC填料具有大的孔体积,可确保对聚合物分离有着高的分辨率。 Mono GPC对于脂溶性&beta -内酰胺类抗生素中高分子杂质的检测具有良好的效果。Zenix-150对头孢地嗪钠高分子杂质的检测注:分离度按照2010版《中国药典》附录VH计算。&mdash &mdash 样品来源于某制药公司良好的批间重现性&mdash &mdash 色谱条件同上 Zenix SEC-150 材料 表面键合亲水薄膜的硅胶颗粒大小 3 &mu m孔径 (Å )~ 150蛋白分子量范围 500 - 150,000水溶性聚合物分子量范围 500 - 25,000pH 稳定性 2 &ndash 8.5,短时可耐pH 8.5-9.5反压 (7.8x300 mm)~ 1,500 psi最大耐受压力 (psi)~ 4,500盐浓度范围 20 mM - 2.0 M最高使用温度 (oC)~ 80流动相的兼容性 常规水相及有机相溶剂应用实例头孢地嗪钠头孢西丁头孢米诺钠头孢拉定头孢呋辛酯头孢地尼头孢泊肟酯美洛西林钠磺苄西林钠头孢尼西头孢噻肟钠头孢噻吩钠比阿培南阿莫西林头孢噻利头孢丙烯泰比培南酯磺苄西林钠破坏物盐酸头孢替安头孢硫脒头孢特仑新戊酯头孢哌酮钠 注:点击链接可见图谱。 优质服务● 提供免费的产品试用● 提供实际样品的色谱柱筛选和方法确认促销公告即日起至8月30日,凡购买一支体积排阻色谱柱,第二支体积排阻色谱柱享受五折优惠或赠送一支高端C18柱。注:第二支体积排阻色谱柱市场价不得高于第一支。订货信息产品名称粒度孔径规格订货号 SRT SEC-1005 &mu m100 Å 7.8x300 mm215100-7830 SRT SEC-1505 &mu m150 Å 7.8x300 mm215150-7830Zenix SEC-1003 &mu m100 Å 7.8x300 mm213100-7830Zenix SEC-1503 &mu m150 Å 7.8x300 mm213150-7830Mono GPC-1005 &mu m100 Å 7.8x300 mm230100-7830关于赛分科技 赛分科技有限公司(Sepax Technologies, Inc)总部位于美国特拉华州高新技术开发区,致力于开发和生产药物与生物大分子分离和纯化领域的技术和产品。赛分科技是集研发、生产和全球销售为一体的实业型企业。公司主要产品为液相色谱柱及耗材、固相萃取柱(SPE)及耗材、液相色谱填料以及分离纯化仪器设备。在液相色谱领域里,赛分科技已开发出了100多种不同型号的液相色谱材料,涵盖了反相、正相、超临界(SFC)、手性(Chiral)、离子交换、体积排阻、亲和、HILIC等各种类别,为世界范围内液相色谱产品最为完善的企业之一。 赛分科技的创新技术使之生产出具有最高分辨率及最高效的生物分离产品,包括体积排阻、离子交换、抗体分离、和糖类化合物分离色谱填料和色谱柱,可广泛地应用于单克隆抗体、各种蛋白、DNA、RNA、多肽、多糖和疫苗等生物样品的分析、分离和纯化。赛分科技先进的技术和完善的产品线已使赛分成为全球生物分离的领航者。 公司网站: www.sepax-tech.com.cn www.sepax-tech.com