一、凝胶制备1. 微波炉溶解琼脂糖时,胶液沸腾冲溢出三角锥瓶微波炉加热时胶液可能发生剧烈沸腾,(1)总液体量不宜超过三角锥瓶的50%容量。(2)2%以上胶液设置中火加热。 (3)胶液剧烈沸腾时,停止加热,移开三角锥瓶,请戴上防热手套,小心摇动三角锥瓶,然后再次加热,胶液沸腾直至胶液清澈,保证琼脂糖完全溶解。 2. 琼脂糖电泳图像背景模糊不清:琼脂糖没有完全溶解会造成电泳图像背景模糊不清。完全溶解的琼脂糖胶液清澈,三角锥瓶内壁应没有粘附琼脂糖颗粒。 3.加热后水分蒸发,如需要应加入热的蒸馏水,补足到原来的重量,摇匀。 二、电泳1. DNA条带模糊,拖尾。 (1)DNA降解。避免核酸酶污染。 (2)DNA上样量过多。减少凝胶中DNA上样量。 (3)电泳缓冲液陈旧:电泳缓冲液多次使用后,离子强度降低,pH值上升,缓冲能力减弱,从而影响电泳效果。建议经常更换电泳缓冲液。 (4)电泳条件不合适。电泳时电压不应超过20 V/cm,温度<30℃,巨大DNA链,温度应<15℃,核查所用电泳缓冲液是否有足够的缓冲能力。 (5)DNA样含盐过高。泳前通过乙醇沉淀去除过多的盐。 (6)有蛋白污染。电泳前抽提去除蛋白。 (7)DNA变性。电泳前勿加热,用20 mM NaCl缓冲液稀释DNA。[/c

琼脂糖凝胶电泳是分子实验的基础,方法步骤也再熟悉不过了,把它下来主要是和大家一起分享自己的操作习惯和通过图片展示一下操作环境,并一起讨论实验中遇到的问题。一 简单概述琼脂糖凝胶电泳时用琼脂糖作支持介质的一种电泳方法,因为琼脂糖凝胶具有网络状的结构,小分子可以顺利通过,而大分子在通过时会受到阻力,从而把大分子和小分子分离来。在电泳时,分子移动速度与分子大小和分子所带电荷有关,分子越大移动速度也慢。蛋白质是高分子物质,因此不适用于凝胶电泳,现今凝胶电泳被广泛应用于类似核酸的小分子的研究中。二 实验操作总结1准备好各种试剂和设备,设备包括电泳槽,电泳仪,微波炉,三角瓶,搅拌器,制胶槽和梳子,电子秤,量筒;试剂包括电泳缓冲液TAE,琼脂糖,核酸染料。2 根据制胶的大小和浓度,称量相应重量琼脂糖,加入对应体积的缓冲液,混匀,用微波炉加热至琼脂糖完全溶解,此时溶液澄清,无游离状物质漂浮于液体中。http://ng1.17img.cn/bbsfiles/images/2015/08/201508062230_559545_3030887_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/08/201508062228_559542_3030887_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/08/201508062230_559549_3030887_3.jpg3 加热溶解后冷却,期间加入核酸染料,一点即可。4冷却至不烫手即可导入到制胶槽中。冷却的目的是防止琼脂糖溶液温度过高是制胶槽和梳子变形。倒入制胶槽后,赶走胶上的气泡,插上梳子。http://ng1.17img.cn/bbsfiles/images/2015/08/201508062230_559547_3030887_3.jpg5等待十分钟左右至胶凝固,拔掉梳子。注意的是经常有人拔梳子时吧点样孔破坏,所以拔梳子时手掌先压住电泳槽,然后拿住梳子两边,快速向上用力将梳子拔出,这样能较好的避免点样孔的损失。6胶制好后,点样。点样分为干点和湿点两种,干点是不在缓冲液中点,直接在外界中操作;湿点是将胶放入缓冲液中点样,样品点样前先加入Ladding Buffer,Ladding Buffer目的是帮助样品沉淀,有时干点可不加,但是湿点的时候最好要加。7电泳,将点样后的胶放入电泳槽中,注意电极方向,根据电泳槽大小设置电泳时间和电压。http://ng1.17img.cn/bbsfiles/images/2015/08/201508062230_559548_3030887_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/08/201508062230_559546_3030887_3.jpg8成像。电泳完后,在琼脂糖凝胶显色系统中拍照保存,进行后续实验。http://ng1.17img.cn/bbsfiles/images/2015/08/201508062229_559544_3030887_3.jpg9 分析。从上面的图片可以看出有些带相对较亮,有些带相对较弱,可能与DNA浓度有关。另外有些带似乎有拖带,可能是引物二聚体。不过总体还说结果还算可以,带型清晰可变。三 写在后面的话总的来说步骤有些多,但是并不是很复杂,也没有很难的技术要点,但是根据成相系统拍摄出来的照片效果显色,一个同样的样品,有时因为制胶的原因,呈现的效果完全不一样,这可能与胶的溶解和加入染料的量、电泳条件等等有关,因此琼脂糖凝胶电泳时需不断总结经验,做出来的胶图才能很漂亮。
急!求降低油脂熔点的方法!!!
各位大家好!可以告知琼脂糖介质的使用方法吗?谢谢!我这里有DEAE CM Q SP的,以及凝胶过滤的!
请问没定有机物的熔点和滴点分别有什么意义石蜡等蜡状膏状物熔点怎么测
请问斑竹:低熔点金属是否可以用透射电镜进行分析,如Sn、Pb等,是否会被电子束加热熔化而污染镜子?谢
电泳基本原理 迁移率(或泳动度)是指带电颗粒在单位电场强度下泳动的速度,可用下列公式计算: U =υ/E =(d/t)/(V/l) =dl/Vt U为迁移率(cm2•V-1•min-1);υ为颗粒泳动速度(cm•s-1);E 为电场强度( V•cm-1);d为颗粒泳动的距离(cm);l为滤纸有效长度(cm);V为实际电压(V);t为通电时间(s或min)。通过测量d, l, V, t, 即可计算出被分离物质的迁移率。 1迁移率单位= 10-5 cm2•V-1•min-1在确定的条件下,某物质的迁移率为常数,是该物质的化学特征常数。 颗粒带净电荷多,直径小而接近于球形,则在电场中泳动速度快,反之则泳动速度慢。 迁移率还与分子的形状,介质粘度,颗粒所带电荷有关,迁移率与颗表面电荷成正比,与介质粘度及颗粒半径成反比。 影响琼脂糖电泳迁移的主要因素 电场强度 溶液的pH值 溶液的离子强度 电渗现象 温度的影响 支持物的影响 按分离原理分类: 1.区带电泳 2.移界电泳 3.等速电泳 4.聚焦电泳 按有无固体支持物分类 1. 纸上电泳 2. 醋酸纤维素膜电泳 3. 薄层电泳 4. 非凝胶性支持物区带电泳(支持物有:淀粉、纤维素粉、玻璃粉、硅胶) 5. 凝胶支持区带电泳(淀粉凝胶、聚丙稀酰胺凝胶、琼脂糖凝胶) 影响琼脂糖电泳迁移的主要因素 DNA的大小 DNA的构象 琼脂糖浓度 缓冲液 不同构像质粒 缓冲液 TAE:乙酸盐缓冲液 TBE:硼酸盐缓冲液 TPE:磷酸盐缓冲液 实验操作 1. 用胶带将洗净、干燥的水平板的边缘封住,形成一个胶模并水平放置。 2. 按水平板的长×宽×0.5cm胶厚,量取0.5×TBE,并按0.7%的浓度称取agarose琼脂糖,在微波炉或电炉上加热至全熔(清澈透明)。 3. 等凝胶温度降至大约50-60以下时,加入1 mg/L溴化乙锭(EB)至终浓度为0.5ug/mL ;摇匀并轻快地倒入水平板中,除掉气泡,插入梳子。 4. 凝固后,将梳子轻轻拔出。 5.去掉胶带,将水平板放入加有0.5×TBE电泳缓冲液的电泳槽中,并且使电泳缓冲液高出凝胶约1mm。 6.在parafilm膜上依次加: ddH2O 6ul,上样Buffer 2ul ,DNA 4ul 分别混匀后点样,记录点样次序。 7. 在水平板两边的点样孔中分别加入6 μ l的λΔΝΑ/EcoRI+HindIII marker。 8. 盖好电泳槽盖子,选择适当的电泳电压(≤5V/cm)及电泳方向(DNA阴极阳极),开始电泳。 9. 当色素接近胶的先端,停止电泳,样品在紫外灯下观察、成像℃
据我所知,Na2CO3(mp:850℃)和K2CO3(mp:890℃)Na2CO3与K2CO3按1∶1形成的混合物,其熔点为700℃左右;另外,用Na2CO3作熔剂时,加入少量NaOH,可提高其分解能力并降低熔点;是不是将Na2CO3与K2CO3按1∶1混合,再加入少量NaOH,是不是熔点就可以降低700℃以下?我现在做试验需要用到Na2CO3熔融,只有镍坩埚,什么办法可以让熔点降到700℃以下,实在不懂混合物熔点是怎么变化的,恳请高人指点,谢谢![em06]
直读光谱激发低熔点软金属和高熔点硬金属的时间有多大差异?在操作软件里有特定设置没有?
如题,熔点低的化合物测干燥失重,如熔点可能只有70度,如果此时用常压恒温干燥法(最后干燥温度为105度)测该物质的干燥失重,结果准确吗?
[em09511]请问各位,琼脂糖凝胶在什么地方运用比较多啊?我们公司自主研发了琼脂糖系列凝胶。有谁需要试用的吗?我可以提供样品。
[align=left][/align][align=left]最近买了一台熔点仪,物光的WRS-3,三根一起测定,是自动测定的。[/align][align=left]但是我测了几个买来的AR级或者GR级的试药,检测了一下熔点,结果总是不在这个物质的标准熔点范围内,[/align][align=left]有的是偏高了有的是偏低了。[/align][align=left]三根的平行性是还好的,但是结果却不准确。[/align][align=left]我是把初始温度设置在低于初熔值十度的位置,三根样品都是一起装料,>3mm,一起从1m以上的管子做自由落体填料,且都大于15次。[/align][align=left]尝试过升温速率2℃/min,也尝试过1℃/min,结果相差不多,偏低的依然是偏低,偏高的依然是偏高。[/align][align=left][/align][align=left]请问这是什么原因,熔点结果范围在怎样的偏差内属于正常?[/align]

[font=宋体][size=10.5000pt]琼脂糖预制胶电泳试剂盒是一种非常适合核酸[/size][/font][font=宋体][size=10.5000pt]PCR[font=宋体]实验、酶切反应实验等的一种可以直接进行核酸凝胶电泳实验的试剂盒,电泳实验效率大大提高,可以节约大量时间。[/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]此款琼脂糖电泳试剂盒跟其它琼脂糖试剂盒有区别,因此使用方法也有一些区别,不需要再四处采购琼脂糖、核酸染料、电泳液和[/font]loading buffer[font=宋体]等试剂;而且琼脂糖预制胶是经过核酸染料预染的,既不用进行繁琐的制胶,也不用电泳液染色或后染色,即开即用;再加上配备的高压快速电泳液,电泳速度远远快与传统的[/font][font=Calibri]TAE[/font][font=宋体]或[/font][font=Calibri]TBE[/font][font=宋体]电泳液。[/font][/size][/font][img=,519,396]https://ng1.17img.cn/bbsfiles/images/2020/07/202007101051212160_1649_3880864_3.jpg!w519x396.jpg[/img][font=宋体][size=10.5000pt]使用方法:[/size][/font][font=宋体][size=10.5000pt]1. [/size][/font][font=宋体][size=10.5000pt][font=宋体]在低温条件下高压快速电泳有时会有结晶析出,请[/font]65[font=宋体]℃水浴加热溶解,用去离子水稀释[/font][font=Calibri]100[/font][font=宋体]倍,用作电泳液,倒入电泳槽中。本产品配置的电泳液可重复使用两三次,如果大电泳槽次数更多。[/font][/size][/font][font=宋体][size=10.5000pt]2. [/size][/font][font=宋体][size=10.5000pt][font=宋体]取出琼脂糖凝胶,剪刀剪开,标签面即孔突出面朝上,公测端为负极,放入高压快速电泳液中,没过胶面[/font]1mm[font=宋体],如有孔内有气泡,设法除去。[/font][/size][/font][font=宋体][size=10.5000pt]3. [/size][/font][font=宋体][size=10.5000pt][font=宋体]在[/font]DNA[font=宋体]样品中加入[/font][font=Calibri]1μl[/font][font=宋体]的[/font][font=Calibri]6[/font][font=宋体]× [/font][font=Calibri]loading buffer[/font][font=宋体]混匀,用[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液器[/color][/url][/color][/url]将混合液缓慢加入凝胶加样孔,同时加入[/font][font=Calibri]Marker[/font][font=宋体]。[/font][/size][/font][font=宋体][size=10.5000pt]4. [/size][/font][font=宋体][size=10.5000pt][font=宋体]开启电源,红色为正极,黑色为负极,注意[/font]DNA[font=宋体]样品有负极向正极电泳移动。[/font][/size][/font][font=宋体][size=10.5000pt]5. [/size][/font][font=宋体][size=10.5000pt]根据迁移距离及指示剂迁移的位置,判断是否终止电泳。[/size][/font][font=宋体][size=10.5000pt]6. [/size][/font][font=宋体][size=10.5000pt][font=宋体]电泳完毕,关电源,将凝胶放在成像仪中观察电泳条带及其位置,并与[/font]Marker[font=宋体]比较被扩增产物的大小。[/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]以上是德晟琼脂糖预制胶电泳试剂盒的具体使用方法以及在高压快速电泳时需要注意的一些小细节,虽然与其他试剂盒相比也一些差异,但是在核酸[/font]PCR[font=宋体]或者酶切反应等对分辨率要求不高的实验中,是非常适合的,而且省去了大量时间和金钱成本。[/font][/size][/font]
为什么一化合物中混有杂质,熔点就会降低,而不是升高呢???另外请问合金的熔点是不是比其中任何一种金属的熔点都要低啊????
请问下哪位大神知道,用什么方法和设备可以测琼脂糖的分子量?或者哪里有这种设备可以开展检查服务的,谢谢!
做了一小段时间的琼脂糖凝胶电泳, 有一些体会给新手们参考, 不当之处也请专家们指正.1. 加热时, 一定要煮沸, 以保证琼脂糖的完全溶解.2. 待溶液冷却至不烫手, 感觉温暖舒适时加EB. 一定要在通风柜里.3. 倒胶时, 可用干净的纸巾拭去气泡.4. 胶凝固后先倒入些电泳缓冲液以方便取梳子.5. 保证缓冲液淹过胶的边沿, 边沿部分常高出1-2mm.6. 有时需要大的上样孔, 可用胶带把几个相邻的梳齿粘在一起, 这种情况下, 尽量让胶液冷一些再倒胶.7. 如果只是为了看一下结果(不需要照相), 同一块胶可重复用1-3次. 有一次我跑了4遍, 条带很弱, 用加了EB的缓冲液(约10ul EB in 50ml 缓冲液)泡半小时后就如正常了.8. 要保存胶到第二天用, 可以保鲜膜包裹后放入4 度冰箱.9. TAE 电泳缓冲液也可重复使用, 至少10次没有问题.10. 为了防止电泳时两极缓冲液槽内pH和离子强度的改变,可在每次电泳后合并两极槽内 的缓冲液,混匀后再用。
熔点标准物质是熔点仪和熔点测量中温度的标准物质,它是保障熔点测量量值统一和准确的最有效的工具,主要供仪器制造、化工、医药和计量检定部门使用。一级熔点标准物质有对硝基甲苯(GBW13231a)、萘(GBW13232a)、苯甲酸(GBW13233a)、1,6-己二酸(GBW13234a)、对甲氧基苯甲酸(GBW13235a)、蒽(GBW13236)、对硝基苯甲酸(GBW13237a)、蒽醌(GBW13238a)。 售价均为:110元/瓶(2克/瓶), 毛细管装填熔点标准物质售价为:400元/套(八种:50支/种),快递费50元。二级熔点标准物质有偶氮苯[GBW(E)130133]、香草醛[GBW(E)130134]、乙酰苯胺[GBW(E)130135]、非那西丁[GBW(E)130136]、磺胺[GBW(E)130137]、丁二酸[GBW(E)130138]、磺胺二甲嘧啶[GBW(E)130139]、二氰二胺[GBW(E)130140]、糖精[GBW(E)130141]、咖啡因[GBW(E)130142]、酚酞[GBW(E)130143]。 售价均为:100元/瓶(2克/瓶),快递费50元。
要做实验测定!1、熔点的测定化合物的熔点是指在常压下该物质的固—液两相达到平衡时的温度。但通常把晶体物质受热后由固态转化为液态时的温度作为该化合物的熔点。纯净的固体有机化合物一般都有固定的熔点。在一定的外压下,固液两态之间的变化是非常敏锐的,自初熔至全熔(称为熔程)温度不超过0.5-1℃。若混有杂质则熔点有明确变化,不但熔点距扩大,而且熔点也往往下降。因此,熔点是晶体化合物纯度的重要指标。有机化合物熔点一般不超过350℃,较易测定,故可借测定熔点来鉴别未知有机物和判断有机物的纯度。在鉴定某未知物时,如测得其熔点和某已知物的熔点相同或相近时,不能认为它们为同一物质。还需把它们混合,测该混合物的熔点,若熔点仍不变,才能认为它们为同一物质。若混合物熔点降低,熔程增大,则说明它们属于不同的物质。故此种混合熔点试验,是检验两种熔点相同或相近的有机物是否为同一物质的最简便方法。熔点装置图:2、沸点的测定液体的分子由于分子运动有从表面逸出的倾向,这种倾向随着温度的升高而增大,进而在液面上部形成蒸气。当分子由液体逸出的速度与分子由蒸气中回到液体中的速度相等,液面上的蒸气达到饱和,称为饱和蒸气。它对液面所施加的压力称为饱和蒸气压。实验证明,液体的蒸气压只与温度有关。即液体在一定温度下具有一定的蒸气压。当液体的蒸气压增大到与外界施于液面的总压力(通常是大气压力)相等时,就有大量气泡从液体内部逸出,即液体沸腾。这时的温度称为液体的沸点。通常所说的沸点是指在101.3kPa下液体沸腾时的温度。在一定外压下,纯液体有机化合物都有一定的沸点,而且沸点距也很小(0.5-1℃)。所以测定沸点是鉴定有机化合物和判断物质纯度的依据之一。测定沸点常用的方法有常量法(蒸馏法)和微量法(沸点管法)两种。 实验步骤1、熔点的测定毛细管法:①准备熔点管:将毛细管截成6~8cm长,将一端用酒精灯外焰封口(与外焰成40o角转动加热)。防止将毛细管烧弯、封出疙瘩。②装填样品:取0.1~0.2g预先研细并烘干的样品,堆积于干净的表面皿上,将熔点管开口一端插入样品堆中,反复数次,就有少量样品进入熔点管中。然后将熔点管在垂直的约40cm的玻璃管中自有下落,使样品紧密堆积在熔点管的下端,反复多次,直到样品高约2~3cm为止,每种样品装2~3根。③仪器装置:将b形管固定于铁架台上,倒入液体石蜡做为浴液,其用量以略高于b形管的上侧管为宜。将装有样品的熔点管用橡皮圈固定于温度计的下端,使熔点管装样品的部分位于水银球的中部。然后将此带有熔点管的温度计,通过有缺口的软木塞小心插入b形管中,使之与管同轴,并使温度计的水银球位于b形管两支管的中间。④熔点测定:粗测:慢慢加热b形管的支管连接处,使温度每分钟上升约5℃。观察并记录样品开始熔化时的温度,此为样品的粗测熔点,作为精测的参考。精测:待浴液温度下降到30℃左右时,将温度计取出,换另一根熔点管,进行精测。开始升温可稍快,当温度升至离粗测熔点约10℃时,控制火焰使每分钟升温不超过1℃。当熔点管中的样品开始塌落,湿润,出现小液滴时,表明样品开始溶化,记录此时温度即样品的始熔温度。继续加热,至固体全部消失变为透明液体时再记录温度,此即样品的全熔温度。样品的熔点表示为:t始熔~t全熔。实测:尿素(已知物,133~135℃)、桂皮酸(未知物,132~133℃),混合物(尿素-桂皮酸=1:1,100℃左右)。实验过程中,粗测一次,精测两次。2、沸点的测定微量法测定沸点:①沸点管的制备:沸点管由外管和内管组成,外管用长7~8厘米、内径0.2~0.3cm的玻璃管将一端烧熔封口制得,内管用市购的毛细管截取3~4cm封其一端而成。测量时将内管开口向下插入外管中。②沸点的测定:取1~2滴待测样品滴入沸点管的外管中(思考题9),将内管插入外管中,然后用小橡皮圈把沸点附于温度计旁,再把该温度计的水银球位于b形管两支管中间,然后加热。加热时由于气体膨胀,内管中会有小气泡缓缓逸出,当温度升到比沸点稍高时,管内会有一连串的小气泡快速逸出。这时停止加热,使溶液自行冷却,气泡逸出的速度即渐渐减慢。在最后一气泡不再冒出并要缩回内管的瞬间记录温度,此时的温度即为该液体的沸点,待温度下降15~20℃后,可重新加热再测一次(2次所得温度数值不得相差1℃)。按上述方法进行如下测定:CCl4沸点(76℃)。 注意事项1.熔点管必须洁净。如含有灰尘等,能产生4—10OC的误差。2.熔点管底未封好会产生漏管。3.样品粉碎要细,填装要实,否则产生空隙,不易传热,造成熔程变大。4.样品不干燥或含有杂质,会使熔点偏低,熔程变大。5.样品量太少不便观察,而且熔点偏低;太多会造成熔程变大,熔点偏高。6.升温速度应慢,让热传导有充分的时间。升温速度过快,熔点偏高。7.熔点管壁太厚,热传导时间长,会产生熔点偏高。
请问下哪位大神知道,用什么方法和设备可以测琼脂糖的分子量?或者哪里有这种设备可以开展检查服务的,谢谢!
市面上出售琼脂糖填料的公司很多啊,不知道那家的比较好,有求各位了
我想要用葡聚糖凝胶色谱来分离纯化半刀豆球蛋白分子量是104000,它本身会结合葡萄糖,那用葡聚糖凝胶色谱还能不能分来,如果不行的话,琼脂糖凝胶可以不?琼脂糖凝胶我还没有用过,所以不知道DEAE琼脂糖凝胶 FF能不能用来分离,谢谢大家了!
符合WHO、PulseNet网络标准文件规定的PFGE专用琼脂糖粉是哪些个品牌?
按药典方法,用熔点仪测原料药熔点,作者猜测以下因素对测熔点结果有影响:样品干燥程度、 样品在毛细管中填充高度(猜想填得过高,刚开始熔化看得更明显,初熔点偏低)、 样品被碾碎得是否充分、 样品在毛细管中填充的密实程度。但不知那些因素的影响较大。请各位专家高手讨论。还有什么因素没有列出的大家也可讨论一下。
琼脂糖电泳步骤之超级基础篇一、电泳前准备准备内容作用1.刷干净电泳制胶的梳子,板子,槽子,蒸馏水洗净晾干防止不必要的重复污染,减少外来的污染。梳子干净有利于梳孔的形成。2.检查电泳槽,根据情况更换buffer排除电泳槽的电极接触不良,确保buffer的缓冲能力,减少污染。3.根据DNA的分离范围选择合适的胶浓度并记录达到较好的分离效果,防止样过快跑出胶或者是过慢浪费时间。4.计算agarose的用量和制胶 buffer的用量记录,胶最终越薄越好。实验记录备查 二、制胶步骤注意事项1.称量agarose和bufferBuffer不要用成H2O,称量相对准确2.融胶,加热到胶产生大量的气泡时,拿出摇匀,继续加热到完全溶解,拿出摇匀,再加热到沸腾。非常热,小心烫手,另外注意不要加热过度使胶冲出瓶子。因此注意选择起码为胶体积2倍以上的瓶子。保证胶混匀和完全溶解,减少可能因此引起的胶中孔径不均匀影响分离效果。3.倒胶,可用水浴的办法使胶冷却到60度左右,即手可以握住瓶子的温度,沿着制胶板的一侧,缓缓地一次性倒入。梳子最好是预先放好并固定的,注意梳孔的体积能点的下所有的样。用枪头赶掉气泡。制胶的桌面相对水平。倒胶时尽量减少气泡的产生。EB如果在制胶时加入,在60度左右时加入,使终浓度为0.5ug/ml。不宜过低,染色成像不明显;不宜过高,导致背景太深。摇匀要沿着瓶壁摇动,尽量减少气泡产生的可能性。高浓度胶例如2%以上的EB很难摇匀,而且凝的速度也相对快,强烈建议跑完胶之后再用EB染色。4.室温凝胶30分钟过程中不要碰到梳子,尽量保持胶的位置不移动。时间不宜过久,导致胶干燥变形;不宜过短,影响胶内部孔径形成。5.拔梳子,放入电泳槽。缓缓地将梳子垂直从梳孔拔出,尽可能使梳子是同时从各个胶孔拔出的。暂时不用的胶最好放入电泳槽电泳液中浸泡。电泳液要浸没胶1mm。 三、上样电泳[
熔点是指物质在大气压力下固态与液态处于平衡时的温度。固体物质熔点的测定通常是将晶体物质加热到一定温度时,晶体就开始由固态转变为液态,测定此时的温度就是该晶体物质的熔点。熔点测定是辨认物质本性的基本手段,也是纯度测定的重要方法之一。因此,熔点仪在化学工业、医药研究中据有重要地位,是生产药物、香料、染料及其他有机晶体物质的必备仪器,也是实验室常用的基础仪器之一。纯净的固体有机物,一般都有固定的熔点,而且熔点范围(又称熔程或熔距,是指由始熔至全熔的温度间隔)很小,一般不超过0.5—1℃;若物质不纯时,熔点就会下降,且熔点范围就会扩大。利用这一性质来判断物质的纯度和鉴别未知化合物。例如,一个未知化合物,测得其熔点与某一已知化合物的熔点相同或者十分相近时,将未知样品与已知样品等量混合后测定其混合熔点。若熔点没有变化,且熔点范围不超过1℃时,一般可以认为二者是同一物质,如果混合熔点发生变化,熔点范围大,则可判定它们不是同一物质。这种鉴定方法叫做混合熔点法。测量熔点的方法有两种:一种是毛细管熔点测定法,另一种则是熔点仪测定熔点法。基于科技的发展与进步,熔点仪不断的更新换代,实现了许多实用性功能,且操作方便,数据精确。因此实验室常用的是采用熔点仪测定熔点的方法。目前全球使用最广泛的熔点仪是美国斯坦佛大学研究所最新研究成果的MPA100全自动熔点仪。MPA100熔点仪是按照药典规定的熔点检测方法而设计的,MPA100熔点仪利用电子技术实现温度程控,初熔和终熔数字显示。应用了线性校正的铂电阻作为检测元件,并用电子线路实现了快速“起始温度”设定,三通道同时设定及可供选择的线性的升温速率。MPA100熔点仪采用药典规定的毛细管作为样品管,通过高分辨率的数码成像检测器观察毛细管内样品的熔化过程,清晰直观,是制药、化工、燃料、香料、橡胶等行业理想的熔点检测仪器。http://www.sinoinstrument.com/UploadFiles/Image/s2013050910524395610(2).jpg
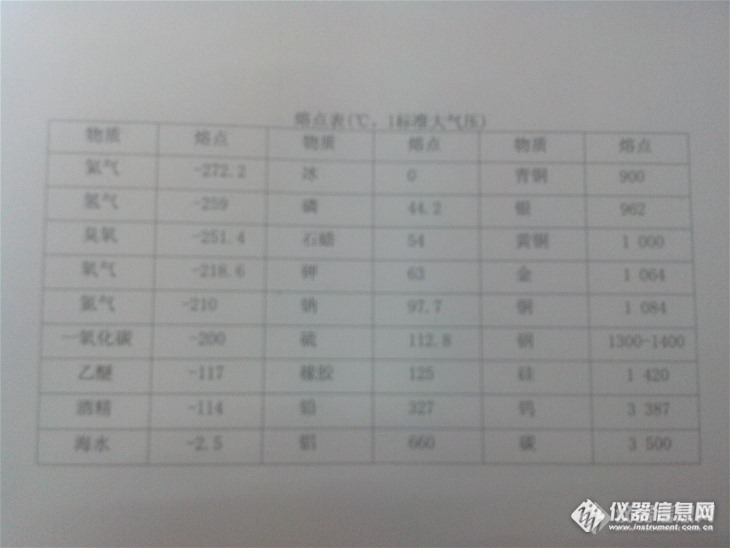
物质熔点测定方法物质的熔点,一般情况下就是指该物质固、液两相可以共存并处于平衡的温度,一说到这个,我们就会想到冰和水,以冰熔化成水为例,在一个大气压下冰的熔点是0℃,而温度为0℃时,冰和水可以共存在通常的情况下,物体在不同的温度下,其状态也是不同的,且即时在同一温度,其状态也是不确定的,如晶体处于熔点温度时,可能有三种状态,即可能固态、可能液态、也可能固液共存,常用物质溶解表如下:熔点表http://ng1.17img.cn/bbsfiles/images/2013/11/201311131143_476934_2154459_3.jpg那么上表这些物质的熔点怎么得来的的呢?有没有什么方法可以测试物质的熔点呢,那就看看吧!1.原理以加热的方式使毛细管中的试样从低于其初熔时的温度逐渐升至高于其终熔时的温度,通过目测分别观察其初熔和终熔温度,即为试样的初熔点和终熔点。2.仪器(1)毛细管:硬质玻璃毛细管,内径0.9~1.1mm,壁厚0.15~0.2mm,长110~120mm,一端封口。(2)测量温度计:分度值为0.1℃,长约400mm,全浸或局浸式并经校正的温度计,根据熔点范围选择适当量程。(3)辅助温度计:分度值为1℃的普通温度计,量程与测量温度计一致。(4)加热器:加热均匀、安全、易控制温度的加热装置。(5)熔点测定装置:容积250ml的内热式烧瓶,直径80mm,瓶长130~140mm,瓶口处有一温度计插口直径约10mm的圆孔,在瓶口上方有两个相对称的毛细管插口直径约2mm的圆孔。3.传热液体201型甲基硅油(粘度在500号以上),或硫酸与硫酸钾混合液(220ml浓硫酸中加入70~80g无水硫酸钾,再加入0.1~0.2g硝酸钾)。4.样品的干燥取少量混匀、研细的试样放于干燥、清洁的表面皿中,于105℃干燥箱中干燥30min后取出,放在干燥器中冷却备用。5.测定将少量干燥、研细的试样装入清洁、干燥、一端封口的毛细管中,取一高约800mm、直径10mm的干燥玻璃管直立于玻璃板上,将装有试样的毛细管经玻璃管投掷8~10次,直至毛细管内试样紧缩至3-4mm高,再将开口一端封熔,圆底烧瓶中注入其体积四分之三的传热液体,测量温度计插入试管内的传热液体中,并使温度计的中间泡也浸没于传热液体中,温度计不得碰及管底。加热使传热液体温度缓缓上升至熔点前10℃时,将装有试样的毛细管通过锥形导管插入试管内并附着于温度计水银球的中部,继续加热,调节加热器使温度上升速度为0.5~1.0℃/min。观察毛细管中试样熔化情况,当试样开始出现明显的局部液化现象时的温度为初熔点。6.结果的表示与计算若测定中使用的是局浸式温度计,初熔点t=t+△t;若测定中使用的是全浸式温度计,初熔点t按下式计算: t=t1+△t1+△t2+△t3△t1=0.00016h1(t1-t2)△t2=0.00016h2(t1-t3)式中 t——初熔点,℃△t1——温度计露出液面至塞口处的水银柱校正值,℃△t2——温度计露出塞外的水银柱校正值,℃△t3——温度计的示值校正值,℃t1——观察温度,t2——试管内液面至塞口的中间处的温度,t3[
测完一个样品后将毛细管拔出,熔点仪显示里面还有一根熔点管从而报错不能使用,可里面没有熔点管了啊。该怎么办呢?
本公司有一产品,在做燃点的过程中,终熔老是出不来,其实已经溶解,样品是D-核糖,我们用的是wrs-2A熔点仪,样品终熔不是完全透明的液体,而是有熔融状态,我们应该选择什么样的熔点仪器??有没有很强的光源透过该熔融状态的熔点仪器??国标,药典上都没有该样品.我该怎么做???求助专家
专家你好!我刚才问的关于熔点的问题,我发现,该物质在测熔点的时候,形成一层簿膜.但是就是没有明显的液滴.这该怎么解释?
需要测试渗透探伤剂中汞,砷,锌,铅等低熔点金属含量测定,其中汞铅含量小于1ppm。是否能做?据国内的供应商说不能做,但是我们有美国供应商做过相关实验的报告。